文档内容
【基础知识】原子结构与性质
考点三 元素周期表 粒子半径
【必备知识】
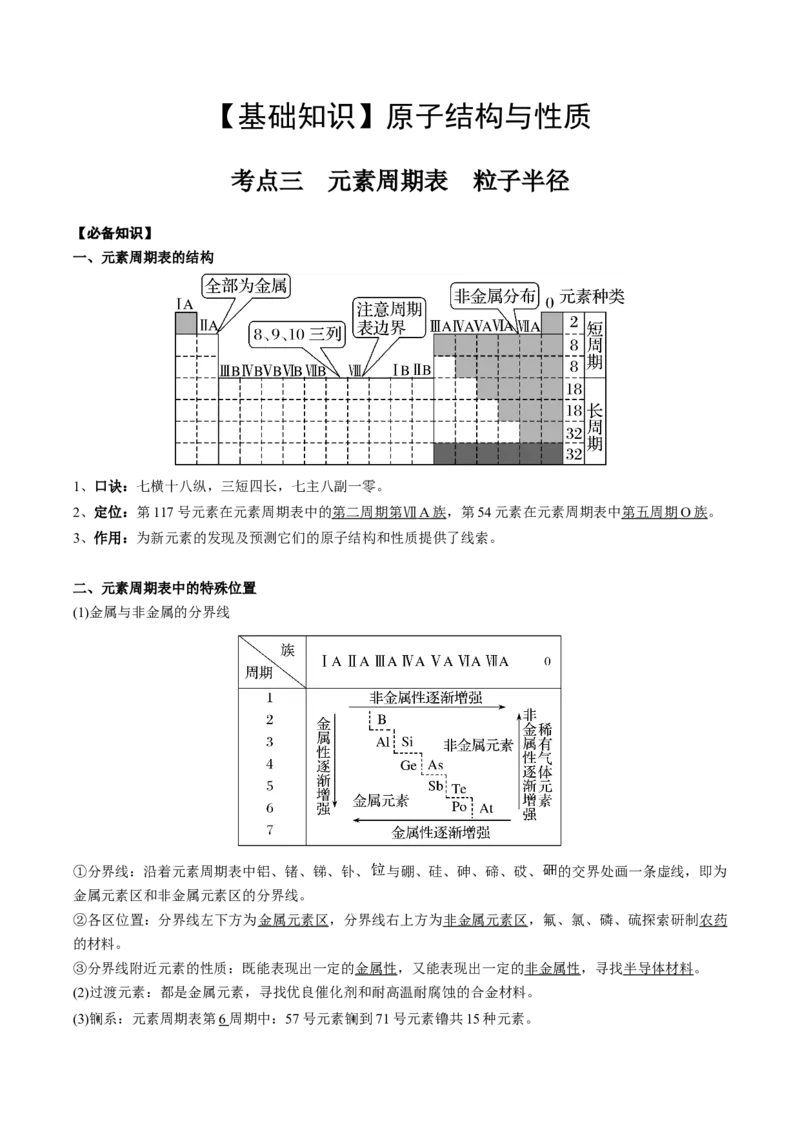
一、元素周期表的结构
1、口诀:七横十八纵,三短四长,七主八副一零。
2、定位:第117号元素在元素周期表中的 第二周期第Ⅶ A 族 ,第54元素在元素周期表中 第五周期 O 族 。
3、作用:为新元素的发现及预测它们的原子结构和性质提供了线索。
二、元素周期表中的特殊位置
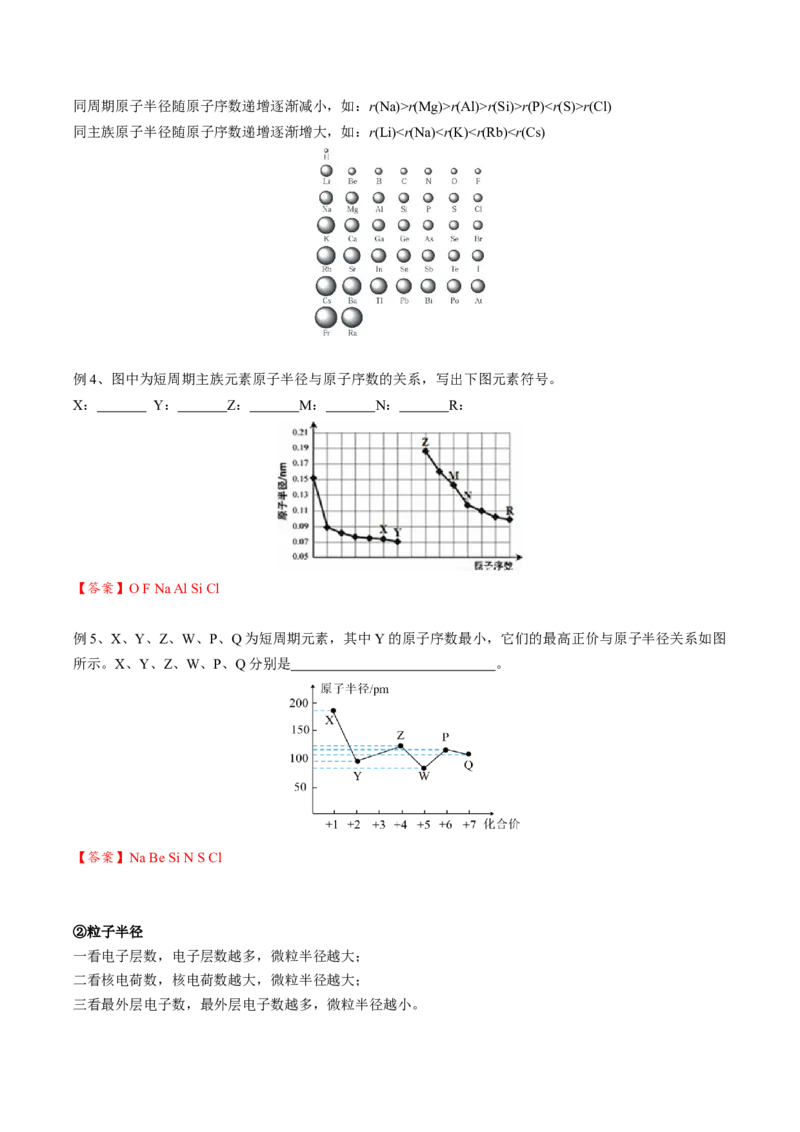
(1)金属与非金属的分界线
①分界线:沿着元素周期表中铝、锗、锑、钋、 与硼、硅、砷、碲、砹、 的交界处画一条虚线,即为
金属元素区和非金属元素区的分界线。
②各区位置:分界线左下方为金属元素区,分界线右上方为非金属元素区,氟、氯、磷、硫探索研制农药
的材料。
③分界线附近元素的性质:既能表现出一定的金属性,又能表现出一定的非金属性,寻找半导体材料。
(2)过渡元素:都是金属元素,寻找优良催化剂和耐高温耐腐蚀的合金材料。
(3)镧系:元素周期表第6 周期中:57号元素镧到71号元素镥共15种元素。(4)锕系:元素周期表第7 周期中:89号元素锕到103号元素铹共15种元素。
例1、请在下表中画出元素周期表的轮廓,并在表中按要求完成下列问题:
(1)标出族序数、周期序数。
(2)将主族元素前六周期的元素符号补充完整。
(3)画出金属与非金属的分界线,并用阴影表示出过渡元素的位置。
(4)标出镧系、锕系的位置。
(5)写出各周期元素的种类(数目)。
(6)写出稀有气体元素的原子序数,标出113号~117号元素的位置。
【答案】
三、原子结构与元素周期表的关系
1、元素周期表分区2、各区价电子排布特点
①主族元素的价电子排布特点
主族 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
排布特点 n s 1 n s 2 n s 2 n p 1 n s 2 n p 2 n s 2 n p 3 n s 2 n p 4 n s 2 n p 5
②0族元素的价电子排布:He为1s2;其他为ns2np6。
③过渡元素(镧系、锕系元素除外)的价电子排布:(n-1)d1~10ns1~2。
例2、指出下列元素在元素周期表中的位置。
(1)1s22s22p63s23p5 (2)[Kr]4d105s25p2 (3)[Ar]3d34s2 (4) [Ar]3d104s1 (5) [Ar]4s1
【答案】(1)第三周期第ⅦA族 (2)第五周期第ⅣA族 (3)第四周期第ⅤB族 (4)第四周期第ⅠB族 (5)第四
周期第ⅠA族
四、化合价、粒子半径
1、主族化合价
最高正价=主族序数,最低负价=主族序数-8(金属无负价,F无正价,O无最高正价)
例3、图中为短周期主族元素化合价与原子序数的关系,写出下图元素符号。
a: b: c: d: e: f:
【答案】C N O Na Al Si S
2、粒子半径大小的比较方法
①原子半径同周期原子半径随原子序数递增逐渐减小,如:r(Na)>r(Mg)>r(Al)>r(Si)>r(P)r(Cl)
同主族原子半径随原子序数递增逐渐增大,如:r(Li)B>C B.原子半径:C>B>A
C.离子半径:A2->C->B2+ D.原子最外层电子数:C>A>B
【答案】 B
【解析】 由题意可推出A为S、B为Mg、C为F。原子序数:S>Mg>F,故A项正确;不同周期元素,
电子层数越多,原子半径越大,同一周期元素,核电荷数越大,原子半径越小,因此原子半径:
Mg>S>F,故B项错误;S2-的电子层数为3,离子半径最大,Mg2+与F-的电子层数为2,且具有相同的核
外电子数,核电荷数越大,离子半径越小,因此离子半径:S2->F->Mg2+,故C项正确;F原子最外层电
子数为7,S原子最外层电子数为6,Mg原子最外层电子数为2,因此原子最外层电子数:F>S>Mg,故D
项正确。
【解题技巧】电子层结构相同(核外电子排布相同)的离子半径(包括阴、阳离子)随核电荷数的增加而减小,
如O2->F->Na+>Mg2+>Al3+。可归纳为电子层排布相同的离子,(表中位置)阴离子在阳离子前一周期,原
子序数大的半径小,概括为“阴前阳下,序大径小”。
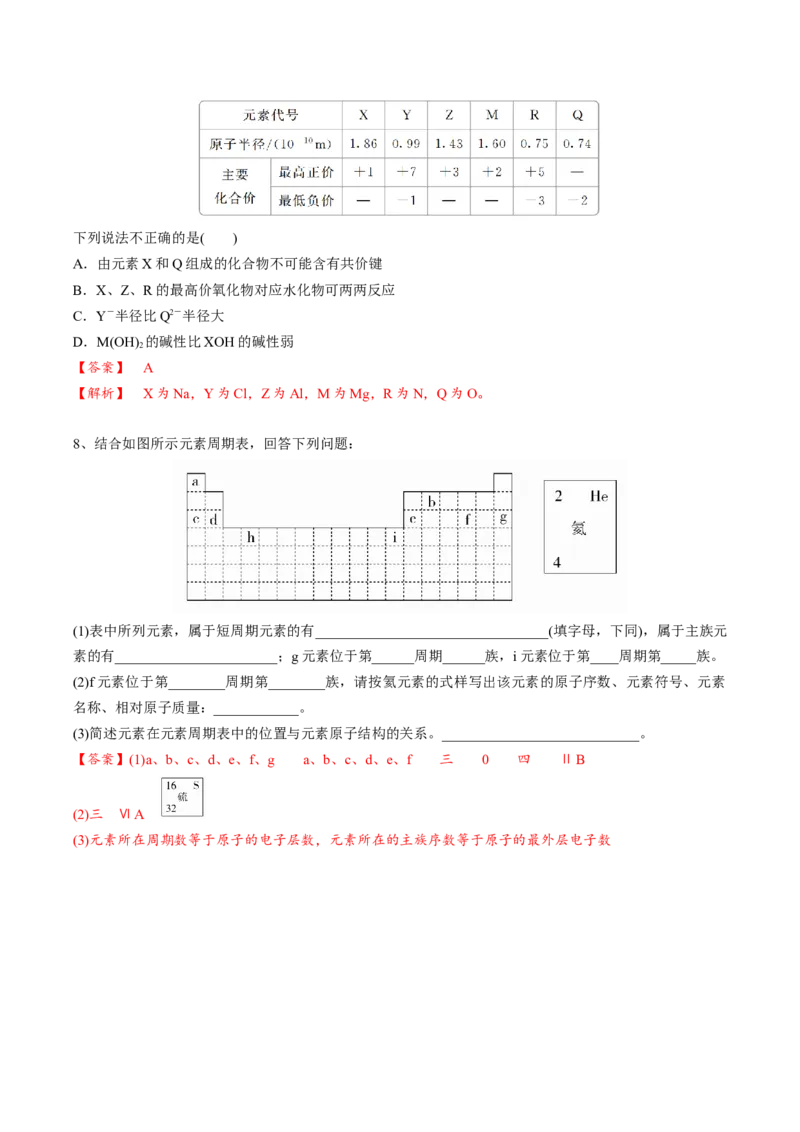
7、几种短周期元素的原子半径及主要化合价如下表:下列说法不正确的是( )
A.由元素X和Q组成的化合物不可能含有共价键
B.X、Z、R的最高价氧化物对应水化物可两两反应
C.Y-半径比Q2-半径大
D.M(OH) 的碱性比XOH的碱性弱
2
【答案】 A
【解析】 X为Na,Y为Cl,Z为Al,M为Mg,R为N,Q为O。
8、结合如图所示元素周期表,回答下列问题:
(1)表中所列元素,属于短周期元素的有_________________________________(填字母,下同),属于主族元
素的有_______________________;g元素位于第______周期______族,i元素位于第____周期第_____族。
(2)f元素位于第________周期第________族,请按氦元素的式样写出该元素的原子序数、元素符号、元素
名称、相对原子质量:____________。
(3)简述元素在元素周期表中的位置与元素原子结构的关系。____________________________。
【答案】(1)a、b、c、d、e、f、g a、b、c、d、e、f 三 0 四 ⅡB
(2)三 ⅥA
(3)元素所在周期数等于原子的电子层数,元素所在的主族序数等于原子的最外层电子数