文档内容
第2讲 元素周期表和元素周期律
[考纲要求]
1.掌握元素周期律的实质。了解元素周期表(长式)的结构(周期、族)及其应用。2.
以第三周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系。3.以ⅠA和ⅦA
族为例,掌握同一主族内元素性质递变规律与原子结构的关系。4.了解金属、非金属在元素
周期表中的位置及其性质递变的规律。
考点一 元素周期表
1知识梳理
1.原子序数:按照元素在周期表中的顺序给元素所编的序号。原子序数=________
=__________=______。
2.编排原则
3.元素周期表的结构
(1)周期(7个横行,7个周期)
短周期 长周期
序号 一 二 三 四 五 六 七
元素种数 ____ ____ ____ ____ ____ ____ ____
0族元素
____ ____ ____ ____ ____ ____ ____
原子序数
(2)族(18个纵行,16个族)
列 1 2 13 14 15 16 17
主
族
族 ____ ⅡA ____ ⅣA ____ ⅥA ____
列 3 4 5 6 7 11 12
副
族
族 ____ ⅣB ⅤB ⅥB ⅦB ____ ⅡB
Ⅷ族 第__________,共3个纵行0族 第____纵行
(3)元素周期表的分区
族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
1
2
3
4
5
6
7
①分界线:如上图所示,沿着元素周期表中__________与____________的交界处画
一条斜线,即为________和____________的分界线(氢元素除外)。
②分界线附近的元素,既能表现出一定的______,又能表现出一定的__________。
4.元素周期表中的特殊位置
(1)过渡元素:元素周期表中部从____族到____族10个纵列共六十多种元素,这些
元素都是金属元素。
(2)镧系:元素周期表第____周期中,57号元素镧到71号元素镥共____种元素。
(3)锕系:元素周期表第____周期中,89号元素锕到103号元素铹共____种元素。
(4)超铀元素:在锕系元素中92号元素铀(U)以后的各种元素。
[思考]
(1)甲、乙是元素周期表中同一周期的ⅡA族和ⅦA族元素,原子序数分别为m、n,
则m和n的关系为____________________。
(2)甲、乙是元素周期表中同一主族相邻周期的两种元素(其中甲在上一周期),若甲
的原子序数为x,则乙的原子序数可能是____________________。
(3) 若A、B是相邻周期同主族元素(A在B的上一周期),A、B所在周期分别有m种
和n种元素,A的原子序数为x,B的原子序数为y,则x、y的关系为________________。
[判断] (正确的打“√”,错误的打“×”)
(1)元素周期表中共有18个纵行,16个族( )
(2)同主族元素的最外层电子数一定相同( )
(3)元素周期表中位于金属与非金属分界线附近的元素属于过渡元素( )
(4)ⅠA族全部是金属元素( )(5)元素周期表中镧系元素和锕系元素都占据同一格,它们是同位素( )
(6)两短周期元素原子序数相差8,则周期数一定相差1( )
(7)某元素原子的核电荷数为53,则该元素位于第五周期ⅦA族( )
[提醒]
(1)在描述元素在Ⅷ族时,不要写成ⅧB。
(2)元素周期表中,族序数Ⅱ、Ⅲ是主族和副族的分界线,第一次分界时主族(ⅡA)
在副族(ⅢB)之前,第二次分界时副族(ⅡB)在主族(ⅢA)之前。
(3)元素种类最多的族是ⅢB族,共有32种元素,形成化合物种类最多的为ⅣA族。
2 对点速练
练点一 元素周期表的结构信息
1.铟产业被称为“信息时代的朝阳产业”。元素周期表中铟的数据如图,下列说法
完全正确的是( )
A.铟元素的质量数是114.8
B.铟元素的相对原子质量是114
C.铟元素是一种副族元素
D.铟原子最外层有3个电子
2.结合如图所示元素周期表,回答下列问题:
(1)表中所列元素,属于短周期元素的有________(填字母,下同),属于主族元素的
有________;g元素位于第________周期________族;i元素位于第________周期第________
族。
(2)f元素位于第________周期第________族,请按氦元素的式样写出该元素的原子
序数、元素符号、元素名称、相对原子质量:______________。
练点二 元素周期表局部判断
3.A、B、C均为短周期元素,它们在周期表中的位置如图所示。已知B、C元素的原子
序数之和是A元素原子序数的4倍,则A、B、C分别为( )
A.Be、Na、Al B.B、Mg、Si
C.O、P、Cl D.C、Al、P
4.
如图为元素周期表中前四周期的一部分,若B元素的核电荷数为x,则这五种元素的
核电荷数之和为( )
A.5x+10 B.5x
C.5x+14 D.5x+16
5.已知X、Y、Z三种主族元素在周期表中的位置如图所示,设 X的原子序数为a。
则下列说法不正确的是( )
Y
X
Z
A.Y与Z的原子序数之和可能为2a
B.Y的原子序数可能为a-17
C.Z的原子序数可能为a+31
D.X、Y、Z一定为短周期元素
规律技巧
元素周期表结构中隐含的两个关系
1.同周期主族元素原子序数差的关系
(1)短周期元素原子序数差=族序数差。
(2)两元素分布在过渡元素同侧时,原子序数差=族序数差。两元素分布在过渡元素
两侧时,四或五周期元素原子序数差=族序数差+10,六周期元素原子序数差=族序数差+
24。
(3)第四、五周期的第ⅡA与ⅢA族原子序数之差都为11,第六周期为25。2.同主族、邻周期元素的原子序数差的关系
(1)ⅠA族元素,随电子层数的增加,原子序数依次相差2、8、8、18、18、32。
(2)ⅡA族和0族元素,随电子层数的增加,原子序数依次相差8、8、18、18、32。
(3)ⅢA~ⅦA族元素,随电子层数的增加,原子序数依次相差8、18、18、32。
考点二 元素周期律
1 知识梳理
1.元素周期律
2.元素周期律的具体内容
项目 同周期(左→右) 同主族(上→下)
核电荷数 逐渐____ 逐渐____
电子层数 ____ 逐渐____
原
子 原子半径 逐渐____ 逐渐____
结
阳离子逐渐____
构
离子半径 阴离子逐渐____ 逐渐____
r(阴离子)__r(阳离子)
最高正化合价由
____→____(O、F除外)
相同
化合价 负化合价= 最高正化合价=______(O、F
_________________________
除外)
_________________________
______________________
元素的金
金属性逐渐____ 金属性逐渐____
性 属性和非
质 非金属性逐渐____ 非金属性逐渐____
金属性
离子的氧化 阳离子氧化性逐渐____ 阳离子氧化性逐渐____
性、还原性 阴离子还原性逐渐____ 阴离子还原性逐渐____
气态氢化物
逐渐____ 逐渐____
稳定性
最高价氧化物 碱性逐渐____ 碱性逐渐____对应的水化物
酸性逐渐____ 酸性逐渐____
的酸碱性
3.元素周期律(表)的现实意义
(1)根据元素周期表中的位置寻找未知元素
(2)预测元素的性质(由递变规律推测)
①比较不同主族、不同周期元素的性质
如金属性Mg>Al,Ca>Mg,则碱性Mg(OH)>Al(OH),Ca(OH)>Mg(OH)。
2 3 2 2
②推测未知元素的某些性质
如:已知Ca(OH) 微溶,Mg(OH) 难溶,可推知Be(OH) 难溶。
2 2 2
(3)启发人们在一定区域内寻找新物质
①半导体元素在金属与非金属分界线附近,如:Si、Ge、Ga等。
②农药中常用元素在右上方,如:F、Cl、S、P、As等。
③催化剂和耐高温、耐腐蚀合金材料主要在过渡元素中找,如:Fe、Ni、Rh、Pt、
Pd等。
[判断] (正确的打“√”,错误的打“×”)
(1)I的原子半径大于Br,HI比HBr的热稳定性强( )
(2)P的非金属性强于Si,HPO 比HSiO 的酸性强( )
3 4 2 3
(3)O、S、P元素的原子半径及它们的气态氢化物的热稳定性均依次递增( )
(4)同主族元素含氧酸的酸性随核电荷数的增加而减弱( )
(5)第二周期元素从左到右,最高正价从+1递增到+7( )
(6)同周期金属元素的化合价越高,其原子失电子能力越强( )
(7)在主族元素中,最高正化合价均等于主族序数( )
(8)元素的原子得电子越多,非金属性越强;失电子越多,金属性越强( )
2 对点速练
1.比较下列微粒半径大小(用“>”或“<”填空):
(1)Na________Mg________Cl
(2)Li________Na________K
(3)Na+________Mg2+________Al3+
(4)F-________Cl-________Br-
(5)Cl-________O2-________Na+________Mg2+(6)Fe2+________Fe3+
2.已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则下列叙
述中正确的是( )
A.原子序数:D>C>B>A
B.原子半径:B>A>C>D
C.离子半径:C3->D->A2+>B+
D.氧化性:A2+>B+,还原性:C3-”或“<”填空):
(1)金属性:K________Na________Mg,
非金属性:F________O________S。
(2)碱性:Mg(OH)________Ca(OH)________KOH。
2 2
(3)酸性:HClO________HSO________HClO。
4 2 4
(4)热稳定性:CH________NH________HO。
4 3 2
(5)还原性:HBr________HCl,I-________S2-。
(6)氧化性:Fe3+________Cu2+________Fe2+。
5.根据下表(部分短周期元素的原子半径及主要化合价)信息,下列叙述正确的是(
)
元素代号 A B C D E
原子半径/nm 0.186 0.143 0.089 0.104 0.074主要化合价 +1 +3 +2 +6、-2 -2
A.E2-与B3+的核外电子数不可能相等
B.离子半径大小A+E
6.已知1~18号元素的离子 W3+、X+、Y2-、Z-具有相同的电子层结构,下列关系
a b c d
正确的是( )
A.质子数:c>d
B.离子的还原性:Y2->Z-
C.氢化物的稳定性:HY>HZ
2
D.原子半径:XX>Y>Z B.原子半径:Z>Y>X>W
C.元素X的含氧酸均为强酸 D.Y的氧化物水化物为强碱
3.[2019·全国卷Ⅰ,13]科学家合成出了一种新化合物(如图所示),其中W、X、
Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是(
)
A.WZ的水溶液呈碱性
B.元素非金属性的顺序为X>Y>Z
C.Y的最高价氧化物的水化物是中强酸
D.该新化合物中Y不满足8电子稳定结构
4.[2019·全国卷Ⅱ,9]今年是门捷列夫发现元素周期律150周年。下表是元素周
期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法错
误的是( )
W
X Y Z
A.原子半径:WAl
D.碱性:In(OH)>RbOH
3
2.下列有关第114号和第116号元素的说法错误的是( )
A.两种元素位于同一周期
B.116号元素位于第ⅥA族C.两种元素都是活泼的非金属元素
D.114号元素的原子半径比116号元素的大
3.W、X、Y、Z均为短周期主族元素,原子序数依次增加,X与Y形成的化合物能与
水反应生成酸且X、Y同主族,两元素核电荷数之和与W、Z的原子序数之和相等,则下列说
法正确的是( )
A.Z元素的含氧酸是最强酸
B.原子半径:X>Z
C.气态氢化物热稳定性:W>X
D.W与Y可以存在于同一离子化合物中
4.a、b、c、d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原
子次外层的电子数相同;c所在周期数与族数相同;d与a同族。下列叙述正确的是( )
A.原子半径:d>c>b>a
B.4种元素中b的金属性最强
C.c的氧化物的水化物是强碱
D.d单质的氧化性比a单质的氧化性强
5.根据元素周期表和元素周期律,判断下列叙述不正确的是( )
A.气态氢化物的稳定性:HO>NH>SiH
2 3 4
B.氢元素与其他元素可形成共价化合物或离子化合物
C.如图所示实验可证明元素的非金属性:Cl>C>Si
D.用中文“ ”(ào)命名的第118号元素在周期表中位于第七周期0族
6.有A、B、C、D四种短周期元素在周期表中的位置如图所示。已知:A2+与C原子
的电子数相差2。
… C
A B D
下列推断不正确的是( )A.A和D组成的化合物是弱电解质且水溶液呈酸性
B.与A同周期且与C同主族的E元素,其最高价氧化物对应水化物在某些化学反应
中常作催化剂
C.离子半径:C>A>B
D.B与C形成的化合物是冶金工业的一种原料
7.
如图为元素周期表的一部分,X、Y、Z、W均为短周期元素,其中W原子的最外层电
子数是最内层电子数的3倍。下列判断正确的是( )
A.最高价氧化物对应水化物的酸性:Y>Z>W
B.含Y元素的盐溶液一定显酸性
C.原子半径:r>r>r>r
W Z Y X
D.X与W的气态氢化物可相互反应生成离子化合物
8.X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图
所示。下列说法不正确的是( )
A.R的氧化物都含有离子键
B.M的氢化物常温常压下为气体
C.最高价含氧酸的酸性:Z<Y
D.Y形成的化合物种类最多
9.
短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化
合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L-1r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是(
)
A.原子半径的大小WX>Y
C.Y的氢化物常温常压下为液态
D.X的最高价氧化物的水化物为强酸
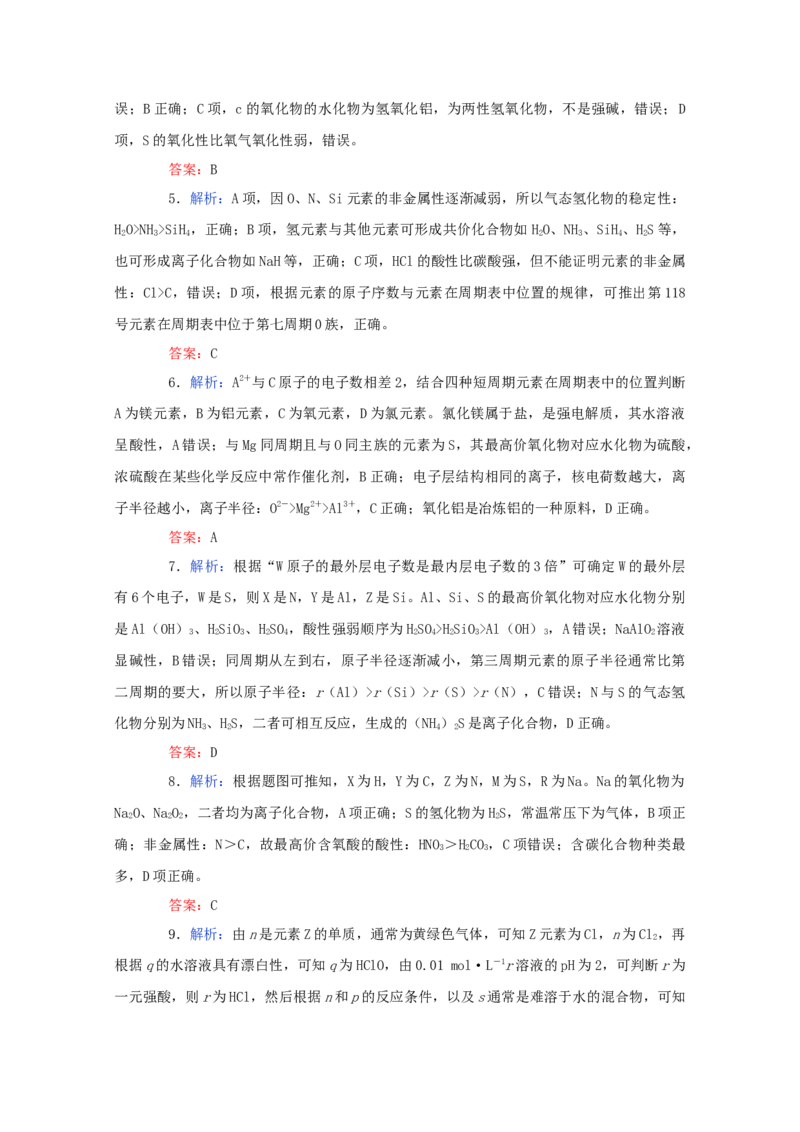
10.短周期元素W、X、Y、Z的原子序数依次增大,W、Z位于同主族,四种元素组成
的一种化合物的结构式为 。下列说法不正确的是( )
A.W的最简单氢化物的稳定性比X的弱
B.X、Y形成的化合物水溶液显碱性
C.W与Y形成的化合物中一定含有离子键
D.原子半径:Y>Z>X>W
第2讲 元素周期表和元素周期律
考点一
1知识梳理
1.核电荷数 核外电子数 质子数
2.原子序数 最外层电子数 电子层数
3.(1)2 8 8 18 18 32 32 2 10 18 36 54 86 118 (2)ⅠA
ⅢA ⅤA ⅦA ⅢB ⅠB 8、9、10 18 (3)B、Si、As、Te、At Al、Ge、Sb、Po
金属元素 非金属元素 金属性 非金属性
4.(1)ⅢB ⅡB (2)六 15 (3)七 15
思考 答案:(1)n=m+5 n=m+15 n=m+29 (2)x+2 x+8 x+18 x+32 (3)y=x+m或y=x+n
判断 答案:(1)√ (2)√ (3)× (4)× (5)× (6)√ (7)√
2对点速练
1.解析:该元素的原子序数为49,位于第五周期第ⅢA族,和Al处于同一主族,
故D正确。
答案:D
2.答案:(1)a、b、c、d、e、f、g a、b、c、d、e、f 三 0 四 ⅡB
(2)三 ⅥA
3.解析:设A的原子序数为x,则B的原子序数为x+8-1,C的原子序数为x+8+
1,(x+8-1)+(x+8+1)=4x,解得x=8,所以A为O元素,B为P元素,C为Cl元素,
故选C。
答案:C
4.解析:
答案:A
5.解析:X、Y、Z为主族元素,Y一定不在第一周期,所以D项错误;若Y、X、Z
分别位于第三、四、五周期的右边,则Y的原子序数为a-17,Y与Z的原子序数之和为2a,
A、B正确;若Y、X、Z分别位于第四、五、六周期的右边,则Z的原子序数为a+31,C正确。
答案:D
考点二
1知识梳理
1.原子序数 核外电子排布
2.增大 增大 相同 增多 减小 增大 减小 减小 > 增大 +1 +7 -
(8-主族序数) 主族序数 减弱 增强 增强 减弱 增强 减弱 减弱 增强 增强
减弱 减弱 增强 增强 减弱
判断 答案:(1)× (2)√ (3)× (4)× (5)× (6)× (7)×
(8)×
2对点速练
1.答案:(1)> > (2)< < (3)> > (4)< < (5)> > > (6)>2.解析:由于四种离子具有相同的电子层结构,离子所对应的元素应位于相邻两个
周期,根据阴阳离子所带的电荷数,得出元素在周期表中的位置关系:。原子序数大小应为
A>B>D>C,A项错误;根据原子半径的递变规律,可以判断 B正确;离子半径应为C3->D->B+
>A2+,C错误;还原性为C3->D-,D错误。
答案:B
3.解析:比较微粒半径有以下原则:①同周期元素原子半径从左到右逐渐减小,A
为P>S>Cl>O;②同主族元素原子半径从上到下逐渐增大;③核外电子排布相同时,核电荷数
越大,微粒半径越小,Mg2+>Al3+;④各层排布都饱和,一般电子层数越多,微粒半径越大。
故只有C正确。
答案:C
4.答案:(1)> > > > (2)< < (3)> > (4)< < (5)> <
(6)> >
5.答案:B
6.解析:因四种离子的电子层结构相同,所以质子数a、b、c、d的大小关系应为
a>b>d>c,且Y、Z在上一周期,Y在Z的左边,Y的非金属性弱于Z;W、X在下一周期,X在
W的左边,X的金属性强于W。质子数d>c,A项错误;非金属性:YZ-,B项正确;非金属性:Z>Y,故氢化物稳定性:HZ>HY,C项错误;同周期元素,从左到
2
右原子半径逐渐减小,故原子半径:X>W,D项错误。
答案:B
本讲真题研练
1.解析:W、X、Y、Z为原子序数依次增大的短周期主族元素且原子序数总和为
24,结合题给化合物的结构式可知,W 为 H、X 为 B、Y 为 N、Z 为 Na。A 项,
中H、B、N之间均为共价键,正确;B项,Na既可与水反应,
也可与甲醇反应,正确;C项,Y(N)的最高价氧化物的水化物为HNO ,属于强酸,正确;D
3
项,BF 中,1个B原子与3个F原子形成3个共价键,B外围只有6个电子,不满足8电子稳
3定结构,错误。
答案:D
2.解析:由化合物XW 与WZ相遇会产生白烟,可知XW 和WZ分别是NH 和HCl,即W
3 3 3
是H元素,X是N元素,Z是Cl元素;再根据四种元素的核外电子总数满足X+Y=W+Z,可
知Y是Na元素。A项,Na(Y)是金属元素,其非金属性不可能大于Cl(Z),错误;B项,
原子半径:Na(Y)>Cl(Z),错误;C项,N(X)元素的含氧酸不全为强酸,如HNO 是弱
2
酸,错误;D项,Na(Y)的氧化物的水化物为NaOH,是强碱,正确。
答案:D
3.解析:由W、X、Y、Z为同一短周期元素,结合新化合物的结构式可知,X为ⅣA
族元素,Z为卤族元素,W为碱金属元素,再由Z的核外最外层电子数是X核外电子数的一半
可知,Z为Cl、X为Si,进而推知W为Na、Y为P。A项,NaCl的水溶液呈中性,错误;B项,
元素的非金属性:SiN,
气态氢化物热稳定性:HO(g)>NH ,C项错误;N与S可以存在于同一离子化合物中,如
2 3
(NH)SO 中含有N、S,D项正确。
4 2 4
答案:D
4.解析:a、b、c、d分别为O、Na或Mg、Al、S。A项,原子半径b>c>d>a,错误;B正确;C项,c的氧化物的水化物为氢氧化铝,为两性氢氧化物,不是强碱,错误;D
项,S的氧化性比氧气氧化性弱,错误。
答案:B
5.解析:A项,因O、N、Si元素的非金属性逐渐减弱,所以气态氢化物的稳定性:
HO>NH>SiH ,正确;B项,氢元素与其他元素可形成共价化合物如HO、NH 、SiH 、HS等,
2 3 4 2 3 4 2
也可形成离子化合物如NaH等,正确;C项,HCl的酸性比碳酸强,但不能证明元素的非金属
性:Cl>C,错误;D项,根据元素的原子序数与元素在周期表中位置的规律,可推出第118
号元素在周期表中位于第七周期0族,正确。
答案:C
6.解析:A2+与C原子的电子数相差2,结合四种短周期元素在周期表中的位置判断
A为镁元素,B为铝元素,C为氧元素,D为氯元素。氯化镁属于盐,是强电解质,其水溶液
呈酸性,A错误;与Mg同周期且与O同主族的元素为S,其最高价氧化物对应水化物为硫酸,
浓硫酸在某些化学反应中常作催化剂,B正确;电子层结构相同的离子,核电荷数越大,离
子半径越小,离子半径:O2->Mg2+>Al3+,C正确;氧化铝是冶炼铝的一种原料,D正确。
答案:A
7.解析:根据“W原子的最外层电子数是最内层电子数的3倍”可确定W的最外层
有6个电子,W是S,则X是N,Y是Al,Z是Si。Al、Si、S的最高价氧化物对应水化物分别
是Al(OH) 、HSiO 、HSO ,酸性强弱顺序为HSO>HSiO>Al(OH) ,A错误;NaAlO 溶液
3 2 3 2 4 2 4 2 3 3 2
显碱性,B错误;同周期从左到右,原子半径逐渐减小,第三周期元素的原子半径通常比第
二周期的要大,所以原子半径:r(Al)>r(Si)>r(S)>r(N),C错误;N与S的气态氢
化物分别为NH、HS,二者可相互反应,生成的(NH)S是离子化合物,D正确。
3 2 4 2
答案:D
8.解析:根据题图可推知,X为H,Y为C,Z为N,M为S,R为Na。Na的氧化物为
NaO、NaO,二者均为离子化合物,A项正确;S的氢化物为HS,常温常压下为气体,B项正
2 2 2 2
确;非金属性:N>C,故最高价含氧酸的酸性:HNO >HCO ,C项错误;含碳化合物种类最
3 2 3
多,D项正确。
答案:C
9.解析:由n是元素Z的单质,通常为黄绿色气体,可知Z元素为Cl,n为Cl,再
2
根据q的水溶液具有漂白性,可知q为HClO,由0.01 mol·L-1r溶液的pH为2,可判断r为
一元强酸,则r为HCl,然后根据n和p的反应条件,以及s通常是难溶于水的混合物,可知p为烷烃,s为烷烃的氯代物;根据题意,W、X、Y、Z是短周期原子序数依次增加的四种元
素,可进一步推知W、X、Y、Z分别为H、C、O、Cl。A项,根据原子半径的变化规律,可知
原子半径:HC,
再由CCl 、ClO 中化合价的正负,可知非金属性:O>Cl>C,错误;C项,氧的氢化物可能为
4 2
HO或HO,常温常压下二者均为液态,正确;D项,碳的最高价氧化物的水化物HCO 为弱酸,
2 2 2 2 3
错误。
答案:C
10.解析:本题主要考查原子结构与元素周期律的知识,侧重考查学生元素推断和
知识迁移能力。W、X、Y、Z四种元素依次为O、F、Na、S。氧的非金属性比氟的弱,稳定性:
HOS>O>F,D项错误。
答案:D