文档内容
第1讲 弱电解质的电离平衡
[考纲要求]
1.了解电解质的概念。了解强电解质和弱电解质的概念。
2.了解电解质在水溶液中的电离,以及电解质溶液的导电性。
3.理解弱电解质在水溶液中的电离平衡,能利用电离平衡常数进行计算。
考点一 弱电解质的电离平衡
1知识梳理
1.强、弱电解质的概念
(1)概念
全部电离强电解质,包括______、______、______等部分电离弱电解质,包括______、
______、______等
(2)与化合物类型的关系
强电解质主要是大部分____化合物及某些____化合物,弱电解质主要是某些____化合
物。
[思考]
电离方程式的书写
(1)弱电解质
①多元弱酸分步电离,且第一步电离程度远远________第二步,如HCO 的电离方程式:
2 3
__________________________,______________________。
② 多 元 弱 碱 电 离 方 程 式 一 步 写 成 , 如 Fe(OH) 的 电 离 方 程 式 :
3
________________________。
(2)酸式盐溶液
① 强 酸 的 酸 式 盐 完 全 电 离 , 如 NaHSO 的 电 离 方 程 式 :
4
__________________________________。
②弱酸的酸式盐中酸式酸根不能完全电离,如 NaHCO 的电离方程式:
3
________________________________。
2.弱电解质的电离平衡
(1)电离平衡的建立
在一定条件(如温度、浓度等)下,当弱电解质分子电离成离子的速率和离子结合成弱电解质分子的速率相等时,电离过程就达到平衡。如图所示:
(2)电离平衡的特征
(3)外界条件对电离平衡的影响
①温度:温度升高,电离平衡________移动,电离程度________。
②浓度:稀释溶液,电离平衡________移动,电离程度________。
③同离子效应:加入与弱电解质具有相同离子的强电解质,电离平衡________移动,
电离程度________。
④加入能反应的物质:电离平衡________移动,电离程度________。
[判断] (正确的打“√”,错误的打“×”)
(1)HClO是弱酸,所以NaClO是弱电解质( )
(2)弱电解质溶液中存在溶质分子,而强电解质溶液中不存在溶质分子( )
(3)AgCl的水溶液不导电,而CHCOOH的水溶液能导电,故AgCl是弱电解质,CHCOOH
3 3
是强电解质( )
(4)弱电解质在溶液里达到电离平衡时,分子的浓度和离子的浓度一定相等( )
(5)强电解质的导电能力一定比弱电解质的导电能力强( )
(6)弱电解质一定是共价化合物( )
(7)醋酸在醋酸钠溶液中电离的程度大于在纯水中电离的程度( )
(8)稀释一弱电解质溶液时,溶液中所有粒子浓度都会减小( )
(9)氨气溶于水,当c(OH-)=c(NH+
)时,表明NH·HO电离处于平衡状态( )
4 3 2
[提醒]
电离平衡移动与离子浓度变化1.稀醋酸加水稀释时,溶液中的各离子浓度并不是都减小,如c(OH-)是增大的。
2.电离平衡右移,电解质分子的浓度不一定减小,如稀醋酸中加入冰醋酸。
3.冰醋酸和0.1 mol·L-1的醋酸加水稀释时导电能力的变化曲线示意图,反映了离
子浓度变化趋势。
2对点速练
练点一 电离平衡的移动
1.已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CHCOOH CHCOO-+H+,要使溶液
3 ⇌ 3
中c(H+)/c(CHCOOH)的值增大,可以采取的措施是( )
3
①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸
④加水
A.①② B.①③
C.②④ D.③④
2.将浓度为0.1 mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是( )
c (F− ) c (H+ )
A.c(H+) B.K(HF) C. D.
a c(H+ ) c(HF)
练后整理
以0.1 mol·L-1CHCOOH溶液为例,填写外界条件对CHCOOH CHCOO-+H+ ΔH>0的
3 3 ⇌ 3
影响。
改变条件 平衡移动方向 n(H+) c(H+) 导电能力 K
a
加水稀释 向右 增大 减小 减弱 不变
加入少量
向右 增大 增大 增强 不变
冰醋酸
通入HCl(g) 向左 增大 增大 增强 不变
加NaOH(s) 向右 减小 减小 增强 不变
加
向左 减小 减小 增强 不变
CH3COONa(s)
加入镁粉 向右 减小 减小 增强 不变
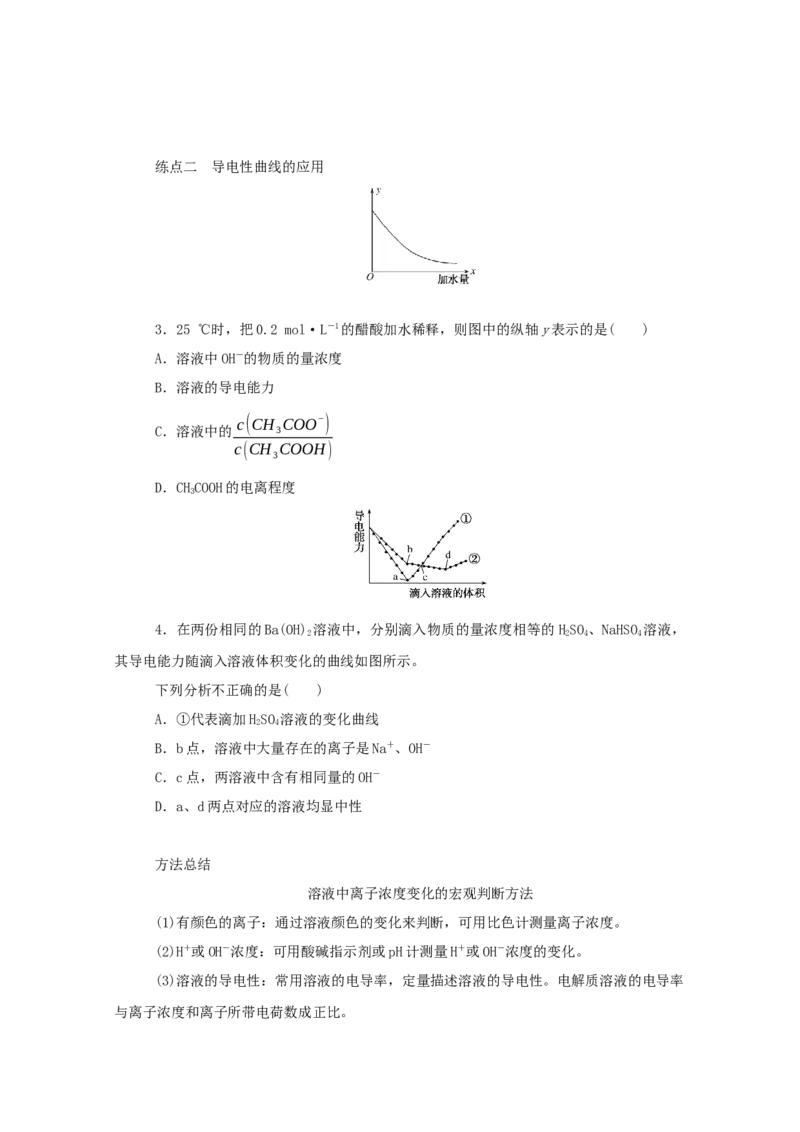
升高温度 向右 增大 增大 增强 增大练点二 导电性曲线的应用
3.25 ℃时,把0.2 mol·L-1的醋酸加水稀释,则图中的纵轴y表示的是( )
A.溶液中OH-的物质的量浓度
B.溶液的导电能力
c(CH COO−)
C.溶液中的 3
c(CH COOH)
3
D.CHCOOH的电离程度
3
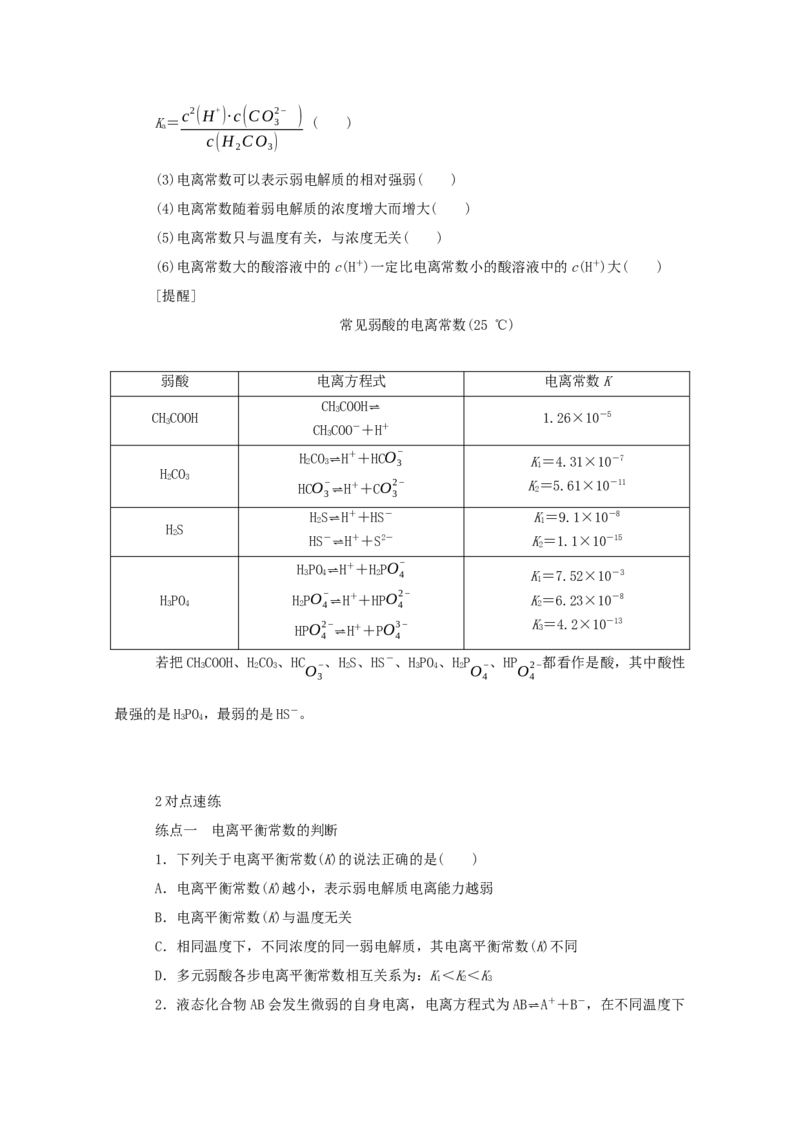
4.在两份相同的Ba(OH) 溶液中,分别滴入物质的量浓度相等的HSO 、NaHSO 溶液,
2 2 4 4
其导电能力随滴入溶液体积变化的曲线如图所示。
下列分析不正确的是( )
A.①代表滴加HSO 溶液的变化曲线
2 4
B.b点,溶液中大量存在的离子是Na+、OH-
C.c点,两溶液中含有相同量的OH-
D.a、d两点对应的溶液均显中性
方法总结
溶液中离子浓度变化的宏观判断方法
(1)有颜色的离子:通过溶液颜色的变化来判断,可用比色计测量离子浓度。
(2)H+或OH-浓度:可用酸碱指示剂或pH计测量H+或OH-浓度的变化。
(3)溶液的导电性:常用溶液的电导率,定量描述溶液的导电性。电解质溶液的电导率
与离子浓度和离子所带电荷数成正比。考点二 电离平衡常数 电离度
1知识梳理
1.电离平衡常数
(1)表达式:
①一元弱酸HA的电离常数:根据HA H++A-,可表示为Ka=__________。
⇌
②一元弱碱BOH的电离常数:根据BOH B++OH-,可表示为K=____________。
⇌ b
(2)意义:相同条件下,K值越大,表示该弱电解质越____电离,所对应的酸性或碱性
相对越____。
(3)特点:多元弱酸是分步电离的,各级电离常数的大小关系是K a1≫K a2≫K
a3
,所以其
酸性主要决定于第____步电离。
2.电离度
(1)概念
在一定条件下的弱电解质达到电离平衡时,已经电离的电解质分子数占原电解分子总
数的百分比。
(2)表示方法
已电离的弱电解质分子数
a= ×100%
溶液中原有弱电解质的总分子数
弱电解质的某离子浓度
也可表示为a= ×100%
弱电解质的初始浓度
(3)影响因素
①相同温度下,同一弱电解质,浓度越大,其电离度(a)越____。
②相同浓度下,同一弱电解质,温度越高,其电离度(a)越____。
[判断] (正确的打“√”,错误的打“×”)
(1)电离平衡右移,电离常数一定增大( )
(2)HCO 的电离常数表达式:
2 3c2(H+)·c(CO2− )
K= 3 ( )
a
c(H CO )
2 3
(3)电离常数可以表示弱电解质的相对强弱( )
(4)电离常数随着弱电解质的浓度增大而增大( )
(5)电离常数只与温度有关,与浓度无关( )
(6)电离常数大的酸溶液中的c(H+)一定比电离常数小的酸溶液中的c(H+)大( )
[提醒]
常见弱酸的电离常数(25 ℃)
弱酸 电离方程式 电离常数K
CHCOOH
3 ⇌
CHCOOH 1.26×10-5
3
CHCOO-+H+
3
H 2 CO 3⇌
H++HCO−
3 K 1 =4.31×10-7
HCO
2 3
HCO− 3⇌ H++CO 3 2− K 2 =5.61×10-11
HS H++HS- K=9.1×10-8
2 ⇌ 1
HS
2
HS- H++S2- K=1.1×10-15
⇌ 2
HPO
H++HPO−
3 4⇌ 2 4 K=7.52×10-3
1
HPO HPO− H++HPO2− K=6.23×10-8
3 4 2 4⇌ 4 2
HPO2− H++PO3− K 3 =4.2×10-13
4 ⇌ 4
若把CHCOOH、HCO 、HC 、HS、HS-、HPO 、HP 、HP 都看作是酸,其中酸性
3 2 3 O− 2 3 4 2 O− O2−
3 4 4
最强的是HPO,最弱的是HS-。
3 4
2对点速练
练点一 电离平衡常数的判断
1.下列关于电离平衡常数(K)的说法正确的是( )
A.电离平衡常数(K)越小,表示弱电解质电离能力越弱
B.电离平衡常数(K)与温度无关
C.相同温度下,不同浓度的同一弱电解质,其电离平衡常数(K)不同
D.多元弱酸各步电离平衡常数相互关系为:K<K<K
1 2 3
2.液态化合物AB会发生微弱的自身电离,电离方程式为AB A++B-,在不同温度下
⇌其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是( )
A.c(A+)随温度升高而降低
B.35 ℃时,c(A+)>c(B-)
C.AB的电离程度:α(25 ℃)>α(35 ℃)
D.AB的电离是吸热过程
3.已知25 ℃时有关弱酸的电离平衡常数如下表:
下列推断正确的是( )
A.HX、HY两种弱酸的酸性:HX>HY
B.相同条件下溶液的碱性:NaX>NaCO>NaY>NaHCO
2 3 3
C.向NaCO 溶液中加入足量HY,反应的离子方程式:HY+C ===HC +Y-
2 3 O2− O−
3 3
D.HX和HY酸性相同,都比HCO 弱
2 3
弱酸化学式 HX HY HCO
2 3
K=4.4×10-7
1
电离平衡常 7.8×10- 3.7×10-
数 9 15 K 2 =4.7×10-
11
归纳总结
电离平衡常数的四大应用
(1)判断弱酸(或弱碱)的相对强弱,电离常数越大,酸性(或碱性)越强。
(2)判断盐溶液的酸性(或碱性)强弱,电离常数越大,对应的盐水解程度越小,碱性
(或酸性)越弱。
(3)判断复分解反应能否发生,一般符合“强酸制弱酸”规律。
(4)判断微粒浓度比值的变化。
练点二 电离平衡常数的计算
4.常温常压下,空气中的CO 溶于水,达到平衡时,溶液的pH=5.60,c(HCO)=
2 2 3
1.5×10-5。若忽略水的电离及 HCO 的第二级电离,则 HCO HC +H+的平衡常数
2 3 2 3⇌ O−
3
K≈________(结果保留一位小数)。(已知:10-5.60=2.5×10-6)
1
5.已知25 ℃时弱电解质电离平衡常数:
K(CHCOOH)=1.8×10-5,K(HSCN)=0.13。
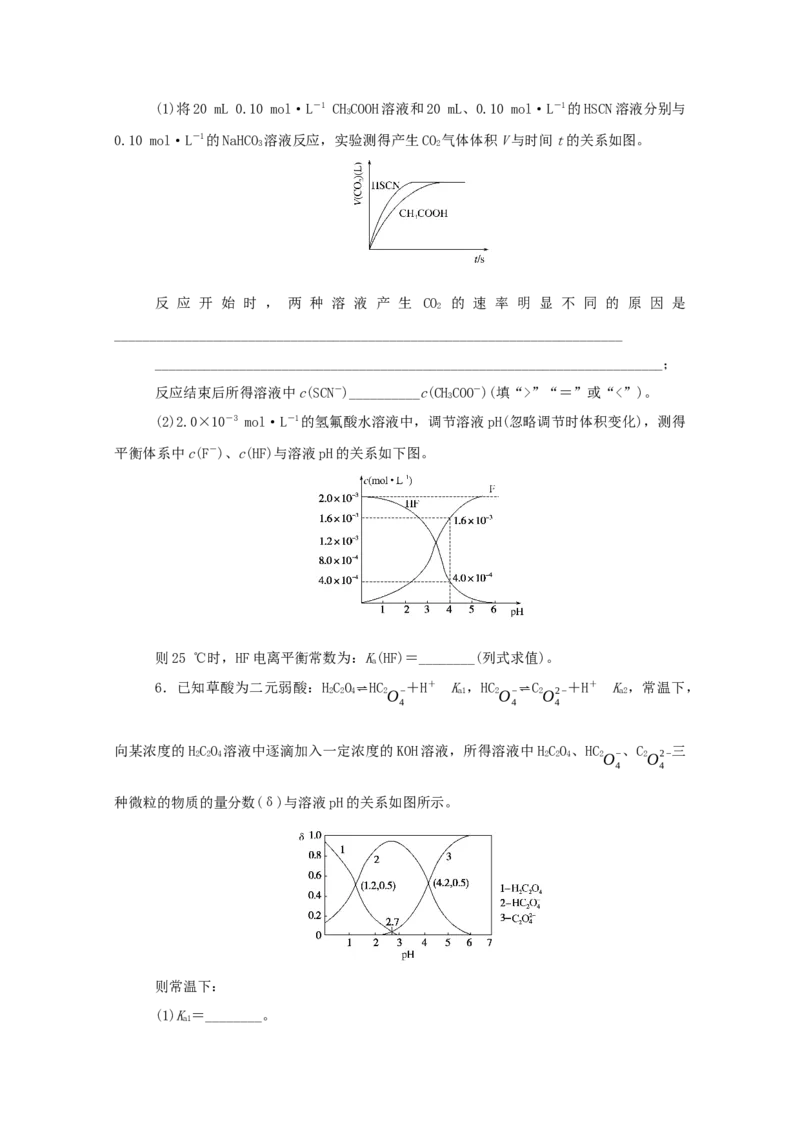
a 3 a(1)将20 mL 0.10 mol·L-1 CHCOOH溶液和20 mL、0.10 mol·L-1的HSCN溶液分别与
3
0.10 mol·L-1的NaHCO 溶液反应,实验测得产生CO 气体体积V与时间t的关系如图。
3 2
反 应 开 始 时 , 两 种 溶 液 产 生 CO 的 速 率 明 显 不 同 的 原 因 是
2
________________________________________________________________________
________________________________________________________________________;
反应结束后所得溶液中c(SCN-)__________c(CHCOO-)(填“>”“=”或“<”)。
3
(2)2.0×10-3 mol·L-1的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得
平衡体系中c(F-)、c(HF)与溶液pH的关系如下图。
则25 ℃时,HF电离平衡常数为:K(HF)=________(列式求值)。
a
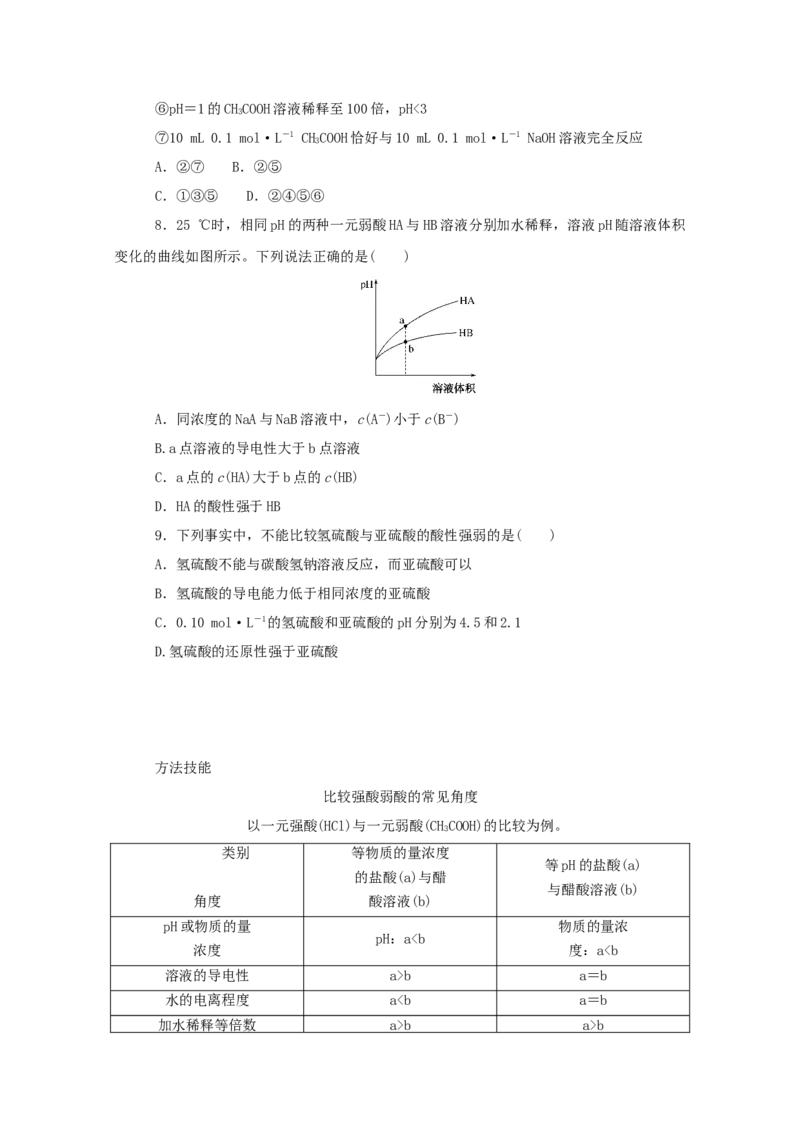
6.已知草酸为二元弱酸:HCO HC +H+ K ,HC C +H+ K ,常温下,
2 2 4⇌ 2O− a1 2O−⇌ 2O2− a2
4 4 4
向某浓度的HCO 溶液中逐滴加入一定浓度的KOH溶液,所得溶液中HCO 、HC 、C 三
2 2 4 2 2 4 2O− 2O2−
4 4
种微粒的物质的量分数(δ)与溶液pH的关系如图所示。
则常温下:
(1)K=________。
a1(2)K=________。
a2
c2 (HC O− )
(3)pH=2.7时,溶液中 2 4 =________。
c(H C O )·c(C O2− )
2 2 4 2 4
方法总结
电离常数计算的两种方法(以弱酸HX为例)
1.已知c(HX) 和c(H+),求电离常数
始
由于弱酸只有极少一部分电离,c(H+)的数值很小,可做近似处理:c(HX) -c(H
始
+)≈c(HX) ,则K=
c2 (H+
) ,代入数值求解即可。
始 a
c(HX)
始
2.已知c(HX) 和电离常数,求c(H+)
始
同理可得K= c2 (H+ ) ≈ c2 (H+ ) ,
a
c(HX) −c(H+ ) c(HX)
始 始
则:c(H+)=, 代入数值求解即可。
√K ·c(HX)
a 始
练点三 电离平衡与酸碱性的强弱判断方法
7.下列事实中一定不能证明CHCOOH是弱酸的是( )
3
①常温下某CHCOONa溶液的pH=8
3
②用CHCOOH溶液做导电实验,灯泡很暗
3
③等pH等体积的盐酸、CHCOOH溶液和足量锌反应,CHCOOH放出的氢气较多
3 3
④pH=1的CHCOOH溶液和pH=13的KOH溶液等体积混合,溶液呈酸性
3
⑤CHCOONa和稀HPO 反应,生成CHCOOH
3 3 4 3⑥pH=1的CHCOOH溶液稀释至100倍,pH<3
3
⑦10 mL 0.1 mol·L-1 CHCOOH恰好与10 mL 0.1 mol·L-1 NaOH溶液完全反应
3
A.②⑦ B.②⑤
C.①③⑤ D.②④⑤⑥
8.25 ℃时,相同pH的两种一元弱酸HA与HB溶液分别加水稀释,溶液pH随溶液体积
变化的曲线如图所示。下列说法正确的是( )
A.同浓度的NaA与NaB溶液中,c(A-)小于c(B-)
B.a点溶液的导电性大于b点溶液
C.a点的c(HA)大于b点的c(HB)
D.HA的酸性强于HB
9.下列事实中,不能比较氢硫酸与亚硫酸的酸性强弱的是( )
A.氢硫酸不能与碳酸氢钠溶液反应,而亚硫酸可以
B.氢硫酸的导电能力低于相同浓度的亚硫酸
C.0.10 mol·L-1的氢硫酸和亚硫酸的pH分别为4.5和2.1
D.氢硫酸的还原性强于亚硫酸
方法技能
比较强酸弱酸的常见角度
以一元强酸(HCl)与一元弱酸(CHCOOH)的比较为例。
3
类别 等物质的量浓度
等pH的盐酸(a)
的盐酸(a)与醋
与醋酸溶液(b)
角度 酸溶液(b)
pH或物质的量 物质的量浓
pH:ab a=b
水的电离程度 ab a>bpH的变化量
等体积溶液中和
a=b ab 相同
的速率
等体积溶液与过
量活泼金属产生 相同 aK(CHCOOH),溶液中c(H+):HSCN>CHCOOH,c(H
2 a a 3 3
+)大反应速率快。反应结束后,溶质为 CHCOONa和NaSCN,因CHCOOH酸性弱于HSCN,故
3 3
CHCOONa水解程度大,c(CHCOO-)K(CHCOOH),溶液中c(H+):HSCN>CHCOOH,c(H+)大反应速
a a 3 3
率快 >
c(H+ )·c(F-
)
1×10-4×1.6×10-3
(2)K(HF)= = =4×10-4
a c(HF) 4.0×10-4
6.解析:(1)由图像可以知道pH=1.2时,c(HCO− )=c(HCO),则K =c(H+)=10-
2 4 2 2 4 a1
1.2。(2)pH=4.2时,c(HCO− )=c(CO2− ),则K=c(H+)=10-4.2。
2 4 2 4 a2
C2(H C O−) K 10-1.2
(3)由电离常数表达式可以知道 2 2 4 = a1 = =103=1
C(H C O )·C(C O2− ) K 10-4.2
2 2 4 2 4 a2
000。
答案:(1)10-1.2 (2)10-4.2 (3)1 000
7.解析:①说明溶液水解呈碱性,应为强碱弱酸盐,可证明 CHCOOH是弱酸,正确;
3
②只能说明溶液离子浓度较小,错误;③说明醋酸还可电离出氢离子,可证明 CHCOOH是弱
3
酸,正确;④说明醋酸有剩余,即醋酸没有完全电离,可以证明 CHCOOH是弱酸,正确;⑤
3
说明醋酸的酸性比磷酸弱,而磷酸为中强酸,则醋酸为弱酸,正确;⑥说明存在电离平衡,
证明CHCOOH是弱酸,正确;⑦只能说明一元酸碱恰好反应,不能说明醋酸是弱酸,错误。
3
答案:A
8.解析:由于稀释过程中HA的pH变化较大,故HA的酸性强于HB,D项正确;酸的酸性越强,对应的盐的水解程度越小,故NaB的水解程度大,同浓度的NaA与NaB溶液中c(B-)
小于c(A-),A项错误;b点溶液的pH小于a点溶液的pH,说明b点溶液中c(H+)较大、c(B
-)较大,故溶液导电性较强,B项错误;稀释相同倍数时,HA的电离程度较大,故a点的
c(HA)小于b点的c(HB),C项错误。
答案:D
9.解析:HSO 能和NaHCO 反应放出CO,说明酸性:HSO>HCO,而HS不能和NaHCO
2 3 3 2 2 3 2 3 2 3
反应,说明酸性:HSCHCOOH,则曲线Ⅰ代表CHCOOH溶液,曲线Ⅱ代表
2 3 3
HNO 溶液,A项错误;当稀释相同倍数时,b点溶液中c(H+)大于c点,对水的电离的抑制作
2
c(HA)·c(OH− ) K
用:b点>c点,所以水的电离程度:b点c(HNO),同体积的两种酸溶液分别与NaOH恰好中和后,溶液中n(Na+)不同,
3 2
D项错误。
答案:C
3.解析:0.1 mol·L-1的NH·HO中c(OH-)小于0.1 mol ·L-1,说明部分电离,A
3 2
项正确;0.1
mol·L-1的NHCl溶液呈酸性,说明NH+
水解,B项正确;同浓度时,氨水的导
4 4
电能力弱于一元强碱,说明部分电离,C项正确;D项,只能说明NH·HO显碱性,不能说明
3 2
其是弱碱,错误。
答案:D
4.解析:A.只能证明乙酸具有酸性,不能证明其酸性强弱,错误;B.该盐水溶液显碱
性,由于NaOH是强碱,故可以证明乙酸是弱酸,正确;C.可以证明乙酸的酸性比碳酸强,但
是不能证明其酸性强弱,错误;D.可以证明乙酸具有酸性,但是不能证明其酸性强弱,错误。
答案:B5.解析:根据甲、乙的电离平衡常数可得,这两种物质都是弱电解质,在温度不变、
浓度相等时,电离程度CHCOOH