文档内容
第 14 讲 钠及其化合物的计算与实验探究
复习目标 1.多角度认识NaO 与HO、CO 的反应。2.掌握NaCO 、NaHCO 与盐酸反应
2 2 2 2 2 3 3
的原理与定量分析。3.学会用实验的方法测定NaCO 的质量分数。
2 3
考点一 Na O 与 H O、CO 的反应规律与实验探究
2 2 2 2
1.NaO 与CO、HO的反应规律
2 2 2 2
NaO 与CO 、HO(g)的混合气体反应,可看作NaO 先与CO 反应,完毕后再与HO(g)反
2 2 2 2 2 2 2 2
应。
2.气体体积关系
若CO 和水蒸气的混合气体(或单一气体)通过足量NaO ,气体体积的减少量等于原混合气
2 2 2
体体积的且等于生成氧气的体积,即ΔV=V(O )=V(混合)。
2
3.电子转移关系
当 NaO 与 CO 、HO 反应时,物质的量关系为 2NaO ~O ~2e-,n(e-)=n(Na O)=
2 2 2 2 2 2 2 2 2
2n(O )。
24.固体质量关系
相当于固体(Na O)只吸收了CO 中的“CO”、HO中的“H”,可以看作发生相应的反应:
2 2 2 2 2
NaO +CO===NaCO 、NaO +H===2NaOH(实际上两反应不能发生),所以固体增加的质
2 2 2 3 2 2 2
量Δm(CO)=28 g·mol-1×n(CO),Δm(H O)=2 g·mol-1×n(H O)。
2 2 2 2
题组一 NaO 与HO、CO 反应的定量分析
2 2 2 2
1.用单线桥分析NaO 与水反应中电子转移的方向和数目:___________________________。
2 2
(1)氧化剂和还原剂是____________________________,氧化产物是_____________________,
还原产物是_____________________________________________________________________。
(2)Na O 与CO 反应时,生成0.1 mol氧气时,转移的电子数________。
2 2 2
答案
(1)Na O O NaOH
2 2 2
(2)0.2N (或1.204×1023)
A
2.下列物质均为a g,将它们在氧气中完全燃烧的产物全部通入到足量的过氧化钠固体中,
则过氧化钠固体增重为a g的是( )
①CO ②H ③CH ④HCHO ⑤CHCOOH ⑥HCOOH
2 4 3
A.①②⑤⑥ B.②③④⑤
C.①②④⑤ D.①②③⑤
答案 C
解析 H 、CO发生反应的化学方程式为 2H +O=====2HO,2Na O +2HO===4NaOH+
2 2 2 2 2 2 2
O↑;2CO+O=====2CO,2NaO+2CO===2NaCO+O,由反应方程式可知,过氧化钠
2 2 2 2 2 2 2 3 2
增加的质量即为H、CO的质量。因此只要是CO或H 或它们的混合气体或化学式组成符合
2 2
(CO) ·(H ),则过氧化钠固体增重质量等于原物质的质量,则①②符合,而④HCHO可以改
m 2 n
写成CO·H ,⑤CHCOOH可以改写成(CO) ·(H ) ,⑥HCOOH可以改写成CO·H ,故⑥不
2 3 2 2 2 2 2
符合,①②④⑤符合,故选C。
3.将一定量的NaO 和NaHCO 混合后,在密闭容器中加热充分反应,排出气体,冷却后
2 2 3
有固体物质剩余,下列选项不正确的是( )
选项 剩余的固体物质
A 1 2 NaCO
2 3
B 1.5 2 NaO、NaCO
2 2 2 3
C 2 1 NaO、NaOH、NaCO
2 2 2 3
D 2 2 NaOH、NaCO
2 3答案 B
解 析 将 NaO 与 NaHCO 的 混 合 物 加 热 , 有 关 反 应 的 化 学 方 程 式 依 次 为
2 2 3
2NaHCO =====NaCO + CO↑ + HO 、 2CO + 2NaO===2NaCO + O 、 2NaO +
3 2 3 2 2 2 2 2 2 3 2 2 2
2HO===4NaOH+O↑。当NaO 与NaHCO 的物质的量之比为1∶2时,二者反应的总方程
2 2 2 2 3
式为2NaO +4NaHCO =====4NaCO +O↑+2HO;当NaO 与NaHCO 的物质的量之比
2 2 3 2 3 2 2 2 2 3
为1∶1时,二者反应的总方程式为2NaO +2NaHCO =====2NaCO +O↑+2NaOH,即当
2 2 3 2 3 2
n(Na O)∶ n(NaHCO )≤1∶2 时 , 反 应 后 剩 余 固 体 为 NaCO , 当
2 2 3 2 3
1∶21∶1时,反应后剩余固体为NaO 、NaOH、NaCO ,由此可以判断
2 2 3 2 2 2 3
A、C、D正确,B错误。
ω g化学式符合通式(CO) ·(H ) 的物质(其中m、n为自然数)在O 中充分燃烧后,将其产物
m 2 n 2
通过足量的NaO 固体,反应完毕,固体增重ω g。
2 2
中学阶段常见符合这一关系的物质有
①无机物:H、CO及H 和CO的混合气体;
2 2
②有机物:CHOH(甲醇)、HCHO(甲醛)、CHCOOH(乙酸)、HCOOCH (甲酸甲酯)、
3 3 3
C H O(葡萄糖)等。
6 12 6
题组二 过氧化钠性质实验探究
4.比较下列四组反应,回答下列问题:
第一组:①NaO+CO ②NaO+SO
2 2 2 2 2 2
第二组:③NaO+FeCl (溶液) ④NaO+FeCl (溶液)
2 2 3 2 2 2
第三组:⑤SO 通入品红溶液中,加热 ⑥NaO 加入品红溶液中,加热
2 2 2
第四组:⑦NaOH溶液滴入紫色石蕊溶液中 ⑧NaO 固体加入紫色石蕊溶液中
2 2
(1) 若 第 一 组 ② 不 产 生 气 体 , 用 化 学 方 程 式 解 释 原 因 :
__________________________________
_______________________________________________________________________________
。
(2)预测第二组中③④的现象是否可能相同:_________________________________________。
(3)预测⑤⑥反应中可能产生的现象并分析原因。
(4)预测⑦⑧反应中可能产生的现象并分析原因。
答案 (1)Na O+SO ===NaSO
2 2 2 2 4
(2)可能相同
(3)⑤溶液红色褪去,加热后又恢复红色;⑥溶液红色褪去,加热后不能恢复红色。前者是
因为SO 与品红溶液生成的无色物质不稳定,受热易分解;后者是因为NaO 具有强氧化性,
2 2 2
将品红溶液氧化为无色。(4)⑦溶液变蓝,⑧溶液先变蓝后褪色。前者是因为NaOH溶液呈碱性,使紫色石蕊溶液变
蓝;后者是因为NaO 与HO反应生成NaOH,溶液呈碱性,同时NaO 又有漂白性。
2 2 2 2 2
5.某课外活动小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。
(1)过氧化钠与二氧化碳反应的化学方程式是_______________________________________,
该反应中,反应物的总能量________(填“大于”或“小于”)生成物的总能量。
(2)装置Ⅰ中的试剂是________(填字母)。
a.稀盐酸 b.稀硫酸
c.小苏打 d.石灰石
(3)实验时,应先打开弹簧夹________(填“K”或“K”),观察到预期现象后,关闭它,再
1 2
打开另一个弹簧夹。
(4)实验过程中将带火星的木条置于a口,观察到带火星的木条始终不复燃。
①为观察到最终木条复燃,甲建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是
________________________________________________________________________。
②乙认为即使采纳甲的建议且最终观察到木条复燃,也不能证明 CO 参与了反应,原因是
2
________________________________________________________________________。
(5)为进一步达到实验目的,应补充的实验是:取最终反应后 Ⅲ中所得固体,
________________________________________________________________________。
答案 (1)2Na O+2CO===2NaCO+O 大于
2 2 2 2 3 2
(2)bc (3)K
2
(4)①除去未充分反应的CO
2
②水与NaO 反应生成O
2 2 2
(5)加入稀盐酸,将产生的气体通入澄清石灰水中(答案合理即可)
解析 (1)此反应是放热反应。
(2)依据实验目的,需要干燥CO,所以装置Ⅰ是制取CO 的装置,因为盐酸易挥发出HCl,
2 2
所以应选择稀硫酸、小苏打。
(3)先通干燥CO,再通湿润CO 进行对比。
2 2
(5)证明反应后固体中含有CO。
6.现有一定量含有NaO杂质的NaO 试样,用如图所示实验装置测定NaO 试样的纯度。
2 2 2 2 2
(可供选用的反应物只有CaCO 固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
3回答下列问题:
(1)装置A中液体试剂选用______________________________________________________。
(2)装置B的作用是____________________________________________________________,
装置E中碱石灰的作用是______________________________________________________。
(3)装置D中发生反应的化学方程式为___________________________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则
NaO 试样的纯度为________。
2 2
答案 (1)6 mol·L-1盐酸
(2)除去气体中的HCl 吸收装置D中反应剩余的CO
2
(3)2Na O+2CO===2NaCO+O、NaO+CO===NaCO
2 2 2 2 3 2 2 2 2 3
(4)78%
解析 (1)A是用来制取二氧化碳的装置,碳酸钙和硫酸反应时,生成的硫酸钙微溶于水,
会覆盖在碳酸钙的表面,使反应不能继续进行,所以用盐酸而不用硫酸来反应,故装置A
中液体试剂选用6 mol·L-1盐酸。
(2)碳酸钙和盐酸反应生成的二氧化碳中含有氯化氢气体,可用饱和碳酸氢钠溶液来除去;
装置E中碱石灰的作用是吸收二氧化碳,防止二氧化碳对氧气的体积测量造成干扰。
(3)装置D中含有氧化钠和过氧化钠,CO 分别与它们发生反应。
2
(4)根据反应2NaO +2CO===2Na CO +O ,反应结束后测得气体体积为224 mL(标准状况),
2 2 2 2 3 2
即生成的氧气的物质的量为=0.01 mol,则过氧化钠的物质的量为0.02 mol,故试样中过氧
化钠的纯度为×100%=78%。
考点二 Na CO 、NaHCO 与酸反应图像及计算
2 3 3
1.NaCO、NaHCO 与足量盐酸反应的比较
2 3 3
二者浓度相同时生成CO 的速率 NaHCO 快
2 3
二者等质量 NaCO 耗酸多
2 3
耗酸量
二者等物质的量 NaCO 耗酸多
2 3
生成CO 的体积 二者等质量 NaHCO 产生的多
2 3二者等物质的量 相等
2.依据图像特点判断溶液溶质成分的方法
(1)化学原理:向碳酸钠溶液中逐滴滴加稀盐酸至过量,依次发生①CO+H+===HCO、
②HCO+H+===HO+CO↑,①②完成时消耗盐酸的量相等。
2 2
(2)图像分析
依据图像特点判断溶液溶质成分
涉及离子方程式Oa:CO+H
若V(Oa)=V(ab)(即Oa
+===HCO
段与ab段消耗盐酸的 溶液中的溶质为NaCO
2 3
ab:HCO+H+===HO+
2
体积相同)
CO↑
2
涉及离子方程式Oa:OH-+
若V(Oa)>V(ab)(即Oa H+===HO
2
溶液中的溶质为NaCO
2 3
段消耗盐酸的体积大于 CO+H+===HCO
和 NaOH
ab段消耗盐酸的体积) ab:HCO+H+===HO+
2
CO↑
2
涉及离子方程式Oa:
若V(Oa)V ,据此判断溶液中溶质的成
1 2 1
分是NaCO 和NaHCO 。根据NaCO +HCl===NaHCO +NaCl,NaHCO +HCl===NaCl+
2 3 3 2 3 3 3
HO+CO↑,可知NaHCO 和NaCO 的物质的量之比等于两个过程分别消耗盐酸的体积之
2 2 3 2 3
比,则n(NaHCO )∶n(Na CO)=(150 mL-50 mL-50 mL)∶50 mL=1∶1。
3 2 3
(3)当加入150 mL盐酸时,恰好完全反应,此时溶液中溶质为NaCl。据物料守恒有n(NaOH)
=n(Na+)=n(Cl-)=0.2 mol·L-1×0.15 L=0.03 mol,所以原氢氧化钠溶液的物质的量浓度为
=1.5 mol·L-1。
考点三 Na CO 的制备和质量分数测定
2 3
一、侯氏制碱法
1.制备原料
食盐、氨气、二氧化碳——合成氨厂用水煤气制取氢气时的废气;其反应为 C+
HO(g)=====CO+H,CO+HO(g)=====CO+H。
2 2 2 2 2
2.工艺流程
3.反应原理
(1)产生NaHCO 的反应:
3
NH + NaC l + CO + H O == = NaHCO ↓ + NH Cl。
3 2 2 3 4
(2)产生NaCO 的反应:
2 3
2NaHCO =====NaCO+HO+CO↑。
3 2 3 2 2
4.绿色思想
循环使用的物质为CO、饱和食盐水。
2
二、测定碳酸钠质量分数的常用方法
1.气体法(1)测定原理:NaCO+HSO ===NaSO +HO+CO↑。
2 3 2 4 2 4 2 2
依据CO 的体积确定NaCO 的物质的量,进而确定纯碱中NaCO 的含量。
2 2 3 2 3
(2)实验操作:向m g纯碱样品中加入足量的稀硫酸,准确测量产生 CO 气体的体积为V
2
mL(已折算为标准状况)。
(3)数据处理
纯碱样品中NaCO 的质量为 mol×106 g·mol-1= g,则纯碱样品中NaCO 的质量分数为
2 3 2 3
×100%=%。
2.沉淀法
(1)测定原理:NaCO+BaCl ===BaCO ↓+2NaCl。
2 3 2 3
依据BaCO 沉淀的质量,确定NaCO 的物质的量,进而确定纯碱中NaCO 的含量。
3 2 3 2 3
(2)实验操作:先将m g纯碱样品溶于水配成溶液,向溶液中加入过量的BaCl 溶液,经过滤、
2
洗涤、干燥得BaCO 沉淀的质量为n g。
3
(3)数据处理
纯碱样品中NaCO 的质量为×106 g·mol-1= g,则纯碱样品中NaCO 的质量分数为×100%
2 3 2 3
=×100%。
题组一 侯氏制碱法
1.以下是在实验室模拟“侯氏制碱法”生产流程的示意图:
―――→――――――→――→――→
则下列叙述错误的是( )
A.A气体是NH ,B气体是CO
3 2
B.侯氏制碱法的工艺过程中应用了物质溶解度的差异
C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D.第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶
答案 D
解析 A项,利用NH 极易溶于水,且水溶液显碱性,可以提高CO 的吸收,因此先通NH
3 2 3
后通CO ,正确;B项,NaHCO 的溶解度小于NaCO 的溶解度,利用了溶解度的差异,正
2 3 2 3
确;C项,操作Ⅲ是过滤,因此用到玻璃仪器:烧杯、漏斗、玻璃棒,正确;D项,晶体是
NaHCO ,利用NaHCO 的不稳定性,2NaHCO =====NaCO+CO↑+HO,错误。
3 3 3 2 3 2 2
2.实验室模拟侯氏制碱法制取纯碱和氯化铵溶液,下列有关操作错误的是( )A.图1为制取氨气将其溶于饱和食盐水
B.图2为过滤获得碳酸钠晶体
C.图3为灼烧碳酸氢钠制取碳酸钠
D.图4为蒸发浓缩氯化铵溶液
答案 B
解析 A项,用氯化铵和氢氧化钙共热制备氨气,正确;B项,侯氏制碱法中溶液析出的晶
体为碳酸氢钠,故应过滤获得碳酸氢钠,错误;C项,在坩埚中灼烧碳酸氢钠分解制备碳酸
钠,正确;D项,蒸发皿中蒸发浓缩氯化铵溶液,并不断搅拌,正确。
题组二 NaCO 质量分数的测定
2 3
3.为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W g样品进行实验,
下列实验方法所对应的实验方案和测量数据合理的是( )
选项 实验方法 实验方案 测量数据
将样品配成100 mL溶液,取10 mL,加入
A 滴定法 消耗盐酸的体积
酚酞,用标准盐酸滴定
将样品与盐酸反应,生成的气体全部被碱
B 量气法 碱石灰增加的质量
石灰吸收
将样品放入烧瓶中,置于电子天平上,加
C 重量法 减少的质量
入足量盐酸
将样品与盐酸反应,气体通过排水量气装
D 量气法 排出水的体积
置量气
答案 A
解析 用酚酞作指示剂时,NaCO 与盐酸发生反应 NaCO +2HCl===2NaCl+CO↑+
2 3 2 3 2
HO,依据消耗盐酸的量可以计算出样品中NaCO 的量,进而确定样品中NaCO 的质量分
2 2 3 2 3
数,A项正确;测量碱石灰增重的方法是重量法而不是量气法,B项错误;样品中加入足量
盐酸,因盐酸的质量未知,无法通过重量法测量NaCO 的质量,C项错误;因部分CO 能
2 3 2
溶解到水里,与水反应生成HCO,故排出水的体积并不是CO 的体积,D项错误。
2 3 2
4.(2020·河南安阳模拟)为了测定NaCl、NaCO·10H O和NaHCO 的混合物中各组分的含
2 3 2 3
量,某同学设计如下实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,
测定该混合物中各组分的质量分数。下列说法中错误的是( )
A.①②③中可以依次盛装碱石灰、无水CaCl 、碱石灰
2
B.硬质玻璃管加热前,应关闭b,打开a,缓缓通入空气,直至a处出来的空气不再使澄清石灰水变浑浊为止
C.若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏大
D.实验过程中一直通入空气,停止加热后再停止通入空气
答案 C
解析 根据实验目的和装置的连接顺序可知:装置①用于吸收空气中的CO 和水蒸气,可以
2
使用碱石灰;装置②吸收 NaCO·10H O 和 NaHCO 分解生成的水蒸气,可以使用无水
2 3 2 3
CaCl ;装置③吸收碳酸氢钠分解生成的CO ,使用碱石灰,A项正确;实验前必须将装置
2 2
中的水蒸气和CO 赶净,避免影响测定结果,硬质玻璃管加热前,应关闭 b,打开a,缓缓
2
通入空气,直至a处出来的空气不再使澄清石灰水变浑浊为止,B项正确;若将①装置换成
盛放NaOH溶液的洗气瓶,则会增加水的质量,使测得NaCO·10H O和NaHCO 的含量偏
2 3 2 3
高,NaCl的含量偏低,C项错误;实验过程中一直通入空气,停止加热后继续通入空气使
存留在装置中的CO 和水蒸气完全被吸收,D项正确。
2
5.小苏打长期放置在空气中会变质(部分转变为NaCO),某研究小组欲测定某小苏打样品
2 3
中NaHCO 的质量分数,设计如下实验方案:
3
Ⅰ.加热分解法
利用图1装置,充分加热小苏打样品。
(1)仪器a的名称为_____________________________________________________________。
(2)在实验过程中,需要测量的实验数据如下:
①仪器a的质量;②_____________________;③________________。
Ⅱ.测量气体体积法
利用图2装置,测定反应生成气体的体积。
(3)组装好仪器后,首先进行的操作为______________________________________________。
(4)导管g的作用为______________________________________________________________。
(5)为了减小实验误差,B、C中最好用____________溶液代替水。
(6)待反应结束,气体冷却至室温后,利用图示装置读取气体体积时,应注意的事项如下:
①________________________________________________________________________。
②________________________________________________________________________。
(7)若所取样品的质量为m g,反应前量气管C的读数为V mL,反应结束后量气管C的读
1
数为V mL,则样品中NaHCO 和NaCO 的物质的量之和为________(气体体积均已换算为
2 3 2 3
标准状况下的体积)。答案 (1)坩埚 (2)②加热前,仪器a和样品的总质量 ③加热冷却后,仪器a和残留物的
总质量
(3)检查装置气密性
(4)平衡分液漏斗与锥形瓶内的气压,使液体顺利流下;滴入锥形瓶的稀硫酸的体积等于进
入分液漏斗的气体体积,从而消除因加入稀硫酸而引起的气体体积误差
(5)饱和NaHCO
3
(6)①读数时应上下移动C管,使B、C两管液面相平
②视线与液面最低处相平
(7) mol
解析 (7)根据碳原子守恒,1 mol碳原子对应1 mol二氧化碳,二氧化碳的物质的量为 mol,
所以样品中NaHCO 和NaCO 的物质的量之和为 mol。
3 2 3
1.NaO 是中学化学常用试剂,下列说法错误的是( )
2 2
A.0.1 mol Na O 与足量CO 反应转移的电子的物质的量为0.1 mol
2 2 2
B.NaO 与SO 反应生成NaSO 和O
2 2 2 2 3 2
C.等物质的量的NaO 与NaO溶于等质量水中得到的NaOH的物质的量浓度相同
2 2 2
D.等质量的NaO 与NaS晶体中含有相同数目的阴离子
2 2 2
答案 B
2.(2019·湖北黄石二中周测)有关碱金属的叙述正确的是( )
A.随核电荷数的增加,碱金属单质的熔点逐渐降低,密度逐渐增大
B.碱金属单质的金属性很强,均易与Cl、O、N 等发生反应
2 2 2
C.CsCO 用酒精灯加热时不能分解为CO 和CsO
2 3 2 2
D.无水硫酸铯的化学式为CsSO ,它不易溶于水
2 4
答案 C
3.下列有关NaCO 和NaHCO 的叙述中正确的是( )
2 3 3
A.向NaCO 溶液中逐滴加入等物质的量的稀盐酸,生成的 CO 与原NaCO 的物质的量之
2 3 2 2 3
比为1∶2
B.等质量的NaHCO 和NaCO 分别与足量盐酸反应,在同温同压下,生成的CO 体积相同
3 2 3 2
C.物质的量浓度相同时,NaCO 溶液的pH小于NaHCO 溶液
2 3 3
D.向NaCO 饱和溶液中通入CO,有NaHCO 晶体析出
2 3 2 3
答案 D
解析 根据化学方程式NaCO +HCl===NaCl+NaHCO ,当碳酸钠和盐酸物质的量相等时,
2 3 3
不会产生二氧化碳,A 项错误;NaHCO 和 NaCO 都与盐酸反应生成二氧化碳气体:
3 2 3
NaCO +2HCl===2NaCl+HO+CO↑,NaHCO +HCl===NaCl+HO+CO↑,等质量的
2 3 2 2 3 2 2
NaCO 和NaHCO 分别与过量盐酸反应,放出CO 的质量不相等,所以同温同压下,生成
2 3 3 2CO 的体积不一样,B项错误;在NaCO 、NaHCO 溶液中,碳酸根离子和碳酸氢根离子均
2 2 3 3
能水解,导致溶液呈碱性,但是碳酸根离子水解程度大,所以碳酸钠的碱性强于碳酸氢钠,
即NaCO 溶液的pH大于NaHCO 溶液的pH,C项错误;向NaCO 饱和溶液中通入CO ,
2 3 3 2 3 2
会发生反应 NaCO +CO +HO===2NaHCO ↓,常温下在相同的溶剂中,NaCO 比
2 3 2 2 3 2 3
NaHCO 易溶,所以会析出碳酸氢钠晶体,D项正确。
3
4.现有25 mL 2 mol·L-1的NaCO 溶液和75 mL 1 mol·L-1的稀盐酸。(1)将NaCO 溶液逐
2 3 2 3
滴滴入稀盐酸中;(2)将稀盐酸逐滴滴入NaCO 溶液中。两操作的现象及结果(标准状况下)
2 3
为( )
A.现象相同,所得气体的体积相等
B.现象相同,所得气体的体积不等
C.现象不同,所得气体的体积相等
D.现象不同,所得气体的体积不等
答案 D
解析 n(Na CO)=0.05 mol,n(HCl)=0.075 mol
2 3
(1)操作:NaCO+ 2HCl===2NaCl+CO↑+HO
2 3 2 2
0.05 mol 0.075 mol n(CO)
2
n(CO)=×0.075 mol;
2
(2)操作:NaCO+ HCl===NaCl+NaHCO
2 3 3
0.05 mol 0.05 mol 0.05 mol
NaHCO +HCl===NaCl+CO↑+HO
3 2 2
0.05 mol 0.025 mol n(CO)
2
n(CO)=0.025 mol。
2
5.(2020·黄山高三模拟)在一密闭容器中有CO、H、O 共16.5 g和足量的NaO 用电火花引
2 2 2 2
燃,使其完全反应,NaO 增重7.5 g,则原混合气体中O 的质量分数是( )
2 2 2
A.54.5% B.40%
C.36% D.33.3%
答案 A
解析 CO、H 、O 完全反应后生成的二氧化碳、水与过氧化钠反应生成碳酸钠、氢氧化钠,
2 2
所以过氧化钠固体增重的质量等于CO、H 的质量,所以原混合气体中CO、H 的质量一共
2 2
是 7.5 g,则 O 的质量是 16.5 g-7.5 g=9.0 g,所以原混合气体中 O 的质量分数是
2 2
×100%≈54.5%。
6.某干燥粉末可能由NaO、NaO 、NaCO 、NaHCO 、NaCl中的一种或几种组成。将该
2 2 2 2 3 3
粉末与足量的盐酸反应有气体X逸出,X通过足量的NaOH溶液后体积缩小(同温同压下测
定),若将原混合物粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原
混合粉末的质量。下列判断正确的是( )A.粉末中一定有NaO、NaCO、NaHCO
2 2 2 3 3
B.粉末中一定不含有NaCO 和NaCl
2 3
C.粉末中一定不含有NaO和NaCl
2
D.无法确定粉末里是否含有NaCO 和NaCl
2 3
答案 D
解析 向混合物中加入足量的盐酸,有气体放出,与盐酸反应产生气体的物质可能为
NaO(生成O)、NaCO 或NaHCO (生成CO),X通过NaOH溶液后体积缩小(而不是气体
2 2 2 2 3 3 2
全部消失),说明X由O 和CO 组成,原粉末中NaO 一定存在,NaCO 和NaHCO 至少有
2 2 2 2 2 3 3
一种存在。将原混合粉末加热,有气体放出,说明混合物中一定有NaHCO ,但NaHCO 受
3 3
热分解会使粉末质量减小,而实际剩余固体的质量却增加了,原因只能是发生了反应:
2NaO+O=====2NaO ;综上分析,混合物中一定有NaO、NaO 、NaHCO ,无法确定混
2 2 2 2 2 2 2 3
合物中是否有NaCO 和NaCl。
2 3
7.有甲、乙两个完全相同的装置,分别在它们的侧管中装入 1.06 g Na CO 和 0.84 g
2 3
NaHCO ,试管中各有10 mL相同浓度的盐酸(如图),同时将两个侧管中的物质全部倒入各
3
自的试管中,下列叙述正确的是( )
A.甲装置的气球膨胀速率大
B.若最终两气球体积相同,则一定有c(HCl)≥2 mol·L-1
C.若最终两气球体积不同,则一定有c(HCl)≤1 mol·L-1
D.最终两溶液中Na+、Cl-的物质的量相同
答案 B
解析 碳酸钠和盐酸的反应分步进行,先生成碳酸氢钠,后碳酸氢钠和盐酸反应生成二氧化
碳,所以甲装置的气球膨胀速率小,故A错误;1.06 g Na CO 和0.84 g NaHCO 的物质的量
2 3 3
相同,都是 0.01 mol,根据方程式 NaHCO +HCl===NaCl+HO+CO↑,NaCO +
3 2 2 2 3
2HCl===2NaCl+HO+CO↑知,若最终两气球体积相同,说明酸的物质的量大于或等于 0.02
2 2
mol,所以其浓度大于或等于2 mol·L-1,故B正确;碳酸钠和盐酸反应的离子方程式为CO
+H+===HCO、HCO+H+===CO↑+HO,碳酸氢钠和盐酸反应的离子方程式为 HCO+H
2 2
+===CO↑+HO,若最终两气球体积不同,所需酸的物质的量范围是 0<n(HCl)<0.02
2 2
mol,故C错误;1.06 g Na CO 和0.84 g NaHCO 的物质的量相同,都是0.01 mol,所以
2 3 3
NaCO 和NaHCO 中钠离子的物质的量不同,故D错误。
2 3 3
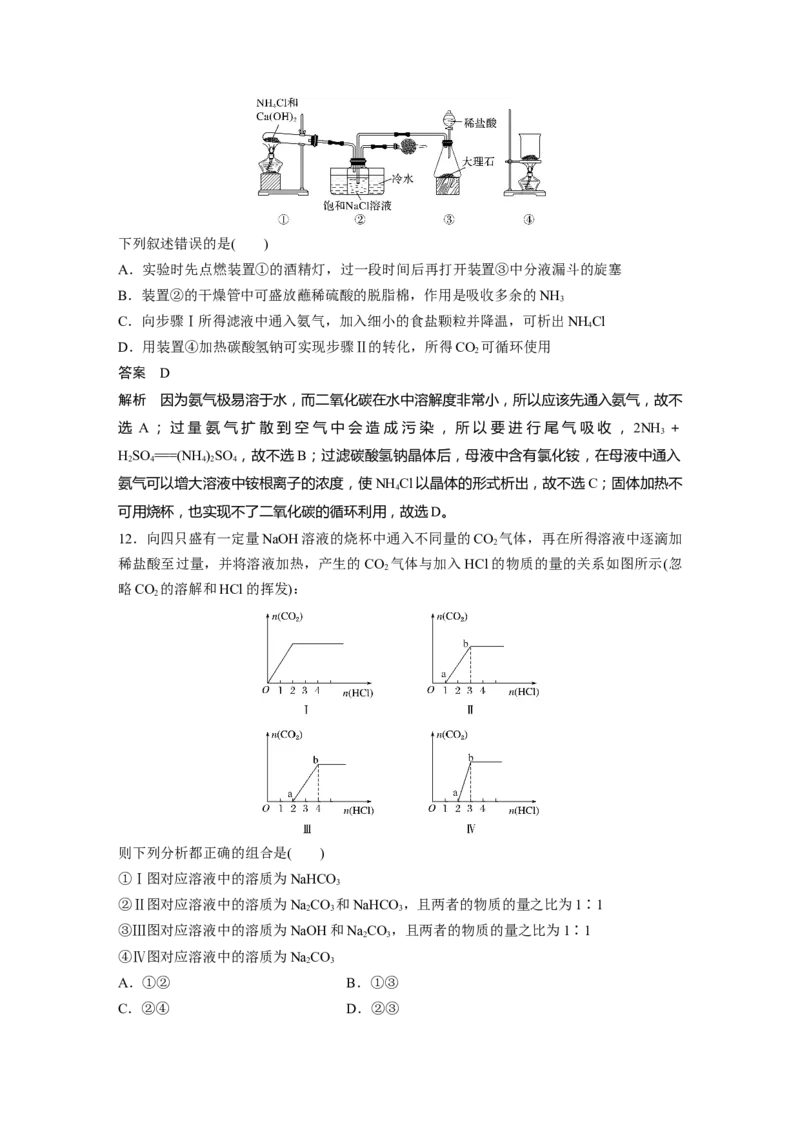
8.某同学为测定NaCO 固体(含少量NaCl)的纯度,设计如下装置(含试剂)进行实验。
2 3下列说法不正确的是( )
A.必须在②③间添加吸收HCl的装置
B.④的作用是防止空气中的气体影响实验的精确度
C.通入空气的作用是保证②中产生的气体完全转移到③中
D.称取样品和③中产生的沉淀的质量即可求算NaCO 固体的纯度
2 3
答案 A
解析 氢氧化钡足量,挥发出的HCl先被吸收,不会影响BaCO 沉淀的生成和测定,无需
3
单独添加吸收HCl的装置,故A项错误;碱石灰可与二氧化碳反应、吸收水分,可防止空
气中的气体影响实验的精确度,故B项正确;根据③中沉淀的质量计算碳酸钠的纯度,故
需要通入空气,保证②中产生的二氧化碳完全转移到③中,被充分吸收,减小实验误差,故
C项正确;③中产生的沉淀为碳酸钡,根据碳酸钡的质量可计算生成二氧化碳的质量,根据
生成二氧化碳的质量计算样品中的碳酸钠质量,根据称取样品的质量即可求算碳酸钠固体的
纯度,故D项正确。
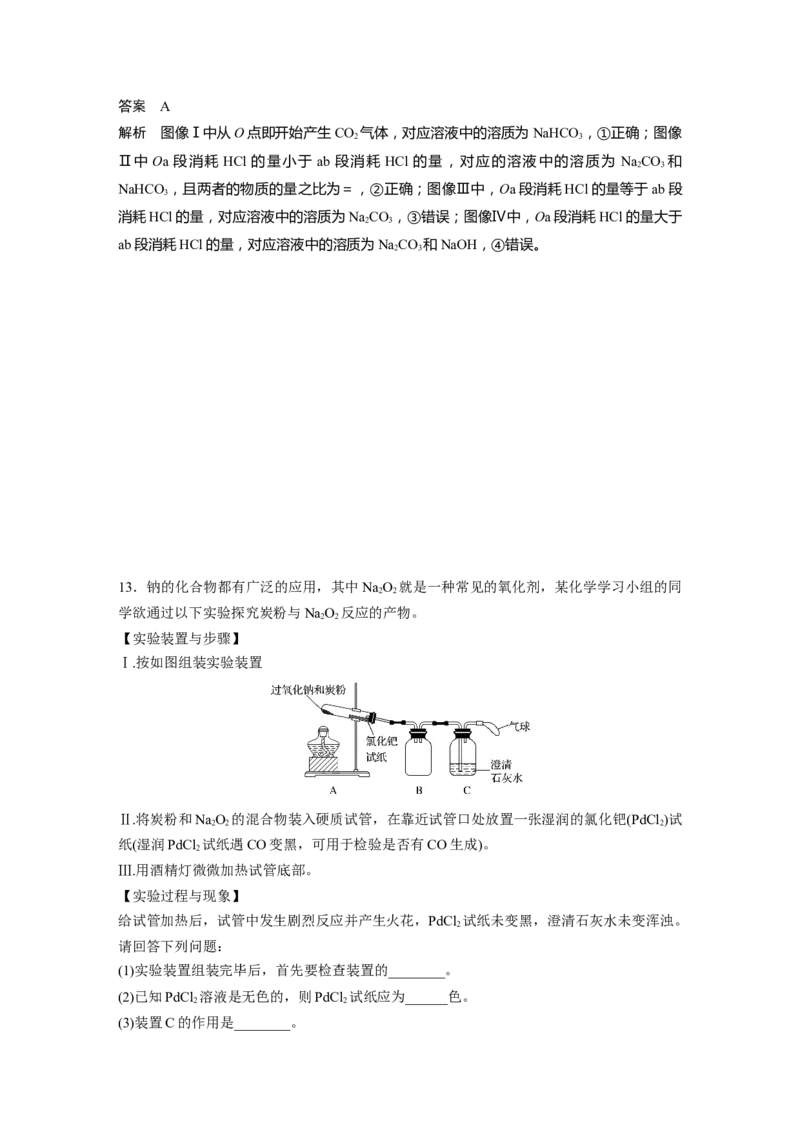
9.向50 mL NaOH溶液中逐渐通入一定量的 CO(假设溶液体积不变),随后取此溶液10
2
mL,将其稀释至100 mL,并向此稀释后的溶液中逐滴加入0.1 mol·L-1的盐酸,产生CO 气
2
体的体积(标准状况下)与所加入的盐酸的体积关系如图,下列分析错误的是( )
A.OA段所发生反应的离子方程式:H++OH-===HO
2
B.NaOH在吸收CO 后,所得溶液的溶质为NaOH和NaCO,其物质的量浓度之比为1∶1
2 2 3
C.产生的CO 体积(标准状况下)为0.056 L
2
D.稀释液中NaOH的物质的量浓度为0.025 mol·L-1
答案 A
解析 根据图像可知在A~B段发生反应:HCO+H+===HO+CO↑;则产生HCO的反应:
2 2
CO+H+===HCO;二者反应消耗的酸的物质的量相等,由于产生气体体积达到最大消耗的
盐酸是25 mL,则产生的HCO的反应也消耗盐酸25 mL,因此在O~A段发生的反应是H+
+OH-===HO、CO+H+===HCO,A项错误;NaOH在吸收CO 后,所得溶液的溶质为
2 2
NaOH和NaCO ,根据消耗的HCl的物质的量的关系可知二者的物质的量之比是1∶1,由
2 3
于溶质处于同一溶液,所以其物质的量浓度之比为 1∶1,B项正确;n(CO)=n(HCl)=0.1
2
mol·L-1×0.025 L=0.002 5 mol,在标准状况下产生的 CO 体积是 V(CO)=0.002 5 mol
2 2×22.4 L·mol-1=0.056 L,C 项正确;HCl+NaOH===NaCl+HO,n(NaOH)=n(HCl)=0.1
2
mol·L-1
×0.025 L=0.002 5 mol;c(NaOH)·V(NaOH)=n(NaOH)=0.002 5 mol;c(NaOH)==0.025
mol·L-1,D项正确。
10.(2019·安徽淮南十校联考)工业上以粗盐(含Ca2+、Mg2+、SO等杂质)为主要原料,采用
“侯氏制碱法”生产纯碱和化肥NH Cl,实验室模拟工艺流程如图甲所示。下列说法正确的
4
是( )
A.饱和食盐水中先通入的气体为CO
2
B.流程图中的“系列操作”中一定需要使用玻璃棒
C.如图乙所示装置可以比较NaCO 和NaHCO 晶体的热稳定性
2 3 3
D.对粗盐溶液除杂可依次加入过量NaOH、NaCO 、BaCl 溶液,过滤后再加入盐酸调节
2 3 2
溶液的pH
答案 B
解析 A项,二氧化碳在水中溶解度较小,氨气在水中溶解度较大,故应先通入氨气,使溶
液为碱性溶液,再通入二氧化碳,才可以达到实验目的,错误;B项,从溶液中得到固体,
需要加热浓缩、冷却结晶、过滤等操作,因此流程图中的“系列操作”中一定需要玻璃棒搅
拌、引流等,正确;C项,NaCO 加热不易分解,NaHCO 晶体加热容易分解,故小试管中
2 3 3
盛放NaHCO ,大试管中盛放NaCO,错误;D项,除去粗盐中的Ca2+、Mg2+、SO及泥沙,
3 2 3
可以依次加过量BaCl 除去SO,然后加NaOH除去Mg2+,用NaCO 除去Ca2+和过量的Ba2
2 2 3
+,盐酸要在最后加入,除去过量的NaOH和NaCO,错误。
2 3
11.“侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某实验小组模
拟“侯氏制碱法”的工艺流程及实验装置(部分夹持装置省略)如下:下列叙述错误的是( )
A.实验时先点燃装置①的酒精灯,过一段时间后再打开装置③中分液漏斗的旋塞
B.装置②的干燥管中可盛放蘸稀硫酸的脱脂棉,作用是吸收多余的NH
3
C.向步骤Ⅰ所得滤液中通入氨气,加入细小的食盐颗粒并降温,可析出NH Cl
4
D.用装置④加热碳酸氢钠可实现步骤Ⅱ的转化,所得CO 可循环使用
2
答案 D
解析 因为氨气极易溶于水,而二氧化碳在水中溶解度非常小,所以应该先通入氨气,故不
选 A;过量氨气扩散到空气中会造成污染,所以要进行尾气吸收,2NH +
3
HSO ===(NH )SO ,故不选B;过滤碳酸氢钠晶体后,母液中含有氯化铵,在母液中通入
2 4 4 2 4
氨气可以增大溶液中铵根离子的浓度,使NH Cl以晶体的形式析出,故不选C;固体加热不
4
可用烧杯,也实现不了二氧化碳的循环利用,故选D。
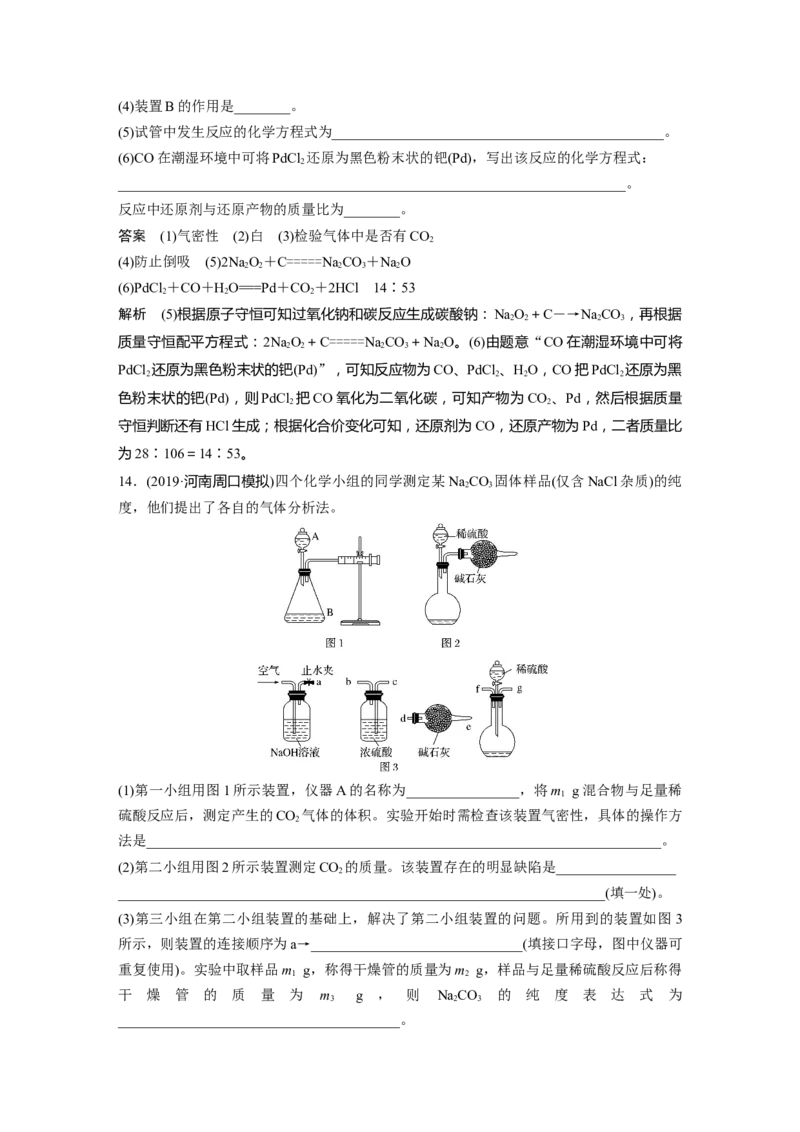
12.向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO 气体,再在所得溶液中逐滴加
2
稀盐酸至过量,并将溶液加热,产生的CO 气体与加入HCl的物质的量的关系如图所示(忽
2
略CO 的溶解和HCl的挥发):
2
则下列分析都正确的组合是( )
①Ⅰ图对应溶液中的溶质为NaHCO
3
②Ⅱ图对应溶液中的溶质为NaCO 和NaHCO ,且两者的物质的量之比为1∶1
2 3 3
③Ⅲ图对应溶液中的溶质为NaOH和NaCO,且两者的物质的量之比为1∶1
2 3
④Ⅳ图对应溶液中的溶质为NaCO
2 3
A.①② B.①③
C.②④ D.②③答案 A
解析 图像Ⅰ中从O点即开始产生CO 气体,对应溶液中的溶质为NaHCO ,①正确;图像
2 3
Ⅱ中 Oa 段消耗 HCl 的量小于 ab 段消耗 HCl 的量,对应的溶液中的溶质为 NaCO 和
2 3
NaHCO ,且两者的物质的量之比为=,②正确;图像Ⅲ中,Oa段消耗HCl的量等于ab段
3
消耗HCl的量,对应溶液中的溶质为NaCO ,③错误;图像Ⅳ中,Oa段消耗HCl的量大于
2 3
ab段消耗HCl的量,对应溶液中的溶质为NaCO 和NaOH,④错误。
2 3
13.钠的化合物都有广泛的应用,其中NaO 就是一种常见的氧化剂,某化学学习小组的同
2 2
学欲通过以下实验探究炭粉与NaO 反应的产物。
2 2
【实验装置与步骤】
Ⅰ.按如图组装实验装置
Ⅱ.将炭粉和NaO 的混合物装入硬质试管,在靠近试管口处放置一张湿润的氯化钯(PdCl )试
2 2 2
纸(湿润PdCl 试纸遇CO变黑,可用于检验是否有CO生成)。
2
Ⅲ.用酒精灯微微加热试管底部。
【实验过程与现象】
给试管加热后,试管中发生剧烈反应并产生火花,PdCl 试纸未变黑,澄清石灰水未变浑浊。
2
请回答下列问题:
(1)实验装置组装完毕后,首先要检查装置的________。
(2)已知PdCl 溶液是无色的,则PdCl 试纸应为______色。
2 2
(3)装置C的作用是________。(4)装置B的作用是________。
(5)试管中发生反应的化学方程式为_______________________________________________。
(6)CO在潮湿环境中可将PdCl 还原为黑色粉末状的钯(Pd),写出该反应的化学方程式:
2
________________________________________________________________________。
反应中还原剂与还原产物的质量比为________。
答案 (1)气密性 (2)白 (3)检验气体中是否有CO
2
(4)防止倒吸 (5)2Na O+C=====NaCO+NaO
2 2 2 3 2
(6)PdCl +CO+HO===Pd+CO+2HCl 14∶53
2 2 2
解析 (5)根据原子守恒可知过氧化钠和碳反应生成碳酸钠:NaO +C―→NaCO ,再根据
2 2 2 3
质量守恒配平方程式:2NaO +C=====NaCO +NaO。(6)由题意“CO在潮湿环境中可将
2 2 2 3 2
PdCl 还原为黑色粉末状的钯(Pd)”,可知反应物为CO、PdCl 、HO,CO把PdCl 还原为黑
2 2 2 2
色粉末状的钯(Pd),则PdCl 把CO氧化为二氧化碳,可知产物为CO 、Pd,然后根据质量
2 2
守恒判断还有HCl生成;根据化合价变化可知,还原剂为CO,还原产物为Pd,二者质量比
为28∶106=14∶53。
14.(2019·河南周口模拟)四个化学小组的同学测定某NaCO 固体样品(仅含NaCl杂质)的纯
2 3
度,他们提出了各自的气体分析法。
(1)第一小组用图1所示装置,仪器A的名称为________________,将m g混合物与足量稀
1
硫酸反应后,测定产生的CO 气体的体积。实验开始时需检查该装置气密性,具体的操作方
2
法是_________________________________________________________________________。
(2)第二小组用图2所示装置测定CO 的质量。该装置存在的明显缺陷是_________________
2
_____________________________________________________________________(填一处)。
(3)第三小组在第二小组装置的基础上,解决了第二小组装置的问题。所用到的装置如图 3
所示,则装置的连接顺序为a→______________________________(填接口字母,图中仪器可
重复使用)。实验中取样品m g,称得干燥管的质量为m g,样品与足量稀硫酸反应后称得
1 2
干 燥 管 的 质 量 为 m g , 则 NaCO 的 纯 度 表 达 式 为
3 2 3
________________________________________。(4)第四小组设计用沉淀法来测定。方法是滴加沉淀剂使碳酸钠转化为沉淀,然后过滤、洗
涤、干燥后称量沉淀质量。经讨论认为应用Ba(OH) 溶液代替澄清石灰水作沉淀剂,其原因
2
是________(填字母)。
a.Ba(OH) 比Ca(OH) 便宜
2 2
b.Ba(OH) 的溶解度大于Ca(OH) 的,可以增大Ba(OH) 的浓度,无须加入过大体积的沉淀
2 2 2
剂
c.相同条件下,CaCO 的溶解度明显小于BaCO
3 3
d.吸收等量的CO 生成BaCO 的质量大于CaCO ,测量误差小
2 3 3
答案 (1)分液漏斗 关闭仪器A的活塞,将注射器活塞拉出一定距离,一段时间后松开活
塞,若活塞能回到原位,证明该装置的气密性良好
(2)CO 气体中混有水蒸气(或空气中的CO 和水蒸气会进入干燥管中或装置中的CO 没有全
2 2 2
部被碱石灰吸收)
(3)fgcbdede ×100%
(4)bd
解析 (3)样品m g,称得干燥管质量为m g,与足量稀硫酸反应后称得干燥管质量为 m
1 2 3
g,干燥管增加的质量等于生成的CO 的质量为(m-m) g,依据碳元素守恒计算,碳酸钠的
2 3 2
纯度为×100%=×100%。
(4)Ca(OH) 比Ba(OH) 便宜,a项错误;相同条件下,CaCO 、BaCO 的溶解度相差不大,c
2 2 3 3
项错误。