文档内容
第 15 讲 铁及其重要化合物
复习目标 1.掌握铁及其重要化合物的主要性质及其应用。2.了解铁及其化合物的制备方
法。
考点一 铁的单质、氧化物、氢氧化物
1.单质铁
(1)铁在自然界中的存在
铁位于元素周期表中第四周期Ⅷ族,是一种应用最广泛的过渡金属元素;铁元素是一种典型
的变价金属元素。
(2)铁的物理性质
银白色固体,熔点较高,具有良好的导热、导电、延展性,能被磁铁吸引。
(3)铁的化学性质
铁的原子结构示意图:还原性较强,失去电子后生成+2价或+3价的铁。
生成不同价态的反应关系如下:
按要求填空:
①Fe在O、Cl 中燃烧的现象及化学方程式:
2 2
铁在氧气中燃烧,火星四射:3Fe + 2O=====Fe O 。铁在氯气中燃烧,产生棕褐色的烟:
2 3 4
2Fe+3Cl=====2FeCl (不论铁的量多少,与氯气反应的产物都是氯化铁)。
2 3
②Fe与S、水蒸气反应的化学方程式:
Fe与S:Fe+S=====FeS(不论铁的量多少,与硫反应的产物都是硫化亚铁)。
Fe与水蒸气:3Fe+4HO(g)=====Fe O+4H。
2 3 4 2
③与氧化性酸(如HNO)的反应(写离子方程式)。
3
Fe与过量稀HNO 的反应:
3
Fe+NO+4H+===Fe3++NO↑+2HO。
2
Fe与少量稀HNO 的反应:
3
3Fe+2NO+8H+===3Fe2++2NO↑+4HO。
2
④Fe与FeCl 溶液的反应(写离子方程式):
3
Fe+2Fe3+===3Fe2+。
特别提醒 铁遇冷的浓硝酸、浓硫酸时,表面会生成一层致密的氧化膜,化学上称之为钝化,
属于化学变化。
2.铁的氧化物比较
化学式 FeO Fe O Fe O
2 3 3 4
俗名 铁红 磁性氧化铁
黑色晶体
颜色状态 黑色粉末 红棕色粉末
(有磁性)
溶解性 难溶于水 难溶于水 难溶于水
铁的化合价 + 2 + 3 + 2 、+ 3
稳定性 不稳定 稳定 稳定
与H+反应的 FeO+2H+===Fe2++ Fe O+6H+===2Fe3+ Fe O+8H+===Fe2+
2 3 3 4
离子方程式 HO +3HO +2Fe3++4HO
2 2 2
与CO的反
FeO+yCO=====xFe+yCO
x y 2
应(炼铁原理)
3.氢氧化铁和氢氧化亚铁的比较
化学式 Fe(OH) Fe(OH)
2 3色态 白色固体 红褐色固体
与盐酸反应 Fe(OH) +2H+===Fe2++2HO Fe(OH) +3H+===Fe3++3HO
2 2 3 2
受热分解 2Fe(OH) =====Fe O+3HO
3 2 3 2
可溶性亚铁盐与碱溶液反应 可溶性铁盐与碱溶液反应
制法
Fe2++2OH-===Fe(OH) ↓ Fe3++3OH-===Fe(OH) ↓
2 3
在空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,现象
2 3
二者的关系 是白色絮状沉淀迅速变成灰绿色,最后变成红褐色,化学方程式
为4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
(1)铁位于元素周期表中第四周期ⅧB族(×)
错因: 铁位于 Ⅷ 族,不是副族 。
(2)铁的化学性质比较活泼,所以铁在自然界中全部以化合态存在(×)
错因:在陨铁中存在铁单质。
(3)Fe在足量Cl 中燃烧生成FeCl ,在少量Cl 中燃烧生成FeCl (×)
2 3 2 2
错因: Fe 与 Cl 反应生成 FeC l ,与 C l 的量无关。
2 3 2
(4)Fe分别与氯气、盐酸反应得到相同的氯化物(×)
错因: Fe 与 Cl 反应生成 FeC l ,与盐酸反应生成 FeC l ,产物不同。
2 3 2
(5)Fe O 中Fe的化合价有+2价和+3价,因而Fe O 是FeO与Fe O 的混合物(×)
3 4 3 4 2 3
错因:Fe O 是一种化合物,不是混合物。
3 4
题组一 铁及重要化合物性质
1.(2020·湖北枝江月考)下列关于铁的说法正确的是( )
A.铁在硫蒸气中燃烧生成Fe S
2 3
B.纯铁的抗腐蚀能力较差,铁在干燥的空气里易被氧化
C.工业上用CO在高温条件下还原含Fe O 的铁矿石炼铁
2 3
D.铁在纯氧中燃烧或在氯气中燃烧所得产物中铁的化合价均为+3价
答案 C
解析 Fe与S反应生成FeS,A项错误;纯铁不易发生电化学腐蚀,抗腐蚀能力较强,铁在
干燥的空气里不易被氧化,B项错误;铁在纯氧中燃烧产物是Fe O,其中铁的化合价有+2
3 4
价和+3价两种价态,D项错误。
2.铁是日常生活中使用最广泛的金属,下列关于铁的一些说法正确的是( )
A.常温下浓硫酸与铁不反应,故常温下可用铁制容器贮藏、贮运浓硫酸
B.铁是较活泼的金属,它与卤素单质(X )反应的生成物均为FeX
2 3
C.Fe(OH) 易被氧化成Fe(OH) ,说明稳定性:Fe(OH) Fe O
2 3 3 4
D.FeO、Fe O 和Fe O 均可与盐酸反应,且反应类型均为复分解反应
2 3 3 4
答案 D
解析 FeO和Fe O 均为黑色固体,Fe O 为红棕色固体,故A错误;Fe O 是一种纯净物,
3 4 2 3 3 4
化合价是一种复合化合价,故B错误;在1 400 ℃以上的温度下加热Fe O 时,Fe O 会部
2 3 2 3
分失去氧,生成Fe O ,说明Fe O 比Fe O 稳定,故C错误;FeO、Fe O 和Fe O 均可与盐
3 4 3 4 2 3 2 3 3 4
酸反应生成盐和水,反应过程中无元素化合价变化,反应类型均为复分解反应,故D正确。
5.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO 全部用足量的澄
2
清石灰水吸收,得到沉淀4.00 g,则这种铁的氧化物为( )
A.Fe O B.Fe O
3 4 2 3
C.FeO D.以上都不是
答案 C
解析 4.00 g CaCO 沉淀的物质的量为0.04 mol,则CO、CO 的物质的量也为0.04 mol,增
3 2
加的氧元素为0.04 mol,质量为0.04 mol×16 g·mol-1=0.64 g,铁的氧化物中氧元素的质量
为0.64 g,铁元素质量为2.88 g-0.64 g=2.24 g,铁的氧化物中铁元素与氧元素的物质的量
之比为∶0.04 mol=1∶1,则这种铁的氧化物的化学式为FeO。6.(2019·舟山质检)有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰好将之完全
溶解,所得溶液还能吸收0.025 mol Cl ,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能
2
的化学式为( )
A.Fe O B.Fe O C.Fe O D.Fe O
2 3 3 4 4 5 5 7
答案 D
解析 根据2Fe2++Cl===2Fe3++2Cl-,可知铁的“氧化物”样品用盐酸溶解后所得溶液中
2
n(Fe2+)=0.025 mol×2=0.05 mol,根据电荷守恒得2n(Fe2+)+3n(Fe3+)=n(Cl-),则n(Fe3+)
=0.2 mol,故n(Fe2+)∶n(Fe3+)=0.05∶0.2=1∶4,故该氧化物可表示为 FeO·2Fe O ,即
2 3
Fe O。
5 7
确定铁的氧化物组成的基本方法
设铁的氧化物中铁元素与氧元素的质量比为m∶n,
则氧化物中n(Fe)∶n(O)=∶=a∶b,
若a∶b=1∶1,则铁的氧化物为FeO;
若a∶b=2∶3,则铁的氧化物为Fe O;
2 3
若a∶b=3∶4,则铁的氧化物是Fe O 或FeO与Fe O 按物质的量之比为1∶1的混合物或
3 4 2 3
FeO、Fe O、Fe O 的混合物(其中FeO、Fe O 物质的量之比为1∶1,Fe O 为任意值)。
2 3 3 4 2 3 3 4
题组三 铁与水蒸气反应的实验探究
7.某化学兴趣小组利用如图装置进行“铁与水蒸气反应”的实验,并检验产物的性质,下
列说法正确的是( )
A.实验时,应先点燃B处的酒精喷灯,再点燃A处的酒精灯
B.B中发生反应的化学方程式是:2Fe+3HO(g)=====Fe O+3H
2 2 3 2
C.B中生成1 mol H 时,E处有1 mol CuO被还原
2
D.碱石灰的作用是吸收水蒸气
答案 D
解析 实验时,应先点燃A处的酒精灯,再点燃B处的酒精灯,防止铁被氧气氧化,故 A
错误;B中发生反应的化学方程式是:3Fe+4HO(g)=====Fe O+4H,故B错误;B中生成
2 3 4 2
1 mol H 时,由于H 要先排出装置内空气,再与CuO反应,因此E处CuO被还原的物质的
2 2量小于1 mol,故C错误;碱石灰的作用是吸收水蒸气,干燥H,故D正确。
2
8.铁与水蒸气反应,通常有以下两种装置,请回答下列问题:
装置一 装置二
(1)装置二中湿棉花的作用为______________________________________________________。
(2)实验完毕后,取出装置一的少量固体,溶于足量稀盐酸,再滴加 KSCN溶液,溶液颜色
无明显变化,试解释原因:_______________________________________(用离子方程式表
示)。
答案 (1)提供水蒸气 (2)Fe O+8H+===Fe2++2Fe3++4HO、2Fe3++Fe===3Fe2+
3 4 2
考点二 Fe2+和 Fe3+的性质及其检验
1.亚铁盐
(1)Fe2+的氧化性和还原性
含有Fe2+的溶液呈浅绿色,Fe2+处于铁的中间价态,既有氧化性,又有还原性,其中以还原
性为主,遇Br 、Cl、HO、NO(H+)等均表现为还原性。
2 2 2 2
Fe2+的酸性溶液与HO 反应的离子方程式:2Fe2++HO+2H+===2Fe3++2HO。
2 2 2 2 2
(2)可水解
Fe(OH) 是弱碱,含Fe2+的盐(如硫酸亚铁)溶液呈酸性。配制硫酸亚铁溶液时常加少量硫酸
2
抑制Fe2+的水解,加少量铁屑防止Fe2+被氧化。
2.铁盐的性质及应用
(1)氧化性:含有Fe3+的溶液呈棕黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、HS等均表
2
现为氧化性。
①Fe3+与S2-、I-、HS-、SO等具有较强还原性的离子不能大量共存。
②Fe3+可腐蚀印刷电路板上的铜箔,反应的离子方程式为2Fe3++Cu===Cu2++2Fe2+。
(2)易水解:Fe(OH) 是很弱的碱,且溶度积很小,因而Fe3+极易水解,只能存在于酸性较强
3
的溶液中。
利用Fe3+易水解的性质,实验室可用FeCl 滴入沸水中制取氢氧化铁胶体,反应的化学方程
3
式:FeCl +3HO=====Fe(OH) (胶体)+3HCl。
3 2 3
3.Fe2+、Fe3+的检验方法
(1)用KSCN溶液和氯水(2)用NaOH溶液
(3)含Fe2+、Fe3+的混合溶液中Fe2+、Fe3+的检验
――――――→溶液变红色,说明含有Fe3+。
―――――→KMnO 溶液紫红色褪去,说明含有Fe2+。
4
(4)Fe2+的特征检验方法
溶液―――――――→产生蓝色沉淀,说明溶液中含有 Fe2+,3Fe2++2[Fe(CN) ]3-===
6
Fe [Fe(CN) ]↓。
3 6 2
(1)金属阳离子只有氧化性,不可能有还原性(×)
错因: Fe 2 + 具有还原性 。
(2)氢氧化铁与HI溶液反应仅能发生中和反应(×)
错因: Fe 3 + 与 I - 会发生氧化还原反应 。
(3)中性溶液中可能大量存在Fe3+、Cl-、K+、SO(×)
错因: 在溶液呈中性时, F e 3 + 转化为 Fe(OH ) ,不能大量存在。
3
(4)用酸性KMnO 溶液检验FeCl 溶液中是否含有FeCl (×)
4 3 2
错因: Cl - 也能与 KMnO 反应,使其褪色。
4
(5)能通过化合反应制取FeCl (√)
2
1.在Fe (SO ) 溶液中,加入a g铜,完全溶解后,再加b g铁,充分反应后得到c g残余
2 4 3
固体,且a>c。试分析残留固体的成分为________,所得溶液中阳离子为________。
答案 Cu Cu2+、Fe2+
2.混合溶液中除去Fe3+、Fe2+的常用方法
已知:沉淀的pH
化合物 Fe(OH) Fe(OH) Mg(OH) Cu(OH)
3 2 2 2
pH 1.14~3.0 5.8~8.3 8.4~10.8 4.2~6.7
(1)除去Mg2+中混有的Fe3+的方法
向混合溶液中加入________、____________、__________其中之一,与Fe3+水解产生的H+
反应,促进Fe3+的水解,将Fe3+转化为Fe(OH) 沉淀除去。
3
(2)除去Mg2+中混有的Fe2+的方法
先加入氧化剂(如______)将溶液中的Fe2+氧化成Fe3+,然后再按(1)的方法除去溶液中的Fe3
+。(3)请设计实验方案:除去CuCl 溶液中混有的少量FeCl 。
2 2
答案 (1)MgO MgCO Mg(OH) (2)H O
3 2 2 2
(3)先通入适量 Cl(或加入 HO),再向混合溶液中加入足量 CuO[或CuCO 、Cu(OH) 、
2 2 2 3 2
Cu (OH) CO 其中之一],充分反应后过滤。
2 2 3
题组一 Fe2+、Fe3+的性质及应用
1.《新修本草》中关于“青矾”的描述:“本来绿色,新出窟未见风者,正如琉璃,烧之
赤色”。《物理小识》中说:“青矾厂气熏人,衣服当之易烂,栽木不茂”,下列相关叙述
不正确的是( )
A.赤色固体可能是Fe O
2 3
B.青矾宜密闭保存,防止氧化变质
C.青矾燃烧过程中发生了电子转移
D.“青矾厂气”可能是CO和CO
2
答案 D
解析 根据《新修本草》关于青矾的描述可知为FeSO ·7H O,其分解产生的气体二氧化硫
4 2
有刺激性气味,三氧化硫有腐蚀性,不可能产生CO和CO。
2
2.在FeCl 、CuCl 混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法正
3 2
确的是( )
A.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+
B.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe2+,可能含Cu2+和Fe3+
C.若滤出的固体中只有铜,则溶液中一定含有的阳离子是Fe3+和Fe2+,一定不含Cu2+
D.若滤出的固体中含有铁和铜,则溶液中一定含有的阳离子是Fe2+,一定不含Cu2+和Fe3+
答案 D
解析 氧化性:Fe3+>Cu2+>Fe2+,加入铁粉后有固体剩余,Fe3+一定不存在;若剩余固体
全部是Cu,溶液中还可能有Cu2+,也可能恰好被完全置换;若剩余固体是 Cu和Fe,则溶
液中不可能有Cu2+和Fe3+。
3.下列有关Fe3+、Fe2+的性质及应用的说法正确的是____________(填序号)。
①Fe (SO ) 易溶于水,所以可用作净水剂
2 4 3
②向Fe (SO ) 溶液中加入过量铁粉,可制得硫酸亚铁溶液
2 4 3
③室温下,向FeCl 溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色,则说明
3
Fe3+的氧化性比I 的强
2
④Fe2+与HO 在酸性溶液中的反应:2Fe2++HO+2H+===2Fe3++2HO
2 2 2 2 2
⑤硫酸亚铁片和维生素C同时服用,能增强治疗缺铁性贫血的效果
答案 ②③④⑤
解析 Fe3+水解生成Fe(OH) 胶体,可用于净水,与Fe (SO ) 是否易溶于水无对应关系,①
3 2 4 3错误;2Fe3++Fe===3Fe2+,②正确;Fe3+将I-氧化成I ,依据氧化剂的氧化性大于氧化产
2
物的氧化性,可知Fe3+的氧化性强于I ,③正确;HO 具有强氧化性,能将Fe2+氧化为Fe3
2 2 2
+,④正确;维生素C具有还原性,能防止硫酸亚铁片中的Fe2+被氧化,⑤正确。
题组二 Fe2+、Fe3+的检验
4.要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时,最佳顺序为( )
①加入足量氯水 ②加入足量酸性KMnO 溶液 ③加入少量NH SCN溶液
4 4
A.①③ B.③② C.③① D.①②③
答案 C
解析 在该溶液中先加入少量NH SCN溶液,溶液不变红色,证明无Fe3+存在,再加入氯
4
水,将Fe2+氧化成Fe3+,溶液变为红色。KMnO 溶液呈紫红色,溶液颜色变化不明显,所
4
以不能用酸性KMnO 溶液检验。
4
5.(2020·济南质检)将0.2 mol·L-1的KI溶液和0.05 mol·L-1Fe (SO ) 溶液等体积混合充分反
2 4 3
应后,取混合液分别完成下列实验,能说明溶液中存在化学平衡 2Fe3++2I-2Fe2++I
2
的是( )
A.向混合液中滴入KSCN溶液,溶液变红色
B.向混合液中滴入AgNO 溶液,有黄色沉淀生成
3
C.向混合液中滴入K[Fe(CN) ]溶液,有蓝色沉淀生成
3 6
D.向混合液中滴入淀粉溶液,溶液变蓝色
答案 A
解析 0.2 mol·L-1的KI溶液和0.05 mol·L-1 Fe (SO ) 溶液等体积混合,KI过量,向混合液
2 4 3
中滴入KSCN溶液,溶液变红色,说明溶液中仍含有Fe3+,能说明溶液中存在化学平衡2Fe3
++2I-2Fe2++I ,A项正确;KI过量,溶液中存在I-,B项错误;该反应生成Fe2+,向
2
混合液中滴入K[Fe(CN) ]溶液,有蓝色沉淀生成,只能说明溶液中含有Fe2+,C项错误;
3 6
该反应生成I,向混合液中滴入淀粉溶液,溶液变蓝色,说明溶液中含有碘单质,D项错误。
2
检验Fe2+和Fe3+时的注意事项
(1)检验Fe2+时不能先加氯水后加KSCN溶液,也不能将加KSCN后的混合溶液加入足量的
新制氯水中(新制氯水能氧化SCN-)。
(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性KMnO ,
4 4
有干扰)。
(3)检验Fe2+、Fe3+的其他方法
检验Fe3+也可用苯酚(C HOH);检验Fe2+最好用K[Fe(CN) ]溶液。
6 5 3 61.正误判断
(1)向HO 溶液中滴加少量FeCl ,2Fe3++HO===O↑+2H++2Fe2+( )
2 2 3 2 2 2
(2020·全国卷Ⅲ,11C)
(2)室温下,Fe与浓HSO 反应生成FeSO ( )(2020·江苏,6D)
2 4 4
(3)Fe在稀硝酸中发生钝化( )(2019·江苏,6A)
(4)将废铁屑加入FeCl 溶液中,可除去工业废气中的Cl( )(2019·天津,3A)
2 2
(5)将NaOH溶液滴入FeSO 溶液中,产生白色沉淀,随后变为红褐色,该颜色的变化与氧
4
化还原反应无关( )(2018·北京,9A)
(6)向FeCl 溶液中滴加NH SCN溶液,溶液显红色( )(2018·江苏,6A)
2 4
(7)给定条件下,能实现转化:Fe――→FeCl ――――→Fe(OH) ( )(2017·江苏,7A)
2 2
答案 (1)× (2)× (3)× (4)√ (5)× (6)× (7)×
2.(高考选项组合题)有关铁及其化合物的说法正确的是( )
A.将NaOH浓溶液滴加到饱和的FeCl 溶液中,制备Fe(OH) 胶体(2016·全国卷Ⅱ,13A)
3 3
B.FeCl 腐蚀Cu刻制印刷电路板,说明铁比铜金属性强(2016·全国卷Ⅲ,7B)
3
C.配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释(2016·全国卷Ⅰ,10C)
D.Fe与Cl 反应生成FeCl ,推测Fe与I 反应生成FeI(2016·上海,21C)
2 3 2 3
答案 C
解析 A项,制备Fe(OH) 胶体,应将饱和氯化铁溶液滴入沸水中,错误;B项,铁离子与
3
铜反应生成铜离子和亚铁离子,说明铜的还原性比亚铁离子的还原性强,无法证明金属性的
强弱,错误;C项,在溶液中铁离子极易发生水解反应,产生难溶性的氢氧化铁,为了抑制
铁离子的水解,应该先将氯化铁溶解在较浓的盐酸中,然后再加水稀释到相应的浓度,正确;
D项,因I 的氧化性较弱,故与铁反应生成FeI,错误。
2 2
3.(2020·江苏,19)实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料
α-Fe O。
2 3
其主要实验流程如下:
(1)酸浸。用一定浓度的HSO 溶液浸取铁泥中的铁元素。若其他条件不变,实验中采取下
2 4
列措施能提高铁元素浸出率的有________(填序号)。
A.适当升高酸浸温度
B.适当加快搅拌速度
C.适当缩短酸浸时间
(2)还原。向“酸浸”后的滤液中加入过量铁粉,使Fe3+完全转化为Fe2+。“还原”过程中
除生成Fe2+外,还会生成______________(填化学式);检验Fe3+是否还原完全的实验操作是
____________________________________________________________________________。
(3)沉铁。将提纯后的FeSO 溶液与氨水-NH HCO 混合溶液反应,生成FeCO 沉淀。
4 4 3 3①生成FeCO 沉淀的离子方程式为______________________________________________。
3
②设计以 FeSO 溶液、氨水-NH HCO 混合溶液为原料,制备 FeCO 的实验方案:
4 4 3 3
____________________________________________________________________________。
[FeCO 沉淀需“洗涤完全”,Fe(OH) 开始沉淀的pH=6.5]
3 2
答案 (1)AB
(2)H 取少量清液于试管中,向其中滴加几滴KSCN溶液,观察溶液颜色是否呈红色
2
(3)①Fe2++HCO+NH ·H O===FeCO↓+NH+HO(或Fe2++HCO+NH ===FeCO↓+NH)
3 2 3 2 3 3
②在搅拌条件下向FeSO 溶液中缓慢加入氨水-NH HCO 混合溶液,控制溶液pH不大于
4 4 3
6.5;静置后过滤,所得沉淀用蒸馏水洗涤2~3次;取最后一次洗涤后的滤液,滴加盐酸酸
化的BaCl 溶液,不出现白色沉淀
2
解析 (1)其他条件不变,实验中适当升高酸浸温度、适当加快搅拌速度都能提高铁元素浸
出率,缩短酸浸时间会降低铁元素浸出率,故应选A、B项。
(2)铁泥的主要成分为铁的氧化物,加入一定浓度的 HSO 溶液“酸浸”,滤液中含有Fe3
2 4
+、Fe2+、H+、SO等,加入过量铁粉,Fe3+、H+均与Fe发生反应,故除生成Fe2+外,还会
生成H 。可利用KSCN溶液检验Fe3+是否被完全还原,实验操作为取少量清液,向其中滴
2
加几滴KSCN溶液,观察溶液颜色是否呈红色,若不变色,证明Fe3+被完全还原。
(3)①FeSO 溶液与氨水-NH HCO 混合溶液反应,Fe2+与CO结合生成FeCO 沉淀,促进了
4 4 3 3
HCO的电离,离子方程式为Fe2++HCO+NH ·H O===FeCO↓+NH+HO或Fe2++HCO
3 2 3 2
+NH ===FeCO↓+NH。
3 3
②Fe(OH) 开始沉淀的pH=6.5,且要求FeCO 沉淀需“洗涤完全”,应控制溶液的pH不大
2 3
于6.5,防止产生Fe(OH) 沉淀;得到FeCO 沉淀,静置后过滤,用蒸馏水洗涤沉淀2~3次,
2 3
并通过检验洗涤液中是否含有SO,判断是否洗涤干净。则制备FeCO 的具体实验方案为在
3
搅拌条件下向FeSO 溶液中缓慢加入氨水-NH HCO 混合溶液,控制溶液pH不大于6.5;静
4 4 3
置后过滤,所得沉淀用蒸馏水洗涤 2~3次;取最后一次洗涤后的滤液,滴加盐酸酸化的
BaCl 溶液,不出现白色沉淀。
2
1.北宋沈括的《梦溪笔谈》对指南针已有详细记载:“方家以磁石磨针锋,则能指南。”
磁石的主要成分是( )
A.Fe O B.Fe O C.FeO D.CuFeS
3 4 2 3 2
答案 A
2.铁是一种应用广泛的金属,下列有关铁的说法正确的是( )
A.铁与盐酸反应生成氯化铁和氢气
B.常温下,铁在浓硫酸中钝化
C.铁在氧气中燃烧,生成物为Fe O
2 3D.纯铁(块状)是黑色金属
答案 B
解析 A项,铁与盐酸反应生成氯化亚铁和氢气,错误;C项,铁在氧气中燃烧的生成物为
Fe O,错误;D项,纯铁(块状)是银白色金属,错误。
3 4
3.某同学欲探究铁及其化合物的性质,下列实验方案可行的是( )
A.将铁粉加入热的浓硫酸中:探究铁的活泼性
B.将热的NaOH溶液滴入FeCl 溶液中:制备Fe(OH) 胶体
3 3
C.在蒸发皿中加热蒸干FeSO 溶液:制备FeSO ·6H O晶体
4 4 2
D.将铜粉加入FeCl 溶液中:验证Fe3+的氧化性强于Cu2+
3
答案 D
解析 由于浓硫酸具有强氧化性,铁与其反应生成Fe (SO ) 和SO ,无法说明铁的活泼性,
2 4 3 2
故A项方案不可行;将NaOH加入FeCl 溶液中,得到Fe(OH) 沉淀,无法得到Fe(OH) 胶
3 3 3
体,故B项方案不可行;在蒸发皿中加热蒸干FeSO 溶液,一方面氧气可将FeSO 氧化,另
4 4
一方面会得到不含结晶水的化合物,故C项方案不可行;将铜粉加入FeCl 溶液中,发生反
3
应:Cu+2Fe3+===Cu2++2Fe2+,该反应说明Fe3+的氧化性强于Cu2+,故D项方案可行。
4.证明某溶液只含有Fe2+而不含有Fe3+的实验方法是( )
A.先滴加氯水,再滴加KSCN溶液后显红色
B.先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C.滴加NaOH溶液,先产生白色沉淀,后变为灰绿色,最后呈红褐色
D.只需滴加KSCN溶液
答案 B
解析 Fe2+和Fe3+检验设计是常考的热点。设计的步骤:先加KSCN溶液,无现象,可证明
溶液中不含Fe3+,再滴加氯水,若溶液呈红色,说明溶液中含有Fe2+。
5.在含有Fe3+、Fe2+、Al3+、NH稀溶液中,加入足量的NaO 固体,充分反应后,再加入
2 2
过量的稀盐酸,完全反应后,离子数目没有变化的是( )
A.Fe2+ B.Al3+
C.Fe3+ D.NH
答案 B
解析 亚铁离子与氧气反应变为铁离子,和氢氧根反应生成沉淀,又加盐酸,沉淀溶解,最
后又变为铁离子,因此亚铁离子数目减少,故 A错误;铝离子与足量氢氧根反应生成偏铝
酸根,偏铝酸根与足量盐酸反应,最后又生成铝离子,数目不发生改变,故B正确;亚铁
离子被氧化成了铁离子,铁离子数目增加,故C错误;铵根离子和氢氧根离子反应生成氨
气和水,铵根离子数目减少,故D错误。
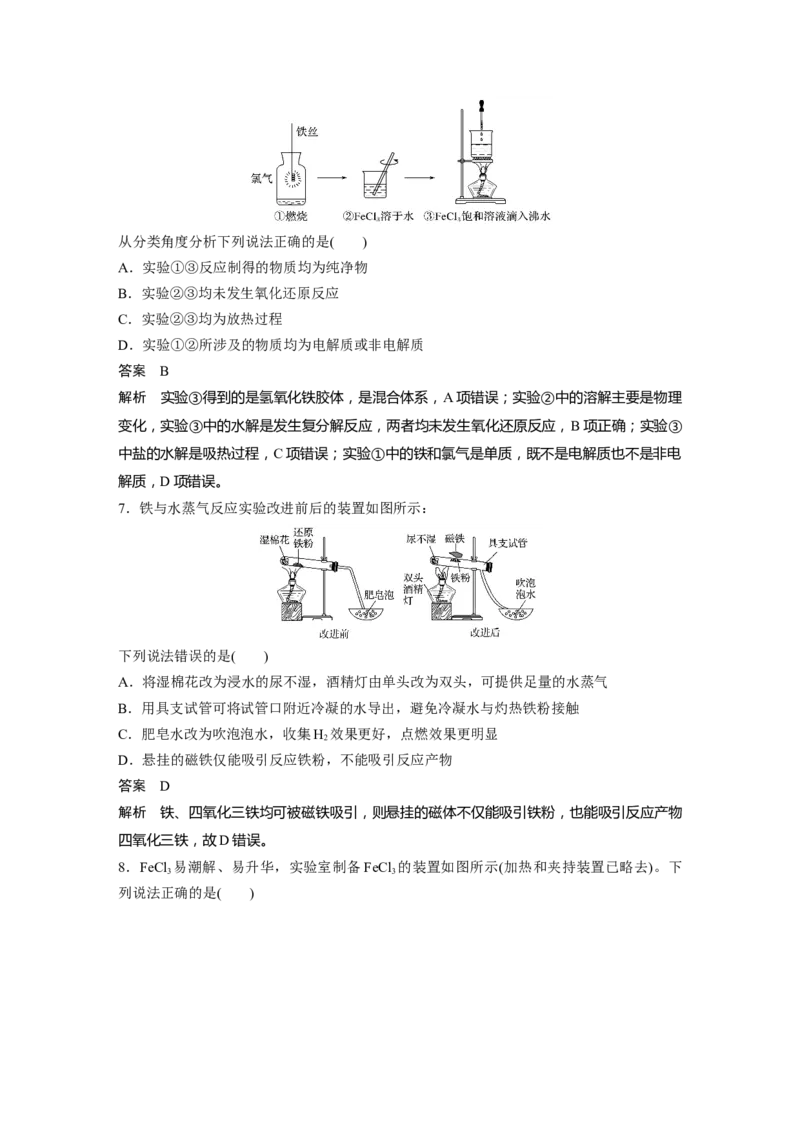
6.某学生以铁丝和Cl 为原料进行下列实验。
2从分类角度分析下列说法正确的是( )
A.实验①③反应制得的物质均为纯净物
B.实验②③均未发生氧化还原反应
C.实验②③均为放热过程
D.实验①②所涉及的物质均为电解质或非电解质
答案 B
解析 实验③得到的是氢氧化铁胶体,是混合体系,A项错误;实验②中的溶解主要是物理
变化,实验③中的水解是发生复分解反应,两者均未发生氧化还原反应,B项正确;实验③
中盐的水解是吸热过程,C项错误;实验①中的铁和氯气是单质,既不是电解质也不是非电
解质,D项错误。
7.铁与水蒸气反应实验改进前后的装置如图所示:
下列说法错误的是( )
A.将湿棉花改为浸水的尿不湿,酒精灯由单头改为双头,可提供足量的水蒸气
B.用具支试管可将试管口附近冷凝的水导出,避免冷凝水与灼热铁粉接触
C.肥皂水改为吹泡泡水,收集H 效果更好,点燃效果更明显
2
D.悬挂的磁铁仅能吸引反应铁粉,不能吸引反应产物
答案 D
解析 铁、四氧化三铁均可被磁铁吸引,则悬挂的磁体不仅能吸引铁粉,也能吸引反应产物
四氧化三铁,故D错误。
8.FeCl 易潮解、易升华,实验室制备FeCl 的装置如图所示(加热和夹持装置已略去)。下
3 3
列说法正确的是( )A.导管g的作用是增强装置的气密性
B.试剂X和试剂Y分别为浓硫酸、饱和食盐水
C.直接用E接收产物比用导管连接D、E的优点是可防止堵塞
D.出于简化装置的目的,F装置可拆除
答案 C
解析 导管g的作用是平衡气压,保证液体顺利滴下,A错误;为得到干燥纯净的Cl ,应
2
先用饱和食盐水除去HCl,再通过浓硫酸干燥气体,B错误;FeCl 易潮解,而F中的浓硫
3
酸起到干燥的作用,防止G中水蒸气进入D中,不能拆除,D错误。
9.将1.12 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是( )
A.铁粉有剩余,溶液呈浅绿色,Cl-浓度基本不变
B.往溶液中滴入KSCN溶液,溶液变红色
C.Fe2+和Fe3+的物质的量之比为5∶1
D.氧化产物与还原产物的物质的量之比为2∶5
答案 B
解析 n(Fe)==0.02 mol,n(FeCl )=2 mol·L-1×0.025 L=0.05 mol,由反应 Fe+2Fe3+
3
===3Fe2+知,0.02 mol铁粉完全反应需要0.04 mol氯化铁。铁完全反应,氯化铁有剩余,Cl
-浓度基本不变,A错误;氯化铁有剩余,往溶液中滴入KSCN溶液,显红色,B正确;
0.02 mol Fe反应生成Fe2+为0.06 mol,Fe3+剩余0.01 mol,其物质的量之比为6∶1,C错误;
氧化产物与还原产物均为氯化亚铁,Fe被氧化,氯化铁被还原,则氧化产物与还原产物的
物质的量之比为1∶2,D错误。
10.(2016·全国卷Ⅱ,28)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液。在FeCl 溶液中需加
2
入少量铁屑,其目的是___________________________________________________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明
2
Cl 可将Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为_____________________________。
2 2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl 溶液中先加入0.5 mL 煤油,
2
再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是____________。
(4)丙组同学取10 mL 0.1 mol·L-1KI溶液,加入6 mL 0.1 mol·L-1 FeCl 溶液混合。分别取 2
3
mL 此溶液于3支试管中进行如下实验:①第一支试管中加入1 mL CCl 充分振荡、静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K[Fe(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中
仍含有________(填离子符号),由此可以证明该氧化还原反应为________。
(5)丁组同学向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,发生
2 2 2
反 应 的 离 子 方 程 式 为
_______________________________________________________________;
一段时间后,溶液中有气泡出现,并放热,随后有红色沉淀生成。产生气泡的原因是
__________
____________________________________,生成沉淀的原因是______________________(用
平衡移动原理解释)。
答案 (1)防止Fe2+被氧化 (2)2Fe2++Cl===2Fe3++2Cl- (3)隔绝空气(排除氧气对实验的
2
影响)
(4)Fe2+ Fe3+ 可逆反应 (5)H O +2Fe2++2H+===2Fe3++2HO Fe3+催化HO 分解产生
2 2 2 2 2
O HO 分解反应放热,促进Fe3+的水解平衡正向移动
2 2 2
解析 (1)亚铁离子具有还原性,能被空气中的氧气氧化,所以在配制的 FeCl 溶液中加入少
2
量铁屑的目的是防止Fe2+被空气氧化。(2)Cl 可将Fe2+氧化成Fe3+,自身得电子生成Cl-,
2
反应的离子方程式为2Fe2++Cl===2Fe3++2Cl-。(3)煤油的作用是隔绝空气,防止空气中的
2
氧气将Fe2+氧化,产生干扰。(4)根据Fe2+的检验方法,向溶液中加入1滴K[Fe(CN) ] 溶液,
3 6
生成蓝色沉淀,一定含有Fe2+,则实验②检验的离子是Fe2+;碘易溶于CCl ,在CCl 中呈
4 4
紫色,Fe3+遇KSCN溶液显红色,实验①和③说明,在I-过量的情况下,溶液中仍含有Fe3
+,由此可以证明该氧化还原反应为可逆反应,反应为2Fe3++2I-2Fe2++I 。(5)H O 溶
2 2 2
液中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,发生反应的离子方程式为HO +2Fe2+
2 2 2
+2H+===2Fe3++2HO,铁离子的溶液呈棕黄色;一段时间后,溶液中有气泡出现,并放热,
2
随后有红褐色沉淀生成,产生气泡的原因是反应产生的 Fe3+是HO 分解的催化剂,促使
2 2
HO 分解生成O ,同时HO 分解反应是放热反应,促进了 Fe3+的水解平衡Fe3++3HO
2 2 2 2 2 2
Fe(OH) +3H+正向移动,产生较多 Fe(OH) ,聚集形成沉淀。
3 3