文档内容
专项提能特训 10 新型电源工作原理
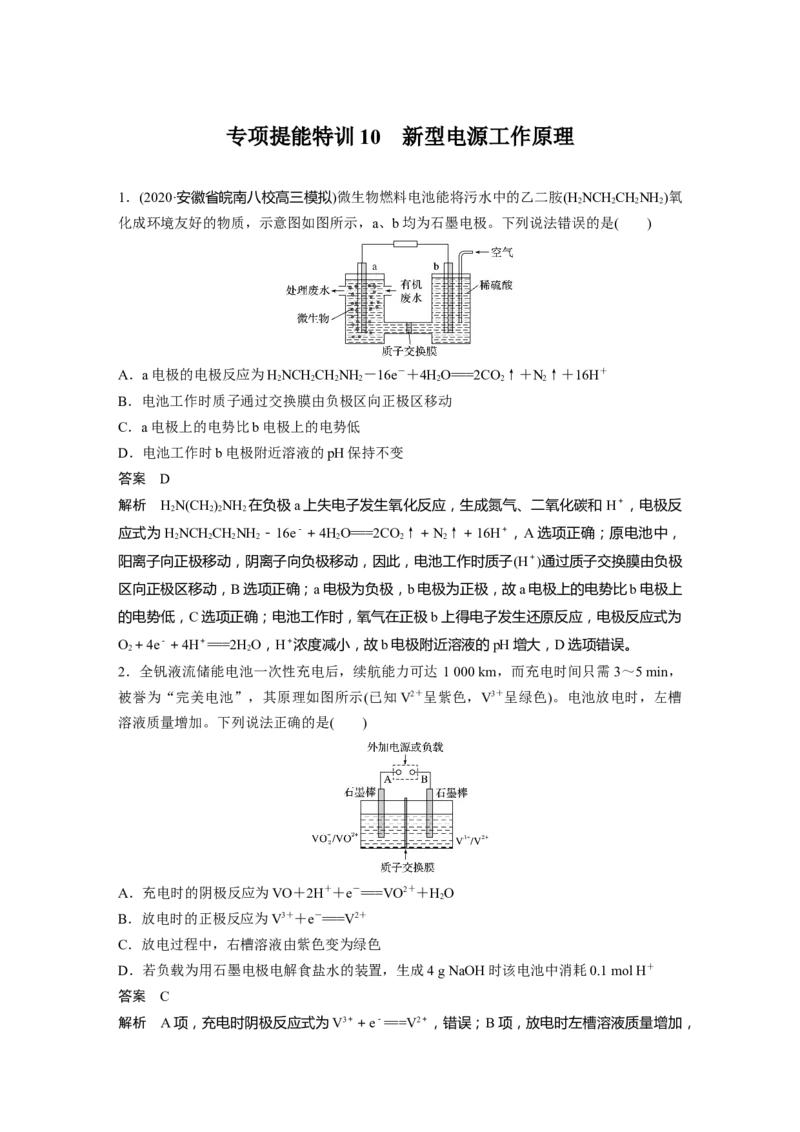
1.(2020·安徽省皖南八校高三模拟)微生物燃料电池能将污水中的乙二胺(H NCH CHNH )氧
2 2 2 2
化成环境友好的物质,示意图如图所示,a、b均为石墨电极。下列说法错误的是( )
A.a电极的电极反应为HNCH CHNH -16e-+4HO===2CO↑+N↑+16H+
2 2 2 2 2 2 2
B.电池工作时质子通过交换膜由负极区向正极区移动
C.a电极上的电势比b电极上的电势低
D.电池工作时b电极附近溶液的pH保持不变
答案 D
解析 HN(CH )NH 在负极a上失电子发生氧化反应,生成氮气、二氧化碳和 H+,电极反
2 2 2 2
应式为HNCH CHNH -16e-+4HO===2CO↑+N↑+16H+,A选项正确;原电池中,
2 2 2 2 2 2 2
阳离子向正极移动,阴离子向负极移动,因此,电池工作时质子(H+)通过质子交换膜由负极
区向正极区移动,B选项正确;a电极为负极,b电极为正极,故a电极上的电势比b电极上
的电势低,C选项正确;电池工作时,氧气在正极b上得电子发生还原反应,电极反应式为
O+4e-+4H+===2HO,H+浓度减小,故b电极附近溶液的pH增大,D选项错误。
2 2
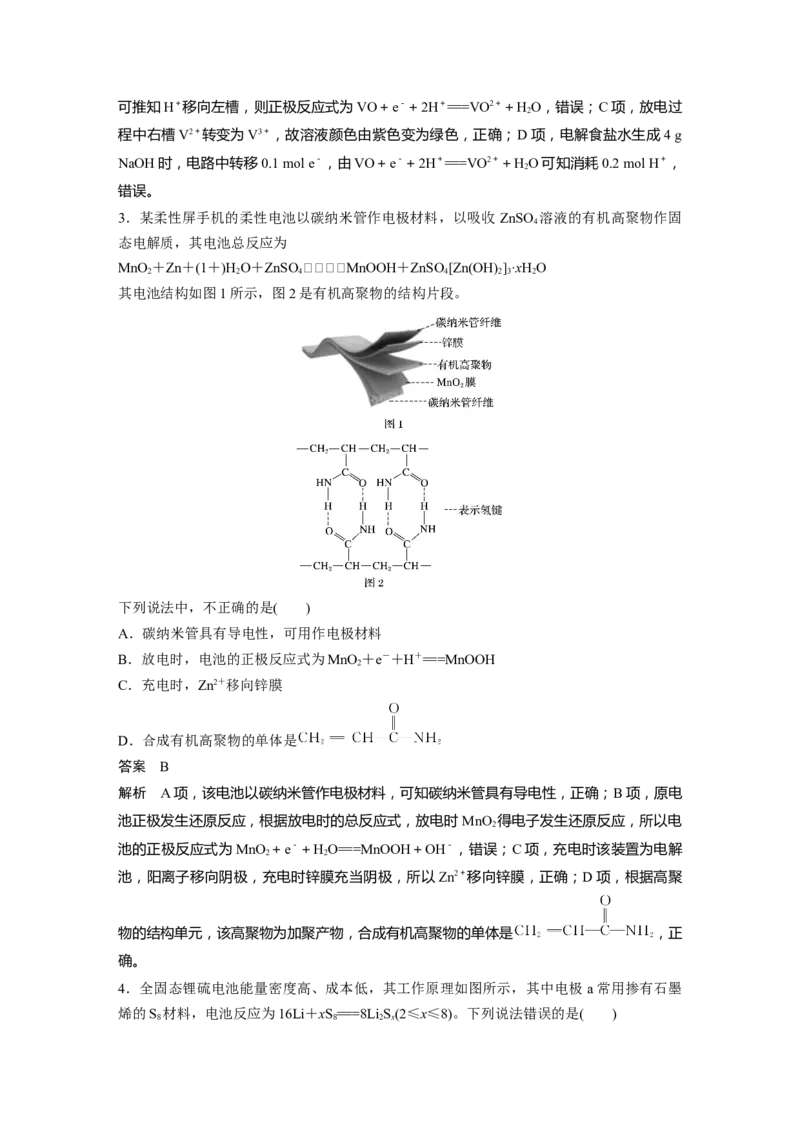
2.全钒液流储能电池一次性充电后,续航能力可达 1 000 km,而充电时间只需3~5 min,
被誉为“完美电池”,其原理如图所示(已知V2+呈紫色,V3+呈绿色)。电池放电时,左槽
溶液质量增加。下列说法正确的是( )
A.充电时的阴极反应为VO+2H++e-===VO2++HO
2
B.放电时的正极反应为V3++e-===V2+
C.放电过程中,右槽溶液由紫色变为绿色
D.若负载为用石墨电极电解食盐水的装置,生成4 g NaOH时该电池中消耗0.1 mol H+
答案 C
解析 A项,充电时阴极反应式为V3++e-===V2+,错误;B项,放电时左槽溶液质量增加,可推知H+移向左槽,则正极反应式为VO+e-+2H+===VO2++HO,错误;C项,放电过
2
程中右槽V2+转变为V3+,故溶液颜色由紫色变为绿色,正确;D项,电解食盐水生成4 g
NaOH时,电路中转移0.1 mol e-,由VO+e-+2H+===VO2++HO可知消耗0.2 mol H+,
2
错误。
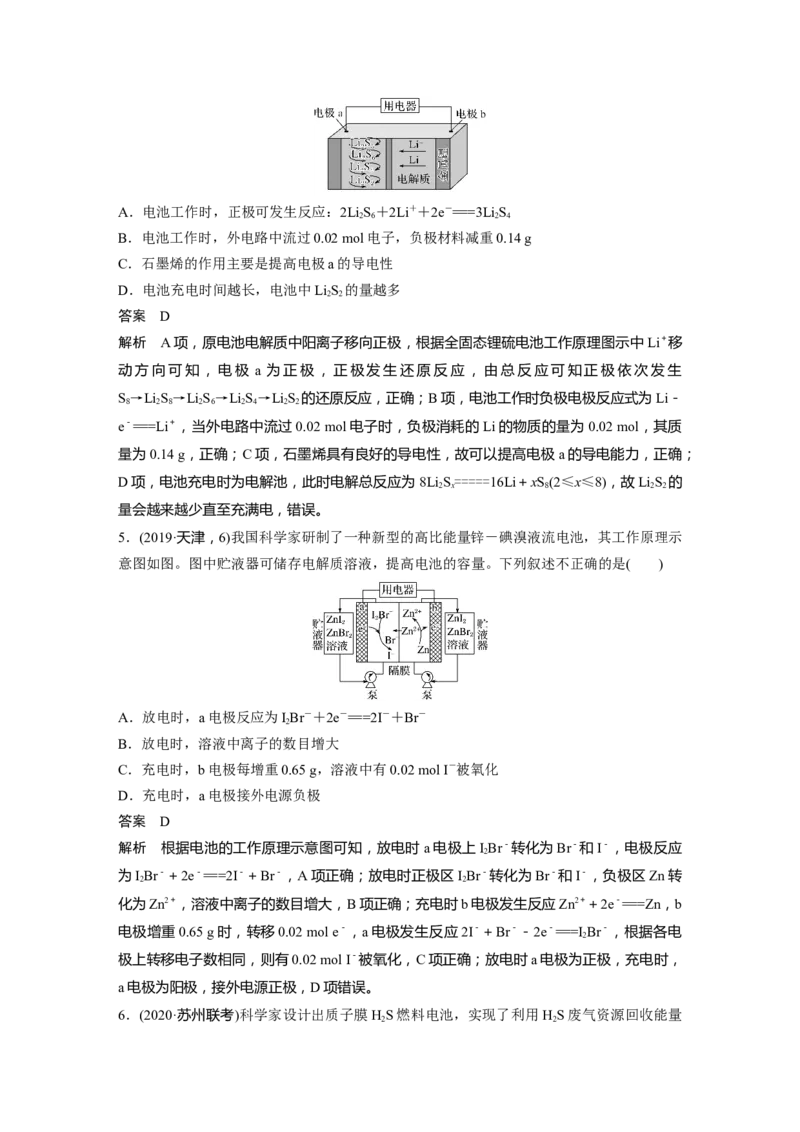
3.某柔性屏手机的柔性电池以碳纳米管作电极材料,以吸收 ZnSO 溶液的有机高聚物作固
4
态电解质,其电池总反应为
MnO +Zn+(1+)H O+ZnSOMnOOH+ZnSO[Zn(OH) ]·xHO
2 2 4 4 2 3 2
其电池结构如图1所示,图2是有机高聚物的结构片段。
下列说法中,不正确的是( )
A.碳纳米管具有导电性,可用作电极材料
B.放电时,电池的正极反应式为MnO +e-+H+===MnOOH
2
C.充电时,Zn2+移向锌膜
D.合成有机高聚物的单体是
答案 B
解析 A项,该电池以碳纳米管作电极材料,可知碳纳米管具有导电性,正确;B项,原电
池正极发生还原反应,根据放电时的总反应式,放电时 MnO 得电子发生还原反应,所以电
2
池的正极反应式为MnO +e-+HO===MnOOH+OH-,错误;C项,充电时该装置为电解
2 2
池,阳离子移向阴极,充电时锌膜充当阴极,所以Zn2+移向锌膜,正确;D项,根据高聚
物的结构单元,该高聚物为加聚产物,合成有机高聚物的单体是 ,正
确。
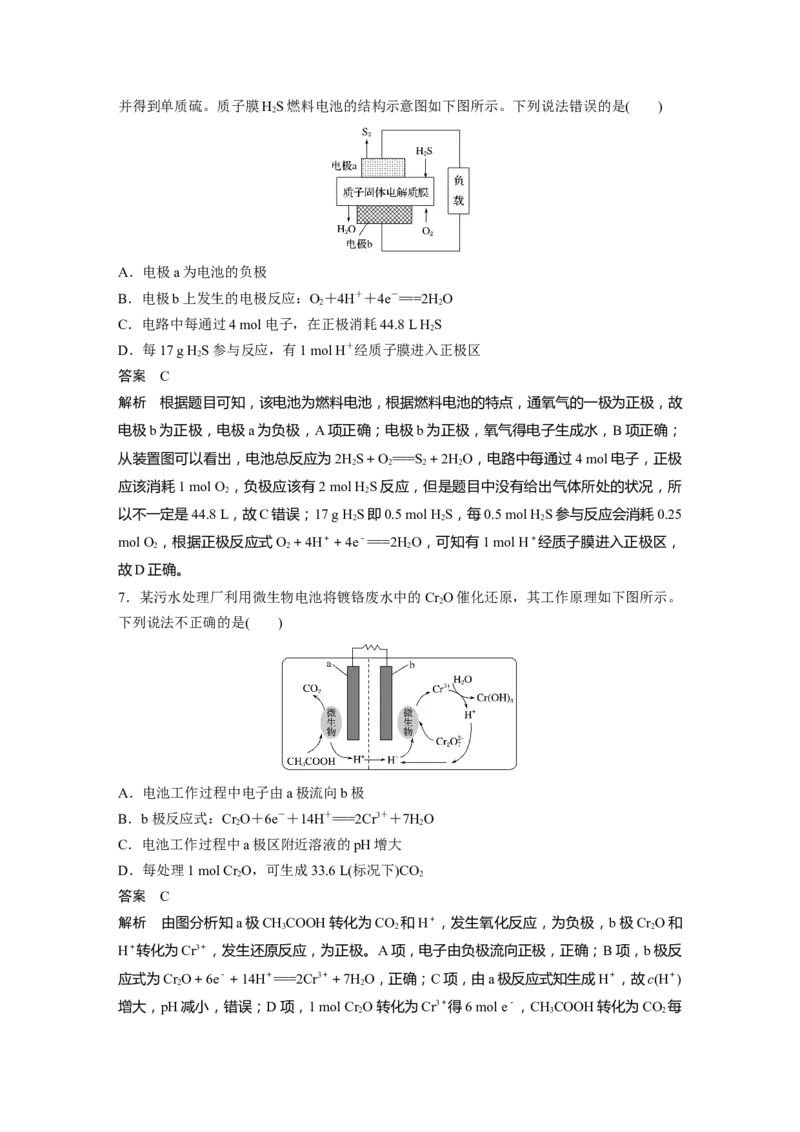
4.全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极 a常用掺有石墨
烯的S 材料,电池反应为16Li+xS===8LiS(2≤x≤8)。下列说法错误的是( )
8 8 2 xA.电池工作时,正极可发生反应:2LiS+2Li++2e-===3LiS
2 6 2 4
B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C.石墨烯的作用主要是提高电极a的导电性
D.电池充电时间越长,电池中LiS 的量越多
2 2
答案 D
解析 A项,原电池电解质中阳离子移向正极,根据全固态锂硫电池工作原理图示中Li+移
动方向可知,电极 a 为正极,正极发生还原反应,由总反应可知正极依次发生
S→LiS→LiS→LiS→LiS 的还原反应,正确;B项,电池工作时负极电极反应式为Li-
8 2 8 2 6 2 4 2 2
e-===Li+,当外电路中流过0.02 mol电子时,负极消耗的Li的物质的量为0.02 mol,其质
量为0.14 g,正确;C项,石墨烯具有良好的导电性,故可以提高电极a的导电能力,正确;
D项,电池充电时为电解池,此时电解总反应为8LiS=====16Li+xS(2≤x≤8),故LiS 的
2 x 8 2 2
量会越来越少直至充满电,错误。
5.(2019·天津,6)我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示
意图如图。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是( )
A.放电时,a电极反应为IBr-+2e-===2I-+Br-
2
B.放电时,溶液中离子的数目增大
C.充电时,b电极每增重0.65 g,溶液中有0.02 mol I-被氧化
D.充电时,a电极接外电源负极
答案 D
解析 根据电池的工作原理示意图可知,放电时 a电极上IBr-转化为Br-和I-,电极反应
2
为IBr-+2e-===2I-+Br-,A项正确;放电时正极区IBr-转化为Br-和I-,负极区Zn转
2 2
化为Zn2+,溶液中离子的数目增大,B项正确;充电时b电极发生反应Zn2++2e-===Zn,b
电极增重0.65 g时,转移0.02 mol e-,a电极发生反应2I-+Br--2e-===IBr-,根据各电
2
极上转移电子数相同,则有0.02 mol I-被氧化,C项正确;放电时a电极为正极,充电时,
a电极为阳极,接外电源正极,D项错误。
6.(2020·苏州联考)科学家设计出质子膜HS燃料电池,实现了利用HS废气资源回收能量
2 2并得到单质硫。质子膜HS燃料电池的结构示意图如下图所示。下列说法错误的是( )
2
A.电极a为电池的负极
B.电极b上发生的电极反应:O+4H++4e-===2HO
2 2
C.电路中每通过4 mol电子,在正极消耗44.8 L H S
2
D.每17 g HS参与反应,有1 mol H+经质子膜进入正极区
2
答案 C
解析 根据题目可知,该电池为燃料电池,根据燃料电池的特点,通氧气的一极为正极,故
电极b为正极,电极a为负极,A项正确;电极b为正极,氧气得电子生成水,B项正确;
从装置图可以看出,电池总反应为2HS+O===S +2HO,电路中每通过4 mol电子,正极
2 2 2 2
应该消耗1 mol O ,负极应该有2 mol H S反应,但是题目中没有给出气体所处的状况,所
2 2
以不一定是44.8 L,故C错误;17 g H S即0.5 mol H S,每0.5 mol H S参与反应会消耗0.25
2 2 2
mol O ,根据正极反应式O +4H++4e-===2HO,可知有1 mol H+经质子膜进入正极区,
2 2 2
故D正确。
7.某污水处理厂利用微生物电池将镀铬废水中的Cr O催化还原,其工作原理如下图所示。
2
下列说法不正确的是( )
A.电池工作过程中电子由a极流向b极
B.b极反应式:Cr O+6e-+14H+===2Cr3++7HO
2 2
C.电池工作过程中a极区附近溶液的pH增大
D.每处理1 mol Cr O,可生成33.6 L(标况下)CO
2 2
答案 C
解析 由图分析知a极CHCOOH转化为CO 和H+,发生氧化反应,为负极,b极Cr O和
3 2 2
H+转化为Cr3+,发生还原反应,为正极。A项,电子由负极流向正极,正确;B项,b极反
应式为Cr O+6e-+14H+===2Cr3++7HO,正确;C项,由a极反应式知生成H+,故c(H+)
2 2
增大,pH减小,错误;D项,1 mol Cr O转化为Cr3+得6 mol e-,CHCOOH转化为CO 每
2 3 2生成1 mol CO 失4 mol e-,故每处理1 mol CrO生成CO 的物质的量为 mol(标况下33.6 L),
2 2 2
正确。
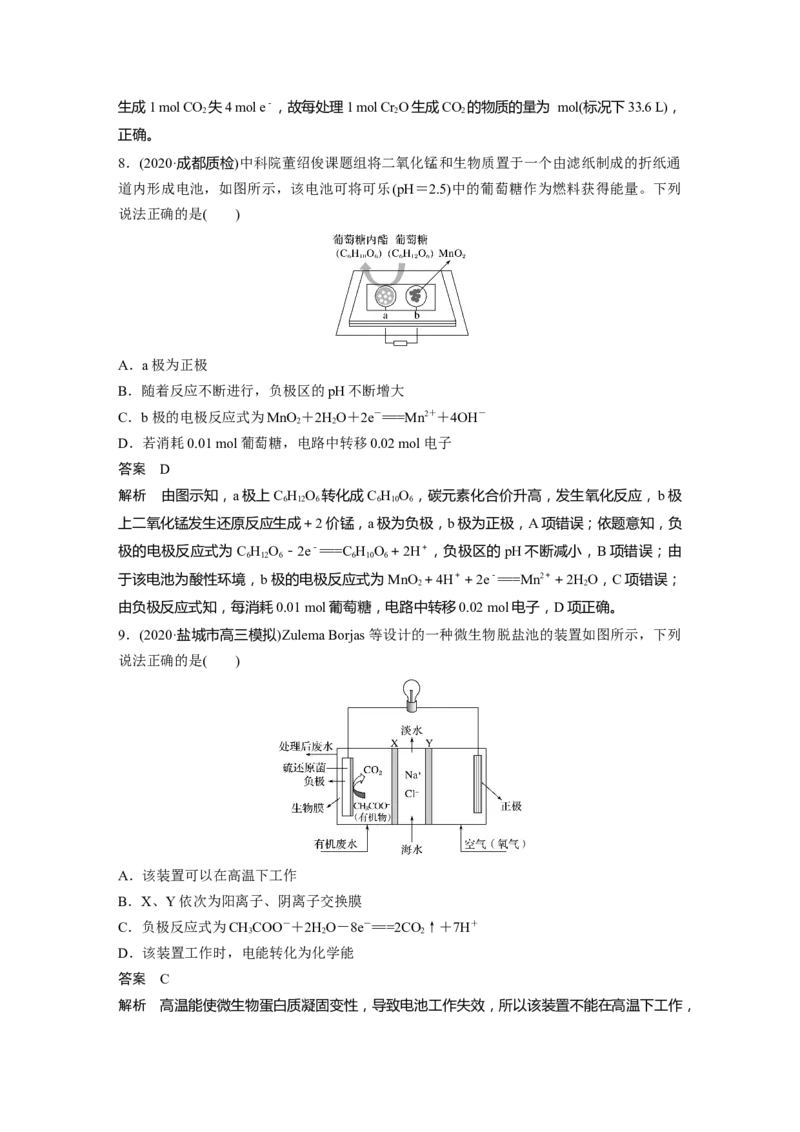
8.(2020·成都质检)中科院董绍俊课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通
道内形成电池,如图所示,该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列
说法正确的是( )
A.a极为正极
B.随着反应不断进行,负极区的pH不断增大
C.b极的电极反应式为MnO +2HO+2e-===Mn2++4OH-
2 2
D.若消耗0.01 mol葡萄糖,电路中转移0.02 mol电子
答案 D
解析 由图示知,a极上C H O 转化成C H O ,碳元素化合价升高,发生氧化反应,b极
6 12 6 6 10 6
上二氧化锰发生还原反应生成+2价锰,a极为负极,b极为正极,A项错误;依题意知,负
极的电极反应式为C H O -2e-===C H O +2H+,负极区的pH不断减小,B项错误;由
6 12 6 6 10 6
于该电池为酸性环境,b极的电极反应式为MnO +4H++2e-===Mn2++2HO,C项错误;
2 2
由负极反应式知,每消耗0.01 mol葡萄糖,电路中转移0.02 mol电子,D项正确。
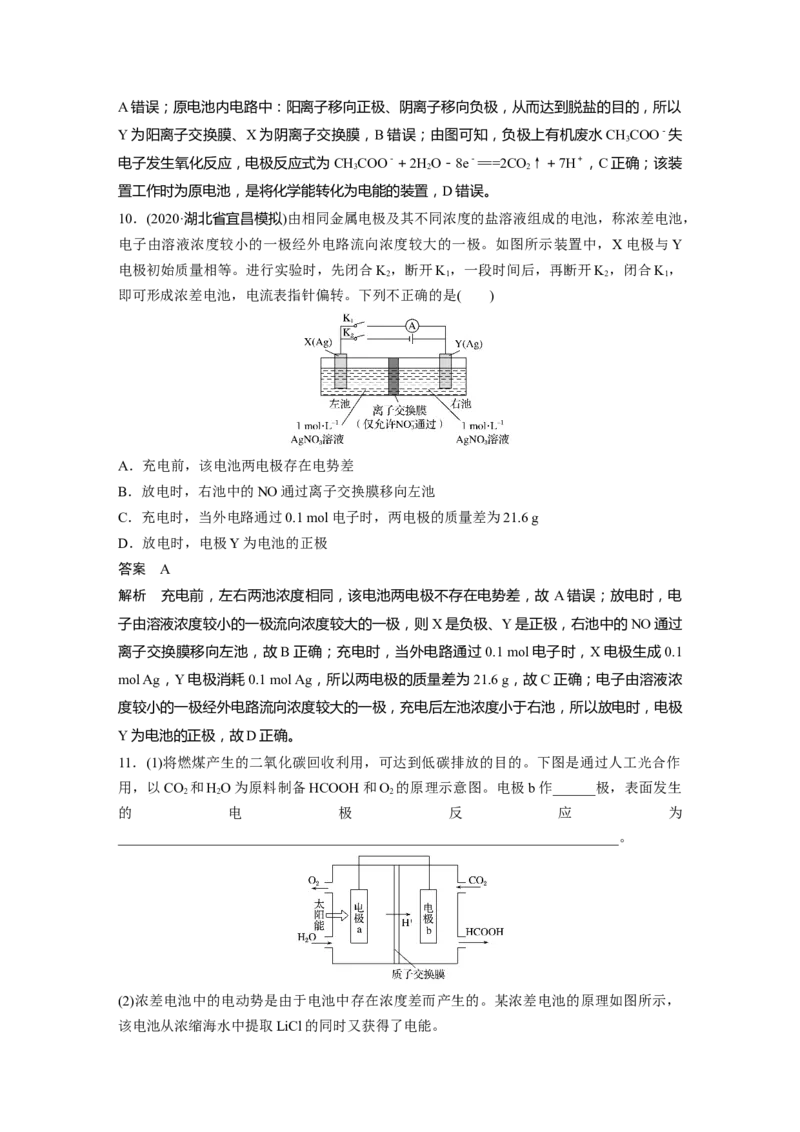
9.(2020·盐城市高三模拟)Zulema Borjas等设计的一种微生物脱盐池的装置如图所示,下列
说法正确的是( )
A.该装置可以在高温下工作
B.X、Y依次为阳离子、阴离子交换膜
C.负极反应式为CHCOO-+2HO-8e-===2CO↑+7H+
3 2 2
D.该装置工作时,电能转化为化学能
答案 C
解析 高温能使微生物蛋白质凝固变性,导致电池工作失效,所以该装置不能在高温下工作,A错误;原电池内电路中:阳离子移向正极、阴离子移向负极,从而达到脱盐的目的,所以
Y为阳离子交换膜、X为阴离子交换膜,B错误;由图可知,负极上有机废水CHCOO-失
3
电子发生氧化反应,电极反应式为CHCOO-+2HO-8e-===2CO↑+7H+,C正确;该装
3 2 2
置工作时为原电池,是将化学能转化为电能的装置,D错误。
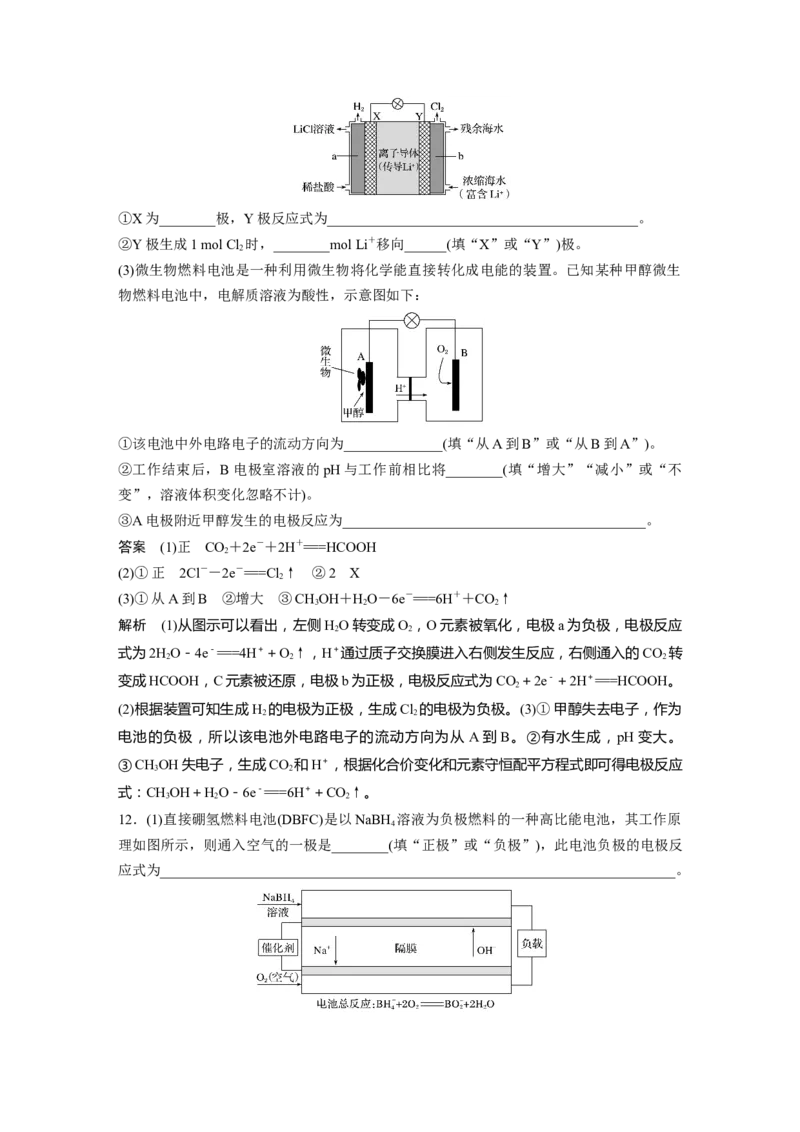
10.(2020·湖北省宜昌模拟)由相同金属电极及其不同浓度的盐溶液组成的电池,称浓差电池,
电子由溶液浓度较小的一极经外电路流向浓度较大的一极。如图所示装置中,X电极与Y
电极初始质量相等。进行实验时,先闭合K ,断开K ,一段时间后,再断开K ,闭合K ,
2 1 2 1
即可形成浓差电池,电流表指针偏转。下列不正确的是( )
A.充电前,该电池两电极存在电势差
B.放电时,右池中的NO通过离子交换膜移向左池
C.充电时,当外电路通过0.1 mol电子时,两电极的质量差为21.6 g
D.放电时,电极Y为电池的正极
答案 A
解析 充电前,左右两池浓度相同,该电池两电极不存在电势差,故 A错误;放电时,电
子由溶液浓度较小的一极流向浓度较大的一极,则X是负极、Y是正极,右池中的NO通过
离子交换膜移向左池,故B正确;充电时,当外电路通过0.1 mol电子时,X电极生成0.1
mol Ag,Y电极消耗0.1 mol Ag,所以两电极的质量差为21.6 g,故C正确;电子由溶液浓
度较小的一极经外电路流向浓度较大的一极,充电后左池浓度小于右池,所以放电时,电极
Y为电池的正极,故D正确。
11.(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作
用,以CO 和HO为原料制备HCOOH和O 的原理示意图。电极b作______极,表面发生
2 2 2
的 电 极 反 应 为
_______________________________________________________________________。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,
该电池从浓缩海水中提取LiCl的同时又获得了电能。①X为________极,Y极反应式为____________________________________________。
②Y极生成1 mol Cl 时,________mol Li+移向______(填“X”或“Y”)极。
2
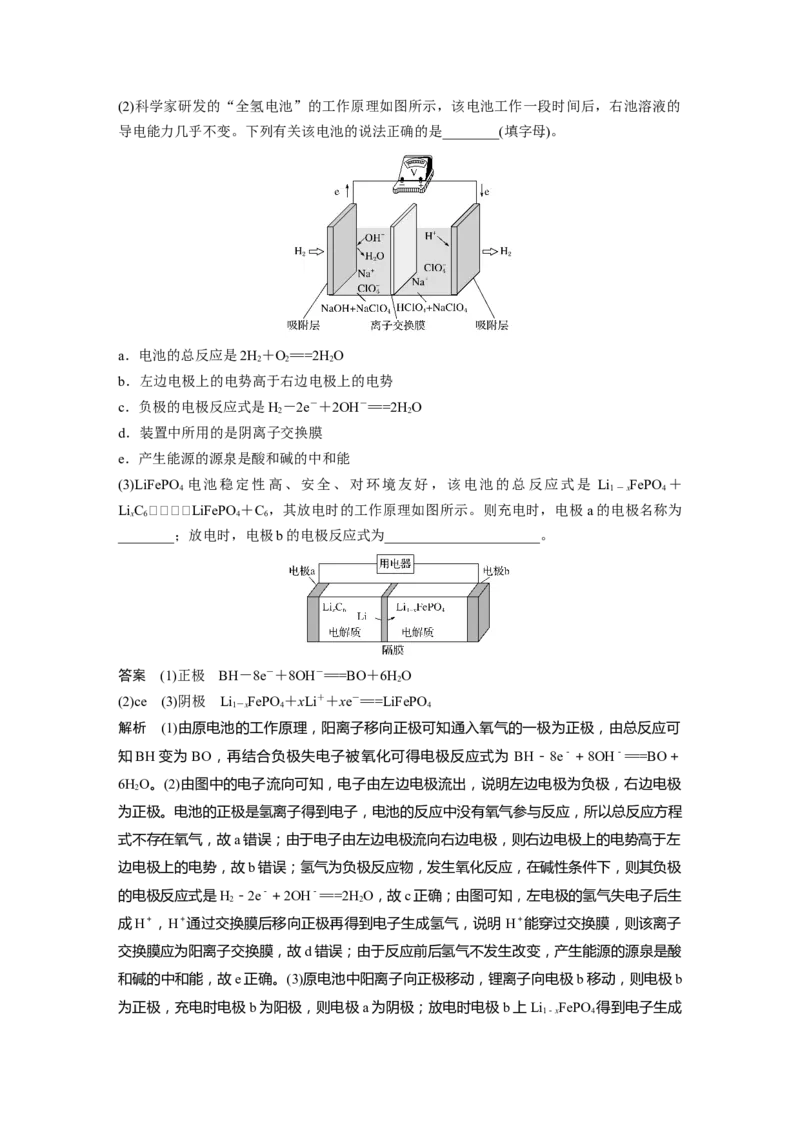
(3)微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生
物燃料电池中,电解质溶液为酸性,示意图如下:
①该电池中外电路电子的流动方向为______________(填“从A到B”或“从B到A”)。
②工作结束后,B电极室溶液的pH与工作前相比将________(填“增大”“减小”或“不
变”,溶液体积变化忽略不计)。
③A电极附近甲醇发生的电极反应为___________________________________________。
答案 (1)正 CO+2e-+2H+===HCOOH
2
(2)①正 2Cl--2e-===Cl↑ ②2 X
2
(3)①从A到B ②增大 ③CHOH+HO-6e-===6H++CO↑
3 2 2
解析 (1)从图示可以看出,左侧HO转变成O ,O元素被氧化,电极a为负极,电极反应
2 2
式为2HO-4e-===4H++O↑,H+通过质子交换膜进入右侧发生反应,右侧通入的CO 转
2 2 2
变成HCOOH,C元素被还原,电极b为正极,电极反应式为CO+2e-+2H+===HCOOH。
2
(2)根据装置可知生成H 的电极为正极,生成Cl 的电极为负极。(3)①甲醇失去电子,作为
2 2
电池的负极,所以该电池外电路电子的流动方向为从 A到B。②有水生成,pH变大。
③CHOH失电子,生成CO 和H+,根据化合价变化和元素守恒配平方程式即可得电极反应
3 2
式:CHOH+HO-6e-===6H++CO↑。
3 2 2
12.(1)直接硼氢燃料电池(DBFC)是以NaBH 溶液为负极燃料的一种高比能电池,其工作原
4
理如图所示,则通入空气的一极是________(填“正极”或“负极”),此电池负极的电极反
应式为_________________________________________________________________________。(2)科学家研发的“全氢电池”的工作原理如图所示,该电池工作一段时间后,右池溶液的
导电能力几乎不变。下列有关该电池的说法正确的是________(填字母)。
a.电池的总反应是2H+O===2HO
2 2 2
b.左边电极上的电势高于右边电极上的电势
c.负极的电极反应式是H-2e-+2OH-===2HO
2 2
d.装置中所用的是阴离子交换膜
e.产生能源的源泉是酸和碱的中和能
(3)LiFePO 电池稳定性高、安全、对环境友好,该电池的总反应式是 Li FePO +
4 1-x 4
LiC LiFePO +C ,其放电时的工作原理如图所示。则充电时,电极 a的电极名称为
x 6 4 6
________;放电时,电极b的电极反应式为______________________。
答案 (1)正极 BH-8e-+8OH-===BO+6HO
2
(2)ce (3)阴极 Li FePO +xLi++xe-===LiFePO
1-x 4 4
解析 (1)由原电池的工作原理,阳离子移向正极可知通入氧气的一极为正极,由总反应可
知BH变为BO,再结合负极失电子被氧化可得电极反应式为 BH-8e-+8OH-===BO+
6HO。(2)由图中的电子流向可知,电子由左边电极流出,说明左边电极为负极,右边电极
2
为正极。电池的正极是氢离子得到电子,电池的反应中没有氧气参与反应,所以总反应方程
式不存在氧气,故a错误;由于电子由左边电极流向右边电极,则右边电极上的电势高于左
边电极上的电势,故b错误;氢气为负极反应物,发生氧化反应,在碱性条件下,则其负极
的电极反应式是H-2e-+2OH-===2HO,故c正确;由图可知,左电极的氢气失电子后生
2 2
成H+,H+通过交换膜后移向正极再得到电子生成氢气,说明 H+能穿过交换膜,则该离子
交换膜应为阳离子交换膜,故d错误;由于反应前后氢气不发生改变,产生能源的源泉是酸
和碱的中和能,故e正确。(3)原电池中阳离子向正极移动,锂离子向电极b移动,则电极b
为正极,充电时电极b为阳极,则电极a为阴极;放电时电极b上Li FePO 得到电子生成
1-x 4LiFePO ,电极反应式为Li FePO +xLi++xe-===LiFePO 。
4 1-x 4 4