文档内容
第 40 讲 盐类水解
复习目标 1.了解盐类水解的原理及其一般规律。2.掌握水解离子方程式的书写。3.了解影
响盐类水解程度的主要因素。4.了解盐类水解的应用。5.能利用水解常数(K )进行相关计算。
h
考点一 盐类水解及其规律
1.盐类的水解
2.盐类水解规律
有弱才水解,越弱越水解;谁强显谁性,同强显中性。
是否 溶液的
盐的类型 实例 水解的离子 溶液的pH
水解 酸碱性
强酸强碱盐 NaCl、KNO 否 - 中性 pH = 7
3
NH Cl、
4
强酸弱碱盐 是 NH 、 Cu 2 + 酸性 pH < 7
Cu(NO )
3 2
CHCOONa、
3
弱酸强碱盐 是 CH COO - 、 CO 碱性 pH>7
3
NaCO
2 3
3.盐类水解离子方程式的书写
(1)由于水解是微弱的反应,因而反应物与生成物用“”连接,易挥发性物质不标
“↑”,难溶物不标“↓”,易分解的物质不拆开书写(相互促进水解者除外)。
如NaHCO (aq):____________________________________________________________。
3
NH Cl(aq):________________________________________________________________。
4(2)多元弱酸盐的水解分步写:
如NaS(aq):第一步:S2-+HOHS-+OH-;
2 2
第二步:HS-+HOHS+OH-,水解以第一步水解为主。
2 2
(3)金属阳离子(弱碱的阳离子)水解一步写到底:
如 AlCl (aq) :
3
__________________________________________________________________。
(4)相互促进水解时,由于反应彻底,故生成物中出现的不溶于水的________或________均
要注明状态,即写上“↓”或“↑”符号,中间用“===”连接。如NaHCO 与Al (SO ) 混
3 2 4 3
合反应:3HCO+Al3+===Al(OH) ↓+3CO↑。
3 2
答案 (1)HCO+HOHCO+OH-
2 2 3
NH+HONH ·H O+H+
2 3 2
(3)Al3++3HOAl(OH) +3H+
2 3
(4)沉淀 气体
(1)溶液呈中性的盐一定是强酸、强碱生成的盐(×)
错因: 发生水解的盐溶液不一定呈酸性或碱性,也可能呈中性,如 CH COONH。
3 4
(2)酸式盐溶液可能呈酸性,也可能呈碱性(√)
(3)pH相同的盐酸和氯化铵溶液中由水电离出的c(H+)相同(×)
错因:酸抑制水的电离,盐类水解促进水的电离。
(4)Na CO 溶液中CO的水解:CO+HO===HCO+OH-(×)
2 3 2
错因:水解微弱,应该用可逆号。
(5)FeCl 溶液与NaHCO 溶液混合:Fe3++3HCO===Fe(OH) ↓+3CO↑(√)
3 3 3 2
1.怎样用最简单的方法区别NaCl溶液、氯化铵溶液和碳酸钠溶液?
答案 三种溶液各取少许分别滴入紫色石蕊溶液,不变色的为 NaCl溶液,变红色的为氯化
铵溶液,变蓝色的为碳酸钠溶液。
2.常温下,同浓度的①NaCO ,②CHCOONa,③NaHCO 溶液,pH由大到小的顺序是
2 3 3 3
________。
答案 ①>③>②
3.已知常温下三种物质的电离常数,CHCOOH(K),NH ·H O(K ),HCO(K )其关系为
3 a 3 2 b 2 3 a1
______________则 CHCOONH 溶液显________性(填“酸”“碱”或“中”,下同),
3 4
NH HCO 溶液显________性。
4 3
答案 K=K >K 中 碱
a b a1
题组一 盐类水解的实质及规律1.常温下,浓度均为0.1 mol·L-1的下列四种盐溶液,其pH测定如表所示:
序号 ① ② ③ ④
溶液 CHCOONa NaHCO NaCO NaClO
3 3 2 3
pH 8.8 9.7 11.6 10.3
下列说法正确的是( )
A.四种溶液中,水的电离程度:①>②>④>③
B.NaCO 和NaHCO 溶液中,粒子种类相同
2 3 3
C.将等浓度的CHCOOH和HClO溶液比较,pH小的是HClO
3
D.NaCO 溶液中,c(Na+)=c(CO)+c(HCO)+c(H CO)
2 3 2 3
答案 B
解析 这几种盐都是强碱弱酸盐,弱酸根离子发生水解反应使溶液显碱性,当盐的浓度相同
时,酸的酸性越弱,酸根离子水解的程度就越大,水的电离程度就越大,溶液的碱性就越强。
根据表格数据可知四种溶液中,水的电离程度:①<②<④<③,A 错误;在 NaCO 和
2 3
NaHCO 溶液中,存在的粒子有Na+、HCO、CO、HCO 、HO、H+、OH-,所以粒子种类
3 2 3 2
相同,B正确;根据盐的水解程度大小可知,等浓度的 CHCOOH和HClO溶液的酸性:
3
CHCOOH>HClO,所以pH小的是CHCOOH,C错误;在NaCO 溶液中,根据物料守恒
3 3 2 3
可得c(Na+)=2c(CO)+2c(HCO)+2c(H CO),D错误。
2 3
2.室温下,0.1 mol·L-1的NH CN溶液的pH等于9.32,据此,下列说法错误的是( )
4
A.上述溶液能使甲基橙试剂变黄色
B.室温下,NH ·H O是比HCN更弱的电解质
3 2
C.上述溶液中CN-的水解程度大于NH的水解程度
D.室温下,0.1 mol·L-1 NaCN溶液中,CN-的水解程度小于上述溶液中CN-的水解程度
答案 B
解析 室温下,溶液呈碱性,则溶液能使甲基橙试剂变黄色,故 A正确;HCN和NH ·H O
3 2
均是弱电解质,溶液呈碱性,说明CN-的水解程度大于NH的水解程度,由越弱越水解知
NH ·H O是比HCN强的电解质,故B错误,C正确;CN-、NH相互促进水解,所以0.1 mol·L
3 2
-1
NaCN溶液中,CN-的水解程度小于同浓度下NH CN溶液中CN-的水解程度,故D正确。
4
3.A+、B+、C-、D-四种离子两两组成四种可溶性盐,其中:AC和BD盐溶液pH=7,
BC盐溶液pH>7,则下列说法不正确的是( )
A.AD盐溶液pH<7
B.在AC盐溶液中c(A+)+c(AOH)=c(C-)+c(HC)
C.碱的电离程度一定是AOH>BOH
D.酸的电离程度一定是HD>HC答案 C
解析 在盐类水解中,遵循“有弱就水解,越弱越水解,谁强显谁性,同强显中性”的规律,
C项错误,D项正确;AD为强酸弱碱盐,显酸性,A项正确;由物料守恒可知,B项正确。
题组二 水解离子方程式的书写与判断
4.下列物质在常温时发生水解,对应的离子方程式正确的是( )
A.NaCO:CO+2HOHCO+2OH-
2 3 2 2 3
B.CuSO :Cu2++2HO===Cu(OH) +2H+
4 2 2
C.NaAlO :AlO+2HOAl(OH) +OH-
2 2 3
D.NaF:F-+HO===HF+OH-
2
答案 C
解析 A项,应为CO+HOHCO+OH-、HCO+HOHCO +OH-;B项,应为Cu2
2 2 2 3
++2HOCu(OH) +2H+;D项,应为F-+HOHF+OH-。
2 2 2
5.写出下列物质常温下溶于水发生反应的离子方程式,判断指定溶液的酸碱性。
(1) 明 矾 ______________________________________________________________ ,
pH______7。
(2) CH COONH______________________________________________________ ,
3 4
pH______7。
(3) Al S_________________________________________________________________。
2 3
答案 (1)Al3++3HOAl(OH) +3H+ <
2 3
(2) CH COO-+NH+HOCHCOOH+NH ·H O =
3 2 3 3 2
(3) Al S+6HO===2Al(OH) ↓+3HS↑
2 3 2 3 2
6.解答下列问题
(1)NaHS溶液呈碱性的原因_____________________________________________。
(2)对于易溶于水的正盐 MR 溶液,已知只有一种离子可能水解,若 pH>7,其原因是
n m
_____________(用离子方程式说明,下同);若pH<7,其原因是________________________。
答案 (1)NaHS溶液中存在:水解HS-+HOHS+OH-和电离HS-H++S2-两个平
2 2
衡,其水解程度大于电离程度,因而溶液呈碱性
(2)Rn-+HOHR(n-1)-+OH-
2
Mm++mHOM(OH) +mH+
2 m
解析 pH大于7是由于弱酸酸根离子水解呈碱性,pH小于7是由于弱碱阳离子水解呈酸性。
1.判断酸式盐的水溶液的酸碱性要看该盐的构成微粒的实际表现。
(1)强酸的酸式盐只电离,不水解,溶液一定显酸性,如:NaHSO===Na++H++SO。
4
(2)弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
①电离程度小于水解程度,溶液显碱性,如NaHCO 溶液中:
3HCOH++CO(次要)
HCO+HOHCO+OH-(主要)
2 2 3
使c(OH-)>c(H+),溶液显碱性。
同理NaHS溶液、NaHPO 溶液显碱性。
2 4
②电离程度大于水解程度,溶液显酸性,如NaHSO 溶液中:
3
HSOH++SO(主要)
HSO+HOHSO +OH-(次要)
2 2 3
使c(H+)>c(OH-),溶液显酸性。同理NaH PO 溶液显酸性。
2 4
2.NH与CHCOO-、HCO、CO等在水解时相互促进,其水解程度比单一离子的水解程度
3
大,但水解程度仍然比较弱,不能进行完全,在书写水解方程式时用“”。
考点二 盐类水解的影响因素及应用
1.影响盐类水解平衡的因素
(1)内因:生成盐的弱酸或弱碱越弱,其对应的弱酸酸根离子或弱碱阳离子的水解程度越大,
溶液的碱性或酸性越强。
如水解程度:NaCO>NaSO ,NaCO>NaHCO 。
2 3 2 3 2 3 3
(2)外因
(3)以FeCl 水解为例:Fe3++3HOFe(OH) +3H+,分析外界条件对水解平衡的影响。
3 2 3
条件 平衡移动方向 H+数 pH 现象
升温 向右 增多 减小 颜色变深
通HCl 向左 增多 减小 颜色变浅
加HO 向右 增多 增大 颜色变浅
2
加NaHCO 向右 减小 增大 生成红褐色沉淀,放出气体
3
2.盐类水解的应用
(1)判断溶液的酸碱性
NaCO 溶液呈碱性的原因:
2 3
CO+HOHCO+OH-
2
(2)配制或贮存易水解的盐溶液
如配制FeCl 溶液时,先将它溶解在较浓的盐酸中,再加水至指定浓度;配制CuSO 溶液时,
3 4
加入少量的HSO ,以抑制Cu2+水解。
2 4
(3)判断盐溶液蒸干灼烧时所得的产物如将AlCl 、FeCl 溶液蒸干后得到Al(OH) 、Fe(OH) ,灼烧得到Al O 、Fe O ;CuSO 溶液
3 3 3 3 2 3 2 3 4
蒸干后得到CuSO 固体。
4
(4)离子共存
如Al3+、Fe3+与HCO、CO、AlO因相互促进水解而不共存。Al3+与S2-因相互促进水解而
不共存,但Fe3+与S2-发生氧化还原反应,不共存。
(5)解释生活中的现象
如明矾净水、热纯碱溶液除油污,草木灰不能与铵盐混用、泡沫灭火器工作原理等。
(6)离子浓度大小的比较
如碳酸氢钠溶液中离子浓度大小顺序为c(Na+)>c(HCO)>c(OH-)>c(H+)。
(7)物质的提纯(水解除杂)
如MgCl 溶液中混有少量Fe3+杂质时,因Fe3+的水解程度比Mg2+的水解程度大,可加入
2
MgO或Mg(OH) 等,使水解平衡右移,生成Fe(OH) 沉淀而除去。
2 3
在酸性较强的环境中Fe3+比Al3+、Mg2+、Cu2+更易发生水解,可采用加入CuO、Cu(OH)
2
等调节pH的方法生成Fe(OH) 沉淀除去,但不能用会引入杂质离子的物质。
3
(1)稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强(×)
错因: 盐的浓度越小,水解程度越大,生成的 H + ( 或 OH - ) 的物质的量越多,但 H + ( 或 OH - )
的浓度是减小的。
(2)加热0.1 mol·L-1 Na CO 溶液,减小(×)
2 3
错因:升温,CO的水解程度增大,应增大。
(3)通入适量的HCl气体使FeCl 溶液中增大(×)
3
错因:通入HCl抑制了Fe3+的水解,Fe3+浓度增大的很少,Cl-浓度增大的多,故减小。
(4)水解相互促进的离子在同一溶液中一定不能共存(×)
错因:水解相互促进没有沉淀和气体生成的离子可以共存,例如:铵根和醋酸根。
题组一 水解平衡移动及结果分析
1.向三份0.1 mol·L-1的CHCOONa溶液中分别加入少量NH NO 、NaSO 、FeCl 固体(忽
3 4 3 2 3 2
略溶液体积变化),则CHCOO-浓度的变化依次为( )
3
A.减小、增大、减小 B.增大、减小、减小
C.减小、增大、增大 D.增大、减小、增大
答案 A
解析 CHCOONa 溶液中存在水解平衡 CHCOO-+HOCHCOOH+OH-,加入的
3 3 2 3
NH NO 和FeCl 水解显酸性,故促进其平衡正向移动,则 CHCOO-浓度减小;加入的
4 3 2 3
NaSO 水解显碱性,对水解有抑制作用,故CHCOO-浓度增大。
2 3 3
2.下列有关电解质溶液的说法不正确的是( )A.向NaCO 溶液中通入NH ,减小
2 3 3
B.将0.1 mol·L-1的KC O 溶液从25 ℃升温至35 ℃,增大
2 2 4
C.向0.1 mol·L-1的HF溶液中滴加NaOH溶液至中性,=1
D.向0.1 mol·L-1的CHCOONa溶液中加入少量水,增大
3
答案 D
解析 NaCO 溶液中存在平衡 CO+HOHCO+OH-,通入 NH ,NH 溶于水生成
2 3 2 3 3
NH ·H O,存在电离NH ·H ONH+OH-,抑制了CO的水解,c(CO)增大,又因为c(Na
3 2 3 2
+)不变,所以减小,故A正确;KC O 溶液中存在C O水解,水解吸热,若从25 ℃升温至
2 2 4 2
35 ℃,促进了C O的水解,c(C O)减小,又因为c(K+)不变,所以增大,故B正确;向0.1
2 2
mol·L-1的HF溶液中滴加NaOH溶液至中性,根据电荷守恒c(Na+)+c(H+)=c(F-)+c(OH
-),c(H+)=c(OH-),则c(Na+)=c(F-),即=1,故C正确;CHCOOH的电离常数K=,
3 a
所以=,电离常数只受温度影响,温度不变则K 不变,故D错误。
a
3.(2020·长沙模拟)在一定条件下,NaS溶液中存在水解平衡:S2-+HOHS-+OH-。
2 2
下列说法正确的是( )
A.稀释溶液,水解平衡常数增大
B.加入CuSO 固体,HS-浓度减小
4
C.升高温度,减小
D.加入NaOH固体,溶液pH减小
答案 B
解析 水解常数只与温度有关,A错误;Cu2++S2-===CuS↓,平衡左移,HS-浓度减小,
B正确;水解为吸热反应,升高温度平衡右移,因而增大,C错误;加入NaOH固体,溶液
pH增大,D错误。
题组二 水解原理的应用
4.下列有关问题与盐的水解有关的是( )
①NH Cl与ZnCl 溶液可作焊接金属时的除锈剂
4 2
②NaHCO 与Al (SO ) 两种溶液可作泡沫灭火剂
3 2 4 3
③草木灰与铵态氮肥不能混合施用
④实验室中盛放NaCO 溶液的试剂瓶不能用磨口玻璃塞
2 3
⑤加热蒸干CuCl 溶液得到Cu(OH) 固体
2 2
⑥要除去FeCl 溶液中混有的Fe2+,可先通入氧化剂Cl,再调节溶液的pH
3 2
A.①②③⑥ B.②③④⑥
C.①④⑤⑥ D.①②③④⑤
答案 D
解析 ①NH Cl和ZnCl 均为强酸弱碱盐,溶液中NH与Zn2+均发生水解反应,溶液显酸性,
4 2
可以除去金属表面的锈;②HCO与Al3+发生相互促进的水解反应,产生CO ,可作灭火剂;
2③草木灰的主要成分为KCO,水解显碱性,而铵态氮肥水解显酸性,因而二者不能混合施
2 3
用;④NaCO 溶液水解显碱性,而磨口玻璃塞中的二氧化硅会与碱反应生成NaSiO,将瓶
2 3 2 3
塞与瓶口黏合在一起,因此实验室盛放NaCO 溶液的试剂瓶应用橡胶塞;⑤CuCl 溶液中
2 3 2
存在水解平衡,CuCl +2HOCu(OH) +2HCl,加热时,HCl挥发使平衡不断右移,最终
2 2 2
得到Cu(OH) 固体;⑥Cl 能将Fe2+氧化成Fe3+,且没有引入杂质,与盐的水解无关。
2 2
5.下列根据反应原理设计的应用,不正确的是( )
A.CO+HOHCO+OH- 用热的纯碱溶液清洗油污
2
B.Al3++3HOAl(OH) (胶体)+3H+ 明矾净水
2 3
C.TiCl +(x+2)H O(过量)TiO·xHO↓+4HCl 用TiCl 制备TiO
4 2 2 2 4 2
D.SnCl +HOSn(OH)Cl↓+HCl 配制氯化亚锡溶液时加入NaOH固体
2 2
答案 D
解析 升高温度,促使CO的水解平衡正向移动,溶液中c(OH-)增大,碱性增强,有利于
油污的水解及清洗,A正确;明矾是KAl(SO )·12H O,Al3+发生水解生成Al(OH) 胶体,可
4 2 2 3
吸附水中的悬浮杂质,起到净水作用,B正确;TiCl 发生水解反应生成TiO·xHO沉淀,经
4 2 2
脱水制备TiO ,C正确;SnCl 易发生水解反应,而配制其溶液时,加入NaOH固体,消耗
2 2
HCl促使水解平衡正向移动,生成Sn(OH)Cl沉淀,故应加入HCl溶液抑制其水解,D错误。
6.下列物质的水溶液在空气中小心加热蒸干至质量不再减少为止,能得到较纯净的原溶质
的是( )
①CuSO ②FeSO ③KCO ④Ca(HCO ) ⑤NH HCO ⑥KMnO ⑦FeCl
4 4 2 3 3 2 4 3 4 3
A.全部都可以 B.仅①②③
C.仅①③⑥ D.仅①③
答案 D
解析 FeSO 溶液加热过程中生成 Fe(OH) 和 HSO ,又由于 Fe(OH) 会被氧化生成
4 2 2 4 2
Fe(OH) ,故蒸干后得到Fe (SO ) 和Fe(OH) 的混合物;Ca(HCO ) 受热会分解生成CaCO ;
3 2 4 3 3 3 2 3
NH HCO 受热分解生成NH 、HO、CO ;KMnO 受热分解生成KMnO 和MnO ;FeCl 受
3 3 3 2 2 4 2 4 2 3
热促进水解生成Fe(OH) 和盐酸,而盐酸挥发进一步促进其水解,最终水解彻底,受热分解
3
得到的固体物质是Fe O。
2 3
题组三 平衡移动与实验探究
7 .已知: [FeCl(H O) ] -为黄色,溶液中可以存在可逆反应: Fe3++ 4Cl -+
4 2 2
2HO[FeCl(H O) ]-,下列实验所得结论不正确的是( )
2 4 2 2
① ② ③ ④
加热前溶液为浅 加热前溶液接近无 加入NaCl后,溶液 加热前溶液为黄黄色,加热后颜 色,加热后溶液颜 立即变为黄色,加热 色,加热后溶液颜
色变深 色无明显变化 后溶液颜色变深 色变深
注:加热为微热,忽略体积变化。
A.实验①中,Fe (SO ) 溶液显浅黄色原因是Fe3+水解产生了少量Fe(OH)
2 4 3 3
B.实验②中,酸化对Fe3+水解的影响程度大于温度的影响
C.实验③中,加热,可逆反应:
Fe3++4Cl-+2HO[FeCl (H O) ]-正向移动
2 4 2 2
D.实验④,可证明升高温度,颜色变深一定是因为Fe3+水解平衡正向移动
答案 D
解析 加热促进水解,铁离子水解生成氢氧化铁,则实验①中,Fe (SO ) 溶液显浅黄色原因
2 4 3
是Fe3+水解产生了少量Fe(OH) ,故A项正确;由Fe3++3HOFe(OH) +3H+可知,酸化
3 2 3
后加热溶液颜色无明显变化,氢离子抑制水解,则实验②中酸化对Fe3+水解的影响程度大
于温度的影响,故B项正确;加入NaCl后,溶液立即变为黄色,发生反应:Fe3++4Cl-+
2HO[FeCl (H O) ]-,[FeCl (H O) ]-为黄色,加热时平衡正向移动,溶液颜色变深,故C
2 4 2 2 4 2 2
项正确;实验④中存在Fe3++4Cl-+2HO[FeCl (H O) ]-,升高温度平衡正向移动,溶液
2 4 2 2
颜色变深,不能证明对Fe3+水解平衡的影响,故D项错误。
8.某同学在实验室探究NaHCO 的性质:常温下,配制0.10 mol·L-1 NaHCO 溶液,测得
3 3
其pH为9.7;取少量该溶液滴加CaCl 溶液至pH=7,滴加过程中产生白色沉淀,但无气体
2
放出。下列说法不正确的是( )
A.NaHCO 溶液呈碱性的原因是HCO的水解程度大于电离程度
3
B.加入CaCl 促进了HCO的水解
2
C.反应的离子方程式为
2HCO+Ca2+===CaCO ↓+HCO
3 2 3
D.反应后的溶液中存在:c(Na+)+2c(Ca2+)=c(HCO)+2c(CO)+c(Cl-)
答案 B
解析 NaHCO 既能电离又能水解,水解出OH-,电离出H+,NaHCO 溶液呈碱性的原因
3 3
是HCO的水解程度大于其电离程度,A项正确;溶液中存在HCOCO+H+,加入CaCl
2
消耗CO,促进HCO的电离,B项错误;HCO与Ca2+生成CaCO 和H+,H+结合HCO生成
3
HCO ,则反应的离子方程式为2HCO+Ca2+===CaCO ↓+HCO ,C项正确;溶液中存在
2 3 3 2 3
电荷守恒,c(Na+)+c(H+)+2c(Ca2+)=c(HCO)+2c(CO)+c(Cl-)+c(OH-),溶液的pH=7,
c(H+)=c(OH-),c(Na+)+2c(Ca2+)=c(HCO)+2c(CO)+c(Cl-),D项正确。
盐溶液蒸干灼烧时所得产物的几种判断类型
(1)盐溶液水解生成难挥发性酸时,蒸干后一般得原物质,如CuSO (aq)――→CuSO (s);
4 4盐 溶 液 水 解 生 成 易 挥 发 性 酸 时 , 蒸 干 灼 烧 后 一 般 得 对 应 的 氧 化 物 , 如
AlCl (aq)――→Al(OH) ――→Al O。
3 3 2 3
(2)酸根离子易水解的强碱盐,如NaCO 溶液等蒸干后可得到原物质。
2 3
(3)考虑盐受热时是否分解。
(4)还原性盐在蒸干时会被O 氧化,
2
如NaSO (aq)――→NaSO (s)。
2 3 2 4
(1)解答此类题的思维过程
①找出存在的平衡体系(即可逆反应或可逆过程)
②找出影响平衡的条件
③判断平衡移动的方向
④分析平衡移动的结果及移动结果与所解答问题的联系
(2)答题模板
……存在……平衡,……(条件)……(变化),使平衡向……(方向)移动,……(结论)。
1.为探究盐类水解是一个吸热过程,请用NaCO 溶液和其他必要试剂,设计一个简单的实
2 3
验方案:_______________________________________________________________________。
答案 取NaCO 溶液,滴加酚酞溶液呈红色,然后分成两份,加热其中一份,若红色变深,
2 3
则盐类水解吸热
2.常温下,0.1 mol·L-1 NaHCO 溶液的pH大于8,则溶液中c(H CO)>(填“>”“=”或
3 2 3
“<”)c(CO),原因是:HCOCO+H+,HCO+HOHCO +OH-,HCO的水解程度
2 2 3
大于电离程度(用离子方程式和必要的文字说明)。
3.(1)若在空气中加热MgCl ·6H O,生成的是Mg(OH)Cl或MgO,写出相应反应的化学方
2 2
程式:MgCl ·6H O=====Mg(OH)Cl+HCl↑+5HO↑,MgCl ·6H O=====MgO+2HCl↑+
2 2 2 2 2
5HO↑或Mg(OH)Cl=====MgO+HCl↑。
2
(2)在干燥的HCl气流中加热MgCl ·6H O时,能得到无水MgCl ,其原因是 在干燥的 HC l 气
2 2 2
流中,抑制了 MgC l 的水解,且带走 MgC l ·6H O 受热产生的水蒸气,故能得到无水
2 2 2
MgCl 。
2
4.(1)把AlCl 溶液蒸干灼烧,最后得到的主要固体是什么?为什么?如何操作溶质不变?
3
(用化学方程式表示并配以必要的文字说明)。
答案 在AlCl 溶液中存在着如下平衡:AlCl +3HOAl(OH) +3HCl,加热时水解平衡
3 3 2 3
右移,HCl浓度增大,蒸干时HCl挥发,使平衡进一步向右移动得到Al(OH) ,在灼烧时发
3
生反应2Al(OH) =====Al O +3HO,因此最后得到的固体是Al O ;在HCl气流中加热蒸发
3 2 3 2 2 3溶质不变。
(2)MgO可除去MgCl 溶液中的Fe3+,其原理是______________________________________。
2
答案 Fe3++HOFe(OH) +3H+,加入MgO,MgO和H+反应,使c(H+)减小,平衡右
2 3
移,生成Fe(OH) 沉淀除去
3
1.(2020·天津,7)常温下,下列有关电解质溶液的说法错误的是( )
A.相同浓度的HCOONa和NaF两溶液,前者的pH较大,则K(HCOOH)>K(HF)
a a
B.相同浓度的 CHCOOH 和 CHCOONa 两溶液等体积混合后 pH 约为 4.7,则溶液中
3 3
c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则K (FeS)>K (CuS)
sp sp
D.在1 mol·L-1 Na S溶液中,c(S2-)+c(HS-)+c(H S)=1 mol·L-1
2 2
答案 A
解析 HCOONa 和 NaF 均属于强碱弱酸盐,越弱越水解,HCOONa 的 pH 较大,所以
K(HCOOH)<K(HF),A项错误;两溶液等体积混合后pH<7,说明溶液显酸性,c(H+)>
a a
c(OH-),醋酸的电离程度大于醋酸根离子的水解程度,则 c(CHCOO-)>c(Na+)>c(H+)>
3
c(OH-),B 项正确;硫化亚铁溶于稀硫酸,而硫化铜不溶于稀硫酸,可得 K (FeS)>
sp
K (CuS),C项正确;在1 mol·L-1的NaS溶液中,根据物料守恒可得 c(S2-)+c(HS-)+
sp 2
c(H S)=1 mol·L-1,D项正确。
2
2.(2019·上海,20)常温下0.1 mol·L-1①CHCOOH、②NaOH、③CHCOONa,下列叙述
3 3
正确的是( )
A.①中c(CHCOOH)>c(CHCOO-)>c(H+)>c(OH-)
3 3
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合以后,溶液呈酸性,则c(Na+)>c(CHCOO-)>c(H+)
3
D.①②等体积混合后水的电离程度比①③等体积混合后水的电离程度小
答案 B
解析 A项,0.1 mol·L-1 CHCOOH发生部分电离产生CHCOO-和H+,水发生微弱电离
3 3
产生H+和OH-,故①中c(CHCOOH)>c(H+)>c(CHCOO-)>c(OH-),错误;B项,①②等
3 3
体积混合后恰好反应生成CHCOONa,且c(CHCOONa)=0.05 mol·L-1,由于①②混合后
3 3
c(CHCOONa)小于③,则混合液中CHCOO-的水解程度比③大,故混合液中c(CHCOO-)
3 3 3
小于③中c(CHCOO-),正确;C 项,①③等体积混合后为等物质的量的CHCOOH 和
3 3
CHCOONa的混合溶液,溶液显酸性说明CHCOOH的电离程度大于CHCOO-的水解程度,
3 3 3
则 c(CHCOO-)>c(Na+)>c(H+),错误;D 项,①②等体积混合后恰好生成 CHCOONa,
3 3
CHCOO-水解促进水的电离,①③等体积混合后,由于CHCOOH电离程度大于CHCOO-
3 3 3
的水解程度,水的电离被抑制,故①②等体积混合后水的电离程度比①③等体积混合后水的电离程度大,错误。
3.(2016·全国卷Ⅲ,13)下列有关电解质溶液的说法正确的是( )
A.向0.1 mol·L-1 CHCOOH溶液中加入少量水,溶液中减小
3
B.将CHCOONa溶液从20 ℃升温至30 ℃,溶液中增大
3
C.向盐酸中加入氨水至中性,溶液中>1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO,溶液中不变
3
答案 D
解析 A项,=,加水稀释,c(CHCOO―)减小,K 不变,所以比值增大,错误;B项,=,
3 a
温度升高水解常数K 增大,比值减小,错误;C项,向盐酸中加入氨水至中性,根据电荷
h
守恒:c(NH)+c(H+)=c(Cl―)+c(OH―),此时c(H+)=c(OH―),故c(NH)=c(Cl-),所以=
1,错误;D项,在饱和溶液中=,温度不变,溶度积K 不变,则溶液中不变,正确。
sp
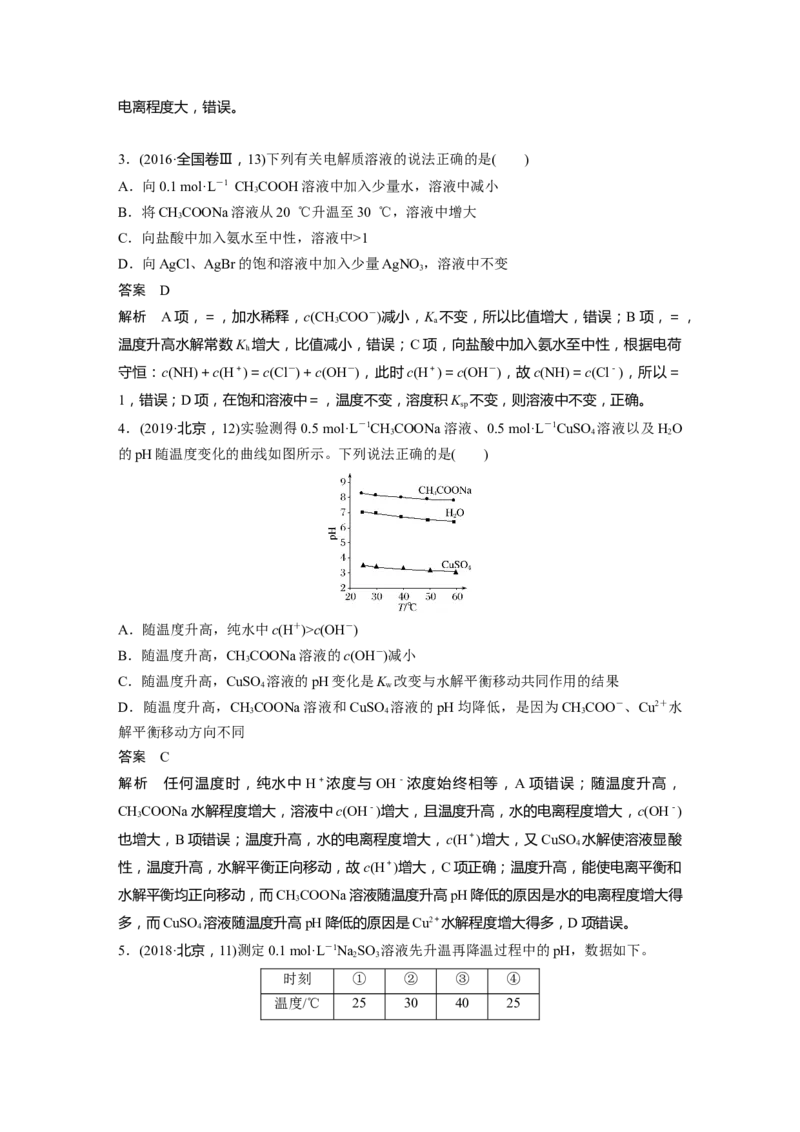
4.(2019·北京,12)实验测得0.5 mol·L-1CHCOONa溶液、0.5 mol·L-1CuSO 溶液以及HO
3 4 2
的pH随温度变化的曲线如图所示。下列说法正确的是( )
A.随温度升高,纯水中c(H+)>c(OH-)
B.随温度升高,CHCOONa溶液的c(OH-)减小
3
C.随温度升高,CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结果
4 w
D.随温度升高,CHCOONa溶液和CuSO 溶液的pH均降低,是因为CHCOO-、Cu2+水
3 4 3
解平衡移动方向不同
答案 C
解析 任何温度时,纯水中 H+浓度与 OH-浓度始终相等,A 项错误;随温度升高,
CHCOONa水解程度增大,溶液中c(OH-)增大,且温度升高,水的电离程度增大,c(OH-)
3
也增大,B项错误;温度升高,水的电离程度增大,c(H+)增大,又CuSO 水解使溶液显酸
4
性,温度升高,水解平衡正向移动,故 c(H+)增大,C项正确;温度升高,能使电离平衡和
水解平衡均正向移动,而CHCOONa溶液随温度升高pH降低的原因是水的电离程度增大得
3
多,而CuSO 溶液随温度升高pH降低的原因是Cu2+水解程度增大得多,D项错误。
4
5.(2018·北京,11)测定0.1 mol·L-1NaSO 溶液先升温再降温过程中的pH,数据如下。
2 3
时刻 ① ② ③ ④
温度/℃ 25 30 40 25pH 9.66 9.52 9.37 9.25
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 溶液做对比实验,④产生白色沉淀
2
多。
下列说法不正确的是( )
A.NaSO 溶液中存在水解平衡:SO+HOHSO+OH-
2 3 2
B.④的pH与①不同,是由SO浓度减小造成的
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D.①与④的K 值相等
w
答案 C
解析 ①→③的过程中,pH变小,说明SO水解产生的c(OH-)减小;升高温度,SO的水解
平衡正向移动,溶液中SO水解产生的c(OH-)增大,pH应增大,而实际上溶液的pH减小,
其主要原因是实验过程中部分SO被空气中的O 氧化生成SO,溶液中c(SO)减小,水解平
2
衡逆向移动,则溶液中c(OH-)减小,pH减小;①→③的过程中,温度升高,SO的水解平
衡正向移动,而c(SO)减小,水解平衡逆向移动,二者对水解平衡移动方向的影响不一致,
C错误;NaSO 是强碱弱酸盐,在水溶液中发生水解,存在水解平衡:SO+HOHSO+
2 3 2
OH-,A对;实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 溶液做对比实验,④
2
产生白色沉淀多,说明④中的SO数目大于①中的,④中的SO数目小于①中的,所以④中
OH-数目小于①中的,pH不同,B对;K 只与温度有关,D对。
w
1.(2019·怀化高三期末)常温下,某NH Cl溶液的pH=4,下列说法中正确的是( )
4
①溶液中c(H+)>c(OH-)
②由水电离产生的c(H+)约为10-10 mol·L-1
③溶液中离子浓度关系为c(Cl-)>c(NH)>c(H+)>c(OH-)
④在纯水中加入该NH Cl溶液,水的电离被抑制
4
A.①② B.①③ C.①④ D.①②③④
答案 B
2.室温下,将0.05 mol Na CO 固体溶于水配成100 mL溶液,向溶液中加入下列物质,有
2 3
关结论正确的是( )
选项 加入的物质 结论
A 50 mL 1 mol·L-1 HSO 反应结束后,c(Na+)=c(SO)
2 4
B 0.05 mol CaO 溶液中增大
C 50 mL H O 由水电离出的c(H+)·c(OH-)不变
2
D 0.1 mol NaHSO 固体 反应完全后,溶液pH减小,c(Na+)不变
4答案 B
解析 NaCO 溶液中存在水解平衡CO+HOHCO+OH-,所以溶液呈碱性。A项,向
2 3 2
溶液中加入50 mL 1 mol·L-1HSO ,NaCO 与HSO 恰好反应生成0.05 mol·L-1NaSO ,根
2 4 2 3 2 4 2 4
据物料守恒可得c(Na+)=2c(SO),错误;B项,向NaCO 溶液中加入0.05 mol CaO后,发
2 3
生反应CaO+HO===Ca(OH) ,生成0.05 mol的Ca(OH) ,Ca(OH) 恰好与NaCO 反应:
2 2 2 2 2 3
Ca(OH) +NaCO===CaCO ↓+2NaOH,则c(CO)减小,c(OH-)增大,c(HCO)减小,所以
2 2 3 3
增大,正确;C项,加入50 mL H O,CO的水解平衡正向移动,但c(OH-)减小,溶液中的
2
OH-全部来源于水的电离,由于水电离出的 H+、OH-浓度相等,故由水电离出的c(H
+)·c(OH-)减小,错误;D项,加入0.1 mol NaHSO 固体与0.05 mol Na CO 恰好反应生成
4 2 3
0.1 mol Na SO ,溶液呈中性,故溶液pH减小,加入NaHSO ,引入Na+,所以c(Na+)增大,
2 4 4
错误
3.下列溶液中,操作和现象对应正确的是( )
选项 溶液 操作 现象
A 滴有酚酞的明矾溶液 加热 颜色变深
B 滴有酚酞的氨水 加入少量NH Cl固体 颜色变浅
4
滴有酚酞的CHCOONa 加入少量的CHCOONa
3 3
C 颜色变浅
溶液 固体
D 氯化铁溶液 加热 颜色变浅
答案 B
解析 明矾溶液中Al3+水解使溶液呈酸性,加热,Al3+的水解程度增大,溶液的酸性增强,
无颜色变化,A项错误;加入NH Cl固体,氨水的电离程度减小,碱性减弱,溶液颜色变浅,
4
B项正确;加入少量CHCOONa固体会使CHCOO-+HOCHCOOH+OH-平衡向右移
3 3 2 3
动,c(OH-)增大,颜色变深,C项错误;加热氯化铁溶液时促进 FeCl 水解为红褐色的
3
Fe(OH) ,颜色加深,D项错误。
3
4.常温下,HF的电离常数K=6.61×10-4,NH ·H O的电离常数K =1.78×10-5。下列说
a 3 2 b
法正确的是( )
A.NH F溶液中lg >0
4
B.NH F溶液中水的电离程度小于纯水的电离程度
4
C.NH F溶液中F-的水解平衡常数K (F-)≈1.51×10-11
4 h
D.NH F与NH Cl的混合溶液中有下列关系:c(NH)>c(F-)+c(Cl-)
4 4
答案 C
解析 HF的电离平衡常数大于NH ·H O的电离平衡常数,所以氟离子的水解程度小于铵根
3 2
离子水解程度,溶液显酸性,氢氧根离子与氢离子的比值的对数应小于0,故A项错误;铵根离子和氟离子的水解促进水的电离,所以NH F溶液中水的电离程度大于纯水的电离程度,
4
故B项错误;NH F溶液中F-的水解平衡常数=≈1.51×10-11,故C项正确;NH F与NH Cl
4 4 4
的混合溶液中c(NH)+c(H+)=c(F-)+c(Cl-)+c(OH-),又溶液显酸性,c(H+)>c(OH-),所
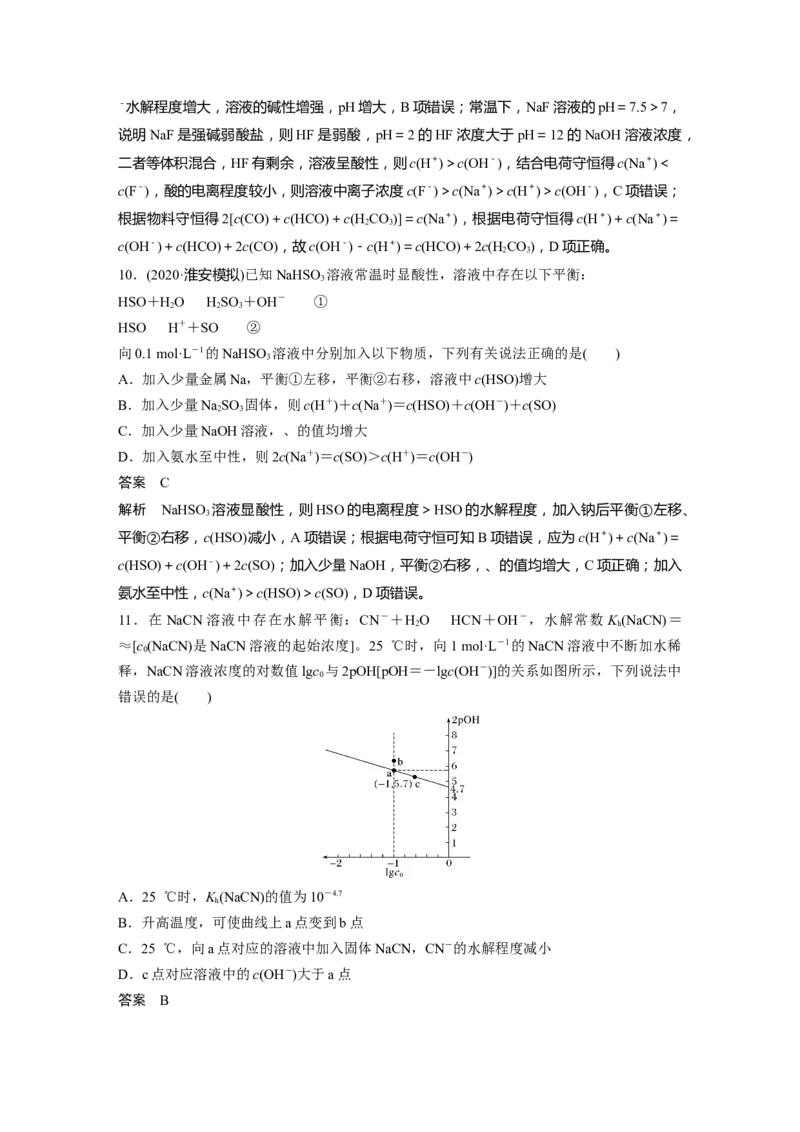
以c(NH)K ,等物质的量浓度的NaHA、NaA等体积混合,HA-的电离程度大
a a h 2
于A2-的水解程度,所得c(HA-)3,故D错误。
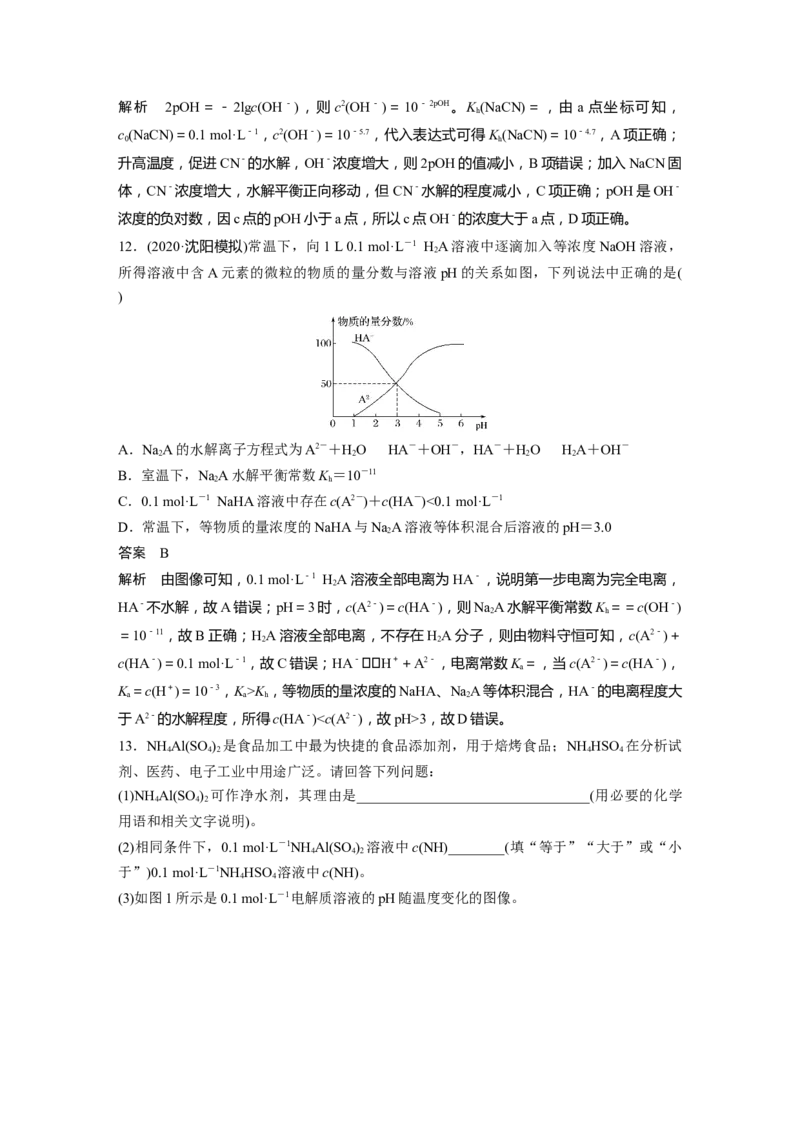
13.NH Al(SO ) 是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH HSO 在分析试
4 4 2 4 4
剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH Al(SO ) 可作净水剂,其理由是_________________________________(用必要的化学
4 4 2
用语和相关文字说明)。
(2)相同条件下,0.1 mol·L-1NH Al(SO ) 溶液中c(NH)________(填“等于”“大于”或“小
4 4 2
于”)0.1 mol·L-1NH HSO 溶液中c(NH)。
4 4
(3)如图1所示是0.1 mol·L-1电解质溶液的pH随温度变化的图像。①其中符合0.1 mol·L-1 NH Al(SO ) 溶液的pH随温度变化的曲线是________(填字母),导
4 4 2
致pH随温度变化的原因是________________________________________________________。
②20 ℃时,0.1 mol·L-1 NH Al(SO ) 溶液中2c(SO)-c(NH)-3c(Al3+)=________。
4 4 2
(4)室温时,向100 mL 0.1 mol·L-1NH HSO 溶液中滴加0.1 mol·L-1NaOH溶液,所得溶液pH
4 4
与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度
最大的是________点;在b点,溶液中各离子浓度由大到小的排列顺序是_______________。
答案 (1)Al3+水解生成的Al(OH) 胶体具有吸附性,即Al3++3HOAl(OH) (胶体)+3H
3 2 3
+,Al(OH) 胶体吸附悬浮颗粒使其沉降从而净化水
3
(2)小于
(3)①Ⅰ NH Al(SO ) 水解,溶液呈酸性,升高温度使其水解程度增大,pH减小
4 4 2
②10-3 mol·L-1
(4)a c(Na+)>c(SO)>c(NH)>c(OH-)=c(H+)
解析 (2)NH Al(SO ) 与NH HSO 中的NH均发生水解,NH Al(SO ) 中Al3+水解呈酸性抑
4 4 2 4 4 4 4 2
制NH水解,HSO电离出H+同样抑制NH水解,但HSO电离生成的H+浓度比Al3+水解生
成的H+浓度大,所以NH HSO 中NH水解程度比NH Al(SO ) 中的小。(3)①NH Al(SO ) 水
4 4 4 4 2 4 4 2
解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为Ⅰ。②根据电荷守恒,
可以求出2c(SO)-c(NH)-3c(Al3+)=c(H+)-c(OH-)≈10-3 mol·L-1 [c(OH-)太小,可忽略]。
(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完电离出的H+,溶液中只有
(NH )SO 与NaSO ;b、c、d三点溶液均含有NH ·H O,(NH )SO 可以促进水的电离,而
4 2 4 2 4 3 2 4 2 4
NH ·H O抑制水的电离,a点水的电离程度最大,b点溶液呈中性,即溶液含有(NH )SO 、
3 2 4 2 4
NaSO 、NH ·H O三种成分,a点时c(Na+)=c(SO),b点时c(Na+)>c(SO),又根据电荷守
2 4 3 2
恒c(Na+)+c(NH)+c(H+)=c(OH-)+2c(SO),且c(H+)=c(OH-),可以得出c(SO)>c(NH),
故c(Na+)>c(SO)>c(NH)>c(OH-)=c(H+)。
14.Ⅰ.(1)KAl(SO ) 溶液蒸干得到的固体物质是__________,原因是____________________。
4 2
(2)FeCl 溶液蒸干灼烧得到的固体物质是__________,原因是________________________。
2
(3)将 0.5 mol·L-1的 NaClO 溶液加热蒸干灼烧最后所得的固体是________,原因是
_____________________________________________________________________________。
答案 (1)KAl(SO )·12H O 尽管Al3+水解,但由于HSO 为难挥发性酸,最后仍然得到明
4 2 2 2 4
矾。注意温度过高,会脱去结晶水(2)Fe O Fe2+水解生成Fe(OH) 和HCl,在加热蒸干过程中HCl挥发,Fe(OH) 逐渐被氧化
2 3 2 2
生成Fe(OH) ,Fe(OH) 灼烧分解生成Fe O
3 3 2 3
(3)NaCl NaClO 水解的化学方程式为 NaClO+HONaOH+HClO,2HClO=====2HCl+
2
O↑,HCl+NaOH===NaCl+HO,最终得到NaCl
2 2
Ⅱ.[2015·天津理综,10(3)(4)]FeCl 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的
3
絮凝剂,处理污水比FeCl 高效,且腐蚀性小。请回答下列问题:
3
FeCl 在溶液中分三步水解:
3
Fe3++HOFe(OH)2++H+ K
2 1
Fe(OH)2++HOFe(OH)+H+ K
2 2
Fe(OH)+HOFe(OH) +H+ K
2 3 3
以上水解反应的平衡常数K 、K 、K 由大到小的顺序是________________。通过控制条件,
1 2 3
以上水解产物聚合,生成聚合氯化铁,离子方程式为xFe3++yHOFe(OH)+yH+。
2 x
欲使平衡正向移动可采用的方法是________(填字母)。
a.降温 b.加水稀释
c.加入NH Cl d.加入NaHCO
4 3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是________________。
答案 K >K >K bd 调节溶液的pH
1 2 3
解析 Fe3+分三步水解,水解程度越来越小,所以对应的平衡常数也越来越小,有
K >K >K ;生成聚合氯化铁的离子方程式为xFe3++yHOFe(OH)+yH+,由于水解是吸
1 2 3 2 x
热的,降温则水解平衡逆向移动;加水稀释,水解平衡正向移动;NH Cl溶液呈酸性,加入
4
NH Cl,H+浓度增大,平衡逆向移动;加入NaHCO ,消耗H+,H+浓度降低,平衡正向移
4 3
动,故可采用的方法是b、d。从反应的离子方程式可知,氢离子的浓度影响聚合氯化铁的
生成,所以关键条件是调节溶液的pH。