文档内容
2023届高考化学一轮专题强化练习题:化学反应原理综合题
1.(2022·重庆八中高三阶段练习)SO 是造成空气污染的主要原因,一定条件下能变废为宝,请回答下
2
列问题:
(1)实验室可采用NaSO 溶液吸收SO ,该吸收反应的化学方程式是_______,常温下,NaSO 溶液的
2 3 2 2 3
pH_______7,原因是(用离子方程式表示)_______。
(2)利用雅化氧化反应将SO 转化为SO 是工业上生产硫酸的关键步骤。
2 3
已知:SO (g)+ O(g) SO (g)ΔH=-98kJ·mol-1,某温度下该反应的平衡常数K=
2 2 3
①该温度下,向一体积为2L的恒容密闭容器中充入2.0molSO 和1.0molO,反应一段时间后容器压强为
2 2
反应前的80%,此时SO 的转化率为_______。
2
②在①中的反应达到平衡后,改变下列条件,能使SO (g)平衡浓度比原来增大的是_______(填字母)。
2
A.保持温度和容器体积不变,充入1.0molO
2
B.降低温度
C.保持温度和容器体积不变,充入1.0molSO
3
D.增大容器体积
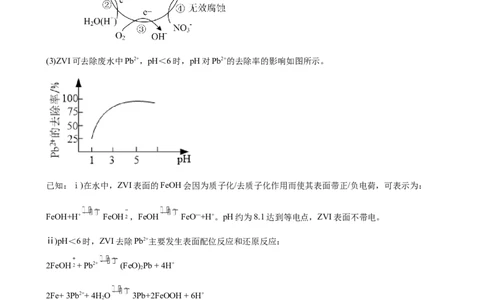
(3)若以如图所示装置,用电化学原理生产硫酸,通入O 电极的电极反应式为_______。
2
(4)为稳定持续生产,硫酸溶液的质量分数应维持不变,则通入SO 和水的质量比为______。
2
2.(2022·江苏泰州·模拟预测)纳米零价铁(ZVI)因其高比表面积、优异的吸附性、较强的还原性和反应
活性等优点被广泛应用于污染物的去除。
(1)ZVI可通过FeCl ·4H O和NaBH 溶液反应制得,同时生成H、B(OH) ,制备过程中需要不断通入高
2 2 4 2
纯氮气,其目的是_______。(2)ZVI电化学腐蚀处理三氯乙烯进行水体修复,H+、O、 等物种的存在会影响效果,水体修复的过
2
程如图所示。有效腐蚀过程中,生成1mol乙烯所转移的电子物质的量为_______mol,过程④对应的电极
反应式为_______。
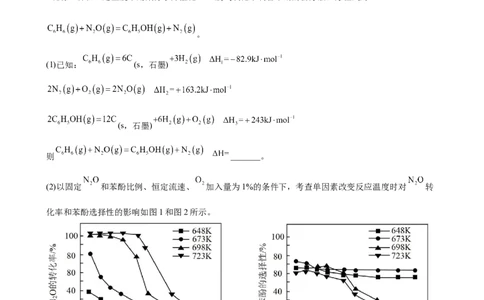
(3)ZVI可去除废水中Pb2+,pH<6时,pH对Pb2+的去除率的影响如图所示。
已知:ⅰ)在水中,ZVI表面的FeOH会因为质子化/去质子化作用而使其表面带正/负电荷,可表示为:
FeOH+H+ FeOH ,FeOH FeO—+H+。pH约为8.1达到等电点,ZVI表面不带电。
ⅱ)pH<6时,ZVI去除Pb2+主要发生表面配位反应和还原反应:
2FeOH + Pb2+ (FeO) Pb + 4H+
2
2Fe+ 3Pb2++ 4H O 3Pb+2FeOOH + 6H+
2
①pH<6时,铁氧化物颗粒不易吸附Pb2+的原因是_______。
②pH<6时,随着pH增大,Pb2+的去除率会增大至接近100%的原因是_______。
(4)催化剂协同ZVI能将水体中的硝酸盐( )转化为N,其催化还原反应的过程如图所示。为有效降低
2
水体中氮元素的含量,宜调整水体pH为4.2,当pH<4.2时,随pH减小,N 生成率逐渐降低的原因是
2
_______。3.(2022·陕西省丹凤中学高三阶段练习)Ⅰ.微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,
其电极分别是 和Zn,电解质溶液为KOH溶液,电极反应式为: ,
。
(1)判断下列叙述中正确的是_______。
A.在使用过程中,电解质KOH不断被消耗
B.使用过程中,电子由 极经外电路流向Zn极
C.Zn是负极, 是正极
D.Zn电极发生还原反应,AgO电极发生氧化反应
(2)写出电池的总反应式:_______。
(3)使用时,负极区的 _______(填“增大”“减小”或“不变”,下同),正极区的 _______,
电解质溶液的 _______。
Ⅱ.工业合成氨反应: 是一个放热的可逆反应,反应条件是高温、高压,并且
需要合适的催化剂。已知形成1molH—H键、1molN—H键、1molN≡N键放出的能量分别为436kJ、
391kJ,946kJ。则:
(4)若1mol 完全反应生成 可_______(填“吸收”或“放出”)热量_______kJ。(5)如果将1mol 和3mol 混合,使其充分反应,放出的热量总小于上述数值,其原因是_______。
(6)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成10mol ,则用
表示的化学反应速率为_______mol/(L·min)。
4.(2022·江苏·南京外国语学校高三阶段练习)苯酚( )是一种广泛使用的化工产品,但若在水体
中存在超标又会导致严重的污染。
I.现有一种在一定温度下用某分子筛催化 废气氧化苯制备苯酚的新方法,方程式为:
。
(1)已知: (s,石墨)
(s,石墨)
则 _______。
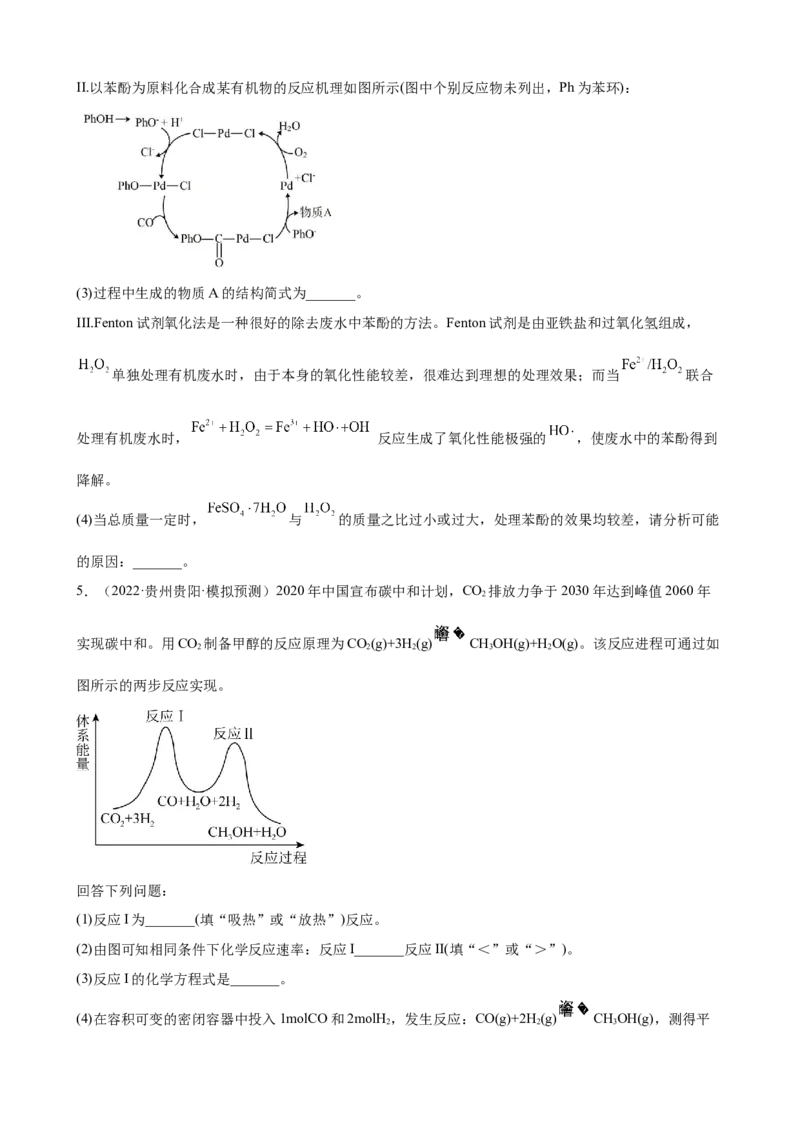
(2)以固定 和苯酚比例、恒定流速、 加入量为1%的条件下,考查单因素改变反应温度时对 转
化率和苯酚选择性的影响如图1和图2所示。
①由图1可见,在723K进行反应时, 的初始转化率很高,随着反应时间的延续, 转化率迅速降
低,究其原因可能是_______。
②由图2可见,在648K和673K反应时,苯酚的选择性基本保持恒定,而在698K和723K时,苯酚选择
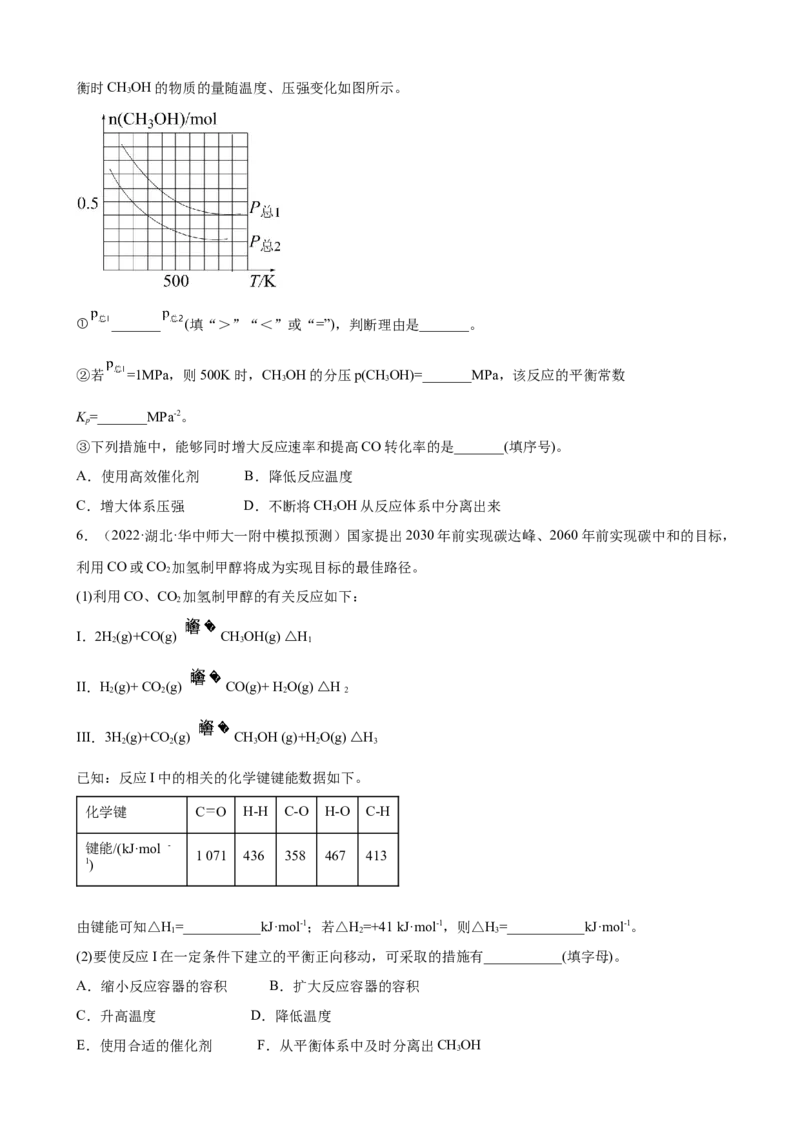
性随着反应进行迅速下降,高温时苯酚选择性下降的原因可能是:_______。II.以苯酚为原料化合成某有机物的反应机理如图所示(图中个别反应物未列出,Ph为苯环):
(3)过程中生成的物质A的结构简式为_______。
III.Fenton试剂氧化法是一种很好的除去废水中苯酚的方法。Fenton试剂是由亚铁盐和过氧化氢组成,
单独处理有机废水时,由于本身的氧化性能较差,很难达到理想的处理效果;而当 联合
处理有机废水时, 反应生成了氧化性能极强的 ,使废水中的苯酚得到
降解。
(4)当总质量一定时, 与 的质量之比过小或过大,处理苯酚的效果均较差,请分析可能
的原因:_______。
5.(2022·贵州贵阳·模拟预测)2020年中国宣布碳中和计划,CO 排放力争于2030年达到峰值2060年
2
实现碳中和。用CO 制备甲醇的反应原理为CO(g)+3H(g) CHOH(g)+H O(g)。该反应进程可通过如
2 2 2 3 2
图所示的两步反应实现。
回答下列问题:
(1)反应I为_______(填“吸热”或“放热”)反应。
(2)由图可知相同条件下化学反应速率:反应I_______反应II(填“<”或“>”)。
(3)反应I的化学方程式是_______。
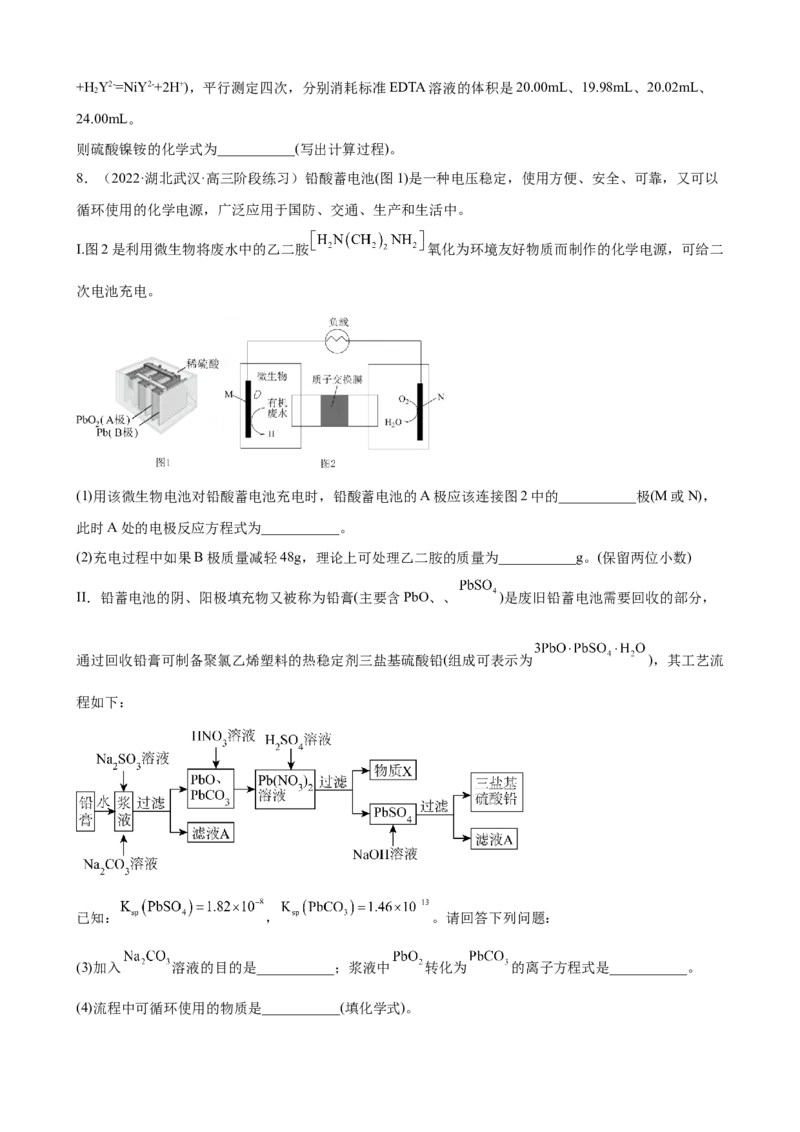
(4)在容积可变的密闭容器中投入1molCO和2molH ,发生反应:CO(g)+2H(g) CHOH(g),测得平
2 2 3衡时CHOH的物质的量随温度、压强变化如图所示。
3
① _______ (填“>”“<”或“=”),判断理由是_______。
②若 =1MPa,则500K时,CHOH的分压p(CHOH)=_______MPa,该反应的平衡常数
3 3
K =_______MPa-2。
p
③下列措施中,能够同时增大反应速率和提高CO转化率的是_______(填序号)。
A.使用高效催化剂 B.降低反应温度
C.增大体系压强 D.不断将CHOH从反应体系中分离出来
3
6.(2022·湖北·华中师大一附中模拟预测)国家提出2030年前实现碳达峰、2060年前实现碳中和的目标,
利用CO或CO 加氢制甲醇将成为实现目标的最佳路径。
2
(1)利用CO、CO 加氢制甲醇的有关反应如下:
2
I.2H(g)+CO(g) CHOH(g) △H
2 3 1
II.H(g)+ CO (g) CO(g)+ H O(g) △H
2 2 2 2
III.3H(g)+CO (g) CHOH (g)+HO(g) △H
2 2 3 2 3
已知:反应I中的相关的化学键键能数据如下。
化学键 C O H-H C-O H-O C-H
键能/(kJ·mol -
1 071 436 358 467 413
1)
由键能可知△H=___________kJ·mol-1;若△H=+41 kJ·mol-1,则△H=___________kJ·mol-1。
1 2 3
(2)要使反应I在一定条件下建立的平衡正向移动,可采取的措施有___________(填字母)。
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.降低温度
E.使用合适的催化剂 F.从平衡体系中及时分离出CHOH
3(3)在不同温度、压强和相同催化剂条件下,发生反应III,初始时CO、H 分别为1.0 mol、3.0mol,测得
2 2
H 的平衡转化率[α(H )]随温度和压强的变化如图所示。
2 2
①压强:p、p、p 的关系为___________。
1 2 3
②250 °C、p 条件下,平衡时α(H )___________α(CO )(填“>”“=”或“<”);此时反应的化学平衡常
1 2 2
数K=___________(分压=总压×物质的量分数)。
p
③若在A点平衡状态下,再充入1 mol CO 和1 mol H O(g), 则速率v (CO)___________(填“>”
2 2 正 2
“<”或“=”)v (CO)。
逆 2
7.(2022·江苏省平潮高级中学模拟预测)镀镍废水是重金属污染源之一,常见处理含镍废水的一种离子
交换和沉淀法工艺如下:
已知该交换树脂为阳离子型树脂HR,HR R-+H+;NiR (aq) Ni2+(aq)+2R-(aq)。
2
(1)Ni2+的核外电子排布式为___________ 。
(2)已知在pH=2时,离子交换过程Ni2+去除率很低,其原因为___________。
(3)“脱络”(指镍元素由络合物NiR 转化成游离的Ni2+)过程中,R-与中间产物·OH(羟基自由基)反应生成难
2
以与Ni2+络合的·R(有机物自由基),但·OH也能与HO 发生反应。反应的方程式如下:
2 2
Ⅰ.Fe2++H O=Fe3++OH-+·OH
2 2
Ⅱ.R-+·OH=OH-+·R
平衡移动的角度解释加入FeSO 和HO 能够实现“脱络”的原因是___________。
4 2 2
(4)NiC O 隔绝空气高温煅烧可制得Ni O,NiC O 受热分解的化学方程式为___________。
2 4 2 3 2 4
(5)硫酸镍铵(NH )Ni (SO ) ·nH O可用于电镀等领域,为测定其组成,进行如下实验:
4 x y 4 m 2
①称取4.670样品,配成250mL溶液A。
②取25.00mL溶液A,加足量浓NaOH溶液并加热,生成NH 44.80mL (标准状况)。
3
③另取25.00mL溶液A,用0.05000mol/L的EDTA(Na HY)标准溶液滴定其中的Ni2+(离子方程式为Ni2+
2 2+H Y2-=NiY2-+2H+),平行测定四次,分别消耗标准EDTA溶液的体积是20.00mL、19.98mL、20.02mL、
2
24.00mL。
则硫酸镍铵的化学式为___________(写出计算过程)。
8.(2022·湖北武汉·高三阶段练习)铅酸蓄电池(图1)是一种电压稳定,使用方便、安全、可靠,又可以
循环使用的化学电源,广泛应用于国防、交通、生产和生活中。
I.图2是利用微生物将废水中的乙二胺 氧化为环境友好物质而制作的化学电源,可给二
次电池充电。
(1)用该微生物电池对铅酸蓄电池充电时,铅酸蓄电池的A极应该连接图2中的___________极(M或N),
此时A处的电极反应方程式为___________。
(2)充电过程中如果B极质量减轻48g,理论上可处理乙二胺的质量为___________g。(保留两位小数)
II.铅蓄电池的阴、阳极填充物又被称为铅膏(主要含PbO、、 )是废旧铅蓄电池需要回收的部分,
通过回收铅膏可制备聚氯乙烯塑料的热稳定剂三盐基硫酸铅(组成可表示为 ),其工艺流
程如下:
已知: , 。请回答下列问题:
(3)加入 溶液的目的是___________;浆液中 转化为 的离子方程式是___________。
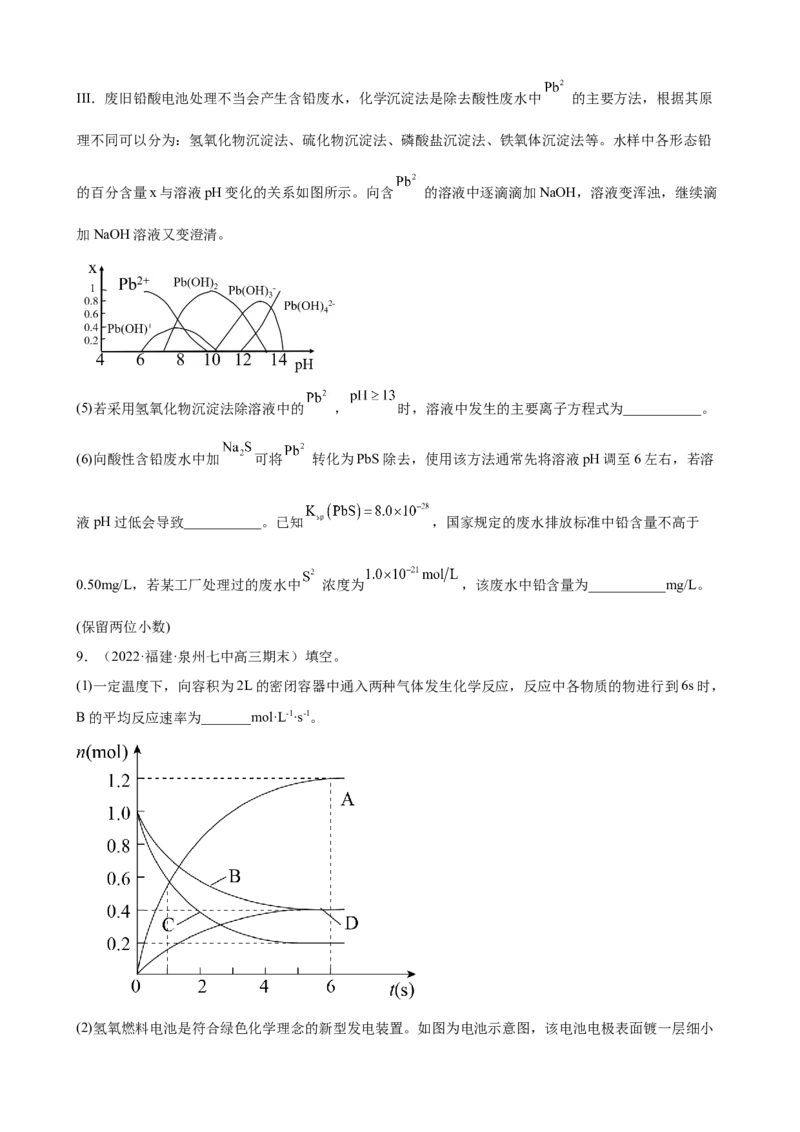
(4)流程中可循环使用的物质是___________(填化学式)。III.废旧铅酸电池处理不当会产生含铅废水,化学沉淀法是除去酸性废水中 的主要方法,根据其原
理不同可以分为:氢氧化物沉淀法、硫化物沉淀法、磷酸盐沉淀法、铁氧体沉淀法等。水样中各形态铅
的百分含量x与溶液pH变化的关系如图所示。向含 的溶液中逐滴滴加NaOH,溶液变浑浊,继续滴
加NaOH溶液又变澄清。
(5)若采用氢氧化物沉淀法除溶液中的 , 时,溶液中发生的主要离子方程式为___________。
(6)向酸性含铅废水中加 可将 转化为PbS除去,使用该方法通常先将溶液pH调至6左右,若溶
液pH过低会导致___________。已知 ,国家规定的废水排放标准中铅含量不高于
0.50mg/L,若某工厂处理过的废水中 浓度为 ,该废水中铅含量为___________mg/L。
(保留两位小数)
9.(2022·福建·泉州七中高三期末)填空。
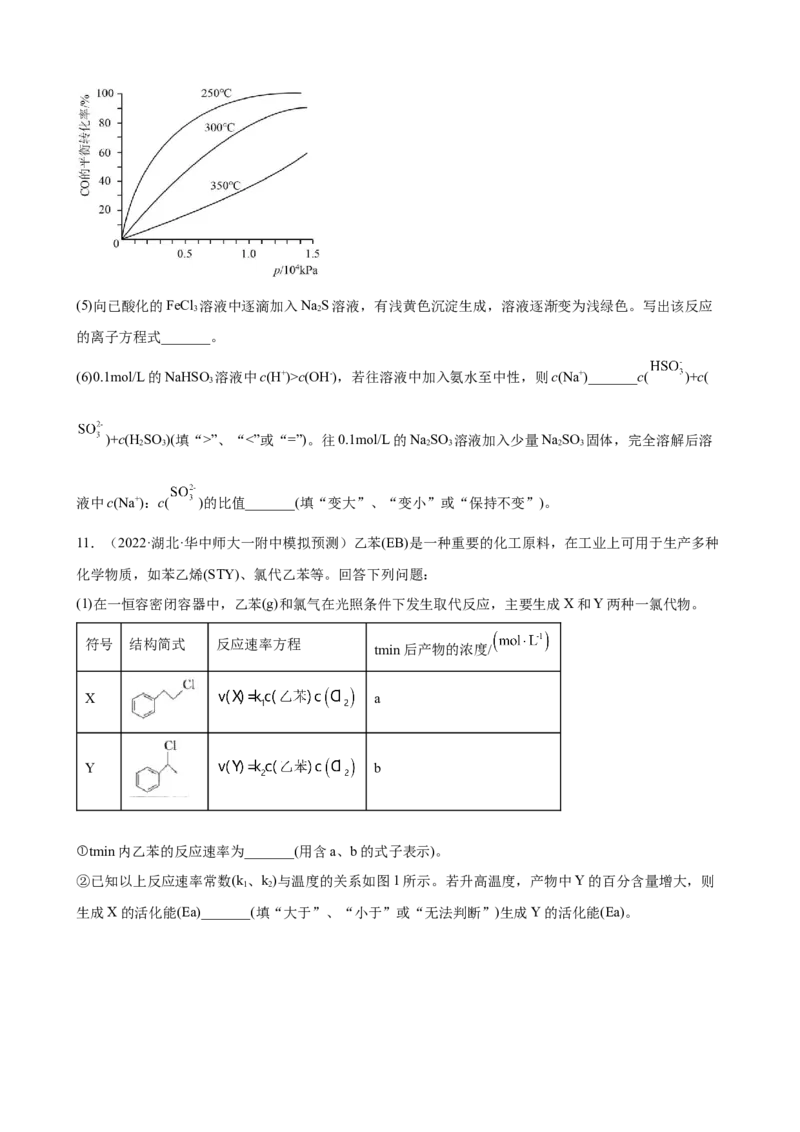
(1)一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物进行到6s时,
B的平均反应速率为_______mol·L-1·s-1。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。该装置负极反应方程式为_______。
(3)写出乙烷和氯气反应生成一氯乙烷的化学方程式:_______,该反应类型为_______;写出乙烯和溴的
四氯化碳溶液反应的化学方程式:_______,该反应类型为_______。
10.(2022·上海市洋泾中学高三阶段练习)研究NO 、SO 、CO等大气污染气体的处理具有重要意义。
2 2
I.利用反应:6NO +8NH 7N+12H O处理NO
2 3 2 2 2。
II.一定条件下NO
2
与SO
2
可发生反应,方程式:NO
2
(g)+SO
2
(g)⇌SO
3
(g)+NO(g) -Q。
III.CO可用于合成甲醇,反应方程式为:CO(g)+2H(g) CHOH(g)。
2 3
(1)对于I中的反应,120℃时,该反应在一容积为2L的⇌容器内反应,20min时达到平衡,10min时电子转
移了1.2mol,则0~10min内,平均反应速率v(NO )=_______。
2
(2)对于II中的反应,将NO 与SO 以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的
2 2
是_______(选填编号)。
a.体系压强保持不变 b.混合气体颜色保持不变
c.NO 和SO 的体积比保持不变 d.混合气体的平均相对分子质量保持不变
2 3
(3)如果II中反应的平衡常数K值变大,该反应_______(选填编号)。
a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
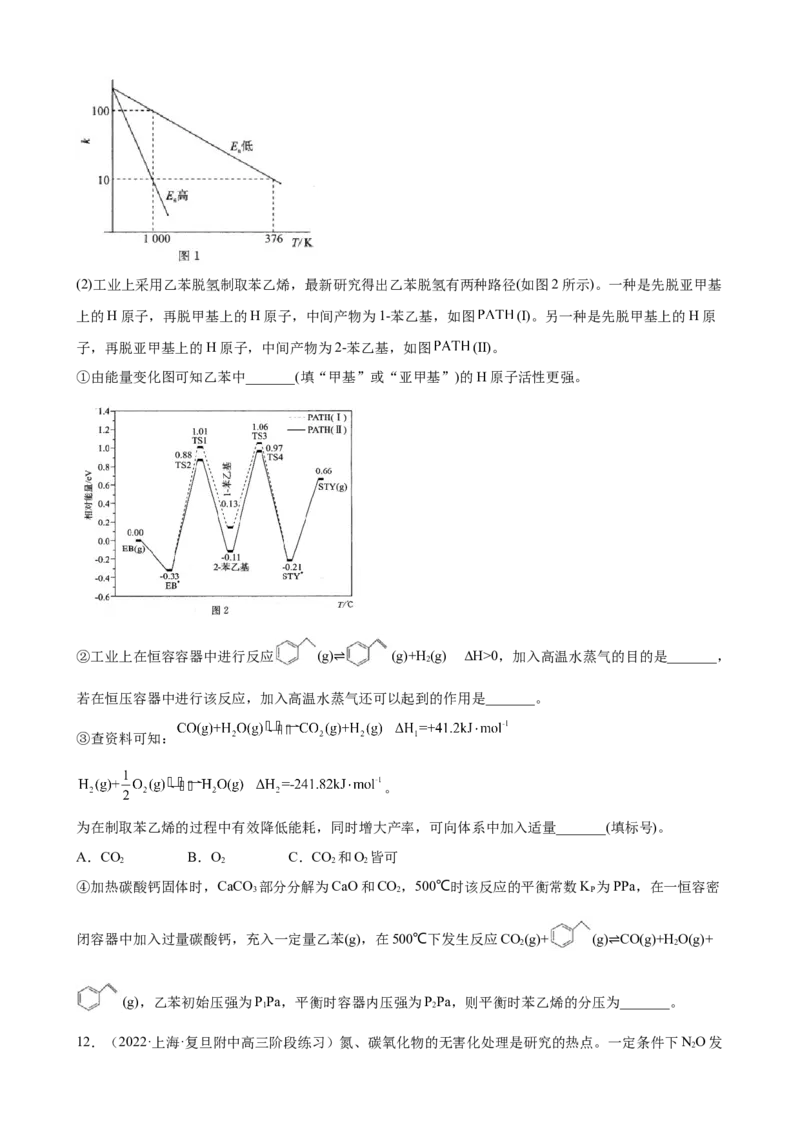
(4)对于III中的反应,CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应是_______反应
(填“放热”或“吸热“)。实际生产条件控制在250℃、1.3×104KPa左右,简述选择此压强的理由:
_______。(5)向已酸化的FeCl 溶液中逐滴加入NaS溶液,有浅黄色沉淀生成,溶液逐渐变为浅绿色。写出该反应
3 2
的离子方程式_______。
(6)0.1mol/L的NaHSO 溶液中c(H+)>c(OH-),若往溶液中加入氨水至中性,则c(Na+)_______c( )+c(
3
)+c(H SO )(填“>”、“<”或“=”)。往0.1mol/L的NaSO 溶液加入少量NaSO 固体,完全溶解后溶
2 3 2 3 2 3
液中c(Na+):c( )的比值_______(填“变大”、“变小”或“保持不变”)。
11.(2022·湖北·华中师大一附中模拟预测)乙苯(EB)是一种重要的化工原料,在工业上可用于生产多种
化学物质,如苯乙烯(STY)、氯代乙苯等。回答下列问题:
(1)在一恒容密闭容器中,乙苯(g)和氯气在光照条件下发生取代反应,主要生成X和Y两种一氯代物。
符号 结构简式 反应速率方程
tmin后产物的浓度/
X a
Y b
①tmin内乙苯的反应速率为_______(用含a、b的式子表示)。
②已知以上反应速率常数(k、k)与温度的关系如图1所示。若升高温度,产物中Y的百分含量增大,则
1 2
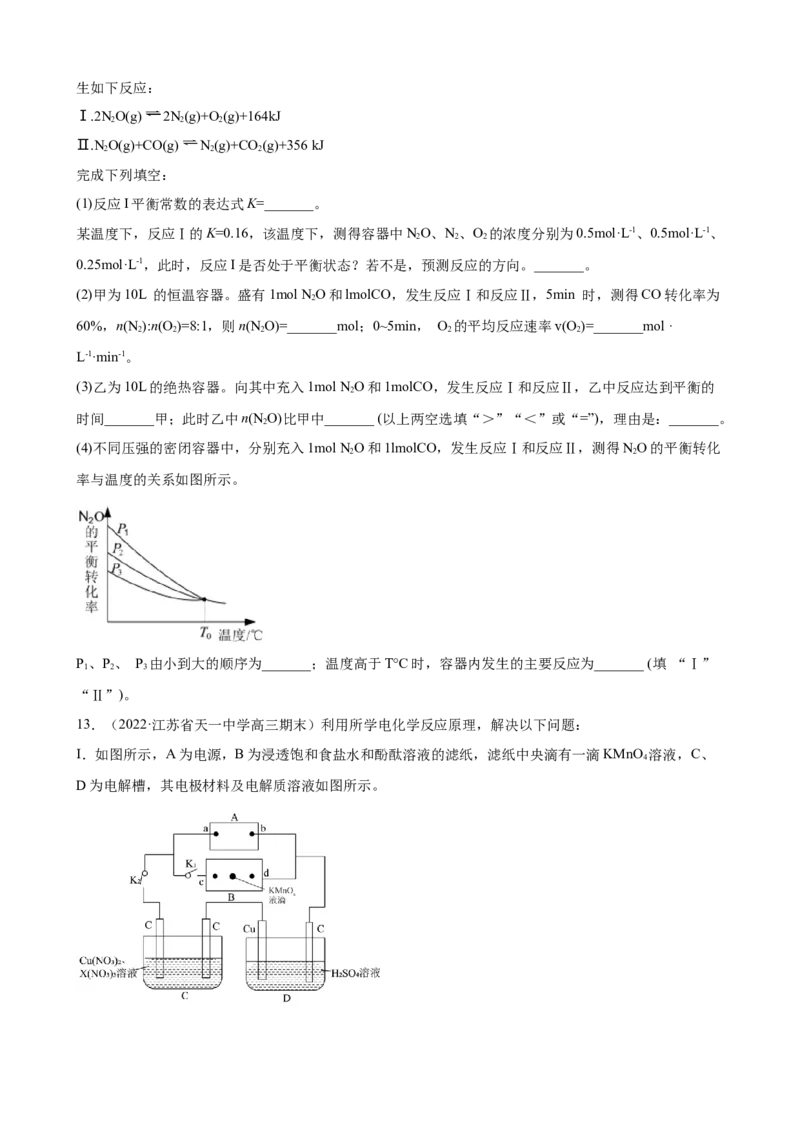
生成X的活化能(Ea)_______(填“大于”、“小于”或“无法判断”)生成Y的活化能(Ea)。(2)工业上采用乙苯脱氢制取苯乙烯,最新研究得出乙苯脱氢有两种路径(如图2所示)。一种是先脱亚甲基
上的H原子,再脱甲基上的H原子,中间产物为1-苯乙基,如图 (I)。另一种是先脱甲基上的H原
子,再脱亚甲基上的H原子,中间产物为2-苯乙基,如图 (II)。
①由能量变化图可知乙苯中_______(填“甲基”或“亚甲基”)的H原子活性更强。
②工业上在恒容容器中进行反应 (g) (g)+H(g) ∆H>0,加入高温水蒸气的目的是_______,
2
⇌
若在恒压容器中进行该反应,加入高温水蒸气还可以起到的作用是_______。
③查资料可知:
。
为在制取苯乙烯的过程中有效降低能耗,同时增大产率,可向体系中加入适量_______(填标号)。
A.CO B.O C.CO 和O 皆可
2 2 2 2
④加热碳酸钙固体时,CaCO 部分分解为CaO和CO,500℃时该反应的平衡常数K 为PPa,在一恒容密
3 2 P
闭容器中加入过量碳酸钙,充入一定量乙苯(g),在500℃下发生反应CO(g)+ (g) CO(g)+HO(g)+
2 2
⇌
(g),乙苯初始压强为PPa,平衡时容器内压强为PPa,则平衡时苯乙烯的分压为_______。
1 2
12.(2022·上海·复旦附中高三阶段练习)氮、碳氧化物的无害化处理是研究的热点。一定条件下NO发
2生如下反应:
Ⅰ.2N O(g) 2N(g)+O(g)+164kJ
2 2 2
Ⅱ.N O(g)+CO(g) N(g)+CO (g)+356 kJ
2 2 2
完成下列填空:
(1)反应I平衡常数的表达式K=_______。
某温度下,反应Ⅰ的K=0.16,该温度下,测得容器中NO、N、O 的浓度分别为0.5mol·L-1、0.5mol·L-1、
2 2 2
0.25mol·L-1,此时,反应I是否处于平衡状态?若不是,预测反应的方向。_______。
(2)甲为10L 的恒温容器。盛有1mol NO和lmolCO,发生反应Ⅰ和反应Ⅱ,5min 时,测得CO转化率为
2
60%,n(N ):n(O )=8:1,则n(N O)=_______mol;0~5min, O 的平均反应速率v(O )=_______mol ·
2 2 2 2 2
L-1·min-1。
(3)乙为10L的绝热容器。向其中充入1mol NO和1molCO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的
2
时间_______甲;此时乙中n(N O)比甲中_______ (以上两空选填“>”“<”或“=”),理由是:_______。
2
(4)不同压强的密闭容器中,分别充入1mol NO和1lmolCO,发生反应Ⅰ和反应Ⅱ,测得NO的平衡转化
2 2
率与温度的关系如图所示。
P、P、 P 由小到大的顺序为_______;温度高于T°C时,容器内发生的主要反应为_______ (填 “Ⅰ”
1 2 3
“Ⅱ”)。
13.(2022·江苏省天一中学高三期末)利用所学电化学反应原理,解决以下问题:
I.如图所示,A为电源,B为浸透饱和食盐水和酚酞溶液的滤纸,滤纸中央滴有一滴KMnO 溶液,C、
4
D为电解槽,其电极材料及电解质溶液如图所示。(1)闭合K,断开K,通电后,d端显红色,则电源b端为_______极,若c、d为惰性电极,检验c端产物
1 2
的方法为_______。滤纸中央 溶液处发生的现象为_______。
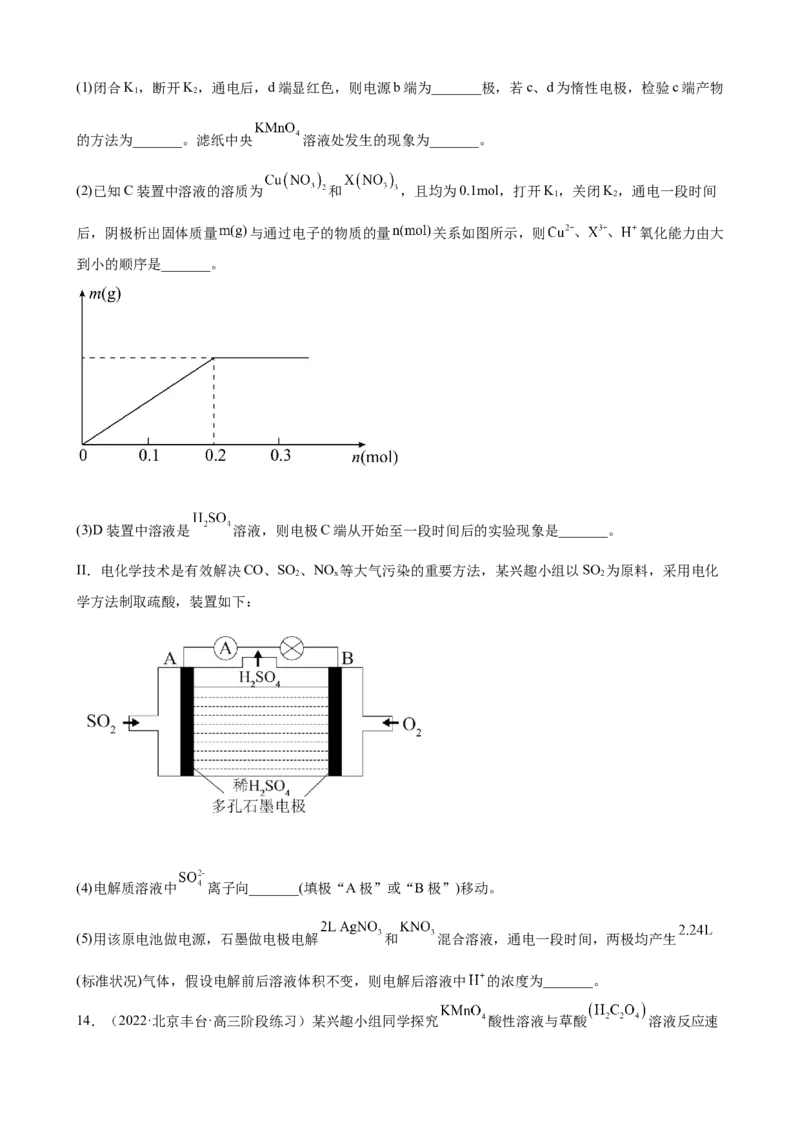
(2)已知C装置中溶液的溶质为 和 ,且均为0.1mol,打开K,关闭K,通电一段时间
1 2
后,阴极析出固体质量 与通过电子的物质的量 关系如图所示,则 氧化能力由大
到小的顺序是_______。
(3)D装置中溶液是 溶液,则电极C端从开始至一段时间后的实验现象是_______。
II.电化学技术是有效解决CO、SO 、NO 等大气污染的重要方法,某兴趣小组以SO 为原料,采用电化
2 x 2
学方法制取疏酸,装置如下:
(4)电解质溶液中 离子向_______(填极“A极”或“B极”)移动。
(5)用该原电池做电源,石墨做电极电解 和 混合溶液,通电一段时间,两极均产生
(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中 的浓度为_______。
14.(2022·北京丰台·高三阶段练习)某兴趣小组同学探究 酸性溶液与草酸 溶液反应速率的影响因素。将 的 酸性溶液与 草酸溶液按如下比例混合。
【设计实验】
序
号 V( 酸性溶液)/ V(草酸溶液)/ 反应温度/
① 2.0 2.0 0 20
② 2.0 1.0 1.0 20
(1)补全 酸性溶液与草酸溶液反应的离子方程式:_______。
(2)实验①和②的目的是_______。
【进行实验】
小组同学进行实验①和②,发现紫色并未直接褪去,而是分成两个阶段:
Ⅰ.紫色溶液变为青色溶液;Ⅱ.青色溶液逐渐褪至无色溶液。
【查阅资料】
a. 酸性溶液与草酸溶液的反应主要包含如下几个过程:
反应ⅰ.
反应ⅱ.
反应ⅲ。
b. 的氧化性较弱,在本实验条件下不能氧化 。
c. 呈绿色,在酸性条件下不稳定,迅速分解为 和 。
【继续探究】
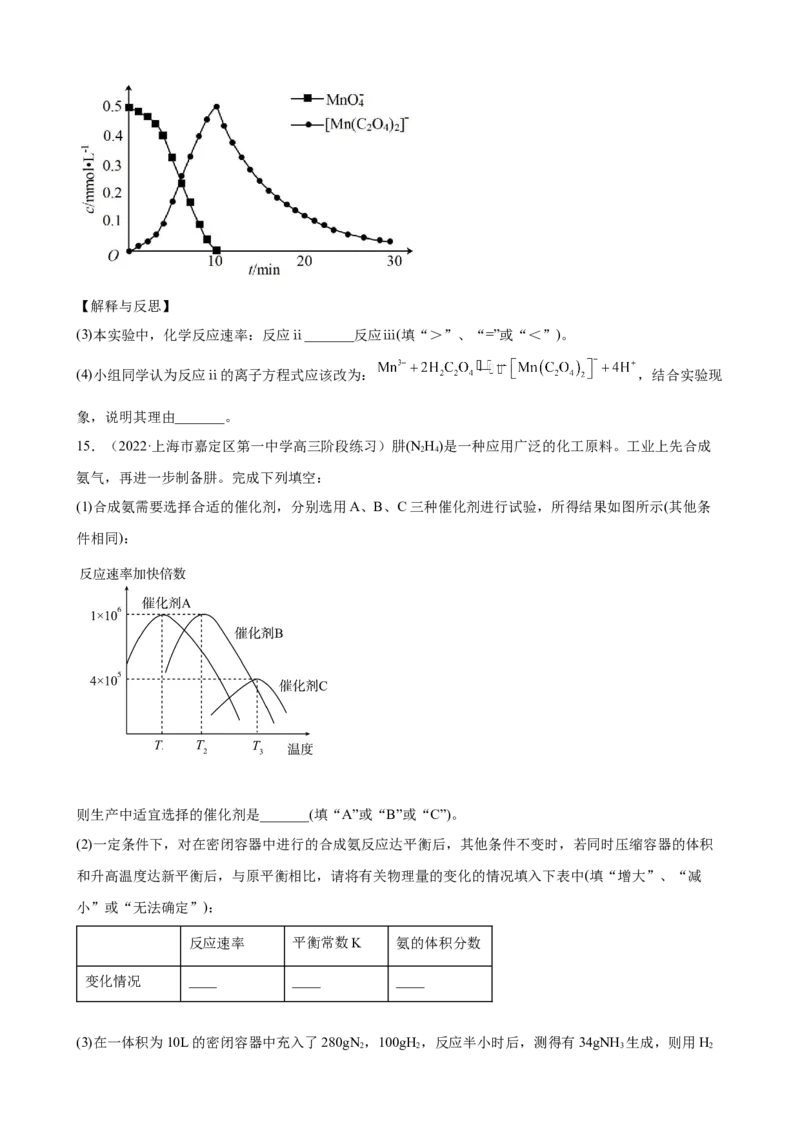
进一步实验证明溶液中含有 ,实验①反应过程中 和 的浓度随时间的变
化如下图。【解释与反思】
(3)本实验中,化学反应速率:反应ⅱ_______反应ⅲ(填“>”、“=”或“<”)。
(4)小组同学认为反应ⅱ的离子方程式应该改为: ,结合实验现
象,说明其理由_______。
15.(2022·上海市嘉定区第一中学高三阶段练习)肼(N H)是一种应用广泛的化工原料。工业上先合成
2 4
氨气,再进一步制备肼。完成下列填空:
(1)合成氨需要选择合适的催化剂,分别选用A、B、C三种催化剂进行试验,所得结果如图所示(其他条
件相同):
则生产中适宜选择的催化剂是_______(填“A”或“B”或“C”)。
(2)一定条件下,对在密闭容器中进行的合成氨反应达平衡后,其他条件不变时,若同时压缩容器的体积
和升高温度达新平衡后,与原平衡相比,请将有关物理量的变化的情况填入下表中(填“增大”、“减
小”或“无法确定”):
反应速率 平衡常数K 氨的体积分数
变化情况 ____ ____ ____
(3)在一体积为10L的密闭容器中充入了280gN,100gH,反应半小时后,测得有34gNH 生成,则用H
2 2 3 2表示该反应的速率为_______mol·L-1·min-1,此时,氮气的转化率为_______。
(4)下列判断可以作为该反应达到平衡的标志的是_______。A.单位时间内每消耗1摩尔氮气的同时消耗
3摩尔氢气
B.混合气体的平均分子量不再发生变化
C.混合气体的密度保持不变
D.体系的温度不再变化
16.(2022·山东·邹城市兖矿第一中学高三期末)研究不同价态硫元素之间的转化是合理利用硫元素的基
本途径。
(1) 的结构与过氧化钠相似,则 的电子式为_______。
(2) (易溶于水)在酸性条件下可生成 和S,该反应的离子方程式为_______。
(3)焦亚硫酸钠( )是一种食品抗氧化剂,易溶于水。其中硫元素的化合价为_______价。向某些饮
料中添加少量焦亚硫酸钠,可降低饮料中溶解氧的含量,发生反应的离子方程式为_______。
(4)某小组同学设计实验实现几种价态硫元素的转化。可选用的实验药品如下:
a. 溶液;b. 浓硫酸;c. 溶液;d. 稀硫酸;e. 酸性 溶液;f.品红溶液;g.铜片。
实验序号 预期转化 选择试剂(填标号) 证明实现转化的现象
Ⅰ
Ⅱ a、c、d 淡黄色沉淀
Ⅲ b、g、f
①实验Ⅰ选择的试剂是a和_______(填标号)。
②实验Ⅱ实现了+4价和-2价S向0价S的转化,写出该转化反应的离子方程式:_______。
③实验Ⅲ中发生反应的化学方程式是_______,证明实现该转化的现象是_______。
17.(2022·宁夏·银川一中模拟预测)当今中国积极推进绿色低碳发展,力争在2030年前实现碳达峰,
2060年前实现碳中和。因此,研发CO 利用技术,降低空气中CO 含量成为研究热点。工业上常用CO
2 2 2
和H 为原料合成甲醇(CHOH),过程中发生如下两个反应:
2 3
反应I:
反应II:(1)①一定条件下,一氧化碳加氢生成甲醇的热化学方程式为: H
△
=___________ kJ·mol-1。
②若反应II逆反应活化能E(逆)为120 kJ·mol-1,则该反应的E(正)活化能为___________ kJ·mol-1。
a a
(2)有研究表明,用可控Cu/Cu O界面材料作催化剂可以提高CO 还原合成甲醇的选择性。将6.0 mol CO
2 2 2
和8.0 mol H 充入一体积为2L的恒温密闭容器中,发生反应3H(g) + CO (g) CHOH(g) + H O(g)
2 2 2 3 2
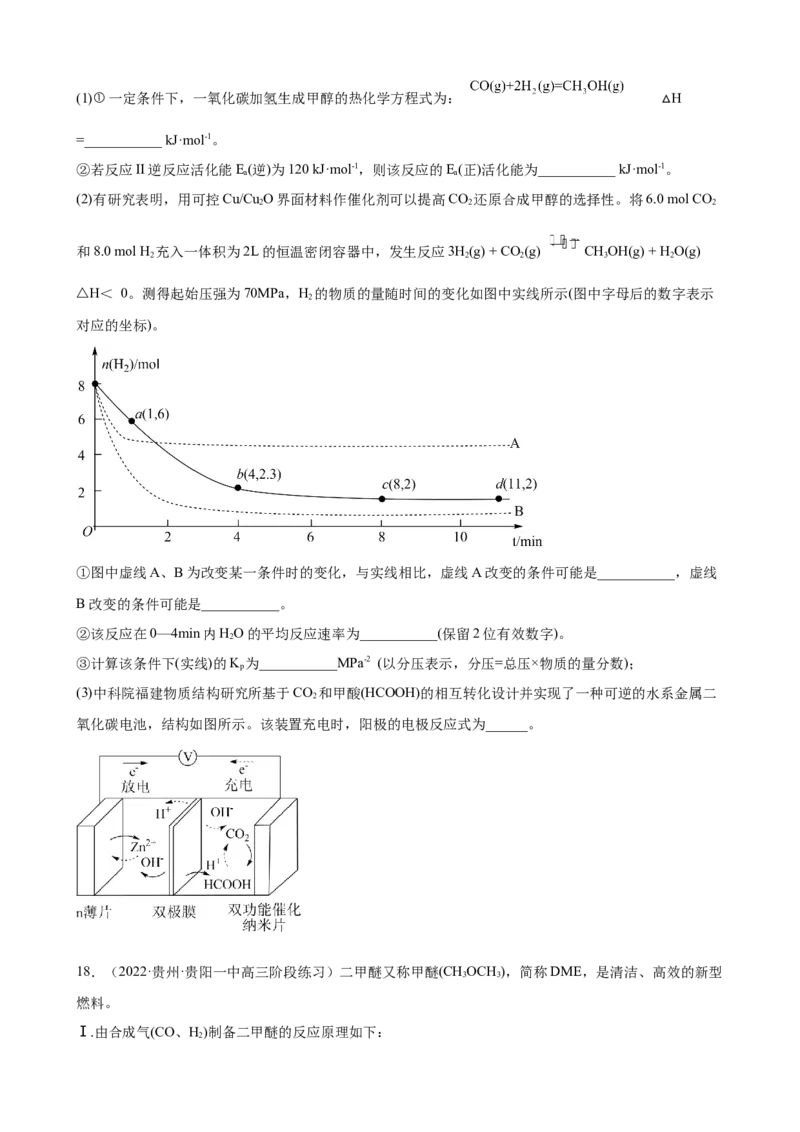
△H< 0。测得起始压强为70MPa,H 的物质的量随时间的变化如图中实线所示(图中字母后的数字表示
2
对应的坐标)。
①图中虚线A、B为改变某一条件时的变化,与实线相比,虚线A改变的条件可能是___________,虚线
B改变的条件可能是___________。
②该反应在0—4min内HO的平均反应速率为___________(保留2位有效数字)。
2
③计算该条件下(实线)的K 为___________MPa-2 (以分压表示,分压=总压×物质的量分数);
p
(3)中科院福建物质结构研究所基于CO 和甲酸(HCOOH)的相互转化设计并实现了一种可逆的水系金属二
2
氧化碳电池,结构如图所示。该装置充电时,阳极的电极反应式为______。
18.(2022·贵州·贵阳一中高三阶段练习)二甲醚又称甲醚(CHOCH ),简称DME,是清洁、高效的新型
3 3
燃料。
Ⅰ.由合成气(CO、H)制备二甲醚的反应原理如下:
2①
②
③
回答下列问题:
(1)由合成气(CO、H)制备 且生成 其热化学方程式为_______。
2
(2)一定条件下在恒温恒容的密闭容器中,按不同投料比充入CO(g)和 进行反应①,平衡时CO(g)
和 的转化率如图所示,则a= _______(填数值)。
(3)在体积一定的密闭容器中发生反应②,如果该反应的平衡常数 值变小,下列说法正确的是
_______(填序号)。
A.平衡向正反应方向移动 B.平衡移动的原因是升高了温度
C.达到新平衡后体系的压强不变 D.容器中 的体积分数减小
Ⅱ.由合成气(CO、H)制备二甲醚的反应原理如下:
2 2
④
⑤
(4)若在体积为2L的密闭容器中,控制 流速为 (已换算为标准状况), 的转化率为
80.0%,则 的反应速率为_______ (保留三位有效数字)。(5)在恒压条件下,按 与 的物质的量之比为1:3投料,测得 平衡转化率和平衡时CO的选
择性转化的 中生成CO的物质的量分数)随温度的变化如图所示:
①曲线n随温度升高显示如图所示变化的原因是_______。
②T℃时反应⑤的平衡常数K=_______ (保留两位有效数字)。
③合成甲醚的适宜温度为260℃, 理由是_______。
④其他条件不变,改为恒容条件,CO平衡选择性比恒压条件下的平衡选择性_______ (填“高”“低”或
“不变”)。
19.(2022·湖北·高三阶段练习)甲烷和水蒸气催化制氢主要有如下两个反应:
①
②
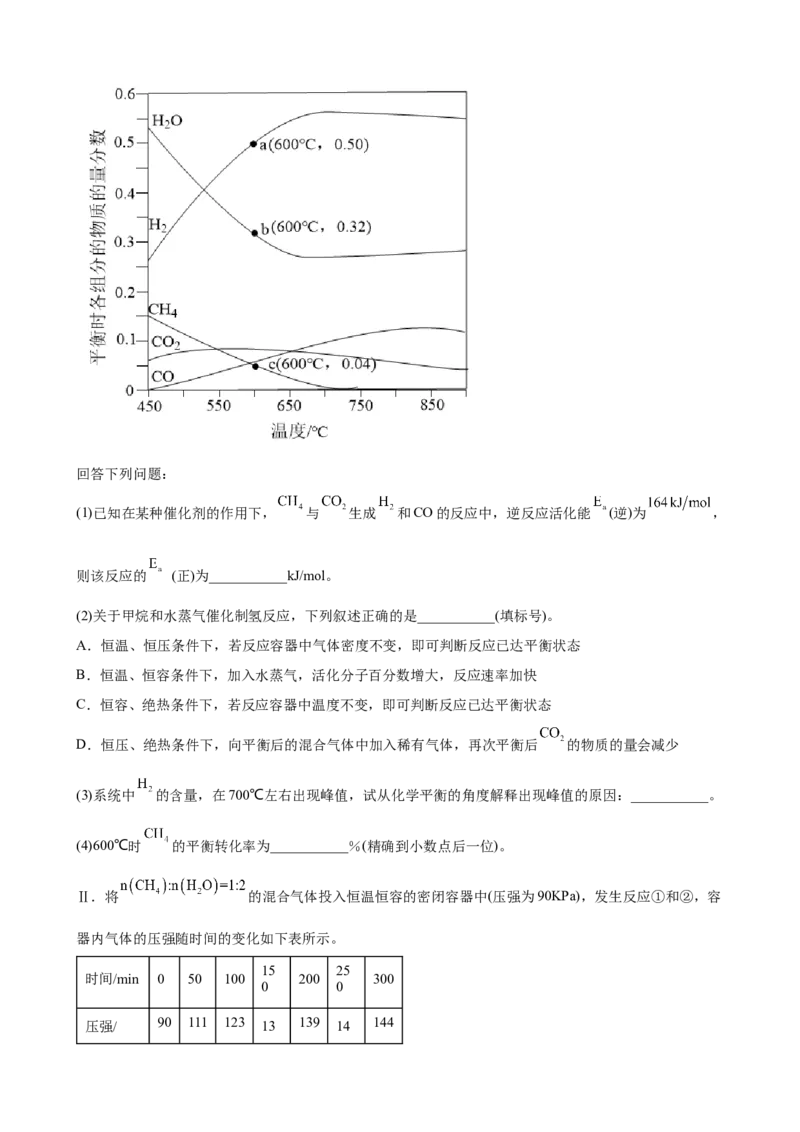
I.恒定压强时,将 的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度
的关系如图所示。回答下列问题:
(1)已知在某种催化剂的作用下, 与 生成 和CO的反应中,逆反应活化能 (逆)为 ,
则该反应的 (正)为___________kJ/mol。
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是___________(填标号)。
A.恒温、恒压条件下,若反应容器中气体密度不变,即可判断反应已达平衡状态
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.恒容、绝热条件下,若反应容器中温度不变,即可判断反应已达平衡状态
D.恒压、绝热条件下,向平衡后的混合气体中加入稀有气体,再次平衡后 的物质的量会减少
(3)系统中 的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:___________。
(4)600℃时 的平衡转化率为___________%(精确到小数点后一位)。
Ⅱ.将 的混合气体投入恒温恒容的密闭容器中(压强为90KPa),发生反应①和②,容
器内气体的压强随时间的变化如下表所示。
15 25
时间/min 0 50 100 200 300
0 0
压强/ 90 111 123 13 139 14 144KPa 2 4
(5)用单位时间内气体分压的变化来表示反应速率,即 ,则反应①前150min内平均反应速率
___________kPa/min,250min末,测得氢气压强 为96kPa, 为用气体分压表示的平衡常数,分
压=总压×物质的量分数,则反应②平衡常数 ___________。
20.(2022·江苏徐州·高三阶段练习)SO 、NOx是空气的主要污染物,有效去除大气中的SO 、NOx可
2 2
以保护大气环境。含氮废水氨态氮(以 存在)和硝态氨(以 存在)引起水体富营养化,
需经处理后才能排放。
(1)用天然碱生产小苏打的母液(主要溶质为碳酸钠)吸收烟气中SO 的相关反应的热化学方程式如下:
2
反应 的∆H=_____
(2)已知拆开 键, 键, 键分别需要的能量是 、 、 ,则N(g)
2
与H(g)反应生成NH (g)的热化学方程式为_______
2 3
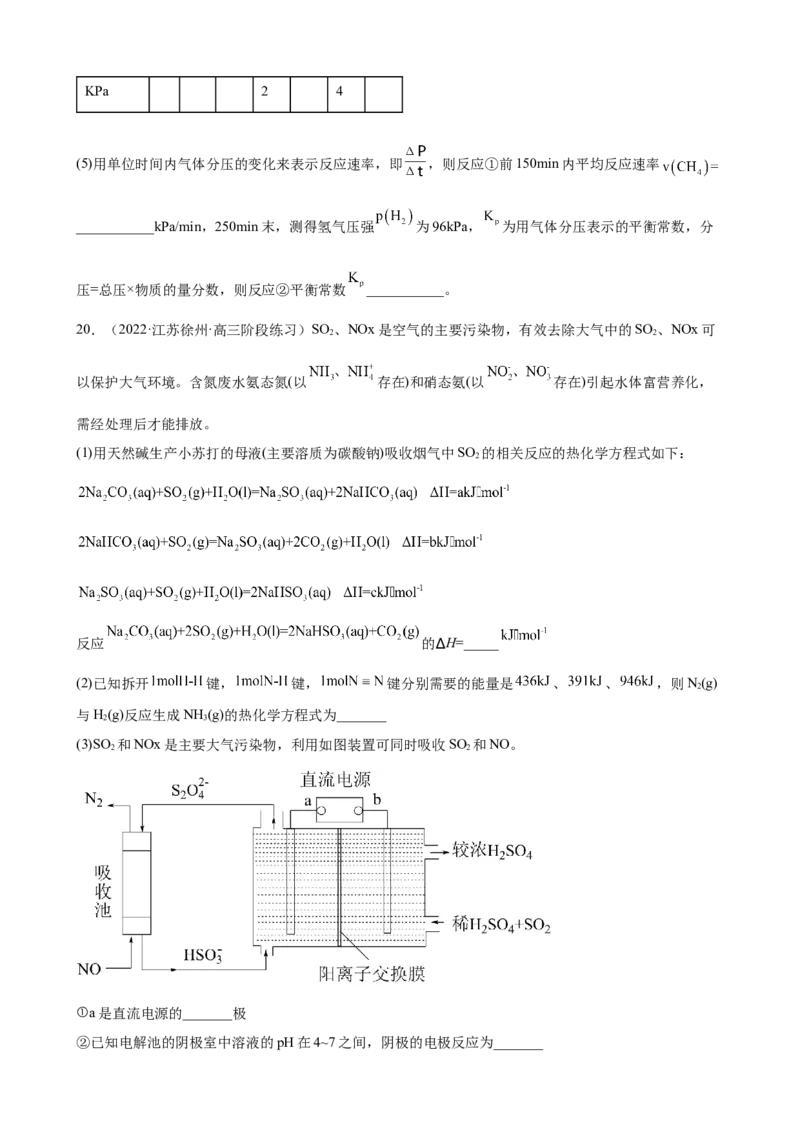
(3)SO 和NOx是主要大气污染物,利用如图装置可同时吸收SO 和NO。
2 2
①a是直流电源的_______极
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为_______③写出电解池中发生反应的离子方程式:_______
21.(2022·江西·临川一中高三阶段练习)回答下列问题
(1)探究外界条件对 分解化学反应速率的影响,相关实验设计如下表所示:
溶液
试管编 水的体积/ 溶液体
实验目的 温度 实验现象
号 体 mL 积/mL
质量分数
积/mL
缓慢产生适
Ⅰ 为编号Ⅱ实验参照 12% 5.0 常温 0 0
量气泡
温度对反应速率的 快速产生大
Ⅱ (_______) 5.0 60℃ 0 0
影响 量气泡
缓慢产生少
Ⅲ 为编号Ⅳ实验参照 4.0% 5.0 常温 (_______) 0
量气泡
快速产生大
Ⅳ (_______) 4.0% 5.0 常温 0 1.0
量气泡
填写表中缺少的内容:Ⅱ_______;Ⅲ_______;Ⅳ_______。
(2)将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其分解:
,能判断该分解反应已经达到化学平衡的是_______A.密闭容器
中氨气的体积分数不变 B.密闭容器中混合气体的密度不变
C. D.密闭容器中
(3)质量相同的铜棒和铁棒用导线连接插入 溶液中,一段时间后取出洗净、干燥、称量,二者质量
差为24g,则导线中通过的电子的物质的量_______mol。
(4)熔融碳酸盐燃料电池原理示意图如图①电池工作时 向电极_______(填A或B)移动。
②电极A上 参与的电极反应为_______。
22.(2022·江苏徐州·高三阶段练习)采用科学技术减少碳氧化物、氮氧化物等物质的排放,可促进社会
主义生态文明建设。
(1) 既是一种重要的能源,也是一种重要的化工原料。
①甲烷高温分解生成氢气和碳。在密闭容器中进行此反应时要先通入适量空气使部分甲烷燃烧,其目的
是_______;
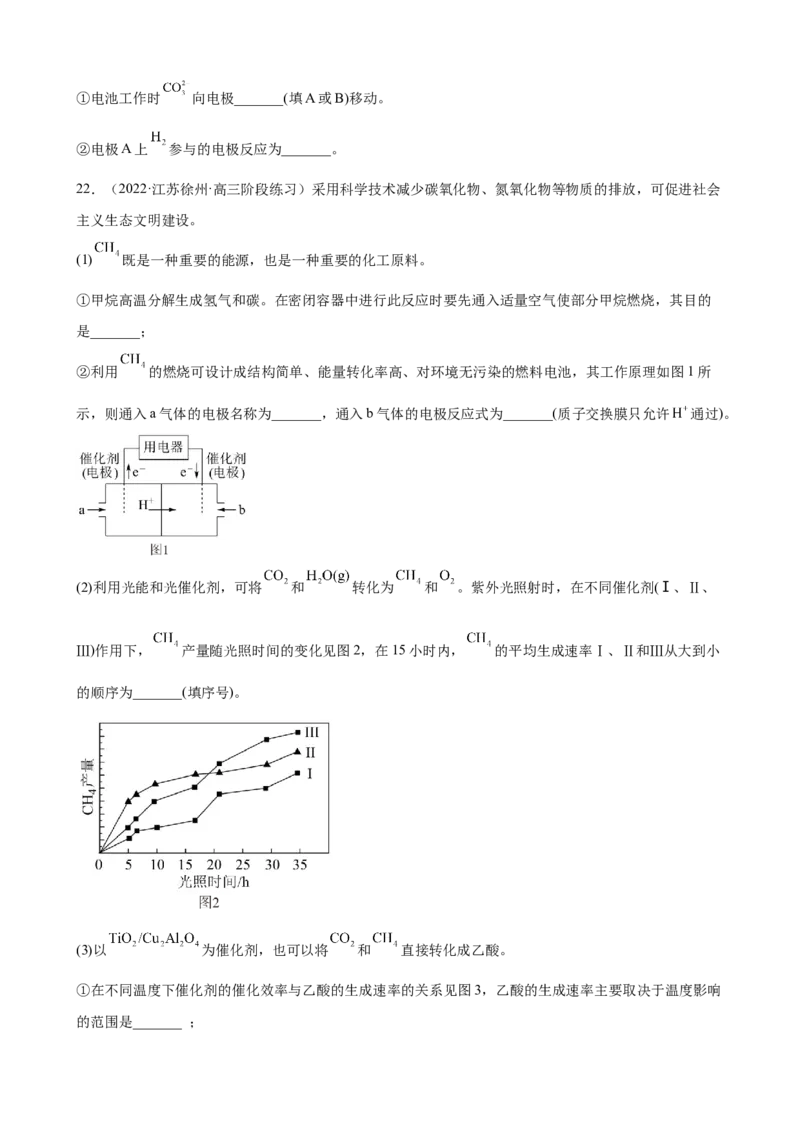
②利用 的燃烧可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图1所
示,则通入a气体的电极名称为_______,通入b气体的电极反应式为_______(质子交换膜只允许 通过)。
(2)利用光能和光催化剂,可将 和 转化为 和 。紫外光照射时,在不同催化剂(Ⅰ、Ⅱ、
Ⅲ)作用下, 产量随光照时间的变化见图2,在15小时内, 的平均生成速率Ⅰ、Ⅱ和Ⅲ从大到小
的顺序为_______(填序号)。
(3)以 为催化剂,也可以将 和 直接转化成乙酸。
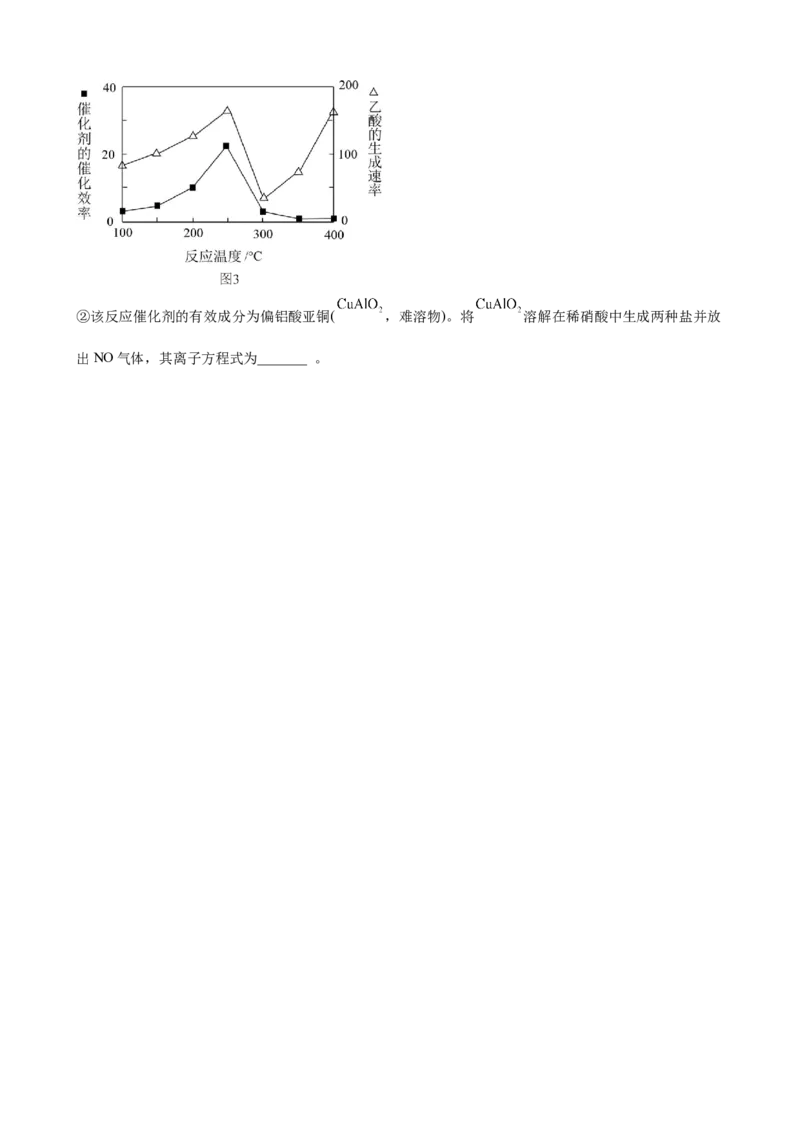
①在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图3,乙酸的生成速率主要取决于温度影响
的范围是_______ ;②该反应催化剂的有效成分为偏铝酸亚铜( ,难溶物)。将 溶解在稀硝酸中生成两种盐并放
出NO气体,其离子方程式为_______ 。参考答案:
1.(1) SO +Na SO +H O=2NaHSO > SO +H O HSO +OH-
2 2 3 2 3 2
(2) 60% CD
(3)O +4e-+4H+=2H O
2 2
(4)16:29
2.(1)排除装置中存在的空气,防止制得的纳米零价铁被氧化;及时排出H,防止爆炸
2
(2) 6 +10H++8e—= +3H O
2
(3) ZVI表面的FeOH会因为质子化作用形成FeOH ,使ZVI表面带正电荷,不利于吸
附Pb2+ 随pH增大,c(H+)减小,ZVI颗粒表面去质子化程度越来越强、与Pb2+的静电引
力越来越大,质子化程度减弱,但配位反应正向进行程度仍然增大,同时也有还原反应的
正向进行程度增大
(4)pH减小,H+浓度增大,会生成更多的H,使 被还原的中间产物NH更多的与H 反
应生成 ,减少N 的生成
2
3.(1)C
(2)Zn+Ag O+HO=Zn(OH) +2Ag
2 2 2
(3) 减小 增大 不变
(4) 放出 92
(5)该反应是可逆反应,1molN 和3molH 不可能完全反应,所以放出的热量小于92kJ
2 2
(6)0.25
4.(1)
(2) 反应初期,温度高, 反应速率快,转化率高;反应后期,苯或苯酚受热分解生
成碳,覆盖催化剂(或堵塞催化剂孔隙),使催化剂活性降低,转化率降低 温度升
高,微量的 会氧化苯酚,造成选择性降低
(3)(4) 质量过小,反应生成 浓度小; 质量过大, 浓度小,
生成 浓度小,且过量 会与 反应
5.(1)吸热
(2)<
(3)CO +H CO+HO
2 2 2
(4) 因为反应物总分子数大于生成物总分子数,所以增大压强,平衡正向移动,CHOH
3
的物质的量增大 > 0.25 4 C
6.(1) -121 -80
(2)ADF
(3) p >p>p = <
1 2 3
7.(1)1s22s22p63s23p63d8或[Ar]3d8
(2)pH=2时,酸性较强,抑制HR电离产生R-,c(R-)低,因而Ni2+去除率低
(3)NiR 在溶液中存在以下平衡:NiR (aq) Ni2+(aq)+2R-(aq)。Fe2+和HO 通过反应Ⅰ和
2 2 2 2
反应Ⅱ将R-转化成难以与Ni2+络合的·R,使c(R-)减小,平衡正向移动,实现“脱络”
(4)2NiC O Ni O+3CO↑+CO ↑
2 4 2 3 2
(5)(NH )Ni(SO )·10H O
4 2 4 2 2
8.(1) N
(2)3.75
(3) 把 转化为更难溶的 ,以便酸能浸出,提高铅的利用率
(4)
(5)
(6) 会产生 气体污染空气 0.179.(1)0.05
(2)H +2OH--2e-=2H O
2 2
(3) CHCH+Cl CHCHCl+HCl 取代反应
3 3 2 3 2
CH=CH +Br →BrCHCHBr 加成反应
2 2 2 2 2
10.(1)0.015mol/(L·min)
(2)bc
(3)a
(4) 放热 在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率
提高不大,而生产成本增加,得不偿失
(5)2Fe3++S2-=2Fe2++S↓
(6) = 变小
11.(1) 小于
(2) 甲基 升高温度,增大反应速率和平衡正向移动,可以提高产率
若在恒压容器中进行该反应,加入高温水蒸气,各组分浓度减小,相当于减压,促进平衡
正向移动,可以提高产率 C
12.(1) 不是平衡状态,反应逆向进行
(2) 0.2 2×10-3
(3) < > 反应Ⅰ和反应Ⅱ都是放热反应,乙是绝热容器,乙容器中
温度比甲容器中高,温度升高,平衡左移,NO转化率降低
2
(4) P<P<P Ⅱ
1 2 3
13.(1) 负 将湿润的淀粉碘化钾试纸置于电极附近,试纸变蓝 紫红
色向c极移动
(2)Cu2+>H+>X3+
(3)在C端开始时有无色无味气体产生,一段时间后有红色物质析出
(4)A极
(5)0.1mol/L
14.(1)6H+(2)探究相同温度下,草酸浓度的改变对化学反应速率的影响
(3)>
(4) 的氧化性较弱,不能氧化 ,而Mn3+与草酸发生过程iii的反应,
使得Mn3+浓度不断减小,只有过程ii存在化学平衡,即
,上述平衡会逆向移动, 浓度逐渐
减小,所得现象为溶液的青绿色逐渐褪去直至无色,故可判断过程ii的反应方程式应该为
。
15.(1)A
(2) 增大 减小 无法确定
(3) 0.01 10%
(4)BD
16.(1)
(2)
(3) +4
(4) e 品
红溶液褪色,溶液颜色逐渐变蓝
17.(1) -92 161
(2) 升高温度 缩小体积(或加压) 0.24mol·L-1·min-1 或0.005或
(3)HCOOH-2e-=CO ↑+2H+
2
18.(1)
(2)2
(3)BD
(4)6.67
(5) ∆H <0,升温反应④平衡逆向移动,CO 的转化率降低,升温过程中,反应④占主要
4 2的,故CO 的转化率降低 0.046 此温度下,CO的选择性较低且反应速率不低,
2
若温度再高CO的选择性增大,不利于合成甲醚 高
19.(1)411
(2)AC
(3)700℃以前,由于反应①吸热,随着温度的升高,反应正向移动程度大,平衡时 的物
质的量逐渐增大;700℃以后,由于②正反应放热,当温度升高时,平衡逆向移动, 的
物质的量逐渐减小
(4)81.5
(5) 0.14 6.67
20.(1)c+ (a+b)
(2)N (g)+3H(g)=2NH (g) ∆H=-92 kJ/mol
2 2 3
(3) 负 2 +2H++2e-= +2H O SO +2 =2H++ +
2 2
21.(1) 12% 1.0 催化剂( )对反应速率的影响
(2)B
(3)0.4
(4) A
22.(1) 提供CH 分解所需的能量 负极 O+4H++4e-=2H O
4 2 2
(2)II>III>I
(3) 300℃