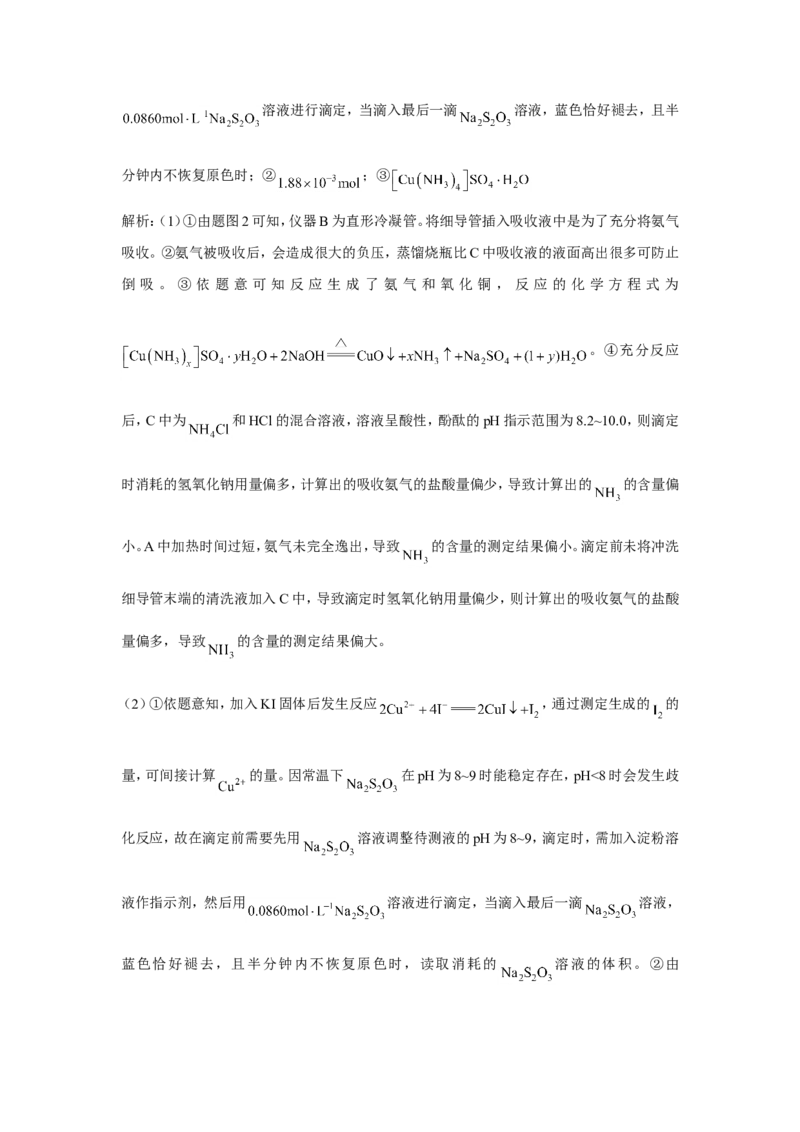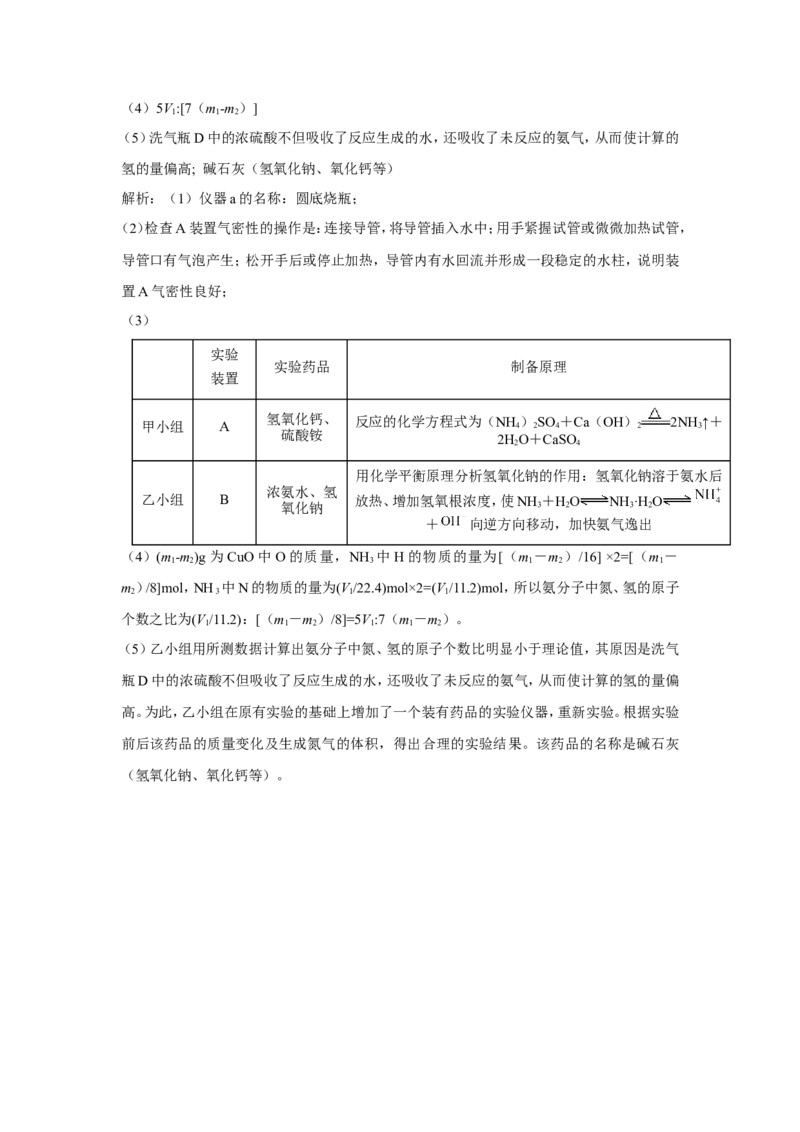文档内容
以流程为载体的实验 专项练习
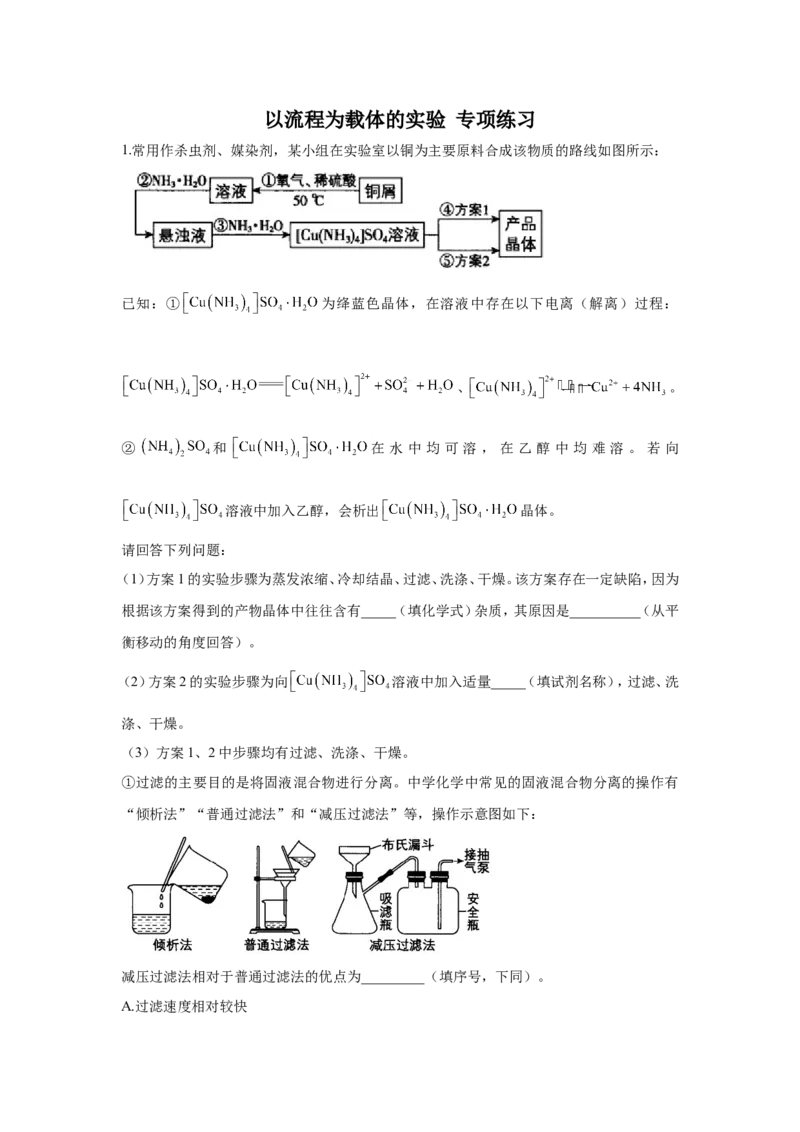
1.常用作杀虫剂、媒染剂,某小组在实验室以铜为主要原料合成该物质的路线如图所示:
已知:① 为绛蓝色晶体,在溶液中存在以下电离(解离)过程:
、 。
② 和 在 水 中 均 可 溶 , 在 乙 醇 中 均 难 溶 。 若 向
溶液中加入乙醇,会析出 晶体。
请回答下列问题:
(1)方案1的实验步骤为蒸发浓缩、冷却结晶、过滤、洗涤、干燥。该方案存在一定缺陷,因为
根据该方案得到的产物晶体中往往含有_____(填化学式)杂质,其原因是__________(从平
衡移动的角度回答)。
(2)方案2的实验步骤为向 溶液中加入适量_____(填试剂名称),过滤、洗
涤、干燥。
(3)方案1、2中步骤均有过滤、洗涤、干燥。
①过滤的主要目的是将固液混合物进行分离。中学化学中常见的固液混合物分离的操作有
“倾析法”“普通过滤法”和“减压过滤法”等,操作示意图如下:
减压过滤法相对于普通过滤法的优点为_________(填序号,下同)。
A.过滤速度相对较快B.能过滤胶体类混合物
C.得到的固体物质相对比较干燥
②下列最适合在“洗涤”步骤中作为洗涤液的是______。
A.蒸馏水
B.乙醇与水的混合液
C.饱和 溶液
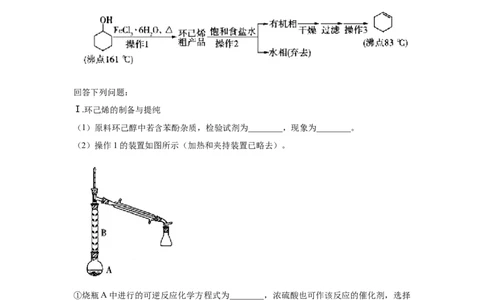
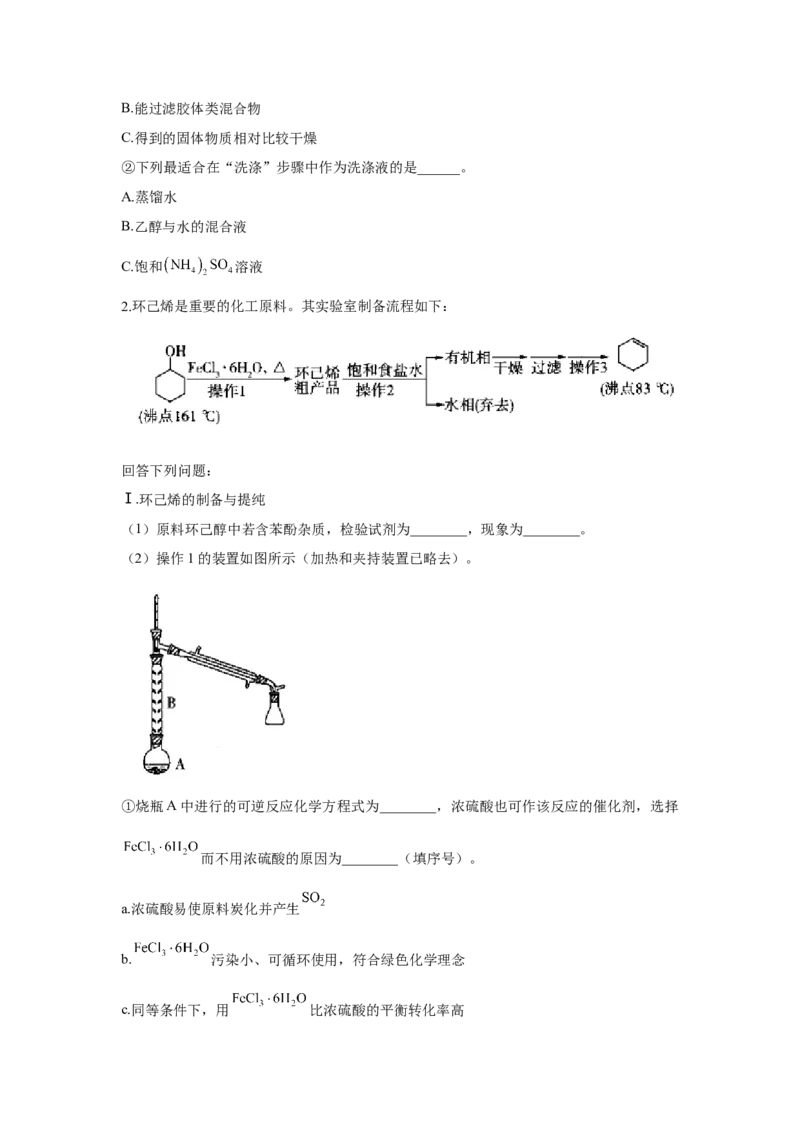
2.环己烯是重要的化工原料。其实验室制备流程如下:
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为________,现象为________。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
①烧瓶A中进行的可逆反应化学方程式为________,浓硫酸也可作该反应的催化剂,选择
而不用浓硫酸的原因为________(填序号)。
a.浓硫酸易使原料炭化并产生
b. 污染小、可循环使用,符合绿色化学理念
c.同等条件下,用 比浓硫酸的平衡转化率高②仪器B的作用为________。
(3)操作2用到的玻璃仪器是________。
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,________,弃去
前馏分,收集83℃的馏分。
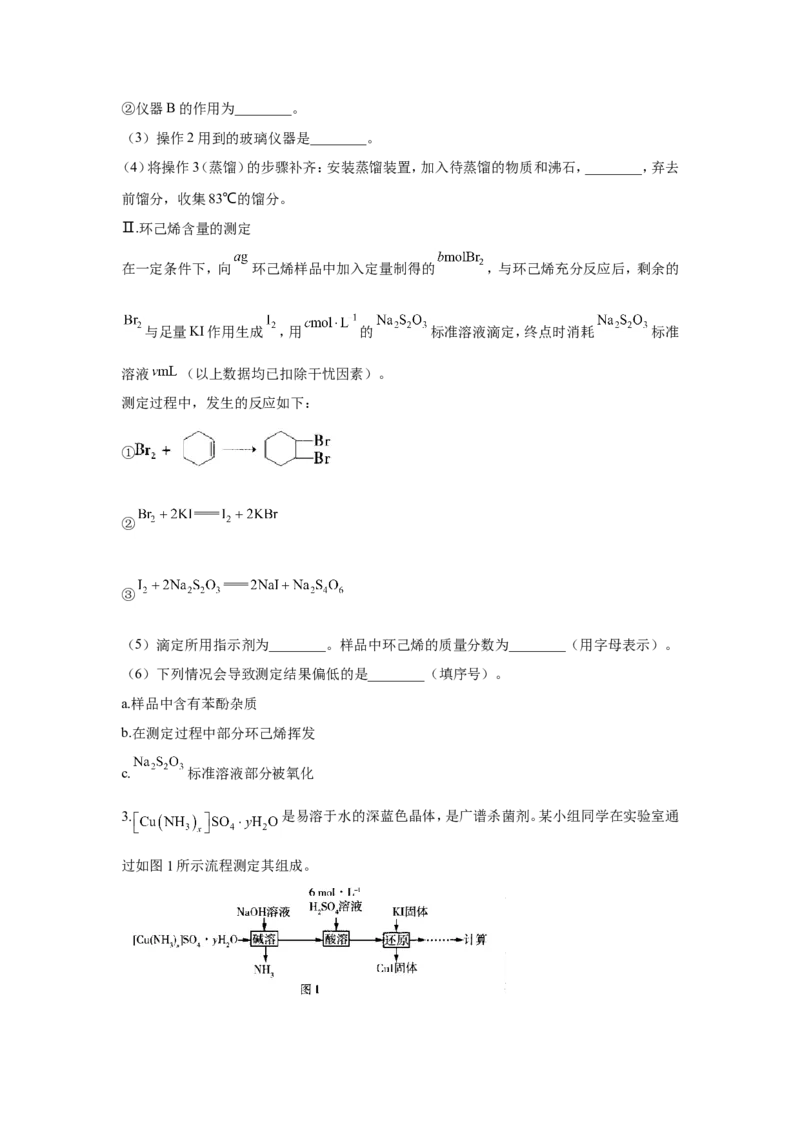
Ⅱ.环己烯含量的测定
在一定条件下,向 环己烯样品中加入定量制得的 ,与环己烯充分反应后,剩余的
与足量KI作用生成 ,用 的 标准溶液滴定,终点时消耗 标准
溶液 (以上数据均已扣除干忧因素)。
测定过程中,发生的反应如下:
①
②
③
(5)滴定所用指示剂为________。样品中环己烯的质量分数为________(用字母表示)。
(6)下列情况会导致测定结果偏低的是________(填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c. 标准溶液部分被氧化
3. 是易溶于水的深蓝色晶体,是广谱杀菌剂。某小组同学在实验室通
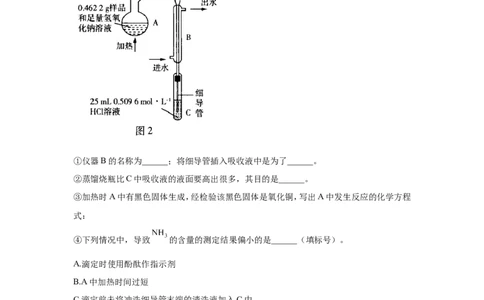
过如图1所示流程测定其组成。回答下列问题:
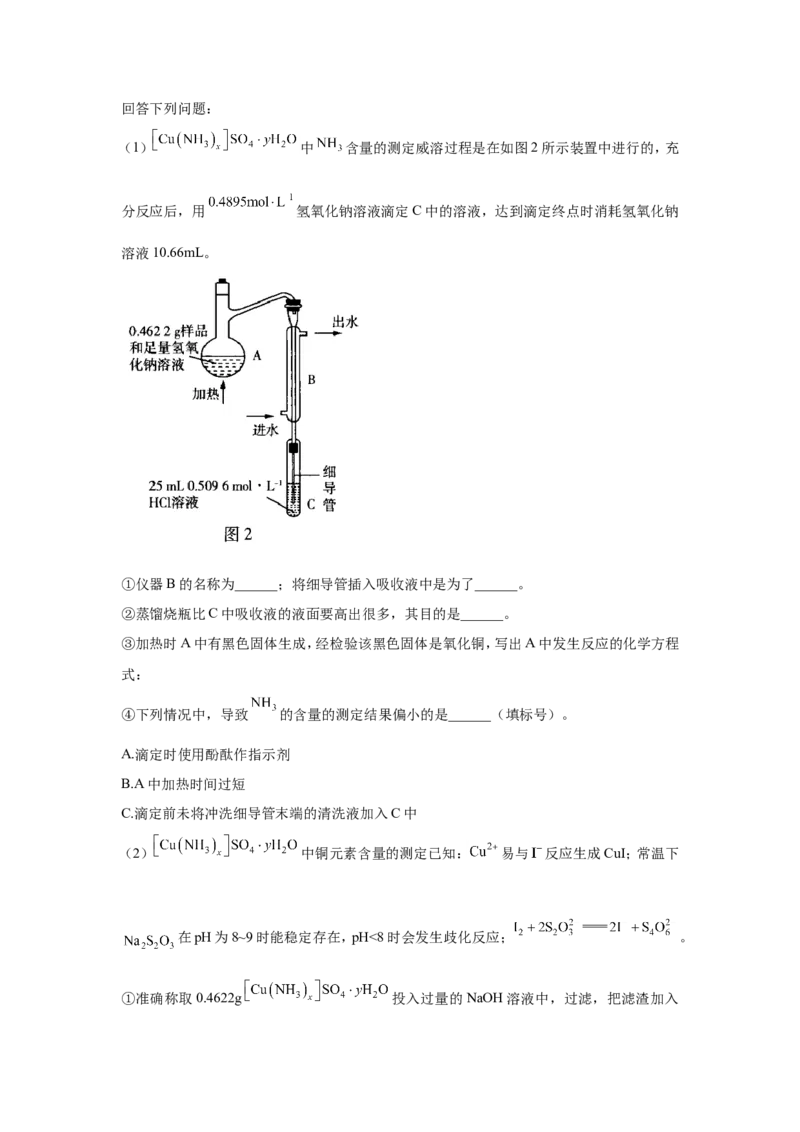
(1) 中 含量的测定威溶过程是在如图2所示装置中进行的,充
分反应后,用 氢氧化钠溶液滴定C中的溶液,达到滴定终点时消耗氢氧化钠
溶液10.66mL。
①仪器B的名称为______;将细导管插入吸收液中是为了______。
②蒸馏烧瓶比C中吸收液的液面要高出很多,其目的是______。
③加热时A中有黑色固体生成,经检验该黑色固体是氧化铜,写出A中发生反应的化学方程
式:
④下列情况中,导致 的含量的测定结果偏小的是______(填标号)。
A.滴定时使用酚酞作指示剂
B.A中加热时间过短
C.滴定前未将冲洗细导管末端的清洗液加入C中
(2) 中铜元素含量的测定已知: 易与 反应生成CuI;常温下
在pH为8~9时能稳定存在,pH<8时会发生歧化反应; 。
①准确称取0.4622g 投入过量的NaOH溶液中,过滤,把滤渣加入溶液中,搅拌使滤渣充分溶解,向溶解后的溶液中加入2gKI(过量)固体,搅
拌,充分反应后,_______,记录消耗 溶液的体积。(需用试剂:
溶液、 溶液、淀粉溶液)
②若反应消耗 溶液的体积为21.86mL,则样品中 _______。
③经计算,该晶体的化学式为_______。
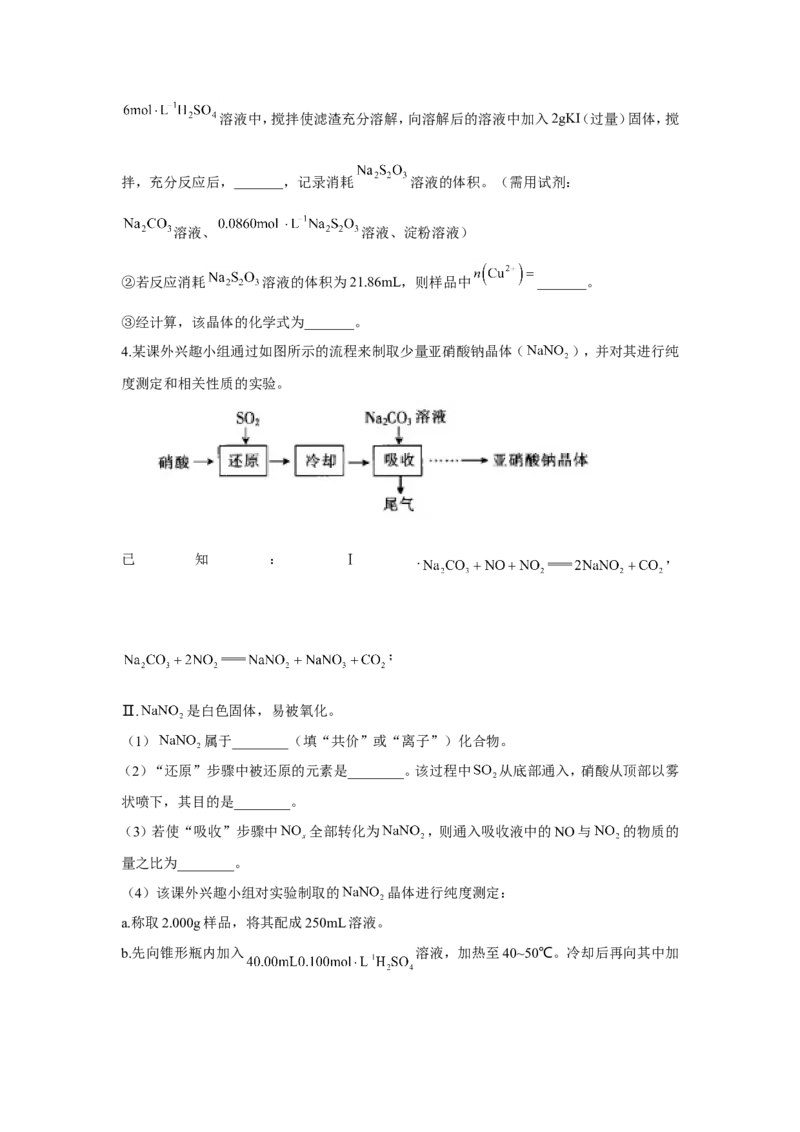
4.某课外兴趣小组通过如图所示的流程来制取少量亚硝酸钠晶体( ),并对其进行纯
度测定和相关性质的实验。
已 知 : Ⅰ . ,
;
Ⅱ. 是白色固体,易被氧化。
(1) 属于________(填“共价”或“离子”)化合物。
(2)“还原”步骤中被还原的元素是________。该过程中 从底部通入,硝酸从顶部以雾
状喷下,其目的是________。
(3)若使“吸收”步骤中 全部转化为 ,则通入吸收液中的NO与 的物质的
量之比为________。
(4)该课外兴趣小组对实验制取的 晶体进行纯度测定:
a.称取2.000g样品,将其配成250mL溶液。
b.先向锥形瓶内加入 溶液,加热至40~50℃。冷却后再向其中加入 溶液,充分混合。
c.最后用待测的样品溶液与之恰好完全反应,重复三次,平均消耗样品溶液50.00mL。(
与 反应的关系式为 )
①整个测定过程中应迅速操作,不宜耗时过长,否则样品的纯度会________(填“偏大”
“偏小”或“无影响”),原因是________。
②通过计算,该样品中 的质量分数为________。
(5)该课外兴趣小组将 溶液逐滴加入含淀粉—KI的酸性溶液中,溶液变蓝,同时放出
NO气体,该反应的离子方程式是________。
5.草酸亚铁( )是黄色晶体,常用作照相显影剂、新型电池材料等。在实验室中以铁粉
为原料,先制得中间原料硫酸亚铁铵 ,再制得水合草酸亚铁(
)。具体流程如图所示:
已知:
Ⅰ.草酸亚铁晶体为淡黄色粉末,难溶于水。
Ⅱ.pH>4时, 易被氧气氧化。
Ⅲ. 的 ; 的 约为 。
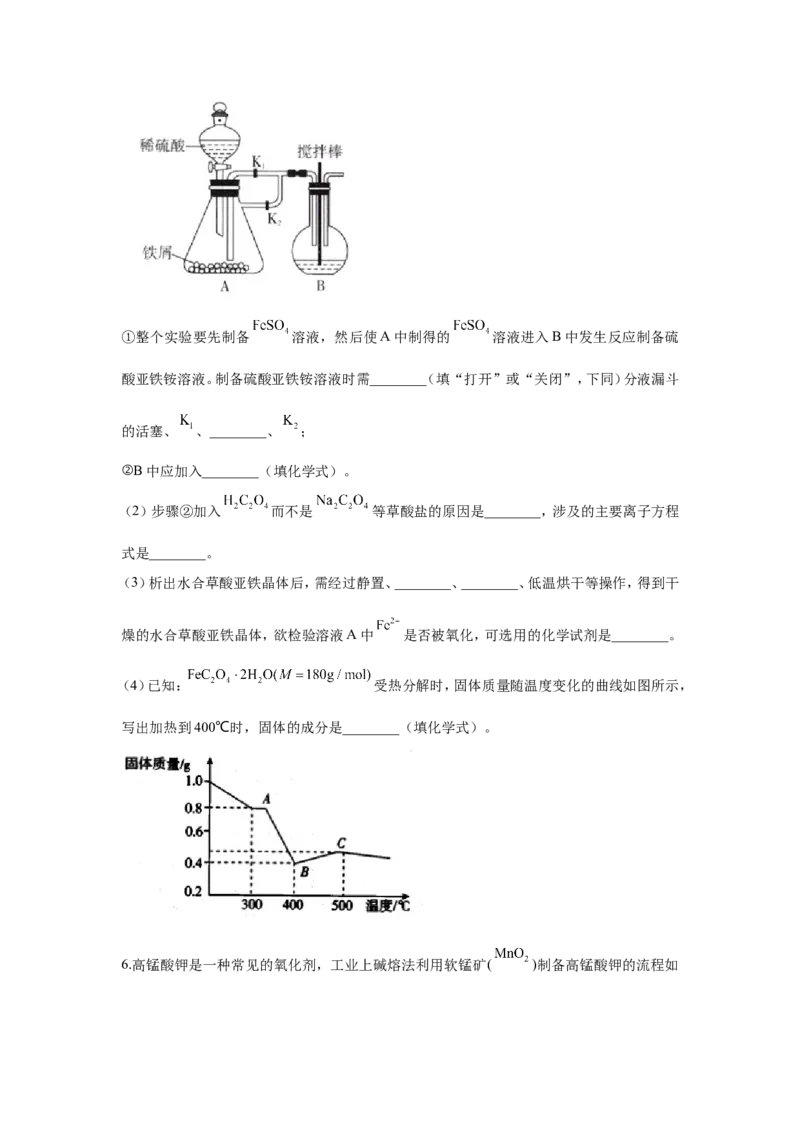
(1)用铁屑制备硫酸亚铁铵时,为了防止 被氧化,可采用下列装置进行实验:①整个实验要先制备 溶液,然后使A中制得的 溶液进入B中发生反应制备硫
酸亚铁铵溶液。制备硫酸亚铁铵溶液时需________(填“打开”或“关闭”,下同)分液漏斗
的活塞、 、________、 ;
②B中应加入________(填化学式)。
(2)步骤②加入 而不是 等草酸盐的原因是________,涉及的主要离子方程
式是________。
(3)析出水合草酸亚铁晶体后,需经过静置、________、________、低温烘干等操作,得到干
燥的水合草酸亚铁晶体,欲检验溶液A中 是否被氧化,可选用的化学试剂是________。
(4)已知: 受热分解时,固体质量随温度变化的曲线如图所示,
写出加热到400℃时,固体的成分是________(填化学式)。
6.高锰酸钾是一种常见的氧化剂,工业上碱熔法利用软锰矿( )制备高锰酸钾的流程如图。某化学活动小组在实验室中模拟该流程制备高锰酸钾,并对产物中 的质量分数
进行测定。
(1)“熔融氧化”步骤在坩埚中进行,则选用坩埚的材料为 ______(填序号)。
A.陶瓷 B.石英 C.铁 D.刚玉
(2)工业上电解制取 溶液时,生成的 ______(填化学式)经回收可以返名回“熔融氧
化”步骤循环利用。
(3)由 溶液获得 晶体的一系列操作为 ______、______、过滤、洗涤、干燥。
(4)按下述步骤测定产物中 的质量分数:
a.用分析天平准确称取 样品 ,配制成 溶液;
b.用分析天平准确称取 ,加入 的锥形瓶中,用100mL蒸馏水溶解,再
加入 硫酸10mL,加热到70~80℃;
c.趁热用高锰酸钾溶液进行滴定;
d.重复步骤b、c三次测定数据如下表,并进行数据处理。
实验序号 1 2 3
消耗 样品溶液体积/mL 25.10 24.80 25.10
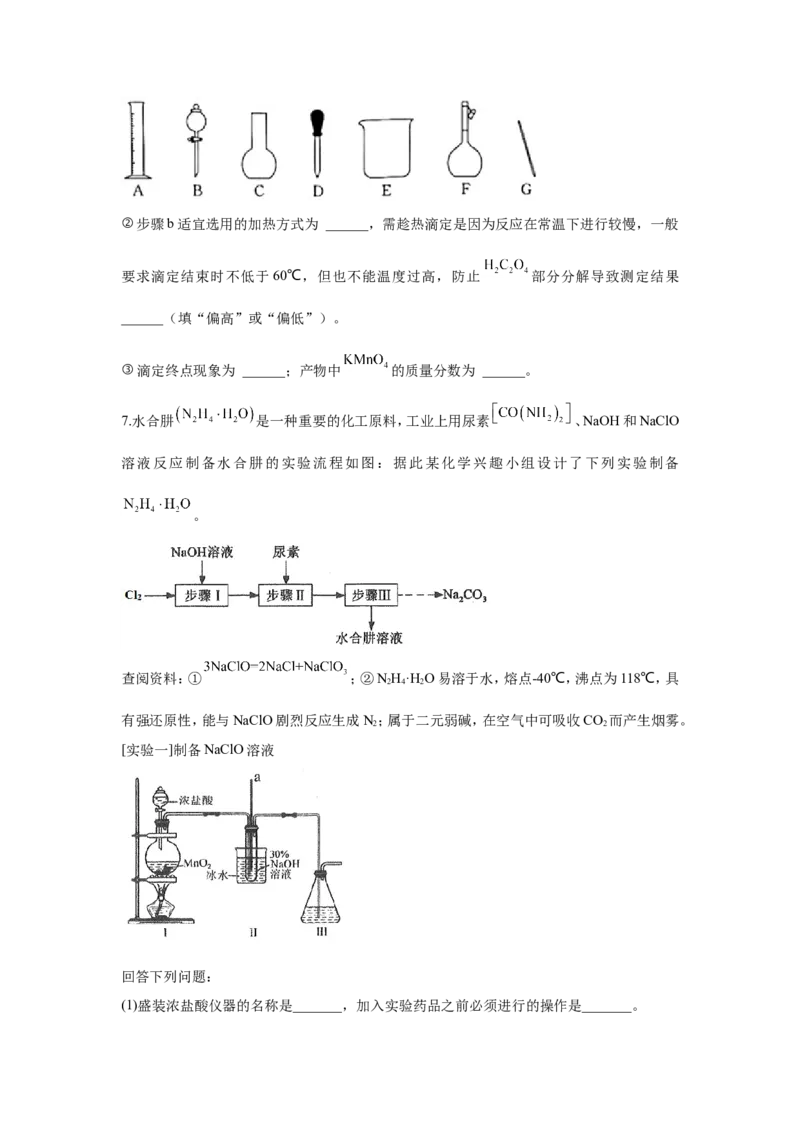
①配制 样品溶液时,下列玻璃仪器中不需要的有 ______(填序号)。②步骤b适宜选用的加热方式为 ______,需趁热滴定是因为反应在常温下进行较慢,一般
要求滴定结束时不低于60℃,但也不能温度过高,防止 部分分解导致测定结果
______(填“偏高”或“偏低”)。
③滴定终点现象为 ______;产物中 的质量分数为 ______。
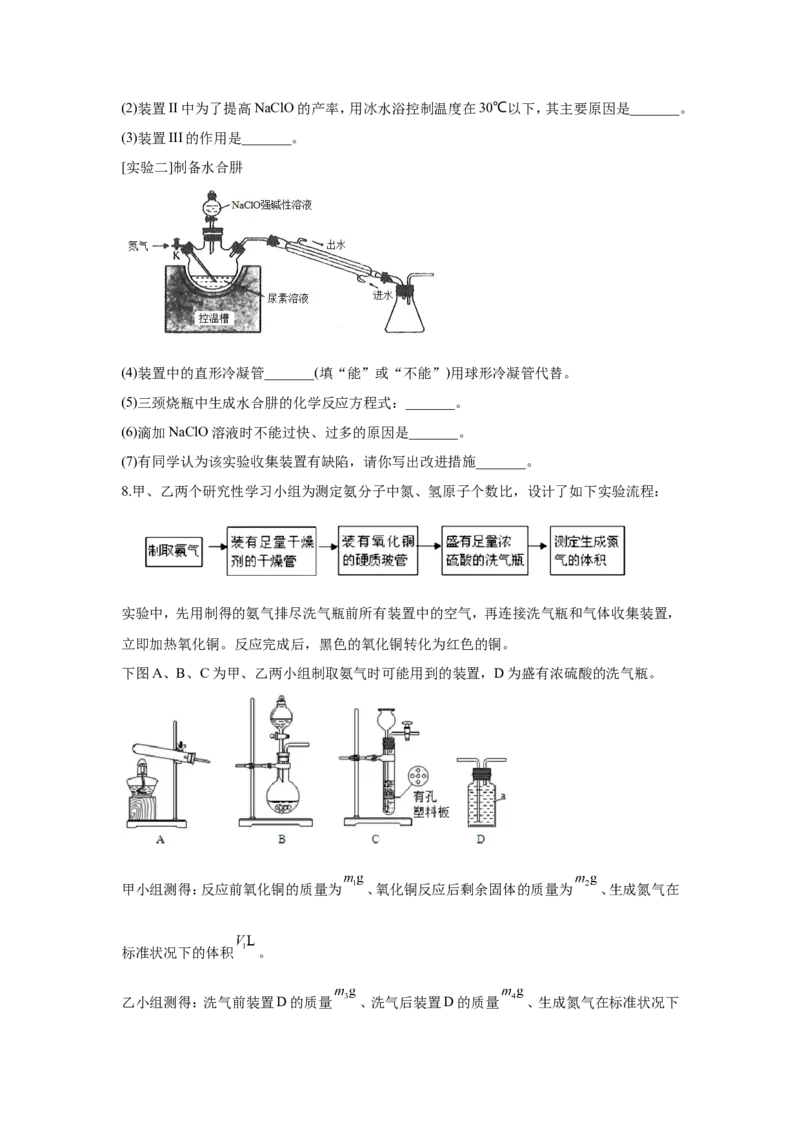
7.水合肼 是一种重要的化工原料,工业上用尿素 、NaOH和NaClO
溶液反应制备水合肼的实验流程如图:据此某化学兴趣小组设计了下列实验制备
。
查阅资料:① ;②NH·H O易溶于水,熔点-40℃,沸点为118℃,具
2 4 2
有强还原性,能与NaClO剧烈反应生成N;属于二元弱碱,在空气中可吸收CO 而产生烟雾。
2 2
[实验一]制备NaClO溶液
回答下列问题:
(1)盛装浓盐酸仪器的名称是_______,加入实验药品之前必须进行的操作是_______。(2)装置II中为了提高NaClO的产率,用冰水浴控制温度在30℃以下,其主要原因是_______。
(3)装置III的作用是_______。
[实验二]制备水合肼
(4)装置中的直形冷凝管_______(填“能”或“不能”)用球形冷凝管代替。
(5)三颈烧瓶中生成水合肼的化学反应方程式:_______。
(6)滴加NaClO溶液时不能过快、过多的原因是_______。
(7)有同学认为该实验收集装置有缺陷,请你写出改进措施_______。
8.甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设计了如下实验流程:
实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,
立即加热氧化铜。反应完成后,黑色的氧化铜转化为红色的铜。
下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
甲小组测得:反应前氧化铜的质量为 、氧化铜反应后剩余固体的质量为 、生成氮气在
标准状况下的体积 。
乙小组测得:洗气前装置D的质量 、洗气后装置D的质量 、生成氮气在标准状况下的体积 。
请回答下列问题:
(1)写出仪器a的名称:__________________________________。
(2)检查A装置气密性的操作是:___________________________________________。
(3)甲、乙两小组选择了不同方法制取氨气,请将实验装置的字母编号和制备原理填写在下
表空格中。
实验装置 实验药品 制备原理
反应的化学方程式为
甲小组 A 氢氧化钙、硫酸铵 ______________
用化学平衡原理分析氢氧化钠的作
乙小组 _____ 浓氨水、氢氧化钠
用:_________________
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为____________________。
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是
_______________________________ 。为此,乙小组在原有实验的基础上增加了一个装有药
品的实验仪器,重新实验.根据实验前后该药品的质量变化及生成氮气的体积,得出合理的实
验结果。该药品的名称是____________________________。答案
1.答案:(1) [或 ];蒸发浓缩过程中 挥发,使平衡
向右移动, 发生水解生成 或
(2)乙醇
(3)①AC②B
解析:(1)本题考查物质的合成路线,涉及物质的分离、实验的设计等。该方案存在明显缺陷,
因为得到的产物晶体中往往含有 或 杂质,因为在蒸发浓缩过程中
挥发,使平衡 向右移动, 发生水解生成
。
(2)根据题给信息②可知,加入的试剂应为乙醇。
(3)①减压过滤可加快过滤速度,并使沉淀比较干燥,因为胶状沉淀易穿透滤纸,沉淀颗粒太
小易在滤纸上形成一层密实的沉淀,溶液不易透过,所以减压过滤不宜过滤胶状沉淀和颗粒
太小的沉淀,A、C项正确;② 晶体易溶于水,难溶于乙醇等,所以可选
用乙醇和水的混合液,不能选用蒸馏水:若用饱和硫酸铵溶液洗涤,则会在
晶体表面残留有硫酸铵杂质,达不到洗涤的目的。
2.答案:(1) 溶液;溶液显紫色
(2)① ;a、b;②减少环己醇蒸出
(3)分液漏斗、烧杯
(4)通冷凝水,加热
(5)淀粉溶液;(6)b、c
解析:本题考查环己烯的制备、提纯及含量测定,考查的核心素养是科学探究与剑新意识。
(1)利用苯酚遇 溶液显紫色,检验环己醇中含有的苯酚。
(2)①烧瓶A中进行的可逆反应为 。a项,浓硫酸易使原料炭
化并产生 ,会降低原料利用率,正确;b项,使用 不产生有毒气体,污染小,
可以循环使用,符合绿色化学理念,正确;C项,同等条件下,浓硫酸能吸收反应生成的水,促
进反应向右进行,故用浓硫酸比用 的平衡转化率高,错误。②仪器B的作用为冷
凝回流,减少环己醇蒸出。
(3)操作2得到有机相和水相,为分液操作,用到的玻璃仪器有分液漏斗、烧杯。
(4)蒸馏实验开始时,先通冷凝水,后加热。
(5)达到滴定终点时,单质碘完全被消耗,可用淀粉溶液作指示剂。根据测定过程中发生的反
应 可 知 , , 则
,故样品中环己烯的质量分数为
。
(6)a项,样品中含有苯酚杂质,苯酚能与溴反应,会导致样品消耗的 偏多,剩余的 偏少,
最终消耗的 溶液偏少,测定结果偏高,错误;b项,在测定过程中部分环己烯挥发,
会导致样品消耗的B,偏少,剩余的 偏多,最终消耗的 溶液偏多,测定结果偏低,
正确;c项, 标准溶液部分被氧化,最终消耗的 溶液偏多,测定结果偏低,
正确。
3. 答 案 : ( 1 ) ① 直 形 冷 凝 管 ; 完 全 吸 收 氨 气 ; ② 防 止 倒 吸 ; ③
;④AB
(2)①加入 溶液调整待测液的 pH 为 8~9,加入淀粉溶液作指示剂,用溶液进行滴定,当滴入最后一滴 溶液,蓝色恰好褪去,且半
分钟内不恢复原色时;② ;③
解析:(1)①由题图2可知,仪器B为直形冷凝管。将细导管插入吸收液中是为了充分将氨气
吸收。②氨气被吸收后,会造成很大的负压,蒸馏烧瓶比C中吸收液的液面高出很多可防止
倒 吸 。 ③ 依 题 意 可 知 反 应 生 成 了 氨 气 和 氧 化 铜 , 反 应 的 化 学 方 程 式 为
。④充分反应
后,C中为 和HCl的混合溶液,溶液呈酸性,酚酞的pH指示范围为8.2~10.0,则滴定
时消耗的氢氧化钠用量偏多,计算出的吸收氨气的盐酸量偏少,导致计算出的 的含量偏
小。A中加热时间过短,氨气未完全逸出,导致 的含量的测定结果偏小。滴定前未将冲洗
细导管末端的清洗液加入C中,导致滴定时氢氧化钠用量偏少,则计算出的吸收氨气的盐酸
量偏多,导致 的含量的测定结果偏大。
(2)①依题意知,加入KI固体后发生反应 ,通过测定生成的 的
量,可间接计算 的量。因常温下 在pH为8~9时能稳定存在,pH<8时会发生歧
化反应,故在滴定前需要先用 溶液调整待测液的pH为8~9,滴定时,需加入淀粉溶
液作指示剂,然后用 溶液进行滴定,当滴入最后一滴 溶液,
蓝色恰好褪去,且半分钟内不恢复原色时,读取消耗的 溶液的体积。②由和 可 得 , 故
。 ③ 由 分 析 可 得
, 故
, 根 据 为 0.4622g 可 得 ,
,故该晶体的化学式为
。
4.答案:(1)离子
(2)N(氮);气液逆向吸收,使硝酸与 充分反应
(3)1:1
(4)①偏小; 被空气中的氧气氧化;②86.25%
(5)
5.答案:(1)①打开;打开;关闭;②
(2)草酸盐水解呈碱性,使得 易被氧气氧化,降低水合草酸亚铁的产率(合理即可) ;
(3)过滤;洗涤;KSCN溶液(或硫氰化钾溶液)
(4)FeO解析:(1)①要使A中制得的 溶液进入B中发生反应,应打开分液漏斗的活塞,使装置
内产生氢气,压强增大,将A中溶液压入B中,同时打开 、关闭 。②亚铁离子需和
反应生成 。
(2)由信息可知pH>4时, 易被 氧化,而草酸盐溶液水解显碱性,使得 易被氧气
氧化,选用草酸的目的是增强溶液酸性,防止 被 氧化;涉及方程式为
。
(3)KSCN溶液可用于检验亚铁离子是否被氧化成三价铁离子。
(4)由400℃时的固体质量可知质量减少了0.6g,剩下固体质量为0.4g,且1g
为 ,失去水的质量为0.2g,则剩下固体为 分解的产物, FeO的质量为
0.4g,故推测可得固体为FeO。
6.答案:(1)C
(2)KOH
(3)蒸发浓缩;冷却结晶
(4)ABC;水浴加热;偏高;最后一滴高锰酸钾溶液滴入锥形瓶,溶液由无色变为粉红色,且半
分钟不褪色;63.2%
7.答案:分液漏斗;检查装置气密性 ;防止温度高,使NaClO分解 ;吸收尾气,防止污染空气;
不能; ;防止水合肼被NaClO氧化 ;
在锥形瓶导管上连接装有碱石灰的干燥管,防止空气中二氧化碳进入收集装置
解析:(1)分析装置图可知,盛放浓盐酸的仪器为分液漏斗,加入实验药品之前必须进行的操
作是检查装置气密性,故答案为:分液漏斗;检查装置气密性(2)I中用冰水浴控制温度在30℃以下,其主要目的是:防止NaClO分解为NaCl和 ,影响水合肼的产率,故答案
为:防止NaClO分解为NaCl和 ,影响水合肼的产率;
(3)应可能会造成氯气逸出,污染空气,故装置II进行尾气处理故答案为:吸收尾气,防止污
染空气
(4)蒸馏过程中如果使用球形冷凝管,会造成产品残余在球形冷凝管的球状结构内,造成损
失,故答案为:不能
( 5 ) 在 恒 温 控 制 下 次 氯 酸 钠 与 尿 素 反 应 生 成 , 方 程 式 为
故 答 案 为 :
(6)如果滴加NaClO溶液过快,会发生副反应 ,
故答案为:发生副反应 ;
(7)属于二元弱碱,在空气中可吸收 而产生烟雾,故应连接一个干燥管除去空气中的二
氧化碳,防止二氧化碳进入到收集装置;故答案为:连接一个千燥管除去空气中的二氧化碳,
防止二氧化碳进入到收集装置
8.答案:(1) 圆底烧瓶
(2)连接导管,将导管插入水中;用手紧握试管或加热试管,导管口有气泡产生;松开手后或
停止加热,导管内有水回流并形成一段稳定的水柱
(3)(NH )SO +Ca(OH) 2NH ↑+2HO+CaSO B 氢氧化钠溶于氨水后放热、增加
4 2 4 2 3 2 4
氢氧根浓度,使NH +HO NH ·H O +OH-向逆方向移动,加快氨气逸出
3 2 3 2(4)5V:[7(m-m)]
1 1 2
(5)洗气瓶D中的浓硫酸不但吸收了反应生成的水,还吸收了未反应的氨气,从而使计算的
氢的量偏高; 碱石灰(氢氧化钠、氧化钙等)
解析:(1)仪器a的名称:圆底烧瓶;
(2)检查A装置气密性的操作是:连接导管,将导管插入水中;用手紧握试管或微微加热试管,
导管口有气泡产生;松开手后或停止加热,导管内有水回流并形成一段稳定的水柱,说明装
置A气密性良好;
(3)
实验
实验药品 制备原理
装置
氢氧化钙、 反应的化学方程式为(NH )SO +Ca(OH) 2NH ↑+
甲小组 A 4 2 4 2 3
硫酸铵 2HO+CaSO
2 4
用化学平衡原理分析氢氧化钠的作用:氢氧化钠溶于氨水后
浓氨水、氢
乙小组 B 放热、增加氢氧根浓度,使NH +HO NH ·H O
氧化钠 3 2 3 2
+ 向逆方向移动,加快氨气逸出
(4)(m-m)g为CuO中O的质量,NH 中H的物质的量为[(m -m )/16] ×2=[(m -
1 2 3 1 2 1
m)/8]mol,NH 中N的物质的量为(V/22.4)mol×2=(V/11.2)mol,所以氨分子中氮、氢的原子
2 3 1 1
个数之比为(V/11.2):[(m-m)/8]=5V:7(m-m)。
1 1 2 1 1 2
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是洗气
瓶D中的浓硫酸不但吸收了反应生成的水,还吸收了未反应的氨气,从而使计算的氢的量偏
高。为此,乙小组在原有实验的基础上增加了一个装有药品的实验仪器,重新实验。根据实验
前后该药品的质量变化及生成氮气的体积,得出合理的实验结果。该药品的名称是碱石灰
(氢氧化钠、氧化钙等)。