文档内容
2023届高考化学一轮强化训练题:物质结构与性质
1.(2022·湖南·新宁县第一中学高三期中)以 、 和 为主要成分的镀液可在某些材料
上镀铜,原理如下:
(1)基态 原子的价层电子排布式为_______。
(2)根据反应原理分析
①镀铜反应中,利用了 的_______性。
②选择 进行化学镀铜的原因之一是它易溶于水。下列分析正确的是_______
a. 、 均属于极性分子
b. 与 之间能形成氢键
c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的 、 、 三种微粒,空间结构为三角形的是_______。
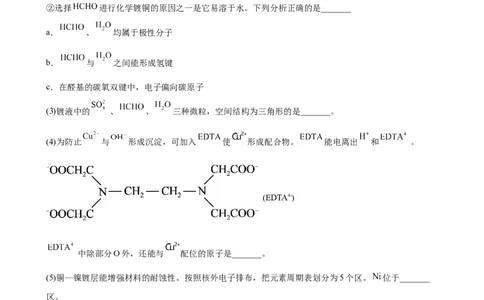
(4)为防止 与 形成沉淀,可加入 使 形成配合物。 能电离出 和 。
(EDTA4-)
中除部分O外,还能与 配位的原子是_______。
(5)铜—镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。 位于_______
区。
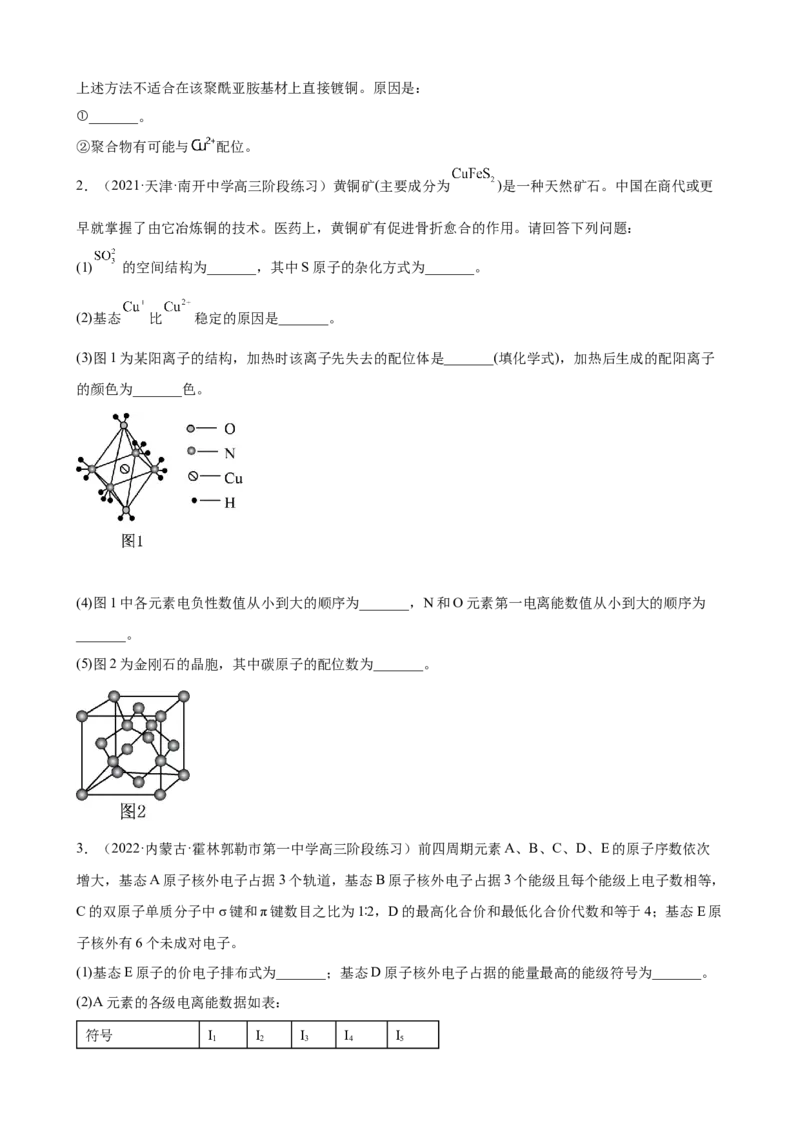
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:上述方法不适合在该聚酰亚胺基材上直接镀铜。原因是:
①_______。
②聚合物有可能与 配位。
2.(2021·天津·南开中学高三阶段练习)黄铜矿(主要成分为 )是一种天然矿石。中国在商代或更
早就掌握了由它冶炼铜的技术。医药上,黄铜矿有促进骨折愈合的作用。请回答下列问题:
(1) 的空间结构为_______,其中S原子的杂化方式为_______。
(2)基态 比 稳定的原因是_______。
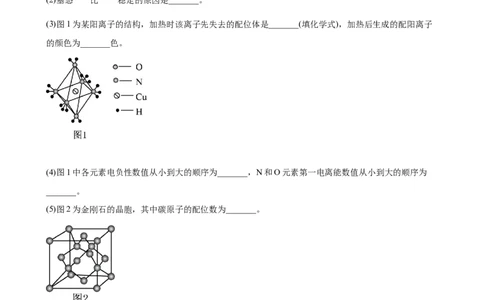
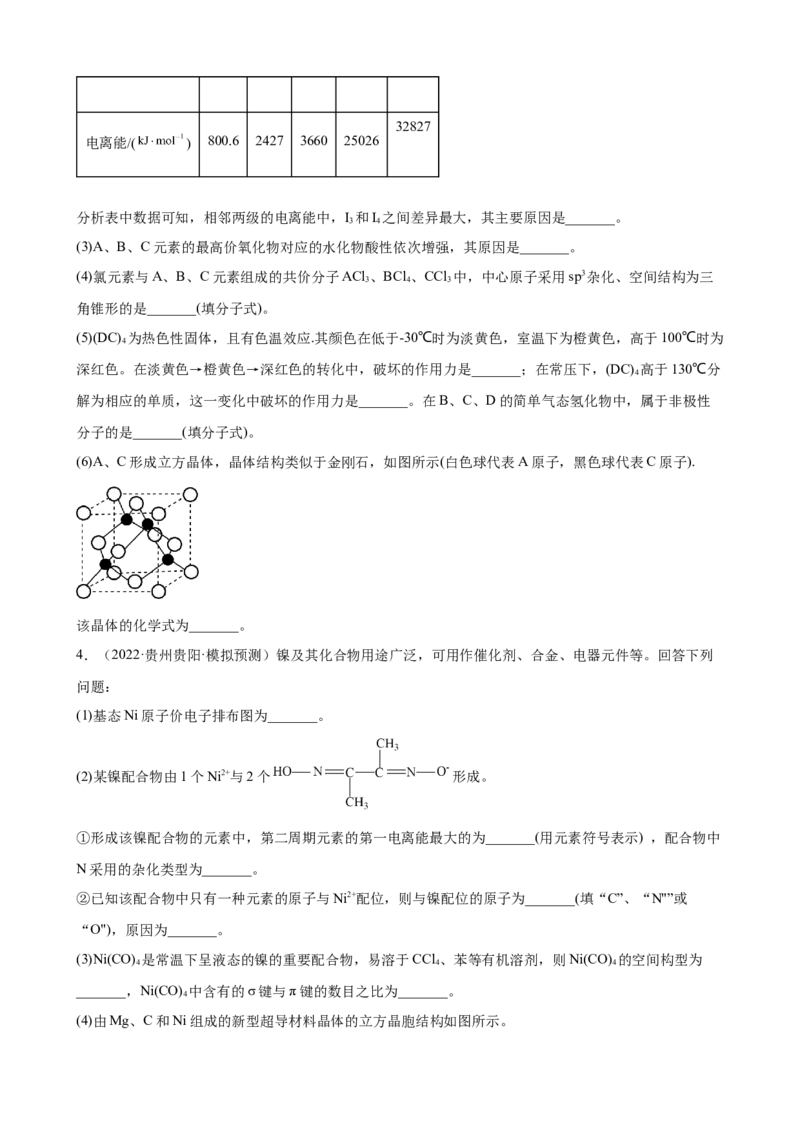
(3)图1为某阳离子的结构,加热时该离子先失去的配位体是_______(填化学式),加热后生成的配阳离子
的颜色为_______色。
(4)图1中各元素电负性数值从小到大的顺序为_______,N和O元素第一电离能数值从小到大的顺序为
_______。
(5)图2为金刚石的晶胞,其中碳原子的配位数为_______。
3.(2022·内蒙古·霍林郭勒市第一中学高三阶段练习)前四周期元素A、B、C、D、E的原子序数依次
增大,基态A原子核外电子占据3个轨道,基态B原子核外电子占据3个能级且每个能级上电子数相等,
C的双原子单质分子中σ键和π键数目之比为1∶2,D的最高化合价和最低化合价代数和等于4;基态E原
子核外有6个未成对电子。
(1)基态E原子的价电子排布式为_______;基态D原子核外电子占据的能量最高的能级符号为_______。
(2)A元素的各级电离能数据如表:
符号 I I I I I
1 2 3 4 532827
电离能/( ) 800.6 2427 3660 25026
分析表中数据可知,相邻两级的电离能中,I 和I 之间差异最大,其主要原因是_______。
3 4
(3)A、B、C元素的最高价氧化物对应的水化物酸性依次增强,其原因是_______。
(4)氯元素与A、B、C元素组成的共价分子ACl 、BCl 、CCl 中,中心原子采用sp3杂化、空间结构为三
3 4 3
角锥形的是_______(填分子式)。
(5)(DC) 为热色性固体,且有色温效应.其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为
4
深红色。在淡黄色→橙黄色→深红色的转化中,破坏的作用力是_______;在常压下,(DC) 高于130℃分
4
解为相应的单质,这一变化中破坏的作用力是_______。在B、C、D的简单气态氢化物中,属于非极性
分子的是_______(填分子式)。
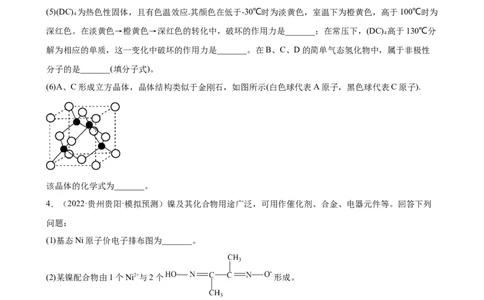
(6)A、C形成立方晶体,晶体结构类似于金刚石,如图所示(白色球代表A原子,黑色球代表C原子).
该晶体的化学式为_______。
4.(2022·贵州贵阳·模拟预测)镍及其化合物用途广泛,可用作催化剂、合金、电器元件等。回答下列
问题:
(1)基态Ni原子价电子排布图为_______。
(2)某镍配合物由1个Ni2+与2个 形成。
①形成该镍配合物的元素中,第二周期元素的第一电离能最大的为_______(用元素符号表示) ,配合物中
N采用的杂化类型为_______。
②已知该配合物中只有一种元素的原子与Ni2+配位,则与镍配位的原子为_______(填“C”、“N"”或
“O"),原因为_______。
(3)Ni(CO) 是常温下呈液态的镍的重要配合物,易溶于CCl 、苯等有机溶剂,则Ni(CO) 的空间构型为
4 4 4
_______,Ni(CO) 中含有的σ键与π键的数目之比为_______。
4
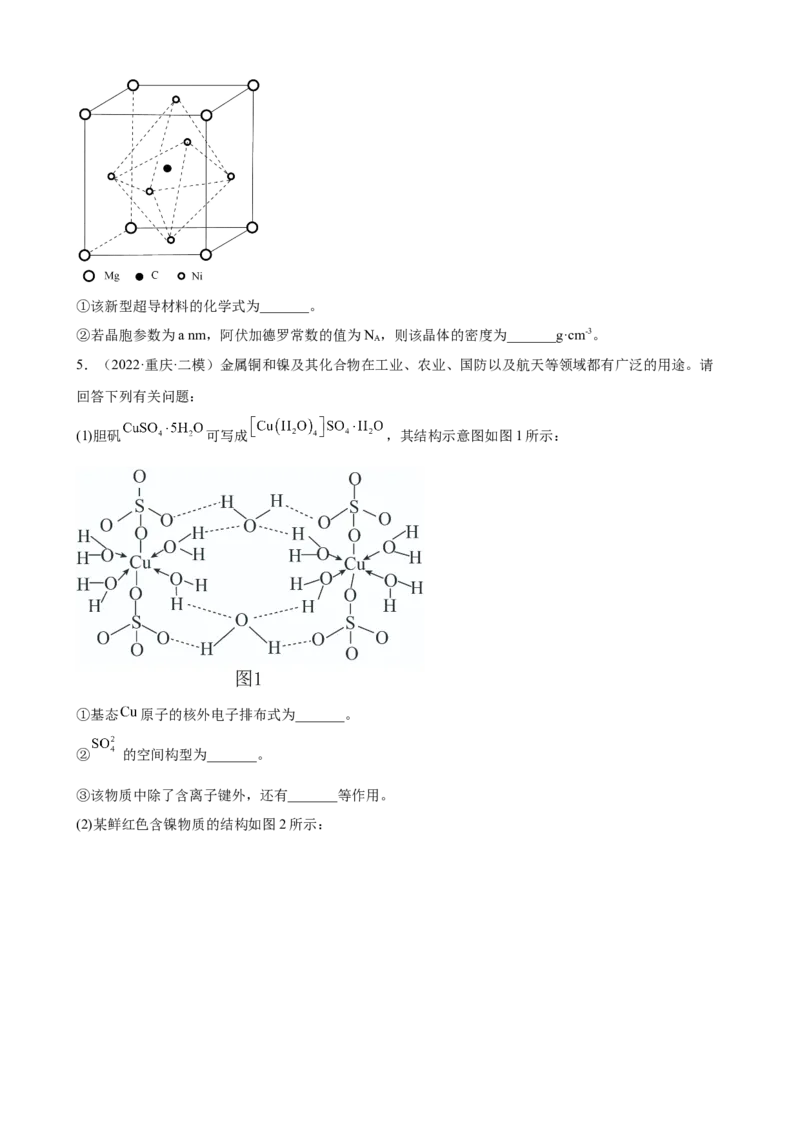
(4)由Mg、C和Ni组成的新型超导材料晶体的立方晶胞结构如图所示。①该新型超导材料的化学式为_______。
②若晶胞参数为a nm,阿伏加德罗常数的值为N ,则该晶体的密度为_______g·cm-3。
A
5.(2022·重庆·二模)金属铜和镍及其化合物在工业、农业、国防以及航天等领域都有广泛的用途。请
回答下列有关问题:
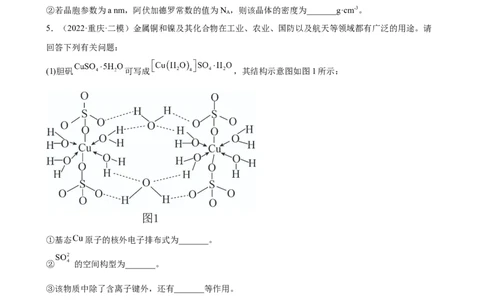
(1)胆矾 可写成 ,其结构示意图如图1所示:
①基态 原子的核外电子排布式为_______。
② 的空间构型为_______。
③该物质中除了含离子键外,还有_______等作用。
(2)某鲜红色含镍物质的结构如图2所示:①图中非金属元素的电负性由大到小的顺序为_______(填元素符号)。
②该物质中C原子的杂化轨道类型是_______。
(3)镍和铜的第二电离能分别为 、 。则 _______ (填“>”“<”或“=”),其原因是_______。
(4)已知氧化镍的晶胞结构如图3所示:
①某缺陷氧化镍的组成为 ,其中 元素只有 和 两种价态,则 和 两种价态的镍离子数之
比为_______。
②若该晶体无缺陷,其密度为 ,晶胞中最近的 之间的距离为 ,则阿伏加德罗常数
_______(用含 、a的代数式表示)。
6.(2022·广广州东·高三阶段练习)前四周期原子序数依次增大的元素a、b、c、d中,a和b的价电子
层中未成对电子均只有1个,并且a-和b+的电子数相差8;c和d与b位于同一周期,c和d的价电子层中
的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:
(1)a元素在元素周期表中的位置是____,属于____区。
(2)基态b原子中,电子占据最高能层的符号是____,基态b+占据的最高能级共有____个原子轨道。
(3)d元素基态原子的简化电子排布式为____。
(4)a、b、c、d四种元素中,电负性最大的为____(填元素符号)。(5)Mn和c两种元素的部分电离能数据如表所示:
电离能/(kJ·mol-1)
元素
I I I
1 2 3
c元素 759 1561 2957
Mn元素 717 1509 3248
比较两元素的I、I 可知,气态Mn2+再失去一个电子比气态c2+再失去一个电子更难,原因是____。
2 3
7.(2022·广东东莞·模拟预测)“金属钯催化的交叉偶联反响研究”曾获得过诺贝尔化学奖。钯位于元
素周期表中第VIII族,与铑(Rh)、铂(Pt)等元素统称为铂系元素,在工业及军事技术上发挥关键作用。
(1)Pd位于第五周期,与镍相邻,其基态原子价电子排布式为4d10。下列Pd的价电子排布图中能量最低的
是_______(填选项字母)。
A. B.
C. D.
(2)已知:2CH=CH +O 2CHCHO。
2 2 2 3
①CH=CH 中含有3种不同的共价键,除了C(sp2杂化轨道)-H(s轨道)形成的σ键外,还含有C(sp2杂化轨
2 2
道)-C(sp2杂化轨道)形成的σ键和_______形成的π键;CHCHO中碳原子的杂化方式为_______。
3
②不同温度下PdCl 的结构不同,α-PdCl 为无限的平面形长链,其结构如图(a)所示,则Pd(II)的配位数为
2 2
_______。β-PdCl 为团簇分子,其结构如图(b)所示,则其化学式为_______。
2
(3)铂与卤离子也可以形成稳定的配离子,已知配离子[Pt(II )Cl ]2-、[Pt( II )Br ]2-、[Pt(II)I ]2-的稳定性依次
4 4 4
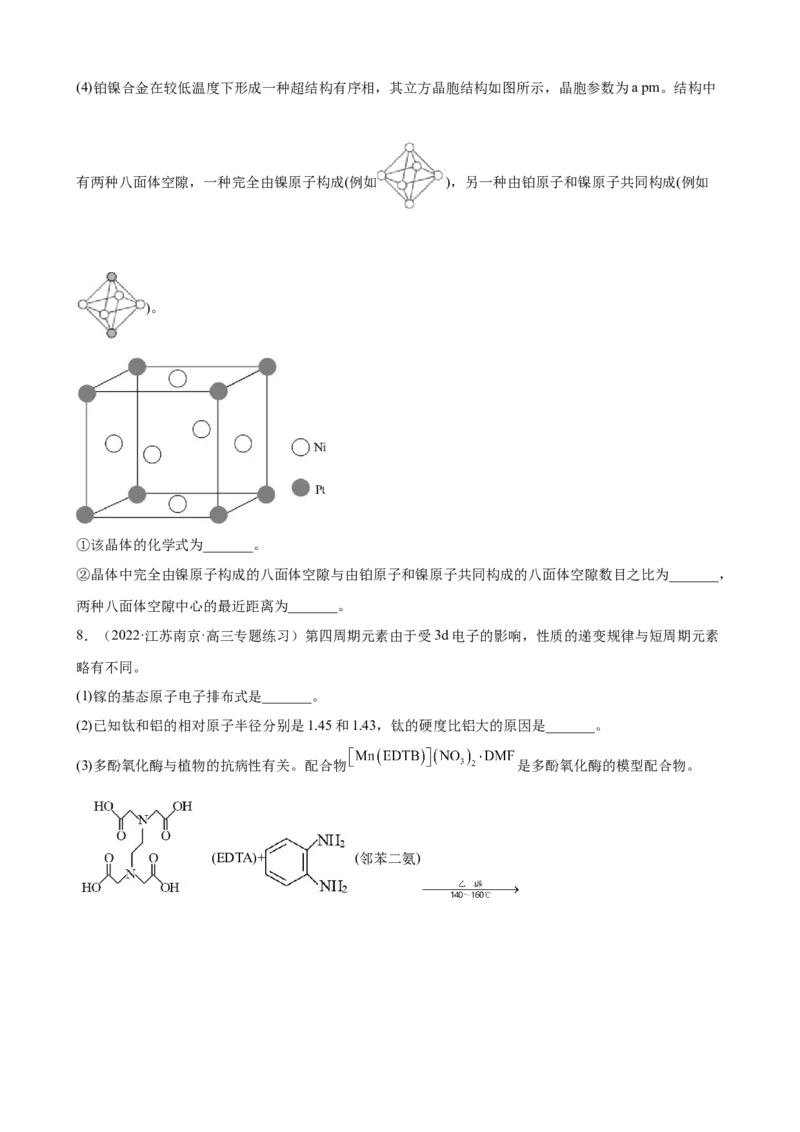
增强,其可能原因是_______。(4)铂镍合金在较低温度下形成一种超结构有序相,其立方晶胞结构如图所示,晶胞参数为a pm。结构中
有两种八面体空隙,一种完全由镍原子构成(例如 ),另一种由铂原子和镍原子共同构成(例如
)。
①该晶体的化学式为_______。
②晶体中完全由镍原子构成的八面体空隙与由铂原子和镍原子共同构成的八面体空隙数目之比为_______,
两种八面体空隙中心的最近距离为_______。
8.(2022·江苏南京·高三专题练习)第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素
略有不同。
(1)镓的基态原子电子排布式是_______。
(2)已知钛和铝的相对原子半径分别是1.45和1.43,钛的硬度比铝大的原因是_______。
(3)多酚氧化酶与植物的抗病性有关。配合物 是多酚氧化酶的模型配合物。
(EDTA)+ (邻苯二氨)(EDTB)
①EDTA中N的杂化轨道类型为_______。
②邻苯二胺分子中 键的数目为_______。
③EDTB分子中所含元素的电负性由小到大的顺序为_______。
④与 互为等电子体的一种阴离子为_______。
⑤配离子 中的配位原子是_______。
(4)向盛有硫酸铜水溶液的试管中加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解,得到深蓝色
透明溶液,向该溶液中加入乙醇,析出深蓝色晶体。蓝色沉淀先溶解、后析出的原因是(用离子方程式和
简单的文字说明加以解释):_______。
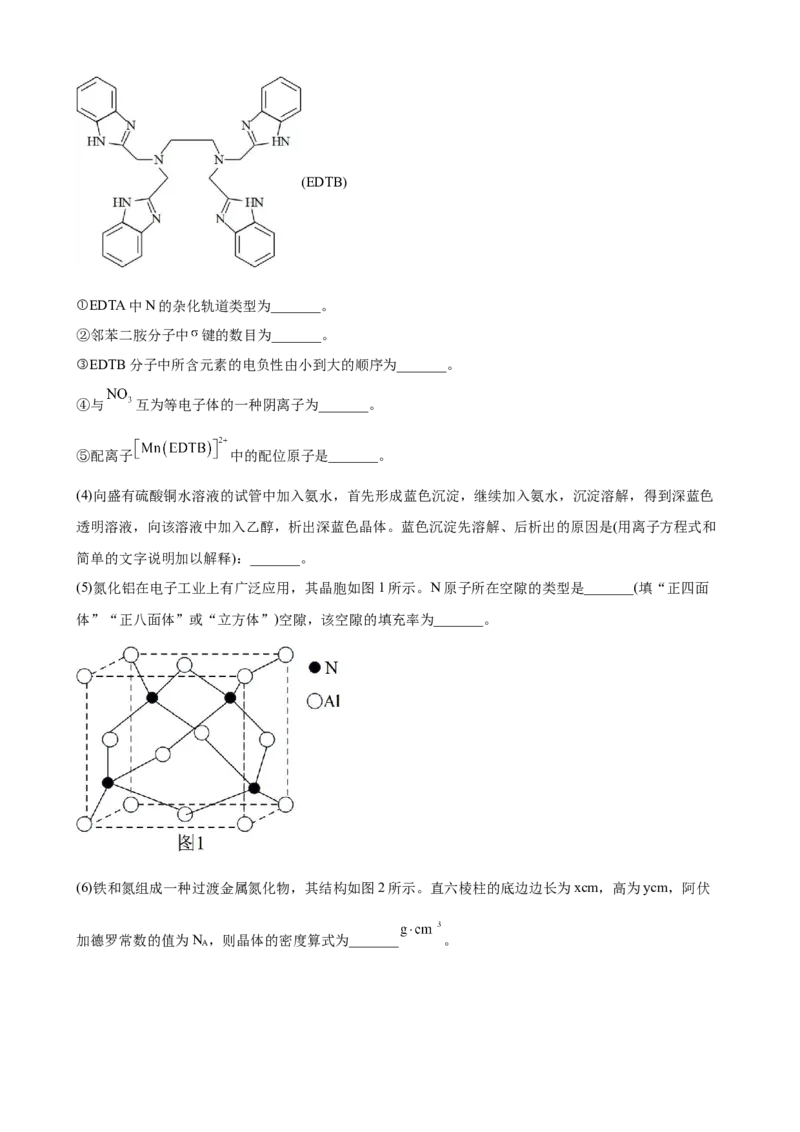
(5)氮化铝在电子工业上有广泛应用,其晶胞如图1所示。N原子所在空隙的类型是_______(填“正四面
体”“正八面体”或“立方体”)空隙,该空隙的填充率为_______。
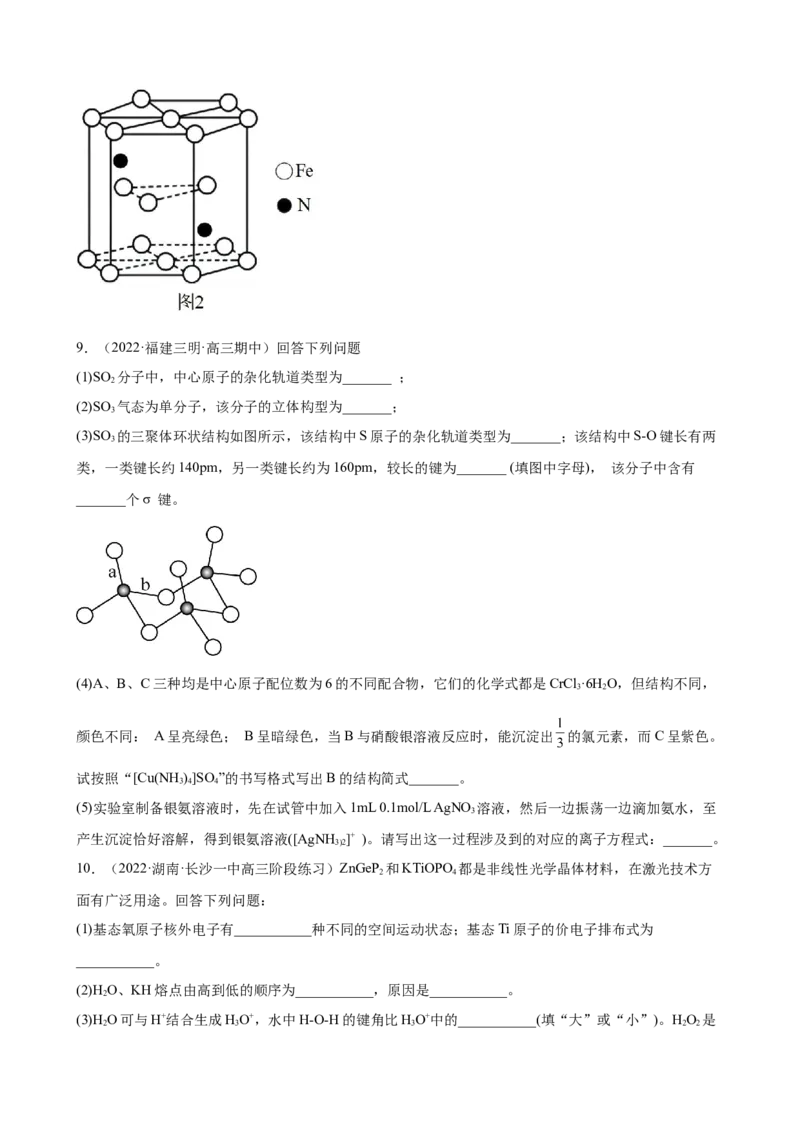
(6)铁和氮组成一种过渡金属氮化物,其结构如图2所示。直六棱柱的底边边长为xcm,高为ycm,阿伏
加德罗常数的值为N ,则晶体的密度算式为_______ 。
A9.(2022·福建三明·高三期中)回答下列问题
(1)SO 分子中,中心原子的杂化轨道类型为_______ ;
2
(2)SO 气态为单分子,该分子的立体构型为_______;
3
(3)SO 的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为_______;该结构中S-O键长有两
3
类,一类键长约140pm,另一类键长约为160pm,较长的键为_______ (填图中字母), 该分子中含有
_______个σ 键。
(4)A、B、C三种均是中心原子配位数为6的不同配合物,它们的化学式都是CrCl ·6H O,但结构不同,
3 2
颜色不同: A呈亮绿色; B呈暗绿色,当B与硝酸银溶液反应时,能沉淀出 的氯元素,而C呈紫色。
试按照“[Cu(NH )]SO ”的书写格式写出B的结构简式_______。
3 4 4
(5)实验室制备银氨溶液时,先在试管中加入1mL 0.1mol/L AgNO 溶液,然后一边振荡一边滴加氨水,至
3
产生沉淀恰好溶解,得到银氨溶液([AgNH ]+ )。请写出这一过程涉及到的对应的离子方程式:_______。
3)2
10.(2022·湖南·长沙一中高三阶段练习)ZnGeP 和KTiOPO 都是非线性光学晶体材料,在激光技术方
2 4
面有广泛用途。回答下列问题:
(1)基态氧原子核外电子有___________种不同的空间运动状态;基态Ti原子的价电子排布式为
___________。
(2)H O、KH熔点由高到低的顺序为___________,原因是___________。
2
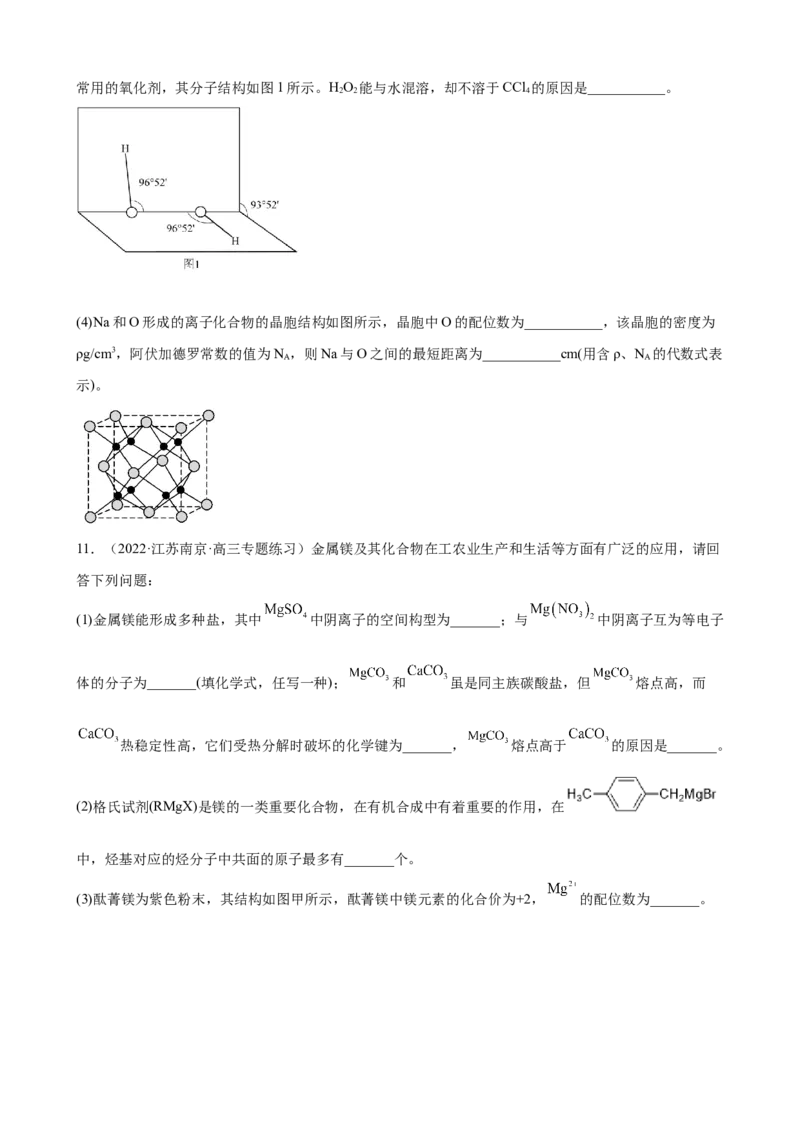
(3)H O可与H+结合生成HO+,水中H-O-H的键角比HO+中的___________(填“大”或“小”)。HO 是
2 3 3 2 2常用的氧化剂,其分子结构如图1所示。HO 能与水混溶,却不溶于CCl 的原因是___________。
2 2 4
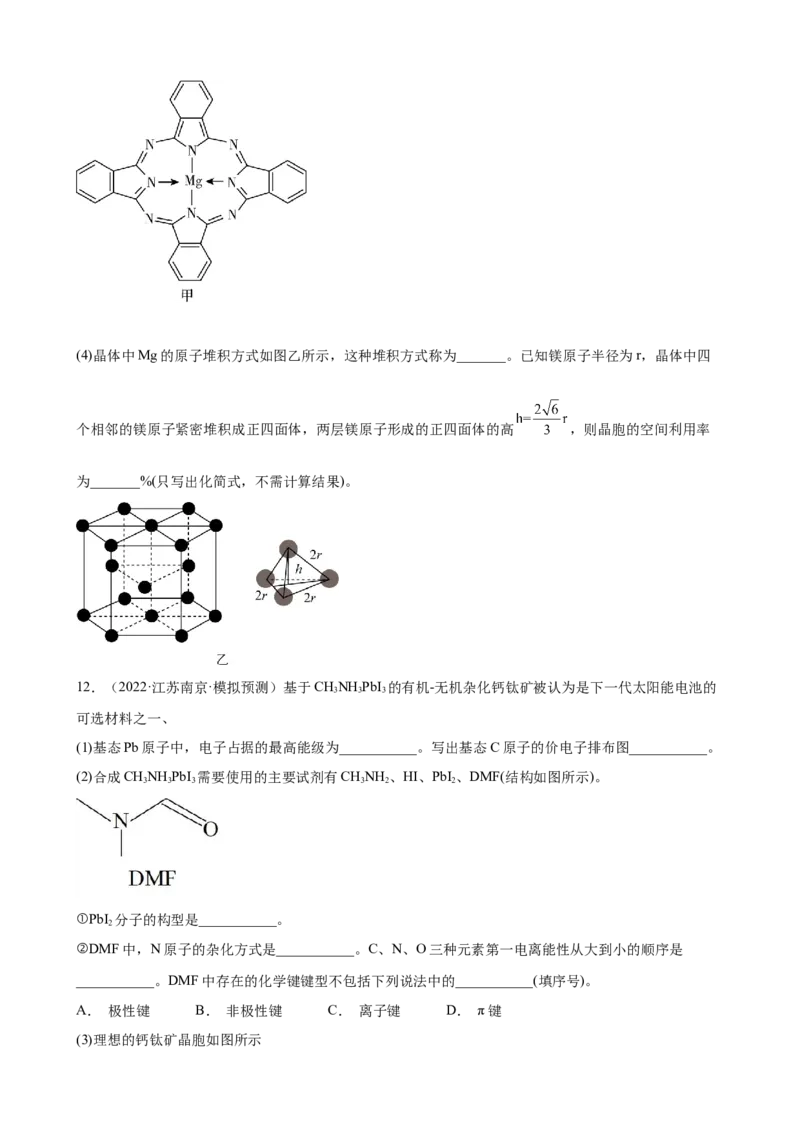
(4)Na和O形成的离子化合物的晶胞结构如图所示,晶胞中O的配位数为___________,该晶胞的密度为
ρg/cm3,阿伏加德罗常数的值为N ,则Na与O之间的最短距离为___________cm(用含ρ、N 的代数式表
A A
示)。
11.(2022·江苏南京·高三专题练习)金属镁及其化合物在工农业生产和生活等方面有广泛的应用,请回
答下列问题:
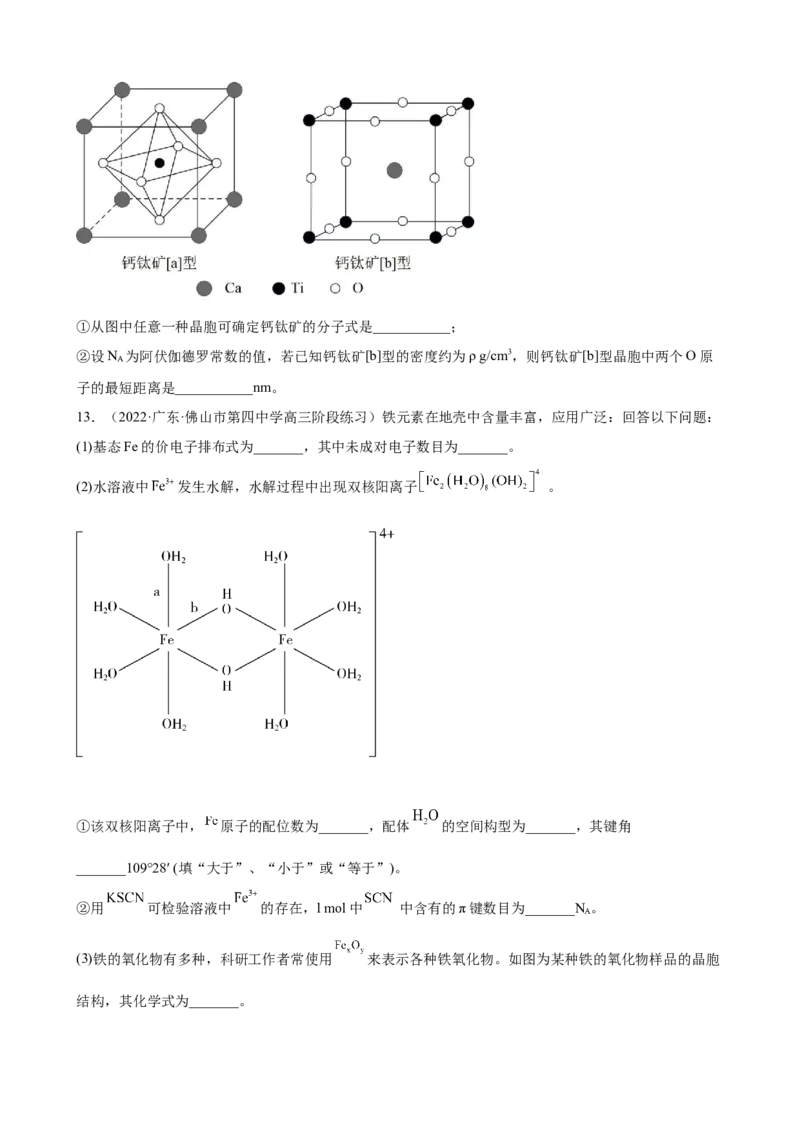
(1)金属镁能形成多种盐,其中 中阴离子的空间构型为_______;与 中阴离子互为等电子
体的分子为_______(填化学式,任写一种); 和 虽是同主族碳酸盐,但 熔点高,而
热稳定性高,它们受热分解时破坏的化学键为_______, 熔点高于 的原因是_______。
(2)格氏试剂(RMgX)是镁的一类重要化合物,在有机合成中有着重要的作用,在
中,烃基对应的烃分子中共面的原子最多有_______个。
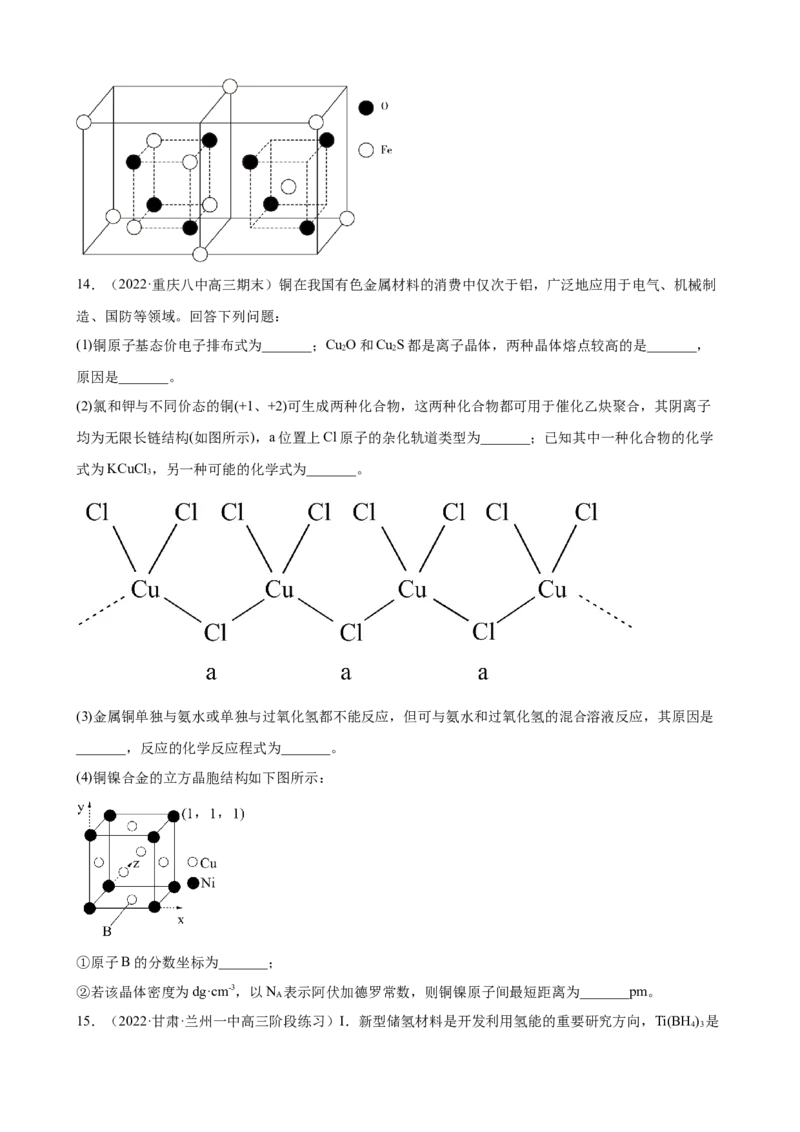
(3)酞菁镁为紫色粉末,其结构如图甲所示,酞菁镁中镁元素的化合价为+2, 的配位数为_______。(4)晶体中Mg的原子堆积方式如图乙所示,这种堆积方式称为_______。已知镁原子半径为r,晶体中四
个相邻的镁原子紧密堆积成正四面体,两层镁原子形成的正四面体的高 ,则晶胞的空间利用率
为_______%(只写出化简式,不需计算结果)。
12.(2022·江苏南京·模拟预测)基于CHNH PbI 的有机-无机杂化钙钛矿被认为是下一代太阳能电池的
3 3 3
可选材料之一、
(1)基态Pb原子中,电子占据的最高能级为___________。写出基态C原子的价电子排布图___________。
(2)合成CHNH PbI 需要使用的主要试剂有CHNH 、HI、PbI 、DMF(结构如图所示)。
3 3 3 3 2 2
①PbI 分子的构型是___________。
2
②DMF中,N原子的杂化方式是___________。C、N、O三种元素第一电离能性从大到小的顺序是
___________。DMF中存在的化学键键型不包括下列说法中的___________(填序号)。
A. 极性键 B. 非极性键 C. 离子键 D. π键
(3)理想的钙钛矿晶胞如图所示①从图中任意一种晶胞可确定钙钛矿的分子式是___________;
②设N 为阿伏伽德罗常数的值,若已知钙钛矿[b]型的密度约为ρ g/cm3,则钙钛矿[b]型晶胞中两个O原
A
子的最短距离是___________nm。
13.(2022·广东·佛山市第四中学高三阶段练习)铁元素在地壳中含量丰富,应用广泛:回答以下问题:
(1)基态Fe的价电子排布式为_______,其中未成对电子数目为_______。
(2)水溶液中 发生水解,水解过程中出现双核阳离子 。
①该双核阳离子中, 原子的配位数为_______,配体 的空间构型为_______,其键角
_______109°28′ (填“大于”、“小于”或“等于”)。
②用 可检验溶液中 的存在,l mol中 中含有的π键数目为_______N 。
A
(3)铁的氧化物有多种,科研工作者常使用 来表示各种铁氧化物。如图为某种铁的氧化物样品的晶胞
结构,其化学式为_______。14.(2022·重庆八中高三期末)铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制
造、国防等领域。回答下列问题:
(1)铜原子基态价电子排布式为_______;Cu O和Cu S都是离子晶体,两种晶体熔点较高的是_______,
2 2
原因是_______。
(2)氯和钾与不同价态的铜(+1、+2)可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子
均为无限长链结构(如图所示),a位置上Cl原子的杂化轨道类型为_______;已知其中一种化合物的化学
式为KCuCl ,另一种可能的化学式为_______。
3
(3)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是
_______,反应的化学反应程式为_______。
(4)铜镍合金的立方晶胞结构如下图所示:
①原子B的分数坐标为_______;
②若该晶体密度为dg·cm-3,以N 表示阿伏加德罗常数,则铜镍原子间最短距离为_______pm。
A
15.(2022·甘肃·兰州一中高三阶段练习)I.新型储氢材料是开发利用氢能的重要研究方向,Ti(BH) 是
4 3一种储氢材料,可由LiBH 和TiCl 反应制得。
4 4
(1)基态Cl原子有_______种运动状态的电子,属于_______区(填“s”或“p”或“d”或“f”);
(2)LiBH 由Li+和 构成, 的立体结构是_______,与 互为等电子体的分子为_______,Li、
4
Be、B元素的第一电离能由大到小排列顺序为_______;
(3)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
I/kJ·mol-1 I/kJ·mol-1 I/kJ·mol-1 I/kJ·mol-1 I/kJ·mol-1
1 2 3 4 5
738 1451 7733 10540 13630
M是_______(填元素符号)。
II.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN )是一种弱酸,其分子结构可表示为H—
3
N=N≡N,肼(N H)被亚硝酸氧化时便可得到氢叠氮酸(HN ),发生的反应为:NH+HNO =2H O+HN HN
2 4 3 2 4 2 2 3。 3
的酸性和醋酸相近,可微弱电离出H+和 。试回答下列问题:
(4)下列有关说法正确的是_______(填序号);A.HN 中含有5个σ键
3
B.HN 中的三个氮原子均采用sp2杂化
3
C.HN 、HNO、HO、NH 都是极性分子
3 2 2 2 4
D.NH 沸点高达113.5℃,说明肼分子间可形成氢键
2 4
(5)叠氮酸根能与许多金属离子等形成配合物,如[Co(N )(NH )]SO ,在该配合物中钴显_______价;根据
3 3 5 4
价层电子对互斥理论判断 的空间构型为_______;
(6)与 互为等电子体的分子有_______(写两种即可)。
16.(2022·天津·南开中学高三阶段练习)氮、磷、砷、铁、钛等元素及其化合物在现代农业、科技和国
防建设中有着许多独特的用途。 是新型锂离子电池的电极材料,可采用 、 、
和苯胺等作为原料制备。
(1)基态P原子的价层电子排布图为_______,其基态原子核外电子共有_______种空间运动状态, 分
子的空间结构为_______。
(2) 中,除磷元素外,其余三种元素电负性由大到小的顺序是_______(填元素符号),N、P和S
第一电离能由大到小的顺序是_______(填元素符号)。(3)苯胺和甲苯相对分子质量接近,但苯胺熔点比甲苯的高,原因是_______。
(4)与 同族的 可形成一种化学式为 的配合物, 的内界中含
有 键的数目为_______(设 为阿代加德罗常数的值)。
(5)钙钛矿晶体的晶胞结构如图所示。若该晶体的密度为 ,阿伏加德罗常数的值为 ,则晶胞边
长 _______ (列出计算式,用 表示)。
17.(2022·湖北武汉·高三期中)2019年1月,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背
面的软着陆:也首次实现了我国地外天体采样返回;所搭载的“玉兔二号”月球车,通过砷化镓( )
太阳能电池提供能量进行工作。带回的月壤中包含了 等多
种元素。回答下列问题:
(1)基态 最高能层中成对电子与未成对电子的数目之比为_______。
(2) 的熔点为1238℃且熔融状态不导电,据此判断它是_______(填“共价”或“离子”)化合物。
(3)H和O可以形成 和 。 是_______(填“极性”或“非极性”)分子。
(4)砷化镓可由 和 在 制得, 中碳原子的杂化方式为_______。
(5)S与O可形成多种酸根离子及化合物,如 、 、 、 等,其中 的 模型是
_______; 的空间构型为_______。
(6) 催化烯烃硝化反应过程中会产生 。键角: _______ (填“>”或“<”)。
18.(2022·海南·文昌中学高三阶段练习)工业上采用还原法治炼黄金(Au)的原理如下:
4Au+O+8NaCN+2H O=4Na[Au(CN) ]+4NaOH
2 2 22Na[Au(CN) ]+Zn=2Au+Na Zn(CN)
2 2 4
请回答下列问题:
(1)在元素周期表中,Au与Cu位于同族,基态Au原子比基态Cu原子多2个电子层。基态Au原子的价层
电子排布式为____,金元素位于____区。
(2)Zn和Cu相邻,第一电离能:I(Cu)____I (Zn)(填“>”、“<”或“=”,下同),第二电离能:
1 1
I(Cu)____I (Zn)。
2 2
(3)1mol[Zn(CN) ]2-中含____molσ键。
4
(4)已知卤化锌的熔点如表所示:
卤化锌 ZnF ZnCl ZnBr ZnI
2 2 2 2
熔点/℃ 872 283 394 446
①ZnF 晶体所属的晶体类型为____。
2
②ZnCl ,ZnBr ,ZnI 的熔点递增的主要原因是____。
2 2 2
(5)通常情况下,金属Au单独与氧气或氰化钠溶液都不能反应,但该反应
4Au+O+8NaCN+2H O=4Na[Au(CN) ]+4NaOH能发生的原因是____。
2 2 2
(6)金晶体的晶胞结构如图,其晶胞参数为408pm,金晶体的密度为____g•cm-3(列计算式,设N 为阿伏加
A
德罗常数的值)。
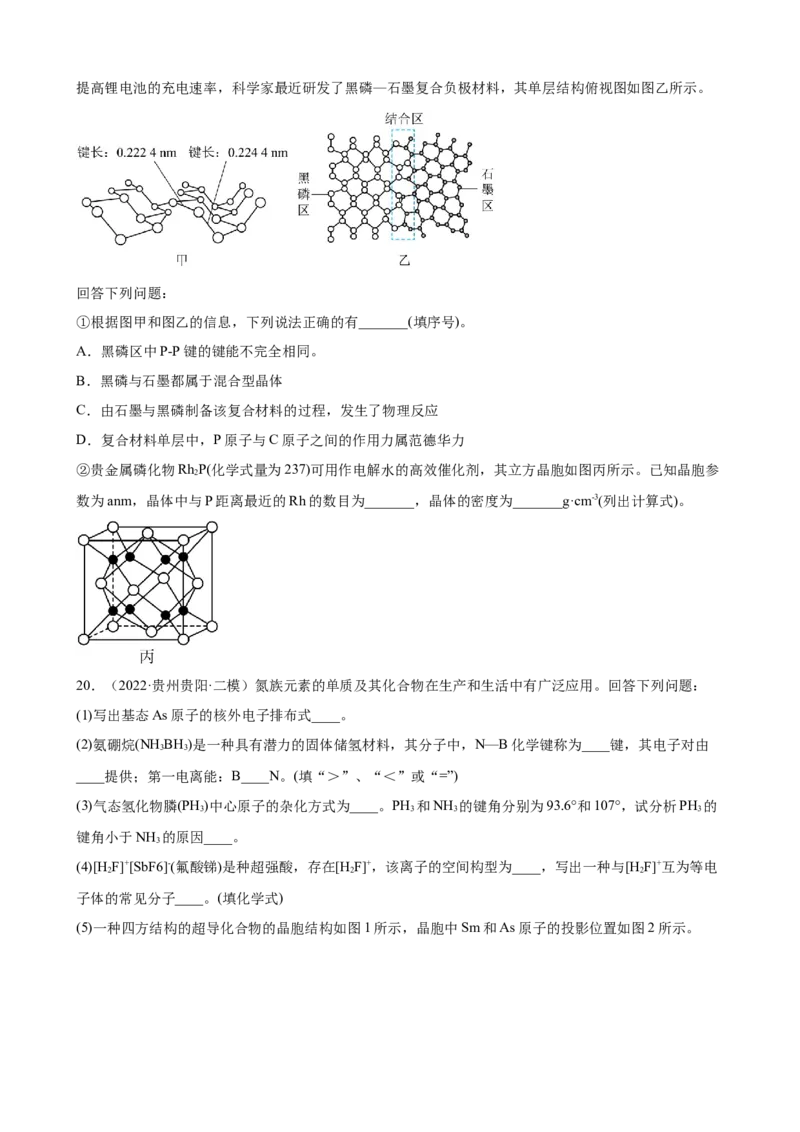
19.(2022·福建三明·高三期中)非金属元素虽然种类不多,但是在自然界中的丰度却很大,请回答下列
问题:
(1)BN(氮化硼,晶胞结构如图)和CO 中的化学键均为共价键,BN的熔点高且硬度大,CO 的晶体干冰却
2 2
松软且极易升华。由此可以判断: BN可能是_______晶体,CO 可能是_______晶体,BN晶体中B原子
2
的杂化轨道类型为_______,干冰中C原子的杂化轨道类型为_______ 。
(2)磷及其化合物在电池、催化等领域有重要应用。黑磷与石墨类似,也具有层状结构(如图甲)。为大幅度提高锂电池的充电速率,科学家最近研发了黑磷—石墨复合负极材料,其单层结构俯视图如图乙所示。
回答下列问题:
①根据图甲和图乙的信息,下列说法正确的有_______(填序号)。
A.黑磷区中P-P键的键能不完全相同。
B.黑磷与石墨都属于混合型晶体
C.由石墨与黑磷制备该复合材料的过程,发生了物理反应
D.复合材料单层中,P原子与C原子之间的作用力属范德华力
②贵金属磷化物Rh P(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图丙所示。已知晶胞参
2
数为anm,晶体中与P距离最近的Rh的数目为_______,晶体的密度为_______g·cm-3(列出计算式)。
20.(2022·贵州贵阳·二模)氮族元素的单质及其化合物在生产和生活中有广泛应用。回答下列问题:
(1)写出基态As原子的核外电子排布式____。
(2)氨硼烷(NH BH)是一种具有潜力的固体储氢材料,其分子中,N—B化学键称为____键,其电子对由
3 3
____提供;第一电离能:B____N。(填“>”、“<”或“=”)
(3)气态氢化物膦(PH )中心原子的杂化方式为____。PH 和NH 的键角分别为93.6°和107°,试分析PH 的
3 3 3 3
键角小于NH 的原因____。
3
(4)[H F]+[SbF6]-(氟酸锑)是种超强酸,存在[H F]+,该离子的空间构型为____,写出一种与[H F]+互为等电
2 2 2
子体的常见分子____。(填化学式)
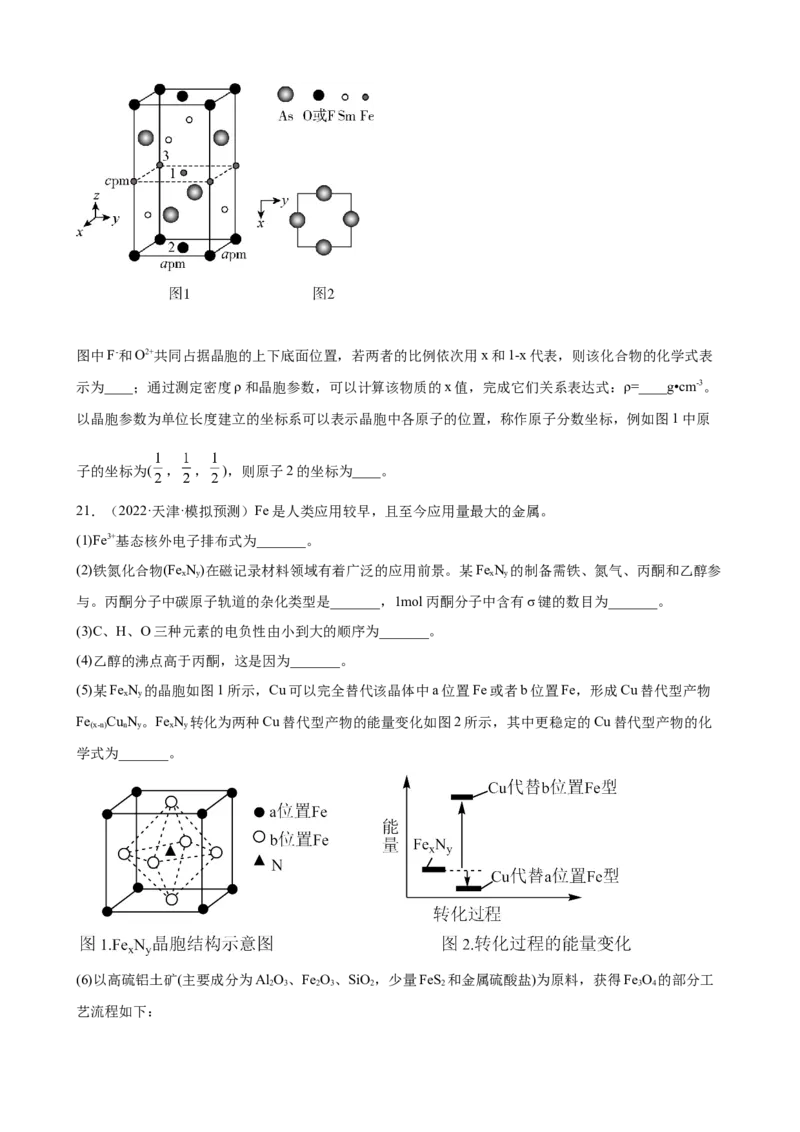
(5)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。图中F-和O2+共同占据晶胞的上下底面位置,若两者的比例依次用x和1-x代表,则该化合物的化学式表
示为____;通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=____g•cm-3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原
子的坐标为( , , ),则原子2的坐标为____。
21.(2022·天津·模拟预测)Fe是人类应用较早,且至今应用量最大的金属。
(1)Fe3+基态核外电子排布式为_______。
(2)铁氮化合物(Fe N)在磁记录材料领域有着广泛的应用前景。某Fe N 的制备需铁、氮气、丙酮和乙醇参
x y x y
与。丙酮分子中碳原子轨道的杂化类型是_______,1mol丙酮分子中含有σ键的数目为_______。
(3)C、H、O三种元素的电负性由小到大的顺序为_______。
(4)乙醇的沸点高于丙酮,这是因为_______。
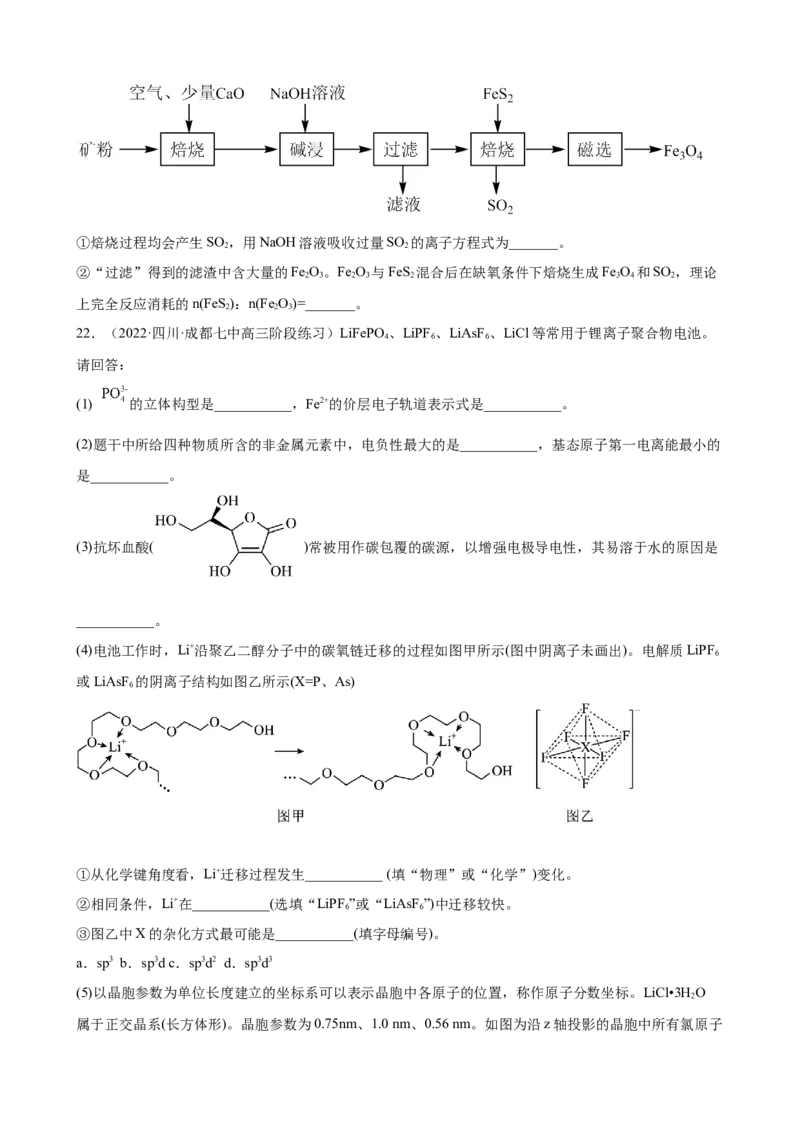
(5)某Fe N 的晶胞如图1所示,Cu可以完全替代该晶体中a位置Fe或者b位置Fe,形成Cu替代型产物
x y
Fe Cu N。Fe N 转化为两种Cu替代型产物的能量变化如图2所示,其中更稳定的Cu替代型产物的化
(x-n) n y x y
学式为_______。
(6)以高硫铝土矿(主要成分为Al O、Fe O、SiO,少量FeS 和金属硫酸盐)为原料,获得Fe O 的部分工
2 3 2 3 2 2 3 4
艺流程如下:①焙烧过程均会产生SO ,用NaOH溶液吸收过量SO 的离子方程式为_______。
2 2
②“过滤”得到的滤渣中含大量的Fe O。Fe O 与FeS 混合后在缺氧条件下焙烧生成Fe O 和SO ,理论
2 3 2 3 2 3 4 2
上完全反应消耗的n(FeS ):n(Fe O)=_______。
2 2 3
22.(2022·四川·成都七中高三阶段练习)LiFePO 、LiPF 、LiAsF、LiCl等常用于锂离子聚合物电池。
4 6 6
请回答:
(1) 的立体构型是___________,Fe2+的价层电子轨道表示式是___________。
(2)题干中所给四种物质所含的非金属元素中,电负性最大的是___________,基态原子第一电离能最小的
是___________。
(3)抗坏血酸( )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
___________。
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF
6
或LiAsF 的阴离子结构如图乙所示(X=P、As)
6
①从化学键角度看,Li+迁移过程发生___________ (填“物理”或“化学”)变化。
②相同条件,Li+在___________(选填“LiPF ”或“LiAsF”)中迁移较快。
6 6
③图乙中X的杂化方式最可能是___________(填字母编号)。
a.sp3 b.sp3d c.sp3d2 d.sp3d3
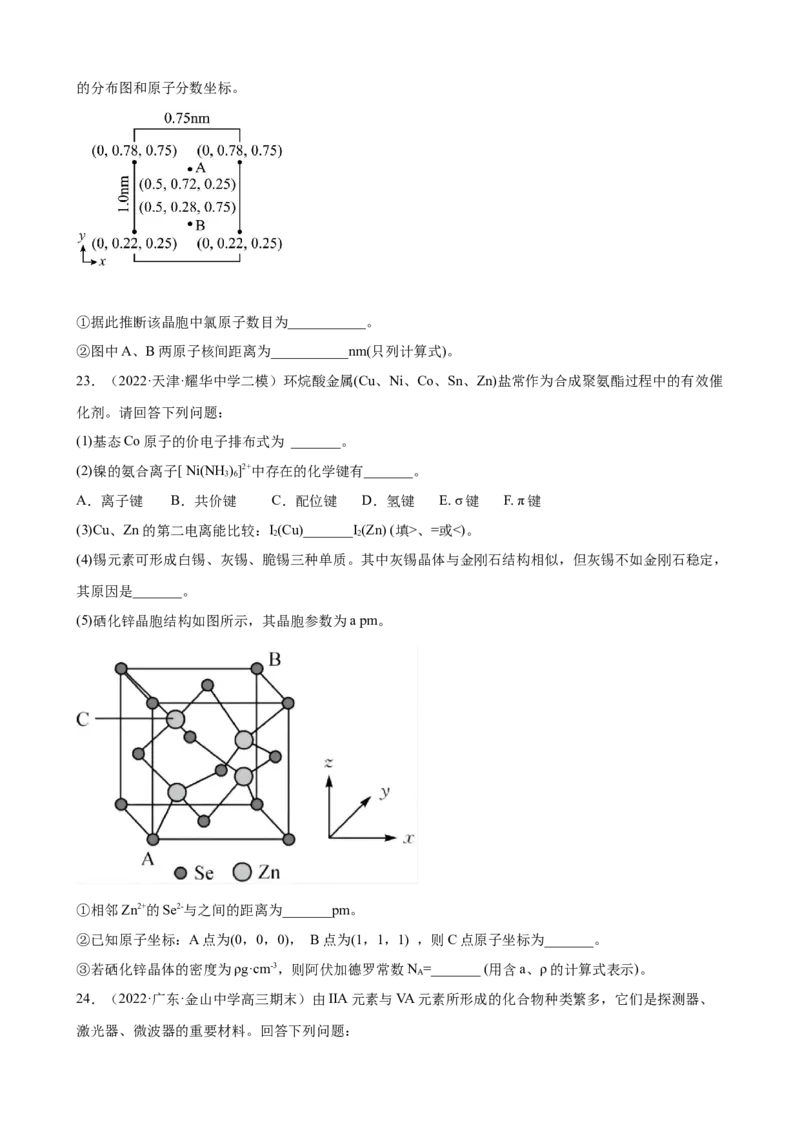
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl•3H O
2
属于正交晶系(长方体形)。晶胞参数为0.75nm、1.0 nm、0.56 nm。如图为沿z轴投影的晶胞中所有氯原子的分布图和原子分数坐标。
①据此推断该晶胞中氯原子数目为___________。
②图中A、B两原子核间距离为___________nm(只列计算式)。
23.(2022·天津·耀华中学二模)环烷酸金属(Cu、Ni、Co、Sn、Zn)盐常作为合成聚氨酯过程中的有效催
化剂。请回答下列问题:
(1)基态Co原子的价电子排布式为 _______。
(2)镍的氨合离子[ Ni(NH )]2+中存在的化学键有_______。
3 6
A.离子键 B.共价键 C.配位键 D.氢键 E. σ键 F. π键
(3)Cu、Zn的第二电离能比较:I(Cu)_______I (Zn) (填>、=或<)。
2 2
(4)锡元素可形成白锡、灰锡、脆锡三种单质。其中灰锡晶体与金刚石结构相似,但灰锡不如金刚石稳定,
其原因是_______。
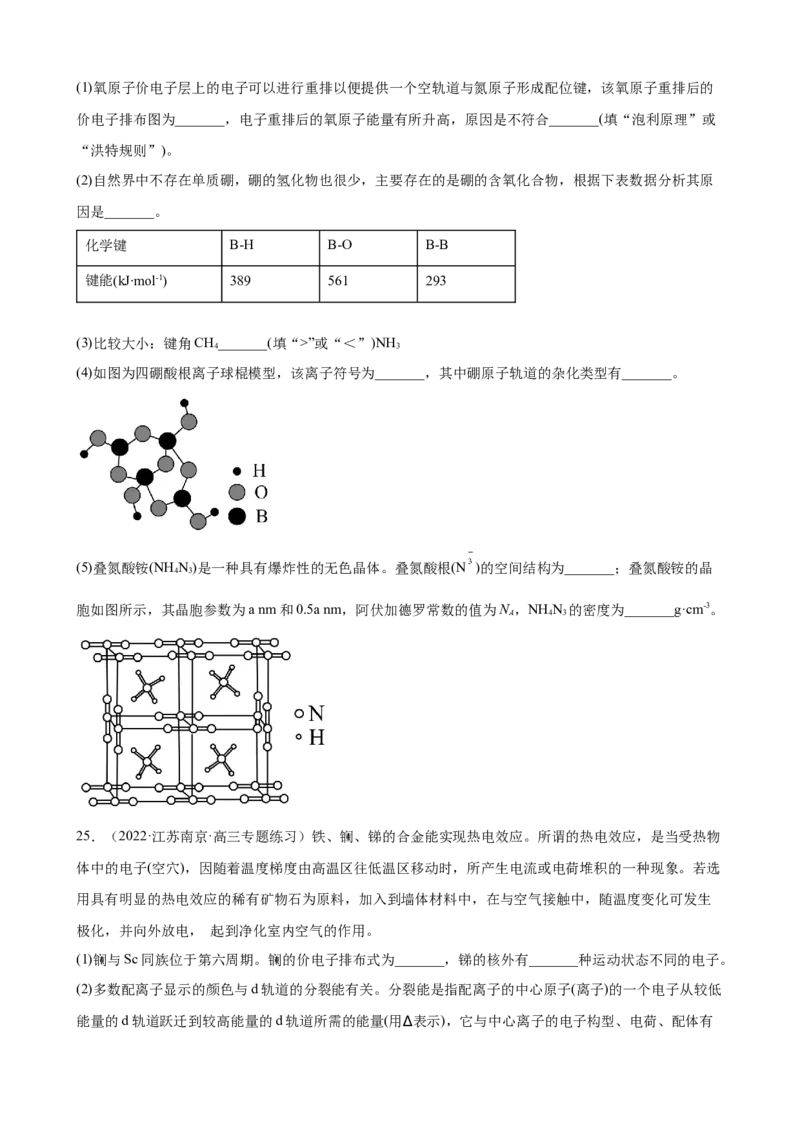
(5)硒化锌晶胞结构如图所示,其晶胞参数为a pm。
①相邻Zn2+的Se2-与之间的距离为_______pm。
②已知原子坐标:A点为(0,0,0), B点为(1,1,1) ,则C点原子坐标为_______。
③若硒化锌晶体的密度为ρg·cm-3,则阿伏加德罗常数N =_______ (用含a、ρ的计算式表示)。
A
24.(2022·广东·金山中学高三期末)由IIA元素与VA元素所形成的化合物种类繁多,它们是探测器、
激光器、微波器的重要材料。回答下列问题:(1)氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的
价电子排布图为_______,电子重排后的氧原子能量有所升高,原因是不符合_______(填“泡利原理”或
“洪特规则”)。
(2)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据下表数据分析其原
因是_______。
化学键 B-H B-O B-B
键能(kJ∙mol-1) 389 561 293
(3)比较大小:键角CH_______(填“>”或“<”)NH
4 3
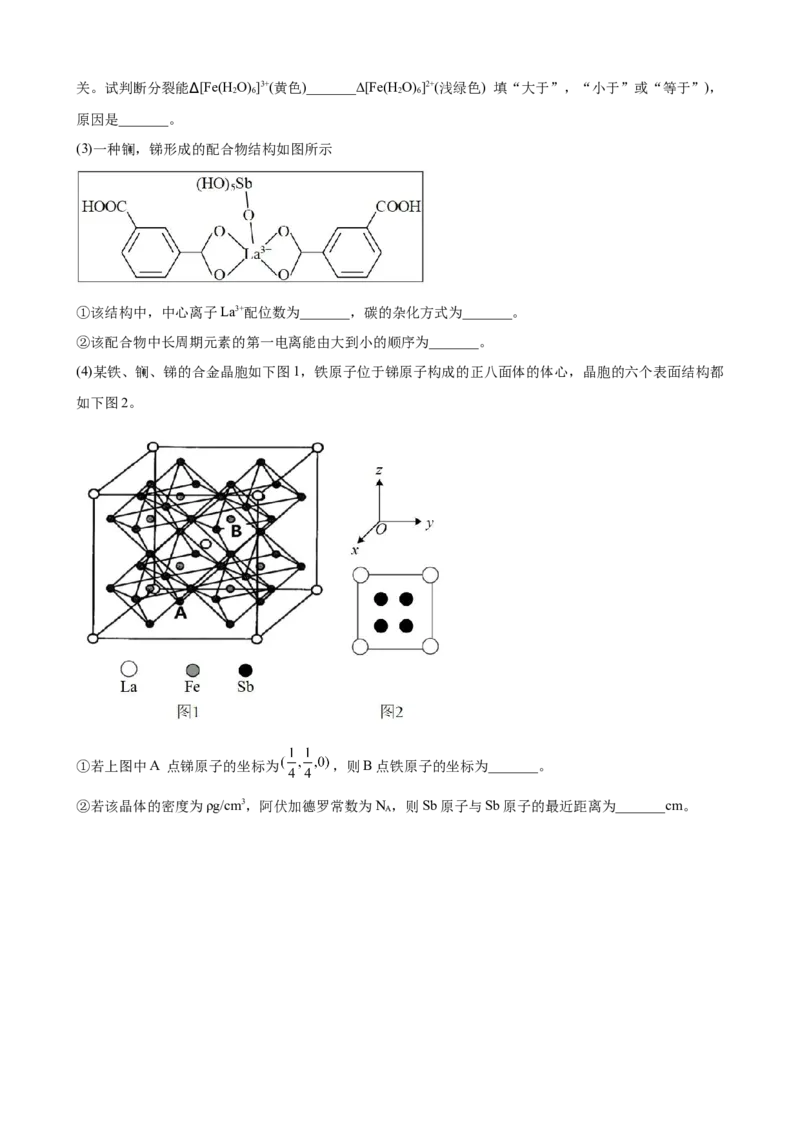
(4)如图为四硼酸根离子球棍模型,该离子符号为_______,其中硼原子轨道的杂化类型有_______。
(5)叠氮酸铵(NH N)是一种具有爆炸性的无色晶体。叠氮酸根(N )的空间结构为_______;叠氮酸铵的晶
4 3
胞如图所示,其晶胞参数为a nm和0.5a nm,阿伏加德罗常数的值为N ,NH N 的密度为_______g·cm-3。
A 4 3
25.(2022·江苏南京·高三专题练习)铁、镧、锑的合金能实现热电效应。所谓的热电效应,是当受热物
体中的电子(空穴),因随着温度梯度由高温区往低温区移动时,所产生电流或电荷堆积的一种现象。若选
用具有明显的热电效应的稀有矿物石为原料,加入到墙体材料中,在与空气接触中,随温度变化可发生
极化,并向外放电, 起到净化室内空气的作用。
(1)镧与Sc同族位于第六周期。镧的价电子排布式为_______,锑的核外有_______种运动状态不同的电子。
(2)多数配离子显示的颜色与d轨道的分裂能有关。分裂能是指配离子的中心原子(离子)的一个电子从较低
能量的d轨道跃迁到较高能量的d轨道所需的能量(用∆表示),它与中心离子的电子构型、电荷、配体有关。试判断分裂能∆[Fe(H O) ]3+(黄色)_______∆[Fe(HO) ]2+(浅绿色) 填“大于”,“小于”或“等于”),
2 6 2 6
原因是_______。
(3)一种镧,锑形成的配合物结构如图所示
①该结构中,中心离子La3+配位数为_______,碳的杂化方式为_______。
②该配合物中长周期元素的第一电离能由大到小的顺序为_______。
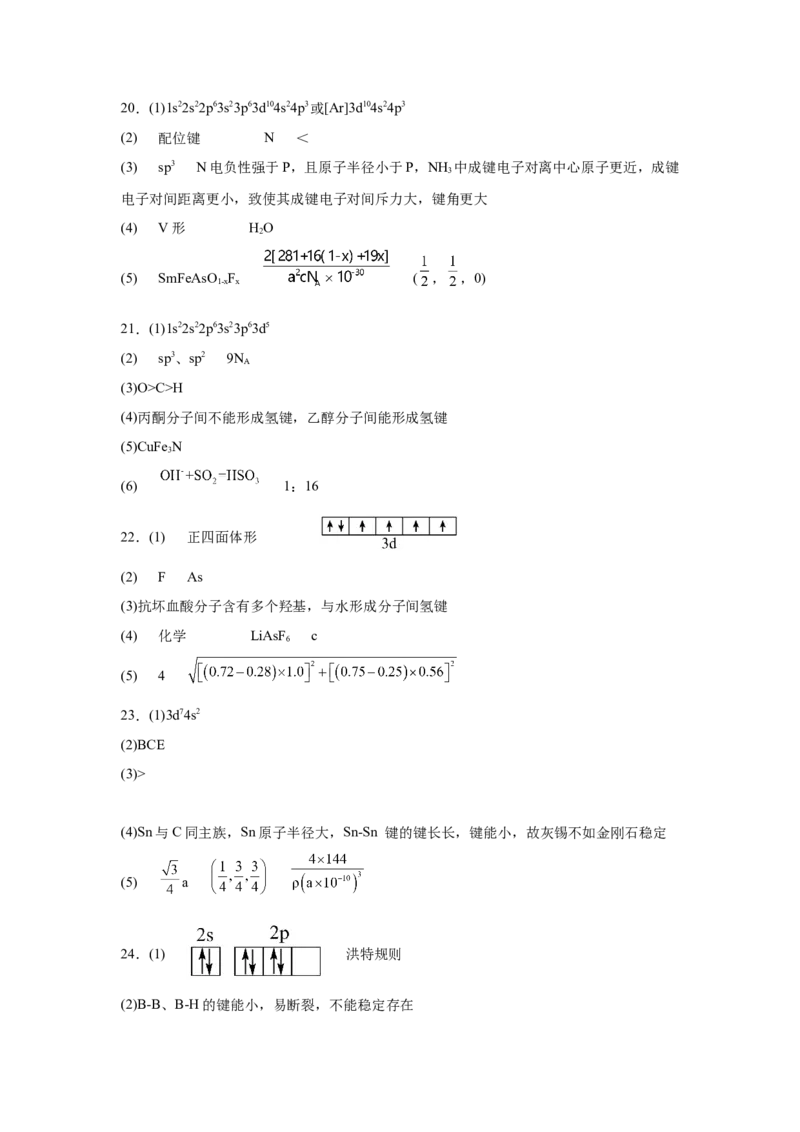
(4)某铁、镧、锑的合金晶胞如下图1,铁原子位于锑原子构成的正八面体的体心,晶胞的六个表面结构都
如下图2。
①若上图中A 点锑原子的坐标为 ,则B点铁原子的坐标为_______。
②若该晶体的密度为ρg/cm3,阿伏加德罗常数为N ,则Sb原子与Sb原子的最近距离为_______cm。
A参考答案:
1.(1)3d104s1
(2) 还原 ab
(3)HCHO
(4)N
(5)d
(6)该聚酰亚胺基材上存在酰胺键,在碱性条件下易发生水解而遭到破
2.(1) 三角锥形 sp3杂化
(2)基态 是Cu失去最外层4s1电子得到[Ar]3d10的稳定结构
(3) HO 深蓝
2
(4) CuN>C>H sp3杂化、sp2杂化
(3) < 失去1个电子后Ni+的价电子排布式为3d84s1,失去1个电子后Cu+的价电子排布
为3d10,此时Cu+的3d轨道处于全充满状态,更稳定
(4) 2:176.(1) 第二周期第ⅦA族 p
(2) N 3
(3)[Ar]3d84s2
(4)F
(5)Mn2+的价电子排布式为3d5,d轨道电子为半充满结构,结构稳定,因此很难再失去电子;
Fe2+的价电子排布式为3d6,再失去一个电子为半充满稳定结构,因此再失去一个电子较容
易
7.(1)C
(2) C(未杂化的p轨道)-C(未杂化的p轨道) sp2、sp3 4 Pd Cl
6 12
(3)随着原子序数的增加,Cl、Br、I的电负性依次降低,孤电子对与中心元素配位的能力
依次增加,形成配离子的稳定性依次增强
(4) Ni Pt(或PtNi ) 1:3 a pm
3 3
8.(1)
(2)Ti原子的价电子数比Al多,金属键更强
(3) 16 HB>Li
4 4
(3)Mg
(4)CD
(5) +3 正四面体形
(6)CO 、CS
2 2
16.(1) 9 三角锥形
(2)
(3)苯胺和甲苯都是分子晶体,苯胺分子间存在氢键,其熔点较高
(4)
(5) 或
17.(1)8:3
(2)共价
(3)极性
(4)sp3
(5) 平面三角形 正四面体形
(6)<
18.(1) 5d106s1 ds
(2) < >
(3)8
(4) 离子晶体 三种晶体均为分子晶体,ZnCl,ZnBr ,ZnI 的相对分子质量依
2 2 2
次增大,范德华力依次增大
(5)O 为氧化剂,Au+与CN-形成配位化合物,两者相互促进使反应进行
2
(6)
19.(1) 共价 分子 sp3 sp
(2) AB 820.(1)1s22s22p63s23p63d104s24p3或[Ar]3d104s24p3
(2) 配位键 N <
(3) sp3 N电负性强于P,且原子半径小于P,NH 中成键电子对离中心原子更近,成键
3
电子对间距离更小,致使其成键电子对间斥力大,键角更大
(4) V形 HO
2
(5) SmFeAsO F ( , ,0)
1-x x
21.(1)1s22s22p63s23p63d5
(2) sp3、sp2 9N
A
(3)O>C>H
(4)丙酮分子间不能形成氢键,乙醇分子间能形成氢键
(5)CuFe N
3
(6) 1:16
22.(1) 正四面体形
(2) F As
(3)抗坏血酸分子含有多个羟基,与水形成分子间氢键
(4) 化学 LiAsF c
6
(5) 4
23.(1)3d74s2
(2)BCE
(3)>
(4)Sn与C同主族,Sn原子半径大,Sn-Sn 键的键长长,键能小,故灰锡不如金刚石稳定
(5) a
24.(1) 洪特规则
(2)B-B、B-H的键能小,易断裂,不能稳定存在(3)>
(4) sp2、sp3
(5) 直线型
25.(1) 5d16s2 51
(2) > Fe3+的正电荷数比Fe2+的多,吸引电子能力更强;Fe3+的3d达到半充满稳定结构,
Fe2+的3d未达到半充满稳定结构;
(3) 5 sp2、sp3 Sb> La
(4) cm