文档内容
第 69 讲 物质结构与性质综合题研究
复习目标 1.熟练掌握物质结构常见考点,构建解题模型。2.借助图像理解,培养空间想象
力。3.能用抽象理论对陌生情境进行判断并加以解释。
1.物质结构常见考点剖析
(1)以原子或离子结构为主线的考查角度
(2)以分子结构为主线的考查角度
(3)以晶体结构为主线的考查角度2.性质比较及解释类问题模型构建
(1)“原因解释”类试题的解题流程
(2)模板构建
→→
(3)模板应用示例
比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:_______________________。
GeCl GeBr GeI
4 4 4
熔点/℃ -49.5 26 146
沸点/℃ 83.1 186 约400
[答题模板]
[标准答案] GeCl 、GeBr 、GeI 的熔、沸点依次增大。原因:分子结构相似,相对分子质
4 4 4
量依次增大,分子间相互作用力逐渐增强
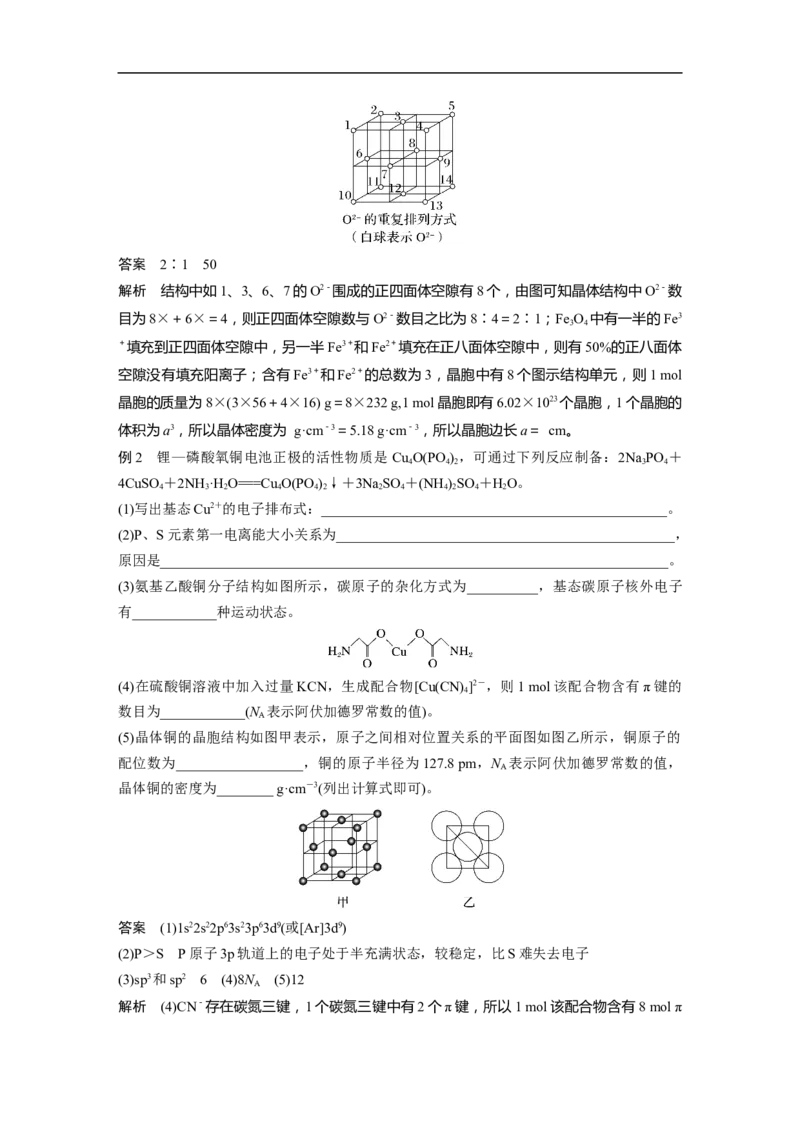
例1 Fe O 晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7
3 4
的O2-围成的正四面体空隙和3、6、7、8、9、12的O2-围成的正八面体空隙。Fe O 中有一
3 4
半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe O 晶体
3 4
中,正四面体空隙数与O2-数目之比为________。有________%的正八面体空隙没有填充阳
离子。Fe O 晶胞中有8个图示结构单元,晶体密度为5.18 g·cm-3,则该晶胞参数a=_____
3 4
cm
(写出计算表达式即可)。答案 2∶1 50
解析 结构中如1、3、6、7的O2-围成的正四面体空隙有8个,由图可知晶体结构中O2-数
目为8×+6×=4,则正四面体空隙数与O2-数目之比为8∶4=2∶1;Fe O 中有一半的Fe3
3 4
+填充到正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则有50%的正八面体
空隙没有填充阳离子;含有Fe3+和Fe2+的总数为3,晶胞中有8个图示结构单元,则1 mol
晶胞的质量为8×(3×56+4×16) g=8×232 g,1 mol晶胞即有6.02×1023个晶胞,1个晶胞的
体积为a3,所以晶体密度为 g·cm-3=5.18 g·cm-3,所以晶胞边长a= cm。
例2 锂—磷酸氧铜电池正极的活性物质是 Cu O(PO ) ,可通过下列反应制备:2NaPO +
4 4 2 3 4
4CuSO +2NH ·H O===Cu O(PO )↓+3NaSO +(NH )SO +HO。
4 3 2 4 4 2 2 4 4 2 4 2
(1)写出基态Cu2+的电子排布式:_________________________________________________。
(2)P、S元素第一电离能大小关系为________________________________________________,
原因是________________________________________________________________________。
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为__________,基态碳原子核外电子
有____________种运动状态。
(4)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN) ]2-,则1 mol该配合物含有π键的
4
数目为____________(N 表示阿伏加德罗常数的值)。
A
(5)晶体铜的晶胞结构如图甲表示,原子之间相对位置关系的平面图如图乙所示,铜原子的
配位数为__________________,铜的原子半径为127.8 pm,N 表示阿伏加德罗常数的值,
A
晶体铜的密度为________ g·cm-3(列出计算式即可)。
答案 (1)1s22s22p63s23p63d9(或[Ar]3d9)
(2)P>S P原子3p轨道上的电子处于半充满状态,较稳定,比S难失去电子
(3)sp3和sp2 6 (4)8N (5)12
A
解析 (4)CN-存在碳氮三键,1个碳氮三键中有2个π键,所以1 mol该配合物含有8 mol π键,数目为8N 。(5)离铜原子距离最近且相等的原子为铜原子的配位原子,根据图甲可知铜
A
原子配位数是 12;根据图乙可知,晶胞的面对角线长为 127.8×4 pm,则晶胞棱长为
2×127.8×10-10 cm,每个晶胞含有铜原子数为 8×+6×=4。1 个晶胞的体积为
(2×127.8×10-10)3 cm3,质量为 g,所以晶体铜的密度为 g·cm-3。
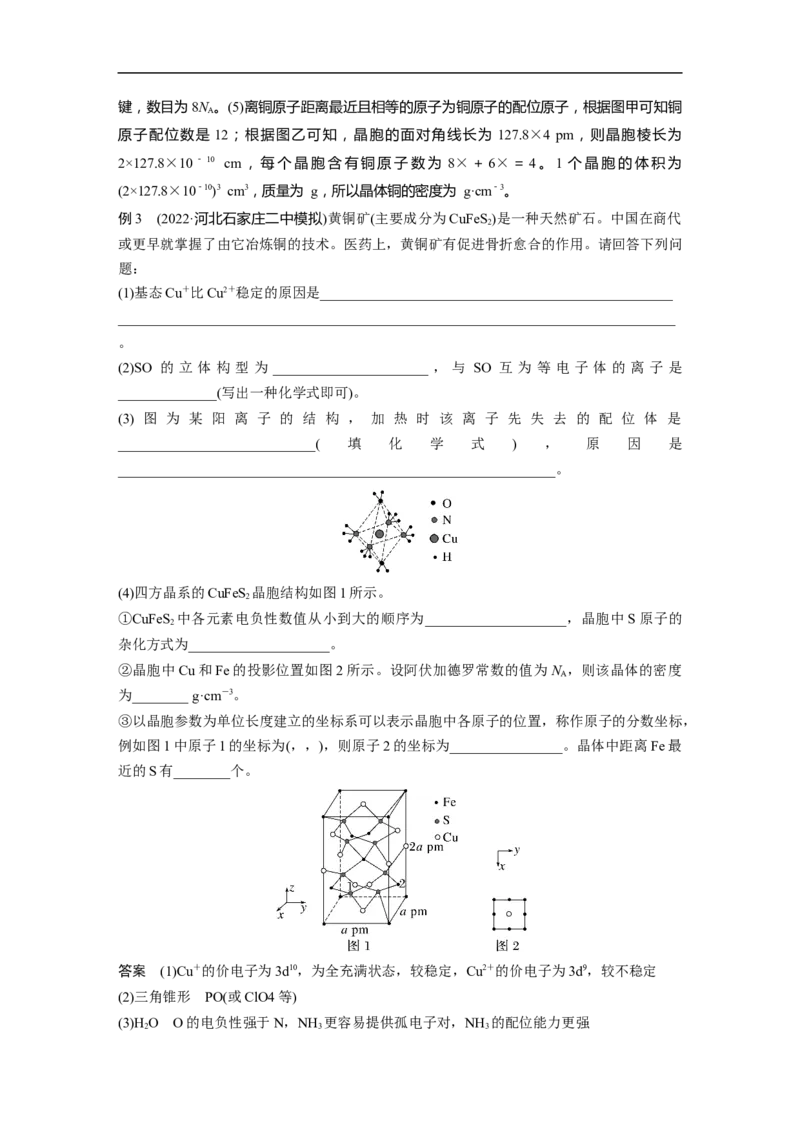
例3 (2022·河北石家庄二中模拟)黄铜矿(主要成分为CuFeS)是一种天然矿石。中国在商代
2
或更早就掌握了由它冶炼铜的技术。医药上,黄铜矿有促进骨折愈合的作用。请回答下列问
题:
(1)基态Cu+比Cu2+稳定的原因是__________________________________________________
_______________________________________________________________________________
。
(2)SO 的 立 体 构 型 为 ______________________ , 与 SO 互 为 等 电 子 体 的 离 子 是
______________(写出一种化学式即可)。
(3) 图 为 某 阳 离 子 的 结 构 , 加 热 时 该 离 子 先 失 去 的 配 位 体 是
____________________________( 填 化 学 式 ) , 原 因 是
______________________________________________________________。
(4)四方晶系的CuFeS 晶胞结构如图1所示。
2
①CuFeS 中各元素电负性数值从小到大的顺序为____________________,晶胞中S原子的
2
杂化方式为____________________。
②晶胞中Cu和Fe的投影位置如图2所示。设阿伏加德罗常数的值为N ,则该晶体的密度
A
为________ g·cm-3。
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,
例如图1中原子1的坐标为(,,),则原子2的坐标为________________。晶体中距离Fe最
近的S有________个。
答案 (1)Cu+的价电子为3d10,为全充满状态,较稳定,Cu2+的价电子为3d9,较不稳定
(2)三角锥形 PO(或ClO4等)
(3)H O O的电负性强于N,NH 更容易提供孤电子对,NH 的配位能力更强
2 3 3(4)①Fe<Cu<S sp3 ②
③(,1,) 4
解析 (2)SO的中心原子价层电子对数为3+×(6+2-2×3)=3+1=4,其立体构型为三角
锥形,根据等电子原理,与SO互为等电子体的离子是PO或ClO等。
(3)图为某阳离子的结构,其配体分别为上下水分子,四周氨气分子,由于 N电负性比O小,
氨气与铜离子形成配位键比水与铜离子形成配位键稳定,因此加热时该离子先失去的配位体
是HO。
2
(4)①根据同周期元素从左到右电负性逐渐增大,同主族元素从上到下电负性逐渐减小,因
此CuFeS 中各元素电负性数值从小到大的顺序为Fe<Cu<S,从图1中可以看出S连了四
2
个价键,因此晶胞中S原子的杂化方式为sp3。
②晶胞中Cu和Fe的投影位置如图2所示,铜原子有4×+6×=4个,铁原子有8×+4×+
1=4个,硫原子有8个,则该晶体的密度为ρ===×1032 g·cm-3。
③根据原子的分数坐标,如图1中原子1的坐标为(,,),则原子2的坐标为(,1,),根据
图中体心Fe与硫的关系得到晶体中距离Fe最近的S有4个。
1.(2021·湖南,18)硅、锗(Ge)及其化合物广泛应用于光电材料领域。回答下列问题:
(1)基态硅原子最外层的电子排布图为______________,晶体硅和碳化硅熔点较高的是
__________(填化学式)。
(2)硅和卤素单质反应可以得到SiX。
4
SiX 的熔、沸点
4
SiF SiCl SiBr SiI
4 4 4 4
熔点/K 183.0 203.2 278.6 393.7
沸点/K 187.2 330.8 427.2 560.7
①0 ℃时,SiF 、SiCl 、SiBr 、SiI 呈液态的是__________(填化学式),沸点依次升高的原
4 4 4 4
因是____________________________________________________________________________
____________________________________________________________________________,
气态SiX 分子的空间结构是____________。
4
②SiCl 与N-甲基咪唑( )反应可以得到M2+,其结构如图所示:
4
N-甲基咪唑分子中碳原子的杂化轨道类型为________,H、C、N的电负性由大到小的顺序
为__________________,1个M2+中含有________个σ键。(3)下图是Mg、Ge、O三种元素形成的某化合物的晶胞示意图。
①已知化合物中Ge和O的原子个数比为1∶4,图中Z表示________原子(填元素符号),该
化合物的化学式为____________。
②已知该晶胞的晶胞参数分别为a nm、b nm、c nm,α=β=γ=90°,则该晶体的密度ρ=
____________g·cm-3(设阿伏加德罗常数的值为N ,用含a、b、c、N 的代数式表示)。
A A
答案 (1) SiC (2)①SiCl
4
SiX 都是结构相似的分子晶体,相对分子质量依次增大,分子间作用力依次增大 正四面体
4
②sp2、sp3 N>C>H 54 (3)①O MgGeO ②×1021
2 4
解析 (1)硅元素的原子序数为14,价电子排布式为3s23p2,则价电子排布图为
;共价晶体的熔点取决于共价键的强弱,晶体硅和碳化硅都是共价晶体,碳
原子的原子半径小于硅原子,非金属性强于硅原子,碳硅键的键能大于硅硅键、键长小于硅
硅键,则碳硅键强于硅硅键,碳化硅的熔点高于晶体硅。
(2) ①由题给熔、沸点数据可知,0 ℃时,四氟化硅为气态,四氯化硅为液态,四溴化硅、
四碘化硅为固态;分子晶体的沸点取决于分子间作用力的大小,SiX 都是结构相似的分子晶
4
体,相对分子质量依次增大,分子间作用力依次增大,则SiX 的沸点依次升高;SiX 分子
4 4
中硅原子的价层电子对数为4,孤电子对数为0,则分子的空间结构为正四面体。
②由M2+的结构可知,离子中含有杂化方式为sp3杂化的单键碳原子和sp2杂化的双键碳原子;
元素的非金属性越强,其电负性越大,元素的非金属性强弱顺序为 N>C>H,则元素电负性
的大小顺序为N>C>H;M2+的结构中含有单键、双键和配位键,单键和配位键都是σ键,
双键中含有1个σ键,则1个M2+中含有54个σ键。
(3)①由晶胞结构可知,晶胞中位于顶点、面心、棱上和体内的 X原子数为8×+6×+4×
+3=8,位于体内的Y原子数和Z原子数分别为4和16,由Ge和O原子的个数比为1∶4
可知,X为Mg原子、Y为Ge原子、Z为O原子,则晶胞的化学式为MgGeO 。
2 4
②由晶胞的质量公式可得 g=abc×10-21 cm3×ρ,解得ρ=×1021 g·cm-3。
2.(2021·广东,20)很多含巯基(—SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒
剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。(1)基态硫原子的价电子排布式为__________________________。
(2)H S、CH、HO的沸点由高到低顺序为__________。
2 4 2
(3)汞的原子序数为80,位于元素周期表第______周期第ⅡB族。
(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有________。
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C—C—C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
(5)汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水
溶性较好的是______________________。
(6)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。
X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。
①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,
理由是________________________________________________________________________。
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为________;该晶胞中粒子个数
比Hg∶Ge∶Sb=__________。
③设X的最简式的式量为M,则X晶体的密度为________________g·cm-3(列出算式)。
r
答案 (1)3s23p4 (2)H O>HS>CH (3)六
2 2 4
(4)AD (5)化合物Ⅲ (6)①不能无隙并置成晶体,不是最小重复单元 ②4 1∶1∶2
③×1021
解析 (1)基态硫原子核外电子排布式为1s22s22p63s23p4,因此基态硫原子价电子排布式为
3s23p4。
(2)H S、CH 、HO均为分子晶体,HO分子间存在氢键,沸点较高,HS、CH 的分子间作
2 4 2 2 2 4
用力随相对分子质量的增大而增加,因此沸点由高到低顺序为HO>HS>CH。
2 2 4
(3)第六周期0族元素的原子序数为86,因此第80号元素Hg位于第六周期第ⅡB族。(4) 中S原子的价层电子对数为2+=4,因此S原子采取sp3杂化,故A正确;
中含有的元素为H、C、O、S、Hg,同周期从左至右元素的电负性逐渐增大,
同主族从上至下元素的电负性逐渐减小,因此5种元素中电负性最大的为O元素,故B错
误; 中C原子成键均为单键,因此C原子采取sp3杂化,所以C—C—C键角接
近109°28′,故C错误; 中存在C—H、C—C、C—S、S==O、S—O、S—H
共价键和 与Na+之间的离子键,故D正确; 中硫氧键分为硫氧单
键和硫氧双键,共价键种类不同,因此二者的键能不同,故 E错误。
(6)①对比图b和图c可得X晶体的晶胞中上下两个单元内的原子位置不完全相同,不符合
晶胞是晶体的最小重复单元要求。②以晶胞立方体中右侧面心中Hg原子为例,同一晶胞中
与Hg距离最近的Sb的数目为2,右侧晶胞中有2个Sb原子与Hg原子距离最近,因此X的
晶体中与Hg距离最近的Sb的数目为4。该晶胞中Sb原子均位于晶胞内,因此1个晶胞中
含有Sb原子数为8;Ge原子位于晶胞顶角、面上、体心,因此1个晶胞中含有Ge原子数为
1+8×+4×=4;Hg原子位于棱边、面上,因此1个晶胞中含有Hg原子数为6×+4×=
4;则该晶胞中粒子个数比Hg∶Ge∶Sb=4∶4∶8=1∶1∶2。③1个晶胞的质量m= g,1
个晶胞的体积V=(x×10-7cm)2×(y×10-7cm)=x2y×10-21cm3,则X晶体的密度为==×1021
g·cm-3。
3.(2021·全国甲卷,35)我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称
为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化
碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si 的价电子层的电子排布式为
______________;单晶硅的晶体类型为______________。SiCl 是生产高纯硅的前驱体,其
4
中Si采取的杂化类型为______________。SiCl 可发生水解反应,机理如下:
4含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl (H O)中Si采取的杂
4 2
化类型为__________(填标号)。
(2)CO 分子中存在______个σ键和______个π键。
2
(3)甲醇的沸点(64.7 ℃)介于水(100 ℃)和甲硫醇(CHSH,7.6 ℃)之间,其原因是
3
_____________________________________________________________________________
_____________________________________________________________________________。
(4)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为 ZnO/ZrO 固溶
2
体。四方ZrO 晶胞如图所示。Zr4+离子在晶胞中的配位数是________,晶胞参数为a pm、
2
a pm、c pm,该晶体密度为____________g·cm-3(写出表达式)。在ZrO 中掺杂少量ZnO后
2
形成的催化剂,化学式可表示为ZnZr O,则y=________________(用x表达)。
x 1-x y
答案 (1)3s23p2 共价晶体 sp3 ② (2)2 2 (3)甲硫醇不能形成分子间氢键,而水和甲
醇均能形成氢键,且水比甲醇的氢键多 (4)8 2-x
解析 (1)基态Si原子的核外电子排布式为1s22s22p63s23p2,因此Si的价电子层的电子排布式
为3s23p2;晶体硅中Si原子与Si原子之间通过共价键相互结合,整块晶体是一个三维的共
价键网状结构,因此单晶硅为共价晶体;SiCl 中Si原子价层电子对数为4+=4,因此Si原
4
子采取sp3杂化;由图可知,SiCl (H O)中Si原子的σ键数为5,说明Si原子的杂化轨道数
4 2
为5,由此可知Si原子的杂化类型为sp3d。
(2)CO 的结构式为O==C==O,1个双键中含有1个σ键和1个π键,因此1个CO 分子中含有
2 2
2个σ键和2个π键。
(3)甲醇分子之间和水分子之间都存在氢键,因此沸点高于不含分子间氢键的甲硫醇,甲醇
分子间氢键的总强度低于水分子间氢键的总强度,因此甲醇的沸点介于水和甲硫醇之间。
(4)以晶胞中右侧面心的Zr4+为例,同一晶胞中与Zr4+连接最近且等距的O2-数为4,同理可
知右侧晶胞中有4个O2-与Zr4+相连,因此Zr4+在晶胞中的配位数是4+4=8;1个晶胞中
含有4个ZrO 微粒,1个晶胞的质量为m= g,1个晶胞的体积为(a×10-10cm)
2
×(a×10-10cm)×(c×10-10cm)=a2c×10-30cm3,因此该晶体密度为== g·cm-3;在ZrO 中
2
掺杂少量ZnO后形成的催化剂,化学式可表示为ZnZr O,其中Zn元素为+2价,Zr为
x 1-x y+4价,O元素为-2价,根据化合物化合价为0可知2x+4×(1-x)=2y,解得y=2-x。
4.[2020·全国卷Ⅰ,35(3)(4)]Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极
材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(3)磷酸根离子的空间结构为________,其中P的价层电子对数为________,杂化轨道类型
为_____________________________________________________________________________。
(4)LiFePO 的晶胞结构示意图如(a)所示。其中O围绕Fe和P分别形成正八面体和正四面体,
4
它们通过共顶点、共棱形成空间链结构。每个晶胞中含有LiFePO 的单元数有________个。
4
电池充电时,LiFePO 脱出部分 Li+,形成 Li FePO ,结构示意图如(b)所示,则 x=
4 1-x 4
_________________________________________________,n(Fe2+ )∶n(Fe3+)=________。
答案 (3)正四面体 4 sp3 (4)4 (或0.187 5) 13∶3
解析 (3)根据价层电子对互斥模型,PO中P的价层电子对数为4+=4,无孤电子对,故杂
化轨道类型为sp3,空间结构为正四面体。
(4)根据(a)图,小圆点为Li+,位于顶点的Li+有8个,位于棱上的Li+有4个,位于面心的
Li+有4个,晶胞中共含有Li+的个数为8×+4×+4×=4,所以每个晶胞中含有LiFePO 的
4
单元数为4。由(b)图与(a)图相比知,(b)图中少了2个Li+,一个是棱上的,一个是面心上的,
所以(b)图中物质含Li+的个数为8×+3×+3×=,=,x=。设化合物中Fe2+为y,Fe3+为
1-y,由化合物呈电中性,(1-)×1+2y+3(1-y)=3,解得y=,1-y=,n(Fe2+)∶n(Fe3+)
=13∶3。
课时精练
1.(2022·昆明高三质检)砷化铝(AlAs)常用作光谱分析试剂和制备电子组件的原料,是一种
新型半导体材料。回答下列问题:
(1)基态As原子的核外价电子的轨道表示式为______________________________________;
第 一 电 离 能 I(As)__________I(Se) ( 填 “ 大 于 ” 或 “ 小 于 ” ) , 其 原 因 是
1 1
______________________________________________________________________________
______________________________________________________________________________。
(2)As S 的分子结构中均为单键,且每个原子最外层均满足8e-稳定结构,则该分子中所含
4 4
共价键数目为__________;分子中 As、S 原子的杂化轨道类型分别为__________、
__________。
(3)AlF 的 熔 点 约 为 1 040 ℃ , AlCl 的 熔 点 为 194 ℃ , 其 晶 体 类 型 分 别 是
3 3____________________、______________________。
(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致
密保护膜可阻止HO 刻蚀液与下层GaAs(砷化镓)反应。
2 2
①上述致密保护膜是一种常见的氧化物,其化学式为________________________。
②已知AlAs的立方晶胞如图2所示,其中As的配位数为________;该晶体密度为ρ g·cm-
3,设N 为阿伏加德罗常数的值,晶胞参数为______ pm。
A
答案 (1) 大于 As最外层的4p能级为半充满结构,能量更低,更
稳定
(2)10 sp3 sp3
(3)离子晶体 分子晶体
(4)①Al O ②4 ×1010
2 3
解析 (2)As S 的分子结构中均为单键,且每个原子最外层均满足8e-稳定结构,可先确定
4 4
As 的结构,即空心正四面体,就有6个As—As,4个As—As中间插入1个S原子,就形成
4
了 ,则该分子中所含共价键数目为10;As、S原子的杂化轨道类型分别为sp3、
sp3。
(3)AlF 的熔点约为1 040 ℃,熔点较高,其晶体类型是离子晶体,AlCl 的熔点为194 ℃,
3 3
熔点较低,其晶体类型是分子晶体。
(4)①由图可知,GaAs能被HO 腐蚀,AlAs和HO 发生氧化还原反应生成致密的氧化物薄
2 2 2 2
膜,HO 作氧化剂,则AlAs中As元素被氧化,所以得到的氧化物为Al O。
2 2 2 3
②根据AlAs晶胞的结构图可知,Al位于晶胞的顶点和面心,As位于晶胞内部,一个As原
子周围距离最近且相等的Al原子的个数为4,则As的配位数为4;晶胞的质量为 g,则晶
胞的边长为×1010 pm。
2.(2022·深圳模拟)铁(Fe)、钴(Co)、镍(Ni)是第四周期第Ⅷ族的元素,在化学上称为铁系元
素,其化合物在生产生活中应用广泛。(1)铁系元素能与CO形成Fe(CO) 、Ni(CO) 等金属羰基化合物。已知室温时Fe(CO) 为浅黄
5 4 5
色液体,沸点103 ℃,则Fe(CO) 中含有的化学键类型包括______________(填字母)。
5
A.极性共价键 B.离子键
C.配位键 D.金属键
(2)以甲醇为溶剂,Co2+可与色胺酮分子配位结合形成对DNA具有切割作用的色胺酮钴配合
物(合成过程如下所示)。色胺酮分子中所含元素(H、C、N、O)第一电离能由大到小的顺序
为__________,色胺酮分子中N原子的杂化类型为__________。X射线衍射分析显示色胺
酮钴配合物晶胞中还含有一个CHOH分子,CHOH是通过__________作用与色胺酮钴配合
3 3
物相结合。
(3)Fe、Co、Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点,Fe、Co、
Ni明显高于Ca,其原因是_____________________________________________________
____________________________________________________________________________。
(4)ZnS是一种使用广泛的荧光材料。已知立方ZnS的晶胞结构如图所示:
①已知A、B点的原子坐标分别为(0,0,0)和(1,,),则C点的原子坐标为____________;
②立方ZnS的晶胞参数a=541 pm,则其晶体密度为________ g·cm-3(列出计算表达式,设
N 为阿伏加德罗常数的值)。
A
答案 (1)AC
(2)N>O>C>H sp2、sp3 氢键
(3)Fe、Co、Ni的原子半径比Ca的小,金属键强,因此熔点高
(4)①(,,) ②
解析 (1)根据物理性质,可以推知Fe(CO) 为分子晶体,故存在的化学键为极性共价键和配
5
位键。(2)色胺酮分子中氮原子有单键和双键两种成键方式,故杂化类型为sp2、sp3,CHOH
3
是通过氢键与色胺酮钴配合物相结合。(4)① 已知 A、B 点的原子坐标分别为(0,0,0)和(1,,),则C点的原子坐标为(,,);②ρ== g·cm-3。
3.(2022·郑州模拟)吴梦昊研究团队设计了一系列稳定的由超碱 PnH和超卤素MX组成的
PnH MX (Pn=N、P;M=B、Al、Fe;X=Cl、Br)超盐晶体。
4 4
(1)基态铁原子价电子排布中未成对电子数与成对电子对数之比为________。
(2)第二周期元素中,第一电离能介于元素B和N之间的元素有________种。
(3)键角:PH________PH(填“大于”或“小于”),请分析原因:_____________________
3
_______________________________________________________________________________
。
(4)写出与超卤素AlCl等电子体的两种分子的化学式:________________________________。
(5)六方相氮化硼晶体结构与石墨相似(如图1),晶体中氮原子的杂化方式为__________。氮
化硼晶体不导电的原因是_________________________________________________________
_______________________________________________________________________________
。
(6)磷化硼晶胞结构如图2所示,晶胞中P原子空间堆积方式为______________;已知晶体
中硼和磷原子半径分别为r pm和r pm,距离最近的硼和磷原子核间距为二者原子半径之
1 2
和。则磷化硼晶胞中原子的体积占晶胞体积的百分率为______________________(写出计算
式)。
答案 (1)2∶1 (2)3 (3)大于 PH 分子中磷原子上孤电子对对共价键的排斥作用大于共价
3
键之间的斥力 (4)CCl 、SiCl (或SiF 等) (5)sp2 层状结构中没有自由移动的电子 (6)面
4 4 4
心立方最密堆积 ×100%
解析 (1)基态铁原子价电子排布式为3d64s2,则未成对电子数与成对电子对数之比为 4∶2
=2∶1。(2)同一周期元素从左到右第一电离能呈增大趋势,但第ⅡA族、第ⅤA族反常,
则第二周期元素中,第一电离能介于元素B和N之间的元素有Be、C、O共3种。(4)原子
总数相等、价电子总数相等的微粒互称为等电子体,则与超卤素 AlCl等电子体的两种分子
的化学式为CCl 、SiCl (或SiF 等)。(5)六方相氮化硼晶体结构与石墨相似,石墨中碳原子的
4 4 4杂化方式是sp2,则晶体中氮原子的杂化方式为sp2,氮化硼晶体不导电的原因是层状结构中
没有自由移动的电子。(6)磷化硼晶胞中P原子在正六面体的面心,则其空间堆积方式为面
心立方最密堆积,P原子个数是8×+6×=4,B原子个数是4,设晶胞的边长为a,体对角
线是a,B原子与P原子最近距离等于体对角线的四分之一,即a=,则磷化硼晶胞中原子
的体积占晶胞体积的百分率为×100%。
4.(2022·山东模拟)铁是人体必需的微量元素,在人类生产和生活中也有重要作用。
(1)①有机物甲所含的元素中,电负性最小的是____________________(填元素符号,下同),
第一电离能最大的是____________________。
②血红蛋白中的铁处于基态时,其最高能级中的单电子数为____________________。
③血红蛋白中N原子的杂化方式为______________________________________________。
(2)FeCl 中的化学键具有明显的共价性,蒸气状态下以双聚分子存在的FeCl 的结构式为
3 3
________________,其中Fe的配位数为_____________________________________________。
(3)LiFePO 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷
4
酸钠等。焦磷酸根离子、三磷酸根离子如图所示。
这类磷酸根离子的化学式可用通式表示为__________(用n代表P原子数)。
(4)铁及其化合物的晶体种类较多。
①Fe的一种晶体结构如甲、乙所示,若按甲中虚线方向切乙,得到的切面图正确的是
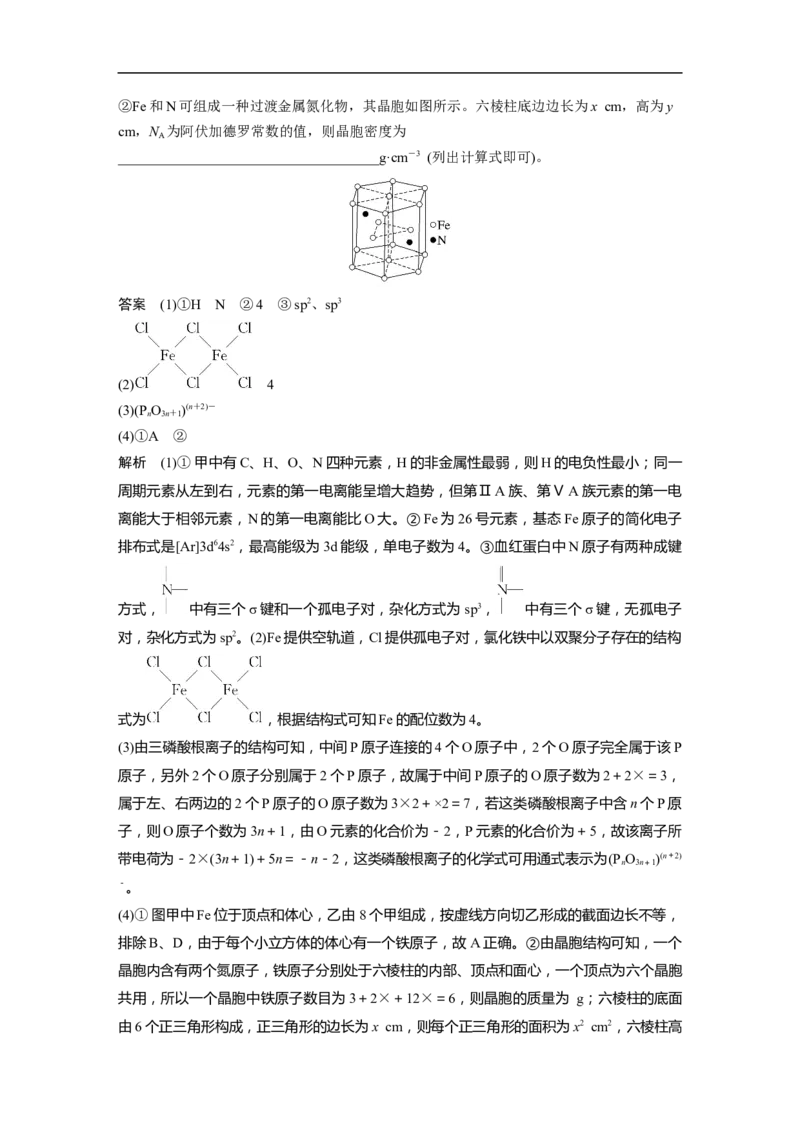
____________(填字母)。②Fe和N可组成一种过渡金属氮化物,其晶胞如图所示。六棱柱底边边长为x cm,高为y
cm,N 为阿伏加德罗常数的值,则晶胞密度为
A
_____________________________________g·cm-3 (列出计算式即可)。
答案 (1)①H N ②4 ③sp2、sp3
(2) 4
(3)(P O )(n+2)-
n 3n+1
(4)①A ②
解析 (1)①甲中有C、H、O、N四种元素,H的非金属性最弱,则H的电负性最小;同一
周期元素从左到右,元素的第一电离能呈增大趋势,但第ⅡA族、第ⅤA族元素的第一电
离能大于相邻元素,N的第一电离能比O大。②Fe为26号元素,基态Fe原子的简化电子
排布式是[Ar]3d64s2,最高能级为3d能级,单电子数为4。③血红蛋白中N原子有两种成键
方式, 中有三个σ键和一个孤电子对,杂化方式为sp3, 中有三个σ键,无孤电子
对,杂化方式为sp2。(2)Fe提供空轨道,Cl提供孤电子对,氯化铁中以双聚分子存在的结构
式为 ,根据结构式可知Fe的配位数为4。
(3)由三磷酸根离子的结构可知,中间P原子连接的4个O原子中,2个O原子完全属于该P
原子,另外2个O原子分别属于2个P原子,故属于中间P原子的O原子数为2+2×=3,
属于左、右两边的2个P原子的O原子数为3×2+×2=7,若这类磷酸根离子中含n个P原
子,则O原子个数为3n+1,由O元素的化合价为-2,P元素的化合价为+5,故该离子所
带电荷为-2×(3n+1)+5n=-n-2,这类磷酸根离子的化学式可用通式表示为(P O )(n+2)
n 3n+1
-。
(4)①图甲中Fe位于顶点和体心,乙由8个甲组成,按虚线方向切乙形成的截面边长不等,
排除B、D,由于每个小立方体的体心有一个铁原子,故A正确。②由晶胞结构可知,一个
晶胞内含有两个氮原子,铁原子分别处于六棱柱的内部、顶点和面心,一个顶点为六个晶胞
共用,所以一个晶胞中铁原子数目为3+2×+12×=6,则晶胞的质量为 g;六棱柱的底面
由6个正三角形构成,正三角形的边长为x cm,则每个正三角形的面积为x2 cm2,六棱柱高为y cm,则晶胞的体积为6×x2y cm3,故晶胞的密度为 g·cm-3。