文档内容
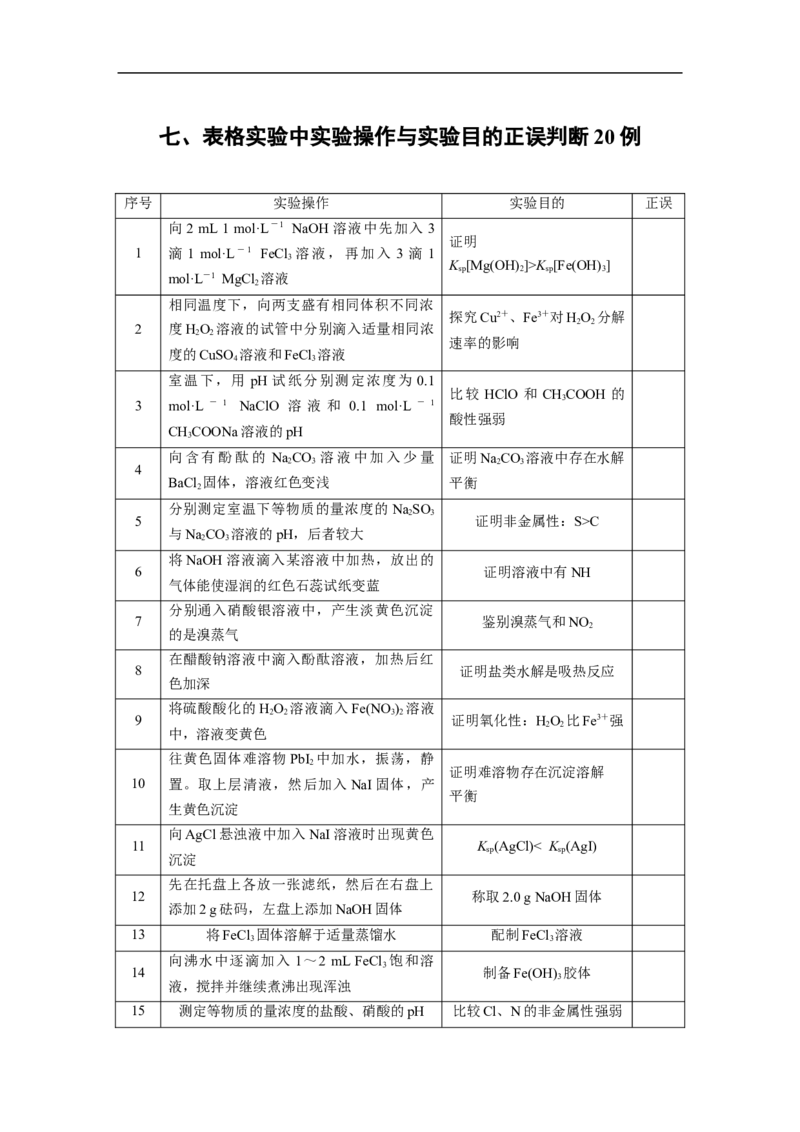
七、表格实验中实验操作与实验目的正误判断 20 例
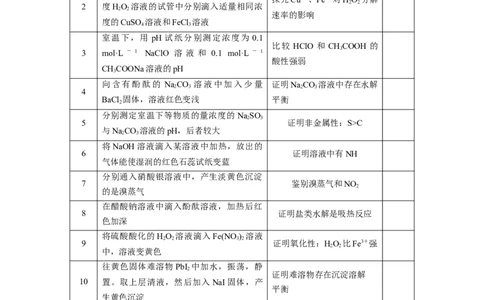
序号 实验操作 实验目的 正误
向2 mL 1 mol·L-1 NaOH 溶液中先加入 3
证明
1 滴 1 mol·L-1 FeCl 溶液,再加入 3 滴 1
3
K [Mg(OH) ]>K [Fe(OH) ]
sp 2 sp 3
mol·L-1 MgCl 溶液
2
相同温度下,向两支盛有相同体积不同浓
探究Cu2+、Fe3+对HO 分解
2 2
2 度HO 溶液的试管中分别滴入适量相同浓
2 2
速率的影响
度的CuSO 溶液和FeCl 溶液
4 3
室温下,用 pH 试纸分别测定浓度为 0.1
比较 HClO 和 CHCOOH 的
3
3 mol·L - 1 NaClO 溶 液 和 0.1 mol·L - 1
酸性强弱
CHCOONa溶液的pH
3
向含有酚酞的 NaCO 溶液中加入少量 证明NaCO 溶液中存在水解
2 3 2 3
4
BaCl 固体,溶液红色变浅 平衡
2
分别测定室温下等物质的量浓度的NaSO
2 3
5 证明非金属性:S>C
与NaCO 溶液的pH,后者较大
2 3
将NaOH溶液滴入某溶液中加热,放出的
6 证明溶液中有NH
气体能使湿润的红色石蕊试纸变蓝
分别通入硝酸银溶液中,产生淡黄色沉淀
7 鉴别溴蒸气和NO
2
的是溴蒸气
在醋酸钠溶液中滴入酚酞溶液,加热后红
8 证明盐类水解是吸热反应
色加深
将硫酸酸化的HO 溶液滴入Fe(NO ) 溶液
2 2 3 2
9 证明氧化性:HO 比Fe3+强
2 2
中,溶液变黄色
往黄色固体难溶物 PbI 中加水,振荡,静
2
证明难溶物存在沉淀溶解
10 置。取上层清液,然后加入NaI固体,产
平衡
生黄色沉淀
向AgCl悬浊液中加入NaI溶液时出现黄色
11 K (AgCl)< K (AgI)
sp sp
沉淀
先在托盘上各放一张滤纸,然后在右盘上
12 称取2.0 g NaOH固体
添加2 g砝码,左盘上添加NaOH固体
13 将FeCl 固体溶解于适量蒸馏水 配制FeCl 溶液
3 3
向沸水中逐滴加入 1~2 mL FeCl 饱和溶
3
14 制备Fe(OH) 胶体
3
液,搅拌并继续煮沸出现浑浊
15 测定等物质的量浓度的盐酸、硝酸的pH 比较Cl、N的非金属性强弱证明二者是离子化合物还是
16 用熔融氧化铝、CCl 做导电性实验
4
共价化合物
向含有少量FeCl 的MgCl 溶液中加入足量
3 2
17 除去MgCl 溶液中少量FeCl
2 3
Mg(OH) 粉末,搅拌一段时间后过滤
2
将CHCHBr与NaOH溶液共热,冷却后,
3 2
检验 CHCHBr 中存在的溴
3 2
18 取出上层水溶液,加入AgNO 溶液,观察
3
元素
是否产生淡黄色沉淀
取一定质量的样品与足量盐酸反应,用碱 测定NaCO(含NaCl)样品
2 3
19
石灰吸收产生的气体 纯度
20 将洗净的容量瓶放在烘箱中烘干 缩短容量瓶干燥的时间
答案 1.× 2.× 3.× 4.√ 5.× 6.√ 7.√ 8.√ 9.× 10.√ 11.× 12.×
13.×
14.× 15.× 16.√ 17.√ 18.× 19.× 20.×