文档内容
[复习目标] 1.掌握常见离子反应发生的条件。2.掌握常见离子的检验方法。
1.下列各组离子在指定的溶液中,一定能大量共存的打“√”,不能大量共存的打“×”。
(1)c (H+)=10-12 mol·L-1的溶液:Na+、K+、CO、SO( )
水
(2)使酚酞变红色的溶液:Na+、Cu2+、Fe2+、NO( )
(3)常温下,pH=12的溶液:K+、Cl-、SO( )
(4)c(H+)=0.1 mol·L-1的溶液:Na+、NH、SO、SO( )
2
(5)使pH试纸显蓝色的溶液:Cu2+、NO、Fe3+、SO( )
(6)与铝粉反应放出H 的无色溶液:NO、Al3+、Na+、SO( )
2
(7)使红色石蕊试纸变蓝的溶液:SO、CO、Na+、K+( )
(8)常温下,=1×10-12的溶液:K+、AlO、CO、Na+( )
(9)中性溶液:Fe3+、Al3+、NO、SO( )
(10)使甲基橙变红色的溶液:Mg2+、K+、SO、SO( )
答案 (1)× (2)× (3)√ (4)× (5)× (6)× (7)√ (8)√ (9)× (10)×
2.按要求回答下列问题:
某溶液中可能含有以下离子:NH、K+、Na+、H+、Mg2+、Al3+、Ba2+、Fe3+、I-、NO、
CO、SO。
(1)用pH试纸检验溶液呈强酸性,则溶液中一定含有________,一定不含________。
(2)取出部分溶液,加入少量CCl 及数滴新制氯水,振荡静置后CCl 层呈紫红色,则溶液中
4 4
一定含有________,一定不含________。
(3)另取部分溶液,向其中加入NaOH溶液至溶液呈碱性,滴加过程中溶液均无沉淀产生,
则溶液中一定不含________。
(4)取(3)中的部分碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,则溶
液中一定含有______________________________________________________________。
(5)另取(3)中的部分碱性溶液,加入 NaCO 溶液,有白色沉淀产生,则溶液中一定含有
2 3
__________,一定不含有________。
(6)通过上述实验可以判断溶液中一定存在的离子是________________________,一定不存
在的离子是____________________________;不能确定的离子是________,要进一步确定该
离子,需补充的实验是______(写实验名称)。答案 (1)H+ CO (2)I- Fe3+、NO (3)Mg2+、Al3+ (4)NH (5)Ba2+ SO (6)H+、I-、
NH、Ba2+ Mg2+、Al3+、Fe3+、NO、CO、SO K+、Na+ 焰色试验
1.离子共存问题审题“三大”注意
(1)审清题干中的要求:①一定能大量共存;②可能大量共存;③不能大量共存。
(2)应注意题干中提示的水的电离程度:室温下,当由水电离出的c(H+)或c(OH-)小于1×10-
7 mol·
L-1时,水的电离受到抑制,溶液可能为酸性溶液或碱性溶液;当由水电离出的c(H+)或c(OH
-)大于1×10-7 mol·L-1时,水的电离得到促进,溶液可能为弱酸盐溶液或弱碱盐溶液。
(3)注意正确理解“透明溶液”,如NaCl溶液、KOH溶液为无色透明溶液,CuSO 溶液、
4
FeCl 溶液是有色透明溶液,不能认为“有色”就不透明。
3
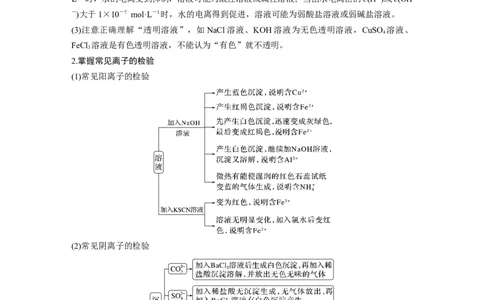
2.掌握常见离子的检验
(1)常见阳离子的检验
(2)常见阴离子的检验
角度一 离子共存
1.(2022·湖北,4)下列各组离子在给定溶液中能大量共存的是( )A.在0.1 mol·L-1氨水中:Ag+、Cu2+、NO、SO
B.在0.1 mol·L-1氯化钠溶液中:Fe3+、I-、Ba2+、HCO
C.在0.1 mol·L-1醋酸溶液中:SO、NH、Br-、H+
D.在0.1 mol·L-1硝酸银溶液中:K+、Cl-、Na+、CO
答案 C
解析 氨水显碱性,会与Ag+、Cu2+反应,不能大量共存,A项错误;Fe3+、I-会发生氧化
还原反应,不能大量共存,且Fe3+与HCO发生相互促进的水反应,也不能大量共存,B项
错误;醋酸溶液显酸性,在醋酸溶液中SO、NH、Br-、H+均不会发生反应,能大量共存,
C项正确;硝酸银中的银离子会与Cl-、CO反应,不能大量共存,D项错误。
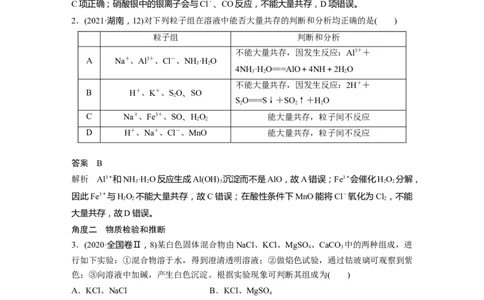
2.(2021·湖南,12)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )
粒子组 判断和分析
不能大量共存,因发生反应:Al3++
A Na+、Al3+、Cl-、NH ·H O
3 2
4NH ·H O===AlO+4NH+2HO
3 2 2
不能大量共存,因发生反应:2H++
B H+、K+、SO、SO
2
SO===S↓+SO ↑+HO
2 2 2
C Na+、Fe3+、SO、HO 能大量共存,粒子间不反应
2 2
D H+、Na+、Cl-、MnO 能大量共存,粒子间不反应
答案 B
解析 Al3+和NH ·H O反应生成Al(OH) 沉淀而不是AlO,故A错误;Fe3+会催化HO 分解,
3 2 3 2 2
因此Fe3+与HO 不能大量共存,故C错误;在酸性条件下MnO能将Cl-氧化为Cl ,不能
2 2 2
大量共存,故D错误。
角度二 物质检验和推断
3.(2020·全国卷Ⅱ,8)某白色固体混合物由NaCl、KCl、MgSO 、CaCO 中的两种组成,进
4 3
行如下实验:①混合物溶于水,得到澄清透明溶液;②做焰色试验,通过钴玻璃可观察到紫
色;③向溶液中加碱,产生白色沉淀。根据实验现象可判断其组成为( )
A.KCl、NaCl B.KCl、MgSO
4
C.KCl、CaCO D.MgSO 、NaCl
3 4
答案 B
解析 由信息①得到澄清透明溶液,可排除碳酸钙;由信息②焰色试验透过钴玻璃可观察到
紫色,说明含有钾元素,可推测含有氯化钾;由信息③向溶液中加入碱产生白色沉淀,可推
测含有硫酸镁,所以B正确。
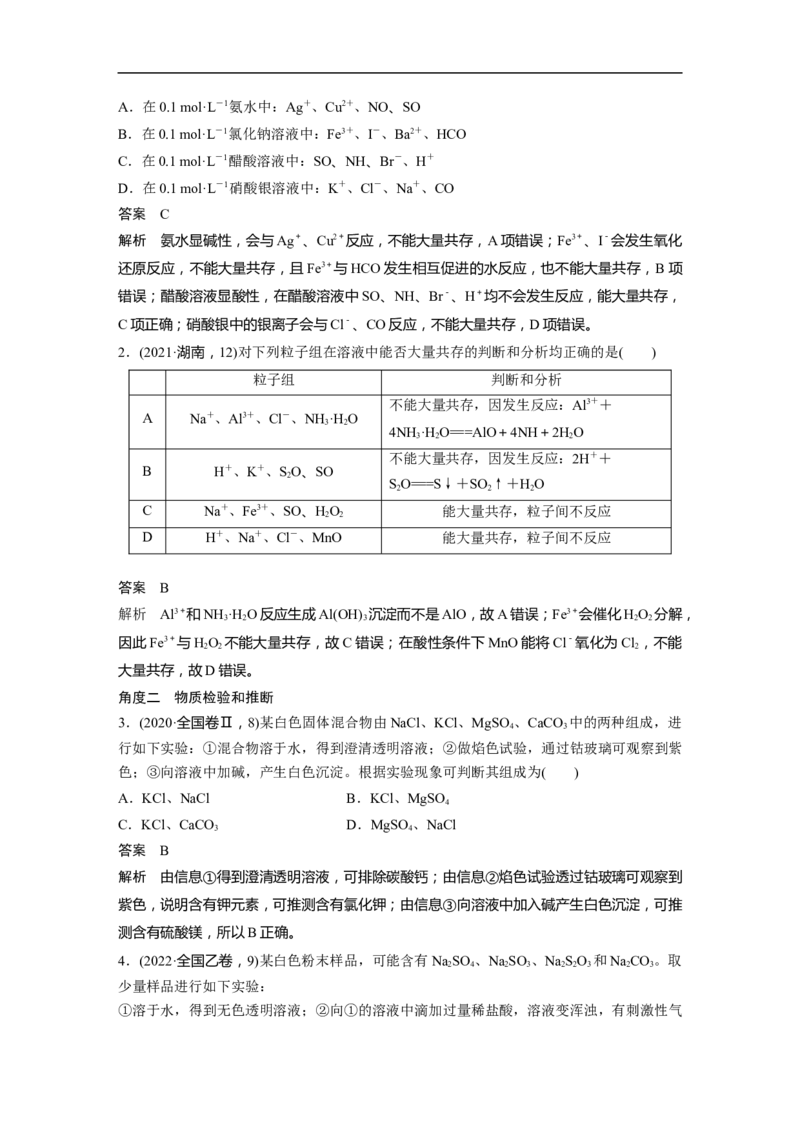
4.(2022·全国乙卷,9)某白色粉末样品,可能含有NaSO 、NaSO 、NaSO 和NaCO。取
2 4 2 3 2 2 3 2 3
少量样品进行如下实验:
①溶于水,得到无色透明溶液;②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出,离心分离;③取②的上层清液,向其中滴加BaCl 溶液有沉淀生成。
2
该样品中确定存在的是( )
A.NaSO 、NaSO
2 4 2 2 3
B.NaSO 、NaSO
2 3 2 2 3
C.NaSO 、NaCO
2 4 2 3
D.NaSO 、NaCO
2 3 2 3
答案 A
解析 向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出,说明固体中存在
NaSO ,发生反应:SO+2H+===S↓+HO+SO ↑,由于盐酸过量,向②的上层清液中
2 2 3 2 2 2
滴加BaCl 溶液,有沉淀生成,则沉淀为BaSO ,说明固体中存在NaSO ,不能确定是否有
2 4 2 4
NaSO 和NaCO ,NaSO 、NaCO 与过量稀盐酸反应的现象可以被NaSO 与过量稀盐酸
2 3 2 3 2 3 2 3 2 2 3
反应的现象覆盖掉。
考向一 离子共存
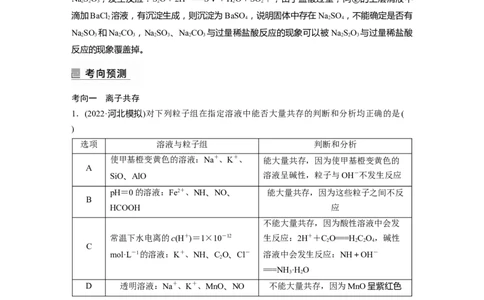
1.(2022·河北模拟)对下列粒子组在指定溶液中能否大量共存的判断和分析均正确的是(
)
选项 溶液与粒子组 判断和分析
使甲基橙变黄色的溶液:Na+、K+、 能大量共存,因为使甲基橙变黄色的
A
SiO、AlO 溶液呈碱性,粒子与OH-不发生反应
pH=0的溶液:Fe2+、NH、NO、 能大量共存,因为这些粒子之间不反
B
HCOOH 应
不能大量共存,因为酸性溶液中会发
常温下水电离的c(H+)=1×10-12 生反应:2H++C O===HC O,碱性
2 2 2 4
C
mol·L-1的溶液:K+、NH、C O、Cl- 溶液中会发生反应:NH+OH-
2
===NH ·H O
3 2
D 透明溶液:Na+、K+、MnO、NO 不能大量共存,因为MnO呈紫红色
答案 C
解析 甲基橙的变色范围为3.1~4.4,使甲基橙变黄色的溶液可能呈酸性、中性或碱性,酸
性条件下:2H++SiO===HSiO↓、H++AlO+HO===Al(OH) ↓,A项错误;pH=0的溶
2 3 2 3
液呈强酸性,会发生反应:3Fe2++NO+4H+===3Fe3++NO↑+2HO,B项错误;常温下
2
水电离的c(H+)=1×10-12 mol·L-1的溶液可能是酸性溶液,也可能是碱性溶液,酸性溶液
中会发生反应:2H++C O===HC O,碱性溶液中会发生反应:NH+OH-===NH ·H O,不
2 2 2 4 3 2
能大量共存,C项正确;透明溶液可能是有色溶液,也可能是无色溶液,D项错误。2.(2022·辽宁沈阳二中二模)常温下,下列各组离子在指定溶液中一定能够大量共存的是(
)
A.c(H+)=c(OH-)的溶液中:Na+、Fe3+、SO、Cl-
B.水电离的c(H+)=1×10-13 mol·L-1的溶液中:K+、Na+、AlO、CO
C.c(OH-)=1×10-13 mol·L-1的溶液中:NH、Ca2+、Cl-、NO
D.与Al反应能放出H 的溶液中:Ca2+、K+、NO、SO
2
答案 C
解析 Fe3+水解显酸性,不能在c(H+)=c(OH-)的溶液中大量共存,A不符合题意;水电离
的c(H+)=1×10-13 mol·L-1的溶液可能是酸性溶液,也可能是碱性溶液,酸性溶液中
AlO、CO不能大量共存,B不符合题意;c(OH-)=1×10-13 mol·L-1的溶液中c(H+)=0.1
mol·L-1,溶液呈强酸性,NH、Ca2+、Cl-、NO之间相互不反应,能够在酸性溶液中大量共
存,C符合题意;Ca2+、SO可形成微溶物CaSO 而不能大量共存,D不符合题意。
4
考向二 离子、物质推断
3.(2022·广东清远高三期末)某强酸性溶液中可能存在Al3+、Fe2+、NH、Ba2+、Cl-、CO、
SO、NO中的若干种,为确定溶液组成进行如下实验:
(1)取100 mL原溶液,加入足量Ba(NO ) 溶液,有白色沉淀a和无色气体b生成,过滤得滤
3 2
液c。
(2)往(1)所得滤液c中加入足量的NaOH溶液并加热,可得气体d和沉淀e,过滤。
(3)取(2)中过滤所得滤液,通入少量的CO,有白色沉淀f生成。
2
下列有关判断正确的是( )
A.试液中一定没有Ba2+、CO、NO、Cl-
B.试液中一定有Fe2+、NH、Al3+、SO
C.气体b和气体d在一定条件下能发生反应生成一种单质和一种无色液体
D.沉淀f一定含有Al(OH) ,可能含有BaCO
3 3
答案 C
解析 在强酸性溶液中,CO不能大量存在,Fe2+和NO也不能同时存在,钡离子和碳酸根
离子不共存;根据实验(1)可知溶液中一定不存在Ba2+、NO,一定存在SO、Fe2+,气体b
为 NO,沉淀 a 为 BaSO ;根据实验(2)可知溶液中含有 NH,气体 d 为 NH ,沉淀 e 为
4 3
Fe(OH) ,可能含有Al3+,因为氢氧化铝溶于氢氧化钠;根据实验(3)可知原溶液中可能含有
3
Al3+,沉淀f可能为BaCO 或BaCO 和Al(OH) 的混合物,因为实验(1)中的Ba(NO ) 溶液是
3 3 3 3 2
过量的。由上述分析可知,原溶液中一定没有的离子为Ba2+、CO、NO,A项错误;由上述
分析可知,原溶液中可能含有Al3+,B项错误;一氧化氮和氨气在一定条件下可以发生反应
生成氮气和水,C项正确;沉淀f一定含有BaCO ,可能含有Al(OH) ,D项错误。
3 3
4.(2022·陕西咸阳一模)某100 mL溶液可能含有Na+、NH、Fe3+、CO、SO、Cl-中的若干
种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,气体全部逸出):下列说法错误的是( )
A.原溶液一定存在CO,理由是沉淀①在盐酸中部分溶解
B.是否存在Na+只有通过焰色试验才能确定
C.原溶液一定不存在Fe3+,可能存在Cl-
D.原溶液中c(Na+)≥0.1 mol·L-1
答案 B
解析 加入BaCl 溶液之后,有沉淀生成,且加入过量的盐酸之后,沉淀质量减少,则说明
2
一定有CO、SO,一定没有Fe3+(Fe3+和CO会发生相互促进的水解反应,不能共存),且沉
淀②为BaSO ,n(BaSO)==0.01 mol,m(BaCO)=4.30 g-2.33 g=1.97 g,则n(BaCO)=
4 4 3 3
=0.01 mol;加入NaOH溶液产生0.672 L(标准状况)气体,则溶液中含有NH,n(NH)=0.03
mol;CO和SO所带的负电荷的物质的量为0.01 mol×2+0.01 mol×2=0.04 mol,NH所
带的正电荷的物质的量为0.03 mol×1=0.03 mol,根据电荷守恒,可以推断出溶液中一定含
有Na+,且最少为0.01 mol(因无法判断是否有Cl-,如果有Cl-,需要多余的Na+去保持溶
液的电中性),据此分析解答。
专题强化练
1.(2022·山西吕梁一模)常温下,下列各组离子在指定溶液中可能大量共存的是( )
A.在=1×1012的溶液中:HCO、K+、Na+、SO
B.含有大量Fe3+的溶液中:Na+、OH-、Br-、K+
C.pH=0的溶液中:Na+、K+、SO、SO
2
D.在=1×10-12 mol·L-1的溶液中:Na+、Ba2+、Cl-、Br-
答案 D
解析 =1×1012的溶液显碱性,含有大量OH-,OH-与HCO反应产生HO、CO,不能大
2
量共存,A错误;含有大量Fe3+的溶液中,Fe3+与OH-反应产生Fe(OH) 沉淀而不能大量共
3
存,B错误;pH=0的溶液呈强酸性,含有大量H+,H+与SO会反应生成HO、S、SO 而
2 2 2
不能大量共存,C错误;=1×10-12 mol·L-1的溶液呈碱性,含有大量OH-,OH-与Na+、
Ba2+、Cl-、Br-不能发生反应,可以大量共存,D正确。
2.(2022·辽宁一模)常温下,下列各组离子在指定溶液中可能大量共存的是( )
A.含NH的溶液中:CO、SiO、SO、Na+B.由水电离产生的c(OH-)=1×10-13 mol·L-1的溶液中:K+、Na+、I-、C O
2
C.在有色透明溶液中:K+、Fe2+、[Fe(CN) ]3-、NO
6
D.加入甲基橙显黄色的溶液:Fe3+、Ba2+、Br-、K+
答案 B
解析 铵根离子和硅酸根离子会发生相互促进的水解反应而不能大量共存,A不符合题意;
水电离产生的c(OH-)=1×10-13 mol·L-1的溶液可能显酸性也可能显碱性,若为碱性溶液,
四种离子相互之间不反应,也不与氢氧根离子反应,可以大量共存,B符合题意;K+、Fe2
+和[Fe(CN) ]3-生成蓝色沉淀而不能大量共存,C不符合题意;加入甲基橙显黄色的溶液的
6
pH>4.4,Fe3+不能大量存在,D不符合题意。
3.(2022·河北邯郸一模)下列各组微粒在溶液中可以大量共存,且在加入试剂X后发生反应
的离子方程式书写也正确的是( )
发生反应的
选项 微粒组 试剂X
离子方程式
Al3++3HCO===3CO↑+
2
A Cl-、NO、Al3+、NH 少量NaHCO 溶液
3
Al(OH) ↓
3
B NH、Fe2+、I-、SO 少量氯水 2Fe2++Cl===2Fe3++2Cl-
2
C Al3+、Ba2+、AlO、NO 适量的NaSO Ba2++SO===BaSO↓
2 4 4
SO+S2-+4H+===2S↓+
D Na+、SO、S2-、Cl- 适量HCl
2HO
2
答案 A
解析 Al3+和HCO发生相互促进的水解反应生成氢氧化铝沉淀和二氧化碳气体:Al3++
3HCO===3CO↑+Al(OH) ↓,A项正确;I-的还原性强于Fe2+的还原性,加入少量氯水时,
2 3
离子方程式为2I-+Cl===I+2Cl-,B项错误;Al3+与AlO会发生相互促进的水解反应生成
2 2
Al(OH) ,C项错误;亚硫酸根离子和硫离子在酸性条件下发生氧化还原反应生成单质 S,
3
故加入适量HCl的离子方程式为SO+2S2-+6H+===3S↓+3HO,D项错误。
2
4.下列说法正确的是( )
A.向溶液X中滴加少量NaOH稀溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝,
无法证明溶液X中是否存在NH
B.向某溶液中加入一定量稀盐酸,产生的气体使澄清石灰水变浑浊,溶液中一定含有CO
C.取少量某溶液于试管中,滴加少量氯水,振荡;再滴入几滴KSCN溶液,溶液变红色,
则原溶液中一定含有Fe3+
D.用洁净的铂丝棒蘸取某溶液在无色火焰上灼烧,透过蓝色钴玻璃观察到紫色,则该溶液
中不含钠元素
答案 A解析 向溶液X中滴加少量NaOH稀溶液,将湿润的红色石蕊试纸置于试管口,试纸不变
蓝,可能是原溶液中无NH,也可能是溶液浓度较小,反应产生的NH ·H O少,没有分解产
3 2
生NH ,因此无法证明溶液X中是否存在NH,A正确;向某溶液中加入一定量稀盐酸,产
3
生的气体使澄清石灰水变浑浊,该气体可能是CO ,也可能是SO ,因此溶液中可能含有
2 2
CO,也可能含有HCO或HSO或SO,B错误;取少量某溶液于试管中,滴加少量氯水,振
荡,再滴入几滴KSCN溶液,溶液变红色,则滴加氯水后的溶液中含有 Fe3+,该Fe3+可能
是原溶液中含有的,也可能是Fe2+被氧化产生的,因此不能确定原溶液中是否含Fe3+,C错
误;用洁净的铂丝棒蘸取某溶液在无色火焰上灼烧,透过蓝色钴玻璃观察到火焰呈紫色,则
该溶液中一定含有钾元素,但不能确定是否含钠元素,D错误。
5.某固体混合物由NaCl、BaCl 、Al (SO ) 、FeCl 、NaCO 中的两种组成,进行如下实验:
2 2 4 3 3 2 3
①将混合物溶于水,溶液变浑浊同时有气泡产生;②向①反应液中滴加稀硫酸至过量,沉淀
完全溶解;③向②溶液中滴加KSCN溶液,未见明显现象;④取③反应后的液体做焰色试
验,可观察到黄色火焰,根据实验现象可判断其组成为( )
A.BaCl 、Al (SO ) B.BaCl 、NaCO
2 2 4 3 2 2 3
C.Al (SO )、NaCO D.FeCl 、NaCO
2 4 3 2 3 3 2 3
答案 C
解析 根据实验①可知溶于水的过程中发生碳酸根离子和 Al3+或Fe3+的反应,根据实验②
可知,沉淀不是BaSO ,结合实验④,可确定一定有NaCO ,根据实验③可知没有FeCl ,
4 2 3 3
则一定有Al (SO ),一定没有BaCl 。
2 4 3 2
6.某固体混合物X含有AlCl 、FeCl 、NaHCO 、NaAlO 和NaHSO 中的几种,进行实验,
3 3 3 2 4
X与水作用有气泡冒出,得到有色沉淀Y和弱碱性溶液Z。下列说法正确的是( )
A.混合物X中必定含有NaHCO 、FeCl ,可能含有NaHSO
3 3 4
B.取有色沉淀Y于试管中,加入浓氢氧化钠溶液,若沉淀部分溶解,证明固体混合物X中
含有AlCl
3
C.溶液Z中肯定含有NaHCO
3
D.向溶液Z中加入铜粉,铜粉会溶解
答案 A
解析 X与水作用有气泡冒出,得到有色沉淀Y和弱碱性溶液Z,能生成气体的物质只有
NaHCO ,生成二氧化碳可能的原因是 NaHCO 与 NaHSO 反应,或者 AlCl 、 FeCl 与
3 3 4 3 3
NaHCO 发生相互促进的水解反应,生成的有色沉淀为Fe(OH) ,则一定存在FeCl ;溶液显
3 3 3
弱碱性,还可能NaHCO 与NaAlO 发生反应生成Al(OH) 和NaCO ,或者NaHCO 有剩余。
3 2 3 2 3 3
混合物X中必定含有NaHCO 、FeCl ,可能含有NaHSO ,A项正确;取有色沉淀Y于试管
3 3 4
中,加入浓氢氧化钠溶液,若沉淀部分溶解,说明沉淀中有 Al(OH) ,Al(OH) 可能是
3 3
NaHCO 与NaAlO 反应生成的,所以不一定含有 AlCl ,B项错误;溶液 Z中可能含有
3 2 3
NaHCO ,C项错误;溶液Z呈弱碱性,则Z中一定不存在FeCl ,加入铜粉,铜粉不会溶解,
3 3D项错误。
7.某白色粉末可能含有CaCO 、BaCl 、NaNO 、KSO 、CuSO 中的一种或几种。现进行
3 2 3 2 4 4
如下操作:
根据以上实验现象,下列说法不正确的是( )
A.白色粉末中一定不含CuSO
4
B.白色粉末中可能含有NaNO 、BaCl
3 2
C.该白色粉末中一定含有CaCO 、KSO
3 2 4
D.无色溶液1发生焰色试验时,可透过蓝色钴玻璃片观察到火焰呈紫色
答案 B
解析 白色粉末溶于水得到白色沉淀,说明含有不溶于水的CaCO ,得到无色溶液,说明不
3
含使溶液呈蓝色的CuSO ,无色溶液1中加入BaCl 溶液和稀硝酸,有白色沉淀生成,说明
4 2
样品中含有KSO ,那么样品一定不含BaCl ,而NaNO 是否含有,根据现有的实验无法确
2 4 2 3
定,则A、C正确,B错误;无色溶液1中含有KSO ,因此发生焰色试验时,可透过蓝色
2 4
钴玻璃片观察到火焰呈紫色,故D正确。
8.某试液中只可能含有K+、NH、Fe2+、Al3+、Cl-、SO、CO、AlO中的若干种离子,离
子浓度均为0.1 mol·L-1。某同学进行了如下实验:
下列说法正确的是( )
A.无法确定原试液中是否含有Al3+、Cl-
B.滤液X中大量存在的阳离子有NH、Fe2+和Ba2+
C.无法确定沉淀C的成分
D.原试液中存在的离子为NH、Fe2+、Cl-、SO
答案 D
解析 试液中加入过量稀硫酸无明显现象,说明无 CO、AlO;再加入过量硝酸钡溶液有气
体生成,说明有Fe2+存在且被氧化,沉淀A为硫酸钡,因稀硫酸过量,故不能说明原溶液
中是否含有SO;再加入过量NaOH溶液有气体生成,说明存在NH,气体为氨气,沉淀B
为氢氧化铁红褐色沉淀;再向滤液中通入少量 CO ,先与OH-、Ba2+反应生成BaCO ,沉
2 3
淀C含有碳酸钡,可能含有Al(OH) 。从上述分析可以确定试液中一定含有NH、Fe2+,一
3
定不含AlO、CO。因为离子浓度均为0.1 mol·L-1,只能含有NH、Fe2+、Cl-、SO才能保证电荷守恒,K+、Al3+必然不能存在。