文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题20
1.化学创造美好生活。下列劳动项目涉及反应的方程式错误的是
A.船舶工程师在船体上镶嵌锌块,防止反应:Fe-3e-=Fe3+
B.药剂师用NaHCO 作抗胃酸药:HCO H+=CO↑+HO
3 + 2 2
C.工人用FeCl 溶液制作电路板:2Fe3++Cu=2Fe2++Cu2+
3
D.消防员用泡沫灭火器灭火:Al3++3HCO Al(OH) ↓+3CO↑
= 3 2
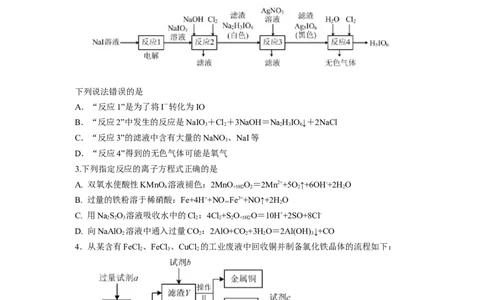
2.正高碘酸(H IO )是白色结晶性粉末,溶于水,主要用作氧化剂和分析试剂。由NaI制取
5 6
HIO 的实验流程如图所示:
5 6
下列说法错误的是
A.“反应1”是为了将I-转化为IO
B.“反应2”中发生的反应是NaIO +Cl+3NaOH=NaHIO ↓+2NaCl
3 2 2 3 6
C.“反应3”的滤液中含有大量的NaNO 、NaI等
3
D.“反应4”得到的无色气体可能是氧气
3.下列指定反应的离子方程式正确的是
A. 双氧水使酸性KMnO 溶液褪色:2MnO O=2Mn2++5O ↑+6OH-+2H O
4 +5H2 2 2 2
B. 过量的铁粉溶于稀硝酸:Fe+4H++NO Fe3++NO↑+2HO
= 2
C. 用NaSO 溶液吸收水中的Cl:4Cl+SO O=10H++2SO+8Cl-
2 2 3 2 2 2 +5H2
D. 向NaAlO 溶液中通入过量CO:2AlO+CO+3H O=2Al(OH) ↓+CO
2 2 2 2 3
4.从某含有FeCl 、FeCl 、CuCl 的工业废液中回收铜并制备氯化铁晶体的流程如下:
2 3 2
则下列说法错误的是
A.试剂a是铁、试剂b是盐酸
B.试剂c是氯气,相应的反应为2Fe2++Cl=2Fe3++2Cl-
2
C.操作Ⅰ、操作Ⅱ所用仪器相同,均要用到烧杯、分液漏斗、玻璃棒
D.加入过量试剂c之后,溶液W依然能使少量酸性KMnO 溶液褪色
45.分类法在化学学科发展中起到了非常重要的作用,下列分类依据合理的是
①根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物等
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否有丁达尔效应将分散系分为溶液、胶体和浊液
④根据组成元素的种类将纯净物分为单质和化合物
⑤根据水溶液溶液能否导电将物质分为电解质和非电解质
A. ②④⑤ B. ②③④ C. ①③⑤ D. ①②④
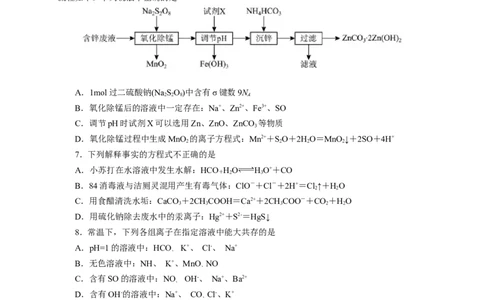
6.以含锌废液(主要成分为ZnSO,含少量的Fe2+、Mn2+)为原料制备ZnCO ·2Zn(OH) 的实验
4 3 2
流程如下。下列说法不正确的是
A.1mol过二硫酸钠(Na SO)中含有σ键数9N
2 2 8 A
B.氧化除锰后的溶液中一定存在:Na+、Zn2+、Fe3+、SO
C.调节pH时试剂X可以选用Zn、ZnO、ZnCO 等物质
3
D.氧化除锰过程中生成MnO 的离子方程式:Mn2++SO+2HO=MnO ↓+2SO+4H+
2 2 2 2
7.下列解释事实的方程式不正确的是
A.小苏打在水溶液中发生水解:HCO HO HO++CO
+ 2 3
B.84消毒液与洁厕灵混用产生有毒气体:ClO-+Cl-+2H+=Cl↑+HO
2 2
C.用食醋清洗水垢:CaCO +2CHCOOH=Ca2++2CHCOO-+CO+HO
3 3 3 2 2
D.用硫化钠除去废水中的汞离子:Hg2++S2-=HgS↓
8.常温下,下列各组离子在指定溶液中能大共存的是
A.pH=1的溶液中:HCO K+、 Cl-、 Na+
、
B.无色溶液中:NH、 K+、MnO NO
、
C.含有SO的溶液中:NO OH-、 Na+、Ba2+
、
D.含有OH-的溶液中:Na+、 CO Cl-、K+
、
9.能正确表示下列反应的离子方程式的为
A.铜和稀硝酸反应:Cu+4H++2NO Cu2++2NO ↑+2HO
= 2 2
B.向酸性高锰酸钾溶液中通入少量二氧化硫:5SO +2MnO 2HO =5SO+2Mn2++4H+
2 + 2
C.氢氧化钡溶液中滴加少量明矾溶液:2Ba2++3OH-+Al3++2SO=Al(OH) ↓+2BaSO↓
3 4
D.铅酸蓄电池正极充电时的反应式:Pb-2e-+SO=PbSO
4
10.下列检验方法或指定反应的离子(或化学)方程式正确的是
A.向NaAlO 溶液中滴入Ca(HCO ) 溶液:AlO+HCO O=Al(OH) ↓+CO
2 3 2 +H2 3
B.用溴水检验丙烯醛CH=CHCHO中的碳碳双键:CH=CHCHO+Br→CHBr-CHBr-CHO
2 2 2 2C.NaS溶液吸收少量SO [已知K (H SO )>K (H S)]:S2-+SO+H O=SO HS↑
2 2 a2 2 3 a1 2 2 2 + 2
D.往二元弱酸亚磷酸(H PO )溶液中滴加过量的烧碱溶液:HPO +2OH-=HPO O
3 3 3 3 +2H2
11.物质A由4种元素组成,按如下流程进行实验。
已知:①每一步反应均完全 ②溶液D仅含一种溶质 ③沉淀E不溶于酸
④Ag SO 溶于HNO
2 4 3
请回答:
(1)物质A的组成元素为_________________(元素符号),其化学式为_________________。
(2)写出A与双氧水反应的化学方程式____________________________________________。
(3)写出F至G的离子方程式_____________________________________________________。
(4)设计实验检验溶液D中的主要离子_______________________。
12.工厂的含砷废水必须经过一定的处理。 某厂用某含砷废水(含HAsO、HSO 、及少量
2 2 4
Fe3+、Cu2+、Bi2+ )提取三氧化二砷(俗称砒霜,分子式:As O)的流程如下:
2 3
已知:K [Fe(OH) ]=2.8 ×10-3920 ,K [Cu(OH) ]=2.2 ×10-22,K [Bi(OH) ]=4.4 ×10-31。
sp 3 sp 2 sp 3
回答下列问题:
(1)滤渣a的成分是___________(写化学式)。
(2)“沉淀”时,CuSO 溶液必须过量的原因是______________________________________。
4
(3)写出“还原”时Cu(AsO ) 与HO、SO 发生反应的化学方程式:______________________。
2 2 2 2
(4)红色还原渣(不溶于水)“氧化”时反应的离子方程式为______________________________。
(5)“沉砷”后废水中残留的砷可用PFS(聚铁)进一步去除,用石灰乳调节废水的pH值,通入空
气,PFS用量[以表示]、终点pH值与砷去除率的关系如图所示。PFS除砷的最佳条件是_________。(6)当废水中砷质量浓度为5.0g·L-1时,若实验取75 L含砷废水,制得475.2 gAs O,则As元的
2 3
素回收率为________。
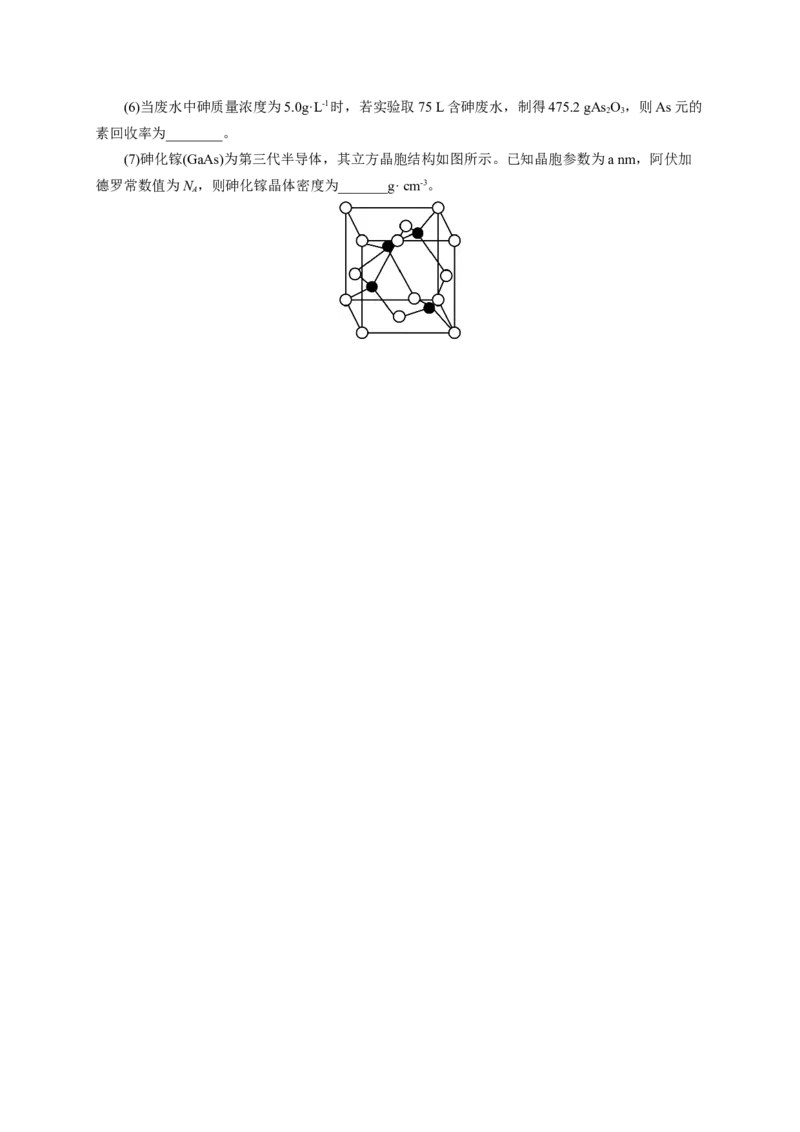
(7)砷化镓(GaAs)为第三代半导体,其立方晶胞结构如图所示。已知晶胞参数为a nm,阿伏加
德罗常数值为N ,则砷化镓晶体密度为_______g· cm-3。
A