文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题24
1.下列离子方程式对事实的表述正确的是
A.向碘化亚铁溶液中滴加少量稀硝酸:NO 2++4H+=3Fe3++NO↑+2HO
+3Fe 2
B.向NaClO溶液中通入少量SO :SO +ClO-+HO=SO+Cl-+2H+
2 2 2
C.向重水中加入NaO:NaO+2H18O=4Na++4OH-+18O↑
2 2 2 2 2 2
D.向硫代硫酸钠溶液中加入过量稀盐酸:SO +=SO ↑S↓+HO
2 +2H 2 2
2.下列各组离子在指定的溶液中,一定能大量共存的是
A.澄清透明的溶液中:Na+、H+、MnO Cl-
、
B.能使酚酞变红的溶液中:Ba2+、NO K+、I-
、
C.常温下,由水电离的c(H+)=10-14mol·L-1的溶液中:CO NH、SO、Na+
、
D.无色溶液中:SCN-、Cu2+、NO Cl-
、
3.下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙:CO CaCO +SO
+CaSO4 3
B.过量铁粉加入稀硝酸中:Fe+4H++NO Fe3++NO↑+2HO
= 2
C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-=AlO+2HO
2
D.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓
4.下列关于Na的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:OH-+2H++CO HCO 2HO
= + 2
B.碱转化为两种盐:2OH-+Cl=ClO-+Cl-+HO
2 2
C.过氧化物转化为碱:2O+2HO=4OH-+O↑
2 2
D.盐转化为另一种盐:NaSiO+2H+=HSiO↓+2Na+
2 3 2 3
5.能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH+2H O=AlO+4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +H O=HSiO HCO
+CO2 2 +
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO=
2 4 4
BaSO↓+2H O
4 2
6.科学的分类能够反映事物的本质特征,有利于人们分门别类地进行深入研究,下列分类方
法或概念表达科学合理的是
A.在水溶液中和熔融状态下都能导电的化合物才属于电解质
B.CaO、Al O、Fe O、NaO、CuO等金属氧化物都属于碱性氧化物
2 3 2 3 2 2
C.依据丁达尔效应可以将分散系分为胶体或非胶体(包括溶液和浊液)两大类
D.金刚石、石墨和C ,H 、D 和T,O 和O 分别属于碳、氢、氧的同位素
60 2 2 2 2 3
7.下列离子方程式正确的是
A.过量铁粉与稀硝酸反应:3Fe+NO +=3Fe3++NO↑+2HO
+4H 2B.铜与浓硫酸在加热条件下反应:Cu+4H++SO===Cu2++SO ↑+2HO
2 2
C.将二氧化硫通入溴水中,溴水褪色:SO +Br +HO=4H++2Br-+SO
2 2 2
D.向H18O中投入NaO 固体:H18O+2NaO=4Na++2OH-+218OH-+O↑
2 2 2 2 2 2 2
8.下列变化中涉及氧化还原反应的是
A.向溴化钠溶液中滴加AgNO 溶液,有浅黄色沉淀产生
3
B.向蛋白质溶液中滴入饱和NaCl溶液,有沉淀产生
C.向碱化的蔗糖水解液中滴加银氨溶液,水浴加热后有光亮的银镜出现
D.向含SO的溶液中滴入硝酸酸化的BaCl 溶液,有白色沉淀产生
2
9.关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是
2 3 6 2 2
A.KHIO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7g I 时,转移0.1mol电子 D.还原剂与氧化剂的物质的量之比为7∶1
2
10.下列解释事实的离子方程式正确的是
A.实验室盛碱液的试剂瓶不用玻璃塞:SiO+2OH-=SiO O
2 +H2
B.铁和稀硝酸反应制得浅绿色溶液:4H++Fe+NO 3++NO↑+2HO
=Fe 2
C.碳酸氢钠和少量氢氧化钙溶液反应:HCO 2++OH-=H O+CaCO ↓
+Ca 2 3
D.向次氯酸钙溶液中通入过量二氧化碳:2ClO-+H O+CO=2HClO+CO
2 2
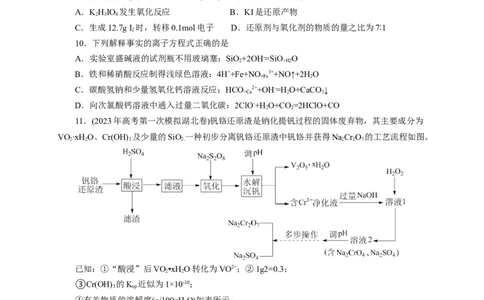
11.(2023年高考第一次模拟湖北卷)钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为
VO ∙xH O、Cr(OH) 及少量的SiO 一种初步分离钒铬还原渣中钒铬并获得NaCr O 的工艺流程如图。
2 2 3 2. 2 2 7
已知:①“酸浸”后VO ▪xH O转化为VO2+;②1g2=0.3;
2 2
③Cr(OH) 的K 近似为1×10-30;
3 sp
④有关物质的溶解度(g/100gHO)如表所示:
2
温度/℃ 20 40 60 80 100
NaCr O 183.6 215.1 269.2 376.4 415.0
2 2 7
NaSO 19.5 48.8 45.3 43.7 42.5
2 4
回答下列问题:
(1)写出“滤渣”的一种用途___________,“氧化”生成VO,反应中氧化剂与还原剂的物质
的量之比为___________。
(2)若“含Cr3+净化液”中c(Cr3+)=0.125mol·L-1,则“水解沉钒”调pH的范围是2.5~___________。(结果保留1位小数)
(3) “溶液1”中含CrO,加入HO 后发生的化学反应方程式为___________________________。
2 2
(4)“溶液2调pH”,所发生反应的离子方程式___________。
(5)“多步操作”包括蒸发浓缩、___________、冷却结晶、过滤、洗涤等步骤。
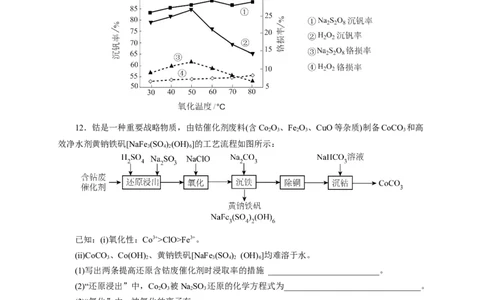
(6)研究温度对NaSO 与HO 的氧化-水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸
2 2 8 2 2
浸液初始温度在80℃左右,降低温度能耗增加。由图可知,分别采用NaSO、HO 进行“氧化”
2 2 8 2 2
时,应选择的适宜温度分别是_____,在“氧化”工艺中不采用HO 氧化的原因是___________(写
2 2
出两点)。
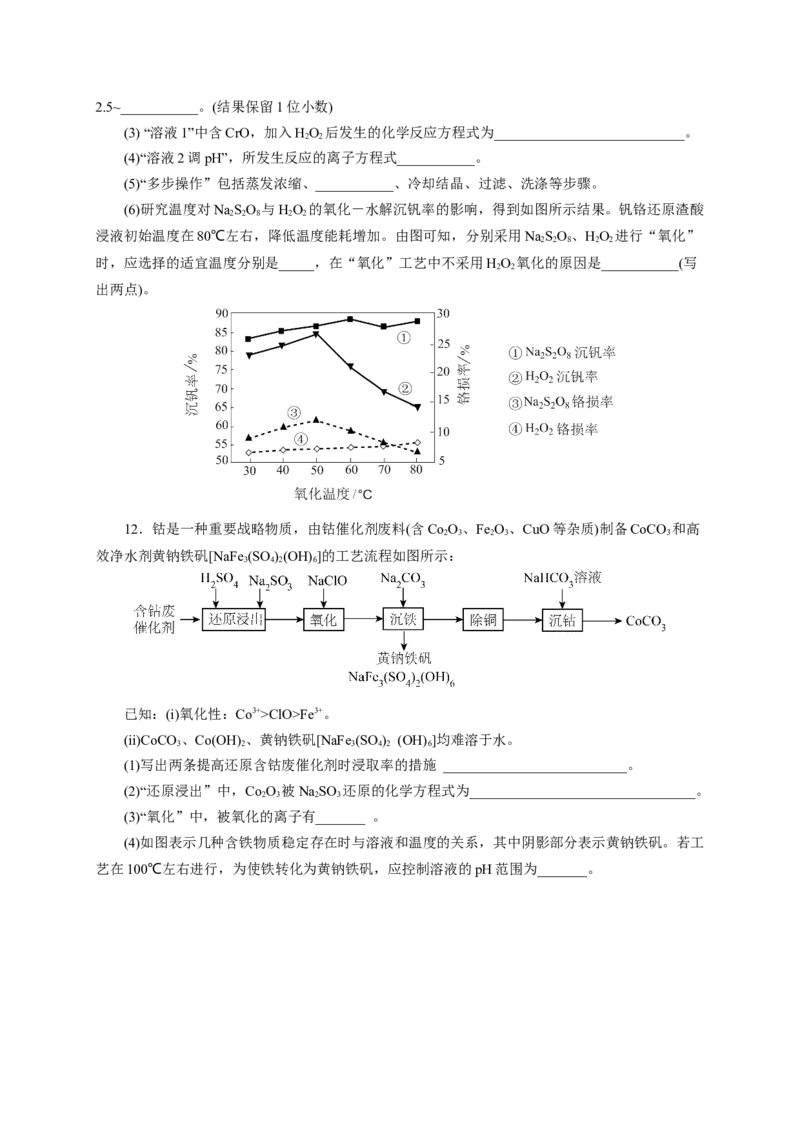
12.钴是一种重要战略物质,由钴催化剂废料(含Co O、Fe O、CuO等杂质)制备CoCO 和高
2 3 2 3 3
效净水剂黄钠铁矾[NaFe (SO )(OH) ]的工艺流程如图所示:
3 4 2 6
已知:(i)氧化性:Co3+>ClO>Fe3+。
(ii)CoCO 、Co(OH) 、黄钠铁矾[NaFe (SO ) (OH) ]均难溶于水。
3 2 3 4 2 6
(1)写出两条提高还原含钴废催化剂时浸取率的措施 __________________________。
(2)“还原浸出”中,Co O 被NaSO 还原的化学方程式为________________________________。
2 3 2 3
(3)“氧化”中,被氧化的离子有_______ 。
(4)如图表示几种含铁物质稳定存在时与溶液和温度的关系,其中阴影部分表示黄钠铁矾。若工
艺在100℃左右进行,为使铁转化为黄钠铁矾,应控制溶液的pH范围为_______。(5)若选用MnS“除铜”,计算常温下“除铜”反应的平衡常数K= _______ [已知常温下,
K (MnS)=2.6 ×10-13,K (CuS)=1.3×10-36]。
sp sp
(6)“沉钴”时,加入小苏打发生反应的离子反应方程式为______________________________,
不宜用 NaCO 代替NaHCO 的原因是____________________________________________。
2 3 3