文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题24
1.下列离子方程式对事实的表述正确的是
A.向碘化亚铁溶液中滴加少量稀硝酸:NO 2++4H+=3Fe3++NO↑+2HO
+3Fe 2
B.向NaClO溶液中通入少量SO :SO +ClO-+HO=SO+Cl-+2H+
2 2 2
C.向重水中加入NaO:NaO+2H18O=4Na++4OH-+18O↑
2 2 2 2 2 2
D.向硫代硫酸钠溶液中加入过量稀盐酸:SO +=SO ↑S↓+HO
2 +2H 2 2
答案:D
解析:A.稀HNO 少量,还原性:I->Fe2+,应该I-先反应,反应离子方程式为2NO -+
3 +6I
8H+=3I+2NO↑+4HO,A错误;
2 2
B.SO 少量,ClO-过量,H+与ClO-不共存,则反应离子方程式为SO +3ClO-+HO=SO+
2 2 2
Cl-+2HClO,B错误;
C.NaO 发生歧化反应,O 中的O来自于NaO,则18O 应在OH-中,C错误;
2 2 2 2 2
D.向硫代硫酸钠溶液中加入过量稀盐酸,发生反应的离子方程式为SO +=SO ↑S↓+HO,
2 +2H 2 2
D正确;
2.下列各组离子在指定的溶液中,一定能大量共存的是
A.澄清透明的溶液中:Na+、H+、MnO Cl-
、
B.能使酚酞变红的溶液中:Ba2+、NO K+、I-
、
C.常温下,由水电离的c(H+)=10-14mol·L-1的溶液中:CO NH、SO、Na+
、
D.无色溶液中:SCN-、Cu2+、NO Cl-
、
答案:B
解析:A.酸性条件下,MnO Cl-,不能大量共存,A错误;
可以氧化
B.能使酚酞变红的溶液为碱性溶液,碱性条件下,这些离子之间不存在任何反应可大量共存,
B正确;
C.常温下,由水电离的c(H+)=10-14mol·L-1的溶液是酸性或碱性溶液,酸性条件下,CO
不能大量
NH不能大量共存,C错误;
共存,碱性条件下,
D.Cu2+是蓝色的,无色溶液中不可能存在Cu2+,D错误;
3.下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙:CO CaCO +SO
+CaSO4 3
B.过量铁粉加入稀硝酸中:Fe+4H++NO Fe3++NO↑+2HO
= 2
C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-=AlO+2HO
2
D.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓
答案:A
解析:A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方程式为:
CO CaCO +SO,故A正确;
+CaSO4 3
B.过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,离子方程式应为:3Fe+8H++2NO3Fe2++2NO↑+4HO,故B错误;
= 2
C.硫酸铝溶液与少量氢氧化钾溶液反应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:
Al3++3OH-=Al(OH) ↓,故C错误;
3
D.硫化氢为弱电解质,书写离子方程式时不能拆,离子方程式应为:Cu2++H S=CuS↓+2H+,
2
故D错误;
4.下列关于Na的化合物之间转化反应的离子方程式书写正确的是
A.碱转化为酸式盐:OH-+2H++CO HCO 2HO
= + 2
B.碱转化为两种盐:2OH-+Cl=ClO-+Cl-+HO
2 2
C.过氧化物转化为碱:2O+2HO=4OH-+O↑
2 2
D.盐转化为另一种盐:NaSiO+2H+=HSiO↓+2Na+
2 3 2 3
答案:B
解析:A.向氢氧化钠溶液中通入足量的二氧化碳,碱可以转化成酸式盐,离子方程式为:
CO+OH-=HCO A错误;
2 ,故
B.氯气通入NaOH溶液中可以生成氯化钠和次氯酸钠两种盐,其离子方程式为:Cl+2OH-=
2
Cl-+ClO-+H O,故B正确;
2
C.钠的过氧化物为NaO,可以和水反应生成氢氧化钠,但在离子方程式里NaO 不能拆成离
2 2 2 2
子,故C错误;
D.硅酸钠溶于水,在离子方程式里要写成离子,故D错误;
5.能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH+2H O=AlO+4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +H O=HSiO HCO
+CO2 2 +
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO=
2 4 4
BaSO↓+2H O
4 2
答案:D
解析:A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO或
NO ,反应的离子方程式为4H++2NO 2-=S↓+2NO↑+2H O(浓)或8H++2NO 2-=3S↓+2NO↑+4H O(稀),
2 +S 2 2 +3S 2
A错误;
B.明矾在水中可以电离出Al3+,可以与氨水电离出的OH-发生反应生成Al(OH) ,但由于氨水
3
的碱性较弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为Al3++3NH·H O=
3 3 2
Al(OH) ↓+3NH,B错误;
3
C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则根据
其通入的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO O+CO=HSiO↓+CO
+H2 2 2 3 (CO2
少量)或SiO O+2CO=H SiO↓+2HCO 过量),C错误;
+2H2 2 2 3 (CO2
D.将等物质的量浓度的Ba(OH) 与NH HSO 溶液以体积比1∶2混合,Ba(OH) 电离出的OH-与
2 4 4 2
NH HSO 电离出的H+反应生成水,Ba(OH) 电离出的Ba2+与NH HSO 电离出的SO反应生成BaSO
4 4 2 4 4 4沉淀,反应的离子方程为为Ba2++2OH-+2H++SO=BaSO↓+2H O,D正确;
4 2
6.科学的分类能够反映事物的本质特征,有利于人们分门别类地进行深入研究,下列分类方
法或概念表达科学合理的是
A.在水溶液中和熔融状态下都能导电的化合物才属于电解质
B.CaO、Al O、Fe O、NaO、CuO等金属氧化物都属于碱性氧化物
2 3 2 3 2 2
C.依据丁达尔效应可以将分散系分为胶体或非胶体(包括溶液和浊液)两大类
D.金刚石、石墨和C ,H 、D 和T,O 和O 分别属于碳、氢、氧的同位素
60 2 2 2 2 3
答案:C
解析:A.在水溶液中或熔融状态下能导电的化合物属于电解质,故A错误;
B.Al O 属于两性氧化物,NaO 不属于碱性氧化物,故B错误;
2 3 2 2
C.丁达尔效应是胶体的特征性质,依据丁达尔效应可以将分散系分为胶体或非胶体(包括溶液
和独液)两大类,故C正确;
D.金刚石、石墨和C 互为同素异形体,O 和O 互为同素异形体,H、D 和T 都是单质,不
60 2 3 2 2 2
属于H的同位素,故D错误;
7.下列离子方程式正确的是
A.过量铁粉与稀硝酸反应:3Fe+NO +=3Fe3++NO↑+2HO
+4H 2
B.铜与浓硫酸在加热条件下反应:Cu+4H++SO===Cu2++SO ↑+2HO
2 2
C.将二氧化硫通入溴水中,溴水褪色:SO +Br +HO=4H++2Br-+SO
2 2 2
D.向H18O中投入NaO 固体:H18O+2NaO=4Na++2OH-+218OH-+O↑
2 2 2 2 2 2 2
答案:D
解析:A.过量铁粉与稀硝酸反应生成的Fe2+而不是Fe3+,A错误;
B.铜与浓硫酸在加热条件下反应离子方程式与化学方程式相同,因为浓硫酸是以分子的形式
存在的,不用拆成离子形式,CuSO 也因没有水存在而没有电离保留化学式,B错误;
4
C.原子不守恒,HO前应配2,C错误;
2
D.该反应离子方程式无误,D正确;
8.下列变化中涉及氧化还原反应的是
A.向溴化钠溶液中滴加AgNO 溶液,有浅黄色沉淀产生
3
B.向蛋白质溶液中滴入饱和NaCl溶液,有沉淀产生
C.向碱化的蔗糖水解液中滴加银氨溶液,水浴加热后有光亮的银镜出现
D.向含SO的溶液中滴入硝酸酸化的BaCl 溶液,有白色沉淀产生
2
答案:C
解析:A.离子方程式为Ag++Br-=AgBr↓,反应过程中无元素化合价的变化,不涉及氧化还原
反应,故A不符合题意;
B.向蛋白质溶液中滴入饱和NaCl溶液,蛋白质的溶解度降低从而析出,即发生盐析,不涉及
化学反应,故B不符合题意;
C.向碱化的蔗糖水解液中滴加银氨溶液,水浴加热后有光亮的银镜出现,说明生成了单质银,银元素的化合价发生变化,涉及氧化还原反应,故C符合题意;
D.离子方程式为SO+ Ba2+=BaSO ↓,反应过程中无元素化合价的变化,不涉及氧化还原反应,
4
故D不符合题意;
9.关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是
2 3 6 2 2
A.KHIO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7g I 时,转移0.1mol电子 D.还原剂与氧化剂的物质的量之比为7∶1
2
答案:D
解析:A.反应中I元素的化合价降低,发生得电子的反应,发生还原反应,A错误;
B.KI中的I-由HI变化而来,化合价没有发生变化,KI既不是氧化产物也不是还原产物,B
错误;
C.12.7g I 的物质的量为0.05mol,根据反应方程式,每生成4mol I 转移7mol电子,则生成
2 2
0.05mol I 时转移电子的物质的量为0.0875mol,C错误;
2
D.反应中HI为还原剂,KHIO 为氧化剂,在反应中每消耗1mol KHIO 就有7mol HI失电
2 3 6 2 3 6
子,则还原剂与氧化剂的物质的量的比为7:1,D正确;
10.下列解释事实的离子方程式正确的是
A.实验室盛碱液的试剂瓶不用玻璃塞:SiO+2OH-=SiO O
2 +H2
B.铁和稀硝酸反应制得浅绿色溶液:4H++Fe+NO 3++NO↑+2HO
=Fe 2
C.碳酸氢钠和少量氢氧化钙溶液反应:HCO 2++OH-=H O+CaCO ↓
+Ca 2 3
D.向次氯酸钙溶液中通入过量二氧化碳:2ClO-+H O+CO=2HClO+CO
2 2
答案:A
解析:A.碱性溶液中氢氧根离子会和玻璃中二氧化硅反应生成硅酸根离子,A正确;
B.铁和稀硝酸反应制得浅绿色溶液,说明铁过量生成亚铁离子,8H++3Fe+2NO 3Fe2++
=
2NO↑+4H O,B错误;
2
C.碳酸氢钠和少量氢氧化钙溶液反应,氢氧根离子完全反应生成碳酸钙沉淀:2HCO 2+
+Ca
+2OH-=2HO+CaCO ↓+CO
2 3 ,C错误;
D.次氯酸钙溶液中通入过量二氧化碳反应生成次氯酸和碳酸氢根离子:ClO-+H O+CO=
2 2
HClO+HCO
,D错误;
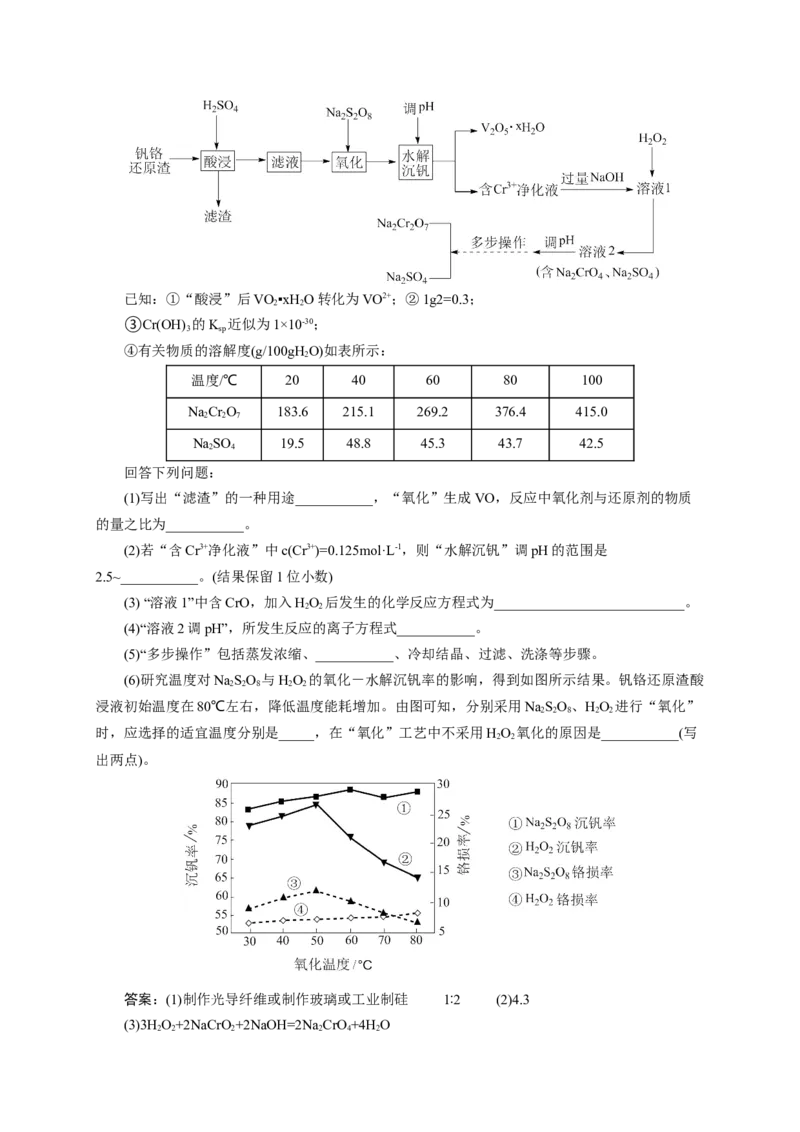
11.(2023年高考第一次模拟湖北卷)钒铬还原渣是钠化提钒过程的固体废弃物,其主要成分为
VO ∙xH O、Cr(OH) 及少量的SiO 一种初步分离钒铬还原渣中钒铬并获得NaCr O 的工艺流程如图。
2 2 3 2. 2 2 7已知:①“酸浸”后VO ▪xH O转化为VO2+;②1g2=0.3;
2 2
③Cr(OH) 的K 近似为1×10-30;
3 sp
④有关物质的溶解度(g/100gHO)如表所示:
2
温度/℃ 20 40 60 80 100
NaCr O 183.6 215.1 269.2 376.4 415.0
2 2 7
NaSO 19.5 48.8 45.3 43.7 42.5
2 4
回答下列问题:
(1)写出“滤渣”的一种用途___________,“氧化”生成VO,反应中氧化剂与还原剂的物质
的量之比为___________。
(2)若“含Cr3+净化液”中c(Cr3+)=0.125mol·L-1,则“水解沉钒”调pH的范围是
2.5~___________。(结果保留1位小数)
(3) “溶液1”中含CrO,加入HO 后发生的化学反应方程式为___________________________。
2 2
(4)“溶液2调pH”,所发生反应的离子方程式___________。
(5)“多步操作”包括蒸发浓缩、___________、冷却结晶、过滤、洗涤等步骤。
(6)研究温度对NaSO 与HO 的氧化-水解沉钒率的影响,得到如图所示结果。钒铬还原渣酸
2 2 8 2 2
浸液初始温度在80℃左右,降低温度能耗增加。由图可知,分别采用NaSO、HO 进行“氧化”
2 2 8 2 2
时,应选择的适宜温度分别是_____,在“氧化”工艺中不采用HO 氧化的原因是___________(写
2 2
出两点)。
答案:(1)制作光导纤维或制作玻璃或工业制硅 1∶2 (2)4.3
(3)3H O+2NaCrO+2NaOH=2Na CrO+4HO
2 2 2 2 4 2(4)2CrO+2H+=Cr O+HO (5)趁热过滤
2 2
(6)80℃、50℃ 沉钒率低,铬损率高;温度较高时HO 易分解,需降温导致能耗增加;对
2 2
储运及投料要求较高
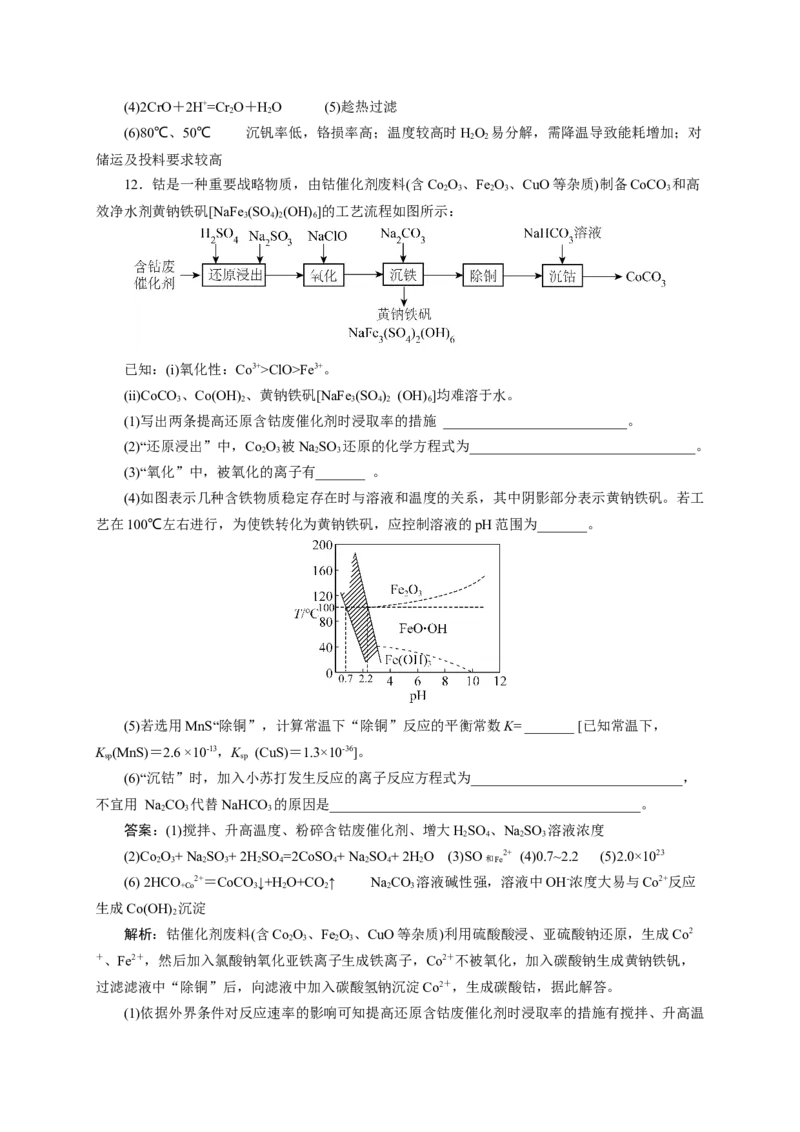
12.钴是一种重要战略物质,由钴催化剂废料(含Co O、Fe O、CuO等杂质)制备CoCO 和高
2 3 2 3 3
效净水剂黄钠铁矾[NaFe (SO )(OH) ]的工艺流程如图所示:
3 4 2 6
已知:(i)氧化性:Co3+>ClO>Fe3+。
(ii)CoCO 、Co(OH) 、黄钠铁矾[NaFe (SO ) (OH) ]均难溶于水。
3 2 3 4 2 6
(1)写出两条提高还原含钴废催化剂时浸取率的措施 __________________________。
(2)“还原浸出”中,Co O 被NaSO 还原的化学方程式为________________________________。
2 3 2 3
(3)“氧化”中,被氧化的离子有_______ 。
(4)如图表示几种含铁物质稳定存在时与溶液和温度的关系,其中阴影部分表示黄钠铁矾。若工
艺在100℃左右进行,为使铁转化为黄钠铁矾,应控制溶液的pH范围为_______。
(5)若选用MnS“除铜”,计算常温下“除铜”反应的平衡常数K= _______ [已知常温下,
K (MnS)=2.6 ×10-13,K (CuS)=1.3×10-36]。
sp sp
(6)“沉钴”时,加入小苏打发生反应的离子反应方程式为______________________________,
不宜用 NaCO 代替NaHCO 的原因是____________________________________________。
2 3 3
答案:(1)搅拌、升高温度、粉碎含钴废催化剂、增大HSO 、NaSO 溶液浓度
2 4 2 3
(2)Co O+ Na SO + 2H SO =2CoSO+ Na SO + 2HO (3)SO 2+ (4)0.7~2.2 (5)2.0×1023
2 3 2 3 2 4 4 2 4 2 和Fe
(6) 2HCO 2+=CoCO↓+H O+CO↑ Na CO 溶液碱性强,溶液中OH-浓度大易与Co2+反应
+Co 3 2 2 2 3
生成Co(OH) 沉淀
2
解析:钴催化剂废料(含Co O、Fe O、CuO等杂质)利用硫酸酸浸、亚硫酸钠还原,生成Co2
2 3 2 3
+、Fe2+,然后加入氯酸钠氧化亚铁离子生成铁离子,Co2+不被氧化,加入碳酸钠生成黄钠铁钒,
过滤滤液中“除铜”后,向滤液中加入碳酸氢钠沉淀Co2+,生成碳酸钴,据此解答。
(1)依据外界条件对反应速率的影响可知提高还原含钴废催化剂时浸取率的措施有搅拌、升高温度、粉碎含钴废催化剂、增大HSO 、NaSO 溶液浓度等。
2 4 2 3
(2)根据原子守恒可知“还原浸出”中,Co O 被NaSO 还原为二价钴同时生成硫酸根离子,化
2 3 2 3
学方程式为Co O+ Na SO + 2H SO =2CoSO + Na SO + 2H O。
2 3 2 3 2 4 4 2 4 2
(3)已知:(i)氧化性:Co3+>ClO>Fe3+。由于亚硫酸钠过量,根据氧化性:Co3+>ClO>Fe3+可知
氧化”中,被氧化的离子有SO 2+。
和Fe
(4)阴影部分表示黄钠铁矾,根据图中几种含铁物质稳定存在时与溶液和温度的关系可判断若工
艺在100℃左右进行,为使铁转化为黄钠铁矾,应控制溶液的pH范围为0.7~2.2。
(5)常温下“除铜”反应的方程式为MnS+Cu2+=CuS+Mn2+,则平衡常数K====2×1023。
(6)“沉钴”时根据原子守恒可知可知还有水和二氧化碳生成,则加入小苏打发生反应的离子反
应方程式为2HCO 2+=CoCO↓+H O+CO↑,由于NaCO 溶液中碳酸根离子水解程度大、溶液碱
+Co 3 2 2 2 3
性强,溶液中OH-浓度大易与Co2+反应生成Co(OH) 沉淀,所以不宜用NaCO 代替NaHCO 。
2 2 3 3