文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题25
1.某溶液中含有下表中的五种离子,且阳离子浓度均为0.5mol·L-1,阴离子浓度均为
1mol·L-1,下列有关该溶液的离子组合正确的是
阳离子 Fe3+、K+、Al3+、NH、Na+、Mg2+、H+
阴离子 Cl-、SO、I-、CO NO OH-
、 、
A.Al3+、Fe3+、Cl-、NO I- B.Na+、K+、Cl-、SO、OH-
、
C.Na+、Mg2+、NH、Cl-、NO D.Na+、NH、H+、K+、CO
答案:C
解析:五种离子,且阳离子浓度均为0.5mol·L-1,阴离子浓度均为1mol·L-1,由溶液呈电中性,
则阳离子带正电之和:阴离子带负电之和=2:1,
A.Fe3+与I-会发生氧化还原反应,不能共存,且正电荷之和:负电荷之和=1∶1,A错误;
B.正电荷之和:负电荷之和=1∶2,B错误;
D.Na+、Mg2+、NH、Cl-、NO =2∶1,C正确;
五种离子中,正电荷之和:负电荷之和
D.H+与CO D错误;
反应产生气体,不能共存,
2.下列化学反应对应的离子方程式正确的是
A.向Ca(ClO) 溶液中通入少量SO :Ca2++3ClO-+HO+SO =Cl-+CaSO↓+2HClO
2 2 2 2 4
B.向NaAlO 溶液中通入过量CO:2AlO+CO+3HO=2Al(OH) ↓+CO
2 2 2 2 3
C.硫酸铜溶液和氢氧化钡溶液混合:Ba2++SO=BaSO↓
4
D.向亚硫酸钠溶液中加入足量的硝酸:SO +=SO ↑+H O
+2H 2 2
答案:A
解析:A.Ca(ClO) 溶液中电离出次氯酸根离子在酸性条件下具有氧化性,SO 具有还原性,
2 2
通入少量SO 两者发生氧化还原反应生成硫酸根离子和氯离子,硫酸根离子和钙离子结合生成硫酸
2
钙沉淀,反应的离子方程式为:Ca2++3ClO-+HO+SO =Cl-+CaSO↓+2HClO,故A正确;
2 2 4
B.向NaAlO 溶液中通入过量CO 反应生成氢氧化铝沉淀和碳酸氢钠溶液,离子方程式为:
2 2
AlO+CO+23HO=Al(OH) ↓+HCO B错误;
2 2 3 ,故
C.硫酸铜溶液中加入过量的氢氧化钡,反应生成硫酸钡和氢氧化铜沉淀,正确的离子方程式
为: Ba2++Cu2++2OH-+SO=BaSO↓+Cu(OH) ↓,故C错误;
4 2
D.向亚硫酸钠溶液中加入足量硝酸的离子反应为3SO NO +=3SO ↑+HO,故D错误;
+2 +2H +2NO 2
3.中华传统文化源远流长,下列说法与氧化还原反应无关的是
A.《七步诗》:“煮豆燃豆萁,豆在釜中泣”
B.《抱朴子》:“丹砂(注:HgS)烧之成水银,积变又还成丹砂”
C.《周礼》:“煤饼烧蛎房(注:牡蛎壳)成灰”
D.《咏煤炭》:“凿开混沌得乌金……不辞辛苦出山林”
答案:D
解析:A.“煮豆燃豆萁,豆在釜中泣”涉及燃烧,有元素化合价的升降,与氧化还原反应有关,A不符合题意;
B.升华和凝华属于物理变化,丹砂(HgS)烧之成水银,即HgS发生分解反应生成水银,积变
又还成丹砂,即Hg和S又生成HgS,两个过程均为氧化还原反应,B不符合题意;
C.牡蛎壳为贝壳,贝壳主要成分为CaCO ,CaCO 灼烧生成CaO,但“煤饼”燃烧属于氧化
3 3
还原反应,C不符合题意;
D.“乌金”的主要成分为煤炭,上述说法中,描述的是开凿得到煤炭的语句,与氧化还原反
应无关,D符合题意;
4.下列离子方程式正确的是
A.向含Fe3+的CuSO 溶液中加入适量CuO:2Fe3++3CuO+3HO=2Fe(OH) +3Cu2+
4 2 3
B.向AgNO 溶液中加入过量氨水:Ag++NH ∙HO=AgOH↓+NH
3 3 2
C.Cu O加入足量稀硝酸中:Cu O+2H+=Cu+Cu2++HO
2 2 2
D.向甲酸溶液中加入足量Cu(OH) 浊液并加热:2HCOOH+Cu(OH) =Cu2++2HCOO-+2HO
2 2 2
答案:A
解析:A.Fe3+水解生成Fe(OH) 和H+,加入CuO消耗H+促进Fe(OH) 生成,离子方程式为
3 3
2Fe3++3CuO+3HO=2Fe(OH) +3Cu2+,故A正确;
2 3
B.向AgNO 溶液中加入过量氨水生成Ag(NH)OH,故B错误;
3 3 2
C.Cu O加入足量稀硝酸中离子方程式为Cu O+14H+ +2NO 2+ + 2NO↑+7H O,故C错误;
2 2 =6Cu 2
D.甲酸含有醛基,与Cu(OH) 反应生成Cu O,故D错误;
2 2
5.向CuSO 溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向
4
反应后的混合物中不断通入SO 气体,溶液逐渐变成无色。下列分析正确的是
2
A.滴加KI溶液时,转移2mol电子时生成1mol白色沉淀
B.通入SO 后溶液逐渐变成无色,体现了SO 的漂白性
2 2
C.通入SO 时,SO 与I 反应,I 作还原剂
2 2 2 2
D.上述实验条件下,物质的氧化性:Cu2+>I>SO
2 2
答案:D
解析:A.滴加KI溶液时,反应为2Cu2++4I-=2CuI↓+I ,当有2molI-参加反应,转移1mole-时
2
生成1mol白色沉淀,则转移2mol电子时生成2molCuI白色沉淀,A错误;
B.通入SO 后溶液逐渐变成无色,SO +I +2H O=2HI+HSO ,体现了SO 的还原性,B错误;
2 2 2 2 2 4 2
C.通入SO 时,SO 与I 反应,SO +I +2H O=2HI+HSO ,I 作氧化剂,C错误;
2 2 2 2 2 2 2 4 2
D.依据反应2Cu2++4I-=2CuI↓+I ,SO +I +2H O=2HI+HSO ,物质的氧化性,得到Cu2+>I
2 2 2 2 2 4 2
>SO ,D正确;
2
6.下列离子组在一定条件下能大量共存,且加入试剂后发生反应的离子方程式正确的是
选项 离子组 加入试剂 发生反应的离子方程式
A K+、AlO、NO 过量CO CO+2HO+AlO=Al(OH) ↓+HCO
2 2 2 3
B Fe3+、I-、ClO- NaOH溶液 Fe3++3OH-=Fe(OH) ↓
3C Ba2+、Na+、OH- NaHCO 溶液 HCO OH-=CO HO
3 + + 2
D Fe3+、Cl-、NO + 少量Fe粉 2Fe3++Fe=3Fe2+
、H
答案:A
解析:A.K+、AlO、NO ,偏铝酸根离子与二氧化碳、水反应生成氢
相互不反应,可以大量共存,加入过量CO2
氧化铝和碳酸氢根离子,离子方程式为:CO
2
+2H
2
O+AlO=Al(OH)
3
↓+HCO
,故A正确;
B.Fe3+、I-、ClO-发生氧化还原反应不能共存,因为三价铁离子和次氯酸根离子都能氧化碘
离子,故B错误;
C.Ba2+、Na+、OH-能大量共存,加入碳酸氢钠,碳酸氢根离子与氢氧根离子反应生成碳酸根
离子和水,碳酸根离子与钡离子反应生成碳酸钡沉淀,离子方程式:HCO OH-=CO HO, CO
+ + 2 +
Ba2+=BaCO ↓,故C错误;
3
D.Fe3+、Cl-、NO +能大量共存,加入少量Fe粉,铁会被酸性条件下的硝酸根离子氧化为
、H
Fe3+,故D错误;
7.下列离子方程式书写正确的是
A.NaSO 溶液在空气中易被氧化:SO =SO
2 3 +O2
B.酸性高锰酸钾溶液与稀草酸反应:5C O+2MnO +=2Mn2++10CO↑+8HO
2 +16H 2 2
C.AgNO 的溶液中滴加NaCl溶液:Ag++Cl-=AgCl↓
3
D.NH HCO 溶液加入过量NaOH溶液加热:NH+OH-=NH∙HO
4 3 3 2
答案:C
解析:A.NaSO 溶液在空气中易被氧化为硫酸钠,反应的离子方程式是2SO =2SO,故A
2 3 +O2
错误;
B.酸性高锰酸钾溶液与稀草酸反应,反应的离子方程式是5HC O+2MnO +=2Mn2++
2 2 +6H
10CO↑+8HO,故B错误;
2 2
C.AgNO 的溶液中滴加NaCl溶液生成氯化银沉淀和硝酸钠,反应的离子方程式是Ag++Cl-=
3
AgCl↓,故C正确;
D.NH HCO 溶液加入过量NaOH溶液加热生成碳酸钠、氨气、水,反应的离子方程式是NH
4 3
+HCO -=NH+2H O+CO
+2OH 3 2 ,故D错误;
8.分类法是一种行之有效、简单易行的科学方法。某同学用如表所示的形式对所学知识进行
分类,其中甲与乙、丙、丁是包含关系。
甲 乙、丙、丁
① 常见干燥剂 浓硫酸、石灰石、碱石灰
② 常见合金 不锈钢、青铜、生铁
③ 腐蚀品 浓硫酸、烧碱、硝酸
④ 碱性氧化物 过氧化钠、氧化镁、氧化铁
⑤ 弱电解质 醋酸、一水合氨、水其中正确的组合是
A.①② B.③④⑤ C.②③⑤ D.①④⑤
答案:C
解析:①中石灰石的主要成分是CaCO ,不能充当干燥剂;②中三种物质均为合金;③中三种
3
物质均具有腐蚀性;④中过氧化钠与酸反应,生成盐和水的同时,还生成O,所以过氧化钠不是
2
碱性氧化物;⑤中三种物质均存在电离平衡,属于弱电解质,答案选C。
9.下列各组物质混合充分反应后,再加热蒸干并灼烧至质量不变,最终残留固体一定是纯净
物的有
A.向FeSO 溶液中通入过量Cl
4 2
B.向NaHCO 溶液中加入一定质量NaO
3 2 2
C.将等浓度的(NH )SO 溶液与BaCl 溶液等体积混合
4 2 4 2
D.向NaI与KBr的混合溶液中通入过量Cl
2
答案:C
解析:A.向FeSO 溶液中通入过量Cl 生成硫酸铁、氯化铁,氯化铁会水解得到氢氧化铁和盐
4 2
酸,盐酸挥发,灼烧氢氧化铁分解最终得到氧化铁,但硫酸是难挥发性酸,最终得到硫酸铁,因此
最终的物质为混合物,故A错误;
B.向NaHCO 溶液中加入一定质量NaO,过氧化钠首先与水反应生成氢氧化钠和氧气,氢
3 2 2
氧化钠和碳酸氢钠反应生成碳酸钠和水,由于碳酸氢钠和过氧化钠的质量不确定,所以最终得到的
不一定是纯净物,故B错误;
C.将等浓度的(NH )SO 溶液与BaCl 溶液等体积混合,反应生成硫酸钡和氯化铵,氯化铵分
4 2 4 2
解生成氨气和HCl,蒸干灼烧后的固体为硫酸钡,为纯净物,故C正确;
D.向NaI与KBr的混合溶液中通入过量Cl,反应生成NaCl、KCl、溴、碘,溴易挥发,碘易
2
升华,蒸干灼烧后的固体为NaCl、KCl,为混合物,故D错误;
10.下列物质在生活中的应用与氧化还原反应无关的是
A.FeSO 补血剂与维生素C配合使用效果更佳 B.用明矾处理污水
4
C.用84消毒液杀灭细菌 D.还原Fe粉用作食品脱氧剂
答案:B
解析:A.人体容易吸收亚铁离子,但亚铁离子具有还原性,很容易被氧化为不易被人体吸收
的铁离子,而维生素C也具体还原性,故两者同服可减少亚铁离子的氧化,效果更佳,故A项与氧
化还原反应有关;
B.明矾是KAl(SO )∙12HO,溶于水电离出的铝离子会发生水解:Al3++3HO Al(OH) +
4 2 2 2 3
3H+形成氢氧化铝胶体,氢氧化铝胶粒由于阳离子会带正电,遇到负点的沉积物胶体便中和为电中
性,当胶体颗粒上没有电荷时,它们聚集在一起下沉,越来越多的颗粒下沉到水底,使水变得清澈
干净。整个过程铝元素化合价均未改变,所以不涉及氧化还原反应,故B项与氧化还原反应无关;
C.84消毒液的有效成分是次氯酸钠,次氯酸钠有强氧化性,可以杀灭细菌,故C项与氧化还
原有关;D.铁粉具有还原性,能和氧气反应生成氧化铁,消耗氧气,使食物保持新鲜,故D项与氧化
还原反应有关。
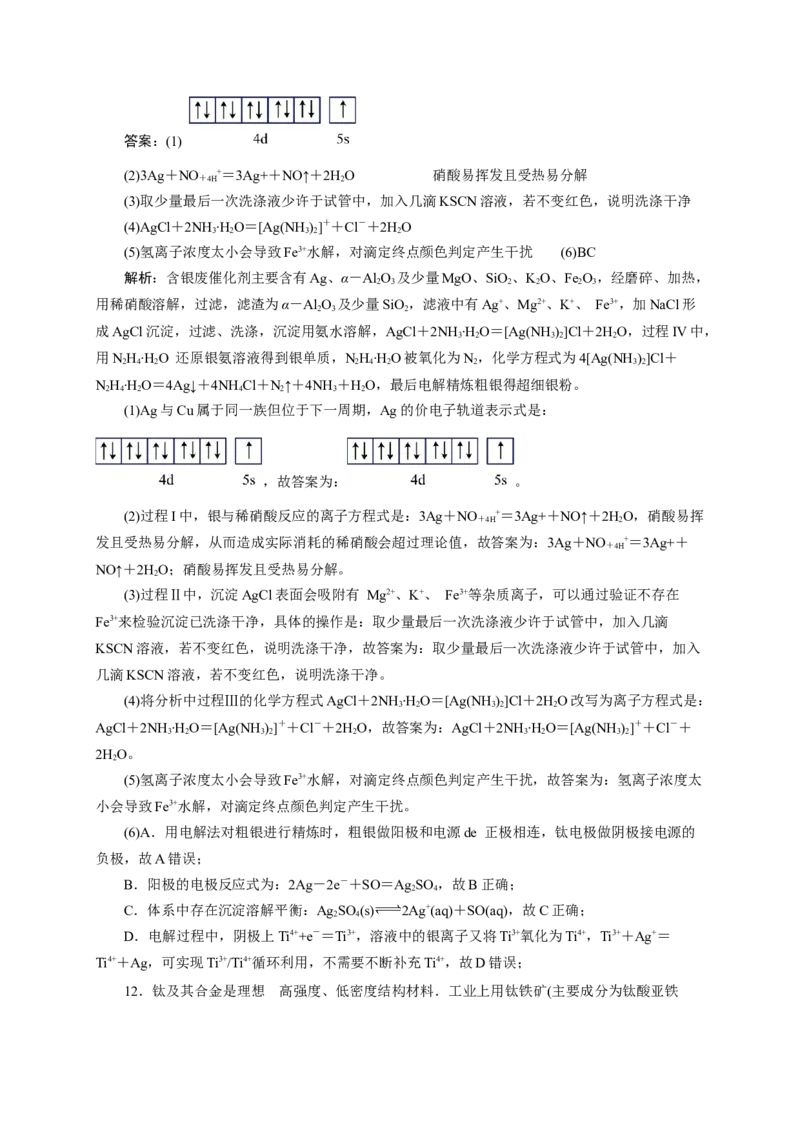
11.超细银粉在光学、生物医疗等领域有着广阔的应用前景。由含银废催化剂粉末制备超细银
粉的过程如下图所示:
资料:i.含银废催化剂成分:主要含Ag、α-Al O 及少量MgO、SiO、KO、Fe O
2 3 2 2 2 3
ⅱ. α-Al O 为载体,且不溶于硝酸
2 3
回答下列问题:
(1)Ag与Cu属于同一族但位于下一周期,Ag的价电子轨道表示式是___________。
(2)过程I中,银与稀硝酸反应的离子方程式是_________________________________,但实际
消耗的稀硝酸会超过理论值,原因是___________________________________。
(3)过程Ⅱ中,检验沉淀已洗涤干净的操作是_______________________________。
(4)过程Ⅲ中反应的离子方程式是_______________________________________。
(5)测定粗银中银的回收率:取样品用硝酸溶解,以NH Fe(SO )∙12HO为指示剂,用KSCN标
4 4 2 2
准溶液滴定,当锥形瓶中溶液变为红色,且半分钟内不褪色即达到滴定终点。
已知:i.AgSCN为自色难溶固体,FeSCN2+离子为红色。
ⅱ.Fe3+开始沉淀的pH为1.9,完全沉淀的pH为3.2
为保证获取数据准确性,滴定时溶液c(H+)一般控制在0.1~1mol·L-1之间,氢离子浓度太小对
实验的影响是_______________________________________________。
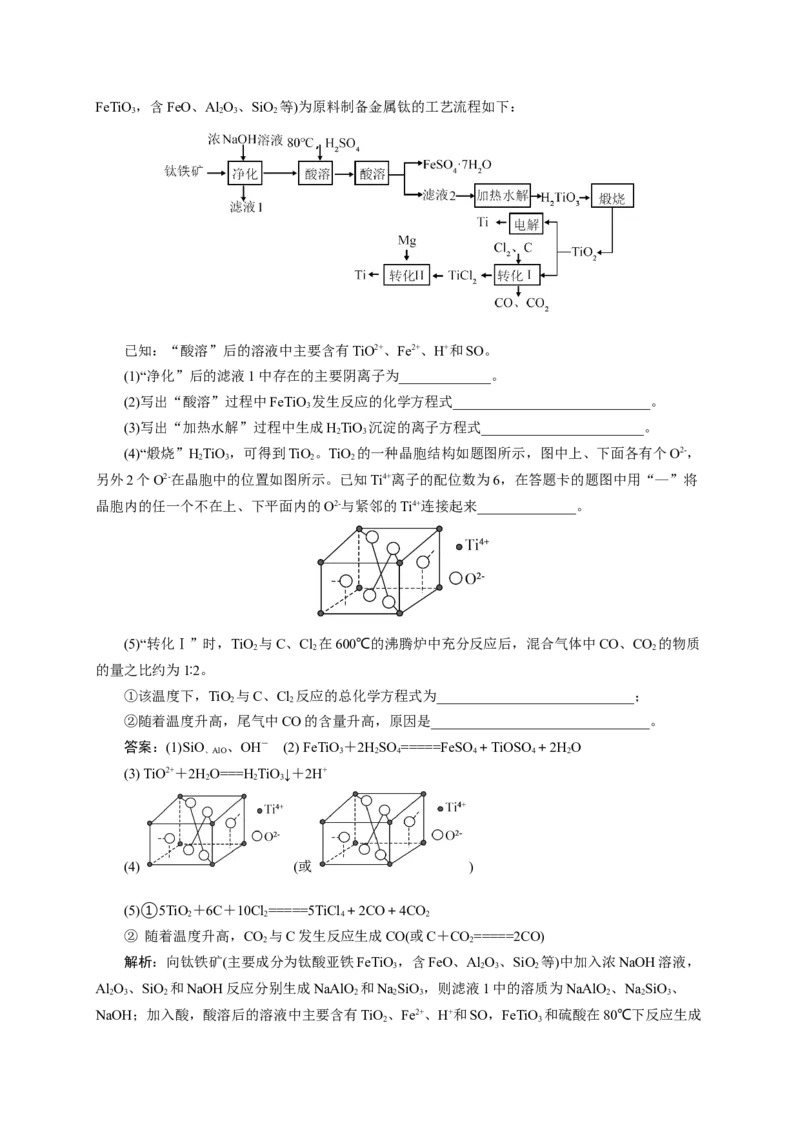
(6)可用电解法对粗银进行精炼,装置如下图所示,电解液为稀HSO (含Ti4+),获得超细银粉
2 4
的原理为Ti3++Ag+=Ti4++Ag。下列说法正确的是_______(填标号)。
A. 钛电极接电源的正极
B. 阳极的电极反应式为:2Ag-2e-+SO=Ag SO
2 4
C. 体系中存在沉淀溶解平衡:Ag SO (s) 2Ag+(aq)+SO(aq)
2 4
D. 电解过程中,需要不断补充Ti4+答案:(1)
(2)3Ag+NO +=3Ag++NO↑+2HO 硝酸易挥发且受热易分解
+4H 2
(3)取少量最后一次洗涤液少许于试管中,加入几滴KSCN溶液,若不变红色,说明洗涤干净
(4)AgCl+2NH ∙HO=[Ag(NH)]++Cl-+2HO
3 2 3 2 2
(5)氢离子浓度太小会导致Fe3+水解,对滴定终点颜色判定产生干扰 (6)BC
解析:含银废催化剂主要含有Ag、α-Al O 及少量MgO、SiO、KO、Fe O,经磨碎、加热,
2 3 2 2 2 3
用稀硝酸溶解,过滤,滤渣为α-Al O 及少量SiO,滤液中有Ag+、Mg2+、K+、 Fe3+,加NaCl形
2 3 2
成AgCl沉淀,过滤、洗涤,沉淀用氨水溶解,AgCl+2NH ∙HO=[Ag(NH)]Cl+2HO,过程IV中,
3 2 3 2 2
用NH∙HO 还原银氨溶液得到银单质,NH∙HO被氧化为N,化学方程式为4[Ag(NH)]Cl+
2 4 2 2 4 2 2 3 2
NH∙HO=4Ag↓+4NH Cl+N↑+4NH +HO,最后电解精炼粗银得超细银粉。
2 4 2 4 2 3 2
(1)Ag与Cu属于同一族但位于下一周期,Ag的价电子轨道表示式是:
,故答案为: 。
(2)过程I中,银与稀硝酸反应的离子方程式是:3Ag+NO +=3Ag++NO↑+2HO,硝酸易挥
+4H 2
发且受热易分解,从而造成实际消耗的稀硝酸会超过理论值,故答案为:3Ag+NO +=3Ag++
+4H
NO↑+2HO;硝酸易挥发且受热易分解。
2
(3)过程Ⅱ中,沉淀AgCl表面会吸附有 Mg2+、K+、 Fe3+等杂质离子,可以通过验证不存在
Fe3+来检验沉淀已洗涤干净,具体的操作是:取少量最后一次洗涤液少许于试管中,加入几滴
KSCN溶液,若不变红色,说明洗涤干净,故答案为:取少量最后一次洗涤液少许于试管中,加入
几滴KSCN溶液,若不变红色,说明洗涤干净。
(4)将分析中过程Ⅲ的化学方程式AgCl+2NH ∙HO=[Ag(NH)]Cl+2HO改写为离子方程式是:
3 2 3 2 2
AgCl+2NH ∙HO=[Ag(NH)]++Cl-+2HO,故答案为:AgCl+2NH ∙HO=[Ag(NH)]++Cl-+
3 2 3 2 2 3 2 3 2
2HO。
2
(5)氢离子浓度太小会导致Fe3+水解,对滴定终点颜色判定产生干扰,故答案为:氢离子浓度太
小会导致Fe3+水解,对滴定终点颜色判定产生干扰。
(6)A.用电解法对粗银进行精炼时,粗银做阳极和电源de 正极相连,钛电极做阴极接电源的
负极,故A错误;
B.阳极的电极反应式为:2Ag-2e-+SO=Ag SO ,故B正确;
2 4
C.体系中存在沉淀溶解平衡:Ag SO (s) 2Ag+(aq)+SO(aq),故C正确;
2 4
D.电解过程中,阴极上Ti4++e-=Ti3+,溶液中的银离子又将Ti3+氧化为Ti4+,Ti3++Ag+=
Ti4++Ag,可实现Ti3+/Ti4+循环利用,不需要不断补充Ti4+,故D错误;
的
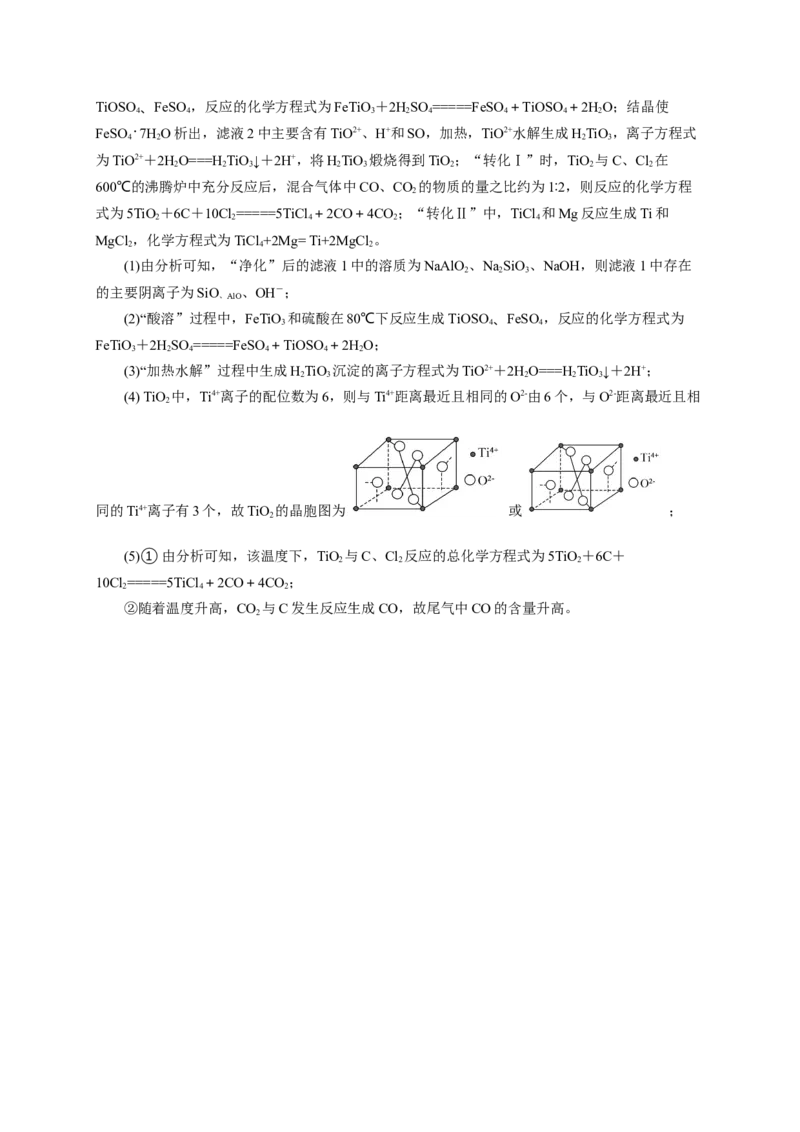
12.钛及其合金是理想 高强度、低密度结构材料.工业上用钛铁矿(主要成分为钛酸亚铁FeTiO,含FeO、Al O、SiO 等)为原料制备金属钛的工艺流程如下:
3 2 3 2
已知:“酸溶”后的溶液中主要含有TiO2+、Fe2+、H+和SO。
(1)“净化”后的滤液1中存在的主要阴离子为_____________。
(2)写出“酸溶”过程中FeTiO 发生反应的化学方程式____________________________。
3
(3)写出“加热水解”过程中生成HTiO 沉淀的离子方程式_______________________。
2 3
(4)“煅烧”HTiO,可得到TiO。TiO 的一种晶胞结构如题图所示,图中上、下面各有个O2-,
2 3 2 2
另外2个O2-在晶胞中的位置如图所示。已知Ti4+离子的配位数为6,在答题卡的题图中用“—”将
晶胞内的任一个不在上、下平面内的O2-与紧邻的Ti4+连接起来______________。
(5)“转化Ⅰ”时,TiO 与C、Cl 在600℃的沸腾炉中充分反应后,混合气体中CO、CO 的物质
2 2 2
的量之比约为1∶2。
①该温度下,TiO 与C、Cl 反应的总化学方程式为____________________________;
2 2
②随着温度升高,尾气中CO的含量升高,原因是_______________________________。
答案:(1)SiO 、OH- (2) FeTiO +2HSO =====FeSO +TiOSO+2HO
、AlO 3 2 4 4 4 2
(3) TiO2++2HO===HTiO↓+2H+
2 2 3
(4) (或 )
(5)①5TiO+6C+10Cl=====5TiCl +2CO+4CO
2 2 4 2
② 随着温度升高,CO 与C发生反应生成CO(或C+CO=====2CO)
2 2
解析:向钛铁矿(主要成分为钛酸亚铁FeTiO,含FeO、Al O、SiO 等)中加入浓NaOH溶液,
3 2 3 2
Al O、SiO 和NaOH反应分别生成NaAlO 和NaSiO,则滤液1中的溶质为NaAlO 、NaSiO、
2 3 2 2 2 3 2 2 3
NaOH;加入酸,酸溶后的溶液中主要含有TiO、Fe2+、H+和SO,FeTiO 和硫酸在80℃下反应生成
2 3TiOSO、FeSO ,反应的化学方程式为FeTiO+2HSO =====FeSO +TiOSO+2HO;结晶使
4 4 3 2 4 4 4 2
FeSO 7HO析出,滤液2中主要含有TiO2+、H+和SO,加热,TiO2+水解生成HTiO,离子方程式
4 2 2 3
为TiO2++2HO===HTiO↓+2H+,将HTiO 煅烧得到TiO;“转化Ⅰ”时,TiO 与C、Cl 在
2 2 3 2 3 2 2 2
600℃的沸腾炉中充分反应后,混合气体中CO、CO 的物质的量之比约为1∶2,则反应的化学方程
2
式为5TiO+6C+10Cl=====5TiCl +2CO+4CO;“转化Ⅱ”中,TiCl 和Mg反应生成Ti和
2 2 4 2 4
MgCl ,化学方程式为TiCl +2Mg= Ti+2MgCl 。
2 4 2
(1)由分析可知,“净化”后的滤液1中的溶质为NaAlO 、NaSiO、NaOH,则滤液1中存在
2 2 3
的主要阴离子为SiO 、OH-;
、AlO
(2)“酸溶”过程中,FeTiO 和硫酸在80℃下反应生成TiOSO、FeSO ,反应的化学方程式为
3 4 4
FeTiO+2HSO =====FeSO +TiOSO+2HO;
3 2 4 4 4 2
(3)“加热水解”过程中生成HTiO 沉淀的离子方程式为TiO2++2HO===HTiO↓+2H+;
2 3 2 2 3
(4) TiO 中,Ti4+离子的配位数为6,则与Ti4+距离最近且相同的O2-由6个,与O2-距离最近且相
2
同的Ti4+离子有3个,故TiO 的晶胞图为 或 ;
2
(5)①由分析可知,该温度下,TiO 与C、Cl 反应的总化学方程式为5TiO+6C+
2 2 2
10Cl=====5TiCl +2CO+4CO;
2 4 2
②随着温度升高,CO 与C发生反应生成CO,故尾气中CO的含量升高。
2