文档内容
2025届高三化学一轮专题复习讲义(14)
专题三 基本理论
3-7 电离和水解平衡(二)(1课时,共2课时)
——溶液中粒子浓度关系
【复习目标】
1.理解弱电解质的电离平衡、水的电离平衡以及盐类的水解平衡的特征。
2.熟练运用三大守恒原理和比较电解质溶液中离子的浓度大小。
【重点突破】
利用电荷守恒、物料守恒和质子守恒原理,理解溶液中微粒浓度大小的比较方法。
【真题再现】
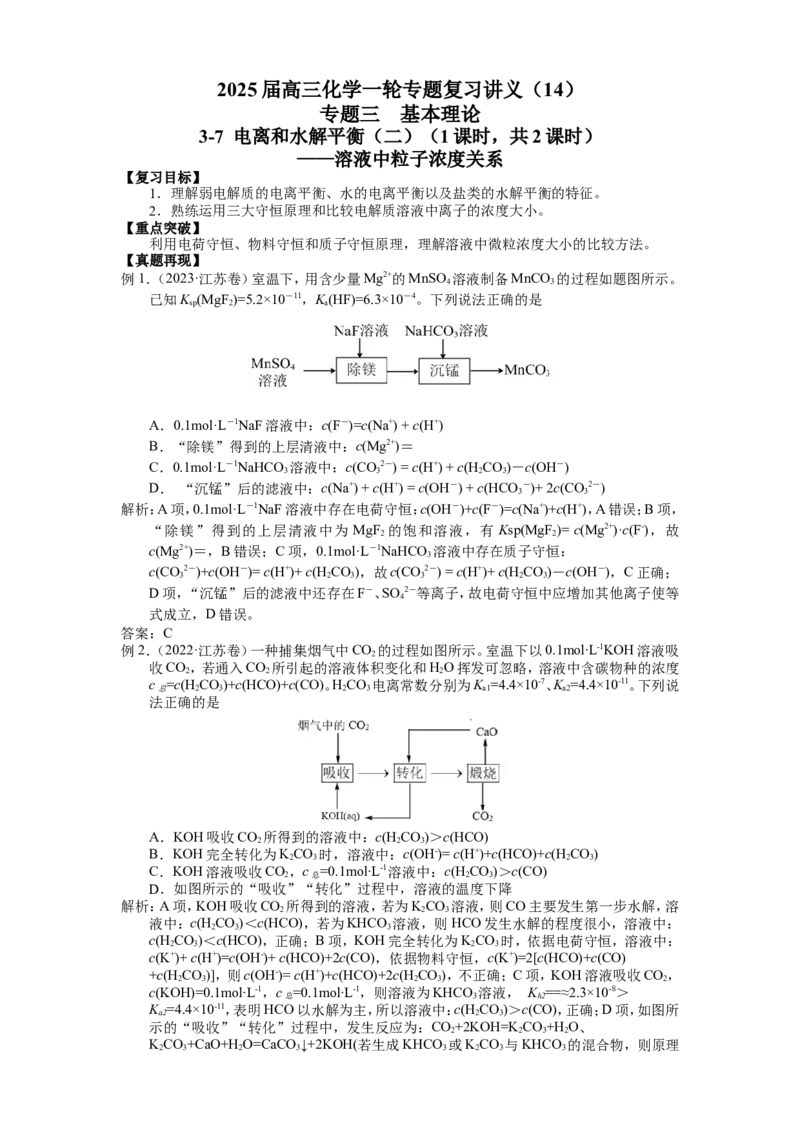
例1.(2023·江苏卷)室温下,用含少量Mg2+的MnSO 溶液制备MnCO 的过程如题图所示。
4 3
已知K (MgF )=5.2×10-11,K(HF)=6.3×10-4。下列说法正确的是
sp 2 a
A.0.1mol·L-1NaF溶液中:c(F-)=c(Na+) + c(H+)
B.“除镁”得到的上层清液中:c(Mg2+)=
C.0.1mol·L-1NaHCO 溶液中:c(CO2-) = c(H+) + c(H CO)-c(OH-)
3 3 2 3
D. “沉锰”后的滤液中:c(Na+) + c(H+) = c(OH-) + c(HCO -)+ 2c(CO2-)
3 3
解析:A项,0.1mol·L-1NaF溶液中存在电荷守恒:c(OH-)+c(F-)=c(Na+)+c(H+),A错误;B项,
“除镁”得到的上层清液中为 MgF 的饱和溶液,有 Ksp(MgF )= c(Mg2+)·c(F-),故
2 2
c(Mg2+)=,B错误;C项,0.1mol·L-1NaHCO 溶液中存在质子守恒:
3
c(CO2-)+c(OH-)= c(H+)+ c(H CO),故c(CO2-) = c(H+)+ c(H CO)-c(OH-),C正确;
3 2 3 3 2 3
D项,“沉锰”后的滤液中还存在F-、SO 2-等离子,故电荷守恒中应增加其他离子使等
4
式成立,D错误。
答案:C
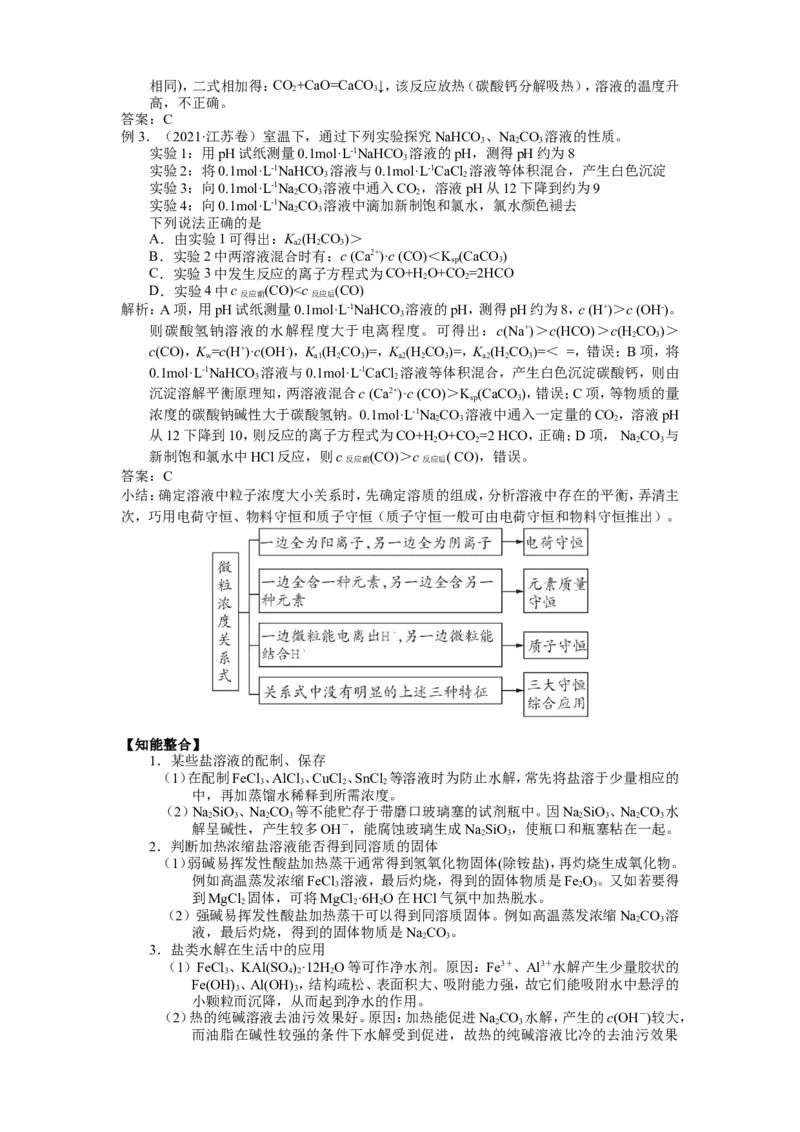
例2.(2022·江苏卷)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸
2
收CO,若通入CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度
2 2 2
c =c(H CO)+c(HCO)+c(CO)。HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。下列说
总 2 3 2 3 a1 a2
法正确的是
A.KOH吸收CO 所得到的溶液中:c(H CO)>c(HCO)
2 2 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c(HCO)+c(H CO)
2 3 2 3
C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c(CO)
2 总 2 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
解析:A项,KOH吸收CO 所得到的溶液,若为KCO 溶液,则CO主要发生第一步水解,溶
2 2 3
液中:c(H CO)<c(HCO),若为KHCO 溶液,则 HCO发生水解的程度很小,溶液中:
2 3 3
c(H CO)<c(HCO),正确;B项,KOH完全转化为KCO 时,依据电荷守恒,溶液中:
2 3 2 3
c(K+)+ c(H+)=c(OH-)+ c(HCO)+2c(CO),依据物料守恒,c(K+)=2[c(HCO)+c(CO)
+c(H CO)],则c(OH-)= c(H+)+c(HCO)+2c(H CO),不正确;C项,KOH溶液吸收CO,
2 3 2 3 2
c(KOH)=0.1mol∙L-1,c =0.1mol∙L-1,则溶液为KHCO 溶液, K ==≈2.3×10-8>
总 3 h2
K =4.4×10-11,表明HCO以水解为主,所以溶液中:c(H CO)>c(CO),正确;D项,如图所
a2 2 3
示的“吸收”“转化”过程中,发生反应为:CO+2KOH=K CO+H O、
2 2 3 2
KCO+CaO+H O=CaCO ↓+2KOH(若生成KHCO 或KCO 与KHCO 的混合物,则原理
2 3 2 3 3 2 3 3相同),二式相加得:CO+CaO=CaCO ↓,该反应放热(碳酸钙分解吸热),溶液的温度升
2 3
高,不正确。
答案:C
例3.(2021·江苏卷)室温下,通过下列实验探究NaHCO 、NaCO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1mol·L-1NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1mol·L-1NaHCO 溶液与0.1mol·L-1CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:向0.1mol·L-1NaCO 溶液中通入CO,溶液pH从12下降到约为9
2 3 2
实验4:向0.1mol·L-1NaCO 溶液中滴加新制饱和氯水,氯水颜色褪去
2 3
下列说法正确的是
A.由实验1可得出:K (H CO)>
a2 2 3
B.实验2中两溶液混合时有:c (Ca2+)·c (CO)<K (CaCO)
sp 3
C.实验3中发生反应的离子方程式为CO+HO+CO=2HCO
2 2
D.实验4中c (CO)c(OH-)>c(NH)。
3 2
②多元弱酸的电离是分步进行的,其主要是第一级电离。
如HS溶液中:c(H S)>c(H+)>c(HS-)>c(S2-)。
2 2
(2)水解(即水解理论)
①弱电解质离子的水解损失是微量的(双水解除外),但由于水的电离,水解后酸
性溶液中c(H+)或碱性溶液中c(OH-)总是大于水解产生的弱电解质溶液的浓
度。
如NH Cl溶液中:c(Cl-)>c(NH)>c(H+)>c(NH ·H O)。
4 3 2
②多元弱酸根离子的水解是分步进行的,其主要是第一步水解。
如在NaCO 溶液中:c(CO)>c(HCO)>c(H CO)。
2 3 2 3
7.把握三种守恒,明确等量关系
(1)电荷守恒:
如在NaCO 溶液中存在离子:Na+、CO、H+、OH-、HCO,它们的浓度存在如下关系:
2 3
c(Na+)+c(H+)=2c(CO)+c(HCO)+c(OH-)。
(2)物料守恒:物料守恒也就是原子守恒,变化前后某种元素的原子个数不变。
(3)质子守恒:即HO电离的H+和OH-浓度相等。
2
如在NaCO 溶液中水电离出OH-和H+,其中水电离出的H+以H+、HCO、HCO
2 3 2 3
三种形式存在于溶液中,则有c(OH-)=c(H+)+c(HCO)+2c(H CO)(由上述电荷守恒式
2 3
减去物料守恒式也可得出质子守恒式)。【体系再构】
【随堂反馈】
基础训练
1.下列有关问题与盐的水解有关的是
①NH Cl与ZnCl 溶液可作焊接金属时的除锈剂
4 2
②NaHCO 与Al (SO ) 两种溶液可作泡沫灭火剂
3 2 4 3
③草木灰与铵态氮肥不能混合施用
④实验室中盛放NaCO 溶液的试剂瓶不能用磨口玻璃塞
2 3
⑤加热蒸干CuCl 溶液得到Cu(OH) 固体
2 2
⑥要除去FeCl 溶液中混有的Fe2+,可先通入氧化剂Cl,再调节溶液的pH
3 2
A.①②③ B.②③④ C.①④⑤ D.①②③④⑤
2.室温下,将0.2mol·L-1的一元酸HA和0.1mol·L-1的NaOH溶液等体积混合后,溶液显碱性,
下列说法不正确的是
A.混合后溶液中:c (A-)+c (HA)=0.1mol·L-1
B.混合后溶液中:c (HA)> c (Na+)> c (A-)> c (OH-)
C.0.1mol·L-1HA溶液与0.1mol·L-1的NaOH溶液中,水电离出来的c (H+)相等
D.混合后溶液中:c (Na+)+c (H+)=c (A-)+c (OH-)
3.室温下,向5 mL 0.1 mol·L-1NaHCO 溶液中滴入2滴0.1 mol·L-1CaCl 溶液,生成白色沉淀,
3 2
且有无色气体产生。下列说法正确的是
A. 0.1 mol·L-1 NaHCO 溶液中存在:
3
c(Na+)=c(H CO)+c(HCO -)+2c(CO2-)
2 3 3 3
B. 0.1 mol·L-1 NaHCO 溶液中存在:c(Na+)+c(H+)=c(OH-)+c(HCO -)+c(CO2-)
3 3 3
C. 0.1 mol·L-1NaHCO 溶液中存在:c(H CO)+c(H+)=c(OH-)+c(CO2-)
3 2 3 3
D.生成白色沉淀的离子方程式为2HCO -+Ca2+===Ca(HCO )↓
3 3 2
4.室温下,通过下列实验探究NaS溶液的性质。
2
实验 实验操作和现象
1 用pH试纸测定0.1 mol·L-1 Na S溶液的pH,测得pH约为13
2
2 向0.1 mol·L-1 Na S溶液中加入过量0.2 mol/L AgNO 溶液,产生黑色沉淀
2 3
3 向0.1 mol·L-1NaS溶液中通入过量HS,测得溶液pH约为9
2 2
4 向0.1 mol·L-1 Na S溶液中滴加几滴0.05 mol·L-1盐酸,观察不到明显现象
2
下列说法正确的是
A. 0.1 mol·L-1 Na S溶液中存在 c(OH-)=c(H+)+c(HS-)+c(H S)
2 2
B.实验2反应静置后的上层清液中有c(Ag+)·c(S2-)=K (Ag S)
sp 2
C.实验3得到的溶液中有c(HS-)+2c(S2-)<0.2 mol·L-1
D.实验4说明HS的酸性比HCl的酸性强
2
拓展训练
5.下列溶液中粒子的物质的量浓度关系正确的是
A.0.1mol·L-1 NaHCO 溶液与0.1mol·L-1 NaOH溶液等体积混合,所得溶液中:
3
c (Na+)>c (CO)>c (HCO)>c (OH-)
B.20mL 0.1mol·L-1 CH COONa溶液与10mL 0.1mol·L-1 盐酸混合后溶液呈酸性,
3
所得溶液中:c (CH COO-)>c (Cl-)>c (CH COOH)>c (H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:
c (Cl-)+c (H+)>c (NH)+c (OH-)
D.0.1mol·L-1 CH COOH溶液与0.1mol·L-1 NaOH溶液等体积混合,所得溶液中:
3
c (OH-)>c (H+)+c (CH COOH)
3
6.室温下,通过下列实验探究NaCO 溶液的性质.
2 3
实 实验操作和现象
验
1 用pH试纸测定0.1mol·L-1 Na CO 溶液的pH,测得pH约为12
2 3
2 向0.1mol·L-1 Na CO 溶液中加入过量0.2mol·L-1 CaCl 溶液,产生白色沉淀
2 3 2
3 向0.1mol·L-1 Na CO 溶液中通入过量CO,测得溶液pH约为8
2 3 2
4 向0.1mol·L-1 Na CO 溶液中滴加几滴0.05mol·L-1 HCl溶液,观察不到实验现象
2 3
下列有关说法正确的是A.0.1mol·L-1 Na CO 溶液中存在c(OH-)=c(H+)+c(HCO)+2c(H CO)
2 3 2 3
B.实验2反应静置后的上层清液中有c(Ca2+)·c(CO)<K (CaCO)
sp 3
C.实验3得到的溶液中有c(HCO)<c(CO)
D.实验4中反应的化学方程式为H++OH-=H O
2
7.室温下:K (H C O)=10-1.26、K (H C O)=10-4.27、K (CaC O)=10-8.64。实验室进行多组实验
a1 2 2 4 a2 2 2 4 sp 2 4
测定某些酸、碱、盐性质,相关实验记录如表。下列所得结论正确的是
实验 实验操作和现象
1 测定0.10 mol·L-1 NaHC O 溶液的pH=a
2 4
2 配制pH相等的(NH )SO 、NH Cl、NH HSO 三种溶液
4 2 4 4 4 4
3 向0.10 mol·L-1NaC O 溶液中滴加等浓度盐酸后,混合溶液的pH=7
2 2 4
向0.10 mol·L-1 NaHC O 溶液加入一定体积的等浓度CaCl 溶液产生白色沉
4 2 4 2
淀,测得上层清液pH=4,c(Ca2+)=10-4 mol·L-1
A.a >7
B.实验2中溶液浓度的大小关系为c(NH Cl)c(HSO)+2c(SO)
C.实验3可以得出:K (H SO )·K (H SO )>K
a1 2 3 a2 2 3 w
D.实验4中反应后的溶液中存在:c(SO)+3c(SO)=c(H SO )
2 3
10.常温下,用0.10 mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10 mol·L-1HA溶液和HB
溶液,所得滴定曲线如图所示(其中HA的滴定曲线部分未画出)。下列说法错误的是
已知:M点溶液中c(A-)=c(HA)
A.=105.8
B.P点溶液中溶质为NaB和HB,由水电离出的c(H+)=1.0×10-7 mol·L-1
C.M点溶液中,2c(Na+)>c(HA)+c(A-)
D.等体积等浓度的HB溶液和NaA溶液混合后的溶液中:c(OH-)<c(H+)
【随堂反馈】答案
1.D 2.C 3.C 4.C 5.B 6.A 7.D 5.B 9.D 10.D
【课后作业】1.25℃时,苯酚(C HOH)的K=1.0×10-10,下列说法正确的是
6 5 a
A.相同温度下,等pH的C HONa和CHCOONa溶液中,c (C HO-)>c (CH COO-)
6 5 3 6 5 3
B.将浓度均为0.10mol·L-1的C HONa和NaOH溶液加热,两种溶液的pH均变大
6 5
C.25℃时,C HOH溶液与NaOH溶液混合,测得pH=10.00,则此时溶液中
6 5
c(C HO-)= c(C HOH)
6 5 6 5
D. 25℃时,0.10mol·L-1的C HOH溶液中加少量C HONa固体,水的电离程度变小
6 5 6 5
2.常温下,下列有关叙述正确的是
A.NaY溶液的pH=8,c (Na+) > c(Y-) > c(OH-) > c(H+)
B.NaCO 溶液中:c(Na+)=2c(CO)+c(HCO -)+c(H CO)
2 3 3 2 3
C.0.1mol·L-1NH Cl的溶液和0.1 mol·L-1NH ·H O的溶液等体积混合后溶液中:
4 3 2
c(Cl-)>c(NH +)>c(OH-)>c(H+)
4
D.10mLpH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,则HA溶液体积
一定是10mL
3.巳知NaHSO 溶液常温时显酸性,溶液中存在以下平衡:
3
HSO+H O HSO +OH-① HSO H++ SO②
2 2 3
向0.1 mol·L-1的NaHSO 溶液中分别加入以下物质, 下列有关说法正确的是
3
A.加入少量金属钠,平衡①左移,平衡②右移,溶液中c (HSO)增大
B.加入少量 NaSO 固体,则c (H+)+ c (Na+)= c (HSO)+ c (OH-)+ c (SO)
2 3
C.加入少量 NaOH溶液,则 、 的值均增大
D.加入氨水至中性。则2 c (Na+)= c (SO)>c (H+)=c (OH-)
4.室温下,向10 mL pH=10的氨水溶液中加入下列物质,对所得溶液的分析错误的是
选项 加入的物质 对所得溶液的分析
A 90 mL HO 水电离的c (OH-)<10-9 mol·L-1
2
B 0.1 mol NH Cl固体 溶液中的c (OH-)比原氨水溶液中的小
4
C 10 mLpH=10的NaOH溶液 c (Na+)+ c (NH)+ c (H+)= c (OH-)
D 10 mL pH=4的HCl溶液 c (NH)>c (Cl-)>c (H+)>c (OH-)
5.室温下,通过下列实验探究NaHCO 溶液的性质。下列有关说法正确的是
3
实验 实验操作和现象
1 用pH计测定0.05 mol·L-1NaHCO 溶液的pH,测得pH约为8.3
3
向10 mL 0.05 mol·L-1 NaHCO 溶液中滴加10 mL 0.05 mol·L-1NaOH溶液,反应
2 3
结束,测得pH约为11.3
向10 mL 0.05 mol·L-1NaHCO 溶液中滴加10 mL 0.05 mol·L-1盐酸,反应结束,
3 3
测得pH约为4.3
4 向0.05 mol·L-1NaHCO 溶液中滴加过量0.1 mol·L-1Ca(OH) 溶液,产生白色沉淀
3 2
A.由实验1可知,NaHCO 溶液中HCO的电离程度大于水解程度
3
B.实验2滴加过程中:c(HCO)+2c(CO)+c(OH-)逐渐减小
C.实验3滴加过程中:c(Na+)=c(HCO)+c(CO)+c(H CO)
2 3
D.实验4反应静置后的上层清液中:c(Ca2+)·c(CO)<K (CaCO)
sp 3
6.室温下取NH Cl溶液、氨水进行如下实验。
4
实验1:将0.1 mol·L-1 NHCl溶液和0.1 mol·L-1氨水等体积混合,混合溶液的pH>7。
4
实验2:将0.1 mol·L-1 NH·H O与0.1 mol·L-1 FeCl 溶液等体积混合,生成红褐色沉淀。
3 2 3
实验3:向0.1 mol·L-1 NHCl溶液中通入少量NH 。
4 3
实验4:向10 mL 0.1 mol·L-1NH ·H O中滴加20 mL 0.1 mol·L-1盐酸。
3 2
下列说法正确的是
A.K (NH ·H O)<10-7
b 3 2
B.实验2说明混合时溶液中存在K [Fe(OH) ]>c3(OH-)·c(Fe3+)
sp 3
C.实验3中NH +的水解程度减小
4
D.实验4所得混合溶液中c(H+)<c(NH +)+c(NH ·H O)+c(OH-)
4 3 2
7.常温下将NaOH溶液滴加到磷酸(H PO )溶液中,混合溶液中的pH与部分离子浓度变化的
3 4
关系如图所示。下列说法正确的是A.NaHPO 溶液中:2c(Na+)=c(H PO )+c(H PO)+c(HPO)+c(PO)
2 4 3 4 2
B.若直线丙表示pH与 的变化关系,应该在甲、乙之间
C.常温下,K (H PO )=10-6.79
a2 3 4
D.当c(HPO)=c(H PO )时,pH=4.68
3 4
8.常温下,Ka(CHCOOH)=1.75×10-5,Ka (HCN)=6.2×10-10,下列说法正确的是
3
A.0.1 mol·L-1 CH COONa溶液与0.1 mol·L-1 KCN溶液:
3
c (Na+)- c (CH COO-)> c (K+)- c (CN-)
3
B.20mL0.1mol·L-1 CH COONa与10mL 0.1mol·L-1 HCl溶液混合后所得酸性溶液:
3
c (Na+)> c (CH COOH)> c (CH COO-)
3 3
C.0.2 mol·L-1HCN溶液与0.1 mol·L-1 NaOH溶液等体积混合所得溶液:
c (Na+)> c (CN-)> c (H+)> c (OH-)
D.向浓度均为0.1 mol·L-1的CHCOOH和HCN混合溶液中滴加0.1 mol·L-1NaOH溶液,
3
当恰好中和时所得溶液:c (CH COOH)+ c (HCN)+ c (H+)= c (OH-)
3
9.室温下,通过下列实验探究NaHSO 溶液的性质。
3
实验 实验操作和现象
1 用pH试纸测定0.1mol·L-1NaHSO 溶液的pH,测得pH约为5
3
2 向0.1mol·L-1NaHSO 溶液中滴加酸性KMnO 溶液,溶液紫红色褪去
3 4
3 将浓度均为0.01mol·L-1的NaHSO 和Ba(OH) 溶液等体积混合,产生白色沉淀
3 2
4 向0.1mol·L-1NaHSO 溶液中滴加稀盐酸,有刺激性气体产生
3
下列有关说法正确的是
A.0.1mol·L-1NaHSO 溶液中存在c (H+)= c (OH-)+ c (SO) - c (HSO )
3 2 3
B.实验2说明NaHSO 溶液具有漂白性
3
C.依据实验3的现象,不能得出K (BaSO)<2.5×10-5的结论
sp 3
D.实验4中生成的刺激性气体可能为Cl
2
10.氢硫酸是一种二元弱酸。NaS是染料工业中用于生产硫化青和硫化蓝的原料,现对常温
2
时NaS溶液的性质进行探究,则下列结论正确的是
2
A.0.1 mol·L-1NaS溶液中存在:c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-)
2
B.已知酸性:HCO>HS,向NaS溶液中通入过量CO,反应的离子方程式为
2 3 2 2 2
CO+S2-+HO===H S↑+CO
2 2 2
C.0.1 mol·L-1的NaS溶液存在:
2
c(OH-)=c(H+)+c(HS-)+2c(H S)
2
D.在5 mL 0.01 mol·L-1的NaS溶液中先滴入几滴0.01 mol·L-1ZnCl 溶液有白色沉淀生
2 2
成,再滴入0.01 mol·L-1CuCl 溶液,出现黑色沉淀,证明K (CuS)<K (ZnS)
2 sp sp
11.室温下,通过下列实验探究NaC O 溶液的性质。
2 2 4
已知25 ℃时,K (H C O)=5.9×10-2,K (H C O)=6.4×10-5。
a1 2 2 4 a2 2 2 4
实验1:用pH计测得0.0100 mol·L-1NaC O 溶液pH为8.60。
2 2 4
实验2:向0.0100 mol·L-1NaC O 溶液中滴加0.02 mol/L CaCl 溶液,产生白色沉淀。
2 2 4 2
实验3:向0.0100 mol·L-1NaC O 溶液中滴加等浓度等体积稀盐酸,无明显现象。
2 2 4
实验4:向0.0100mol·L-1NaC O 溶液中加入足量稀硫酸,再滴加KMnO 溶液,溶液紫红
2 2 4 4
色褪去。
下列说法正确的是
A.实验1溶液中存在c(OH-)=c(H+)+2c(HC O)+c(H C O)
2 2 2 4
B.实验2上层清液中一定存在
c(C O)×0.005 mol·L-1=K (CaC O)
2 sp 2 4
C.实验3溶液中存在c(H+)+c(C O)>c(H C O)+c(OH-)
2 2 2 4
D.实验4溶液中KMnO 参与反应的离子方程式为
4
5C O+2MnO+16H+===10CO ↑+2Mn2++8HO
2 2 2
12.25 ℃时,向20 mL0.1 mol·L-1的HSO 溶液中滴加0.1 mol·L-1NaOH溶液,所得HSO 、SO
2 3 2 3和HSO的物质的量分数随pH的变化如图所示。下列说法不正确的是
A.HSO 的电离平衡常数K =10-1.9,K =10-7.2
2 3 a1 a2
B.向pH=7.2的溶液滴加NaOH溶液,反应的离子方程式为
HSO +OH-===HSO+HO
2 3 2
C.当溶液的pH=7时,溶液中存在:c(Na+)=c(HSO)+2c(SO)
D.当滴加NaOH溶液的体积为10mL时,所得溶液呈酸性
【课后作业】答案
1.C 2.A 3.C 4.D 5.B 6.C 7.D 8.D 9.A 10.C 11.C 12.B