文档内容
2025届高三化学一轮专题复习讲义(27)
专题七 化学热点
7-1 化工流程题(1课时)
【复习目标】
1.培养将实际问题分解,通过运用相关知识,采用分析、综合的方法,解决简单化学问题
的能力。
2.培养将分析和解决问题的过程及成果用正确的化学术语及文字、图表、模型、图形等
表达并做出解释的能力。
【重点突破】化学工艺流程题的分析方法和解题策略
【真题再现】
例1.(2023·江苏高考)V2O5-WO3/TiO2催化剂能催化NH3脱除烟气中的NO,反应为
4NH3(g)+O2(g)+4NO(g)===4N2(g)+6H2O(g) ΔH=-1 632.4 kJ·mol-1。
(1)催化剂的制备。将预先制备的一定量的WO3/TiO2粉末置于80 ℃的水中,在搅拌下
加入一定量的NH4VO3溶液,经蒸发、焙烧等工序得到颗粒状V2O5-WO3/TiO2
催化剂。在水溶液中水解为 H3VO4沉淀的离子方程式为________________;反应
选用 NH4VO3溶液而不选用NaVO3溶液的原因是_____________________。
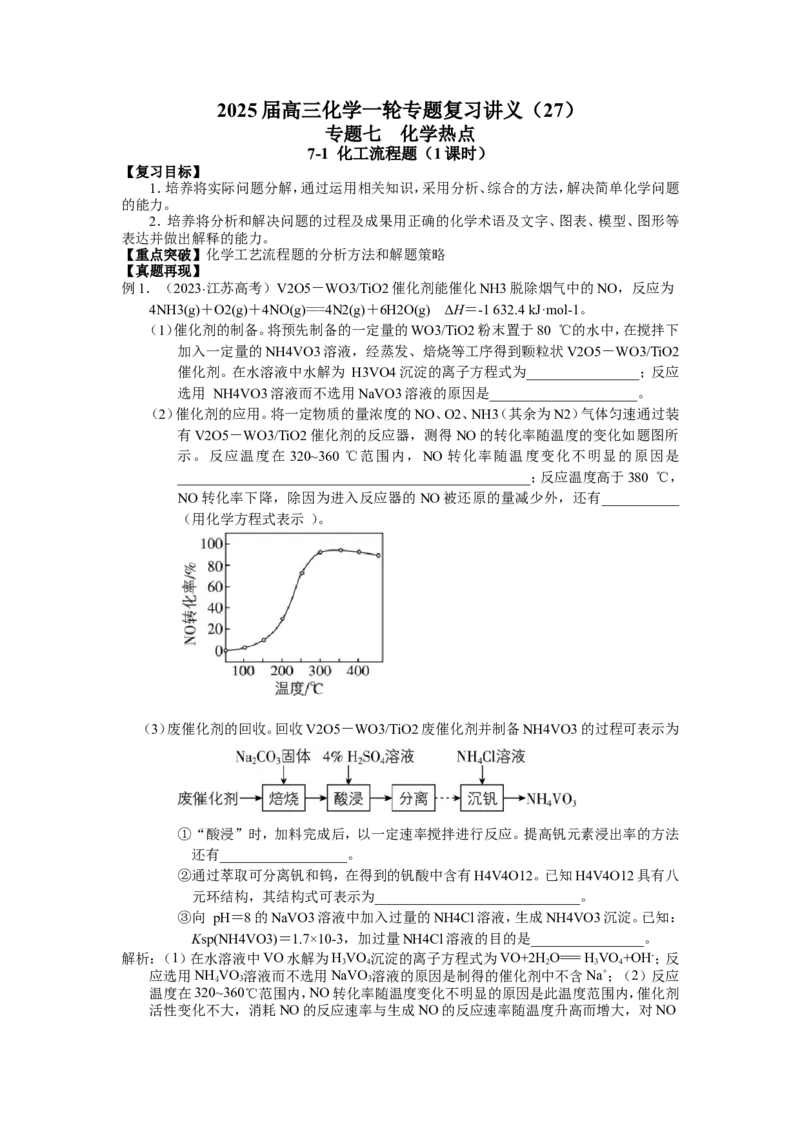
(2)催化剂的应用。将一定物质的量浓度的NO、O2、NH3(其余为N2)气体匀速通过装
有V2O5-WO3/TiO2催化剂的反应器,测得NO的转化率随温度的变化如题图所
示。反应温度在 320~360 ℃范围内,NO 转化率随温度变化不明显的原因是
__________________________________________________;反应温度高于380 ℃,
NO转化率下降,除因为进入反应器的NO被还原的量减少外,还有___________
(用化学方程式表示 )。
(3)废催化剂的回收。回收V2O5-WO3/TiO2废催化剂并制备NH4VO3的过程可表示为
①“酸浸”时,加料完成后,以一定速率搅拌进行反应。提高钒元素浸出率的方法
还有__________________。
②通过萃取可分离钒和钨,在得到的钒酸中含有H4V4O12。已知H4V4O12具有八
元环结构,其结构式可表示为_____________________________。
③向 pH=8的NaVO3溶液中加入过量的NH4Cl溶液,生成NH4VO3沉淀。已知:
Ksp(NH4VO3)=1.7×10-3,加过量NH4Cl溶液的目的是________________。
解析:(1)在水溶液中VO水解为HVO 沉淀的离子方程式为VO+2HO=== HVO +OH-;反
3 4 2 3 4
应选用NH VO 溶液而不选用NaVO 溶液的原因是制得的催化剂中不含Na+;(2)反应
4 3 3
温度在320~360℃范围内,NO转化率随温度变化不明显的原因是此温度范围内,催化剂
活性变化不大,消耗NO的反应速率与生成NO的反应速率随温度升高而增大,对NO转化率的影响相互抵消。反应温度高于380℃,NO转化率下降,有可能体系产生了NO,
如4NH +5O =========4NO+6H O。
3 2 2
(3)提高钒元素浸出率的方法还有提高反应温度、延长浸出时间,已知HVO 具有八元环结
4 4 22
构,且V连有五根共价键,结构式可表示为 。NH4VO3饱和溶液中存
在溶解平衡NH4VO3(s) NH(aq) + VO(aq),加过量NH4Cl溶液有利于增加铵根离
子浓度,促进平衡向析出沉淀的方向移动,提高NH4VO3的含量,促进NH4VO3充分沉
淀。
答案:(1)VO+2HO=== HVO +OH-制得的催化剂中不含Na+
2 3 4
(2)在该温度范围内,催化剂活性变化不大,消耗NO的反应速率与生成NO的反应速
率随温度升高而增大,对NO转化率的影响相互抵消
4NH +5O =========4NO+6H O
3 2 2
(3)①提高反应温度、延长浸出时间 ② ③促进NH4VO3充分沉淀
例2.(2022·江苏高考)实验室以二氧化铈(CeO)废渣为原料制备Cl-含量少的Ce (CO),其
2 2 3 3
部分实验过程如下:
(1)“酸浸”时CeO 与HO 反应生成Ce3+并放出O,该反应的离子方程式为_______。
2 2 2 2
(2)pH约为7的CeCl 溶液与NH HCO 溶液反应可生成Ce (CO) 沉淀,该沉淀中Cl-
3 4 3 2 3 3
含量与加料方式有关。得到含Cl-量较少的Ce (CO ) 的加料方式为_______(填序
2 3 3
号)。
A.将NH HCO 溶液滴加到CeCl 溶液中
4 3 3
B.将CeCl 溶液滴加到NH HCO 溶液中
3 4 3
(3)通过中和、萃取、反萃取、沉淀等过程,可制备Cl-含量少的Ce (CO)。已知Ce3+能被
2 3 3
有机萃取剂(HA)简称)萃取,其萃取原理可表示为
Ce3+ (水层)+3HA(有机层) Ce (A) (有机层)+3H+ (水层)
3
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是
_______。
②反萃取的目的是将有机层Ce3+转移到水层。使Ce3+尽可能多地发生上述转移,应
选择的实验条件或采取的实验操作有_______(填两项)。
③与“反萃取”得到的水溶液比较,过滤Ce (CO) 溶液的滤液中,物质的量减小的
2 3 3
离子有_______(填化学式)。
解析:用稀盐酸和过氧化氢溶液酸浸二氧化铈废渣,得到三价铈,加入氨水调节pH后用萃取
剂萃取其中的三价铈,增大三价铈浓度,之后加入稀硝酸反萃取其中的三价铈,再加入
氨水和碳酸氢铵制备产物。(1)根据信息反应物为CeO 与HO,产物为Ce3+和O,根据
2 2 2 2
电荷守恒和元素守恒可知其离子方程式为:2CeO+H O+6H+===2Ce3++O ↑+4H O;(2)
2 2 2 2 2
反应过程中保持CeCl 少量即可得到含Cl-量较少的Ce (CO ) ,选B;(3)①增大碳酸
3 2 3 3
根离子的浓度有助于生成产物,故降低溶液中氢离子的浓度,促进碳酸氢根离子的电离,
增大溶液中碳酸根离子的浓度;②根据萃取原理可知,应选择的实验条件是酸性条件,
为了使Ce3+尽可能多地发生上述转移,可以采用多次萃取;③“反萃取”得到的水溶液
中含有浓度较大的Ce3+,过滤后溶液中Ce3+离子浓度较小,故为Ce3+。
答案:(1)2CeO+H O+6H+===2Ce3++O ↑+4H O
2 2 2 2 2
(2)B
(3)①降低溶液中氢离子的浓度,促进碳酸氢根离子的电离,增大溶液中碳酸根离子的
浓度
②酸性条件,多次萃取③Ce3+
例3.(2023·新课标)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主
要杂质为铁、铝、硅、磷等的化合物,从铬钒渣中分离提取铬和钒的一种流程如下图所示:
已知:最高价铬酸根在酸性介质中以Cr O存在,在碱性介质中以CrO存在。
2
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
__________(填化学式)。
(2)水浸渣中主要有SiO 和_____。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是______。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀,该步需要控
3 4 4
制溶液的pH≈9以达到最好的除杂效果,若pH<9时,会导致___________;pH>9时,
会导致___________。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到VO 沉淀,VO 在pH<1时,溶解
2 5 2 5
为VO或VO3+在碱性条件下,溶解为VO或VO,上述性质说明VO 具有______(填
2 5
标号)。
A.酸性 B.碱性 C.两性
(6)“还原”步骤中加入焦亚硫酸钠(Na SO)溶液,反应的离子方程式为___________。
2 2 5
解析:(1)由分析可知,煅烧过程中,铬元素转化为铬酸钠,故为:NaCrO;(2)由分析可知,
2 4
水浸渣中主要有二氧化硅、氧化铁,故为:Fe O;(3)由分析可知,沉淀步骤调pH到弱碱
2 3
性的目的是将Al元素转化为氢氧化铝沉淀,故为:Al(OH) ;(4)由分析可知,加入硫酸
3
镁溶液、硫酸铵溶液的目的是将硅元素、磷元素转化为MgSiO 和MgNH PO 沉淀,若溶
3 4 4
液pH<9时,磷酸根会与H+反应使其浓度降低导致MgNH PO 无法完全沉淀,同时可能
4 4
产生硅酸胶状沉淀不宜处理;若溶液pH>9时,会导镁离子生成氢氧化镁沉淀,不能形成
MgSiO 沉淀,导致产品中混有杂质,同时溶液中铵根离子浓度降低导致MgNH PO 无法
3 4 4
完全沉淀,故答案为:磷酸根会与H+反应使其浓度降低导致MgNH PO ,同时可能产生
4 4
硅酸胶状沉淀不宜处理;会导镁离子生成氢氧化镁沉淀,不能形成MgSiO 沉淀,导致产
3
品中混有杂质,同时溶液中铵根离子浓度降低导致MgNH PO 无法完全沉淀;(5)由题
4 4
给信息可知,五氧化二钒水能与酸溶液反应生成盐和水,也能与碱溶液发生生成盐和水
的两性氧化物;(6)由题意可知,还原步骤中加入焦亚硫酸钠溶液的目的是将铬元素转
化为铬离子,反应的离子方程式为2Cr O+3SO+10H+=4Cr3++6SO+5HO。
2 2 2
答案:(1)NaCrO
2 4
(2)Fe O
2 3
(3)Al(OH)
3
(4)磷酸根会与H+反应使其浓度降低导致MgNH PO 无法完全沉淀,同时可能产生硅
4 4
酸胶状沉淀不宜处理会导镁离子生成氢氧化镁沉淀 不能形成MgSiO 沉淀,导
3
致产品中混有杂质,同时溶液中铵根离子浓度降低导致MgNH PO 无法完全沉淀
4 4
(5)C
(6)2Cr O+3SO+10H+=4Cr3++6SO+5HO。
2 2 2
例4.(2023·辽宁)某工厂采用如下工艺处理镍钴矿硫酸浸取液(含 Ni2+、Co2+、Fe2+、Fe3+、
Mg2+和Mn2+)。实现镍、钴、镁元素的回收。已知:
物质 Fe(OH) Co(OH) Ni (OH) Mg(OH)
3 2 2 2
Ksp 10-37.4 10-14.7 10-14.7 10-10.8
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为________(答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸
(HSO ),1mol HSO 中过氧键的数目为__________。
2 5 2 5
(3)“氧化”中,用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO,该反应的离子方程式
2 5 2
为(HSO 的电离第一步完全,第二步微弱);滤渣的成分为MnO、______(填化学
2 5 2
式)。
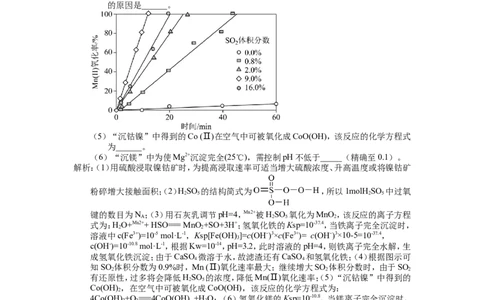
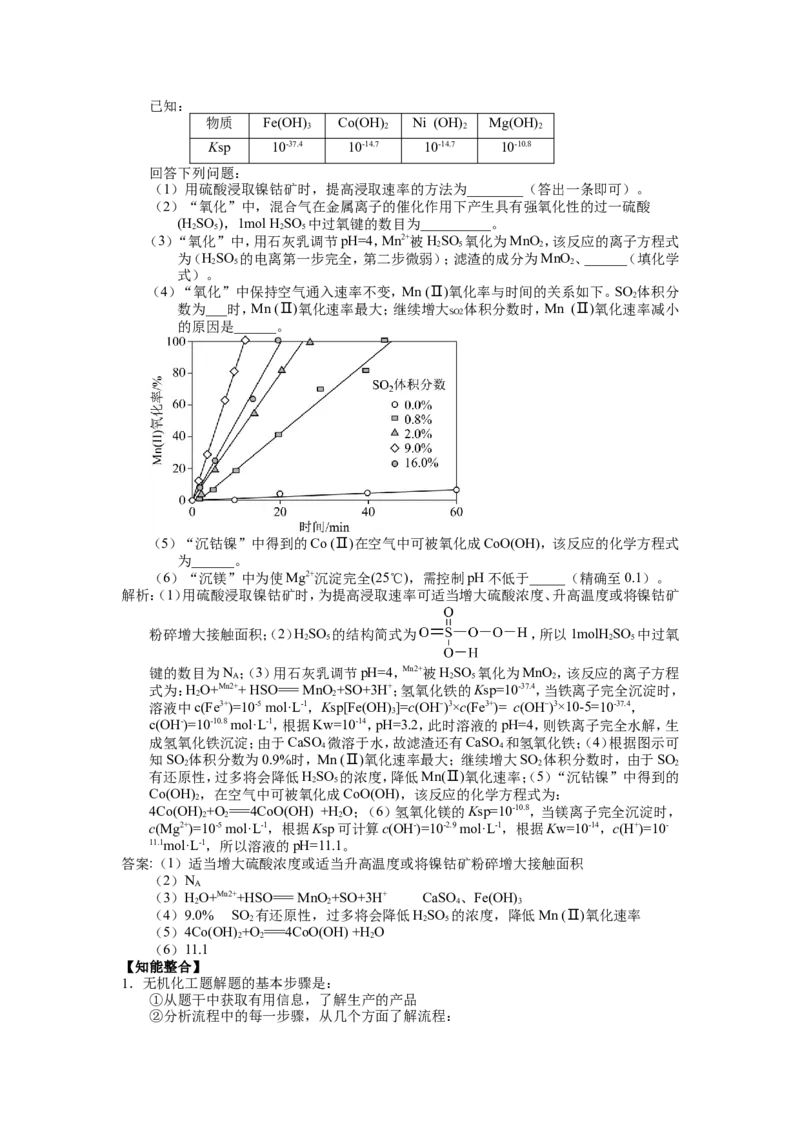
(4)“氧化”中保持空气通入速率不变,Mn (Ⅱ)氧化率与时间的关系如下。SO体积分
2
数为___时,Mn (Ⅱ)氧化速率最大;继续增大 体积分数时,Mn (Ⅱ)氧化速率减小
SO2
的原因是______。
(5)“沉钴镍”中得到的Co (Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式
为______。
(6)“沉镁”中为使Mg2+沉淀完全(25℃),需控制pH不低于_____(精确至0.1)。
解析:(1)用硫酸浸取镍钴矿时,为提高浸取速率可适当增大硫酸浓度、升高温度或将镍钴矿
粉碎增大接触面积;(2)HSO 的结构简式为 ,所以1molHSO 中过氧
2 5 2 5
键的数目为N ;(3)用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO,该反应的离子方程
A 2 5 2
式为:HO+Mn2++ HSO=== MnO+SO+3H+;氢氧化铁的Ksp=10-37.4,当铁离子完全沉淀时,
2 2
溶液中c(Fe3+)=10-5 mol·L-1,Ksp[Fe(OH) ]=c(OH-)3×c(Fe3+)= c(OH-)3×10-5=10-37.4,
3
c(OH-)=10-10.8 mol·L-1,根据Kw=10-14,pH=3.2,此时溶液的pH=4,则铁离子完全水解,生
成氢氧化铁沉淀;由于CaSO 微溶于水,故滤渣还有CaSO 和氢氧化铁;(4)根据图示可
4 4
知SO 体积分数为0.9%时,Mn (Ⅱ)氧化速率最大;继续增大SO 体积分数时,由于SO
2 2 2
有还原性,过多将会降低HSO 的浓度,降低Mn(Ⅱ)氧化速率;(5)“沉钻镍”中得到的
2 5
Co(OH) ,在空气中可被氧化成CoO(OH),该反应的化学方程式为:
2
4Co(OH) +O ===4CoO(OH) +H O;(6)氢氧化镁的Ksp=10-10.8,当镁离子完全沉淀时,
2 2 2
c(Mg2+)=10-5 mol·L-1,根据Ksp可计算c(OH-)=10-2.9 mol·L-1,根据Kw=10-14,c(H+)=10-
11.1mol·L-1,所以溶液的pH=11.1。
答案:(1)适当增大硫酸浓度或适当升高温度或将镍钴矿粉碎增大接触面积
(2)N
A
(3)HO+Mn2++HSO=== MnO+SO+3H+ CaSO、Fe(OH)
2 2 4 3
(4)9.0% SO 有还原性,过多将会降低HSO 的浓度,降低Mn (Ⅱ)氧化速率
2 2 5
(5)4Co(OH) +O ===4CoO(OH) +H O
2 2 2
(6)11.1
【知能整合】
1.无机化工题解题的基本步骤是:
①从题干中获取有用信息,了解生产的产品
②分析流程中的每一步骤,从几个方面了解流程:A.反应物是什么;
B.发生了什么反应;
C.该反应造成了什么后果,对制造产品有什么作用。抓住一个关键点:一切反应或
操作都是为获得产品而服务。
③从问题中获取信息,帮助解题。
2.化工生产的适宜条件
条件 原则
从化学反应速率分析 既不能过快,又不能太慢
既要注意外界条件对速率和平衡影响的一致性,又要注
从化学平衡移动分析
意二者影响的矛盾性
增加易得廉价原料,提高难得高价原料的利用率,从而降
从原料的利用率分析
低生产成本
从实际生产能力分析 如设备承受高温、高压能力等
从催化剂的使用活性分析 注意催化剂的活性对温度的限制
【体系再构】
【巩固练习】
基础训练
1.闭环循环有利于提高资源利用率和实现绿色化学的目标。利用氨法浸取可实现废弃物铜
包钢的有效分离,同时得到的CuCl可用于催化、医药、冶金等重要领域。工艺流程如下:
已知:室温下的Ksp(CuCl)=10-6.8。
回答下列问题:
(1)首次浸取所用深蓝色溶液①由铜毛丝、足量液氨、空气和盐酸反应得到,其主要成分
为________(填化学式)。
(2)滤渣的主要成分为(填化学式)_________________。
(3)浸取工序的产物为[Cu(NH )]Cl,该工序发生反应的化学方程式为_____________。
3 2
浸取后滤液的一半经氧化工序可得深蓝色溶液①,氧化工序发生反应的离子方程
式为_________。
(4)浸取工序宜在30~40℃之间进行,当环境温度较低时,浸取液再生后不需额外加热
即可进行浸取的原因是__________________。
(5)补全中和工序中主反应的离子方程式[Cu(NH )]++2H++Cl-=_____+______。
3 2
(6)真空干燥的目的为________________。
拓展训练
2.利用水钴矿(主要成分为Co O,含少量Fe O、A1 O、MnO、MgO、CaO、SiO 等)可以制取
2 3 2 3 2 3 2
多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:
已知:
①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等。
②沉淀 I中只含有两种沉淀。③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表。
沉淀物 Fe(OH) Fe(OH) Co(OH) Al(OH) Mn(OH)
3 2 2 3 2
开始沉淀 2.7 7.6 7.6 4.0 7.7
完全沉淀 3.7 9.6 9.2 5.2 9.8
(1)浸出过程中Co O 发生反应的离子反应方程式为______。
2 3
(2)NaClO 在浸出液中发生的离子反应方程式为______________。
3
(3)加入NaCO 调pH至5.2,目的是______;萃取剂层含锰元素,则沉淀 II的主要成分
2 3
为______。
(4)操作 I包括:将水层加入浓盐酸调整pH为2~3,______、______、过滤、洗涤、减压
烘干等过程。
(5)为测定粗产品中CoCl ·6HO含量,称取一定质量的粗产品溶于水,加入足量硝酸酸
2 2
化的硝酸银溶液,过滤、洗涤、干燥,测沉淀质量。通过计算发现粗产品中
CoCl ·6HO质量分数大于100%,其原因可能是______(回答一条原因即可)。
2 2
【巩固练习】答案
1.(1)[Cu(NH )]Cl
3 4 2
(2)Fe
(3)[Cu(NH )]Cl +Cu=== 2[Cu(NH )]Cl
3 4 2 3 2
8NH +4[Cu(NH )]++O +4H+===4[Cu(NH )]2++2H O
3 3 2 2 3 4 2
(4)盐酸和液氨反应放热
(5)CuCl↓ 2NH
(6)防止干燥过程中CuCl被空气中的O氧化
2
2.(1)Co O+SO2-+4H+===2Co2++SO2-+2H O
2 3 3 4 2
(2)ClO -+6Fe2++6H+===Cl-+6Fe3++3H O
3 2
(3)使Fe3+和Al3+沉淀完全 CaF 和MgF
2 2
(4)蒸发浓缩;冷却结晶
(5)产品中结晶水含量低 产品中混有氯化钠杂质
【课后作业】
1.金属铬Cr常用于制造不锈钢和仪器仪表的金属表面镀铬。由FeCr O(亚铬酸亚铁)制备
2 4
Cr的流程如下(+6价铬元素在酸性条件下以Cr O的形式存在 。下列说法错误的是
2
A.FeCr O 中Cr元素的化合价为+3价
2 4
B.反应①中参加反应的FeCr O 和NaCO 的物质的量之比为3:1
2 4 2 3
C.反应③的化学方程式为NaCr O+2C=====Cr O+Na CO+CO↑
2 2 7 2 3 2 3
D.反应④中的Si可用Al来代替
2.硫酸锌是制备荧光粉的原料之一。工业上由锌白矿(主要成分是ZnO,还含有Fe O、CuO、
2 3
SiO 等杂质)制备ZnSO·7HO的流程如下。
2 4 2
已知:常温下,溶液中的Fe3+、Zn2+、Fe2+以氢氧化物形式完全沉淀的pH分别为:3.7,6.5,
9.7。
(1)浸取过程中提高浸出效率可采用的措施有 (任答一条),ZnO
和硫酸反应的化学方程式为 。(2)加入适量锌粉的作用为:①使溶液中的Fe3+转化为Fe2+;② 。
(3)氧化过程中HO 发生反应的离子方程式为 。
2 2
(4)加入适量Ca(OH) 调节溶液pH,促进Fe3+水解,Fe3+水解反应的平衡常数表达式K=
2
,Ca(OH) 不能过量的原因是 。
2
3.以高硫铝土矿(主要成分为Al O、Fe O、SiO,少量FeS 和金属硫酸盐)为原料,生产氧化
2 3 2 3 2 2
铝并获得Fe O 的部分工艺流程如下:
3 4
(1)焙烧过程均会产生SO ,用NaOH溶液吸收过量SO 的离子方程式为_________。
2 2
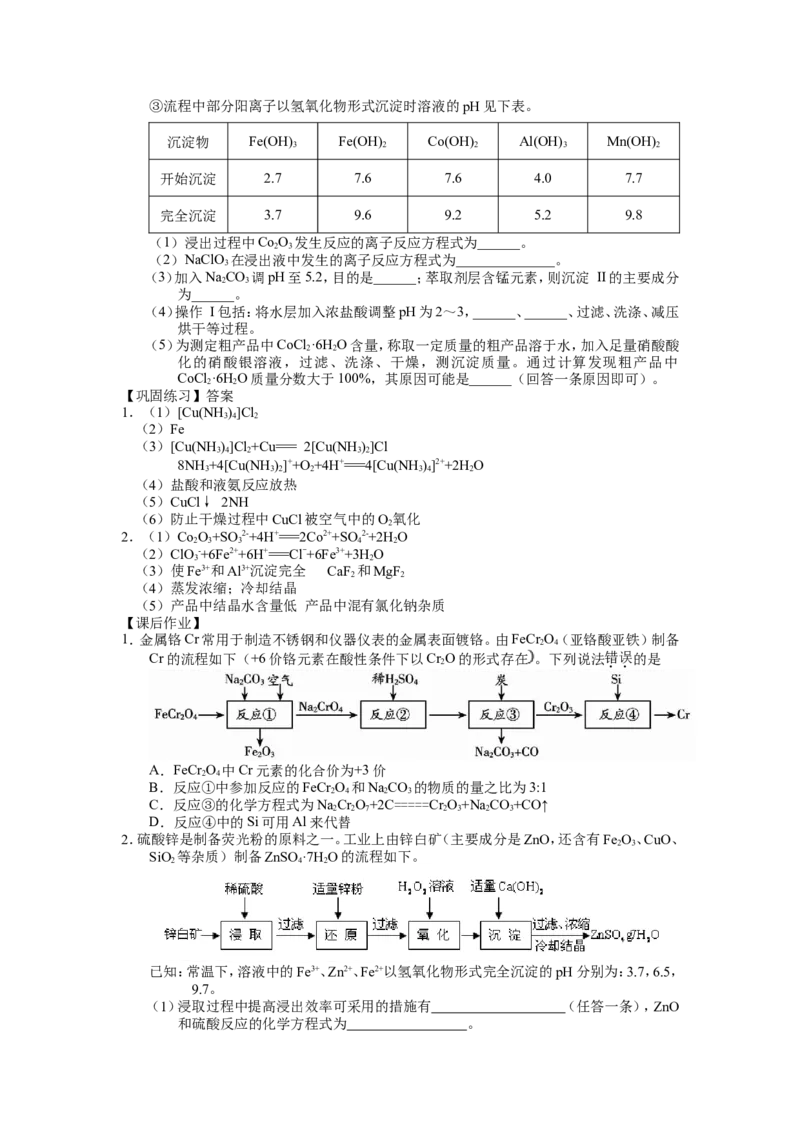
(2)添加1% CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如图所示。
已知:多数金属硫酸盐的分解温度都高于600 ℃
硫去除率=(1-)×100%
①不添加CaO的矿粉在低于500 ℃焙烧时,去除的硫元素主要来源于________。
②700 ℃焙烧时,添加1% CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,
其主要原因是____________________________。
(3)向“过滤”得到的滤液中通入过量CO,铝元素存在的形式由__________(填化学
2
式)转化为__________(填化学式)。
(4)“过滤”得到的滤渣中含大量的Fe O。Fe O 与FeS 混合后在缺氧条件下焙烧生成
2 3 2 3 2
Fe O 和SO ,理论上完全反应消耗的n(FeS )∶n(Fe O)=________。
3 4 2 2 2 3
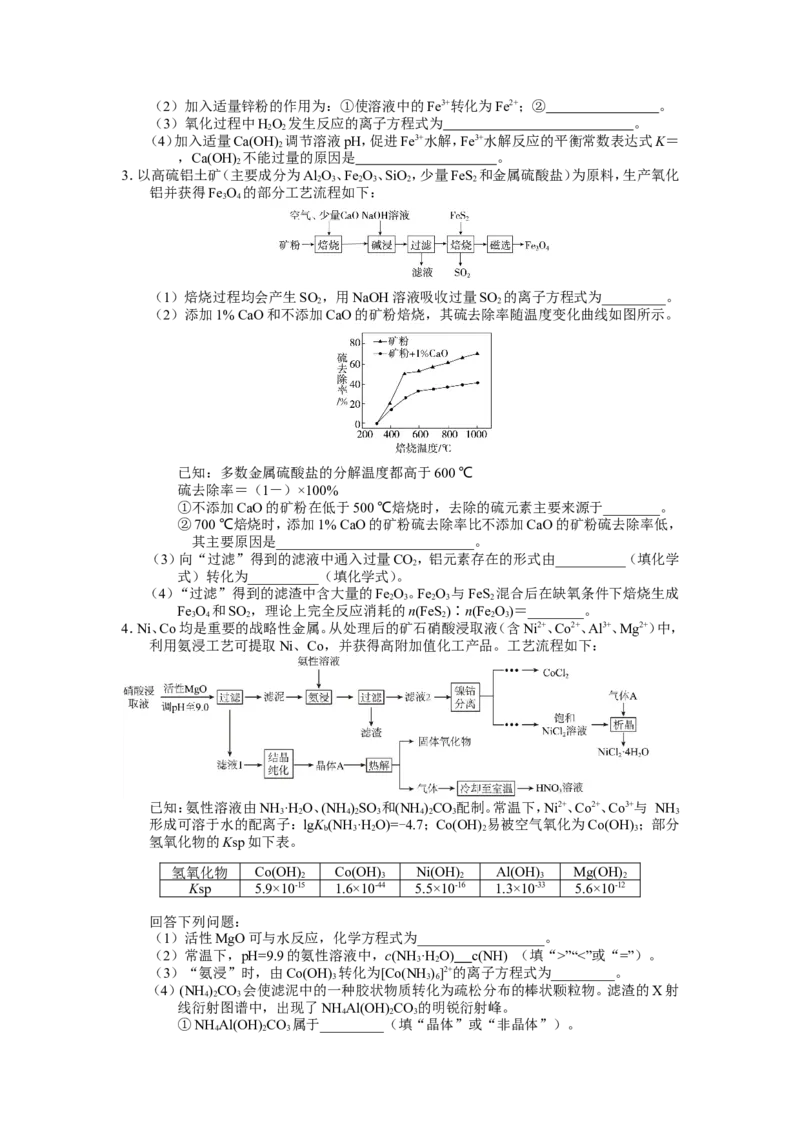
4.Ni、Co均是重要的战略性金属。从处理后的矿石硝酸浸取液(含Ni2+、Co2+、Al3+、Mg2+)中,
利用氨浸工艺可提取Ni、Co,并获得高附加值化工产品。工艺流程如下:
已知:氨性溶液由NH·H O、(NH)SO 和(NH)CO配制。常温下,Ni2+、Co2+、Co3+与 NH
3 2 4 2 3 4 2 3 3
形成可溶于水的配离子:lgK (NH·H O)=-4.7;Co(OH) 易被空气氧化为Co(OH) ;部分
b 3 2 2 3
氢氧化物的Ksp如下表。
氢氧化物 Co(OH) Co(OH) Ni(OH) Al(OH) Mg(OH)
2 3 2 3 2
Ksp 5.9×10-15 1.6×10-44 5.5×10-16 1.3×10-33 5.6×10-12
回答下列问题:
(1)活性MgO可与水反应,化学方程式为__________________。
(2)常温下,pH=9.9的氨性溶液中,c(NH·H O) c(NH) (填“>”“<”或“=”)。
3 2
(3)“氨浸”时,由Co(OH) 转化为[Co(NH )]2+的离子方程式为_________。
3 3 6
(4)(NH)CO 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射
4 2 3
线衍射图谱中,出现了NHAl(OH) CO的明锐衍射峰。
4 2 3
①NHAl(OH) CO 属于_________(填“晶体”或“非晶体”)。
4 2 3②(NH)CO 提高了Ni、Co的浸取速率,其原因是___________。
4 2 3
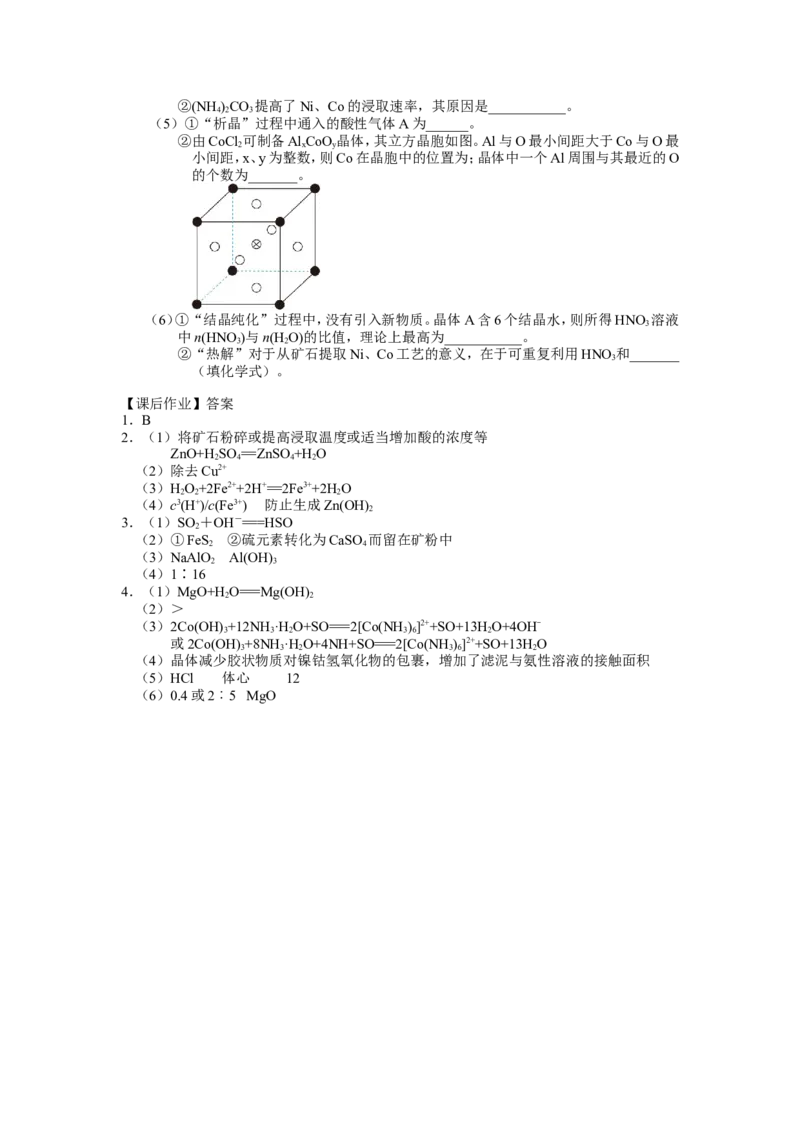
(5)①“析晶”过程中通入的酸性气体A为______。
②由CoCl可制备AlCoO晶体,其立方晶胞如图。Al与O最小间距大于Co与O最
2 x y
小间距,x、y为整数,则Co在晶胞中的位置为;晶体中一个Al周围与其最近的O
的个数为_______。
(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得HNO 溶液
3
中n(HNO)与n(H O)的比值,理论上最高为___________。
3 2
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO 和_______
3
(填化学式)。
【课后作业】答案
1.B
2.(1)将矿石粉碎或提高浸取温度或适当增加酸的浓度等
ZnO+H SO =ZnSO+H O
2 4 4 2
(2)除去Cu2+
(3)HO+2Fe2++2H+=2Fe3++2H O
2 2 2
(4)c3(H+)/c(Fe3+) 防止生成Zn(OH)
2
3.(1)SO +OH-===HSO
2
(2)①FeS ②硫元素转化为CaSO 而留在矿粉中
2 4
(3)NaAlO Al(OH)
2 3
(4)1∶16
4.(1)MgO+HO===Mg(OH)
2 2
(2)>
(3)2Co(OH) +12NH·H O+SO===2[Co(NH )]2++SO+13HO+4OH-
3 3 2 3 6 2
或2Co(OH) +8NH·H O+4NH+SO===2[Co(NH )]2++SO+13HO
3 3 2 3 6 2
(4)晶体减少胶状物质对镍钴氢氧化物的包裹,增加了滤泥与氨性溶液的接触面积
(5)HCl 体心 12
(6)0.4或2︰5 MgO