文档内容
课时检测(九) 物质的量的基本知能评价
1.下列对摩尔(mol)的有关说法错误的是( )
A.摩尔是一个单位而非物理量
B.摩尔既能用来计量纯净物,又能用来计量混合物
C.1 mol任何气体所含分子的数目都相等
D.0.5 mol氦约含有1.204×1024个电子
2.我国航天员成功实现了在太空泡茶,茶装在特制包装袋中,注水后用加热器进行加热就可以饮
用,但要插上吸管以防止水珠飘起来。下列说法正确的是( )
A.航天员喝茶时注入的2 mol H O的摩尔质量是36
2
B.1 mol水的质量是18 g
C.1 mol H O含有3 mol电子
2
D.标准状况下,1 mol冰水混合物的体积约是22.4 L
3.下列说法正确的是( )
A.标准状况下,22.4 L H 和O 的混合物含有的分子数为N
2 2 A
B.标准状况下,18 g H O的体积是22.4 L
2
C.常温常压下,11.2 L N 含有的分子数为0.5N
2 A
D.标准状况下,11.2 L CCl 含有的原子数为2.5N
4 A
4.如图,用油膜法测出一层油酸分子(视为球形)的厚度后,要计算出阿伏加德罗常数的值,还需要
下列哪一个物理量( )
INCLUDEPICTURE "25YLYCXKHX2-3.TIF" \* MERGEFORMAT
A.油酸分子的直径
B.油滴的体积
C.1 mol油酸的体积
D.油酸的摩尔质量
5.下列说法正确的是( )
A.同温同压下,甲烷和氧气的密度之比为2∶1
B.1 g甲烷和1 g氧气所含原子数之比为5∶1
C.等物质的量的甲烷和氧气的质量之比为2∶1
D.标准状况下,等质量的甲烷和氧气的体积之比为1∶2
6.如图所示,甲、乙、丙常温下都为气体,2 mol甲反应生成1 mol丙和3 mol乙,下列判断不正确
的是( )
INCLUDEPICTURE "24YLXGKHXⅡ2-2.TIF" \* MERGEFORMAT
A.1个乙分子中含有2个H原子
B.甲的摩尔质量为17 g·mol-1
C.同温同压下,生成丙和乙的体积比为1∶3D.化学反应中各物质的质量之比等于2∶1∶3
7.某硫原子的质量为a g,12C原子的质量为b g,若N 表示阿伏加德罗常数的值,则下列说法正确
A
的是( )
①该硫原子的相对原子质量为
②m g该硫原子的物质的量为 mol
③该硫原子的摩尔质量是aN g
A
④a g该硫原子所含的电子数为16N
A
A.①③ B.②④ C.①② D.②③
8.在同温同压下的两个容积相同的容器中,一个盛有HCl气体,另一个盛有H 和Cl 的混合气,
2 2
则两容器内的气体一定具有相同的( )
A.原子数 B.密度
C.质量 D.摩尔质量
9.在甲、乙两个体积不同的密闭容器中,分别充入质量相等的CO、CO 气体时,两容器的温度和
2
压强均相同,则下列说法正确的是( )
A.充入的CO分子数比CO 分子数少
2
B.甲容器的体积比乙容器的体积小
C.CO的摩尔体积比CO 的摩尔体积小
2
D.甲中CO的密度比乙中CO 的密度小
2
10.以“物质的量”为中心的计算是化学计算的基础。下列与物质的量相关的计算正确的为( )
A.现有CO、CO 、O 三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
2 3
B.5.6 g CO和4.48 L CO 中含有的碳原子数一定相等
2
C.标准状况下,11.2 L X气体分子的质量为32 g,则X气体的摩尔质量为64
D.a g Cl 中有b个氯原子,则阿伏加德罗常数N 的数值可以表示为
2 A
11.我国科学家屠呦呦因发现青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖。青蒿素的
分子式为C H O,相对分子质量为282,双氢青蒿素的分子式为C H O,相对分子质量为284。N
15 22 5 15 24 5 A
表示阿伏加德罗常数的值,下列关于青蒿素的说法不正确的是( )
A.C H O 的摩尔质量为282 g·mol-1
15 22 5
B.14.2 g双氢青蒿素中含有的原子总数为2.2N
A
C.一个C H O 粒子的质量约为 g
15 22 5
D.含有6.02×1023个碳原子的C H O 的物质的量为1 mol
15 22 5
12.一个密闭容器,被中间一个可自由滑动的隔板(厚度不计)分成两部分,
INCLUDEPICTURE "25YLCXHXⅡ2-3.TIF" \* MERGEFORMAT
当左侧充入1 mol N,右侧充入一定量CO时,隔板处于如图位置(保持温度不变),下列说法正确
2
的是( )
A.左右两侧气体分子数之比为1∶4
B.右侧CO的质量为5.6 g
C.右侧气体密度是相同条件下氢气密度的14倍D.若改变右侧CO的充入量而使隔板处于容器正中间,保持温度不变,则应充入0.2 mol CO
13.向三个密闭容器中分别充入N、H、O 三种气体,以下各种情况下排序正确的是( )
2 2 2
A.当它们的温度和压强均相同时,三种气体的密度:ρ(O )>ρ(N )>ρ(H )
2 2 2
B.当它们的温度和密度都相同时,三种气体的压强:p(O )>p(N )>p(H )
2 2 2
C.当它们的质量、温度和压强均相同时,三种气体的体积:V(O )>V(N )>V(H )
2 2 2
D.当它们的压强、体积和温度均相同时,三种气体的质量:m(H )>m(N )>m(O )
2 2 2
14.现有14.4 g CO和CO 的混合气体,在标准状况下所占的体积约为8.96 L。用N 表示阿伏加德
2 A
罗常数的值,回答下列问题。
(1)该混合气体的平均摩尔质量:
________________________________________________________________________。
(2)混合气体中碳原子的个数:
________________________________________________________________________。
(3)将混合气体依次通过如图装置,最后收集在气球中。
INCLUDEPICTURE "25YLCXHXⅡ2-4.TIF" \* MERGEFORMAT
①气球中收集到的气体的摩尔质量为_________________________________________。
②在标准状况下,气球中收集到的气体的体积为________________。
③气球中收集到的气体的电子总数为__________。
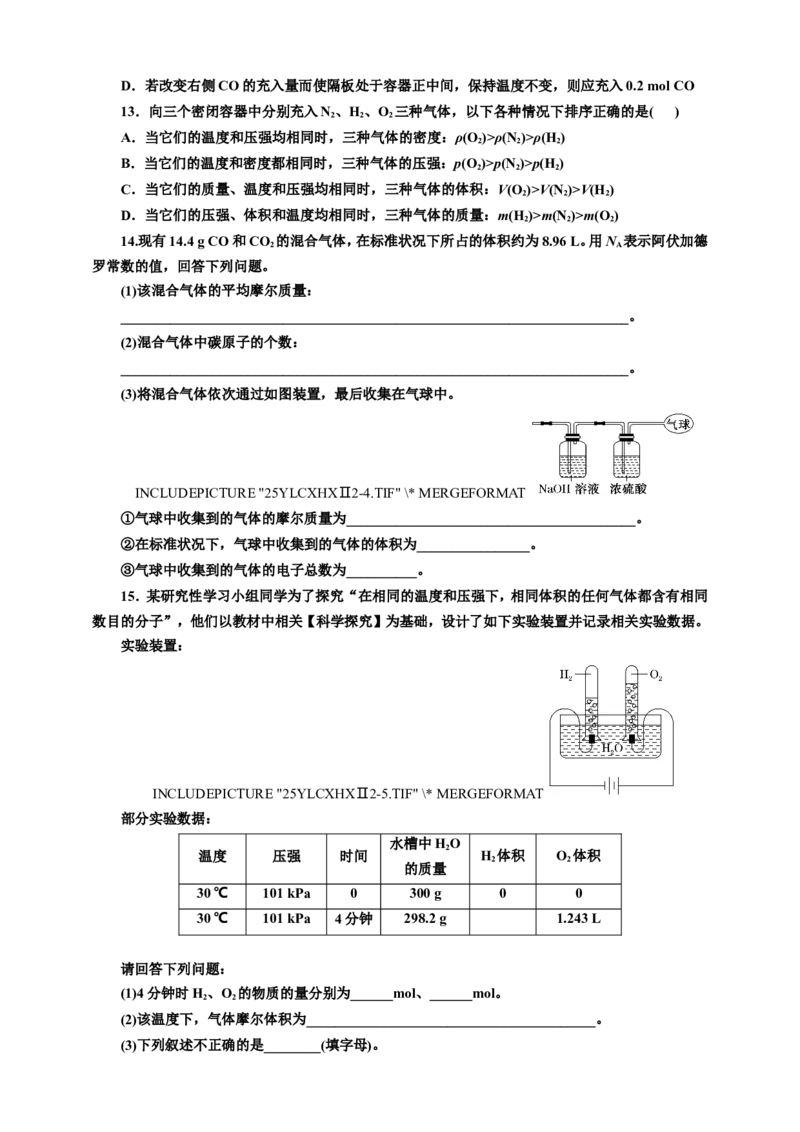
15.某研究性学习小组同学为了探究“在相同的温度和压强下,相同体积的任何气体都含有相同
数目的分子”,他们以教材中相关【科学探究】为基础,设计了如下实验装置并记录相关实验数据。
实验装置:
INCLUDEPICTURE "25YLCXHXⅡ2-5.TIF" \* MERGEFORMAT
部分实验数据:
水槽中HO
2
温度 压强 时间 H 体积 O 体积
2 2
的质量
30 ℃ 101 kPa 0 300 g 0 0
30 ℃ 101 kPa 4分钟 298.2 g 1.243 L
请回答下列问题:
(1)4分钟时H、O 的物质的量分别为______mol、______mol。
2 2
(2)该温度下,气体摩尔体积为_________________________________________。
(3)下列叙述不正确的是________(填字母)。A.气体摩尔体积与气体的温度相关
B.在该实验条件下,3 mol O 的气体摩尔体积为74.58 L·mol-1
2
C.同温同压下,2 mol CO、CO 混合气体和 2 mol O 的体积相同
2 2
D.在该实验条件下,O 的密度约为1.287 g·L-1
2
课时检测(九)
1.D 摩尔是物质的量的单位,A正确;摩尔用来计量微粒的量,可以是纯净物的微粒,也可以是
混合物的微粒,B正确;气体物质的量相等,则气体的分子数目相等,C正确;氦为单原子分子,0.5 mol
氦含有0.5 mol氦原子,1个氦原子含有2个电子,所以0.5 mol氦约含有6.02×1023个电子,D错误。
2.B
3.A 标准状况下,HO、CCl 均为非气态,B、D错误;常温常压下,11.2 L N 不是0.5 mol,C错误。
2 4 2
4.C 由题意可知,一层油酸分子的厚度即为油酸分子的直径,可算出一个油酸分子的体积,设其
体积为V,N =,即只要知道1 mol油酸的体积,即可求出N 。
A A
5.B 同温同压下,甲烷和氧气的密度之比等于二者的相对分子质量之比,则ρ(CH)∶ρ(O )=
4 2
16∶32=1∶2,A错误;1 g甲烷和1 g氧气的物质的量之比为∶=2∶1,二者所含原子数之比为
(2×5)∶(1×2)=5∶1,B正确;根据m=n·M可知,等物质的量的甲烷和氧气的质量之比等于二者的摩
尔质量之比,则m(CH)∶m(O )=16∶32=1∶2,C错误;根据V=n·V 可知,同温同压下,等质量的
4 2 m
甲烷和氧气的体积之比等于二者的物质的量之比,设甲烷和氧气的质量均为m g,则n(CH)∶n(O )=
4 2
∶=2∶1,D错误。
6.D 该化学反应中各物质的质量之比为(2×17)∶(1×28)∶(3×2)=17∶14∶3,D错误。
7.C 该硫原子的相对原子质量为=,①对;该硫原子的摩尔质量为a g×N mol-1=aN g·mol-1,
A A
③错;m g该硫原子的物质的量为= mol,②对;1个硫原子所含的电子数为16,则16 N 为1 mol硫原
A
子所含电子数,④错。
8.A 根据阿伏加德罗定律,在同温同压下的两个容积相同的容器中,一个盛有HCl气体,另一
个盛有H 和Cl 的混合气,则两容器内的气体一定具有相同的分子数,由于HCl、H、Cl 都是双原子
2 2 2 2
分子,所以两容器内的气体一定具有相同的原子数,故选A。
9.D 质量相等的CO和CO 的物质的量之比为44∶28=11∶7,根据N=n·N ,二者分子数之比
2 A
为11∶7,故A错误;在温度和压强相同时,气体体积之比等于物质的量之比,为11∶7,故B错误;在
温度和压强相同时,气体摩尔体积相同,故C错误;根据ρ=,质量相等的CO和CO 的密度之比等于
2
摩尔质量之比,为28∶44=7∶11,故D正确。
10.D 设一氧化碳、二氧化碳和臭氧的物质的量分别为x mol、y mol、z mol,由三种气体含有的
氧原子个数都为1 mol可得x=2y=3z,则三种气体的物质的量之比为6∶3∶2,故A错误;未注明气
体所处状况,无法计算4.48 L二氧化碳的物质的量和含有的碳原子数,故B错误;摩尔质量的单位为
g·mol-1,故C错误;a g氯气的物质的量为 mol,含有的氯原子个数为 mol×2N mol-1=b,则阿伏加
A
德罗常数N 的数值可以表示为,故D正确。
A
11.D 含有6.02×1023个碳原子的C H O 的物质的量为 mol,D错误。
15 22 5
12.C 左右两侧气体温度、压强相同,相同条件下,气体体积之比等于物质的量之比,左右两侧
气体体积之比为4∶1,则左右两侧气体物质的量(分子数)之比为4∶1,分子数之比也为4∶1,A错误;
右侧CO的物质的量为0.25 mol,质量为0.25 mol×28 g·mol-1=7 g,B错误;相同条件下,气体密度之
比等于摩尔质量之比,则右侧气体密度是相同条件下氢气密度的=14倍,故C正确;隔板处于容器正中间时,左右两侧气体的物质的量相同,则右侧应再充入0.75 mol CO,D错误。
13.A 同温同压下,气体密度之比等于摩尔质量之比,N、H、O 三种气体的摩尔质量分别为28
2 2 2
g·mol-1、2 g·mol-1、32 g·mol-1,故密度:ρ(O )>ρ(N )>ρ(H ),A正确;根据pV=nRT=RT得pM=RT
2 2 2
=ρRT,当温度和密度相同时,气体压强与摩尔质量成反比,故压强:p(H )>p(N )>p(O ),B错误;由A
2 2 2
可知同温同压下,密度:ρ(O )>ρ(N )>ρ(H ),现质量也相同,由m=ρV可知密度与体积成反比,故体积:
2 2 2
V(H )>V(N )>V(O ),C错误;由A可知同温同压下,密度:ρ(O )>ρ(N )>ρ(H ),现体积也相同,由ρ=可
2 2 2 2 2 2
知密度与质量成正比,故质量:m(O )>m(N )>m(H ),D错误。
2 2 2
14.解析:(1)14.4 g CO和CO 混合气体的物质的量为=0.4 mol,则该混合气体的平均摩尔质量为
2
=36 g·mol-1。(2)设混合气体中 CO的物质的量为x mol,CO 的物质的量为y mol,根据混合气体的质
2
量为14.4 g,有28x+44y=14.4,根据混合气体的物质的量为0.4 mol,有x+y=0.4,解得x=y=0.2;由
于CO和CO 中均含1个碳原子,故0.2 mol CO和0.2 mol CO 的混合气体中共含0.4 mol 即0.4N 个
2 2 A
碳原子。(3)将混合气体依次通过装置,则CO 会被NaOH溶液吸收,剩余CO,被浓硫酸干燥后,收集
2
在气球中。①CO的摩尔质量为28 g·mol-1。②标准状况下,气球中收集到的CO的体积为0.2
mol×22.4 L·mol-1=4.48 L。③气球中收集到的CO所含电子的总物质的量为0.2 mol×14=2.8 mol,电
子总数为2.8N 。
A
答案:(1)36 g·mol-1 (2)0.4N
A
(3)①28 g·mol-1 ②4.48 L ③2.8N
A
15.解析:(1)4 分钟时水槽中 HO 减轻的质量为 300 g-298.2 g=1.8 g,根据反应:
2
2HO=====2H↑+O↑可知,消耗1.8 g即0.1 mol H O得到0.1 mol H 、0.05 mol O 。(2)0.05 mol O 的
2 2 2 2 2 2 2
体积为1.243 L,所以气体摩尔体积为=24.86 L·mol-1。(3)在其他条件不变时,一定物质的量的气体,
温度越高,其体积越大,所以温度越高,气体摩尔体积也越大,A项正确;气体摩尔体积限定气体的物
质的量为1 mol,所以在该实验条件下,O 的气体摩尔体积为24.86 L·mol-1,B项错误;同温同压下,
2
气体的物质的量相同,其体积也相同,所以2 mol CO、CO 混合气体和2 mol O 的体积相同,C项正确;
2 2
该实验条件下,1 mol O 的体积为24.86 L、质量为32 g,所以O 的密度为≈1.287 g·L-1,D项正确。
2 2
答案:(1)0.1 0.05 (2)24.86 L·mol-1 (3)B