文档内容
课时检测(二十二) 功不可没的“含氯消毒剂”
1. NaClO是家用消毒液的有效成分,可通过Cl 与NaOH反应制得。NaClO能与CO 反应生成
2 2
HClO。下列说法正确的是( )
A.新制氯水需存放在带玻璃塞的棕色试剂瓶中
B.可用广泛pH试纸测定新制氯水的pH值
C.NaClO与CO 反应的离子方程式为NaClO+CO +HO===HClO+Na++HCO
2 2 2
D.使用NaClO消毒时,可用盐酸酸化
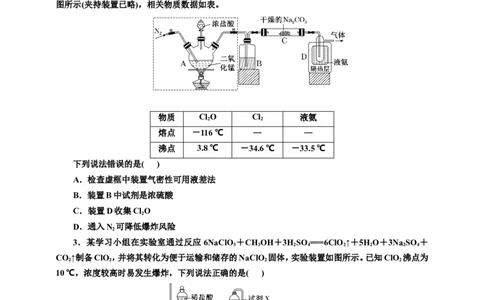
2.(2024·石家庄校联考模拟)一氧化二氯(ClO)是净化饮用水的一种有效的净水剂,浓度过高或加
2
热时易发生分解并爆炸,制备反应为2Cl +2Na CO +HO===2NaHCO +2NaCl+Cl O,反应装置如
2 2 3 2 3 2
图所示(夹持装置已略),相关物质数据如表。
物质 Cl O Cl 液氨
2 2
熔点 -116 ℃ — —
沸点 3.8 ℃ -34.6 ℃ -33.5 ℃
下列说法错误的是( )
A.检查虚框中装置气密性可用液差法
B.装置B中试剂是浓硫酸
C.装置D收集Cl O
2
D.通入N 可降低爆炸风险
2
3.某学习小组在实验室通过反应6NaClO +CH OH+3HSO ===6ClO ↑+5HO+3Na SO +
3 3 2 4 2 2 2 4
CO ↑制备ClO ,并将其转化为便于运输和储存的NaClO 固体,实验装置如图所示。已知ClO 沸点为
2 2 2 2
10 ℃,浓度较高时易发生爆炸,下列说法正确的是( )
A.试剂X是甲醇,试剂Y是硫酸
B.B中开始反应后立即停止通二氧化碳
C.此实验可不用冰水浴
D.C中发生反应的化学方程式为2ClO +2NaOH+HO===2NaClO +2HO+O
2 2 2 2 2 2
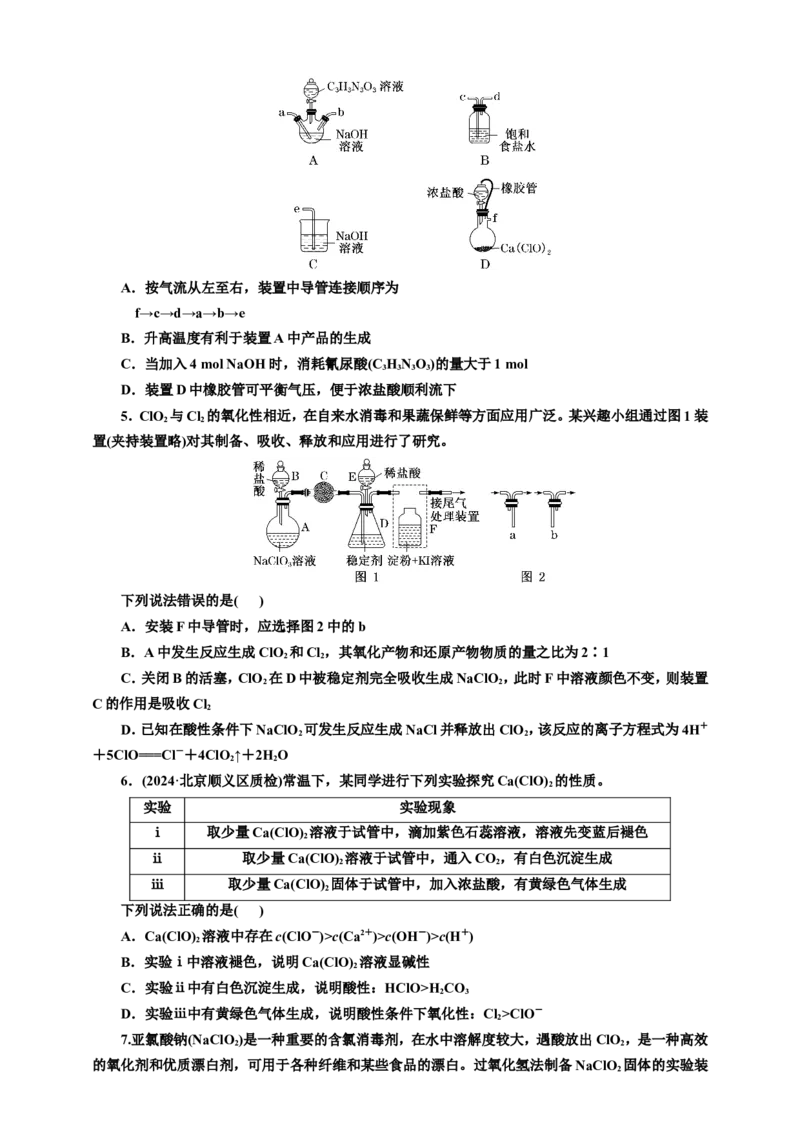
4.反应2NaClO+CHNO===C NOCl Na+NaOH+HO可制备广谱消毒剂CNOCl Na,装
3 3 3 3 3 3 3 2 2 3 3 3 2
置如图所示(夹持装置已略去)。下列说法错误的是( )A.按气流从左至右,装置中导管连接顺序为
f→c→d→a→b→e
B.升高温度有利于装置A中产品的生成
C.当加入4 mol NaOH时,消耗氰尿酸(C HNO)的量大于1 mol
3 3 3 3
D.装置D中橡胶管可平衡气压,便于浓盐酸顺利流下
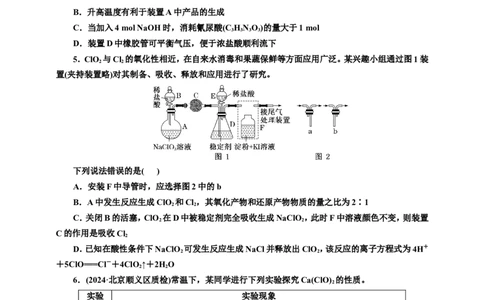
5.ClO 与Cl 的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装
2 2
置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
下列说法错误的是( )
A.安装F中导管时,应选择图2中的b
B.A中发生反应生成ClO 和Cl ,其氧化产物和还原产物物质的量之比为2∶1
2 2
C.关闭B的活塞,ClO 在D中被稳定剂完全吸收生成NaClO ,此时F中溶液颜色不变,则装置
2 2
C的作用是吸收Cl
2
D.已知在酸性条件下NaClO 可发生反应生成NaCl并释放出ClO ,该反应的离子方程式为4H+
2 2
+5ClO===Cl-+4ClO ↑+2HO
2 2
6.(2024·北京顺义区质检)常温下,某同学进行下列实验探究Ca(ClO) 的性质。
2
实验 实验现象
ⅰ 取少量Ca(ClO) 溶液于试管中,滴加紫色石蕊溶液,溶液先变蓝后褪色
2
ⅱ 取少量Ca(ClO) 溶液于试管中,通入CO ,有白色沉淀生成
2 2
ⅲ 取少量Ca(ClO) 固体于试管中,加入浓盐酸,有黄绿色气体生成
2
下列说法正确的是( )
A.Ca(ClO) 溶液中存在c(ClO-)>c(Ca2+)>c(OH-)>c(H+)
2
B.实验ⅰ中溶液褪色,说明Ca(ClO) 溶液显碱性
2
C.实验ⅱ中有白色沉淀生成,说明酸性:HClO>H CO
2 3
D.实验ⅲ中有黄绿色气体生成,说明酸性条件下氧化性:Cl >ClO-
2
7.亚氯酸钠(NaClO )是一种重要的含氯消毒剂,在水中溶解度较大,遇酸放出ClO ,是一种高效
2 2
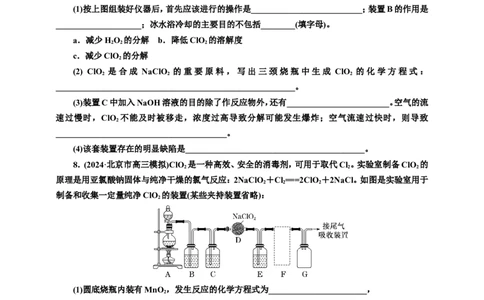
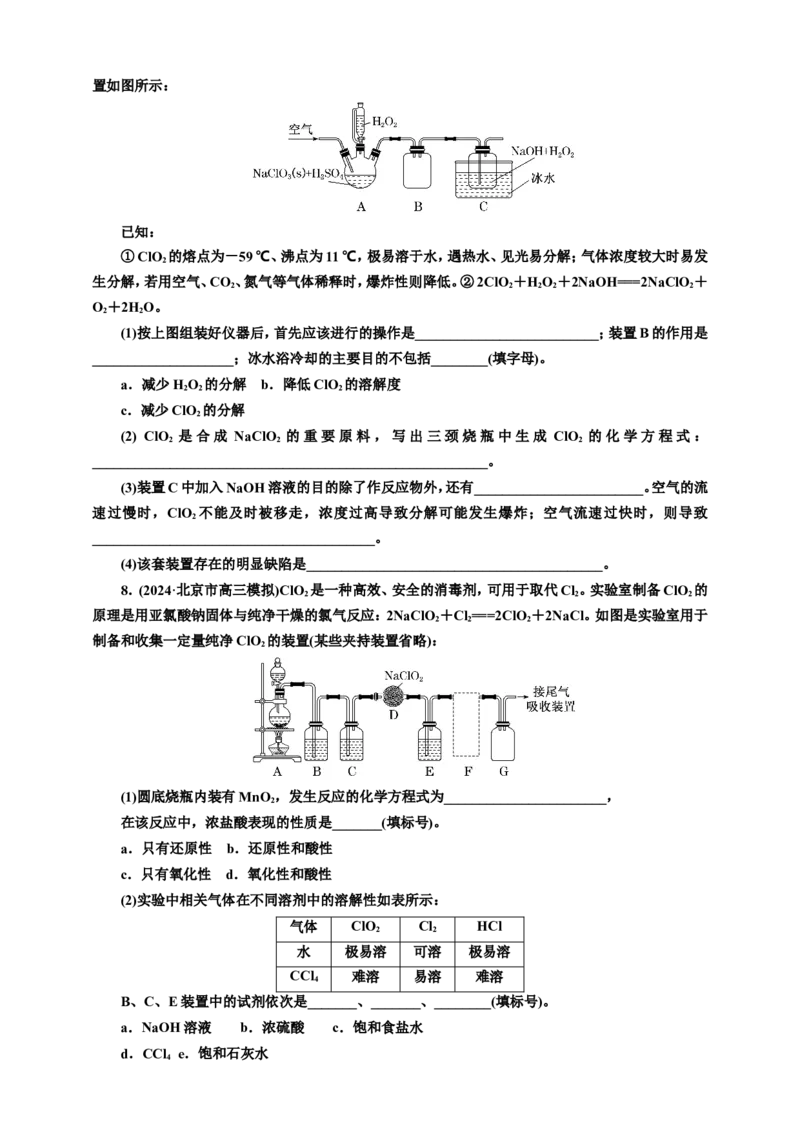
的氧化剂和优质漂白剂,可用于各种纤维和某些食品的漂白。过氧化氢法制备NaClO 固体的实验装
2置如图所示:
已知:
①ClO 的熔点为-59 ℃、沸点为11 ℃,极易溶于水,遇热水、见光易分解;气体浓度较大时易发
2
生分解,若用空气、CO 、氮气等气体稀释时,爆炸性则降低。②2ClO +HO+2NaOH===2NaClO +
2 2 2 2 2
O+2HO。
2 2
(1)按上图组装好仪器后,首先应该进行的操作是__________________________;装置B的作用是
____________________;冰水浴冷却的主要目的不包括________(填字母)。
a.减少HO 的分解 b.降低ClO 的溶解度
2 2 2
c.减少ClO 的分解
2
(2) ClO 是合成 NaClO 的重要原料,写出三颈烧瓶中生成 ClO 的化学方程式:
2 2 2
________________________________________________________。
(3)装置C中加入NaOH溶液的目的除了作反应物外,还有________________________。空气的流
速过慢时,ClO 不能及时被移走,浓度过高导致分解可能发生爆炸;空气流速过快时,则导致
2
________________________________________。
(4)该套装置存在的明显缺陷是__________________________________________。
8.(2024·北京市高三模拟)ClO 是一种高效、安全的消毒剂,可用于取代Cl 。实验室制备ClO 的
2 2 2
原理是用亚氯酸钠固体与纯净干燥的氯气反应:2NaClO +Cl ===2ClO +2NaCl。如图是实验室用于
2 2 2
制备和收集一定量纯净ClO 的装置(某些夹持装置省略):
2
(1)圆底烧瓶内装有MnO ,发生反应的化学方程式为_______________________,
2
在该反应中,浓盐酸表现的性质是_______(填标号)。
a.只有还原性 b.还原性和酸性
c.只有氧化性 d.氧化性和酸性
(2)实验中相关气体在不同溶剂中的溶解性如表所示:
气体 ClO Cl HCl
2 2
水 极易溶 可溶 极易溶
CCl 难溶 易溶 难溶
4
B、C、E装置中的试剂依次是_______、_______、________(填标号)。
a.NaOH溶液 b.浓硫酸 c.饱和食盐水
d.CCl e.饱和石灰水
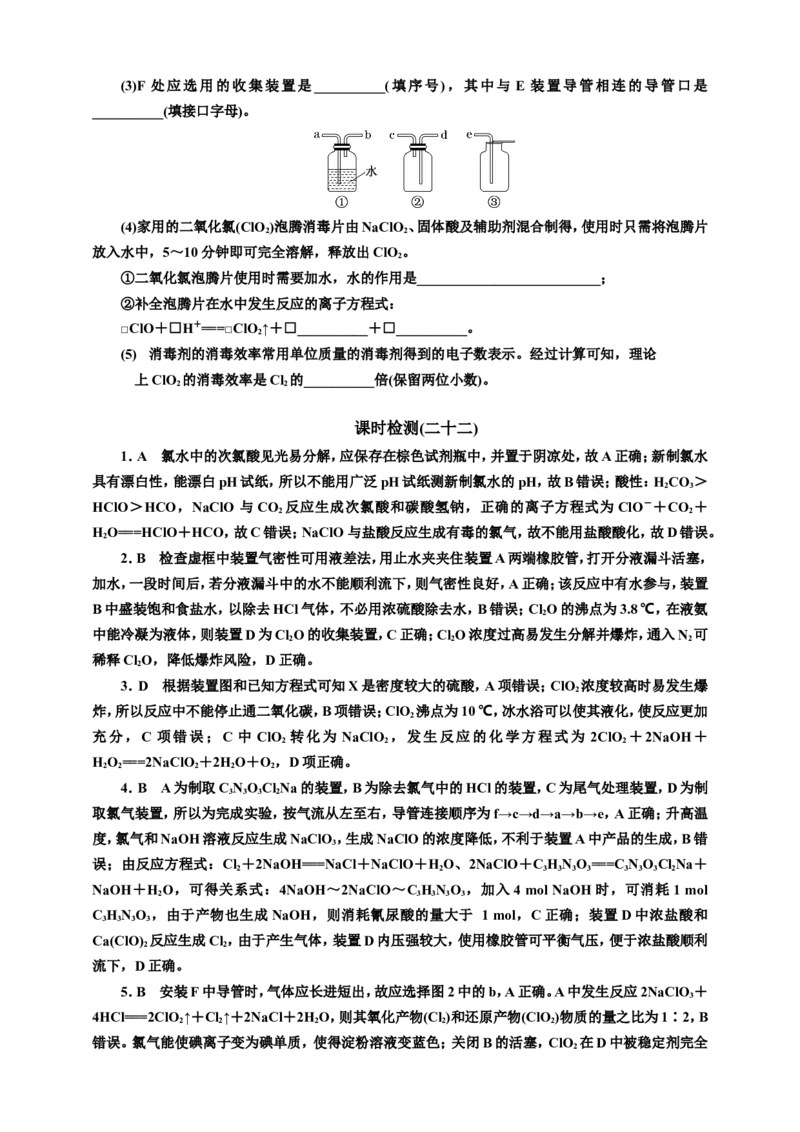
4(3)F 处应选用的收集装置是__________(填序号),其中与 E 装置导管相连的导管口是
__________(填接口字母)。
(4)家用的二氧化氯(ClO )泡腾消毒片由NaClO 、固体酸及辅助剂混合制得,使用时只需将泡腾片
2 2
放入水中,5~10分钟即可完全溶解,释放出ClO 。
2
①二氧化氯泡腾片使用时需要加水,水的作用是__________________________;
②补全泡腾片在水中发生反应的离子方程式:
□ClO+□H+===□ClO ↑+□__________+□__________。
2
(5) 消毒剂的消毒效率常用单位质量的消毒剂得到的电子数表示。经过计算可知,理论
上ClO 的消毒效率是Cl 的__________倍(保留两位小数)。
2 2
课时检测(二十二)
1.A 氯水中的次氯酸见光易分解,应保存在棕色试剂瓶中,并置于阴凉处,故A正确;新制氯水
具有漂白性,能漂白pH试纸,所以不能用广泛pH试纸测新制氯水的pH,故B错误;酸性:HCO >
2 3
HClO>HCO,NaClO 与CO 反应生成次氯酸和碳酸氢钠,正确的离子方程式为ClO-+CO +
2 2
HO===HClO+HCO,故C错误;NaClO 与盐酸反应生成有毒的氯气,故不能用盐酸酸化,故D错误。
2
2.B 检查虚框中装置气密性可用液差法,用止水夹夹住装置A两端橡胶管,打开分液漏斗活塞,
加水,一段时间后,若分液漏斗中的水不能顺利流下,则气密性良好,A正确;该反应中有水参与,装置
B中盛装饱和食盐水,以除去HCl气体,不必用浓硫酸除去水,B错误;Cl O的沸点为3.8 ℃,在液氨
2
中能冷凝为液体,则装置D为Cl O的收集装置,C正确;Cl O浓度过高易发生分解并爆炸,通入N 可
2 2 2
稀释Cl O,降低爆炸风险,D正确。
2
3.D 根据装置图和已知方程式可知X是密度较大的硫酸,A项错误;ClO 浓度较高时易发生爆
2
炸,所以反应中不能停止通二氧化碳,B项错误;ClO 沸点为10 ℃,冰水浴可以使其液化,使反应更加
2
充分,C 项错误;C 中 ClO 转化为 NaClO ,发生反应的化学方程式为 2ClO +2NaOH+
2 2 2
HO===2NaClO +2HO+O,D项正确。
2 2 2 2 2
4.B A为制取CNOCl Na的装置,B为除去氯气中的HCl的装置,C为尾气处理装置,D为制
3 3 3 2
取氯气装置,所以为完成实验,按气流从左至右,导管连接顺序为f→c→d→a→b→e,A正确;升高温
度,氯气和NaOH溶液反应生成NaClO ,生成NaClO的浓度降低,不利于装置A中产品的生成,B错
3
误;由反应方程式:Cl +2NaOH===NaCl+NaClO+HO、2NaClO+CHNO===C NOCl Na+
2 2 3 3 3 3 3 3 3 2
NaOH+HO,可得关系式:4NaOH~2NaClO~CHNO ,加入4 mol NaOH时,可消耗1 mol
2 3 3 3 3
CHNO ,由于产物也生成NaOH,则消耗氰尿酸的量大于 1 mol,C正确;装置D中浓盐酸和
3 3 3 3
Ca(ClO) 反应生成Cl ,由于产生气体,装置D内压强较大,使用橡胶管可平衡气压,便于浓盐酸顺利
2 2
流下,D正确。
5.B 安装F中导管时,气体应长进短出,故应选择图2中的b,A正确。A中发生反应2NaClO +
3
4HCl===2ClO ↑+Cl ↑+2NaCl+2HO,则其氧化产物(Cl)和还原产物(ClO )物质的量之比为1∶2,B
2 2 2 2 2
错误。氯气能使碘离子变为碘单质,使得淀粉溶液变蓝色;关闭B的活塞,ClO 在D中被稳定剂完全
2吸收生成NaClO ,此时F中溶液颜色不变,则装置C的作用是吸收Cl ,C正确。已知在酸性条件下
2 2
NaClO 可发生反应生成NaCl并释放出ClO ,根据元素守恒可知还会生成水,则该反应的离子方程式
2 2
为4H++5ClO===Cl-+4ClO ↑+2HO,D正确。
2 2
6.A Ca(ClO) 是可溶性强电解质,在溶液中发生电离Ca(ClO) ===Ca2++2ClO-,ClO-会发生
2 2
水解ClO-+HO HClO+OH-,则溶液显碱性,故c(OH-)>c(H+),水解的程度是微弱的,则
2
Ca(ClO) 溶液中存⥫在⥬c(ClO-)>c(Ca2+)>c(OH-)>c(H+),A正确。Ca(ClO) 溶液中存在ClO-+HO
2 2 2
HClO+OH-,溶液显碱性,向其中滴加紫色石蕊溶液,溶液变为蓝色,由于HClO具有强氧化性,会⥫⥬将
蓝色物质氧化成无色物质,故不能根据溶液褪色说明Ca(ClO) 溶液显碱性,B错误。取少量Ca(ClO)
2 2
溶液于试管中,通入CO ,生成白色沉淀,发生反应Ca2++2ClO-+CO +HO===CaCO ↓+2HClO,
2 2 2 3
说明酸性:HCO >HClO,C错误。实验ⅲ中有黄绿色气体生成,说明发生歧化反应Cl-+ClO-+2H+
2 3
===Cl↑+HO,则氧化性:ClO->Cl,D错误。
2 2 2
7.解析:三颈烧瓶中NaClO 、HO 在酸性条件下发生氧化还原反应生成ClO ,B是安全瓶,防倒
3 2 2 2
吸,C中发生反应2ClO +HO+2NaOH===2NaClO +O+2HO,生成NaClO 。(1)气体制备装置中,
2 2 2 2 2 2 2
为防止气体泄漏,组装好仪器后,首先检验装置气密性;ClO 极易溶于水,所以易发生倒吸,装置B的
2
作用是防止倒吸;温度较低,过氧化氢分解速率减慢,所以冰水浴可以减少HO 的分解,故不选a;实
2 2
验的目的是ClO 、HO、NaOH溶液反应制备NaClO ,所以不能降低ClO 的溶解度,故选b;ClO 遇
2 2 2 2 2 2
热水易分解,所以冰水浴可以减少ClO 的分解,故不选c。(2)三颈烧瓶中NaClO 、HO 在酸性条件下
2 3 2 2
发生氧化还原反应生成ClO 、氧气、硫酸钠,反应的化学方程式为2NaClO +HO+HSO ===2ClO ↑
2 3 2 2 2 4 2
+O↑+Na SO +2HO。(3)NaClO 遇酸放出ClO ,装置C中加入NaOH溶液的目的除了作反应物外,
2 2 4 2 2 2
还避免NaClO 遇酸放出ClO ;空气流速过快时,则导致ClO 不能被充分吸收,NaClO 的产率下降。
2 2 2 2
(4)该套装置存在的明显缺陷是没有处理尾气,污染空气。
答案:(1)检查装置的气密性 防止倒吸(或稀释ClO 气体) b
2
(2)2NaClO +HO +HSO ===2ClO ↑+O↑+Na SO +2HO (3)避免NaClO 遇酸放出ClO
3 2 2 2 4 2 2 2 4 2 2 2
ClO 不能被充分吸收,NaClO 的产率下降 (4)没有处理尾气
2 2
8.解析:(1)装置A为制取Cl 的发生装置,对应反应的化学方程式为MnO +4HCl(浓)=====
2 2
MnCl +Cl ↑+2HO;该反应中,部分盐酸中氯元素化合价升高,作还原剂,部分氯元素化合价没变,
2 2 2
体现酸性。(2)装置B、C、E所装试剂依次为饱和食盐水、浓硫酸、CCl 。(3)F为收集ClO 装置,由于
4 2
ClO 极易溶于水,故不能用排水法,因ClO 气体的密度比空气密度大,故应选用的装置是②,其中与
2 2
E装置导管相连的导管口是d。(4)①二氧化氯泡腾片使用时加水的作用是作为溶剂,使得固体物质溶
解后充分反应;②反应中,氯元素化合价由+3价升高为+4价,由于+3价处于氯元素中间价态,推测
该反应为氯元素歧化反应,即还有部分氯元素化合价降低转化为Cl-,结合元素守恒推测还有HO生
2
成,根据得失电子守恒、电荷守恒、元素守恒配平得完整方程式为 5ClO+4H+===4ClO ↑+Cl-+
2
2HO。(5)根据转移电子关系式:ClO ~Cl-~5e-,得每克ClO 得到电子数=,由Cl ~2Cl-~2e-,得
2 2 2 2
每克Cl 得到电子数=,则ClO 消毒效率是Cl 的倍数为≈2.63。
2 2 2
答案:(1)MnO +4HCl(浓)=====MnCl +Cl ↑+2HO b (2)c b d (3)② d (4)①作为溶
2 2 2 2
剂,使得固体物质溶解后充分反应 ②5 4 4 1 Cl- 2 HO (5)2.63
2