文档内容
课时检测(四十一) 化学反应中的热效应的基本知能评价
1.下列说法正确的是( )
A.焓的大小受体系的温度、压强等因素的影响
B.化学反应的反应热等于反应前后焓的变化
C.浓硫酸溶于水是放热反应
D.煤的液化有利于实现碳达峰、碳中和
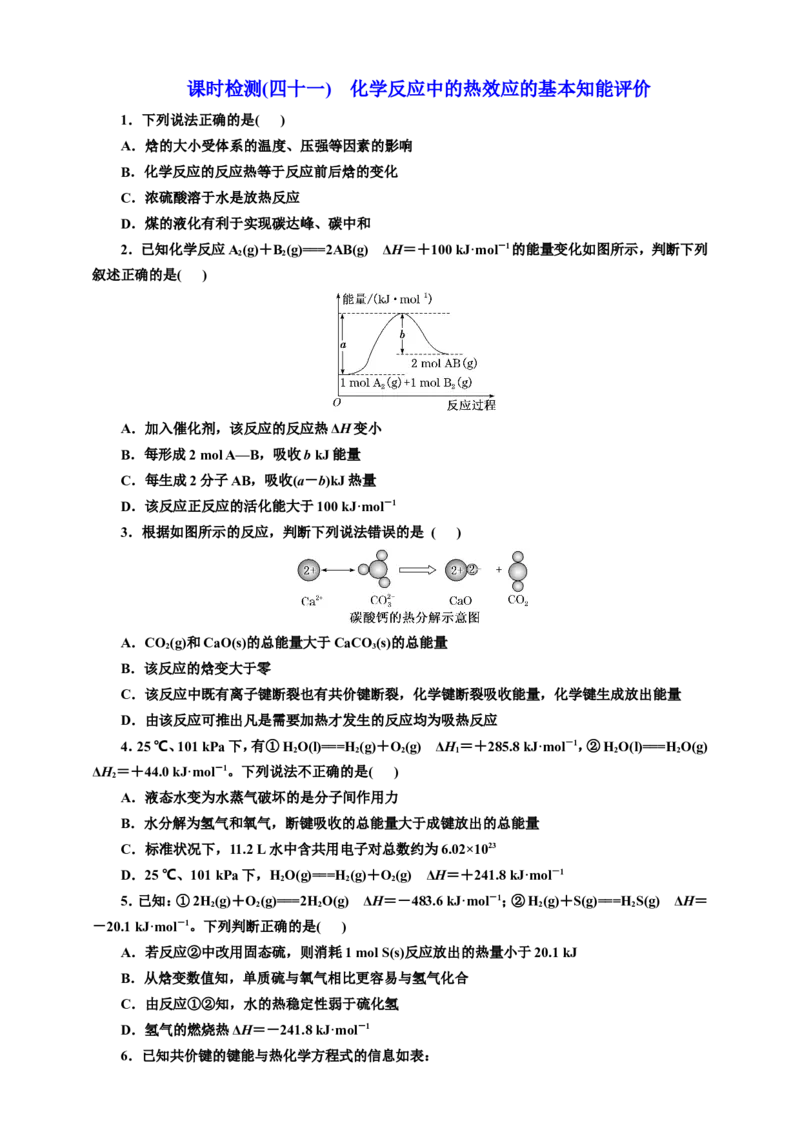
2.已知化学反应A(g)+B (g)===2AB(g) ΔH=+100 kJ·mol-1的能量变化如图所示,判断下列
2 2
叙述正确的是( )
A.加入催化剂,该反应的反应热ΔH变小
B.每形成2 mol A—B,吸收b kJ能量
C.每生成2分子AB,吸收(a-b)kJ热量
D.该反应正反应的活化能大于100 kJ·mol-1
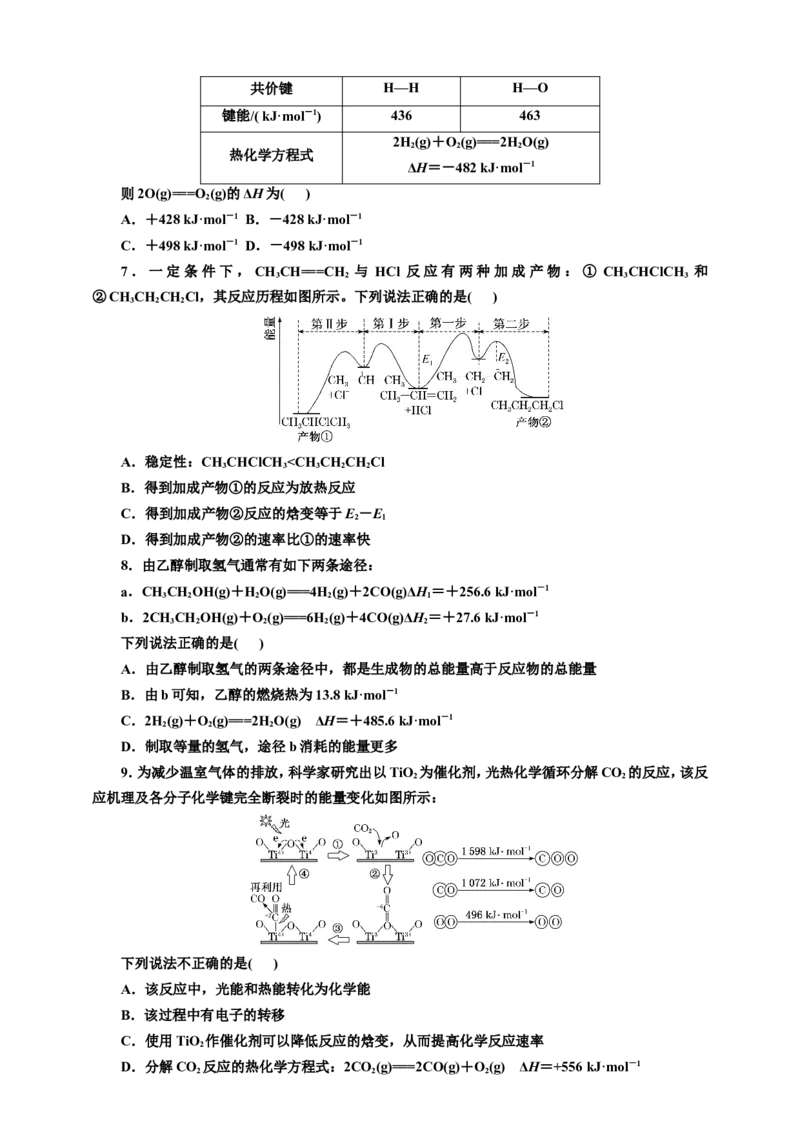
3.根据如图所示的反应,判断下列说法错误的是 ( )
A.CO (g)和CaO(s)的总能量大于CaCO (s)的总能量
2 3
B.该反应的焓变大于零
C.该反应中既有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量
D.由该反应可推出凡是需要加热才发生的反应均为吸热反应
4.25 ℃、101 kPa下,有①HO(l)===H (g)+O(g) ΔH=+285.8 kJ·mol-1,②HO(l)===H O(g)
2 2 2 1 2 2
ΔH=+44.0 kJ·mol-1。下列说法不正确的是( )
2
A.液态水变为水蒸气破坏的是分子间作用力
B.水分解为氢气和氧气,断键吸收的总能量大于成键放出的总能量
C.标准状况下,11.2 L水中含共用电子对总数约为6.02×1023
D.25 ℃、101 kPa下,HO(g)===H (g)+O(g) ΔH=+241.8 kJ·mol-1
2 2 2
5.已知:①2H(g)+O(g)===2H O(g) ΔH=-483.6 kJ·mol-1;②H(g)+S(g)===H S(g) ΔH=
2 2 2 2 2
-20.1 kJ·mol-1。下列判断正确的是( )
A.若反应②中改用固态硫,则消耗1 mol S(s)反应放出的热量小于20.1 kJ
B.从焓变数值知,单质硫与氧气相比更容易与氢气化合
C.由反应①②知,水的热稳定性弱于硫化氢
D.氢气的燃烧热ΔH=-241.8 kJ·mol-1
6.已知共价键的键能与热化学方程式的信息如表:共价键 H—H H—O
键能/( kJ·mol-1) 436 463
2H(g)+O(g)===2H O(g)
2 2 2
热化学方程式
ΔH=-482 kJ·mol-1
则2O(g)===O (g)的ΔH为( )
2
A.+428 kJ·mol-1 B.-428 kJ·mol-1
C.+498 kJ·mol-1 D.-498 kJ·mol-1
7.一定条件下,CH CH===CH 与 HCl 反应有两种加成产物:① CH CHClCH 和
3 2 3 3
②CH CH CH Cl,其反应历程如图所示。下列说法正确的是( )
3 2 2
A.稳定性:CH CHClCH 加成产物①,所以得到加成产物①
的速率比②的速率快,故D错误。
8.A 途径a、途径b均是吸热反应,故A正确;乙醇的燃烧热应该是1 mol 乙醇燃烧生成二氧化
碳和液态水时放出的热量,故B错误;根据盖斯定律,b-2a得2H(g)+O(g)===2H O(g) ΔH=-
2 2 2
485.6 kJ·mol-1,故C错误;根据热化学方程式知,制取等量的氢气,途径a消耗的能量更多,故D错误。
9.C 由题图可知,该反应中,在太阳能的作用下,二氧化碳发生了分解反应,光能和热能转化为
化学能,A正确;该过程中二氧化碳发生了分解反应:2CO ===2CO+O,属于氧化还原反应,故有电
2 2
子的转移,B正确;催化剂不能改变反应的焓变,但是可以降低反应的活化能,故使用TiO 作催化剂可
2
以提高化学反应速率,C不正确;化学反应的焓变等于反应物的键能总和与生成物的键能总和之差,
ΔH= 2×1 598 kJ·mol-1-2×1 072 kJ·mol-1-496 kJ·mol-1=+556 kJ·mol-1,则分解CO 反应的热
2
化学方程式为2CO (g)===2CO(g)+O(g) ΔH=+556 kJ·mol-1,D正确。
2 2
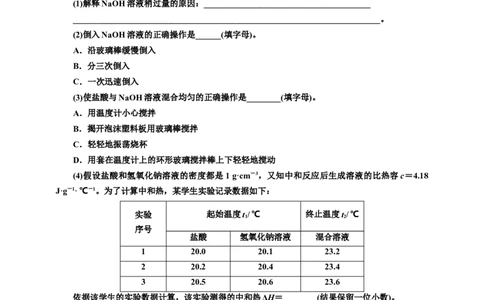
10.解析:(1)在中和热的测定实验中,为了确保一种反应物被完全中和,常常使加入的另一种反应
物稍稍过量。(2)为了减少热量损失,NaOH溶液应该一次迅速倒入。(4)第1次实验盐酸和NaOH溶液
起始平均温度为20.05 ℃,反应后温度为23.2 ℃,反应前后温度差为3.15 ℃;第2次实验盐酸和
NaOH溶液起始平均温度为20.3 ℃,反应后温度为23.4 ℃,反应前后温度差为3.1 ℃;第3次实验盐
酸和NaOH溶液起始平均温度为20.55 ℃,反应后温度为23.6 ℃,反应前后温度差为3.05 ℃;50 mL
0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1氢氧化钠溶液的质量和为100 mL×1 g·cm-3=100 g,反应生
成0.025 mol水放出的热量为4.18 J·g-1·℃-1×100 g×=1.295 8 kJ,所以生成1 mol水放出的热量为
1.295 8 kJ×≈51.8 kJ,该实验测得的中和热ΔH=-51.8 kJ·mol-1。
答案:(1)确保盐酸被完全中和 (2)C (3)D
(4)-51.8 kJ·mol-1
11.解析:(1)反应中放出热量越多,ΔH越小,与1 L 1 mol·L-1NaOH溶液反应时,与稀硝酸相比,
浓硫酸稀释时放出大量热,醋酸电离时吸收热量,故ΔH>ΔH>ΔH。(2)根据盖斯定律,①+②+③得
3 2 1
碳与水制氢气总反应的热化学方程式为C(s)+HO(g)H (g)+CO(g) ΔH=ΔH +ΔH +ΔH =+
2 2 1 2 3
134.5 kJ·mol-1。(3)由题图可知,CO与H 合成CH OH的反应热ΔH=-(510 kJ·mol-1-419 kJ·mol-
2 3
1)=-91 kJ·mol-1,设甲醇中C—H键的键能为x kJ·mol-1,则ΔH=1 084 kJ·mol-1+2×436 kJ·mol-1
-3×x kJ·mol-1-465 kJ·mol-1-343 kJ·mol-1=-91 kJ·mol-1,解得x=413。(4)由题图可知,该反应
的 ΔH=(945+498)kJ·mol-1-2×630 kJ·mol-1=+183 kJ·mol-1,故其热化学方程式为 N(g)+
2
O(g)===2NO(g) ΔH=+183 kJ·mol-1。
2
答案:(1)ΔH>ΔH>ΔH (2)C(s)+HO(g)H (g)+CO(g) ΔH=+134.5 kJ·mol-1 (3)413
3 2 1 2 2
(4)N (g)+O(g)===2NO(g) ΔH=+183 kJ·mol-1
2 2