文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练01 14道选择题+主观流程题
完卷时间:40分钟
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C C D C B B C C D B C D D C
一、选择题(只有1个正确选项)
1.2024年2月第十四届全国冬季运动会在内蒙古召开,见证了中国冰雪运动的“热辣滚
烫”。下列说法不正确的是
A.场馆的照明、运行均由光伏发电和风力发电提供,有利于实现碳达峰
B.速滑竞赛服采用的聚氨酯材料是一种有机高分子材料
C.冬运会场馆建设大量使用到了太阳能,太阳能电池板的主要材料是二氧化硅
D.冬运会采用了先进的二氧化碳制冰技术,比传统制冷剂氟利昂更加环保
【答案】C
【解析】A.场馆的照明、运行均由光伏发电和风力发电提供,以减少化石燃料的燃烧,减
少CO 的排放,故有利于实现碳达峰,A正确;B.速滑竞赛服采用的聚氨酯材料是一种合
2
成纤维,属于有机高分子材料,B正确;C.太阳能电池板的主要材料是晶体硅,C错误;
D.氟利昂会破坏臭氧层,导致臭氧层空洞的环境问题,采用二氧化碳制冰技术,比传统制
冷剂氟利昂更加环保,D正确;故答案为:C。
2.下列化学用语表示正确的是
A.基态铜原子价电子的轨道表示式:
B.顺式聚2-甲基-1,3-丁二烯的结构简式:
C.NaH的形成过程:
D.邻羟基苯甲醛的分子内氢键:
【答案】C
【解析】A.基态铜原子价电子排布式为 ,轨道表示式为:故A错误;B.顺式聚2-甲基-1,3-丁二烯的结构简式为: ,故B错误;
C.NaH是离子化合物,钠原子与氢原子通过得失电子形成的,所以形成过程为:
,故C正确;D.邻羟基苯甲醛中的-OH中的H原子与醛基中的O原
子之间形成分子内氢键,示意图为 ,故D错误;故选C。
3.设N 为阿伏加德罗常数的值。下列叙述中正确的是
A
A.28gCH 的烃分子中含有C-C σ键的数目一定为1.6N
5 10 A
B.在标准状况下,22.4L由SO 和SO 组成的混合物中含有硫原子的数目为N
2 3 A
C.有2.00L0.5mol·L−1的稀硫酸和足量金属钠反应,消耗钠原子的数目为2N
A
D.在2CuH+2HCl==Cu+CuCl+2H↑反应中,每生成4.48L(标准状况)H,反应转移的电
2 2 2
子数目为0.3N
A
【答案】D
【解析】A.CH 可能为环烷烃,可能为烯烃,若为环烷烃时,28gCH 的烃分子中含有C-
5 10 5 10
C σ键的数目为2.0N,A错误;B.标况下,SO 不是气体,无法计算,B错误;C.钠除了
A 3
能与酸反应以外,还能与水反应,由于钠是足量的,无法计算消耗的钠的原子数,C错误;
D.2CuH+2HCl==Cu+CuCl+2H↑中,铜的化合价由+1降到0和升高到+2,H的化合价
2 2
由-1升高到0,故每生成4.48L(标准状况)H,反应转移的电子数目为0.3N,D正确;故
2 A
选D。
4.下列反应的离子方程式正确的是
A.电解饱和的 溶液:
B.漂粉精的制备:
C.乙醛的银镜反应:
D.向胆矾溶液中加入过量的浓氨水:
【答案】C
【解析】A.原离子方程式电荷不守恒,电解饱和的AlCl 溶液正确的离子方程式为2Al3+
3
+6Cl-+6HO 2Al(OH)↓+3H↑ +3Cl↑,故A错误;B.漂粉精的制备是将氯气通入石灰
2 3 2 2
乳,由于不是溶液中的反应,所以不能拆,正确的离子方程式为:
Ca(OH)+2Cl=CaCl+Ca(ClO)+2HO,B错误;C.乙醛发生银镜反应,生成乙酸铵、氨气、
2 2 2 2 2水和银,离子方程式为CHCHO+2[Ag(NH)]++2OH− CHCOO−+ +2Ag↓+3NH+HO,C
3 3 2 3 3 2
正确;D.氨水过量,氢氧化铜溶解,正确的离子方程式为Cu2++4NH 3⋅H
2
O=[Cu(NH
3
)
4
]2+
+4HO,D错误;本题选C。
2
5.实验室中利用洁净的铜片和浓硫酸按图示流程实验,经检测所得固体中含有 和白
色物质W,下列说法错误的是
A.该实验能体现浓硫酸的吸水性和强氧化性
B.当Cu完全反应时共转移电子0.050mol
C.溶解步骤中生成固体Y的质量为0.192g
D.将W溶液蒸发结晶并灼烧可再次得到固体W
【答案】B
【分析】由图知,铜与足量浓硫酸反应生成CuS和白色物质W,无气体生成,生成CuS时
2 2
铜元素从0价升高到+1价、硫元素从+6价降低到-2价,则按得失电子数守恒、必定存在其
他产物(所含元素化合价升高)、按元素质量守恒只能为CuSO,则白色物质W为CuSO,配
4 4
平得到该反应方程式为: ,CuS和白色物质CuSO
2 4
加稀硫酸和稀硝酸时溶解,存在反应: ,
Y为S单质,则NO为还原产物、Y为氧化产物;n(Cu)= =0.03mol,Cu与浓硫酸发
生反应生成CuSO、CuS,设CuS的物质的量为x,则CuSO 的物质的量为(0.03-2x),依据
4 2 2 4
得失电子守恒的原则可得:2x+2(0.03-2x)=8x,从而求出x=0.006mol,0.03-
2x=0.018mol,即CuS为0.006mol,CuSO 为0.018mol,据此回答。
2 4
【解析】A.由 可知,硫元素从+6价降低到-2价
时表现强氧化性,所得固体中含有白色物质W为硫酸铜,表现出吸水性,故A正确;B.微
热5min待Cu反应结束后,按Cu计算,转移电子的物质的量为
0.006mol×2+0.018mol×2=0.048mol,故B错误;C.由分析知,5n(Cu) n(CuS) n(S),
2
n(S)= =0.006mol,m(S)=32g/mol 0.006mol=0.192g,故C正确;D.W为CuSO,
4
将硫酸铜溶液蒸发结晶并灼烧可再次得到固体CuSO,故D正确;答案选B。
4
6.化学与生活和生产密切相关,下列叙述正确的是
A.氢氟酸可用于溶蚀玻璃是由于其具有酸性
B.苯酚可用作消毒防腐药是由于其可使蛋白质变性
C.SiO 可用于生产光导纤维是由于其具有强导电性
2
D.NaO 可用作潜水艇中的供氧剂是由于其分解产生O
2 2 2【答案】B
【解析】A.氢氟酸与二氧化硅反应生成四氟化硅和水,可以腐蚀玻璃,是氢氟酸的一个特
性反应,与其酸性无关,故A错误;B.苯酚能够使蛋白质变性,具有杀菌消毒效力,可用
作消毒防腐药,故B正确;C.SiO 可用于生产光导纤维是由于其具有强导光性,故C错误;
2
D.过氧化钠与水、二氧化碳反应生成氧气,可用作潜水艇中的供氧剂,故D错误。答案选
B。
7.一定条件下,1-苯基丙炔 与HCl发生催化加成,反应如下:
反应Ⅰ: 产物A: ;
反应Ⅱ: 产物B: ;
反应Ⅲ: ;
T℃,向密闭容器中通入2molPh-C≡C-CH(g)和3molHCl(g),平衡时测得Ph-C≡C-CH
3 3
(g)的转化率为 ,反应Ⅲ的平衡常数 ,反应过程中有机物的物质的量分数随时
间变化如图。下列说法错误的是
A.活化能:
B.
C.T℃反应的平衡常数
D.若保持温度和压强不变,再向容器中通N,反应I的化学平衡将逆向移动
2
【答案】C【解析】A.短时间里反应I得到的产物比反应Ⅱ得到的产物多,说明反应I的速率比反应
Ⅱ的速率快,速率越快,其活化能越小,则反应活化能: ,A正确;B.反应Ⅱ=反
应Ⅰ+反应Ⅲ,反应Ⅰ、Ⅲ均为放热反应,反应Ⅱ也为放热反应,且反应Ⅱ放热更多,则
,故 ,B正确;C.设生成产物Axmol,生成产物Bymol,反应Ⅲ的平衡
常数K=6,可得 ,平衡时测得 的转化率为 ,可得x+y=2 ,解得
x3
x= ,反应过程中 和氯化氢1∶1反应,则氯化氢反应2 mol,平衡时
余下(3-2 )mol, 余下2-2 mol,平衡时产物A为 mol,T℃反应Ⅰ的
平衡常数 ,C错误;D.若保持温度和压强不变,再向容器中通N,反
2
应Ⅰ的分压减小,化学平衡将逆向移动,D正确;故选C。
8.在无水环境中,醛或酮可在催化剂的作用下与醇发生反应,其机理如图所示。下列说法
错误的是
A.总反应的化学方程式(不考虑催化剂)为 +2ROH +HO
2
B.甲醛和聚乙烯醇( )发生上述反应时,产物中可能含有六元环结构
C.加入干燥剂或增加 的浓度,可提高醛或酮的平衡转化率
D.在有机合成中,将醛转化为缩醛可保护醛基,缩醛再与水反应可恢复醛基
【答案】C
【解析】A.根据以上反应机理可知,总反应的化学方程式为 +2ROH
+HO,A正确;B.甲醛和聚乙烯醇( )发生上述反应时,聚乙烯醇链节含多个
2
醇羟基,产物中可含有六元环结构,B正确;C.加入干燥剂除去生成物水可提高醛或酮的
平衡转化率,H+是催化剂,增加H+的浓度,不能提高醛或酮的平衡转化率,C错误;D.根
据上述反应机理,在有机合成中,将醛转化为缩醛可保护醛基不被氧化,缩醛再与水反应
可恢复醛基,D正确;故选:C。
9.前四周期元素W、X、Y、Z的原子序数依次增大,且都不在同一周期。X的价电子排布式为nsxnpx+1,Y的最高能级的单电子数是W的3倍,Z与W中的单电子数和最外层电子数均
相同,但两者族序数不同。下列说法不正确的是
A.Y原子核外电子有9种空间运动状态
B.X元素的第一电离能高于其相邻元素
C.X的简单氢化物比Y的简单氢化物键角大
D.Z元素在周期表中的位置可能为第四周期第VIB族
【答案】D
【分析】前四周期元素W、X、Y、Z的原子序数依次增大,且都不在同一周期。则W、X、
Y、Z四种元素分别在第一、第二、第三、第四周期,W为H元素。X的价电子排布式为,
nsxnpx+1,s能级的原子轨道上最多填充2个电子,可知x=2,则X的价层电子排布为
2s22p3,则X为N元素。基态Y的最高能级的单电子数是W的3倍,则Y为第三周期,且有
3个单电子,Y为P元素。Z与W中的单电子数和最外层电子数均相同,但两者族序数不同,
所以Z有1个单电子,最外层有1个电子,且不属于第ⅠA族,则Z为Cu。所以W、X、Y、
Z分别为H元素、N元素、P元素、Cu元素。
【解析】A.P核外电子排布式为1s22s22p63s23p3,轨道表示式为 ,
每个原子轨道上电子具有相同的空间运动状态,P原子的电子填充了9个不同的原子轨道,
因此其核外电子有9种空间运动状态,正确,A不符合题意;B.由于N元素2p轨道处于半
充满状态,能量较低较稳定,N元素的第一电离能高于其相邻C元素、O元素,正确,B不
符合题意;C.X、Y的简单氢化物分别是NH、PH,具有相同的空间构型,但是N的电负性
3 3
大,成键电子对排斥作用大,因此NH 键角比PH 的大,正确,C不符合题意;D.Cu在元
3 3
素周期表中的位置为第四周期第IB族,错误,D符合题意;答案选D。
10.离子化合物 和 与水的反应分别为① ;②
,下列说法不正确的是
A. 、 中均含有非极性共价键
B. 、 中阴、阳离子个数比均为1:1
C.①、②两个反应中水均不作氧化剂或还原剂
D.相同物质的量的 和 与足量的水反应,所得气体的物质的量
【答案】B
【解析】A.过氧化钠和碳化钙都是含有离子键和非极性共价键的离子化合物,故A正确;
B.过氧化钠中钠离子和过氧根离子的个数比为2:1,故B错误;C.由方程式可知,过氧
化钠与水的反应是由元素化合价发生化合价变化的氧化还原反应,碳化钙与水反应是没有
元素化合价发生化合价变化的非氧化还原反应,反应中水均不作氧化剂或还原剂,故C正
确;D.由方程式可知,1mol过氧化钠与水反应生成 mol氧气,1mol碳化钙与水反应生
成 mol乙炔,过氧化钠与水反应生成氧气的物质的量小于碳化钙与水反应生成乙炔的物
质的量,故D正确;故选B。11.关于化合物 和化合物 的性质,下列推测不合理的是
A. 为四面体结构
B. 与水反应产生
C. 与盐酸作用能产生氯气
D. 与足量 溶液反应可生成两种钠盐
【答案】C
【解析】A. 中中心原子Si价层电子对数为4,无孤电子对,分子空间结构为四面
体结构,A正确;B. 可以水解,生成硅酸沉淀、氢气和氯化氢,B正确;C.化合
物 中S显+6价,Cl显示-1价,不能与盐酸发生氧化还原产生氯气,C错误;D.
与足量 溶液反应可生成氯化钠、 和HO,D正确;答案选C。
2
12.某电化学锂富集装置如图,工作步骤如下:Ⅰ.向MnO 所在腔室通入海水,启动电源
2
乙,使海水中 进入MnO 结构形成 ;Ⅱ.关闭电源乙和海水通道,启动电源甲,
2
同时向电极a上通入O 下列说法错误的是
2.
A.电极b与电源乙的正极相连
B.步骤Ⅰ时,腔室2中的 进入MnO 所在腔室
2
C.步骤Ⅱ时,阳极的电极反应式为
D.在电极a上每消耗5.6 L O(换算成标准状况),腔室1质量增加7 g
2
【答案】D
【分析】启动电源乙,使海水中Li+进入MnO 结构形成LiMnO,MnO 中锰元素的化合价降
2 x 2 4 2
低,作阴极,与电源乙的负极相连,电极反应式为:2MnO+xLi++xe-=LiMnO;电极b作阳
2 x 2 4
极,连接电源乙正极,电极反应式为:2HO-4e-=O↑+4H+,关闭电源乙和海水通道,启动
2 2
电源甲,向电极a上通入空气,使LiMnO 中的Li+脱出进入腔室1,则电极a为阴极,电
x 2 4
极反应式为:2HO+O+4e-=4OH-,阳极的电极反应式为:LiMnO-xe-=xLi++2MnO。
2 2 x 2 4 2
【解析】A.由分析得,电极b作阳极,连接电源乙正极,故A正确;B.步骤Ⅰ时,MnO
2
中锰元素的化合价降低,作阴极,腔室2中的 向阴极移动,进入MnO 所在腔室,故B
2
正确;C.由分析得,步骤Ⅱ时,阳极的LiMnO 失去电子,变为Li+和MnO,电极反应式
x 2 4 2
为 ,故C正确;D.电极a为阴极,电极反应式为:2HO+O+4e-=4OH-,每消耗5.6 L O(换算成标准状况),即0.25molO,转移电子数为
2 2 2 2
1mol,即有1molLi+进入腔室1,腔室1增重:0.25mol×32g/mol+1mol×7g/mol=15g,故D
错误;故选D。
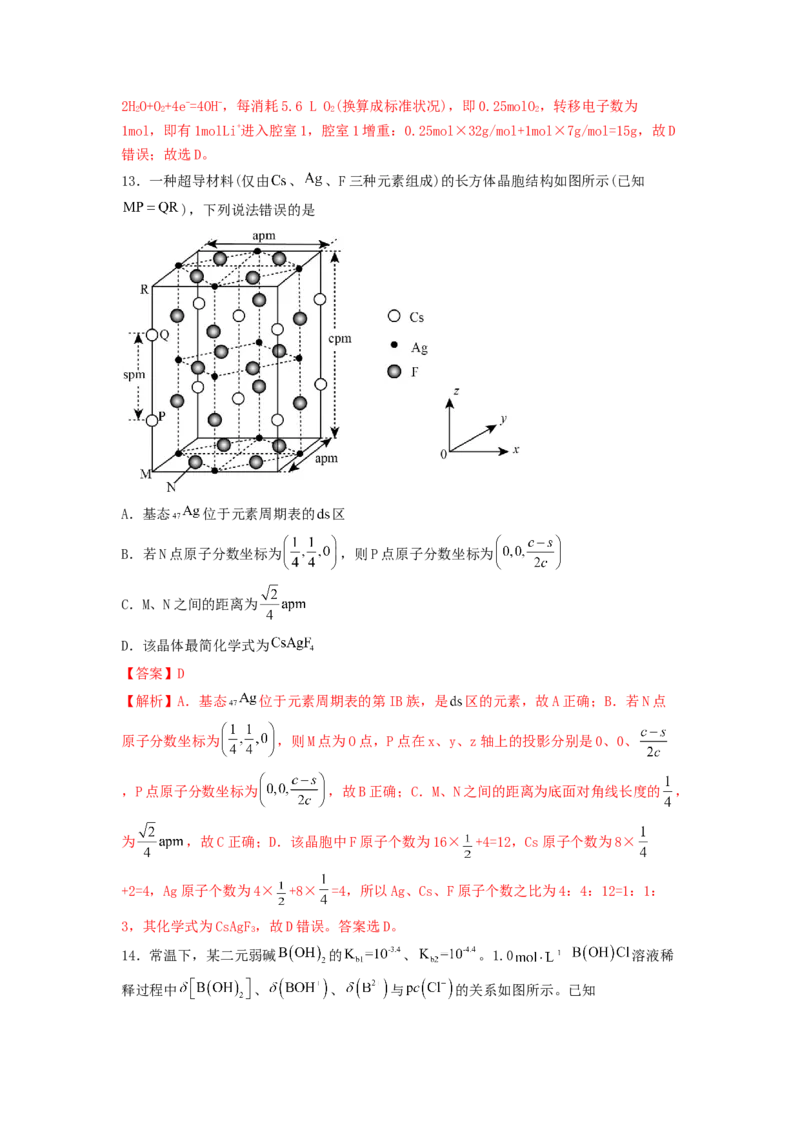
13.一种超导材料(仅由 、 、F三种元素组成)的长方体晶胞结构如图所示(已知
),下列说法错误的是
A.基态 位于元素周期表的 区
B.若N点原子分数坐标为 ,则P点原子分数坐标为
C.M、N之间的距离为
D.该晶体最简化学式为
【答案】D
【解析】A.基态 位于元素周期表的第IB族,是 区的元素,故A正确;B.若N点
原子分数坐标为 ,则M点为O点,P点在x、y、z轴上的投影分别是0、0、
,P点原子分数坐标为 ,故B正确;C.M、N之间的距离为底面对角线长度的 ,
为 ,故C正确;D.该晶胞中F原子个数为16× +4=12,Cs原子个数为8×
+2=4,Ag原子个数为4× +8× =4,所以Ag、Cs、F原子个数之比为4:4:12=1:1:
3,其化学式为CsAgF,故D错误。答案选D。
3
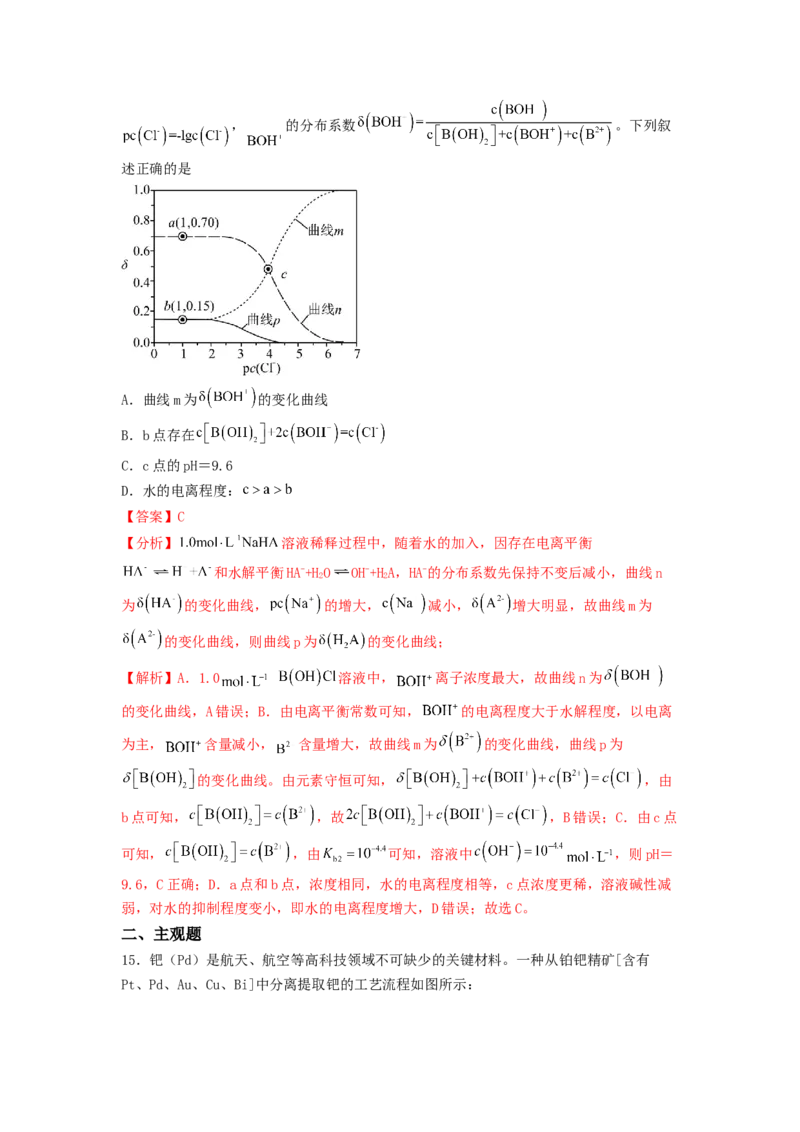
14.常温下,某二元弱碱 的 、 。1.0 溶液稀
释过程中 、 、 与 的关系如图所示。已知, 的分布系数 。下列叙
述正确的是
A.曲线m为 的变化曲线
B.b点存在
C.c点的pH=9.6
D.水的电离程度:
【答案】C
【分析】 溶液稀释过程中,随着水的加入,因存在电离平衡
和水解平衡HA-+HO OH-+HA,HA-的分布系数先保持不变后减小,曲线n
2 2
为 的变化曲线, 的增大, 减小, 增大明显,故曲线m为
的变化曲线,则曲线p为 的变化曲线;
【解析】A.1.0 溶液中, 离子浓度最大,故曲线n为
的变化曲线,A错误;B.由电离平衡常数可知, 的电离程度大于水解程度,以电离
为主, 含量减小, 含量增大,故曲线m为 的变化曲线,曲线p为
的变化曲线。由元素守恒可知, ,由
b点可知, ,故 ,B错误;C.由c点
可知, ,由 可知,溶液中 ,则pH=
9.6,C正确;D.a点和b点,浓度相同,水的电离程度相等,c点浓度更稀,溶液碱性减
弱,对水的抑制程度变小,即水的电离程度增大,D错误;故选C。
二、主观题
15.钯(Pd)是航天、航空等高科技领域不可缺少的关键材料。一种从铂钯精矿[含有
Pt、Pd、Au、Cu、Bi]中分离提取钯的工艺流程如图所示:(1)“滤液1”中含有 和 , 中Cu的化合价为 ;Bi与As在
周期表中位于同一主族,基态As原子的简化电子排布式为 。
(2)“氯化溶解”时氯气的作用是 。
(3)“分金”时, 的氧化性 (填“大于”或“小于”) ,理由是 。
(4)“沉铂”时发生反应的化学方程式为 。
(5)“沉钯”时反应的化学方程式为 。“滤液3”可以进入到 中循环
利用。
(6) (水合肼)将 还原为金属钯时,还原剂与氧化剂的物质的量之
比为 。
【答案】(1)
(2)作氧化剂(合理即可)
(3)大于 只还原了 (合理即可)
(4)
(5) 沉铂、沉钯(合理即可)
(6)1:2
【分析】铂钯精矿[含有Pt、Pd、Au、Cu、Bi]用浓盐酸酸浸,“滤液1”中含有
和 ,滤饼中含有Pt、Pd、Au,氯化溶解后加入亚硫酸钠溶液分金,金不溶解过滤除
去,滤液中加入氯化铵沉铂,过滤后加入氯化铵和次氯酸钠溶液沉钯, (水合
肼)将 还原为金属钯,以此解答。
【解析】(1) 中Cl为-1价,H为+1价,Cu显 价;基态As原子的简化电子排
布式为 。(2)“氯化溶解”时氯气的作用是作氧化剂。
(3)由于“分金”时 只还原了 ,未还原 ,故 的氧化性大
于 。
(4)“沉铂”时发生复分解反应,化学方程式为 。
(5)“沉钯”时次氯酸钠被还原为 , 被氧化为 ,配平后化学方
程式为 。盐酸参与反应的化学方程
式为 ,“滤液3”为 溶液,可以进入
“沉铂”、“沉钯”步骤中循环利用。
(6) (还原剂)中N为 价,被氧化为 时失去 , (氧化
剂)中Pd为 价,被还原为金属Pd时得到 ,根据电子守恒可知,还原剂与氧化剂的
物质的量之比为1:2。