文档内容
专练 3 一定物质的量浓度溶液的配制与计算
1.[2022·辽宁沈阳期中]下列实验操作可以达到实验目的的是( )
编号 实验目的 实验操作
A 配制稀硫酸 先将浓硫酸加入烧杯中,然后缓慢倒入蒸馏水并搅拌
配制 0.10 mol·L-1 的 称取1.0 g固体NaOH于烧杯中,加入少量蒸馏水溶
B
NaOH溶液 解,转移至250 mL容量瓶中定容
配制浓度为0.10 mol·L 称取KMnO 固体1.58 g,放入100 mL容量瓶中,加水
C 4
-1的KMnO 溶液 溶解并稀释至刻度线处
4
向稀盐酸中加入锌粒,将生成的气体依次通过NaOH
D 制取纯净干燥的氢气
溶液和浓硫酸
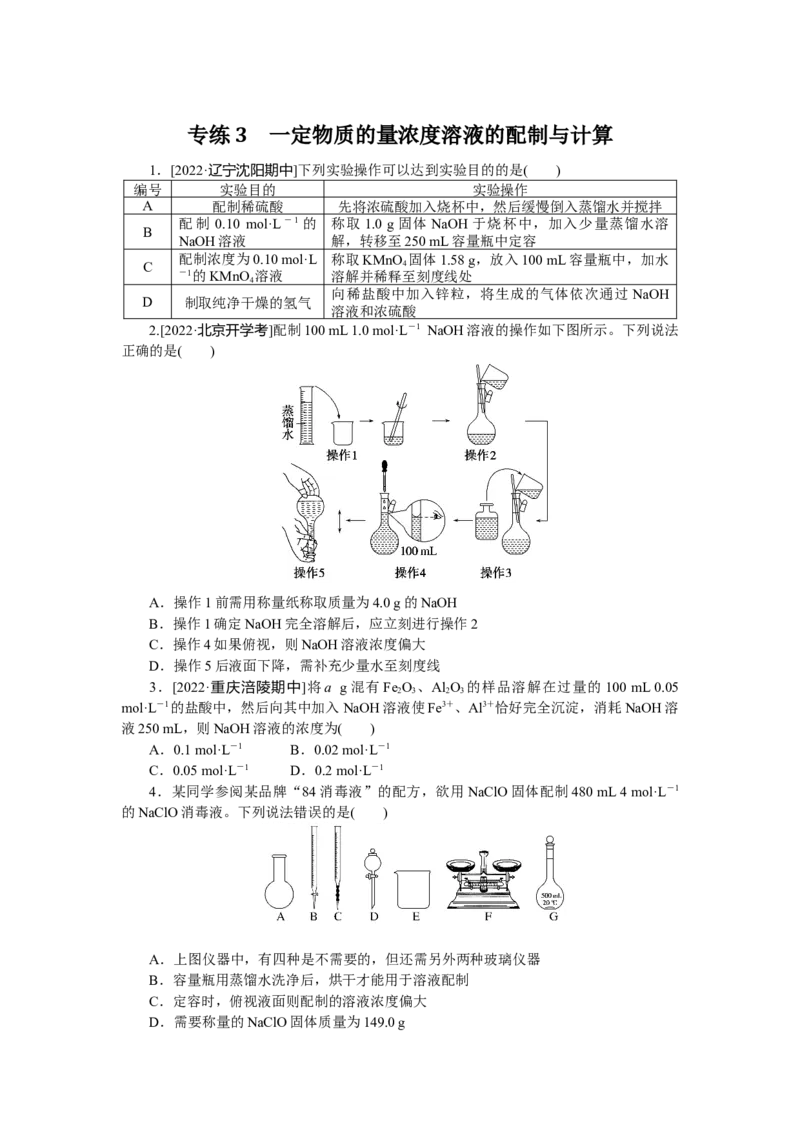
2.[2022·北京开学考]配制100 mL 1.0 mol·L-1 NaOH溶液的操作如下图所示。下列说法
正确的是( )
A.操作1前需用称量纸称取质量为4.0 g的NaOH
B.操作1确定NaOH完全溶解后,应立刻进行操作2
C.操作4如果俯视,则NaOH溶液浓度偏大
D.操作5后液面下降,需补充少量水至刻度线
3.[2022·重庆涪陵期中]将a g混有Fe O 、Al O 的样品溶解在过量的100 mL 0.05
2 3 2 3
mol·L-1的盐酸中,然后向其中加入NaOH溶液使Fe3+、Al3+恰好完全沉淀,消耗NaOH溶
液250 mL,则NaOH溶液的浓度为( )
A.0.1 mol·L-1 B.0.02 mol·L-1
C.0.05 mol·L-1 D.0.2 mol·L-1
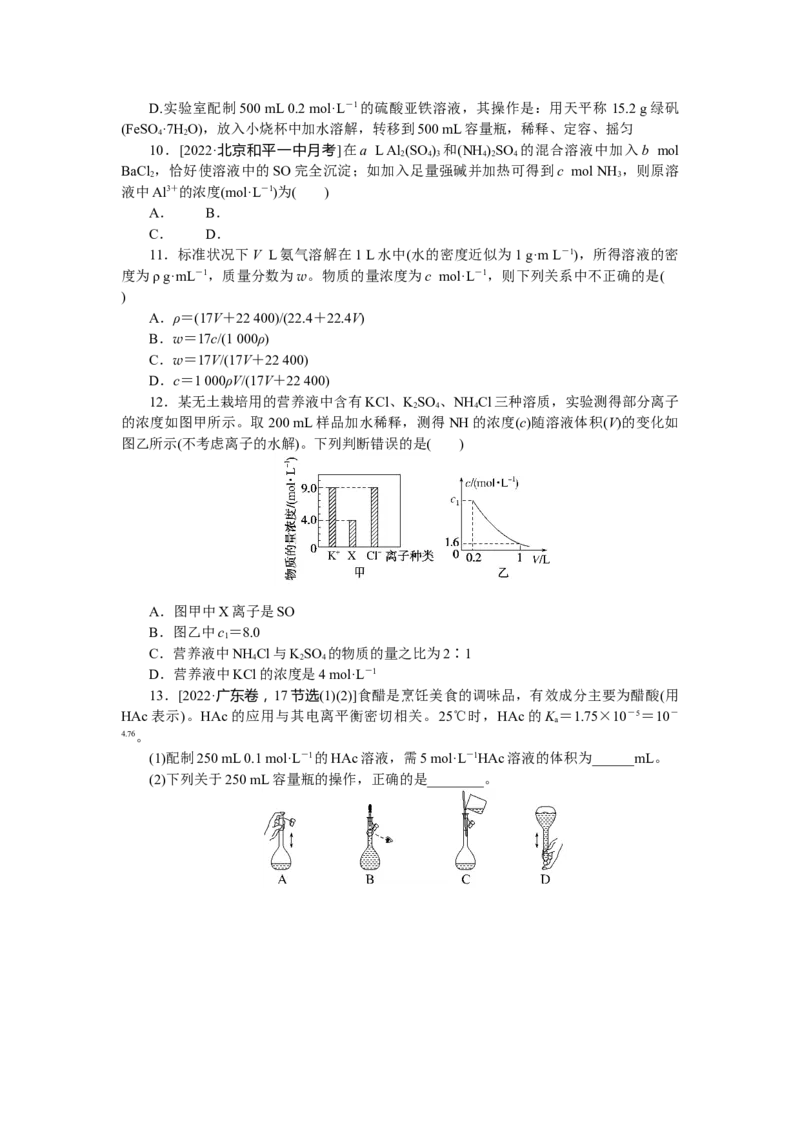
4.某同学参阅某品牌“84消毒液”的配方,欲用NaClO固体配制480 mL 4 mol·L-1
的NaClO消毒液。下列说法错误的是( )
A.上图仪器中,有四种是不需要的,但还需另外两种玻璃仪器
B.容量瓶用蒸馏水洗净后,烘干才能用于溶液配制
C.定容时,俯视液面则配制的溶液浓度偏大
D.需要称量的NaClO固体质量为149.0 g5.[2022·四川成都石室中学开学考]如图是某品牌饮用矿物质水标签的部分内容。下列
说法正确的是( )
A.标签上离子的浓度是物质的量浓度
B.由矿物质水制蒸馏水必须使用的玻璃仪器有圆底烧瓶、酒精灯、温度计、冷凝管、
牛角管和锥形瓶
C.该品牌饮用矿物质水中c(Mg2+)最大值为2×10-4mol·L-1
D.一瓶该品牌饮用矿物质水中SO的物质的量不超过1×10-5 mol
6.某结晶水合物的化学式为R·nHO,其相对分子质量为M。25℃时,a g该晶体能
2
够溶于b g水中形成V mL溶液,下列关系中不正确的是( )
A.该溶液中溶质质量分数w=%
B.该溶液的物质的量浓度c= mol·L-1
C.该溶液中溶剂与溶质的质量比m(水)∶m(溶质)=(+b)∶(a-)
D.该溶液的密度ρ=g·L-1
7.[2022·甘肃兰州一中月考]下图是病人输液用的氯化钠注射液标签的部分内容,下列
说法不正确的是( )
A.该注射液的质量为2.25 g
B.0.9%是氯化钠的质量分数
C.该注射液的密度为1 g·mL-1
D.氯化钠的物质的量浓度约为0.15 mol·L-1
8.浓度为2 mol·L-1 的盐酸V L,欲使其浓度变为4 mol·L-1,以下列出的方法中可行
的是( )
A.通入标准状况下的HCl气体44.8 L
B.将溶液加热蒸发浓缩至0.5V L
C.蒸发掉0.5V L水
D.加入10 mol·L-1盐酸0.6V L,再将溶液稀释至2V L
9.[2022·山西省怀仁县高三月考]下列有关实验原理或操作正确的是( )
A.用20 mL量筒量取15 mL酒精,加水5 mL,配制质量分数为75%的酒精溶液
B.在200 mL某硫酸盐溶液中,含有1.5N 个硫酸根离子,同时含有N 个金属离子,
A A
则该硫酸盐的物质的量浓度为2.5 mol·L-1
C.实验中需用2.0 mol·L-1的NaCO 溶液950 mL,配制时应选用的容量瓶的规格和
2 3
称取NaCO 的质量分数分别为950 mL、201.4 g
2 3D.实验室配制500 mL 0.2 mol·L-1的硫酸亚铁溶液,其操作是:用天平称 15.2 g绿矾
(FeSO ·7H O),放入小烧杯中加水溶解,转移到500 mL容量瓶,稀释、定容、摇匀
4 2
10.[2022·北京和平一中月考]在a L Al (SO ) 和(NH )SO 的混合溶液中加入b mol
2 4 3 4 2 4
BaCl ,恰好使溶液中的SO完全沉淀;如加入足量强碱并加热可得到c mol NH ,则原溶
2 3
液中Al3+的浓度(mol·L-1)为( )
A. B.
C. D.
11.标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·m L-1),所得溶液的密
度为ρ g·mL-1,质量分数为w。物质的量浓度为c mol·L-1,则下列关系中不正确的是(
)
A.ρ=(17V+22 400)/(22.4+22.4V)
B.w=17c/(1 000ρ)
C.w=17V/(17V+22 400)
D.c=1 000ρV/(17V+22 400)
12.某无土栽培用的营养液中含有KCl、KSO 、NH Cl三种溶质,实验测得部分离子
2 4 4
的浓度如图甲所示。取200 mL样品加水稀释,测得NH的浓度(c)随溶液体积(V)的变化如
图乙所示(不考虑离子的水解)。下列判断错误的是( )
A.图甲中X离子是SO
B.图乙中c=8.0
1
C.营养液中NH Cl与KSO 的物质的量之比为2∶1
4 2 4
D.营养液中KCl的浓度是4 mol·L-1
13.[2022·广东卷,17节选(1)(2)]食醋是烹饪美食的调味品,有效成分主要为醋酸(用
HAc表示)。HAc的应用与其电离平衡密切相关。25℃时,HAc的K =1.75×10-5=10-
a
4.76。
(1)配制250 mL 0.1 mol·L-1的HAc溶液,需5 mol·L-1HAc溶液的体积为______mL。
(2)下列关于250 mL容量瓶的操作,正确的是________。