文档内容
专练 53 实验综合应用二
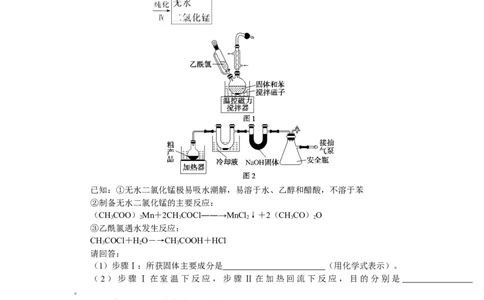
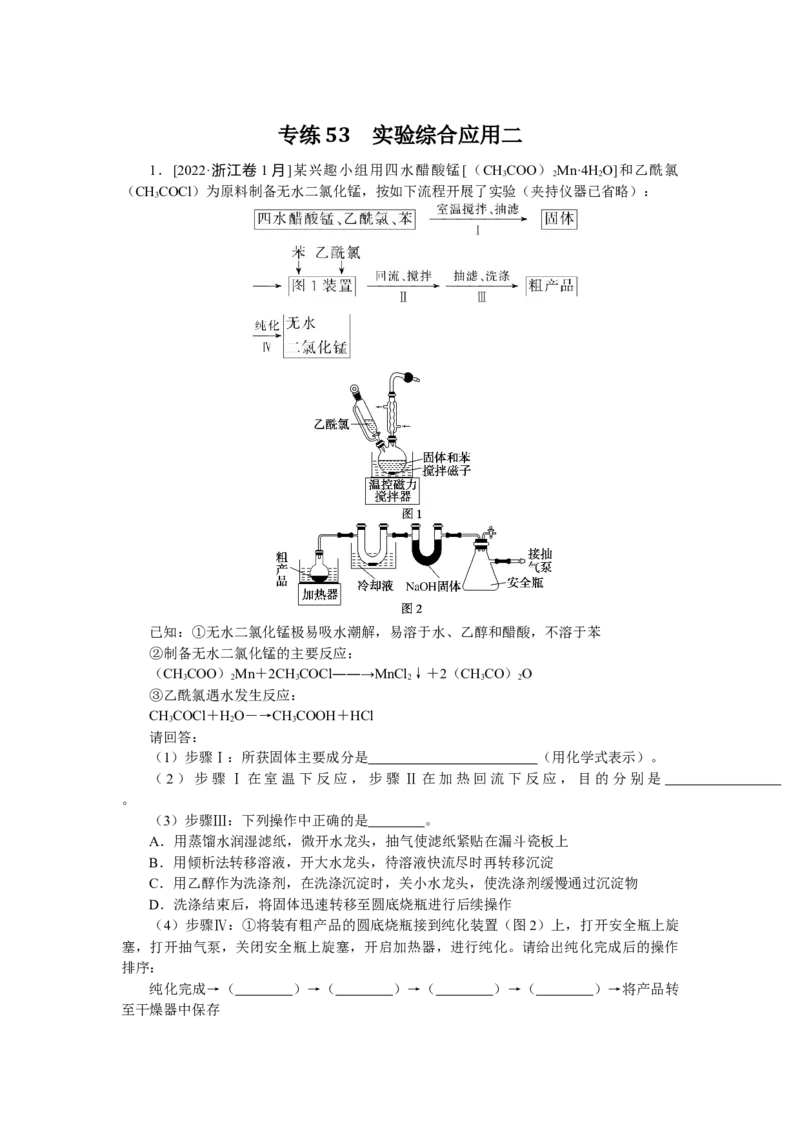
1.[2022·浙江卷 1月]某兴趣小组用四水醋酸锰[(CHCOO) Mn·4H O]和乙酰氯
3 2 2
(CHCOCl)为原料制备无水二氯化锰,按如下流程开展了实验(夹持仪器已省略):
3
已知:①无水二氯化锰极易吸水潮解,易溶于水、乙醇和醋酸,不溶于苯
②制备无水二氯化锰的主要反应:
(CHCOO)Mn+2CHCOCl――→MnCl ↓+2(CHCO)O
3 2 3 2 3 2
③乙酰氯遇水发生反应:
CHCOCl+HO―→CHCOOH+HCl
3 2 3
请回答:
(1)步骤Ⅰ:所获固体主要成分是 (用化学式表示)。
(2)步骤Ⅰ在室温下反应,步骤Ⅱ在加热回流下反应,目的分别是
。
(3)步骤Ⅲ:下列操作中正确的是 。
A.用蒸馏水润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上
B.用倾析法转移溶液,开大水龙头,待溶液快流尽时再转移沉淀
C.用乙醇作为洗涤剂,在洗涤沉淀时,关小水龙头,使洗涤剂缓慢通过沉淀物
D.洗涤结束后,将固体迅速转移至圆底烧瓶进行后续操作
(4)步骤Ⅳ:①将装有粗产品的圆底烧瓶接到纯化装置(图2)上,打开安全瓶上旋
塞,打开抽气泵,关闭安全瓶上旋塞,开启加热器,进行纯化。请给出纯化完成后的操作
排序:
纯化完成→( )→( )→( )→( )→将产品转
至干燥器中保存a.拔出圆底烧瓶的瓶塞
b.关闭抽气泵
c.关闭加热器,待烧瓶冷却至室温
d.打开安全瓶上旋塞
②图2装置中U形管内NaOH固体的作用是 。
(5)用滴定分析法确定产品纯度。甲同学通过测定产品中锰元素的含量确定纯度;乙
同学通过测定产品中氯元素的含量确定纯度。合理的是 (填“甲”或“乙”)同
学的方法。
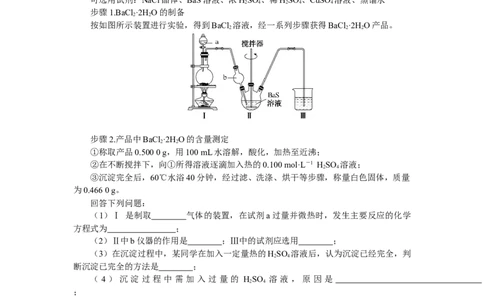
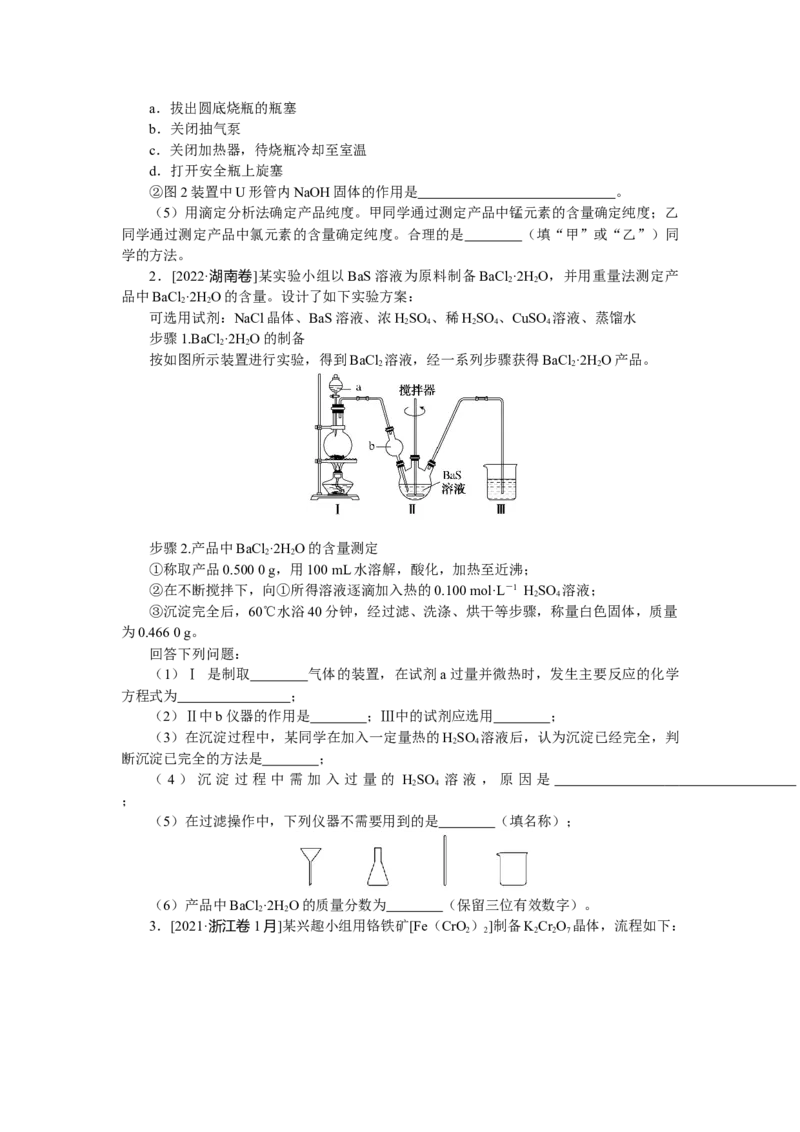
2.[2022·湖南卷]某实验小组以BaS溶液为原料制备BaCl ·2H O,并用重量法测定产
2 2
品中BaCl ·2H O的含量。设计了如下实验方案:
2 2
可选用试剂:NaCl晶体、BaS溶液、浓HSO 、稀HSO 、CuSO 溶液、蒸馏水
2 4 2 4 4
步骤1.BaCl ·2H O的制备
2 2
按如图所示装置进行实验,得到BaCl 溶液,经一系列步骤获得BaCl ·2H O产品。
2 2 2
步骤2.产品中BaCl ·2H O的含量测定
2 2
①称取产品0.500 0 g,用100 mL水溶解,酸化,加热至近沸;
②在不断搅拌下,向①所得溶液逐滴加入热的0.100 mol·L-1 HSO 溶液;
2 4
③沉淀完全后,60℃水浴40分钟,经过滤、洗涤、烘干等步骤,称量白色固体,质量
为0.466 0 g。
回答下列问题:
(1)Ⅰ 是制取 气体的装置,在试剂a过量并微热时,发生主要反应的化学
方程式为 ;
(2)Ⅱ中b仪器的作用是 ;Ⅲ中的试剂应选用 ;
(3)在沉淀过程中,某同学在加入一定量热的HSO 溶液后,认为沉淀已经完全,判
2 4
断沉淀已完全的方法是 ;
( 4 ) 沉 淀 过 程 中 需 加 入 过 量 的 HSO 溶 液 , 原 因 是
2 4
;
(5)在过滤操作中,下列仪器不需要用到的是 (填名称);
(6)产品中BaCl ·2H O的质量分数为 (保留三位有效数字)。
2 2
3.[2021·浙江卷1月]某兴趣小组用铬铁矿[Fe(CrO)]制备KCr O 晶体,流程如下:
2 2 2 2 7已知:4Fe(CrO)+10NaCO+7O=====8NaCrO+4NaFeO +10CO
2 2 2 3 2 2 4 2 2
2H++2CrO⇌Cr
2
O+H
2
O
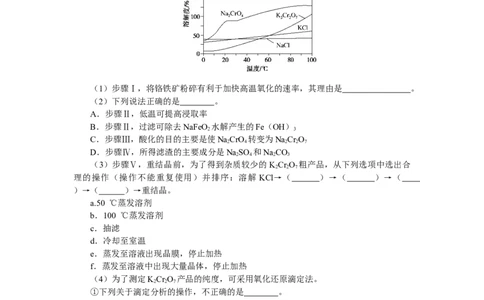
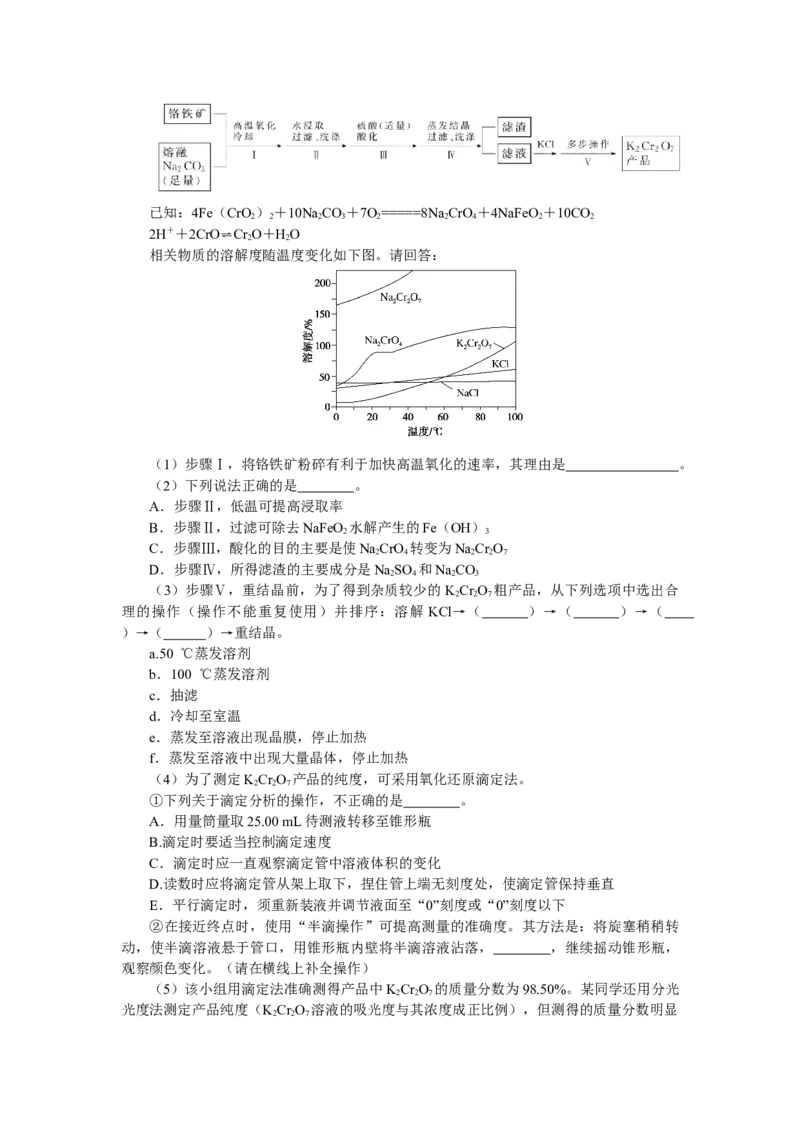
相关物质的溶解度随温度变化如下图。请回答:
(1)步骤Ⅰ,将铬铁矿粉碎有利于加快高温氧化的速率,其理由是 。
(2)下列说法正确的是 。
A.步骤Ⅱ,低温可提高浸取率
B.步骤Ⅱ,过滤可除去NaFeO 水解产生的Fe(OH)
2 3
C.步骤Ⅲ,酸化的目的主要是使NaCrO 转变为NaCr O
2 4 2 2 7
D.步骤Ⅳ,所得滤渣的主要成分是NaSO 和NaCO
2 4 2 3
(3)步骤Ⅴ,重结晶前,为了得到杂质较少的KCr O 粗产品,从下列选项中选出合
2 2 7
理的操作(操作不能重复使用)并排序:溶解 KCl→( )→( )→(
)→( )→重结晶。
a.50 ℃蒸发溶剂
b.100 ℃蒸发溶剂
c.抽滤
d.冷却至室温
e.蒸发至溶液出现晶膜,停止加热
f.蒸发至溶液中出现大量晶体,停止加热
(4)为了测定KCr O 产品的纯度,可采用氧化还原滴定法。
2 2 7
①下列关于滴定分析的操作,不正确的是 。
A.用量筒量取25.00 mL待测液转移至锥形瓶
B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.平行滴定时,须重新装液并调节液面至“0”刻度或“0”刻度以下
②在接近终点时,使用“半滴操作”可提高测量的准确度。其方法是:将旋塞稍稍转
动,使半滴溶液悬于管口,用锥形瓶内壁将半滴溶液沾落, ,继续摇动锥形瓶,
观察颜色变化。(请在横线上补全操作)
(5)该小组用滴定法准确测得产品中KCr O 的质量分数为98.50%。某同学还用分光
2 2 7
光度法测定产品纯度(KCr O 溶液的吸光度与其浓度成正比例),但测得的质量分数明显
2 2 7偏低。分析其原因,发现配制 KCr O 待测水溶液时少加了一种试剂。该试剂是
2 2 7
,添加该试剂的理由是 。