文档内容
专项 11 催化剂、物质转化循环图
该专题分为三个板块
【1】总概括
【2】真题演练
【3】专项练习
【1】总概括
反应历程或机理图像一般取材于实际科研成果,充分体现了化学反应的本质,高考常以此为载体考查反应
原理、活化能、反应热等知识,是近年高考的命题热点,此类试题难点是从陌生图像中提取解题信息。
【2】真题演练
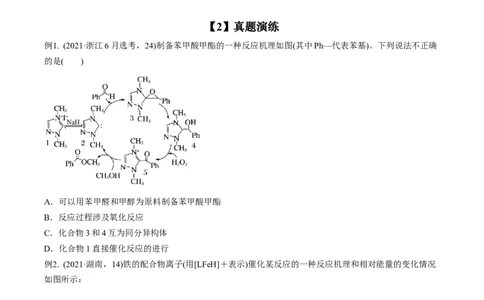
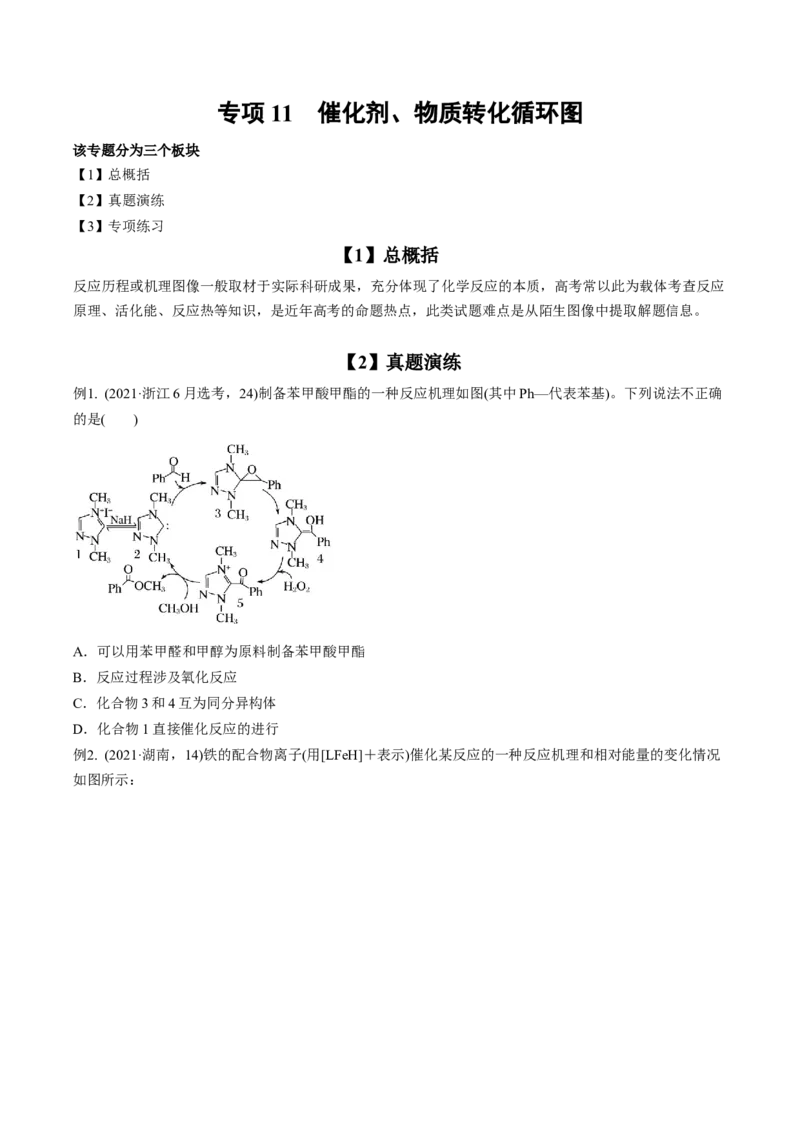
例1. (2021·浙江6月选考,24)制备苯甲酸甲酯的一种反应机理如图(其中Ph—代表苯基)。下列说法不正确
的是( )
A.可以用苯甲醛和甲醇为原料制备苯甲酸甲酯
B.反应过程涉及氧化反应
C.化合物3和4互为同分异构体
D.化合物1直接催化反应的进行
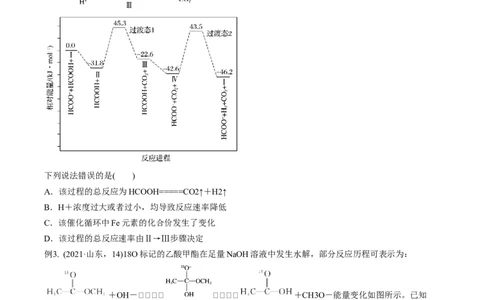
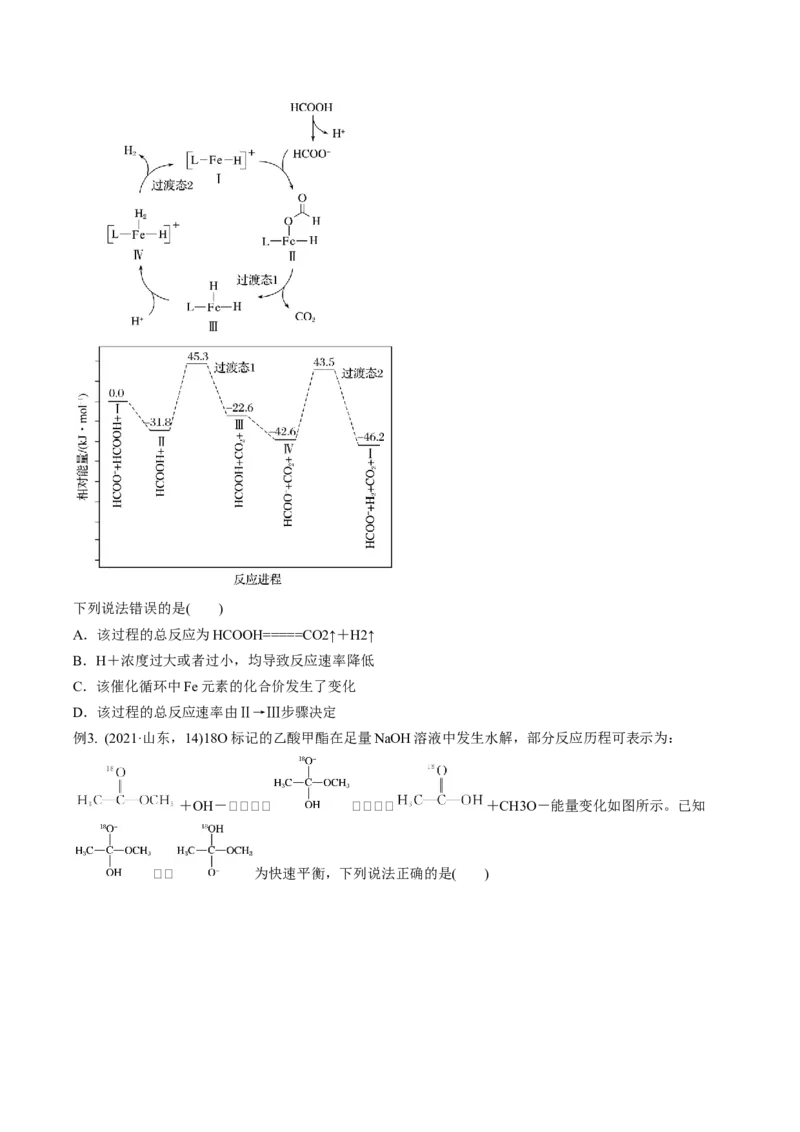
例2. (2021·湖南,14)铁的配合物离子(用[LFeH]+表示)催化某反应的一种反应机理和相对能量的变化情况
如图所示:下列说法错误的是( )
A.该过程的总反应为HCOOH=====CO2↑+H2↑
B.H+浓度过大或者过小,均导致反应速率降低
C.该催化循环中Fe元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
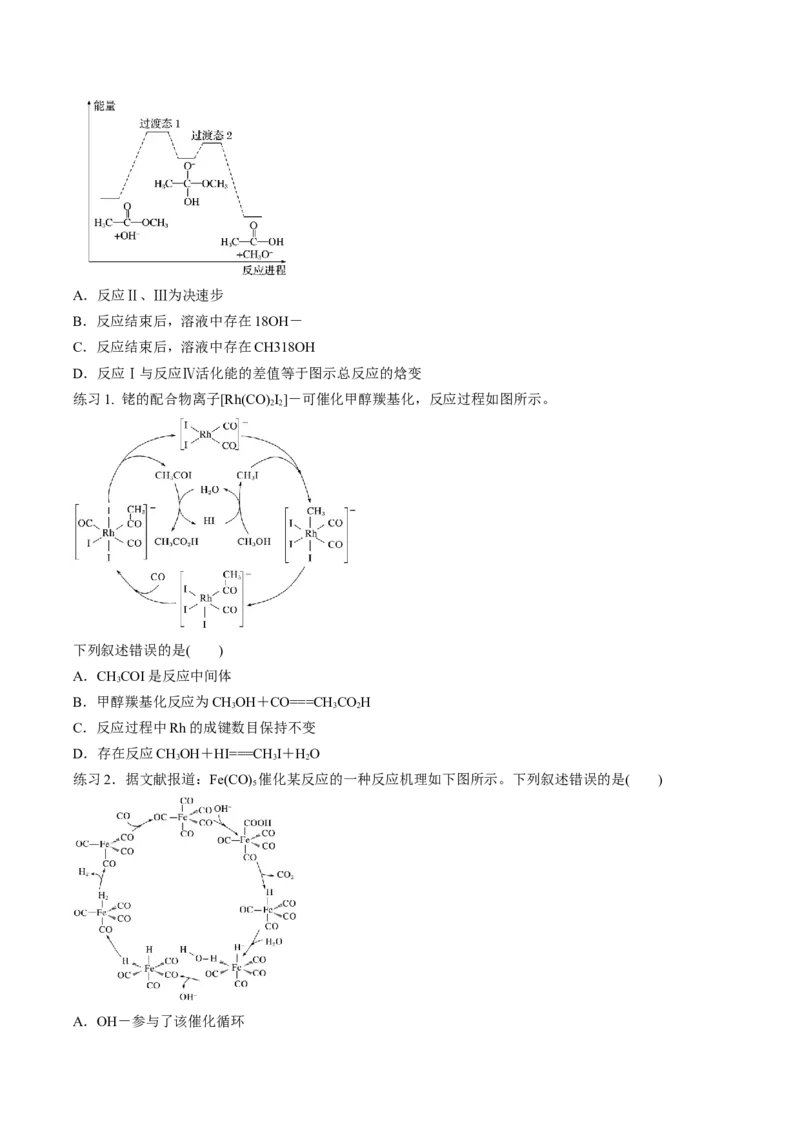
例3. (2021·山东,14)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH3O-能量变化如图所示。已知
为快速平衡,下列说法正确的是( )A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH318OH
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
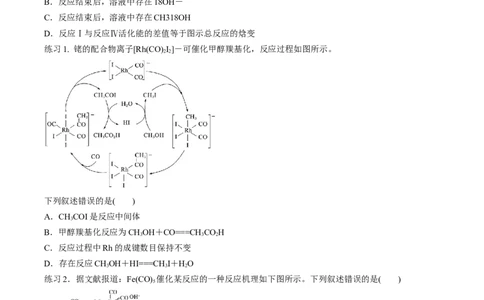
练习1. 铑的配合物离子[Rh(CO) I]-可催化甲醇羰基化,反应过程如图所示。
2 2
下列叙述错误的是( )
A.CHCOI是反应中间体
3
B.甲醇羰基化反应为CHOH+CO===CHCOH
3 3 2
C.反应过程中Rh的成键数目保持不变
D.存在反应CHOH+HI===CH I+HO
3 3 2
练习2.据文献报道:Fe(CO) 催化某反应的一种反应机理如下图所示。下列叙述错误的是( )
5
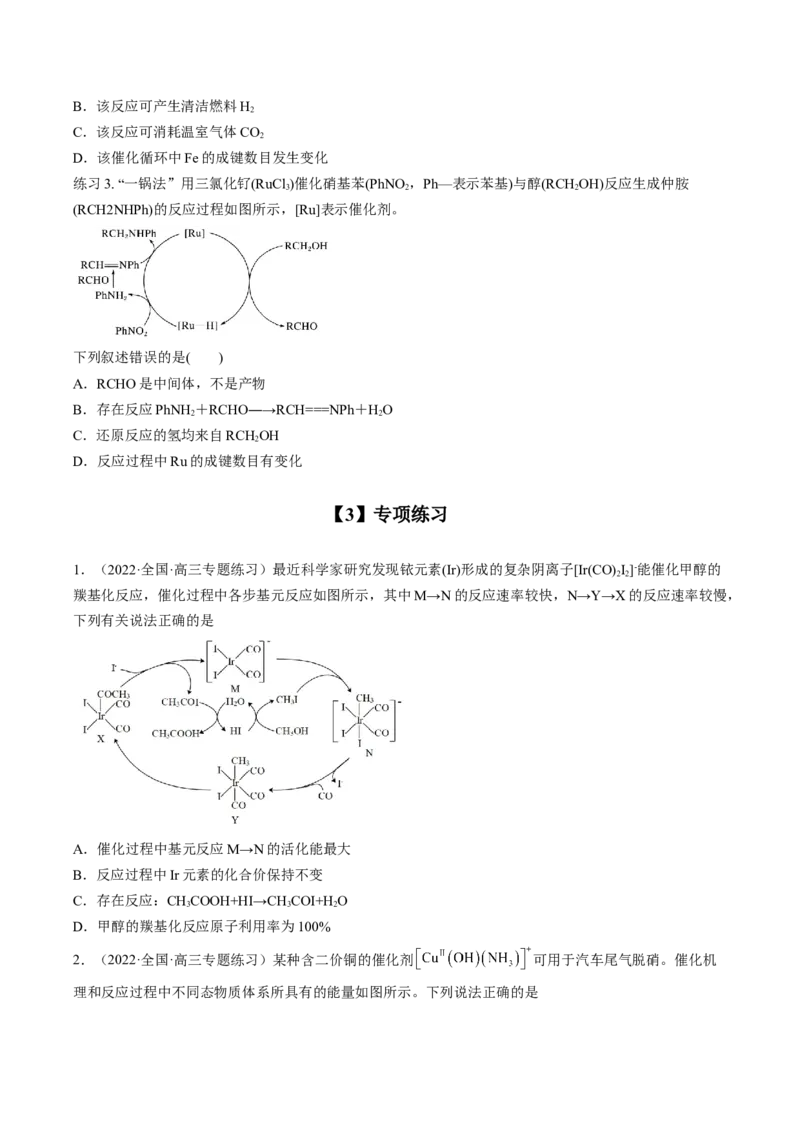
A.OH-参与了该催化循环B.该反应可产生清洁燃料H
2
C.该反应可消耗温室气体CO
2
D.该催化循环中Fe的成键数目发生变化
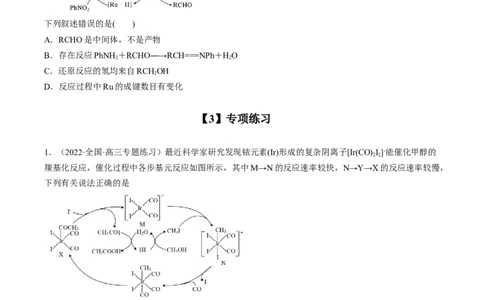
练习3. “一锅法”用三氯化钌(RuCl )催化硝基苯(PhNO ,Ph—表示苯基)与醇(RCHOH)反应生成仲胺
3 2 2
(RCH2NHPh)的反应过程如图所示,[Ru]表示催化剂。
下列叙述错误的是( )
A.RCHO是中间体,不是产物
B.存在反应PhNH +RCHO―→RCH===NPh+HO
2 2
C.还原反应的氢均来自RCHOH
2
D.反应过程中Ru的成键数目有变化
【3】专项练习
1.(2022·全国·高三专题练习)最近科学家研究发现铱元素(Ir)形成的复杂阴离子[Ir(CO) I]-能催化甲醇的
2 2
羰基化反应,催化过程中各步基元反应如图所示,其中M→N的反应速率较快,N→Y→X的反应速率较慢,
下列有关说法正确的是
A.催化过程中基元反应M→N的活化能最大
B.反应过程中Ir元素的化合价保持不变
C.存在反应:CHCOOH+HI→CH COI+HO
3 3 2
D.甲醇的羰基化反应原子利用率为100%
2.(2022·全国·高三专题练习)某种含二价铜的催化剂 可用于汽车尾气脱硝。催化机
理和反应过程中不同态物质体系所具有的能量如图所示。下列说法正确的是A.该脱硝过程总反应的焓变
B.由状态①到状态⑤所发生的反应均为氧化还原反应
C.由状态③到状态④的变化过程有极性键的断裂和形成
D.总反应的化学方程式为
3.(2022·湖南省隆回县第一中学高三期中)利用镍(Ni)及其他过渡金属配合物催化 和 氧化
偶联合成丙烯酸的催化机理如图。下列说法错误的是
A.催化循环过程中包含加成反应
B.该催化剂改变了反应的活化能,降低了焓变
C.该催化循环中Ni的成键数目发生了变化
D.总反应可表示为
4.(2022·安徽·合肥一中模拟预测)近日,中国科学院大连化学物理研究所与上海应物所合作,揭示了双
单原子催化剂中的协同催化机理,如4-硝基苯乙烯选择性加氢反应在不同的催化剂下的反应机理及选择性
如图所示,下列有关两种不同的催化过程说法错误的是A.两种催化反应过程中均存在极性键的断裂和形成
B.Mo单原子位点吸附4-硝基苯乙烯,提高了催化加氢的选择性
C.其它条件相同时,双单原子催化下4-硝基苯乙烯的平衡转化率更高
D.两种催化剂均能降低选择性加氢反应的活化能
5.(2022·全国·高三专题练习)环氧丙烷(C HO,PO)是一种重要的有机化工产品,对Cu O催化剂表面催
3 6 2
化空气氧化丙烯反应机理的DFT计算表明,可能有通过分子氧(甲图)和晶格氧(乙图)两种反应机理(TS代表
中间态)。已知吸附能指在吸附过程中释放的能量,下列说法错误的是中
A.C H 在催化剂上的吸附能低于C H 与O 共吸附在表面的吸附能
3 6 3 6 2
B.空气氧化丙烯生成环氧丙烷是放热反应
C.通过对图象的分析得出,该反应更易按照甲图路径进行
D.总反应方程式为2C H+O 2C HO
3 6 2 3 6
6.(2022·湖北·应城市第一高级中学模拟预测)以SiO 表面隔离的Cr3+催化丙烷无氧脱氢的机理如图,随
2
着反应的进行,副反应产生的积炭会导致催化剂失活。下列说法正确的是A.基态铬原子核外有6种能量不同的电子
B.总反应方程式为C H C H + 2H
3 8 3 4 2
C.Cr3+改变反应活化能的同时改变了反应的热效应
D.在该体系中加入CO 有利于丙烷脱氢
2
7.(2022·全国·高三专题练习)据文献报道,用氢气制备双氧水的一种工艺简单、能耗低的方法,其反应
原理如图所示。下列有关说法正确的是
A.反应过程中所发生的反应均为氧化还原反应
B. 、 均为该反应的催化剂
C. 的过程中有极性键的断裂和非极性键的形成
D. 能降低反应过程中的活化能
8.(2022·广东·广州市第六十五中学高三阶段练习)在钴化合物催化下,烯烃醛基化反应的历程如图所示。
下列叙述错误的是A.反应过程中Co的成键数目发生了变化
B.烯烃中的双键可提供电子与化合物中的Co共用
C.烯烃醛基化总反应为RCH=CH+CO+H →RCHCHCHO
2 2 2 2
D.该含钴化合物可降低烯烃醛基化反应的活化能,提高平衡转化率
9.(2022·福建·厦门双十中学模拟预测)甲烷可在铑/铈氧化物的催化下与过氧化氢反应,转化为甲醇和
甲基过氧化氢(CHOOH),实现了天然气的高效利用,其原理如图所示,下列说法错误的是
3
A.反应③中有极性键的断裂与生成
B.反应⑤中,Ce的化合价降低
C.铑/铈氧化物改变了CH 和HO 的反应历程,降低了反应的活化能
4 2 2
D.若用Hl8O 作反应物,一段时间后CHOH、CHOOH和铑/铈氧化物中均含有18O
2 2 3 3
10.(2022·湖北·华中师大一附中模拟预测)科学工作者探讨了在CO 和H 合成HCOOH过程中固载Ru
2 2
基催化剂可能的反应机理如图所示。下列说法错误的是。A.固载Ru基催化剂可降低该反应的焓变
B.Ru配合物1、2、3、4中Ru的化合价不变
C.总反应的化学方程式为CO+H HCOOH
2 2
D.CO 浓度过大可能会影响催化剂的实际催化效率
2
11.(2022·河南·高三开学考试)某科研团队用PdCl 催化苯酚(PhOH)羰基化合成 (DPC),并提
2
出了合成DPC的反应机理(如图所示),下列有关说法中错误的是
A.Cl-Pd-OPh和 是反应的中间产物
B.反应过程中Pd的化合价始终保持不变
C.反应过程中PdCl 降低了反应的活化能,未改变反应的△H
2
D.总反应方程式为4PhOH+2CO+O →2 +2H O
2 2
12.(2022·全国·高三专题练习)均相芬顿反应原理是高级氧化技术的经典工艺之一,如图所示( 和 为
速率常数)。下列说法错误的是
A.相同条件下,基元反应I比II的活化能低B.基元反应I中氧元素的化合价发生变化
C.基元反应II的化学方程式为HO+Fe3+=HO·+Fe2++H+
2 2 2
D.芬顿反应进行的过程中,整个体系的 几乎不变(忽略体积变化)
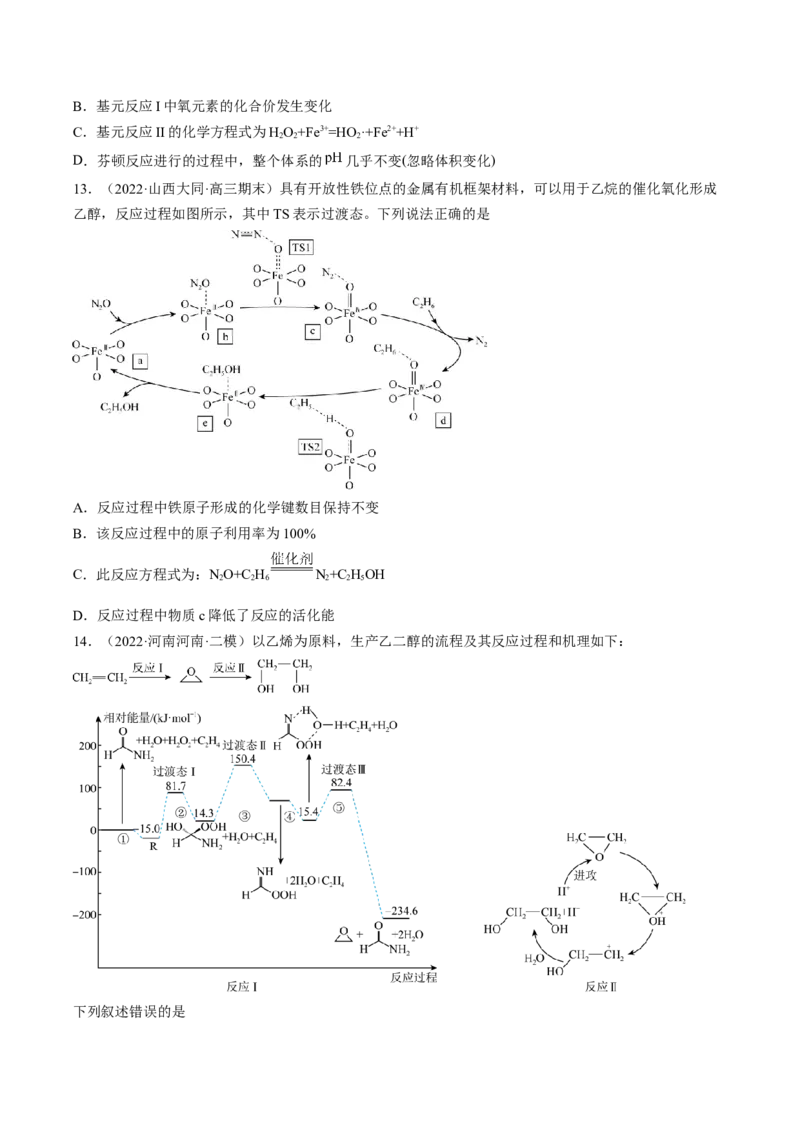
13.(2022·山西大同·高三期末)具有开放性铁位点的金属有机框架材料,可以用于乙烷的催化氧化形成
乙醇,反应过程如图所示,其中TS表示过渡态。下列说法正确的是
A.反应过程中铁原子形成的化学键数目保持不变
B.该反应过程中的原子利用率为100%
C.此反应方程式为:NO+C H N+C HOH
2 2 6 2 2 5
D.反应过程中物质c降低了反应的活化能
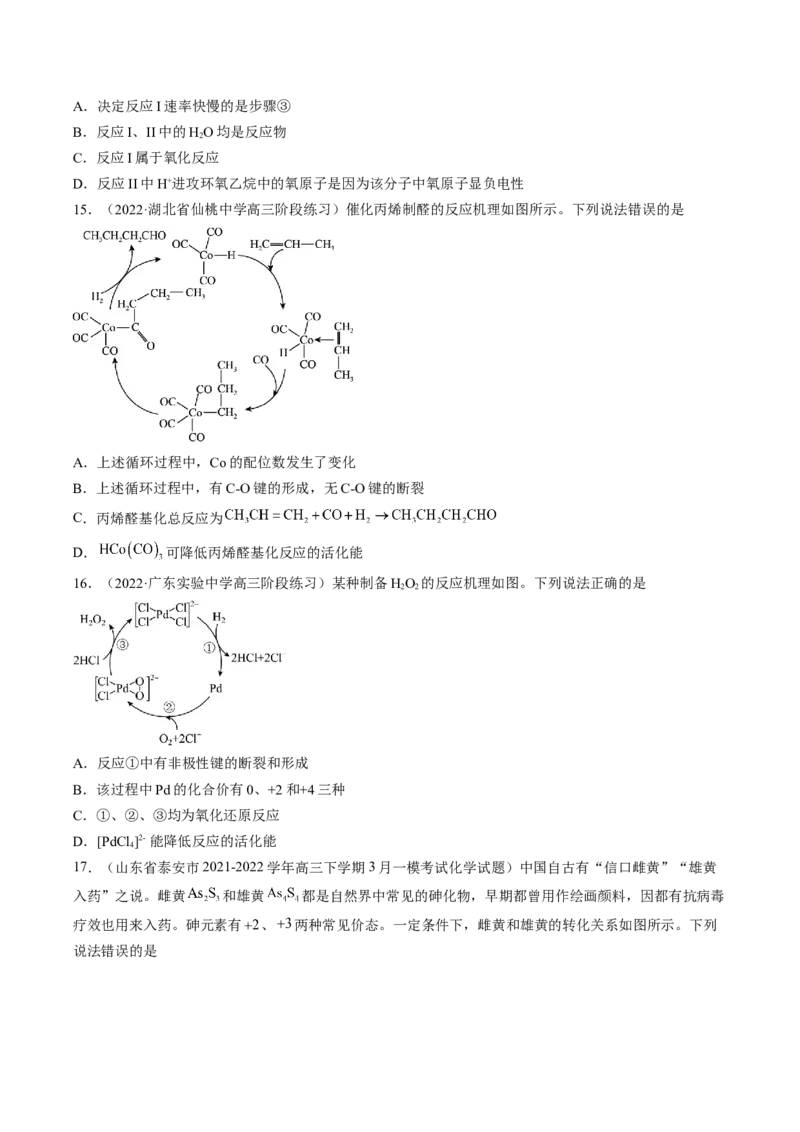
14.(2022·河南河南·二模)以乙烯为原料,生产乙二醇的流程及其反应过程和机理如下:
下列叙述错误的是A.决定反应I速率快慢的是步骤③
B.反应I、II中的HO均是反应物
2
C.反应I属于氧化反应
D.反应II中H+进攻环氧乙烷中的氧原子是因为该分子中氧原子显负电性
15.(2022·湖北省仙桃中学高三阶段练习)催化丙烯制醛的反应机理如图所示。下列说法错误的是
A.上述循环过程中,Co的配位数发生了变化
B.上述循环过程中,有C-O键的形成,无C-O键的断裂
C.丙烯醛基化总反应为
D. 可降低丙烯醛基化反应的活化能
16.(2022·广东实验中学高三阶段练习)某种制备HO 的反应机理如图。下列说法正确的是
2 2
A.反应①中有非极性键的断裂和形成
B.该过程中Pd的化合价有0、+2和+4三种
C.①、②、③均为氧化还原反应
D.[PdCl ]2- 能降低反应的活化能
4
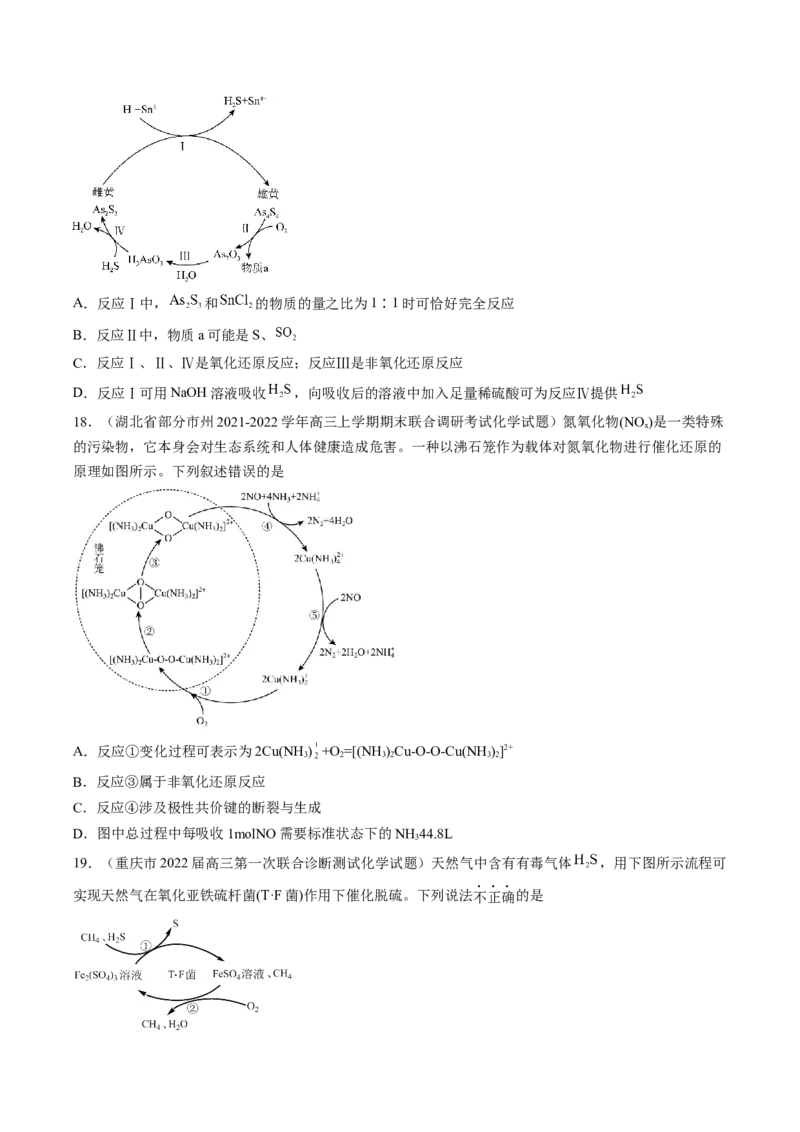
17.(山东省泰安市2021-2022学年高三下学期3月一模考试化学试题)中国自古有“信口雌黄”“雄黄
入药”之说。雌黄 和雄黄 都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒
疗效也用来入药。砷元素有 、 两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。下列
说法错误的是A.反应Ⅰ中, 和 的物质的量之比为1∶1时可恰好完全反应
B.反应Ⅱ中,物质a可能是S、
C.反应Ⅰ、Ⅱ、Ⅳ是氧化还原反应;反应Ⅲ是非氧化还原反应
D.反应Ⅰ可用NaOH溶液吸收 ,向吸收后的溶液中加入足量稀硫酸可为反应Ⅳ提供
18.(湖北省部分市州2021-2022学年高三上学期期末联合调研考试化学试题)氮氧化物(NO )是一类特殊
x
的污染物,它本身会对生态系统和人体健康造成危害。一种以沸石笼作为载体对氮氧化物进行催化还原的
原理如图所示。下列叙述错误的是
A.反应①变化过程可表示为2Cu(NH ) +O =[(NH )Cu-O-O-Cu(NH )]2+
3 2 3 2 3 2
B.反应③属于非氧化还原反应
C.反应④涉及极性共价键的断裂与生成
D.图中总过程中每吸收1molNO需要标准状态下的NH 44.8L
3
19.(重庆市2022届高三第一次联合诊断测试化学试题)天然气中含有有毒气体 ,用下图所示流程可
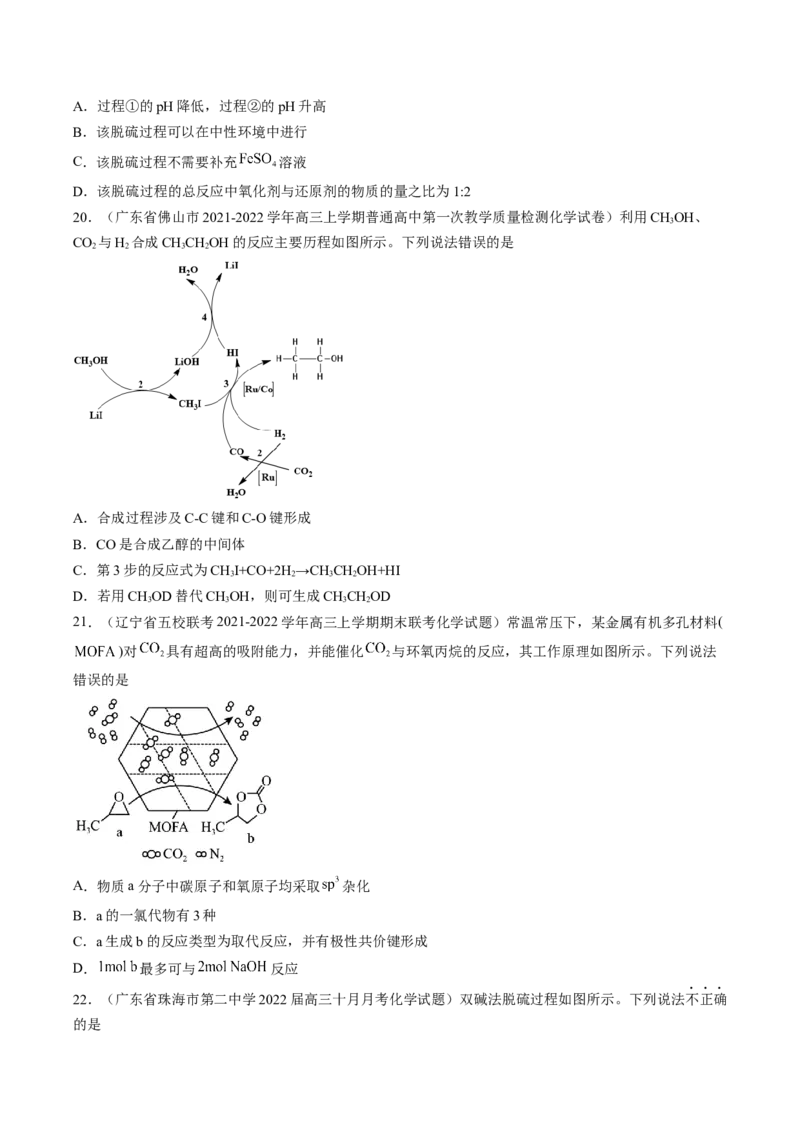
实现天然气在氧化亚铁硫杆菌(T·F菌)作用下催化脱硫。下列说法不正确的是A.过程①的pH降低,过程②的pH升高
B.该脱硫过程可以在中性环境中进行
C.该脱硫过程不需要补充 溶液
D.该脱硫过程的总反应中氧化剂与还原剂的物质的量之比为1:2
20.(广东省佛山市2021-2022学年高三上学期普通高中第一次教学质量检测化学试卷)利用CHOH、
3
CO 与H 合成CHCHOH的反应主要历程如图所示。下列说法错误的是
2 2 3 2
A.合成过程涉及C-C键和C-O键形成
B.CO是合成乙醇的中间体
C.第3步的反应式为CHI+CO+2H →CHCHOH+HI
3 2 3 2
D.若用CHOD替代CHOH,则可生成CHCHOD
3 3 3 2
21.(辽宁省五校联考2021-2022学年高三上学期期末联考化学试题)常温常压下,某金属有机多孔材料(
)对 具有超高的吸附能力,并能催化 与环氧丙烷的反应,其工作原理如图所示。下列说法
错误的是
A.物质a分子中碳原子和氧原子均采取 杂化
B.a的一氯代物有3种
C.a生成b的反应类型为取代反应,并有极性共价键形成
D. 最多可与 反应
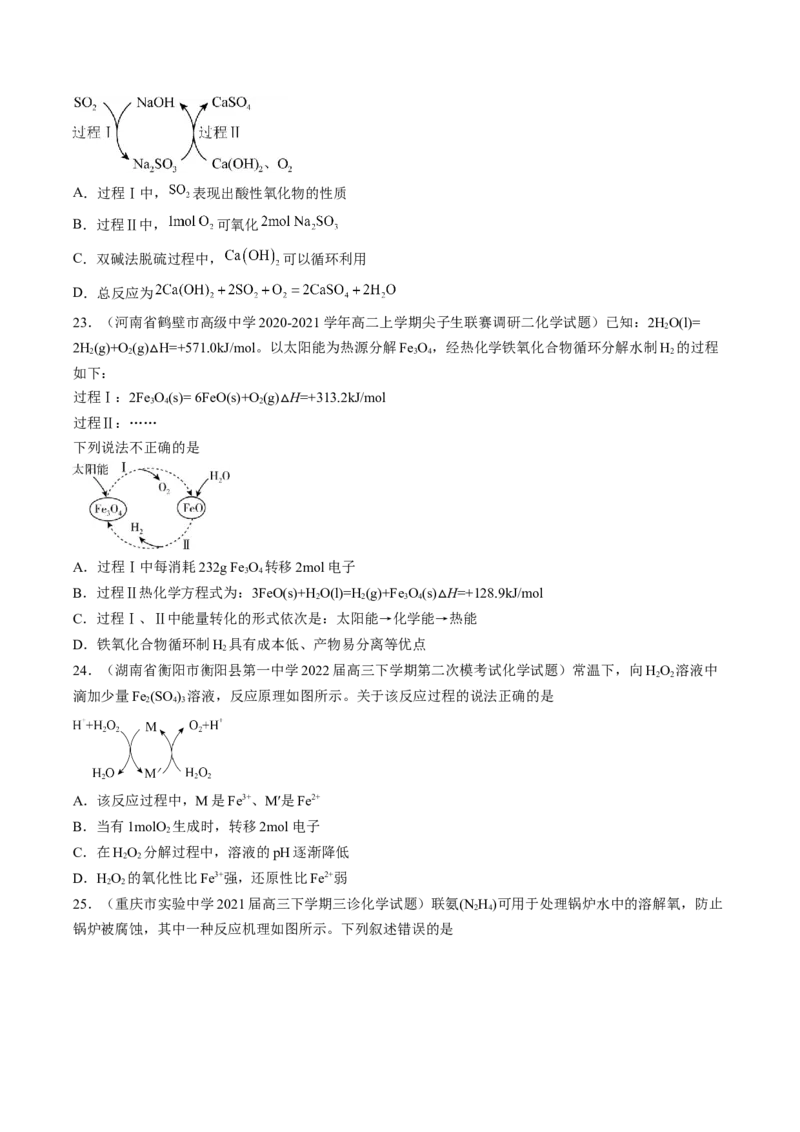
22.(广东省珠海市第二中学2022届高三十月月考化学试题)双碱法脱硫过程如图所示。下列说法不正确
的是A.过程Ⅰ中, 表现出酸性氧化物的性质
B.过程Ⅱ中, 可氧化
C.双碱法脱硫过程中, 可以循环利用
D.总反应为
23.(河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研二化学试题)已知:2HO(l)=
2
2H(g)+O(g) H=+571.0kJ/mol。以太阳能为热源分解Fe O,经热化学铁氧化合物循环分解水制H 的过程
2 2 3 4 2
如下:
△
过程Ⅰ:2Fe O(s)= 6FeO(s)+O (g) H=+313.2kJ/mol
3 4 2
过程Ⅱ:……
△
下列说法不正确的是
A.过程Ⅰ中每消耗232g Fe O 转移2mol电子
3 4
B.过程Ⅱ热化学方程式为:3FeO(s)+H O(l)=H(g)+Fe O(s) H=+128.9kJ/mol
2 2 3 4
C.过程Ⅰ、Ⅱ中能量转化的形式依次是:太阳能→化学能→热能
△
D.铁氧化合物循环制H 具有成本低、产物易分离等优点
2
24.(湖南省衡阳市衡阳县第一中学2022届高三下学期第二次模考试化学试题)常温下,向HO 溶液中
2 2
滴加少量Fe (SO ) 溶液,反应原理如图所示。关于该反应过程的说法正确的是
2 4 3
A.该反应过程中,M是Fe3+、M′是Fe2+
B.当有1molO 生成时,转移2mol电子
2
C.在HO 分解过程中,溶液的pH逐渐降低
2 2
D.HO 的氧化性比Fe3+强,还原性比Fe2+弱
2 2
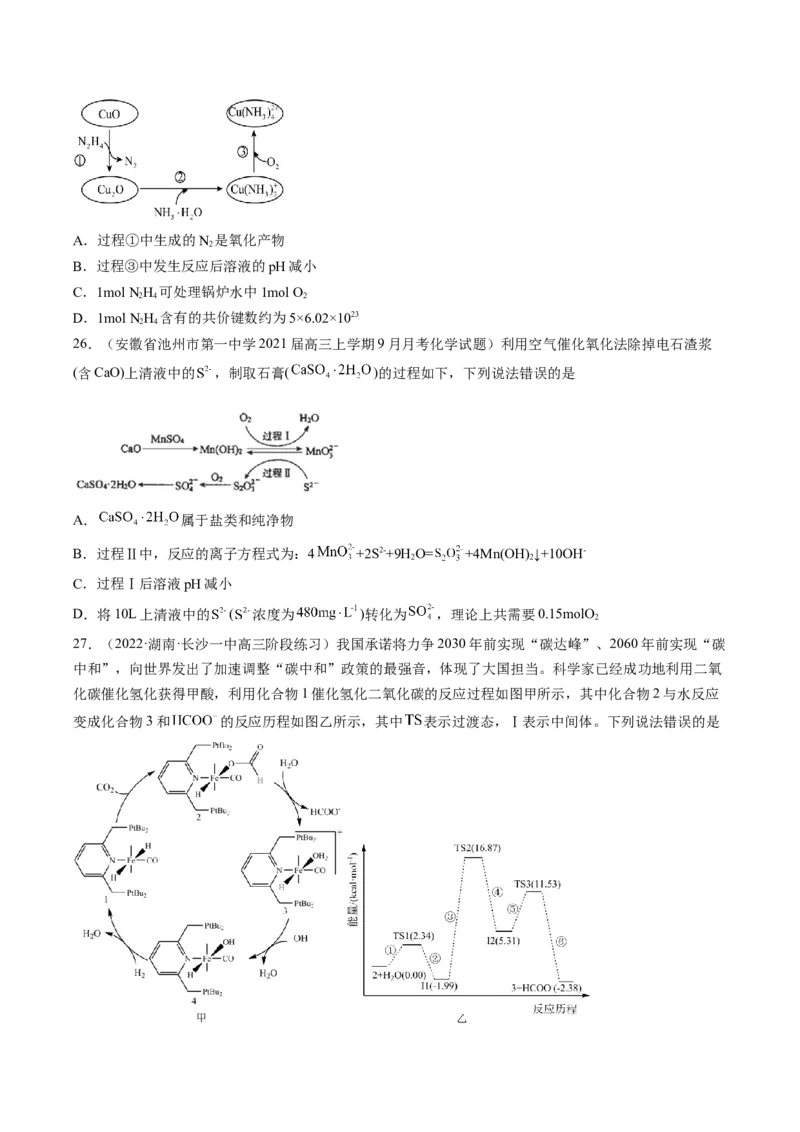
25.(重庆市实验中学2021届高三下学期三诊化学试题)联氨(N H)可用于处理锅炉水中的溶解氧,防止
2 4
锅炉被腐蚀,其中一种反应机理如图所示。下列叙述错误的是A.过程①中生成的N 是氧化产物
2
B.过程③中发生反应后溶液的pH减小
C.1mol NH 可处理锅炉水中1mol O
2 4 2
D.1mol NH 含有的共价键数约为5×6.02×1023
2 4
26.(安徽省池州市第一中学2021届高三上学期9月月考化学试题)利用空气催化氧化法除掉电石渣浆
(含CaO)上清液中的 ,制取石膏( )的过程如下,下列说法错误的是
A. 属于盐类和纯净物
B.过程Ⅱ中,反应的离子方程式为:4 +2S2-+9H O= +4Mn(OH) ↓+10OH-
2 2
C.过程Ⅰ后溶液pH减小
D.将10L上清液中的 ( 浓度为 )转化为 ,理论上共需要0.15molO
2
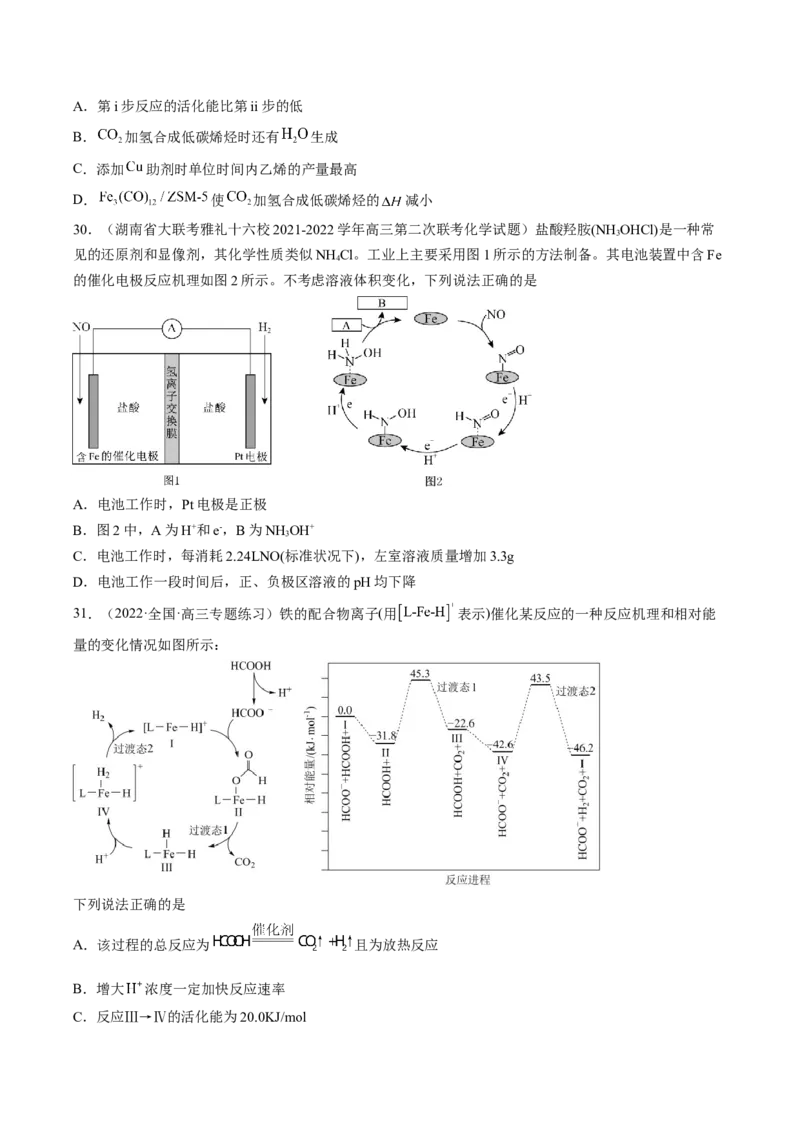
27.(2022·湖南·长沙一中高三阶段练习)我国承诺将力争2030年前实现“碳达峰”、2060年前实现“碳
中和”,向世界发出了加速调整“碳中和”政策的最强音,体现了大国担当。科学家已经成功地利用二氧
化碳催化氢化获得甲酸,利用化合物1催化氢化二氧化碳的反应过程如图甲所示,其中化合物2与水反应
变成化合物3和 的反应历程如图乙所示,其中 表示过渡态,Ⅰ表示中间体。下列说法错误的是A.图甲中, 原子的成键数一直没有改变
B.从平衡移动的角度看,降低温度可促进化合物2与水反应
C.图乙历程中最大能垒(活化能)
D.使用更高效的催化剂可以降低反应所需的活化能,从而提高二氧化碳的反应速率和平衡转化率
28.(2022·湖北·襄阳四中模拟预测)CrO 催化丙烷脱氢的反应路径如图所示,图中括号内的数值表示相
x
对能量、箭头上的数值表示能垒,单位为eV。下列说法错误的是
A.该催化循环过程不需要外界输入能量
B.该催化循环中经历了五个中间体
C.“M2 →M3”过程中形成配位键
D.该催化循环中Cr的成键数目发生变化
29.(2022·湖南郴州·一模)中科院兰州化学物理研究所用 催化 加氢合成低碳烯烃,
反应过程如下图。在其他条件相同时,添加不同助剂(催化剂中添加助剂 、 或 后可改变反应的选
择性),经过相同时间后测得 的转化率和各产物的物质的量分数如下表。
各产物的物质的量分数/%
助剂 的转化率/%
其他
42.5 35.9 39.6 24.5
27.2 75.6 22.8 1.6
9.8 80.7 12.5 6.8
下列说法正确的是A.第i步反应的活化能比第ii步的低
B. 加氢合成低碳烯烃时还有 生成
C.添加 助剂时单位时间内乙烯的产量最高
D. 使 加氢合成低碳烯烃的 减小
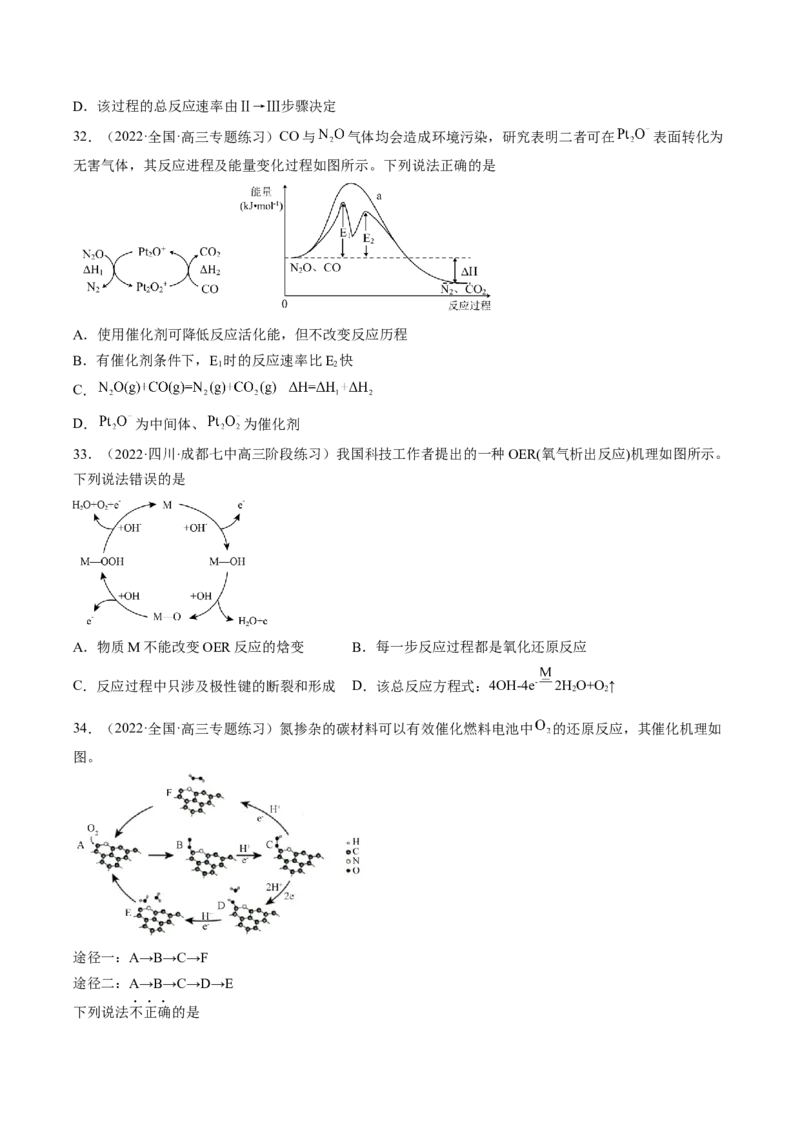
30.(湖南省大联考雅礼十六校2021-2022学年高三第二次联考化学试题)盐酸羟胺(NH OHCl)是一种常
3
见的还原剂和显像剂,其化学性质类似NH Cl。工业上主要采用图1所示的方法制备。其电池装置中含Fe
4
的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
A.电池工作时,Pt电极是正极
B.图2中,A为H+和e-,B为NH OH+
3
C.电池工作时,每消耗2.24LNO(标准状况下),左室溶液质量增加3.3g
D.电池工作一段时间后,正、负极区溶液的pH均下降
31.(2022·全国·高三专题练习)铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能
量的变化情况如图所示:
下列说法正确的是
A.该过程的总反应为 且为放热反应
B.增大 浓度一定加快反应速率
C.反应Ⅲ→Ⅳ的活化能为20.0KJ/molD.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
32.(2022·全国·高三专题练习)CO与 气体均会造成环境污染,研究表明二者可在 表面转化为
无害气体,其反应进程及能量变化过程如图所示。下列说法正确的是
A.使用催化剂可降低反应活化能,但不改变反应历程
B.有催化剂条件下,E 时的反应速率比E 快
1 2
C.
D. 为中间体、 为催化剂
33.(2022·四川·成都七中高三阶段练习)我国科技工作者提出的一种OER(氧气析出反应)机理如图所示。
下列说法错误的是
A.物质M不能改变OER反应的焓变 B.每一步反应过程都是氧化还原反应
C.反应过程中只涉及极性键的断裂和形成 D.该总反应方程式:4OH-4e- 2HO+O↑
2 2
34.(2022·全国·高三专题练习)氮掺杂的碳材料可以有效催化燃料电池中 的还原反应,其催化机理如
图。
途径一:A→B→C→F
途径二:A→B→C→D→E
下列说法不正确的是A.途径一中存在极性共价键的断裂与形成
B.途径一的电极反应是
C.途径二,1mol 得到4mol
D.氮掺杂的碳材料降低了反应的焓变
35.(2022·全国·高三专题练习)CO 催化加氢制CO技术是兼顾新能源和实现碳达峰的重要途径之一,该
2
反应机理如图所示。下列说法错误的是
A.反应CO(g)+H(g) CO(g)+HO(g) ΔH达到平衡后,若升温,c(H )降低,则ΔH>0
2 2 2 2
B.催化剂表面易于形成氧空位,有效促进CO 的吸附活化
2
C.图中的a、b、c、d、e五个步骤中,每个步骤都有化学键的断裂与形成
D.催化剂(InO)能加快催化加氢的速率,是因为降低了反应的活化能
2 3
36.(2021·湖南省临澧县第一中学高三阶段练习)某种含二价铜微料 催化剂可用于汽车尾
气脱硝,催化机理如图1,反应历程中不同状态物质体系所含的能量如图2。
下列说法正确的是
A. 可加快脱硝速率,提高平衡转化率
B.状态②到状态③的变化过程中有极性键的断裂与形成
C.状态④到状态⑤的变化过程决定了整个历程的反应速率
D.在图1所示历程中铜元素的化合价未发生变化
37.(2022·全国·高三专题练习) 加氢耦合苯胺( )的一种反应机理如下图所示。下列叙述不正确
的是A.金属Au可吸附H原子, 可吸附
B.反应过程中N的成键数目保持不变
C.反应过程中 发生还原反应
D.该过程的总反应:
38.(2022·重庆市第十一中学校高三阶段练习)下图是工业上以含铑元素(Rh)的化合物RhH(CO)(PPh ) 作
3 2
催化剂获取直链醛的催化循环示意图,其中Ph表示苯基,下列叙述错误的是
A.A是催化剂,B、C、D、E都是中间产物
B.在反应过程中,铑元素(Rh)的成键数目发生了变化
C.获取直链醛时,使用RhH(CO)(PPh ) 作催化剂可以降低反应的活化能,从而提高反应速率及反应物的
3 2
平衡转化率
D.工业上可以利用此方法,以丙烯为原料合成丁醛
39.(2022·浙江·高三开学考试)铑的配合物离子可催化甲醇羧基化,反应过程如图所示,下列叙述错误
的是A. 是反应中间体, 能提升催化效果
B.甲醇羰基化反应为:
C.Ⅱ、Ⅲ中Rh的成键数目不相同
D.铑的配合物离子Ⅱ是催化剂
40.(2022·北京东城·高三期末) 与 能发生反应: 。
已知:
①该反应由两个基元反应分步完成,第一步为
②两步反应的活化能分别为 、 ,且
下列判断不正确的是
A.第一步为氧化还原反应
B.第一步的化学反应速率大于第二步的化学反应速率
C.已知键能: ,可推知键能:
D.第二步的热化学方程式为
41.(2022·浙江·高三专题练习)有机小分子催化多氟代物的取代反应,机理如图所示,已知反应Ⅰ、反
应Ⅱ和反应Ⅲ的活化能中,反应Ⅱ的活化能最大。下列说法不正确的A.反应方程式为: + → +
B.2是催化剂,4和7都是反应中间体
C.5为 时,1是
D.整个取代反应的反应速率主要由反应Ⅱ的速率决定
42.(2021·河北·石家庄二中高三期中)我国科学家已成功将CO 催化氢化获得甲酸,利用化合物1催化
2
CO 氢化的反应过程如图甲所示,其中化合物2与HO反应生成化合物3,化合物3与HCO -的反应历程如
2 2 3
图乙所示,其中TS表示过渡态,I表示中间体。下列说法正确的是
A.化合物1到化合物2的过程中存在碳氧键的断裂和碳氧键的形成
B.该历程中最大能垒(活化能)E =16.87kcal·mol-1
正
C.使用更高效的催化剂可降低反应所需的活化能。最终提高CO 的转化率
2
D.从平衡移动的角度看,升高温度,可促进化合物2与HO反应生成化合物3与HCOO-
2
43.(2022·河北·高三阶段练习·多选)CO 的综合利用是实现“双碳”的重要手段。利用钌(Ru)基催化剂
2
将CO 转化为有机原料甲酸的反应机理如图所示。下列说法错误的是
2
A.反应II为决速步骤,所以反应II的活化能最低B.水是该反应的中间产物
C.该反应的总方程式:
D.反应过程中既有极性键的生成,又有非极性键的生成
44.(山东省淄博市2022届高三下学期第一次模拟考试化学试题·多选)分子中每个手性碳原子可形成一
对旋光异构体。具有生物降解性能的聚碳酸丙烯酯( )可由碳酸丙烯酯(
)聚合而成。用环氧丙烷( )与CO 催化环加成反应生成碳酸丙
2
烯酯的反应机理如图。下列说法错误的是
A.酸丙烯酯中的π键与σ键数目比为1∶7
B.聚合生成聚碳酸丙烯酯反应中原子利用率是100%
C.环氧丙烷与CO 反应的催化剂为 和I-
2
D.考虑旋光异构现象,环氧丙烷的一氯代物有6种
45.(2022·辽宁实验中学模拟预测·多选)均相芬顿反应原理是高级氧化技术的经典工艺之一,如图所示(
和 为速率常数)。下列说法错误的是
A.相同条件下,基元反应Ⅰ比Ⅱ的活化能低
B.基元反应Ⅰ中氧元素的化合价没有发生变化
C.基元反应Ⅱ的化学方程式为D.芬顿反应进行的过程中,整个体系的 几乎不变(忽略体积变化)
46.(2022·湖南师大附中高三阶段练习·多选)H 在石墨烯负载型Pd单原子催化剂(Pd/SVG)上还原NO生
2
成N 和NH 的路径机理及活化能(kJ·mol–1)如图所示。下列说法错误的是
2 3
A.H 还原NO生成N 的决速步为反应⑥
2 2
B.Pd/SVG上H 还原NO,更容易生成N
2 2
C.根据如图数据可计算NO+5H=NH +H O的ΔH
3 2
D.由图可知,相同催化剂条件下反应可能存在多种反应历程
47.(2022·河北秦皇岛·模拟预测·多选)RRhI(-R为烃基)催化CO 加氢制羧酸(RCOOH)的反应机理如图所
2
示。
下列说法正确的是
A.总反应的原子利用率为100%
B.上述历程中断裂和形成了极性键
C.反应abcde均是氧化还原反应
D.RRhI降低了CO 加氢反应的活化能
2
48.(2022·山东潍坊·高三期末·多选)溴分子易极化,使分子内溴原子分别带部分正电荷和部分负电荷。
在一定条件 下CH=CH-CH=CH 与Br 发生加成反应会得到两种产物,且两种产物可通过
2 2 2
互相转化,反应历程可表示为:CH =CHCHBrCH Br与CHBrCH =CHCH Br相互转化的能量变化如下图所示。已知,同一反应在不同温
2 2 2 2
度下反应速率常数与活化能的关系如下: (其中R为常数)。下列叙述错误的是
A.相同条件下,反应i的速率比反应ii快
B.升高反应温度,更有利于CH = CHCHBrCH Br的生成
2 2
C.反应CH =CHCHBrCH Br(s) →CH BrCH =CHCH Br(s)的ΔH=E +E -E –E
2 2 2 2 a4 a2 a1 a3
D.相同条件下,反应达平衡后产物中CH BrCH = CHCH Br含量更大
2 2
49.(2022·湖南·衡阳市八中高三阶段练习)中国科学家研究在Pd/SVG催化剂上H 还原NO生成N 和
2 2
NH 的路径,各基元反应及活化能E(kJ·mol﹣1)如图所示,下列说法正确的是
3 a
A.生成NH 的各基元反应中,N元素均被还原
3
B.在Pd/SVG催化剂上,NO更容易被H 还原为N
2 2
C.决定NO生成NH 速率的基元反应为NH NO → NHNOH
3 2
D.生成NH 的总反应方程式为2NO+5H 2NH +2H O
3 2 3 2