文档内容
第二篇 元素及其化合物
专项 12 碳达峰与碳中和
2020年我国首次提出:“中国将提高国家自主贡献力度,采取更加有力的政策和措施,二氧化碳排放
力争于2030年前达到峰值,努力争取2060年前实现碳中和。”专家指出:气候变化是人类面临的全球性
问题,随着各国二氧化碳排放,温室气体猛增,对生命系统形成威胁。在这一背景下,世界各国以全球协
约的方式减排温室气体,我国由此提出碳达峰和碳中和目标。
碳达峰:就是指在某一个时点,二氧化碳的排放不再增长达到峰值,之后逐步回落。
碳中和:是指国家、企业、产品、活动或个人在一定时间内直接或间接产生的二氧化碳或温室气体排
放总量,通过植树造林、节能减排等形式,以抵消自身产生的二氧化碳或温室气体排放量,实现正负抵消,
达到相对“零排放”。
1.(2021•海南选择性考试) 2020年9月22日,中国向全世界宣布,努力争取2060年前实现碳中和。
下列措施不利于大气中CO 减少的是( )
2
A.用氨水捕集废气中的CO,将其转化为氮肥
2
B.大力推广使用风能、水能、氢能等清洁能源
C.大力推广使用干冰实现人工增雨,缓解旱情
D.通过植树造林,利用光合作用吸收大气中的CO
2
【答案】C
【解析】A项,氨水能与酸性氧化物二氧化碳反应生成碳酸铵或碳酸氢铵,则用氨水捕集废气中的二
氧化碳,将其转化为氮肥有利于大气中二氧化碳的减少,故A不符合题意;B项,大力推广使用风能、水
能、氢能等清洁能源可以减少化石能源的使用,从而减少二氧化碳气体的排放,有利于大气中二氧化碳的
减少,故B不符合题意;C项,大力推广使用干冰实现人工增雨,会增加大气中二氧化碳的量,不利于大
气中二氧化碳的减少,故C符合题意;D项,通过植树造林,利用光合作用吸收大气中的二氧化碳有利于
大气中二氧化碳的减少,故D不符合题意;故选C。
2.(2021•全国乙卷)我国提出争取在2030年前实现碳达峰,2060年实现碳中和,这对于改善环境,实现绿色发展至关重要。碳中和是指CO 的排放总量和减少总量相当。下列措施中能促进碳中和最直接有效
2
的是( )
A.将重质油裂解为轻质油作为燃料 B.大规模开采可燃冰作为新能源
C.通过清洁煤技术减少煤燃烧污染 D.研发催化剂将CO 还原为甲醇
2
【答案】D
【解析】A项,将重质油裂解为轻质油并不能减少二氧化碳的排放量,达不到碳中和的目的,故A不
符合题意; B项,大规模开采可燃冰做为新能源,会增大二氧化碳的排放量,不符合碳中和的要求,故B
不符合题意;C项,通过清洁煤技术减少煤燃烧污染,不能减少二氧化碳的排放量,达不到碳中和的目的,
故C不符合题意;D项,研发催化剂将二氧化碳还原为甲醇,可以减少二氧化碳的排放量,达到碳中和的
目的,故D符合题意;故选D。
3.(2021•河北选择性考试)当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧
化碳利用技术,降低空气中二氧化碳含量成为研究热点。
(1)大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热
数据如表:
物质 H(g) C(石墨,s) C H(l)
2 6 6
燃烧热△H(kJ•mol-1) -285.8 -393.5 -3267.5
(1)则25℃时H(g)和C(石墨,s)生成C H(l)的热化学方程式为________。
2 6 6
(2)雨水中含有来自大气的CO,溶于水中的CO 进一步和水反应,发生电离:
2 2
①CO(g)=CO (aq)
2 2
②CO(aq)+H O(l)=H+(aq)+HCO-(aq)
2 2 3
25℃时,反应②的平衡常数为K 。
2
溶液中CO 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为
2
ymol•L-1•kPa-1,当大气压强为pkPa,大气中CO(g)的物质的量分数为x时,溶液中H+浓度为
2
________mol•L-1(写出表达式,考虑水的电离,忽略HCO -的电离)
3
(3)105℃时,将足量的某碳酸氢盐(MHCO )固体置于真空恒容容器中,存在如下平衡:2MHCO (s)
3 3
MCO(s)+HO(g)+CO(g)。上述反应达平衡时体系的总压为46kPa。
2 3 2 2
保持温度不变,开始时在体系中先通入一定量的CO(g),再加入足量MHCO (s),欲使平衡时体系中
2 3
水蒸气的分压小于5kPa,CO(g)的初始压强应大于________kPa。
2
(4)我国科学家研究Li—CO 电池,取得了重大科研成果,回答下列问题:
2
①Li—CO 电池中,Li为单质锂片,则该电池中的CO 在___(填“正”或“负”)极发生电化学反应。
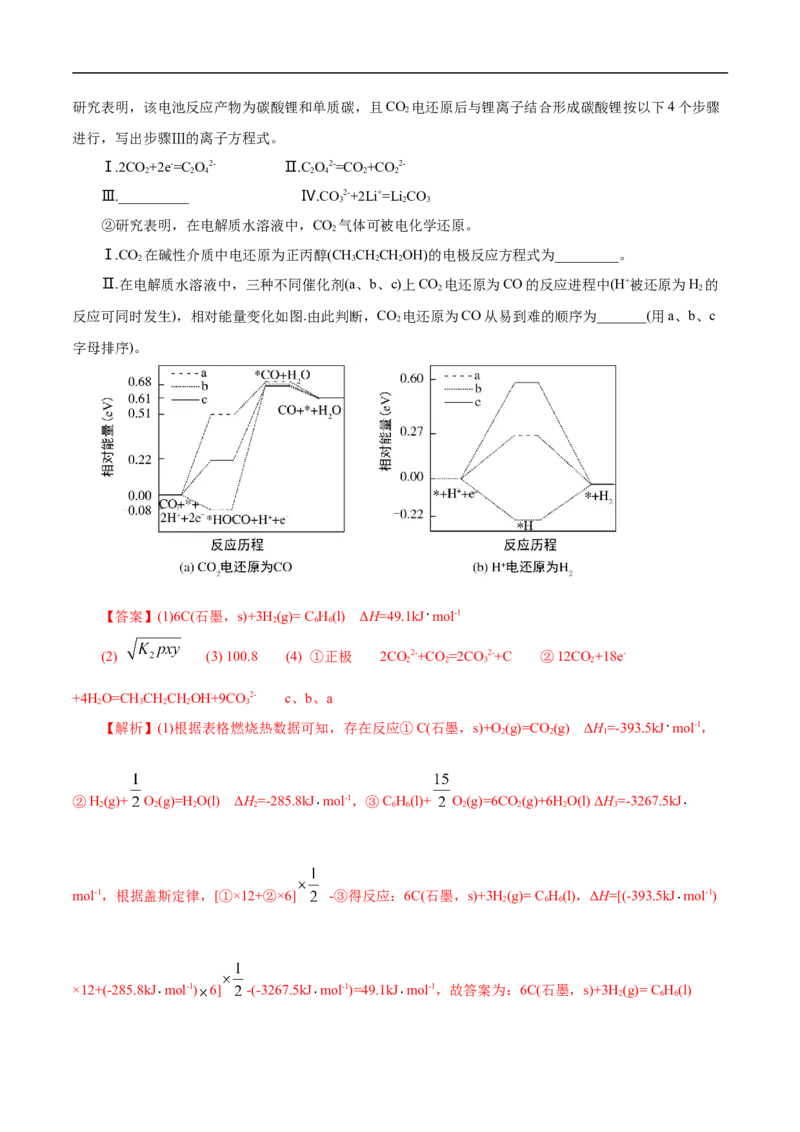
2 2研究表明,该电池反应产物为碳酸锂和单质碳,且CO 电还原后与锂离子结合形成碳酸锂按以下4个步骤
2
进行,写出步骤Ⅲ的离子方程式。
Ⅰ.2CO +2e-=C O2- Ⅱ.C O2-=CO +CO 2-
2 2 4 2 4 2 2
Ⅲ.__________ Ⅳ.CO 2-+2Li+=Li CO
3 2 3
②研究表明,在电解质水溶液中,CO 气体可被电化学还原。
2
Ⅰ.CO 在碱性介质中电还原为正丙醇(CHCHCHOH)的电极反应方程式为_________。
2 3 2 2
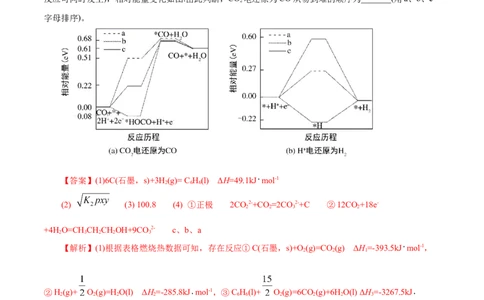
Ⅱ.在电解质水溶液中,三种不同催化剂(a、b、c)上CO 电还原为CO的反应进程中(H+被还原为H 的
2 2
反应可同时发生),相对能量变化如图.由此判断,CO 电还原为CO从易到难的顺序为_______(用a、b、c
2
字母排序)。
【答案】(1)6C(石墨,s)+3H(g)= C H(l) ΔH=49.1kJ mol-1
2 6 6
(2) (3) 100.8 (4) ①正极 2CO2-+CO =2CO 2-+C ②12CO+18e-
2 2 3 2
+4H O=CHCHCHOH+9CO 2- c、b、a
2 3 2 2 3
【解析】(1)根据表格燃烧热数据可知,存在反应①C(石墨,s)+O(g)=CO (g) ΔH=-393.5kJ mol-1,
2 2 1
②H(g)+ O(g)=HO(l) ΔH=-285.8kJ mol-1,③C H(l)+ O(g)=6CO (g)+6HO(l) ΔH=-3267.5kJ
2 2 2 2 6 6 2 2 2 3
mol-1,根据盖斯定律,[①×12+②×6] -③得反应:6C(石墨,s)+3H(g)= C H(l),ΔH=[(-393.5kJ mol-1)
2 6 6
×12+(-285.8kJ mol-1) 6] -(-3267.5kJ mol-1)=49.1kJ mol-1,故答案为:6C(石墨,s)+3H(g)= C H(l)
2 6 6ΔH=49.1kJ mol-1;(2)由题可知,①CO(s) CO(aq),②CO(aq)+H O(l) H+(aq)+HCO- (aq),
2 2 2 2 3
K = ,又因为p(CO)=p(kPa) x,则c(CO)=y(mol•L-1•kPa-1)p(CO )=p x y mol/L,在忽略
2 2 2 2
HCO -的电离时,c(H+)=c(HCO-),所以可得c(H+)= ,故答案为: ;(3)2MHCO(s)
3 3 3
MCO(s)+HO(g)+ CO (g),等温等容条件下,压强之比等于物质的量之比,可用分压表示物质的量
2 3 2 2
浓度,平衡常数K = = =529kPa2。温度不变化学平衡常数K 不变,设平衡时,平
p p
衡体系中CO 的分压为x,则K= = 529kPa2, = kPa=105.8kPa,CO 的初始压强等于平
2 2
衡压强减去碳酸氢盐分解产生的CO 的分压,即CO(g)的初始压强应大于105.8kPa-5kPa=100.8kPa;(4)①
2 2
由题意知,Li-CO 电池的总反应式为:4Li+3CO=2Li CO+C,CO 发生得电子的还原反应,则CO 作为电
2 2 2 3 2 2
池的正极;CO 还原后与Li+结合成LiCO,按4个步骤进行,由步骤II可知生成了CO2-,而步骤IV需要
2 2 3 2
CO2-参加反应,所以步骤III的离子方程式为:2 CO 2-+CO =2 CO2-+C;②I.CO 在碱性条件下得电子生成
3 2 2 3 2
CHCHCHOH,根据电子守恒和电荷守恒写出电极反应式为:12CO+18e-+4H O=CHCHCHOH+9
3 2 2 2 2 3 2 2
CO2-;II.c催化剂条件下,CO 电还原的活化能小于H+电还原的活化能,更容易发生CO 的电还原;而催
3 2 2
化剂a和b条件下,CO 电还原的活化能均大于H+电还原的活化能,相对来说,更易发生H+的电还原。其
2
中a催化剂条件下,H+电还原的活化能比CO 电还原的活化能小的更多,发生H+电还原的可能性更大,因
2
此反应从易到难的顺序为c、b、a,故答案为:c、b、a。
4.(2021•广东选择性考试)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整
4 2
是CO 利用的研究热点之一。该重整反应体系主要涉及以下反应:
2
a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
b)CO(g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
c)CH(g) C(s)+2H(g) ∆H
4 2 3
d)2CO(g) CO(g)+C(s) ∆H
2 4
e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
(1)根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
A.增大CO 与CH 的浓度,反应a、b、c的正反应速率都增加
2 4
B.移去部分C(s),反应c、d、e的平衡均向右移动
C.加入反应a的催化剂,可提高CH 的平衡转化率
4
D.降低反应温度,反应a~e的正、逆反应速率都减小
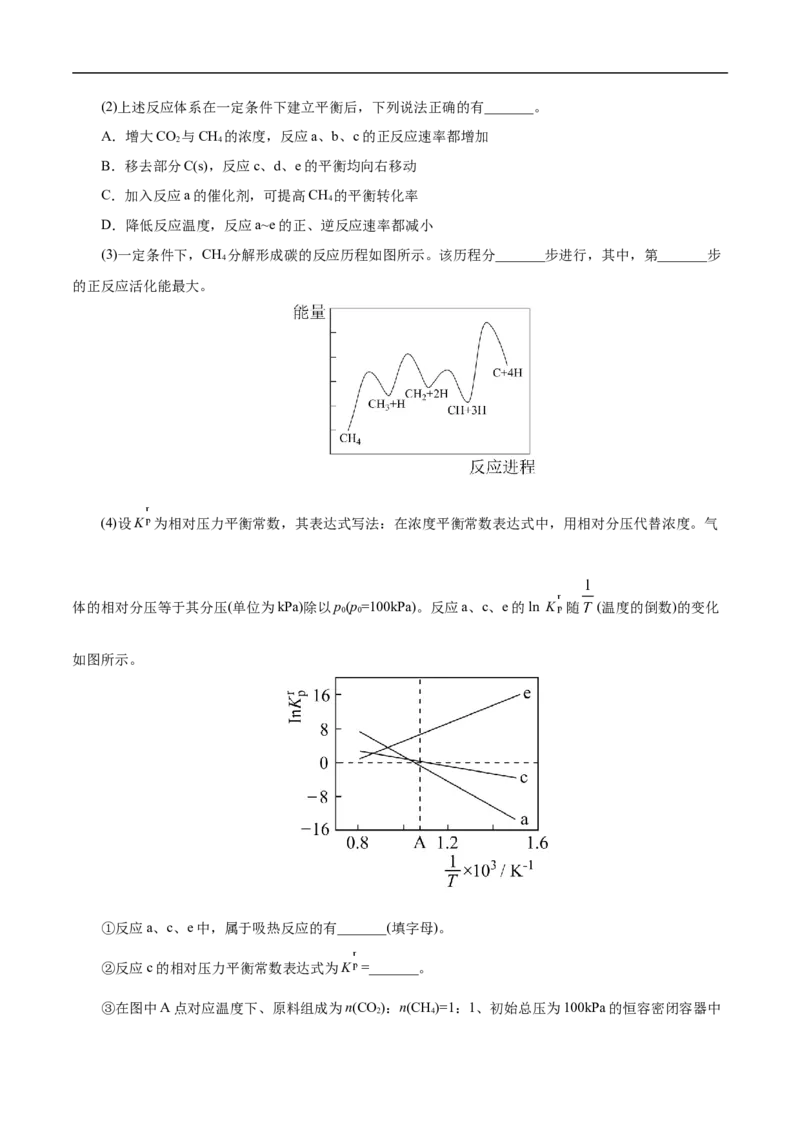
(3)一定条件下,CH 分解形成碳的反应历程如图所示。该历程分_______步进行,其中,第_______步
4
的正反应活化能最大。
(4)设K 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气
体的相对分压等于其分压(单位为kPa)除以p(p=100kPa)。反应a、c、e的ln K 随 (温度的倒数)的变化
0 0
如图所示。
①反应a、c、e中,属于吸热反应的有_______(填字母)。
②反应c的相对压力平衡常数表达式为K =_______。
③在图中A点对应温度下、原料组成为n(CO):n(CH)=1:1、初始总压为100kPa的恒容密闭容器中
2 4进行反应,体系达到平衡时H 的分压为40kPa。计算CH 的平衡转化率,写出计算过程_______。
2 4
(5)CO 用途广泛,写出基于其物理性质的一种用途:_______。
2
【答案】(1)∆H+∆H-∆H 或∆H-∆H (2)AD (3) 4 4
2 3 5 3 4
(4)①ac ② ③68% (5)做冷冻剂
【解析】(1)根据题目所给出的反应方程式关系可知,a=b+c-e=c-d,根据盖斯定律则有∆H=∆H+∆H-
1 2 3
∆H=∆H-∆H;(2)A项,增大CO 和CH 的浓度,对于反应a、b、c来说,均增大了反应物的浓度,反应
5 3 4 2 4
的正反应速率增大,A正确;B项,移去部分C(s),没有改变反应体系中的压强,反应的正逆反应速率均
不变,平衡不移动,B错误;C项,催化剂可以同等条件下增大正逆反应速率,只能加快反应进程,不改
变反应的平衡状态,平衡转化率不变,C错误;D项,降低温度,体系的总能量降低,正、逆反应速率均
减小,D正确;故选AD;(3)由图可知,反应过程中能量变化出现了4个峰,即吸收了4次活化能,经历
了4步反应;且从左往右看4次活化能吸收中,第4次对应的峰最高,即正反应方向第4步吸收的能量最
多,对应的正反应活化能最大。(4)①随着温度的升高,反应a和c的ln K 增大,说明K 的数值增大,反
应向正反应方向进行,反应a和c为吸热反应,同理反应e的ln K 减小,说明K 的减小,反应向逆反应
方向进行,反应e为放热反应,故答案为ac;②用相对分压代替浓度,则反应c的平衡常数表达式K =
;③由图可知,A处对应反应c的ln K =0,即K = =1,解方程的p2(H )=p(CH),
2 4
已知反应平衡时p(H )=40kPa,则有p(CH)=16kPa,且初始状态时p(CH)= ×100kPa=50kPa,故CH 的
2 4 4 4平衡转化率为 ×100%=68%;(5)固态CO 即为干冰,干冰用于制冷或人工降雨均是利用其物
2
理性质。
1.国家层面:
①用新工艺提高煤等传统能源的使用效率;减少传统能源的使用,增加清洁能源(光伏电、风能、水能
等)使用,调整能源结构。
②推动产业结构转型。
③重点领域节能减排。
④加速低碳技术研发推广应用。
⑤健全低碳发展体制机制;限定碳排放额;建立碳交易权市场。
⑥国家金融政策、财税政策支持。
⑦努力增加森林面积。
2.企业层面:
①加速研发低碳技术,实现创新发展,绿色发展;
②实现经济效益和生态效益相统一,注重承担社会责任。
3.公民层面:
优先选择公共交通;使用无纺布购物袋;使用节能灯;随手关闭电源;空调温度不高不低;纸张双面
打印;不浪费粮食;不使用一次性餐具等。
1.(2022·河南省十所名校高中毕业班尖子生高三第一次考试)2022年全国低碳日的活动主题是“落
实‘双碳’行动,共建美丽家园”。下列行为对碳达峰或碳中和没有促进作用的是( )
A.推进风力发电、光伏发电 B.资源化利用二氧化碳
C.将燃煤进行脱硫脱硝 D.植树造林、节能减排
【答案】C
【解析】A项,推进风力发电、光伏发电,可减少煤炭的使用,从而减少大气中二氧化碳的排放,A
不符合题意;B项,资源化利用二氧化碳,可减少大气中二氧化碳的排放,同时减少其他资源的使用,有
利于节能减排,B不符合题意;C项,将燃煤进行脱硫脱硝,可减少大气中二氧化硫及氮氧化物排放,但没有减少大气中二氧化碳的排放,对碳达峰或碳中和没有促进作用,C符合题意;D项,植树造林、节能
减排,有利于大气中二氧化碳的转化与利用,从而减少大气中二氧化碳的含量,有利于促进碳达峰或碳中
和,D不符合题意;故选C。
2.(2023届·山东省名校联盟高三第一次学业质量联合检测)化学与生活、科技、社会发展息息相关。
下列说法错误的是( )
A.利用CO 合成乙酸、聚碳酸酯塑料,有利于实现“碳达峰、碳中和”
2
B.在生产新冠灭活疫苗的过程中,如果温度过高会使病毒失去生理活性
C.植物油与SO 均可使溴水褪色,二者反应原理相同
2
D.我国航空母舰上的阻拦索由钢绳缠绕在特制高分子材料上制作而成,阻拦索属于复合材料
【答案】C
【解析】A项,利用CO 合成乙酸、聚碳酸酯塑料,能减少二氧化碳的排放,有利于实现“碳达峰、
2
碳中和”,A正确;B项,加热、紫外线照射、重金属盐等均可以杀死病毒,使其失去生理活性,B正确;
C项,植物油中含有碳碳双键,能与溴单质发生加成反应,SO 有还原性,能被溴单质氧化,二者反应原
2
理不同,C错误;D项,复合材料是运用先进的材料制备技术将不同性质的材料组分优化组合而成的新材
料,阻拦索由钢绳缠绕在特制高分子材料上制作而成,属于复合材料,D正确;故选C。
3.(2023届·湖北省新高考协作体高三起点考试)我国力争于2030年前做到“碳达峰”,2060年前实现
“碳中和”,一种脱除和利用水煤气中CO 方法的示意图如下:T℃时一定量的CO 被吸收塔中KCO 溶
2 2 2 3
液吸收后进入再生塔再生,最后利用电化学原理将CO 电催化还原为C H(该温度下HCO 的
2 2 4 2 3
, )。下列有关说法错误的是( )
A.若T℃时吸收塔中,c(CO2-):c(CO2-)=28:5,则该溶液的pH=11
3 3
B.再生塔中产生CO 的离子方程式为2HCO - CO↑+CO 2-+H O2HCO - CO↑+CO 2-+H O
2 3 2 3 2 3 2 3 2C.将浓度相等的KCO 溶液与KHCO 溶液等体积混合,所得溶液中离子浓度大小为:c(K+)>
2 3 3
c(CO2-)>c(HCO -)>c(OH-)>c(H+)
3 3
D.CO 电催化还原为C H 的阴极反应式为2CO+12e-+12H+=C H+4H O和AgCl+e-=Ag+Cl-
2 2 4 2 2 4 2
【答案】C
【解析】水煤气中的CO 被吸收塔中KCO 溶液吸收后形成KHCO 溶液并进入再生塔,再生塔中
2 2 3 3
KHCO 分解产生释放CO,再将CO 电催化还原为C H。A项,设c(CO2-)=2.8mol/L,则
3 2 2 2 4 3
c(HCO -)=0.5mol/L,根据CO2-+H O HCO -+OH-可知, ,则
3 3 2 3
,解得c(OH-)=1.010-3mol/L,溶液中c(H+)=1.010-11mol/L,pH=11,A正确;
B项,再生塔中,KHCO 受热分解产生CO,该反应的离子方程式为2HCO - CO↑+CO 2-+H O,B正确;
3 2 3 2 3 2
C项,将浓度相等的KCO 溶液与KHCO 溶液等体积混合,HCO 的电离平衡常数K >K ,则CO2-的水
2 3 3 2 3 a1 a2 3
解程度大于HCO -,故所得溶液中离子浓度大小为c(K+)>c(HCO -)>c(CO2-)>c(OH-)>c(H+),C错误;D
3 3 3
项,CO 在阴极上被还原为C H,电极反应式为2CO+12e-+12H+=C H+4H O和AgCl+e-=Ag+Cl-,D正确;
2 2 4 2 2 4 2
故选C。
4.(2022•广东省复习调研考试)“碳中和”是指一定时期内,二氧化碳排放量与吸收量相平衡的状态.
下列“碳中和”的方法中未涉及氧化还原反应的是( )
A.高温CaO基吸附剂循环捕获CO
2
B.植树造林捕获和储存大气中的CO
2
C.高选择性氧化铟基催化剂将CO 加氢转化为CHOH
2 3
D.在常温、常压条件下电催化将CO 转化为CO、HCOOH
2
【答案】A
【解析】绿色植物吸收CO 的同时放出O ,属氧化还原反应,B项不符合题意;由CO 制甲醇时,
2 2 2
CO 被还原,C项不符合题意;CO 中碳为+4价,CO及HCOOH中碳均为+2价,属于氧化还原反应,
2 2
D项不符合题意。
5.(2022•河南九师联盟检测)我国提出争取在2030年前实现碳达峰、2060年前实现碳中和,这对于改
善环境、实现绿色发展至关重要。CO 催化加氢制CO技术是兼顾新能源和实现碳达峰的重要途径之一,
2
该反应机理如图所示。下列说法错误的是( )A.反应:CO(g)+H(g) CO(g)+HO(g) H,达平衡后,若升温,c(H)降低,则△H>0
2 2 2 2
B.催化剂(In
2
O
3
)表面易于形成丰富的氧空位,有△效促进CO
2
的吸附活化
C.步骤d、e中,CO 的吸附与转化均存在化学键的断裂与形成
2
D.催化剂(InO)能提高催化加氢的速率,是因为降低了反应的活化能
2 3
【答案】C
【解析】对转化反应,升温c(H )降低,说明平衡向正向移动,则说明正反应△H>0,A正确;观察
2
反应机理图可知,催化剂先吸附氢气、氢原子与氧成键后脱水,得到较多的氧空位,促进了CO 的吸附活
2
性,B正确;步骤d中,CO 只是进入氧空位被催化剂吸附,不存在化学键的断裂与形成;步骤 e中,CO
2 2
是断裂一半碳氧双键,同时形成一半碳氧三键,C错误;InO 作催化剂是降低了反应的活化能,从而提高
2 3
化学反应速率,D正确。
6.(2022•湖南永州重点中学联考)第十三届全国人民代表大会第四次会议政府工作报告指出“要扎实
做好碳达峰、碳中和各项工作”,绿色氢能和液态阳光甲醇可助力完成碳中和目标。下列说法正确的是(
)
A.CHOH属于电解质
3
B.用焦炭与HO反应是未来较好获取氢能的方法
2
C.H 与CO 反应,每生成1molCH OH时转移4mol电子
2 2 3
D.植树造林、节能减排等有利于实现碳中和
【答案】D
【解析】CHOH无论熔融还是水溶液均不能导电,为非电解质,A错误;用焦炭与HO反应能源损耗
3 2
过高,不是未来较好获取氢能的方法,B错误;H 与CO 反应,每生成1molCH OH时转移6mol电子,C
2 2 3
错误;植树造林、节能减排等,可以减少CO 排放总量,有利于实现碳中和,D正确。
2
7.(2022•山东部分学校第一次质量检测)碳中和是指CO 排放总量和减少总量相当。我国提出在2060
2
年前实现碳中和,这对于改善环境实现绿色发展至关重要。下列措施中不能实现碳中和的是( )A.煤炭作燃料时先进行脱硫处理 B.以CO 和H 为原料生产碳氢合成燃料
2 2
C.研发能够高效利用CO 的新型电池 D.加大新技术在碳捕捉、应用与储存等领域的运用
2
【答案】A
【解析】煤炭作燃料时进行脱硫处理,可以减少SO 等污染物的排放,并不能减少CO 的排放总量,
2 2
A项符合题意;以CO 和H 为原料生产碳氢合成燃料可以减少CO 的排放总量,B项不符合题意;研发能
2 2 2
够高效利用CO 的新型电池可以减少CO 的排放总量,C项不符合题意;加大新技术在碳捕捉、应用与储
2 2
存等领域的运用,可以减少CO 的排放总量并使CO 被有效利用,D项不符合题意。
2 2
8.(2022•河南高三模拟考试)我国提出争取在2030年前实现碳达峰,2060年前实现碳中和。这对于改
善环境,实现绿色发展至关重要。“碳中和”是指CO 的排放总量和减少总量相当。下列措施中能最直接
2
有效地促进碳中和的是( )
A.研发催化剂将CO 还原为甲醇
2
B.不再使用化石燃料,改用薪柴
C.通过清洁煤技术减少煤燃烧产生的污染
D.通过将来源广泛的水电解获得氢气,从而推广使用氢燃料电池
【答案】A
【解析】薪柴燃烧同样会释放出大量的CO ,B项不符合题意;清洁煤技术主要减少了含硫等大气污
2
染物的排放,对CO 的排放影响不大,C项不符合题意;电解水会消耗大量的电能,同样会排放大量的
2
CO,D项不符合题意。
2
9.(2022•河南部分名校摸底联考)我国力争在2060年前实现碳中和,即二氧化碳排放量“收支相抵”。
下列做法对促进碳中和没有直接效果的是( )
A.有机化工生产中原子利用率达到100% B.用可燃冰代替煤作燃料
C.大力开发新能源代替传统的化石燃料 D.在煤中加石灰石降低污染气体的排放
【答案】D
【解析】有机化工生产中原子利用率达到100%是绿色化学理念,可促进碳中和,A项正确;可燃冰
代替煤可降低二氧化碳的排放量,B项正确;新能源代替传统的化石燃料可减少二氧化碳的排放,C项正
确;煤中加入石灰石可减少SO 排放,但不能减少二氧化碳的排放,D项错误。
2
10.(2022•陕西渭南月考)我国力争于2030年前做到碳达峰,2060年前实现碳中和。甲醇是重要的化
工原料。利用合成气(主要成分为CO、CO 和H)在催化剂的作用下合成甲醇,可能发生的反应如下:
2 2
ⅰ.CO (g)+3H(g) CHOH(g)+HO(g) ΔH
2 2 3 2 1
ⅱ.CO (g)+H(g) CO(g)+HO(g) ΔH
2 2 2 2
ⅲ.CH OH(g) CO(g)+2H(g) ΔH
3 2 3回答下列问题:
(1)已知反应ⅱ中相关化学键键能数据如下:
化学键 H—H C===O C O H—O
E/(kJ·mol-1) 436 803 1 076 465
由此计算ΔH=________kJ·mol-1。已知ΔH=+99 kJ·mol-1,则ΔH=________kJ·mol-1。
2 3 1
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性
与温度的关系如图1所示。
①温度为470 K时,图中P点________(填“是”或“不是”)处于平衡状态。在490 K之前,甲醇产率
随着温度升高而增大的原因是______________________________;
490 K之后,甲醇产率下降的原因是__________________________________________。
②一定能提高甲醇产率的措施是________(填字母)。
A.增大压强 B.升高温度 C.选择合适催化剂 D.加入大量催化剂
(3)图2为一定比例的CO/H 、CO/H、CO/CO/H 条件下甲醇生成速率与温度的关系。
2 2 2 2 2
①490 K时,根据曲线a、c判断合成甲醇的反应机理是________(填“Ⅰ”或“Ⅱ”)。
Ⅰ.CO CO CHOH
2 3
Ⅱ.CO CO CHOH+HO
2 3 2
②490 K时,曲线a与曲线b相比,CO的存在使甲醇生成速率增大,从热力学与动力学角度,并结合
反应ⅰ、ⅱ分析原因:__________________________________________________。
【答案】(1)+36 -63
(2)①不是 温度越高化学反应速率越快 升高温度,反应ⅰ逆向移动、催化剂活性降低 ②A
(3)①Ⅱ ②CO促进反应ⅱ逆向移动,二氧化碳和氢气的量增加,水蒸气的量减少反应ⅰ正向移动
【解析】(1)CO (g)+H(g) CO(g)+HO(g) ΔH,反应热=反应物总键能-反应产物总键能,
2 2 2 2
故ΔH=(2×803+436)kJ·mol-1-(1 076+2×465)kJ·mol-1=+36 kJ·mol-1;根据盖斯定律由ⅱ-ⅲ=ⅰ,故
2
ΔH=ΔH-ΔH=+36 kJ·mol-1-(+99 kJ·mol-1)=-63 kJ·mol-1。(2)①温度为470 K时,图中P点不是处
1 2 3
于平衡状态。在490 K之前,甲醇产率随着温度升高而增大的原因是温度越高化学反应速率越快;490 K
之后,甲醇产率下降的原因是升高温度,反应ⅰ逆向移动、催化剂活性降低;②A项,增大压强,反应ⅰ平衡正向移动,正确;B项,由题图可知,温度高于490 K甲醇产率降低,错误;C项,选择合适催化剂,
反应生成甲醇,提高反应速率,但不影响甲醇产率,错误;D项,加入大量催化剂,不能影响平衡,错误。
(3)①490 K时,从甲醇的生成速率来看,a曲线大于c曲线,即甲醇来源于CO 和H,故490 K时,根据
2 2
曲线a、c判断合成甲醇的反应机理是Ⅱ;②490 K时,曲线a与曲线b相比,CO的存在使甲醇生成速率
增大,原因:对于反应ⅱ,CO是反应产物,CO促进反应ⅱ逆向移动,二氧化碳和氢气的量增加,水蒸气
的量减少,反应ⅰ正向进行,故CO的存在使甲醇生成速率增大。
11.(2022·江西省景德镇市二模)清洁能源的综合利用可有效降低碳排放,是实现“碳中和、碳达
峰"的重要途径。
(1)以环己烷为原料通过芳构化反应生产苯,同时可获取氢气。图甲是该反应过程中几种物质间的能量
关系。
芳构化反应: ΔH=_______kJ/mol。
(2)H 和CO 合成乙醇反应为: 2CO(g)+6H(g) C HOH(g)+3H O(g)。 将等物质的量的CO 和H 充
2 2 2 2 2 5 2 2 2
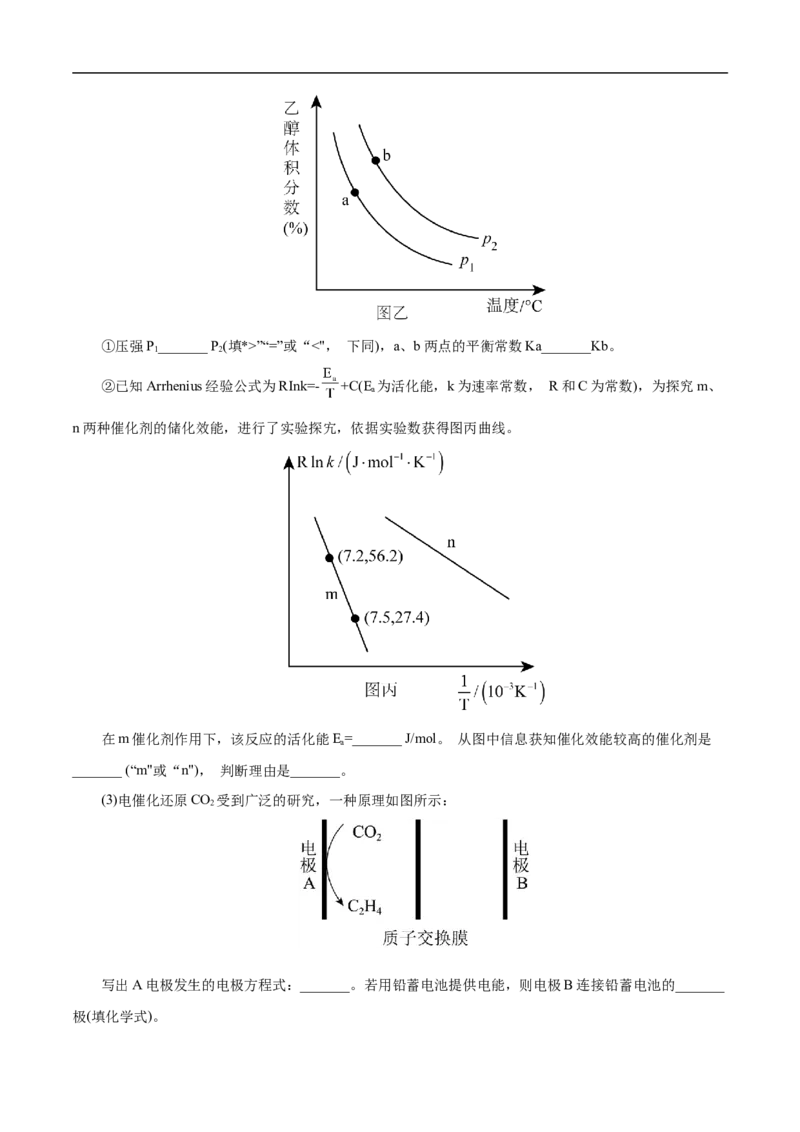
入一刚性容器中,测得平衡时乙醇的体积分数随温度⇌和压强的关系如图乙。①压强P_______ P (填*>”“=”或“<", 下同),a、b两点的平衡常数Ka_______Kb。
1 2
②已知Arrhenius经验公式为RInk=- +C(E 为活化能,k为速率常数, R和C为常数),为探究m、
a
n两种催化剂的储化效能,进行了实验探宄,依据实验数获得图丙曲线。
在m催化剂作用下,该反应的活化能E=_______ J/mol。 从图中信息获知催化效能较高的催化剂是
a
_______ (“m"或“n"), 判断理由是_______。
(3)电催化还原CO 受到广泛的研究,一种原理如图所示:
2
写出A电极发生的电极方程式:_______。若用铅蓄电池提供电能,则电极B连接铅蓄电池的_______
极(填化学式)。【答案】(1)+208.4
(2) < > 9.6×104 n 由图可知,直线n斜率大,E 小,催化效率高
a
(3) 2CO +12e- + 12H+ = C H + 4H O PbO
2 2 4 2 2
【解析】(1)根据图示 ΔH=(237.1-28.7)kJ/mol=+208.4
kJ/mol。(2)①增大压强,平衡正向移动,压强越大乙醇的体积分数越大,所以压强P< P ,根据图示,
1 2
升高温度,乙醇体积分数减小,说明升高温度平衡逆向移动,平衡常数减小,a点温度小于b点,所以a、
b两点的平衡常数Ka>Kb。②在m催化剂作用下, ,计算得该反应的活化能E=9.6×104J/
a
mol。由图可知,直线n斜率大,E 小,催化效率高,所以催化效能较高的催化剂是n。(3)根据图示,A
a
电极二氧化碳得电子生成乙烯和水,电极反应方程式为2CO +12e- + 12H+ = C H + 4H O;A电极发生还
2 2 4 2
原反应,A是阴极、B是阳极,若用铅蓄电池提供电能,则电极B连接铅蓄电池的正极,铅蓄电池正极材
料为PbO 。
2
12.(2022·山东省高三大联考)甲烷、二氧化碳重整制合成气CO和H,是一种有效实现碳达峰、碳
2
中和的关键技术,也是近几年研究的热点之一。回答下列问题:
(1)已知:甲烷、二氧化碳重整工艺的相关反应如下:
①H(g)+CO (g) HO(g)+CO(g) ∆H=+41kJ·mol−1
2 2 2 1
②2CO(g) CO(g)+C(s) ∆H=−172kJ·mol−1
2 2
③CH(g) C(s)+2H(g) ∆H=+75kJ·mol−1
4 2 3
④CO(g)+H(g) C(s)+HO(g) ∆H=−131kJ·mol−1
2 2 4
则甲烷、二氧化碳重整制合成气的热化学方程式为CH(g)+CO (g) 2CO(g)+2H(g)
4 2 2
∆H=_______;为了提高平衡时合成气的产率,反应条件应选择_______(填标号)。
A.高压 B.低压 C.低温 D.高温
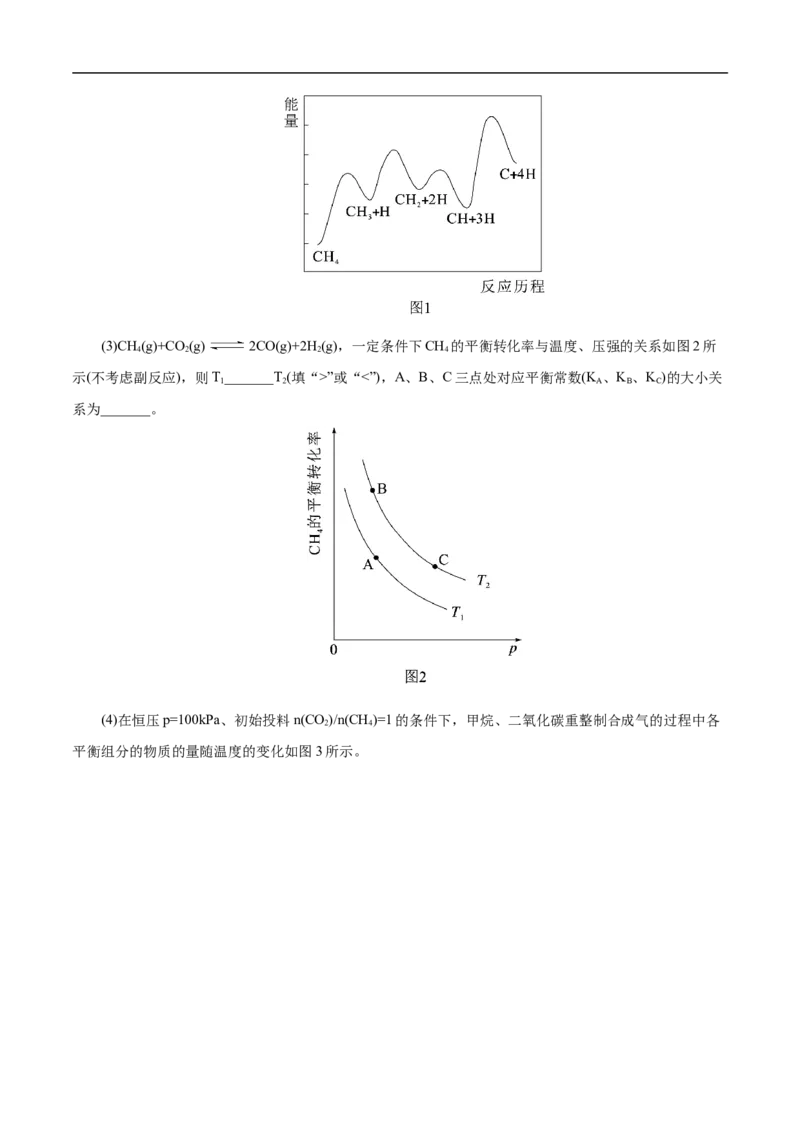
(2)一定条件下,CH 分解生成碳的反应历程如图1所示。该历程分4步进行,其中第_______步为放热
4
反应,正反应活化能最大一步的反应方程式为_______。(3)CH (g)+CO (g) 2CO(g)+2H(g),一定条件下CH 的平衡转化率与温度、压强的关系如图2所
4 2 2 4
示(不考虑副反应),则T_______T(填“>”或“<”),A、B、C三点处对应平衡常数(K 、K 、K )的大小关
1 2 A B C
系为_______。
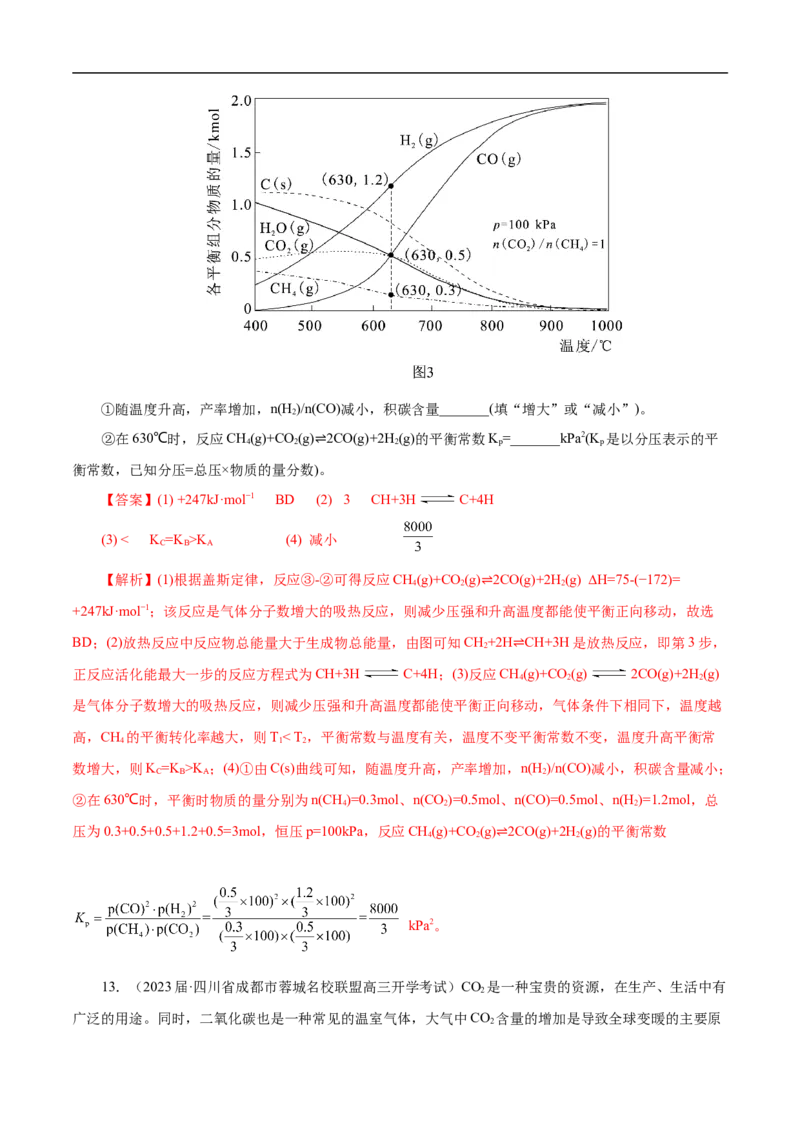
(4)在恒压p=100kPa、初始投料n(CO)/n(CH)=1的条件下,甲烷、二氧化碳重整制合成气的过程中各
2 4
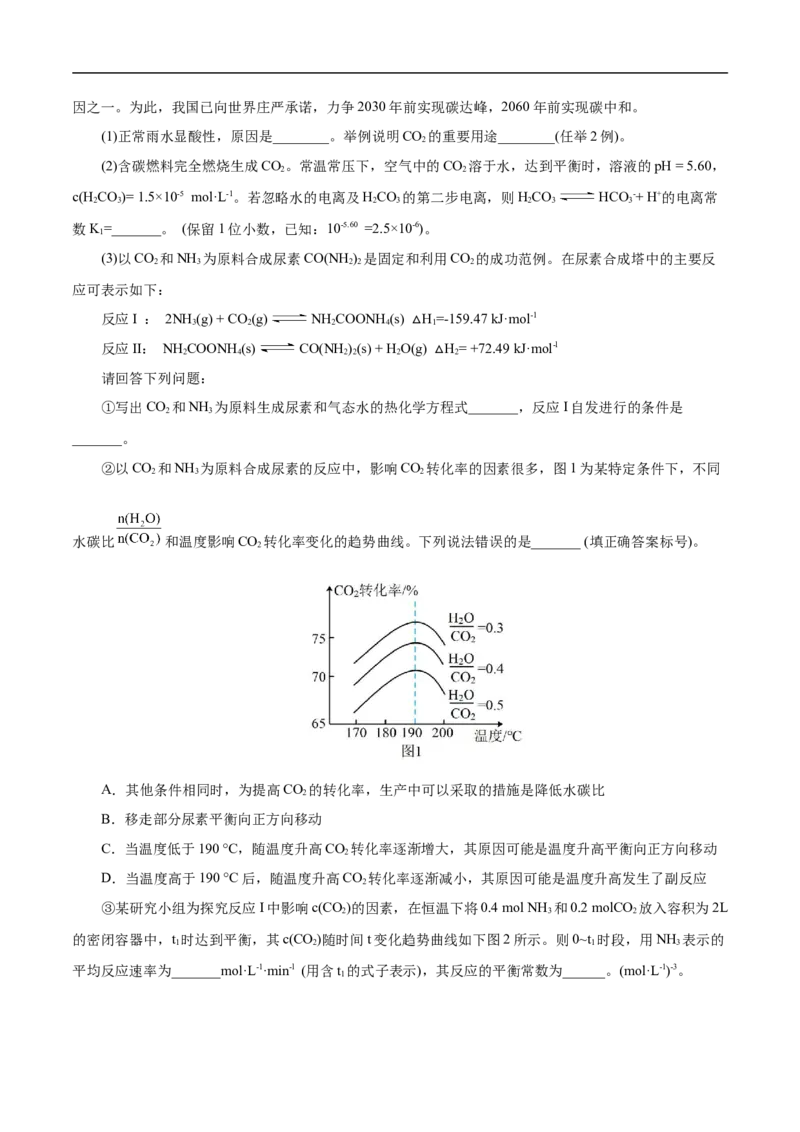
平衡组分的物质的量随温度的变化如图3所示。①随温度升高,产率增加,n(H )/n(CO)减小,积碳含量_______(填“增大”或“减小”)。
2
②在630℃时,反应CH(g)+CO (g) 2CO(g)+2H(g)的平衡常数K=_______kPa2(K 是以分压表示的平
4 2 2 p p
衡常数,已知分压=总压×物质的量分数)⇌。
【答案】(1) +247kJ·mol−1 BD (2) 3 CH+3H C+4H
(3) < K =K >K (4) 减小
C B A
【解析】(1)根据盖斯定律,反应③-②可得反应CH(g)+CO (g) 2CO(g)+2H(g) ∆H=75-(−172)=
4 2 2
+247kJ·mol−1;该反应是气体分子数增大的吸热反应,则减少压强和⇌升高温度都能使平衡正向移动,故选
BD;(2)放热反应中反应物总能量大于生成物总能量,由图可知CH+2H CH+3H是放热反应,即第3步,
2
正反应活化能最大一步的反应方程式为CH+3H C+4H;(3)反应CH⇌(g)+CO (g) 2CO(g)+2H(g)
4 2 2
是气体分子数增大的吸热反应,则减少压强和升高温度都能使平衡正向移动,气体条件下相同下,温度越
高,CH 的平衡转化率越大,则T< T,平衡常数与温度有关,温度不变平衡常数不变,温度升高平衡常
4 1 2
数增大,则K =K >K ;(4)①由C(s)曲线可知,随温度升高,产率增加,n(H )/n(CO)减小,积碳含量减小;
C B A 2
②在630℃时,平衡时物质的量分别为n(CH)=0.3mol、n(CO)=0.5mol、n(CO)=0.5mol、n(H )=1.2mol,总
4 2 2
压为0.3+0.5+0.5+1.2+0.5=3mol,恒压p=100kPa,反应CH(g)+CO (g) 2CO(g)+2H(g)的平衡常数
4 2 2
⇌
kPa2。
13.(2023届·四川省成都市蓉城名校联盟高三开学考试)CO 是一种宝贵的资源,在生产、生活中有
2
广泛的用途。同时,二氧化碳也是一种常见的温室气体,大气中CO 含量的增加是导致全球变暖的主要原
2因之一。为此,我国已向世界庄严承诺,力争2030年前实现碳达峰,2060年前实现碳中和。
(1)正常雨水显酸性,原因是________。举例说明CO 的重要用途________(任举2例)。
2
(2)含碳燃料完全燃烧生成CO。常温常压下,空气中的CO 溶于水,达到平衡时,溶液的pH = 5.60,
2 2
c(HCO)= 1.5×10-5 mol·L-1。若忽略水的电离及HCO 的第二步电离,则HCO HCO -+ H+的电离常
2 3 2 3 2 3 3
数K=_______。 (保留1位小数,已知:10-5.60 =2.5×10-6)。
1
(3)以CO 和NH 为原料合成尿素CO(NH) 是固定和利用CO 的成功范例。在尿素合成塔中的主要反
2 3 2 2 2
应可表示如下:
反应I : 2NH (g) + CO (g) NH COONH(s) H=-159.47 kJ·mol-1
3 2 2 4 1
反应II: NH
2
COONH
4
(s) CO(NH
2
)
2
(s) + H
2
O(△g) H
2
= +72.49 kJ·mol-l
请回答下列问题: △
①写出CO 和NH 为原料生成尿素和气态水的热化学方程式_______,反应I自发进行的条件是
2 3
_______。
②以CO 和NH 为原料合成尿素的反应中,影响CO 转化率的因素很多,图1为某特定条件下,不同
2 3 2
水碳比 和温度影响CO 转化率变化的趋势曲线。下列说法错误的是_______ (填正确答案标号)。
2
A.其他条件相同时,为提高CO 的转化率,生产中可以采取的措施是降低水碳比
2
B.移走部分尿素平衡向正方向移动
C.当温度低于190 °C,随温度升高CO 转化率逐渐增大,其原因可能是温度升高平衡向正方向移动
2
D.当温度高于190 °C后,随温度升高CO 转化率逐渐减小,其原因可能是温度升高发生了副反应
2
③某研究小组为探究反应I中影响c(CO)的因素,在恒温下将0.4 mol NH 和0.2 molCO 放入容积为2L
2 3 2
的密闭容器中,t 时达到平衡,其c(CO)随时间t变化趋势曲线如下图2所示。则0~t 时段,用NH 表示的
1 2 1 3
平均反应速率为_______mol·L-1·min-l (用含t 的式子表示),其反应的平衡常数为______。(mol·L-1)-3。
1【答案】(1) 雨水中溶有CO 人工降雨、制冷、制碳酸饮料、制备纯碱(合理即可)
2
(2)4.2×10-7
(3) ①2NH (g) + CO (g) CO(NH)(s)+ H O(g) ΔH= -86.98 kJ/mol 低温
3 2 2 2 2
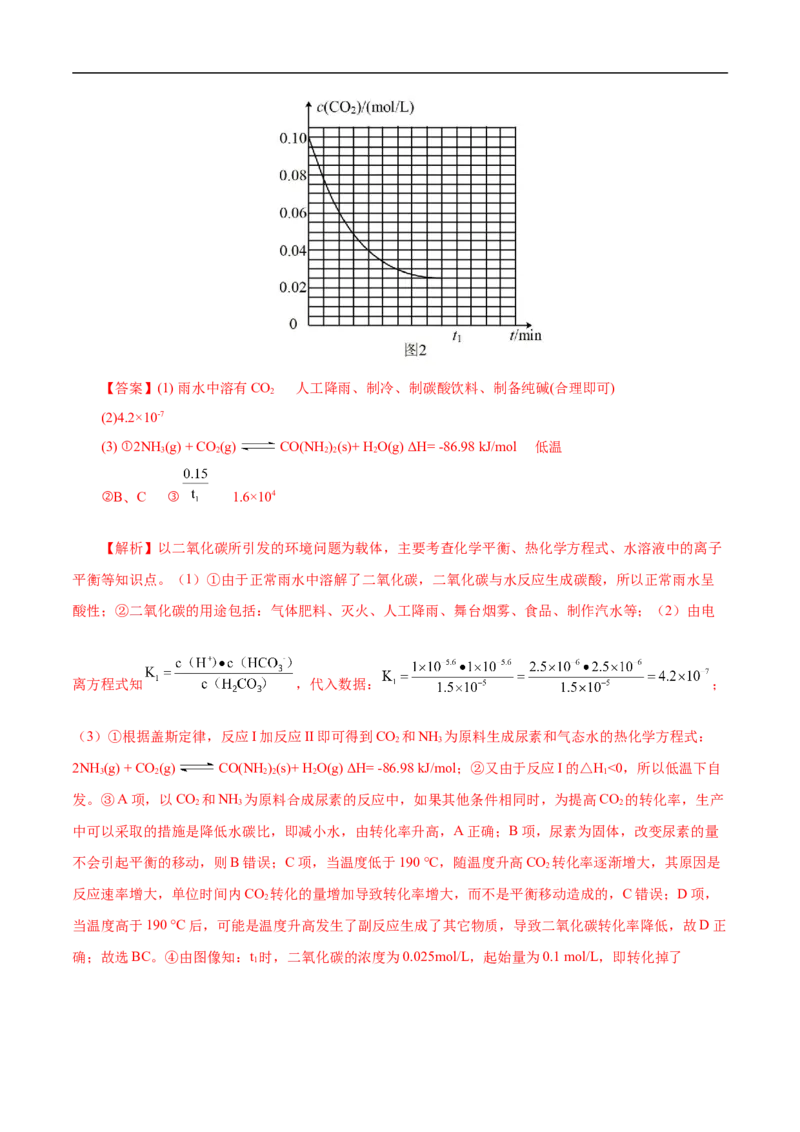
②B、C ③ 1.6×104
【解析】以二氧化碳所引发的环境问题为载体,主要考查化学平衡、热化学方程式、水溶液中的离子
平衡等知识点。(1)①由于正常雨水中溶解了二氧化碳,二氧化碳与水反应生成碳酸,所以正常雨水呈
酸性;②二氧化碳的用途包括:气体肥料、灭火、人工降雨、舞台烟雾、食品、制作汽水等;(2)由电
离方程式知 ,代入数据: ;
(3)①根据盖斯定律,反应I加反应II即可得到CO 和NH 为原料生成尿素和气态水的热化学方程式:
2 3
2NH (g) + CO (g) CO(NH)(s)+ H O(g) ΔH= -86.98 kJ/mol;②又由于反应I的△H<0,所以低温下自
3 2 2 2 2 1
发。③A项,以CO 和NH 为原料合成尿素的反应中,如果其他条件相同时,为提高CO 的转化率,生产
2 3 2
中可以采取的措施是降低水碳比,即减小水,由转化率升高,A正确;B项,尿素为固体,改变尿素的量
不会引起平衡的移动,则B错误;C项,当温度低于190 °C,随温度升高CO 转化率逐渐增大,其原因是
2
反应速率增大,单位时间内CO 转化的量增加导致转化率增大,而不是平衡移动造成的,C错误;D项,
2
当温度高于190 °C后,可能是温度升高发生了副反应生成了其它物质,导致二氧化碳转化率降低,故D正
确;故选BC。④由图像知:t 时,二氧化碳的浓度为0.025mol/L,起始量为0.1 mol/L,即转化掉了
10.075mol/L,则用二氧化碳表示的平均反应速率为: mol•L-1•min-1,在反应I方程式中氨气和二氧化
碳的配平系数分别为2、1,则用氨气表示的平均反应速率为 mol•L-1•min-1。⑤根据反应I可列出平衡
常数的表达式为 ,根据三段式计算:
则 。
14.(2023届·河南省湘豫名校高三摸底考试)为了进一步响应节能减排,实现碳达峰、碳中和,某
企业科研机构利用CO 和CH 反应生成合成气(主要成分为 、H),可减少温室气体的排放。
2 4 2
(1)已知部分反应的热化学方程式为:
①CH (g)=2H(g)+C(s) ΔH=+75kJ·mol−1
4 2
②C(s)+O(g)=CO (g) ΔH=-394kJ·mol−1
2 2
③C(s)+1/2O (g)=CO(g) ΔH=-111kJ·mol−1
2
则由CO 和CH 反应生成合成气的热化学方程式为_______。
2 4
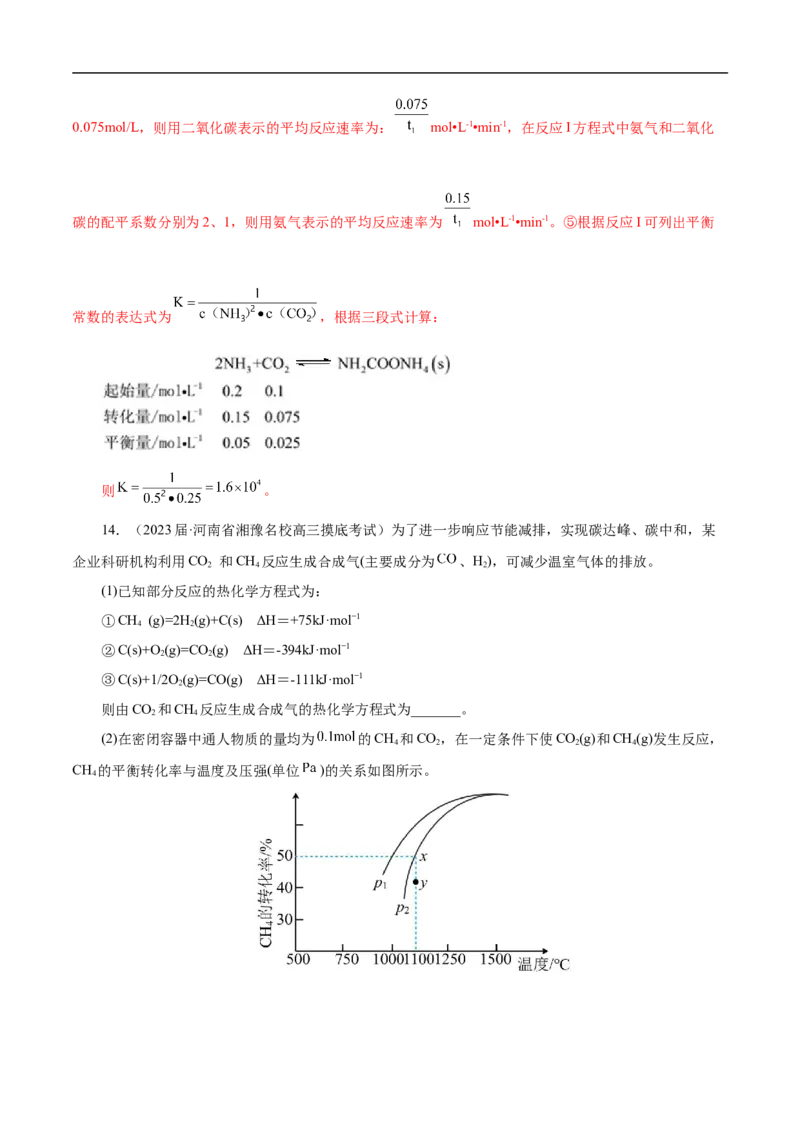
(2)在密闭容器中通人物质的量均为 的CH 和CO,在一定条件下使CO(g)和CH(g)发生反应,
4 2 2 4
CH 的平衡转化率与温度及压强(单位 )的关系如图所示。
4①结合上图,在1100℃下y点时 _______ (填“大于”“小于”或“等于”)。
②在1100℃下x点已达到平衡状态1,用平衡分压代替平衡浓度可以得到平衡常数Kp,则x点对应温
度下反应的平衡常数Kp=_______(已知气体分压p =气体总压p ×气体的物质的量分数)。x点时若升高温
分 总
度,反应CO(g)和CH(g)反应的平衡将_______(填“正向移动"“逆向移动”或“不移动”)。
2 4
③若起始时在上述密闭容器中加入物质的量均为 的H 和 ,该容器中发生的反应_______(填
2
“吸收”或“释放”)热量;在1100℃和p 条件下达到平衡状态2,与平衡状态1相比,该状态下的
2
c(CO)_______(填“变大”“变小”或“不变”)。
2
(3)利用铜基配合物1,10—phenanthroline— 催化剂电催化CO,还原制备碳基燃料(包括 、烷经
2
和酸质子交换膜等)是减少CO 在大气中累积和实现可再生能源有效利用的关键手段,其装置原理如图所示。
2
①电池工作过程中,图中Pt电极附近溶液的pH_______(填“变大”或“变小”)。
②每转移 电子,阴极室溶液质量增加_______g。
【答案】(1) CH (g)+ CO (g)=2H(g)+2CO(g) ΔH=+247kJ·mol−1
4 2 2
(2) 大于 正向移动 释放 不变
(3) 变小 46
【解析】(1)首先写出CH 和CO 的催化重整反应为CH (g)+ CO (g)=2H(g)+2CO(g),再根据盖斯
4 2 4 2 2
定律,①+2×③-②得CH (g)+ CO (g)=2H(g)+2CO(g),
4 2 2
;(2)①由图示可知,y点甲烷的转化率小于平街转化率,反应正向进行,所以y点: 大于 ;②根据三段式计算可得:
则平衡常数 ;根据反应CH (g)+ CO (g)=2H(g)+2CO(g) ΔH=
4 2 2
+247kJ·mol−1,在平衡时升高温度,平衡会向吸热的正反应方向移动;③根据反应CH (g)+ CO (g)=2H(g)
4 2 2
+2CO(g) ΔH=+247kJ·mol−1,正反应方向为吸热反应,若在上述密闭容器中加入0.2 mol的H 和CO发
2
生反应,反应从逆反应方向进行,则反应要释放热量;反应是在等温等压条件下进行的。将0.2 mol H 和
2
0.2 mol CO完全反应,转化为0.1 mol CH 和0.1 mol CO ,则与②中反应等效,反应在1100℃达到平衡状
4 2
态2,c(CO)不变;(3)①由图可知,Pt电极生成氧气,Pt是阳极,电极反应式是2HO-4e-=4H++O ↑,附
2 2 2
近溶液的pH变小;②石墨烯是阴极,CO 在阴极得电子生成甲酸,电极反应式是CO+2H++2e-=HCOOH,
2 2
每转移2 mol电子,生成1mol甲酸,阴极室溶液质量增加46g。