文档内容
第四篇 化学反应速率与化学平衡
专项 28 化学反应速率图象
图象类试题的特征是以图象的形式将一些相关量给出,把题目中的化学原理抽象为数学问题,旨在考
查从图象中获得数据、处理应用数据的能力以及对曲线的数学意义和化学意义之间对应关系的运用能力。
近年来高考,化学反应速率图像题多在非选择题中以填空的形式出现。试题主要是结合图像中的数据及物
质的变化趋势进行分析、判断与计算。常见速率—时间图像(vt图像)类型如下:
由图像变化分析外界条件对其影响,已知反应为mA(g)+nB(g) pC(g)+qD(g) ΔH=Q kJ·mol-1。
(1)“渐变”类vt图像
图像 分析 结论
t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ ,平 t 时其他条件不变,增大反应物
1 正 逆 正 逆 1
衡向正反应方向移动 的浓度
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ ,平 t 时其他条件不变,减小反应物
1 正 逆 逆 正 1
衡向逆反应方向移动 的浓度
t 时v′ 突然增大,v′ 逐渐增大;v′ >v′ ,平 t 时其他条件不变,增大生成物
1 逆 正 逆 正 1
衡向逆反应方向移动 的浓度
t 时v′ 突然减小,v′ 逐渐减小;v′ >v′ ,平 t 时其他条件不变,减小生成物
1 逆 正 正 逆 1
衡向正反应方向移动 的浓度
(2)“断点”类vt图像
图像 分析 结论
t 时其他条件不变,增大反应体系的压强
1
t 时v′ 、v′ 均突然增大,且
且m+n>p+q(正反应为体积减小的反应)
1 正 逆
v′ >v′ ;平衡向正反应方
正 逆
向进行 t 时其他条件不变,升高温度且Q>0(吸
1
热反应)t 时其他条件不变,增大反应体系的压强
1
t 时v′ 、v′ 均突然增大,且
且m+n<p+q(正反应为体积增大的反应)
1 正 逆
v′ >v′ ;平衡向逆反应方
逆 正
向进行 t 时其他条件不变,升高温度且Q<0(放
1
热反应)
t 时其他条件不变,减小反应体系的压强
1
t 时v′ 、v′ 均突然减小,且
且m+n<p+q(正反应为体积增大的反应)
1 正 逆
v′ >v′ ;平衡向正反应方
正 逆
向进行 t 时其他条件不变,降低温度且Q<0(放
1
热反应)
t 时其他条件不变,减小反应体系的压强
1
t 时v′ 、v′ 均突然减小,且
且m+n>p+q(正反应为体积减小的反应)
1 逆 正
v′ >v′ ;平衡向逆反应方
逆 正
向进行 t 时其他条件不变,降低温度且Q>0(吸
1
热反应)
(3)“平台”类vt图像
图像 分析 结论
t 时其他条件不变使用催化剂
1
t 时v′ 、v′ 均突然增大
1 正 逆
且v′ 正 =v′ 逆 ,平衡不移动 t 1 时其他条件不变增大反应体系的压强且m+
n=p+q(反应前后气体体积无变化)
t 时v′ 、v′ 均突然减小 t 时其他条件不变,减小反应体系的压强且m
1 正 逆 1
且v′ =v′ ,平衡不移动 +n=p+q(反应前后气体体积无变化)
正 逆
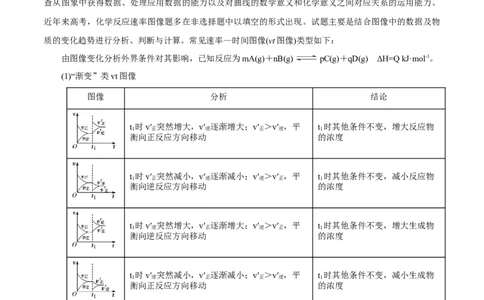
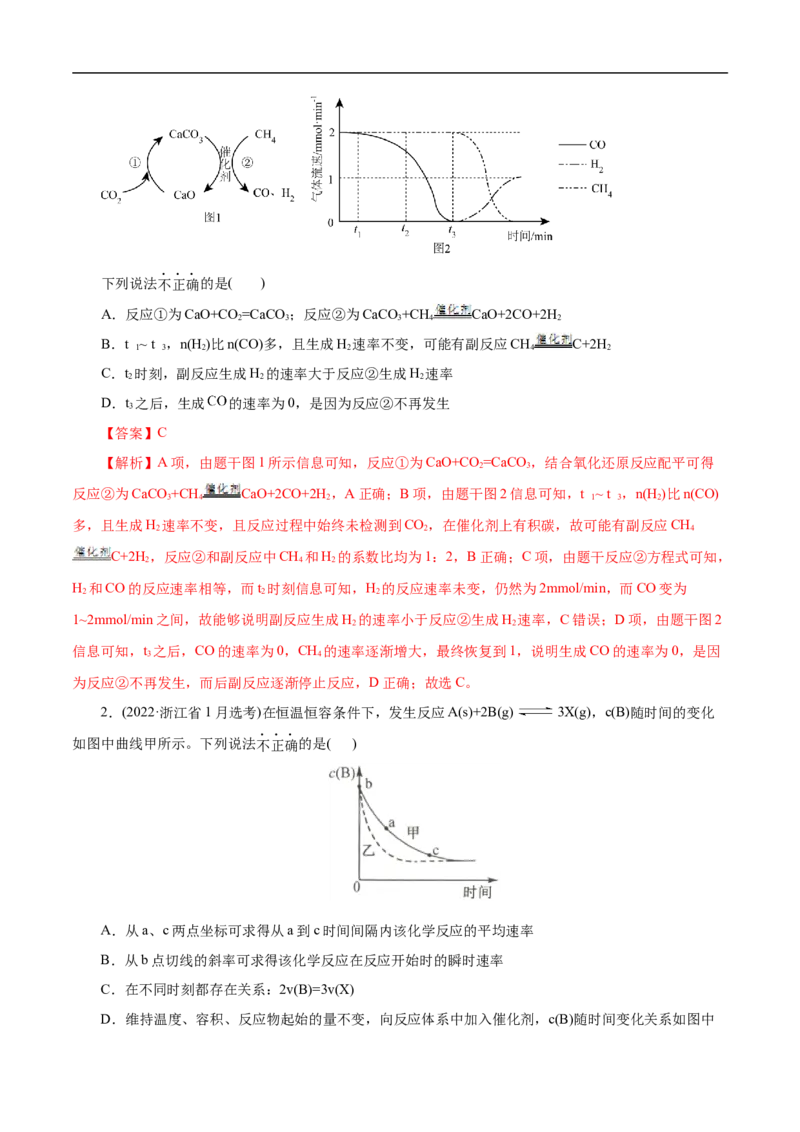
1.(2022•北京卷)CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反应①完成之后,
2 2
以N 为载气,以恒定组成的N、CH 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的
2 2 4
量随反应时间变化如图2所示。反应过程中始终未检测到CO,在催化剂上有积碳。
2下列说法不正确的是( )
A.反应①为CaO+CO=CaCO;反应②为CaCO+CH CaO+2CO+2H
2 3 3 4 2
B.t ~ t ,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成 的速率为0,是因为反应②不再发生
3
【答案】C
【解析】A项,由题干图1所示信息可知,反应①为CaO+CO =CaCO ,结合氧化还原反应配平可得
2 3
反应②为CaCO +CH CaO+2CO+2H ,A正确;B项,由题干图2信息可知,t ~ t ,n(H )比n(CO)
3 4 2 1 3 2
多,且生成H 速率不变,且反应过程中始终未检测到CO,在催化剂上有积碳,故可能有副反应CH
2 2 4
C+2H ,反应②和副反应中CH 和H 的系数比均为1:2,B正确;C项,由题干反应②方程式可知,
2 4 2
H 和CO的反应速率相等,而t 时刻信息可知,H 的反应速率未变,仍然为2mmol/min,而CO变为
2 2 2
1~2mmol/min之间,故能够说明副反应生成H 的速率小于反应②生成H 速率,C错误;D项,由题干图2
2 2
信息可知,t 之后,CO的速率为0,CH 的速率逐渐增大,最终恢复到1,说明生成CO的速率为0,是因
3 4
为反应②不再发生,而后副反应逐渐停止反应,D正确;故选C。
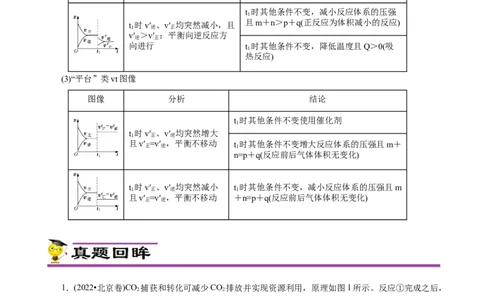
2.(2022·浙江省1月选考)在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变化
如图中曲线甲所示。下列说法不正确的是( )
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线乙所示
【答案】C
【解析】A项,图象中可以得到单位时间内的浓度变化,反应速率是单位时间内物质的浓度变化计算
得到,从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率,A正确; B项,b点处的切线
的斜率是此时刻物质浓度除以此时刻时间,为一氧化碳的瞬时速率,B正确; C项,化学反应速率之比等
于化学方程式计量数之比分析,3v(B)=2v(X),C不正确; D项,维持温度、容积不变,向反应体系中加
入催化剂,平衡不移动,反应速率增大,达到新的平衡状态,平衡状态与原来的平衡状态相同,D错误;
故选C。
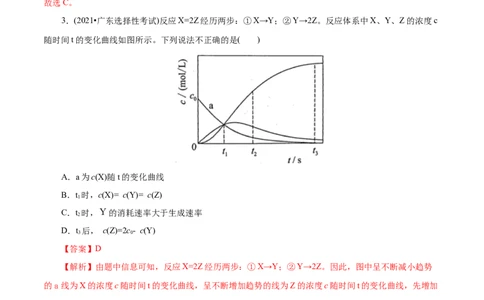
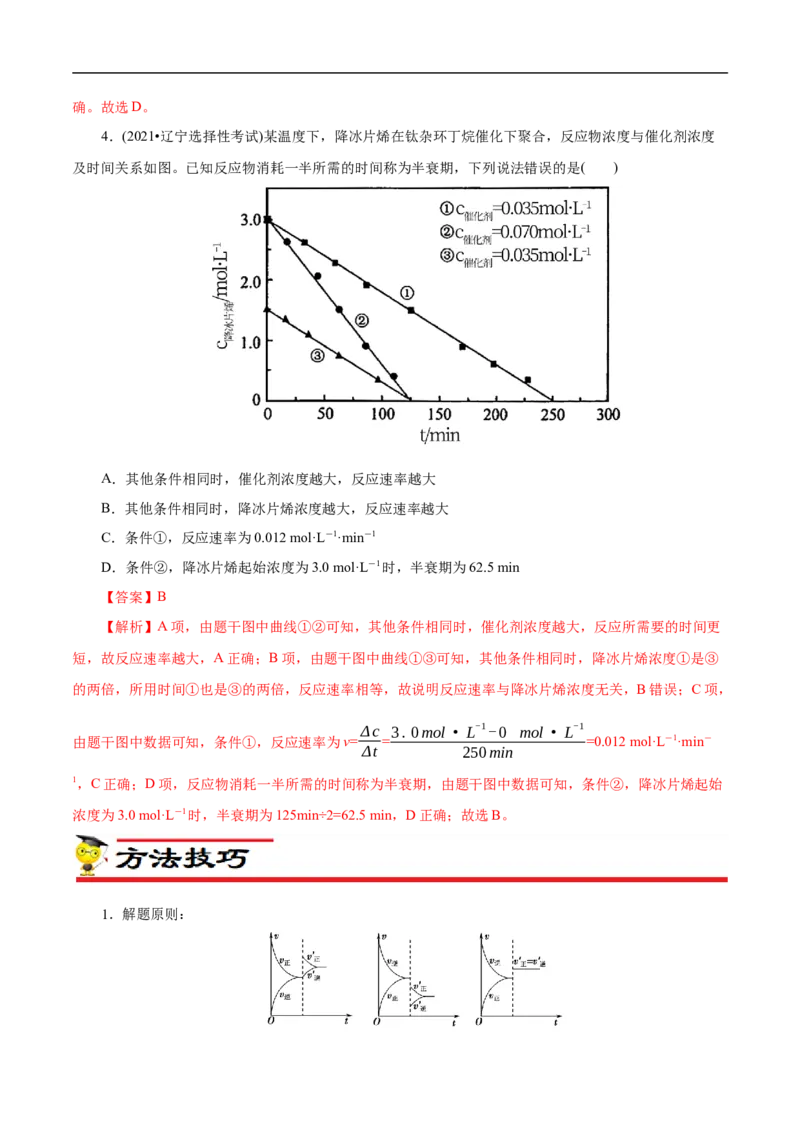
3.(2021•广东选择性考试)反应X=2Z经历两步:①X→Y;②Y→2Z。反应体系中X、Y、Z的浓度c
随时间t的变化曲线如图所示。下列说法不正确的是( )
A.a为c(X)随t的变化曲线
B.t 时,c(X)= c(Y)= c(Z)
1
C.t 时, 的消耗速率大于生成速率
2
D.t 后, c(Z)=2c- c(Y)
3 0
【答案】D
【解析】由题中信息可知,反应X=2Z经历两步:①X→Y;②Y→2Z。因此,图中呈不断减小趋势
的a线为X的浓度c随时间t的变化曲线,呈不断增加趋势的线为Z的浓度c随时间t的变化曲线,先增加
后减小的线为Y的浓度c随时间t的变化曲线。A项,X是唯一的反应物,随着反应的发生,其浓度不断
减小,因此,由图可知,a为c(X)随t的变化曲线,A正确;B项,由图可知,分别代表3种不同物质的曲
线相交于t 时刻,因此,t 时c(X)= c(Y)= c(Z),B正确;C项,由图中信息可知,t 时刻以后,Y的浓度
1 1 2
仍在不断减小,说明t 时刻反应两步仍在向正反应方向发生,而且反应①生成Y的速率小于反应②消耗Y
2
的速率,即t 时Y的消耗速率大于生成速率,C正确;D项,由图可知,t 时刻反应①完成,X完全转化为
2 3
Y,若无反应②发生,则c(Y) =c,由于反应②Y→2Z的发生,t 时刻Y浓度的变化量为c- c(Y),变化量
0 3 0
之比等于化学计量数之比,所以Z的浓度的变化量为2[c- c(Y)],这种关系在t 后仍成立, 因此,D不正
0 3确。故选D。
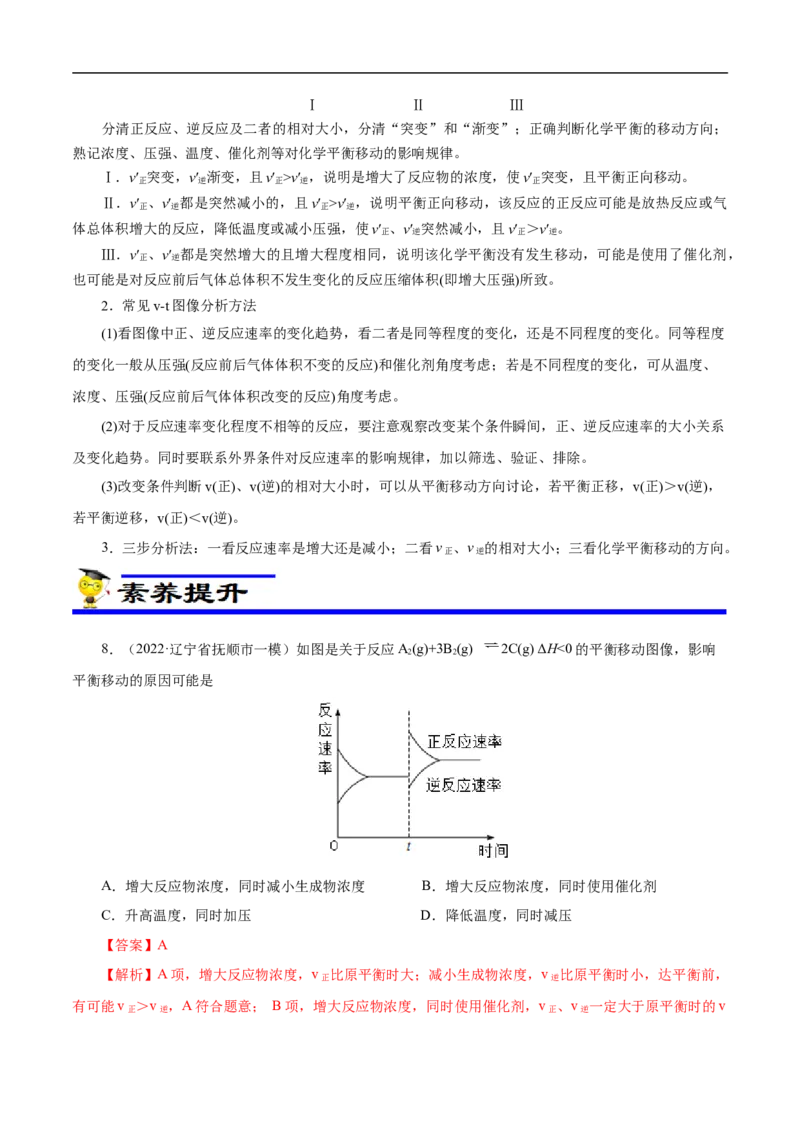
4.(2021•辽宁选择性考试)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度
及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是( )
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为0.012 mol·L-1·min-1
D.条件②,降冰片烯起始浓度为3.0 mol·L-1时,半衰期为62.5 min
【答案】B
【解析】A项,由题干图中曲线①②可知,其他条件相同时,催化剂浓度越大,反应所需要的时间更
短,故反应速率越大,A正确;B项,由题干图中曲线①③可知,其他条件相同时,降冰片烯浓度①是③
的两倍,所用时间①也是③的两倍,反应速率相等,故说明反应速率与降冰片烯浓度无关,B错误;C项,
Δc 3.0mol·L-1-0 mol·L-1
由题干图中数据可知,条件①,反应速率为v= = =0.012 mol·L-1·min-
Δt 250min
1,C正确;D项,反应物消耗一半所需的时间称为半衰期,由题干图中数据可知,条件②,降冰片烯起始
浓度为3.0 mol·L-1时,半衰期为125min÷2=62.5 min,D正确;故选B。
1.解题原则:Ⅰ Ⅱ Ⅲ
分清正反应、逆反应及二者的相对大小,分清“突变”和“渐变”;正确判断化学平衡的移动方向;
熟记浓度、压强、温度、催化剂等对化学平衡移动的影响规律。
Ⅰ.v′ 突变,v′ 渐变,且v′ >v′ ,说明是增大了反应物的浓度,使v′ 突变,且平衡正向移动。
正 逆 正 逆 正
Ⅱ.v′ 、v′ 都是突然减小的,且v′ >v′ ,说明平衡正向移动,该反应的正反应可能是放热反应或气
正 逆 正 逆
体总体积增大的反应,降低温度或减小压强,使v′ 、v′ 突然减小,且v′ >v′ 。
正 逆 正 逆
Ⅲ.v′ 、v′ 都是突然增大的且增大程度相同,说明该化学平衡没有发生移动,可能是使用了催化剂,
正 逆
也可能是对反应前后气体总体积不发生变化的反应压缩体积(即增大压强)所致。
2.常见v-t图像分析方法
(1)看图像中正、逆反应速率的变化趋势,看二者是同等程度的变化,还是不同程度的变化。同等程度
的变化一般从压强(反应前后气体体积不变的反应)和催化剂角度考虑;若是不同程度的变化,可从温度、
浓度、压强(反应前后气体体积改变的反应)角度考虑。
(2)对于反应速率变化程度不相等的反应,要注意观察改变某个条件瞬间,正、逆反应速率的大小关系
及变化趋势。同时要联系外界条件对反应速率的影响规律,加以筛选、验证、排除。
(3)改变条件判断v(正)、v(逆)的相对大小时,可以从平衡移动方向讨论,若平衡正移,v(正)>v(逆),
若平衡逆移,v(正)<v(逆)。
3.三步分析法:一看反应速率是增大还是减小;二看v 、v 的相对大小;三看化学平衡移动的方向。
正 逆
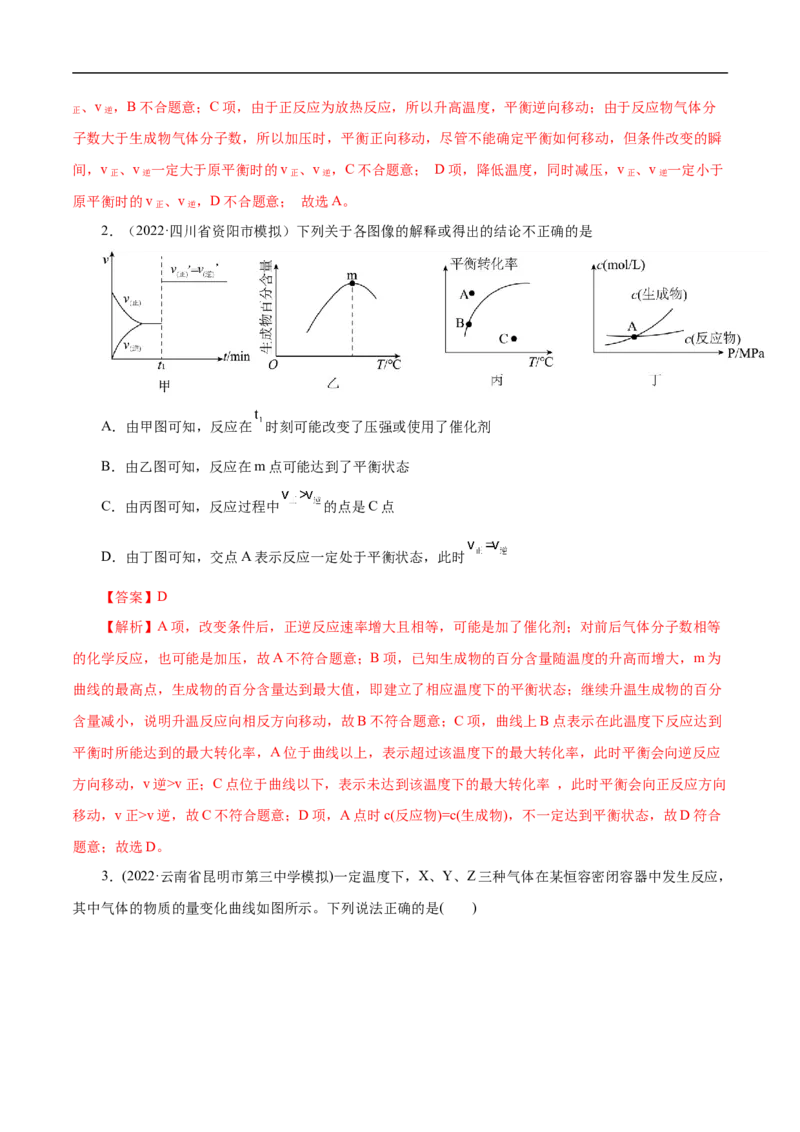
8.(2022·辽宁省抚顺市一模)如图是关于反应A(g)+3B (g) 2C(g) ΔH<0的平衡移动图像,影响
2 2
平衡移动的原因可能是
A.增大反应物浓度,同时减小生成物浓度 B.增大反应物浓度,同时使用催化剂
C.升高温度,同时加压 D.降低温度,同时减压
【答案】A
【解析】A项,增大反应物浓度,v 比原平衡时大;减小生成物浓度,v 比原平衡时小,达平衡前,
正 逆
有可能v >v ,A符合题意; B项,增大反应物浓度,同时使用催化剂,v 、v 一定大于原平衡时的v
正 逆 正 逆、v ,B不合题意;C项,由于正反应为放热反应,所以升高温度,平衡逆向移动;由于反应物气体分
正 逆
子数大于生成物气体分子数,所以加压时,平衡正向移动,尽管不能确定平衡如何移动,但条件改变的瞬
间,v 、v 一定大于原平衡时的v 、v ,C不合题意; D项,降低温度,同时减压,v 、v 一定小于
正 逆 正 逆 正 逆
原平衡时的v 、v ,D不合题意; 故选A。
正 逆
2.(2022·四川省资阳市模拟)下列关于各图像的解释或得出的结论不正确的是
A.由甲图可知,反应在 时刻可能改变了压强或使用了催化剂
B.由乙图可知,反应在m点可能达到了平衡状态
C.由丙图可知,反应过程中 的点是C点
D.由丁图可知,交点A表示反应一定处于平衡状态,此时
【答案】D
【解析】A项,改变条件后,正逆反应速率增大且相等,可能是加了催化剂;对前后气体分子数相等
的化学反应,也可能是加压,故A不符合题意;B项,已知生成物的百分含量随温度的升高而增大,m为
曲线的最高点,生成物的百分含量达到最大值,即建立了相应温度下的平衡状态;继续升温生成物的百分
含量减小,说明升温反应向相反方向移动,故B不符合题意;C项,曲线上B点表示在此温度下反应达到
平衡时所能达到的最大转化率,A位于曲线以上,表示超过该温度下的最大转化率,此时平衡会向逆反应
方向移动,v逆>v正;C点位于曲线以下,表示未达到该温度下的最大转化率 ,此时平衡会向正反应方向
移动,v正>v逆,故C不符合题意;D项,A点时c(反应物)=c(生成物),不一定达到平衡状态,故D符合
题意;故选D。
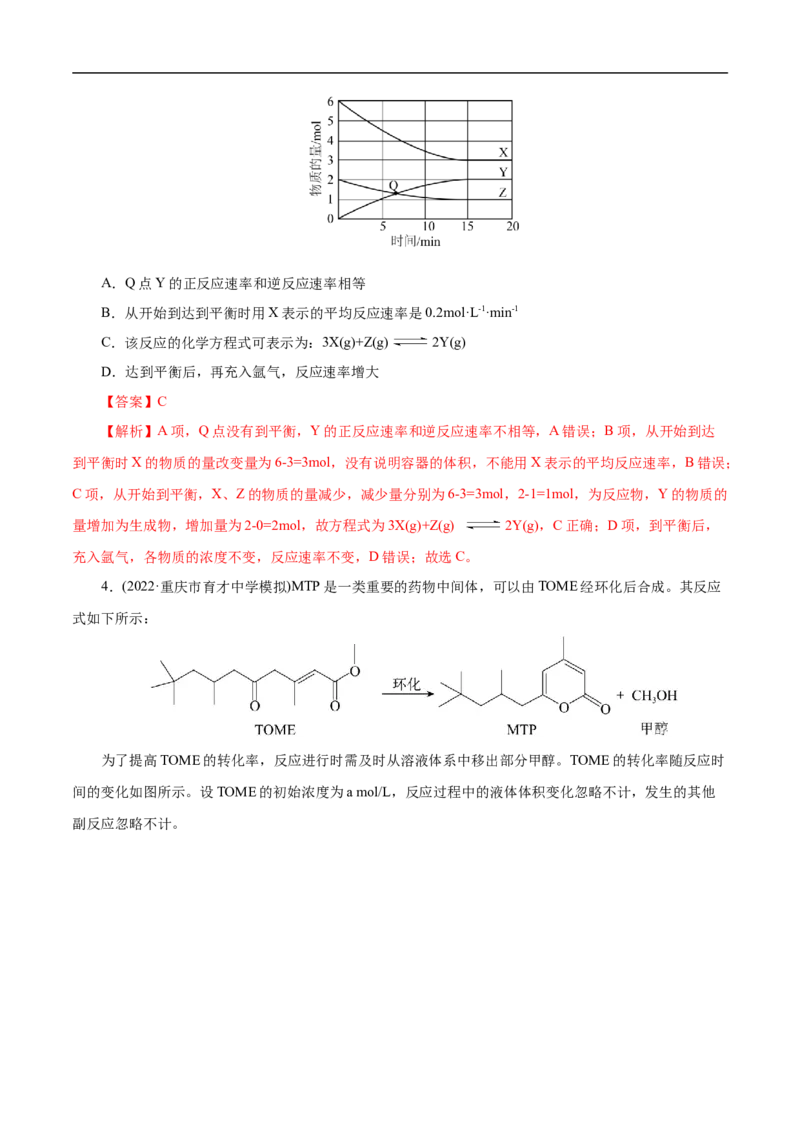
3.(2022·云南省昆明市第三中学模拟)一定温度下,X、Y、Z三种气体在某恒容密闭容器中发生反应,
其中气体的物质的量变化曲线如图所示。下列说法正确的是( )A.Q点Y的正反应速率和逆反应速率相等
B.从开始到达到平衡时用X表示的平均反应速率是0.2mol·L-1·min-1
C.该反应的化学方程式可表示为:3X(g)+Z(g) 2Y(g)
D.达到平衡后,再充入氩气,反应速率增大
【答案】C
【解析】A项,Q点没有到平衡,Y的正反应速率和逆反应速率不相等,A错误;B项,从开始到达
到平衡时X的物质的量改变量为6-3=3mol,没有说明容器的体积,不能用X表示的平均反应速率,B错误;
C项,从开始到平衡,X、Z的物质的量减少,减少量分别为6-3=3mol,2-1=1mol,为反应物,Y的物质的
量增加为生成物,增加量为2-0=2mol,故方程式为3X(g)+Z(g) 2Y(g),C正确;D项,到平衡后,
充入氩气,各物质的浓度不变,反应速率不变,D错误;故选C。
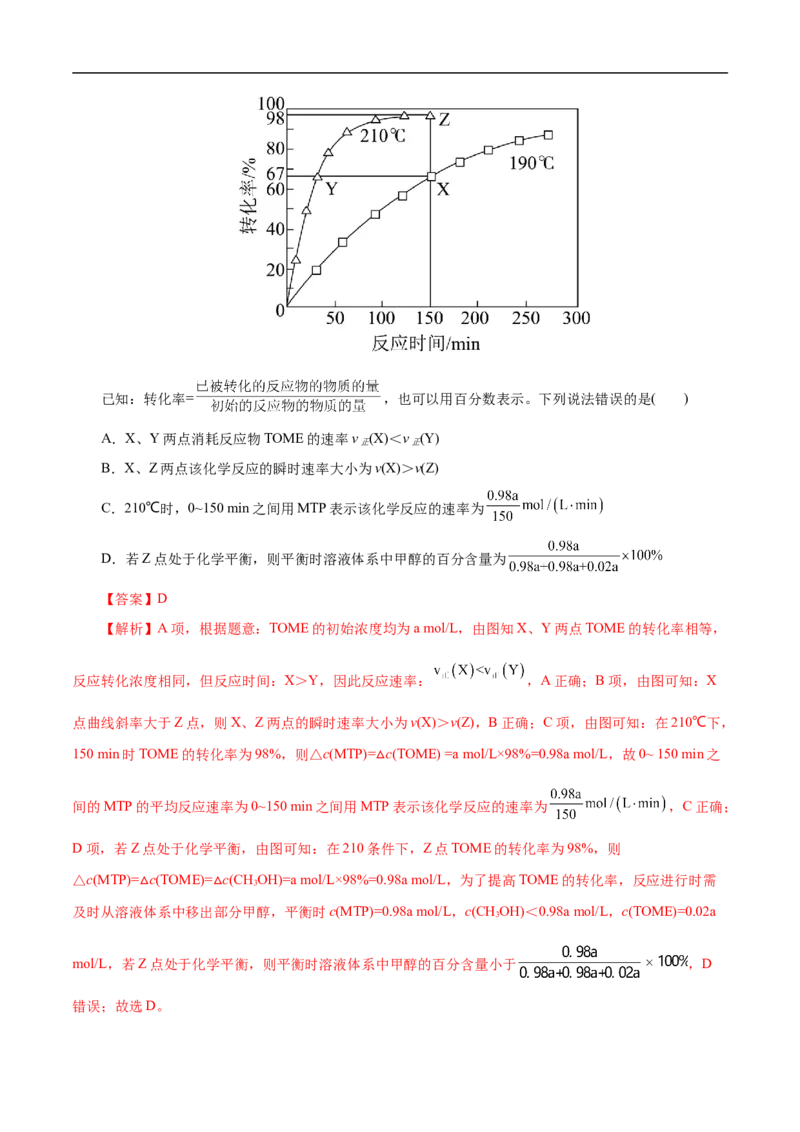
4.(2022·重庆市育才中学模拟)MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应
式如下所示:
为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时
间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计,发生的其他
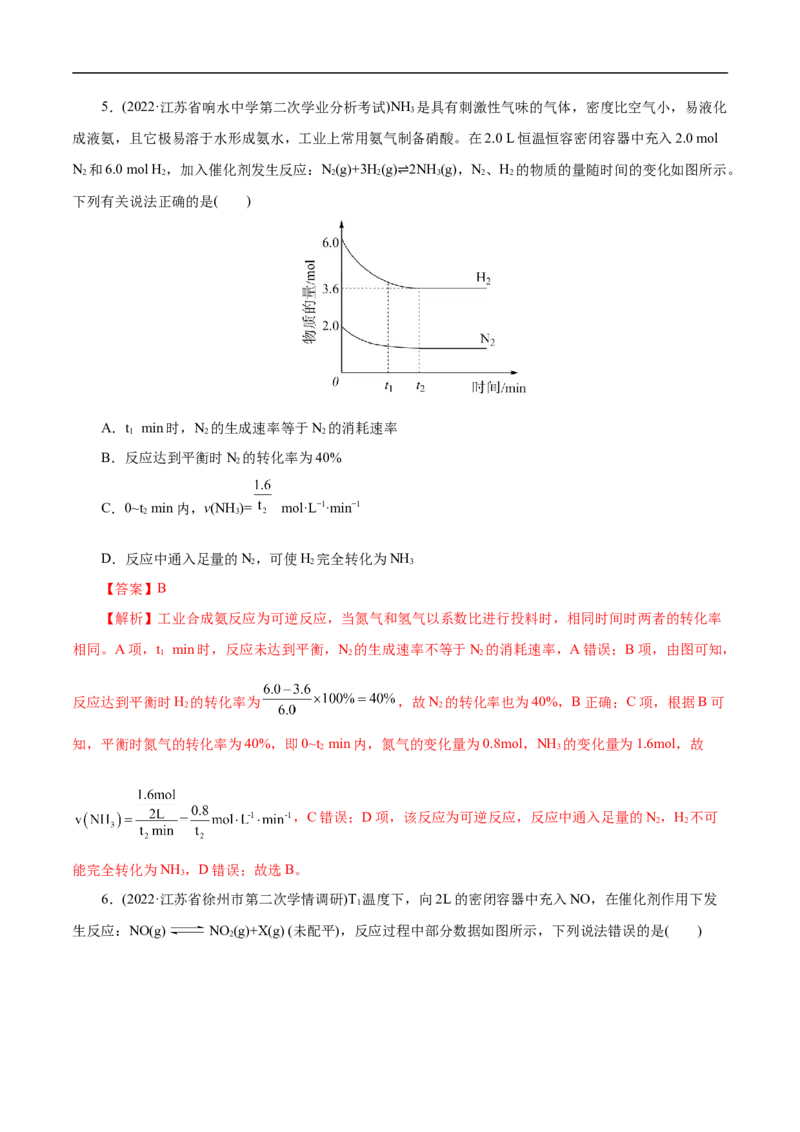
副反应忽略不计。已知:转化率= ,也可以用百分数表示。下列说法错误的是( )
A.X、Y两点消耗反应物TOME的速率v (X)<v (Y)
正 正
B.X、Z两点该化学反应的瞬时速率大小为v(X)>v(Z)
C.210℃时,0~150 min之间用MTP表示该化学反应的速率为
D.若Z点处于化学平衡,则平衡时溶液体系中甲醇的百分含量为
【答案】D
【解析】A项,根据题意:TOME的初始浓度均为a mol/L,由图知X、Y两点TOME的转化率相等,
反应转化浓度相同,但反应时间:X>Y,因此反应速率: ,A正确;B项,由图可知:X
点曲线斜率大于Z点,则X、Z两点的瞬时速率大小为v(X)>v(Z),B正确;C项,由图可知:在210℃下,
150 min时TOME的转化率为98%,则△c(MTP)= c(TOME) =a mol/L×98%=0.98a mol/L,故0~ 150 min之
△
间的MTP的平均反应速率为0~150 min之间用MTP表示该化学反应的速率为 ,C正确;
D项,若Z点处于化学平衡,由图可知:在210条件下,Z点TOME的转化率为98%,则
△c(MTP)= c(TOME)= c(CHOH)=a mol/L×98%=0.98a mol/L,为了提高TOME的转化率,反应进行时需
3
及时从溶液△体系中移出△部分甲醇,平衡时c(MTP)=0.98a mol/L,c(CHOH)<0.98a mol/L,c(TOME)=0.02a
3
mol/L,若Z点处于化学平衡,则平衡时溶液体系中甲醇的百分含量小于 ,D
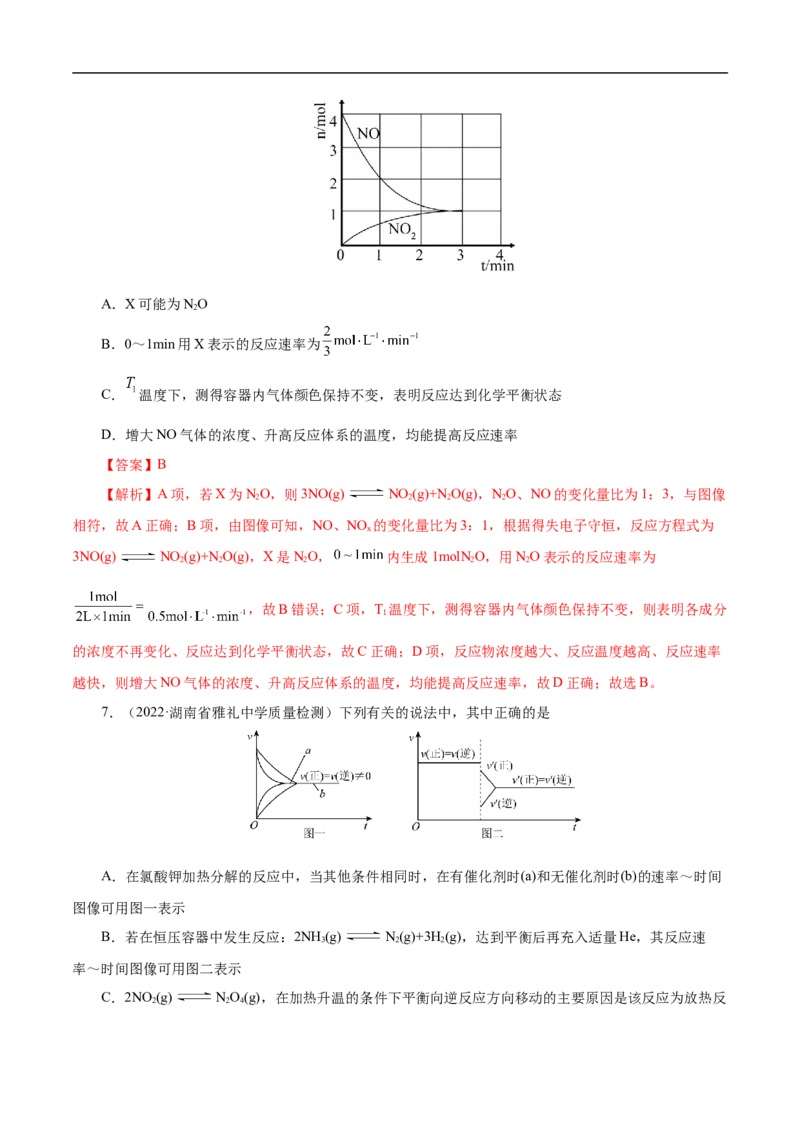
错误;故选D。5.(2022·江苏省响水中学第二次学业分析考试)NH 是具有刺激性气味的气体,密度比空气小,易液化
3
成液氨,且它极易溶于水形成氨水,工业上常用氨气制备硝酸。在2.0 L恒温恒容密闭容器中充入2.0 mol
N 和6.0 mol H,加入催化剂发生反应:N(g)+3H(g) 2NH (g),N、H 的物质的量随时间的变化如图所示。
2 2 2 2 3 2 2
下列有关说法正确的是( ) ⇌
A.t min时,N 的生成速率等于N 的消耗速率
1 2 2
B.反应达到平衡时N 的转化率为40%
2
C.0~t min内,v(NH )= mol·L−1·min−1
2 3
D.反应中通入足量的N,可使H 完全转化为NH
2 2 3
【答案】B
【解析】工业合成氨反应为可逆反应,当氮气和氢气以系数比进行投料时,相同时间时两者的转化率
相同。A项,t min时,反应未达到平衡,N 的生成速率不等于N 的消耗速率,A错误;B项,由图可知,
1 2 2
反应达到平衡时H 的转化率为 ,故N 的转化率也为40%,B正确;C项,根据B可
2 2
知,平衡时氮气的转化率为40%,即0~t min内,氮气的变化量为0.8mol,NH 的变化量为1.6mol,故
2 3
,C错误;D项,该反应为可逆反应,反应中通入足量的N,H 不可
2 2
能完全转化为NH ,D错误;故选B。
3
6.(2022·江苏省徐州市第二次学情调研)T 温度下,向2L的密闭容器中充入NO,在催化剂作用下发
1
生反应:NO(g) NO (g)+X(g) (未配平),反应过程中部分数据如图所示,下列说法错误的是( )
2A.X可能为NO
2
B.0~1min用X表示的反应速率为
C. 温度下,测得容器内气体颜色保持不变,表明反应达到化学平衡状态
D.增大NO气体的浓度、升高反应体系的温度,均能提高反应速率
【答案】B
【解析】A项,若X为NO,则3NO(g) NO (g)+NO(g),NO、NO的变化量比为1:3,与图像
2 2 2 2
相符,故A正确;B项,由图像可知,NO、NO 的变化量比为3:1,根据得失电子守恒,反应方程式为
x
3NO(g) NO (g)+NO(g),X是NO, 内生成1molN O,用NO表示的反应速率为
2 2 2 2 2
,故B错误;C项,T 温度下,测得容器内气体颜色保持不变,则表明各成分
1
的浓度不再变化、反应达到化学平衡状态,故C正确;D项,反应物浓度越大、反应温度越高、反应速率
越快,则增大NO气体的浓度、升高反应体系的温度,均能提高反应速率,故D正确;故选B。
7.(2022·湖南省雅礼中学质量检测)下列有关的说法中,其中正确的是
A.在氯酸钾加热分解的反应中,当其他条件相同时,在有催化剂时(a)和无催化剂时(b)的速率~时间
图像可用图一表示
B.若在恒压容器中发生反应:2NH (g) N(g)+3H(g),达到平衡后再充入适量He,其反应速
3 2 2
率~时间图像可用图二表示
C.2NO (g) NO(g),在加热升温的条件下平衡向逆反应方向移动的主要原因是该反应为放热反
2 2 4应,加热温度升高时导致正反应速率减慢、而逆反应速率加快
D.对于可逆反应C(s)+HO(l) CO(g)+H(g),当其他条件相同时,若增加单质碳(C)的量可使
2 2
平衡一定正向移动
【答案】B
【解析】A项,加入催化剂,反应速率增大,a的反应速率应大于b的反应速率,与图像不符合,故A
错误;B项,该反应是一个气体体积增大的反应,在恒压容器中加入He,为保持恒压条件增大体积,使压
强减小,故正逆反应速率均减小,平衡向正反应方向移动,与图像符合,故B正确;C项,升高温度时正、
逆反应速率均加快,由于逆反应速率增大的倍数大于正反应速率增大的倍数,即 > ,则平衡逆向移动,
逆 正
故C错误;D项,碳是固体,增加单质碳(C)的量不影响平衡,故D错误;故选B。
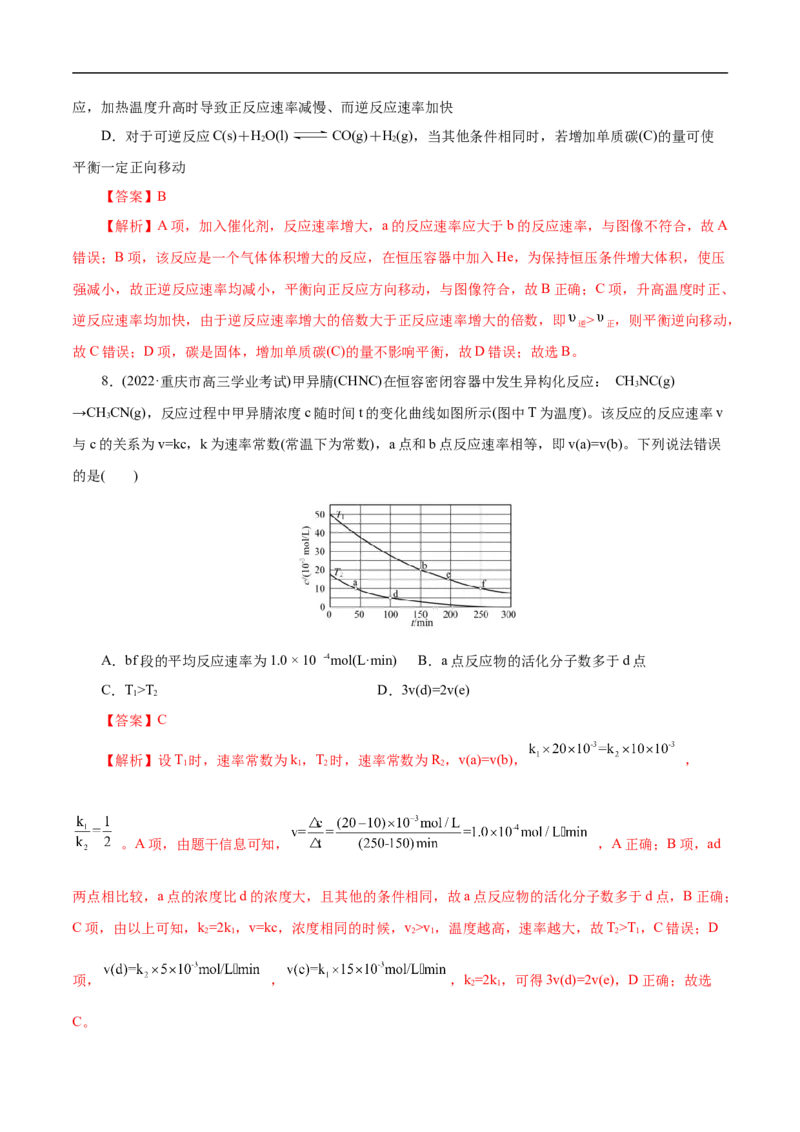
8.(2022·重庆市高三学业考试)甲异腈(CHNC)在恒容密闭容器中发生异构化反应: CHNC(g)
3
→CHCN(g),反应过程中甲异腈浓度c随时间t的变化曲线如图所示(图中T为温度)。该反应的反应速率v
3
与c的关系为v=kc,k为速率常数(常温下为常数),a点和b点反应速率相等,即v(a)=v(b)。下列说法错误
的是( )
A.bf段的平均反应速率为1.0 × 10 -4mol(L·min) B.a点反应物的活化分子数多于d点
C.T>T D.3v(d)=2v(e)
1 2
【答案】C
【解析】设T 时,速率常数为k,T 时,速率常数为R ,v(a)=v(b), ,
1 1 2 2
。A项,由题干信息可知, ,A正确;B项,ad
两点相比较,a点的浓度比d的浓度大,且其他的条件相同,故a点反应物的活化分子数多于d点,B正确;
C项,由以上可知,k=2k,v=kc,浓度相同的时候,v>v,温度越高,速率越大,故T>T,C错误;D
2 1 2 1 2 1
项, , ,k=2k,可得3v(d)=2v(e),D正确;故选
2 1
C。9.(2022·重庆市育才中学模拟预测)在密闭容器中充入1 和1 ,在一定条件下发生反
2NO(g)+2CO(g) N(g)+2CO (g),测得 的平衡转化率与温度及压强的关系如图所示。实验测得,
2 2
, ( 、 为速率常数,只与温度有关),下列说法错误的是(
)
A.达到平衡后,仅升高温度, 增大的倍数小于 增大的倍数
B.若密闭容器( 对应压强下)体积为1L,则b点
C. 的物质的量浓度:b点 点
D.逆反应速率:a点 点
【答案】B
【解析】A项,平衡时,v =v ,即k c2(NO)∙c2(CO)= k c(N )∙c2(CO),升高温度后,正、逆反应的
正 逆 正 逆 2 2
速率增大,但NO的平衡转化率降低,平衡逆向移动,说明逆反应增大的幅度大于正反应,而体系中各组
分的瞬时浓度不变,故k 增大的倍数小于 k 增大的倍数,A正确;B项,a点NO的平衡转化率为80%,
正 逆
CO和NO起始的物质的量均为1mol,根据化学方程式可知CO、NO、N、CO 转化的物质的量分别为
2 2
0.8mol、0.8mol、0.2mol、0.8mol,则CO、NO、N、CO 平衡时的物质的量分别为0.2mol、0.2mol、
2 2
0.2mol、0.8mol,由于容器体积为1L,故CO、NO、N、CO 平衡时的浓度分别为0.2mol/L、0.2mol/L、
2 2
0.2mol/L、0.8mol/L,a点 = = =160;p1对应压强下,b点NO
的平衡转化率还未达到80%,则反应正向进行,即v >v ,故 >160,B错误;C项,a点和b点的
正 逆
NO的起始物质的量相同,a点NO的转化率大于b点,则a点NO转化的物质的量大于b点,故a点剩余NO的物质的量小于b点,由于体积相同,故b点NO的物质的量浓度大于a点,C正确;D项,设压强为
p,温度与a点相同时的点为d点,由C选项可知,d点NO的物质的量浓度大于a点,则a点N、CO 的
2 2 2
浓度大于d点,故a点逆反应速率大于d点;d点和c点的压强相同,d点的温度高于c点,则d点的逆反
应速率大于c点,故a点逆反应速率大于c点,D正确;故选B。
10.(2022·山东省德州市二模)在恒温恒容密闭容器中发生反应2H(g)+2NO(g) 2HO(g)
2 2
+N (g),N 的瞬时生成速率v=k·cm(H )c2 (NO)。控制NO起始浓度为0.5 mol/L,N 的瞬时生成速率和H 起
2 2 2 2 2
始浓度的关系如图所示,下列说法正确的是( )
A.由题可知,该反应的速率常数k为15
B.随着H 起始浓度增大,该反应平衡常数增大
2
C.达平衡后,H 和NO的浓度均增加一倍,则NO转化率减小
2
D.H 起始浓度0.2 mol/L,某时刻NO的浓度为0.4 mol/L,则N 的瞬时生成速率为0.24 mol/L
2 2
【答案】A
【解析】A项,NO起始浓度为0.5 mol/L,由图像可知,N 的瞬时生成速率与H 起始浓度呈直线关系,
2 2
则m=1,将数据(0.2,0.75)代入v=k·c(H )c2 (NO),该反应的速率常数 ,A
2
项正确;B项,反应一定,平衡常数只与温度有关,温度不变,平衡常数不变,B项错误;C项,达平衡
后,H 和NO的浓度均增加一倍,新平衡与原平衡相比,相当于加压,平衡正向移动,则NO转化率增大,
2
C项错误;D项,由2H(g)+2NO(g) 2HO(g) +N (g)可知,NO起始浓度为0.5 mol/L,某时刻NO的浓
2 2 2
度为0.4 mol/L,变化量为0.1 mol/L,则时刻H 的浓度为0.2mol/L-0.1mol/L =0.1mol/L,N 的瞬时生成速率
2 2
为 ,单位错误,D项错误;故选A。
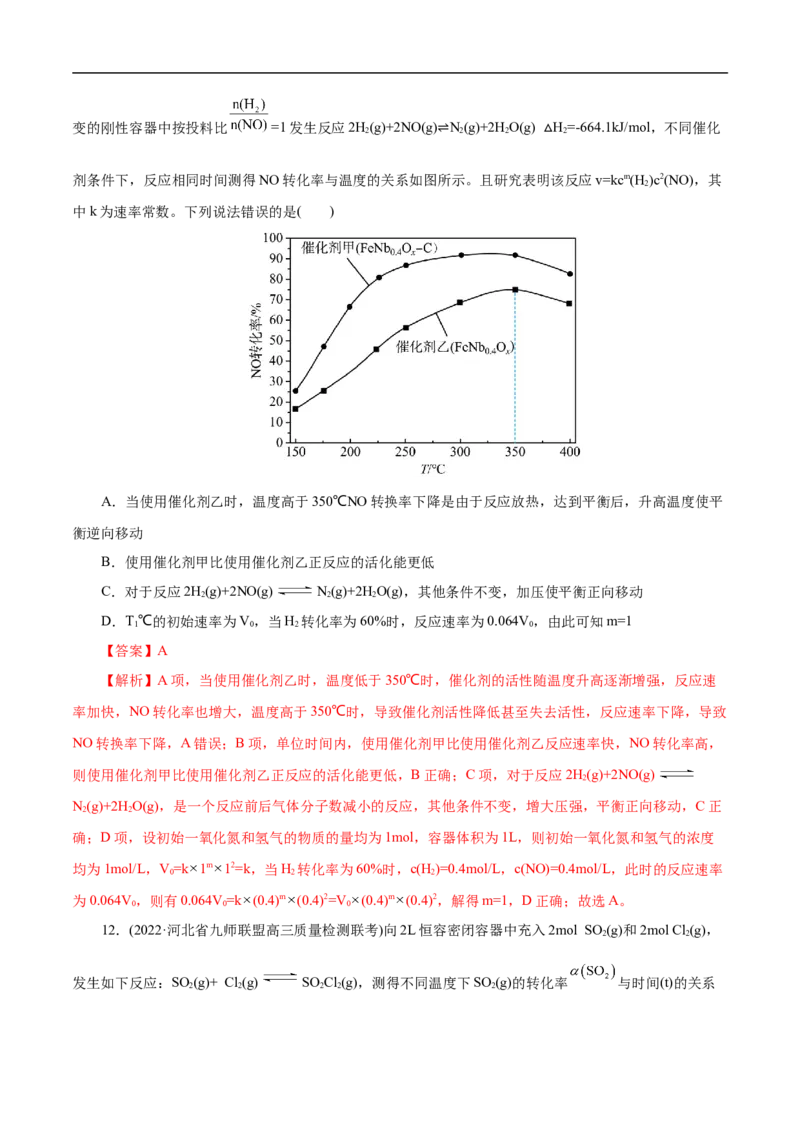
11.(2022·辽宁省高三适应性模拟)含氮化合物在生活、生产、研究领域至关重要。我国学者在容积不变的刚性容器中按投料比 =1发生反应2H(g)+2NO(g) N(g)+2HO(g) H=-664.1kJ/mol,不同催化
2 2 2 2
⇌ △
剂条件下,反应相同时间测得NO转化率与温度的关系如图所示。且研究表明该反应v=kcm(H )c2(NO),其
2
中k为速率常数。下列说法错误的是( )
A.当使用催化剂乙时,温度高于350℃NO转换率下降是由于反应放热,达到平衡后,升高温度使平
衡逆向移动
B.使用催化剂甲比使用催化剂乙正反应的活化能更低
C.对于反应2H(g)+2NO(g) N(g)+2HO(g),其他条件不变,加压使平衡正向移动
2 2 2
D.T℃的初始速率为V,当H 转化率为60%时,反应速率为0.064V ,由此可知m=1
1 0 2 0
【答案】A
【解析】A项,当使用催化剂乙时,温度低于350℃时,催化剂的活性随温度升高逐渐增强,反应速
率加快,NO转化率也增大,温度高于350℃时,导致催化剂活性降低甚至失去活性,反应速率下降,导致
NO转换率下降,A错误;B项,单位时间内,使用催化剂甲比使用催化剂乙反应速率快,NO转化率高,
则使用催化剂甲比使用催化剂乙正反应的活化能更低,B正确;C项,对于反应2H(g)+2NO(g)
2
N(g)+2HO(g),是一个反应前后气体分子数减小的反应,其他条件不变,增大压强,平衡正向移动,C正
2 2
确;D项,设初始一氧化氮和氢气的物质的量均为1mol,容器体积为1L,则初始一氧化氮和氢气的浓度
均为1mol/L,V=k 1m 12=k,当H 转化率为60%时,c(H)=0.4mol/L,c(NO)=0.4mol/L,此时的反应速率
0 2 2
为0.064V ,则有0.064V =k (0.4)m (0.4)2=V (0.4)m (0.4)2,解得m=1,D正确;故选A。
0 0 0
12.(2022·河北省九师联盟高三质量检测联考)向2L恒容密闭容器中充入2mol SO (g)和2mol Cl (g),
2 2
发生如下反应:SO (g)+ Cl (g) SO Cl(g),测得不同温度下SO (g)的转化率 与时间(t)的关系
2 2 2 2 2如图所示。假设反应速率方程为 , (k是速率常数,只与温度有
关),下列说法错误的是( )
A.该反应的ΔH<0 B. 时,
C.M点: D.升高温度, 增大的倍数大于 增大的倍数
【答案】D
【解析】A项,由图知,T>T,温度越高,SO的转化率越小,说明正反应是放热反应,ΔH<0,A
2 1
项正确;B项,T 时,SO 的转化率为80%,平衡时, , ,
1 2
,可算出 ,B项正确;C项,M点为非平衡点,反应正向进行,浓度商小
于K,C项正确;D项,由于该反应ΔH<0,升高温度,平衡逆向移动, , 增大的倍数小于
增大的倍数,D项错误;故选D。
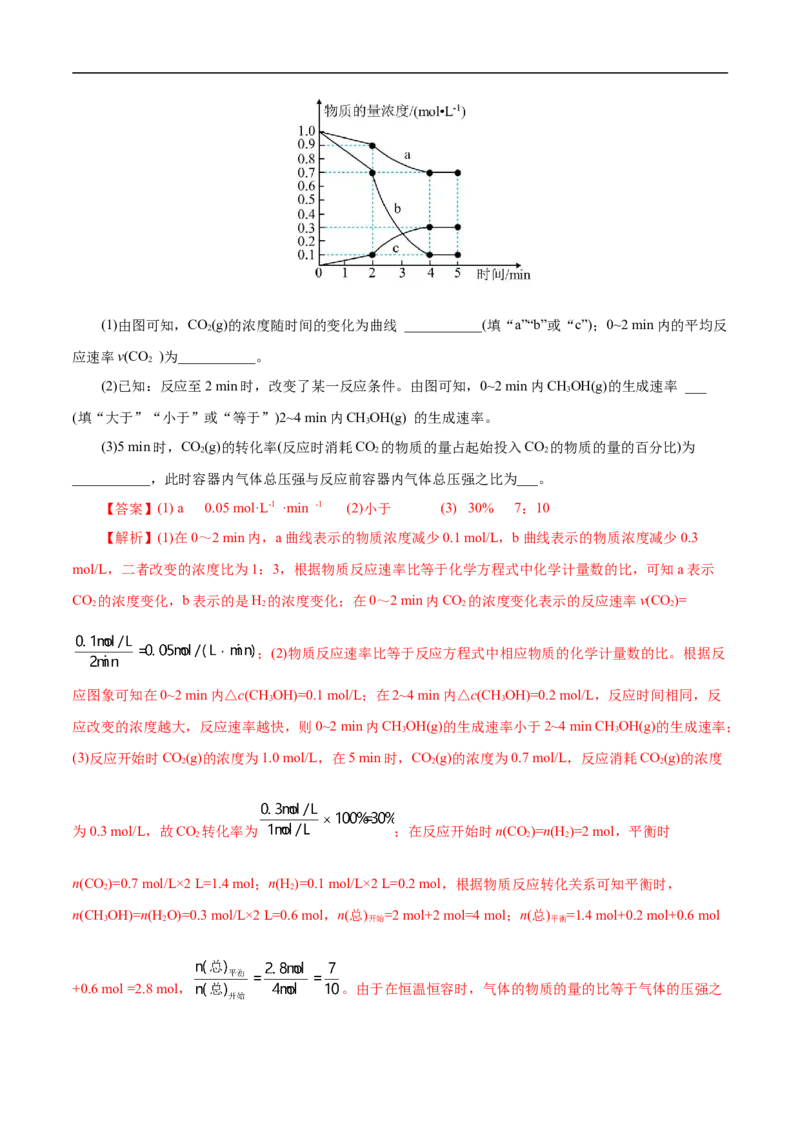
13.(2022·山西省运城市联考)300°C时,向2 L的恒容密闭容器中,充入2 mol CO (g)和2 mol H (g)使
2 2
之发生反应CO(g)+3H(g) CHOH(g)+H O(g),测得各物质的物质的量浓度变化如图所示:
2 2 3 2(1)由图可知,CO(g)的浓度随时间的变化为曲线 ___________(填“a”“b”或“c”);0~2 min内的平均反
2
应速率v(CO )为___________。
2
(2)已知:反应至2 min时,改变了某一反应条件。由图可知,0~2 min内CHOH(g)的生成速率 ___
3
(填“大于”“小于”或“等于”)2~4 min内CHOH(g) 的生成速率。
3
(3)5 min时,CO(g)的转化率(反应时消耗CO 的物质的量占起始投入CO 的物质的量的百分比)为
2 2 2
___________,此时容器内气体总压强与反应前容器内气体总压强之比为___。
【答案】(1) a 0.05 mol·L-1 ·min -1 (2)小于 (3) 30% 7:10
【解析】(1)在0~2 min内,a曲线表示的物质浓度减少0.1 mol/L,b曲线表示的物质浓度减少0.3
mol/L,二者改变的浓度比为1:3,根据物质反应速率比等于化学方程式中化学计量数的比,可知a表示
CO 的浓度变化,b表示的是H 的浓度变化;在0~2 min内CO 的浓度变化表示的反应速率v(CO)=
2 2 2 2
;(2)物质反应速率比等于反应方程式中相应物质的化学计量数的比。根据反
应图象可知在0~2 min内△c(CHOH)=0.1 mol/L;在2~4 min内△c(CHOH)=0.2 mol/L,反应时间相同,反
3 3
应改变的浓度越大,反应速率越快,则0~2 min内CHOH(g)的生成速率小于2~4 min CH OH(g)的生成速率;
3 3
(3)反应开始时CO(g)的浓度为1.0 mol/L,在5 min时,CO(g)的浓度为0.7 mol/L,反应消耗CO(g)的浓度
2 2 2
为0.3 mol/L,故CO 转化率为 ;在反应开始时n(CO)=n(H )=2 mol,平衡时
2 2 2
n(CO)=0.7 mol/L×2 L=1.4 mol;n(H )=0.1 mol/L×2 L=0.2 mol,根据物质反应转化关系可知平衡时,
2 2
n(CHOH)=n(H O)=0.3 mol/L×2 L=0.6 mol,n(总) =2 mol+2 mol=4 mol;n(总) =1.4 mol+0.2 mol+0.6 mol
3 2 开始 平衡
+0.6 mol =2.8 mol, 。由于在恒温恒容时,气体的物质的量的比等于气体的压强之比,所以平衡时容器内气体总压强与反应前容器内气体总压强之比为p(平衡):p(开始)=7:10。