文档内容
第六篇 物质结构与性质
专项 40 大 π 键
共价键的类型按成键方式可分为 σ键和π键。大π键作为π键概念的延伸与拓展,常见于信息题中。
由三个或三个以上的原子形成的π键,在多原子分子或离子中,如有相互平行的 p轨道,它们连贯重叠在
一起构成一个整体,p电子在多个原子间运动形成π型化学键,这种不局限在两个原子之间的π键称为离
域π键或共轭大π键,简称大π键,表达式 :m代表参与形成大π键的原子数,n代表参与形成大π键
Πn
m
的电子数;大π键具有特殊的稳定性。常见分子(或离子)的大π键见下表:
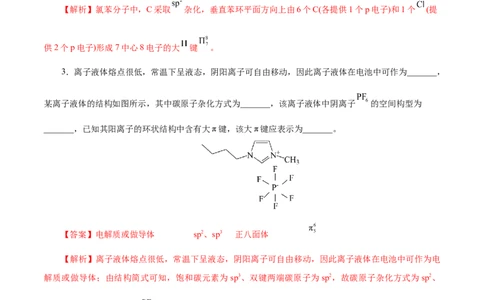
1.(2017•新课标Ⅱ卷节选)我国科学家最近成功合成了世界上首个五氮阴离子盐(N ) (H O) (NH )
5 6 3 3 4
Cl(用R代表),其局部结构如图所示:
4
R中阴离子N—中的σ键总数为 个。分子中的大π键可用符号Π n表示,其中m代表参与
5 m
形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中的大π键可表示为Π6),则N—中的大π
6 5
键应表示为 。
【答案】5N Π 6
A 5
【解析】根据图(b)N ﹣中键总数为5N 个,根据信息,N﹣有6个电子可形成大π键,可用符号Π6表
5 A 5 5
示,故答案为:5N ;Π6。
A 5
2.(2017•新课标III 卷节选)硝酸锰是某种催化剂的原料,Mn(NO) 中的化学键除了σ键外,还存在
3 2
________。【答案】离子键和π键(或 键)
【解析】硝酸锰是离子化合物,硝酸根和锰离子之间形成离子键,硝酸根中 N原子与3个氧原子形成
3个σ键,硝酸根中有一个氮氧双键,所以还存在π键。
大π键中电子数的确定方法
1.分子或离子团中的大π键可表示为 ,其中m表示参与形成大π键的原子数,n表示参与形成大π
键的电子数。已知环戊二烯阴离子(C H-)的结构与苯分子相似,具有芳香性。苯分子中大π键可表示为 ,
5 5
则C H-中大π键应表示为_______。
5 5
【答案】
【解析】根据题意C H-中5个碳原子大π键,每个碳原子有一个电子, 又得到一个电子,因此
5 5
C H-形成大π键应表示为 。
5 52.氯苯 分子中,C采取____杂化,杂化轨道分别与C、H(或Cl)形成σ键,并且Cl的
3p,轨道与C未参与杂化的2p 轨道形成大Π键,可表示为____。(已知m中心n电子的大Π键可表示为
x x
Π )。
【答案】sp2 Π
【解析】氯苯分子中,C采取 杂化,垂直苯环平面方向上由6个C(各提供1个p电子)和1个 (提
供2个p电子)形成7中心8电子的大 键 。
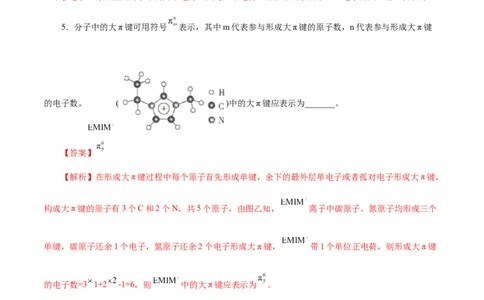
3.离子液体熔点很低,常温下呈液态,阴阳离子可自由移动,因此离子液体在电池中可作为_______,
某离子液体的结构如图所示,其中碳原子杂化方式为_______,该离子液体中阴离子 的空间构型为
_______,已知其阳离子的环状结构中含有大π键,该大π键应表示为_______。
【答案】电解质或做导体 sp2、sp3 正八面体
【解析】离子液体熔点很低,常温下呈液态,阴阳离子可自由移动,因此离子液体在电池中可作为电
解质或做导体;由结构简式可知,饱和碳元素为 sp3、双键两端碳原子为sp2,故碳原子杂化方式为sp2、
sp3;该离子液体中阴离子 中有6个共价键,根据电子对互斥理论可知,空间构型为正八面体;已知其
阳离子的环状结构中含有大π键,由图可知,该大π键为5个原子和6个电子形成的,应表示为 。
4.依据VSEPR模型推测 的空间结构为_______。分子中的大 键可用符号 表示,其中m代
表参与形成大 键的原子数,n代表参与形成大 键的电子数(如苯分子中的大 键可表示为 ),则中的大 键应表示为_______。
【答案】平面三角形
【解析】 中C原子价电子对数为 ,无孤电子对,空间结构为平面三角形。 中碳原子
sp²杂化,有一个未参与杂化的p电子,然后三个氧原子上分别有一个垂直于离子平面的p轨道,分别提供
一个p电子,再加上负离子中的两个电荷一共是六个电荷,所以形成了四中心六电子的大π键,表示为 。
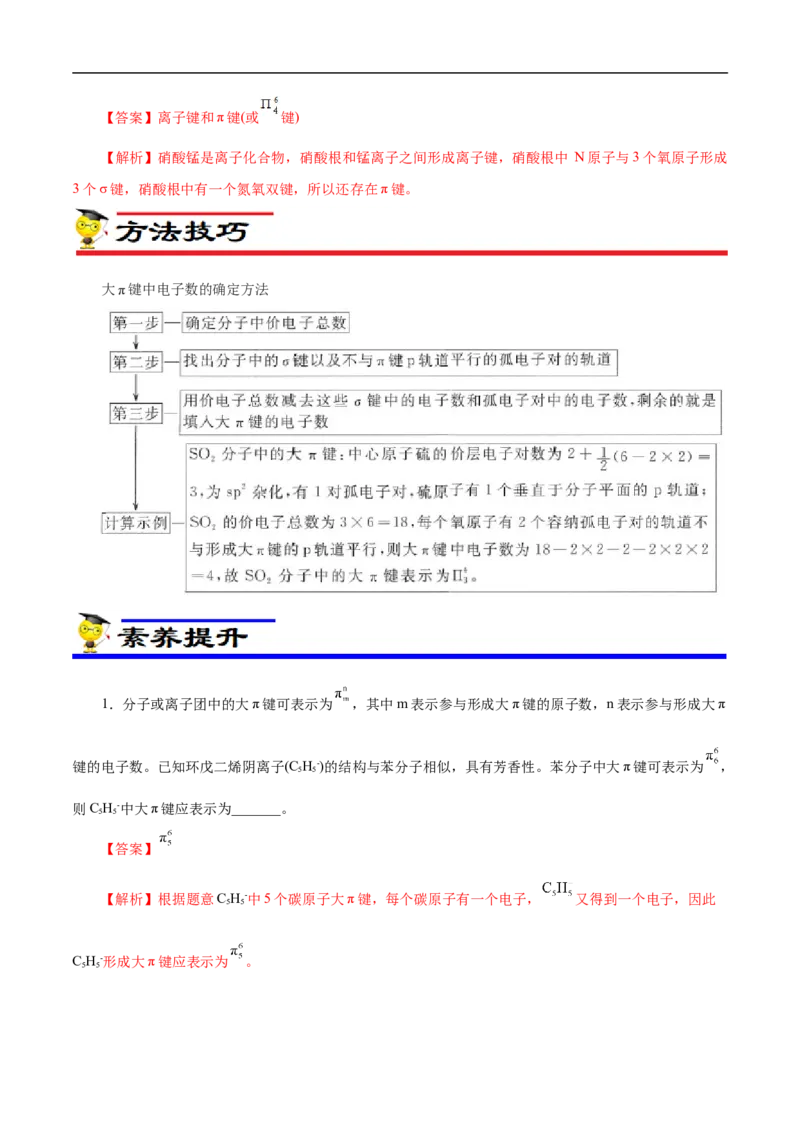
5.分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键
的电子数。 ( )中的大π键应表示为_______。
【答案】
【解析】在形成大π键过程中每个原子首先形成单键,余下的最外层单电子或者孤对电子形成大π键,
构成大π键的原子有3个C和2个N,共5个原子,由图乙知, 离子中碳原子、氮原子均形成三个
单键,碳原子还余1个电子,氮原子还余2个电子形成大π键, 带1个单位正电荷,则形成大π键
的电子数=3 1+2 -1=6,则 中的大π键应表示为 。
6. ( )中阴离子 中的σ键总数为_______个。分子中的大 键可用符
号 表示,其中m代表参与形成大 键的原子数,n代表参与形成大 键的电子数(如苯分子中的大 键可表示为 ),则 中的大 键应表示为_______。
【答案】5
【解析】由图中 的结构可知 中的 键数为5; 中的5个原子参与形成大 键,每个原子中参
与形成大 键的电子数为1(孤电子对不参与),故参与形成大 键的电子数为 , 中大 键应表示
为 。
7.已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个
原子间运动,形成“离域π键”(或大π键)。大π键可用 表示,其中m、n分别代表参与形成大π键的
原子个数和电子数,如苯分子中大π键表示为 。
(1)下列微粒中存在“离域Π键”的是___。
A.CH=CH—CH=CH B.CCl C.HO D.SO
2 2 4 2 2
(2)NaN 中阴离子N-与CO 互为等电子体,均为直线型结构,N-中的2个大π键可表示为___。
3 3 2 3
【答案】(1)AD (2)Π
【解析】(1)CH =CH—CH=CH 、SO 分子中各原子共面,且原子之间均有相互平行的p轨道,可以形
2 2 2
成大Π键,水分子中氢原子没有p轨道,不能形成大Π键,CCl 是正四面体构型,各原子不共面,不能形
4
成大Π键,因此微粒中存在“离域Π键”的是AD;(2)N -与CO 互为等电子体,均为直线型结构,根据二
3 2
氧化碳的结构可以判断出N-中σ键为2个,该离子中两边的氮原子提供1个电子,中间氮原子提供2个电
3
子形成大Π键,所以形成的2个大π键可表示为Π4。
3
8.碳可以形成多种有机化合物,右图所示是噻吩的结构,分子中所有原子都在一个平面上。
(1)噻吩结构中C原子的杂化方式为_______。
(2)分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 )。请问噻吩中的大π键表示为_______。
【答案】(1)sp2杂化 (2)
【解析】(1)碳碳双键中C采取sp2杂化,噻吩结构中C原子的杂化方式为sp2杂化;(2)噻吩分子为平
面结构,S原子价电子排布式为3s23p4,形成两根共价键,环中存在两根π键,为单双建交替,p 轨道交盖
z
可形成离域大π键,S的p 轨道中一对电子与环上的π电子共轭,形成离域大π键,形成五中心六电子的
z
离域大π键,噻吩中的大π键表示为 。
9.下图是两种石墨材料局部结构示意图,其中石墨烯中碳原子紧密堆积成单层二维蜂窝状晶格结构。
石墨烯具有良好的导电性,其中碳原子杂化轨道类型为_______,大π键表示为_______(用n表示电子数),
氧化石墨烯具有较好的亲水性的原因是_______。
【答案】sp2 氧化石墨烯中存在O-H键,它能够与水分子形成氢键,导致氧化石墨烯具有较
好的亲水性
【解析】C为6号元素,其价电子排布式为2s22p2,石墨烯(即单层石墨)是一种碳原子构成的单层二维
蜂窝状晶格结构的新材料,其中碳原子采取sp2杂化,石墨烯每层中的碳原子各有1个未参与杂化的2p轨
道并含有1个电子,n个2p轨道互相平行形成了大π键,该大π键可表示为 。由图可知氧化石墨烯中存
在O-H键,它能够与水分子形成氢键,所以氧化石墨烯具有较好的亲水性。