文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题01 化学用语
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
化学用语题型主要以选择题的形式呈现,整体难度不大,但是考察得非常细。因此,要求考生在复习
的时候,注意把握不同化学用语之间的区别,注意特殊性。预计在2025年高考中,化学用语的考查内容主
要包括物质组成和结构的各种图示,化学反应的各种表达式等。其中结构示意图、核外电子排布式、结构
式、球棍模型、比例模型、核素表示方法等仍是高频考点。复习时要特别关注以下几点:
①区分化学式和实验式的概念。
②结构式和结构简式的区别、注意官能团的正确书写。
③易错物质的电子式的书写。
③球棍模型和填充模型的区别。
⑤区分有机物的习惯命名法和系统命名法。
另外,要特别关注杂化轨道重叠的图示表达、电子云图的表达、VSEPR模型的图示表达、配位化合
物结构的书写等。
1.(2024·广西·高考真题)光照时,纳米 能使水产生羟基自由基 ,可用于处理废水。下列表述正
确的是
A.基态Ti的价电子排布式: B. 的电子式:
C. 的VSEPR模型: D.O的一种核素:
【答案】B
【详解】A.基态Ti的价电子排布式:3d24s2,A错误;
B. 含有1个未成对电子,电子式: ,B正确;
C.HO中心O原子价层电子对数为 ,O原子采用sp3杂化,O原子上含有2对孤电子对,
2
的VSEPR模型为 ,C错误;
D.核素的表示方法为:元素符号左下角为质子数,左上角为质量数;O质子数为8,则O的一种核素不
会是 ,D错误;故选B。
2.(2024·贵州·高考真题)下列叙述正确的是
A.KBr的电子式:
B.聚乙炔的结构简式:
C. 的空间结构:平面三角形
D. 的名称:2-甲基-2-丁烯
【答案】B
【详解】A.KBr的电子式为 ,A错误;
B.聚乙炔的结构为单双键交替结构,结构简式为 ,B正确;
C. 中心原子的价层电子对数为4,孤电子对数为1,空间结构为三角锥形,C错误;
D.CHCHC(CH)=CH 的系统命名为2-甲基-1-丁烯,D错误;
3 2 3 2
故选B。
3.(2024·浙江·高考真题)下列表示不正确的是
A. 的电子式: B. 中共价键的电子云图:
C. 的空间填充模型: D.3,3-二甲基戊烷的键线式:
【答案】A
【详解】A. 的电子式: ,故A错误;
B.Cl 中的共价键是由2个氯原子各提供1个未成对电子的3p原子轨道重叠形成的,共价键电子云图为:
2
,故B正确;
C. 的中心原子N形成3个σ键和1个孤电子对,为sp3杂化, 为三角锥形,空间填充模型:
,故C正确;
D.3,3-二甲基戊烷的主链上有5个C,3号碳上连接有2个甲基,键线式为: ,故D正确;
故选A。
4.(2024·甘肃·高考真题)下列化学用语表述错误的是A. 和 的最外层电子排布图均为
B. 和 的电子式分别为 和
C. 的分子结构模型为
D. 、 和 互为同位素
【答案】B
【详解】A.Ca2+和Cl-的核外电子数都是18,最外层电子排布图均为 ,故A正确;
B.PH 中磷原子和每个氢原子共用一对电子,中心原子P原子价层电子对数为3+ ×(5-3×1)=4,孤电子对
3
数为1,PH 的电子式为 ,故B错误;
3
C.CH=CHCHCHCH 分子中存在1个碳碳双键,位于1号碳原子与2号碳原子之间,存在3个碳碳单
2 2 2 3
键,无支链,且氢原子半径小于碳原子半径,其分子结构模型表示为 ,故C正确;
D. 、 和 是质子数相同、中子数不同的碳原子,是碳元素的不同核素,互为同位素,故D正确;
故选B。
5.(2024·湖南·高考真题)下列化学用语表述错误的是
A. 的电子式:
B.异丙基的结构简式:
C.NaCl溶液中的水合离子:
D. 分子中 键的形成:【答案】C
【详解】A. 由Na+和OH-构成,电子式为: ,故A正确;
B.异丙基的结构简式: ,故B正确;
C.Na+离子半径比Cl-小,水分子电荷情况如图 ,Cl-带负电荷,水分子在Cl-周围时,呈正电性
的H朝向Cl-,水分子在Na+周围时,呈负电性的O朝向Na+,NaCl溶液中的水合离子应为: 、
,故C错误;
D. 分子中的共价键是由2个氯原子各提供1个未成对电子的3p原子轨道重叠形成的p-pσ键,形成过
程为: ,故D正确;
故选C。
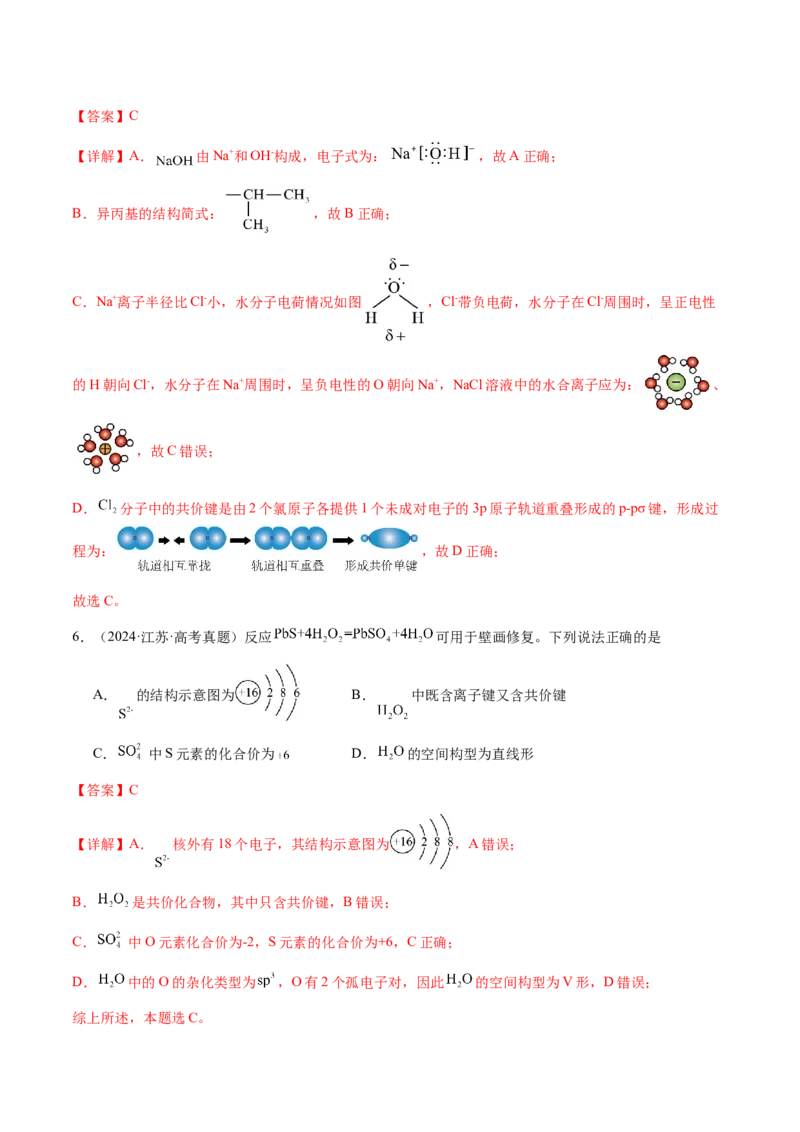
6.(2024·江苏·高考真题)反应 可用于壁画修复。下列说法正确的是
A. 的结构示意图为 B. 中既含离子键又含共价键
C. 中S元素的化合价为 D. 的空间构型为直线形
【答案】C
【详解】A. 核外有18个电子,其结构示意图为 ,A错误;
B. 是共价化合物,其中只含共价键,B错误;
C. 中O元素化合价为-2,S元素的化合价为+6,C正确;
D. 中的O的杂化类型为 ,O有2个孤电子对,因此 的空间构型为V形,D错误;
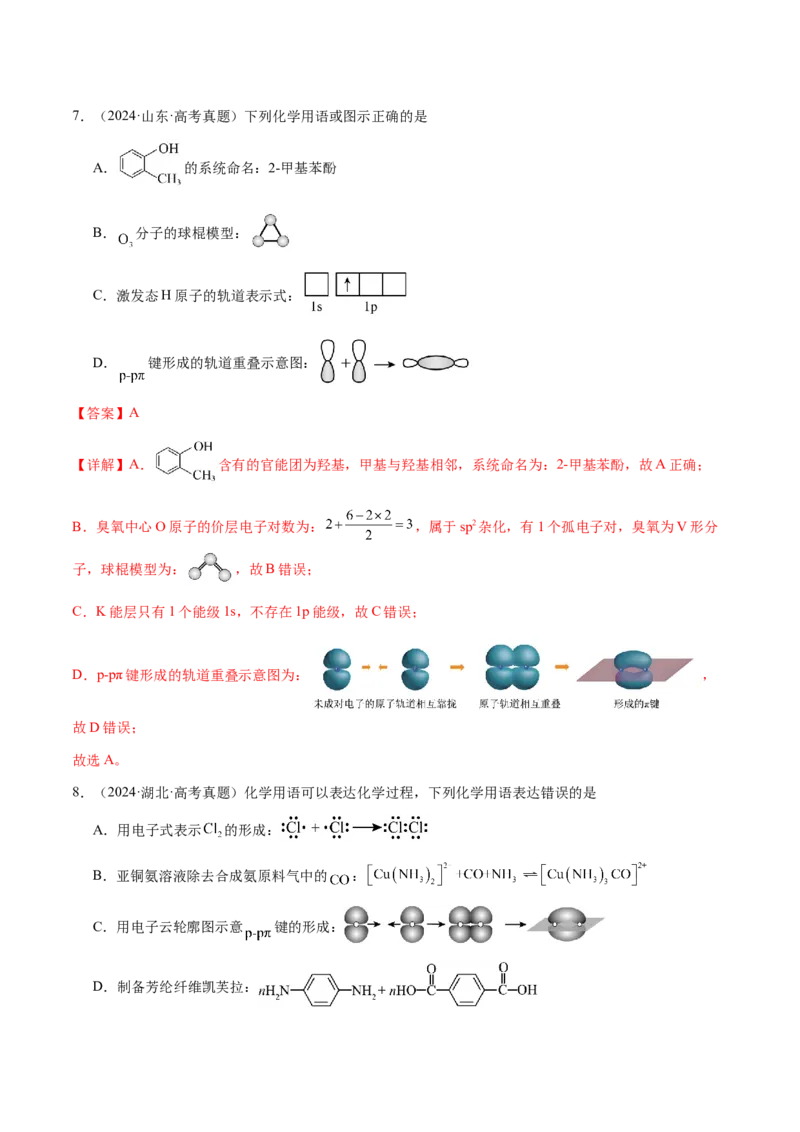
综上所述,本题选C。7.(2024·山东·高考真题)下列化学用语或图示正确的是
A. 的系统命名:2-甲基苯酚
B. 分子的球棍模型:
C.激发态H原子的轨道表示式:
D. 键形成的轨道重叠示意图:
【答案】A
【详解】A. 含有的官能团为羟基,甲基与羟基相邻,系统命名为:2-甲基苯酚,故A正确;
B.臭氧中心O原子的价层电子对数为: ,属于sp2杂化,有1个孤电子对,臭氧为V形分
子,球棍模型为: ,故B错误;
C.K能层只有1个能级1s,不存在1p能级,故C错误;
D.p-pπ键形成的轨道重叠示意图为: ,
故D错误;
故选A。
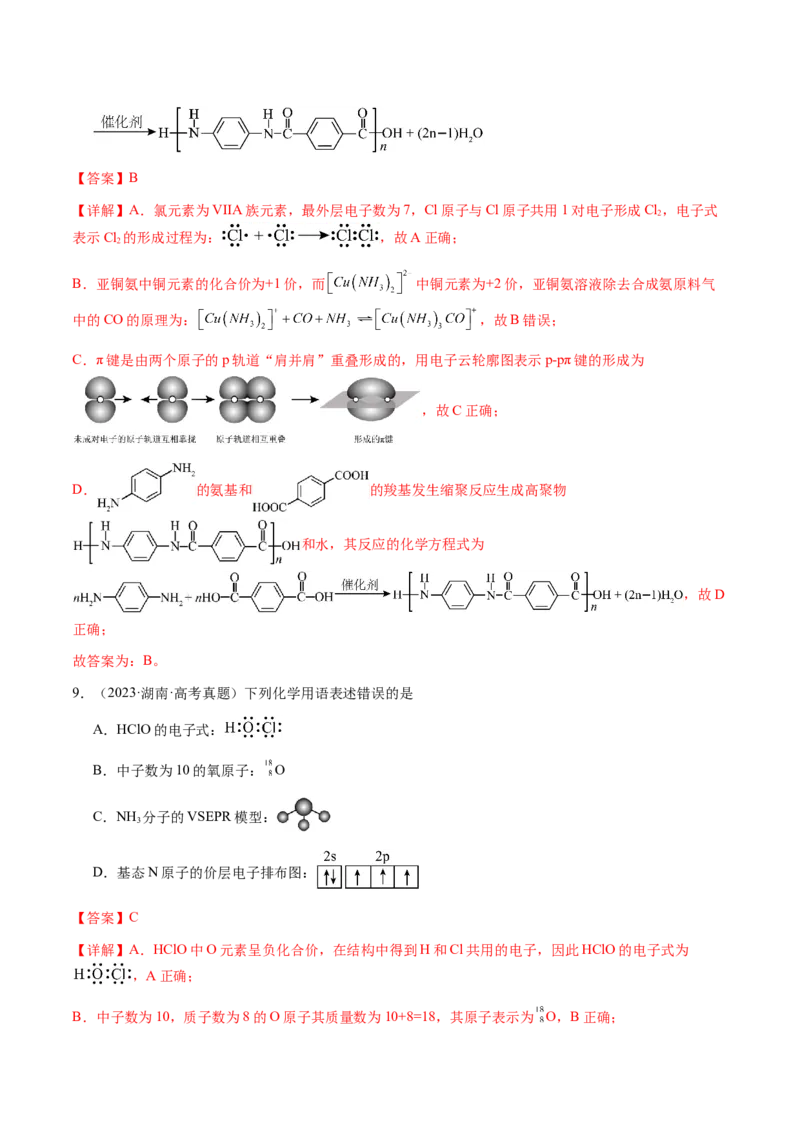
8.(2024·湖北·高考真题)化学用语可以表达化学过程,下列化学用语表达错误的是
A.用电子式表示 的形成:
B.亚铜氨溶液除去合成氨原料气中的 :
C.用电子云轮廓图示意 键的形成:
D.制备芳纶纤维凯芙拉:【答案】B
【详解】A.氯元素为VIIA族元素,最外层电子数为7,Cl原子与Cl原子共用1对电子形成Cl,电子式
2
表示Cl 的形成过程为: ,故A正确;
2
B.亚铜氨中铜元素的化合价为+1价,而 中铜元素为+2价,亚铜氨溶液除去合成氨原料气
中的CO的原理为: ,故B错误;
C.π键是由两个原子的p轨道“肩并肩”重叠形成的,用电子云轮廓图表示p-pπ键的形成为
,故C正确;
D. 的氨基和 的羧基发生缩聚反应生成高聚物
和水,其反应的化学方程式为
,故D
正确;
故答案为:B。
9.(2023·湖南·高考真题)下列化学用语表述错误的是
A.HClO的电子式:
B.中子数为10的氧原子: O
C.NH 分子的VSEPR模型:
3
D.基态N原子的价层电子排布图:
【答案】C
【详解】A.HClO中O元素呈负化合价,在结构中得到H和Cl共用的电子,因此HClO的电子式为
,A正确;
B.中子数为10,质子数为8的O原子其质量数为10+8=18,其原子表示为 O,B正确;C.根据VSEPR模型计算,NH 分子中有1对孤电子对,N还连接有3和H原子,因此NH 的VSEPR模型
3 3
为四面体型,C错误;
D.基态N原子的价层电子排布为2s22p3,其电子排布图为 ,D正确;
故答案选C。
10.(2023·湖北·高考真题)化学用语可以表达化学过程,下列化学用语的表达错误的是
A.用电子式表示 的形成:
B.用离子方程式表示 溶于烧碱溶液:
C.用电子云轮廓图表示H-H的s-sσ键形成的示意图:
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂:
【答案】D
【详解】A.钾原子失去电子,硫原子得到电子形成硫化钾,硫化钾为离子化合物,用电子式表示 的
形成: ,A正确;
B.氢氧化铝为两性氢氧化物,可以和强碱反应生成四羟基合铝酸根离子,离子方程式为:
,B正确;
C.H的s能级为球形,两个氢原子形成氢气的时候,是两个s能级的原子轨道相互靠近,形成新的轨道,
则用电子云轮廓图表示H-H的s-sσ键形成的示意图: ,C
正确;
D.用化学方程式表示尿素与甲醛制备线型脲醛树脂为
,D错误;
故选D。
【策略1】掌握常用的图式及注意事项(1)核素(原子或离子)符号
举例 易错点整理
C、Cl、Cl-、Mg2+
(1)左上角错写成中子数;
(2)左上角漏写质量数。
(2)核反应方程表示
举例 易错点整理
(1)核聚变、核裂变属于核反应,不是化学变化。
钋209的α衰变:Po→Pb+He (2)核反应遵循的两守恒:
查德威克发现中子:Be+He→C+n
①反应前后质量数之和不变。
铀核裂变反应:U+n→Kr+Ba+3n
②反应前后质子数之和不变。
(3)抓住描述对象,突破“四同”判断
同位素——原子,如 H、H。
同素异形体——单质,如O、O。
2 3
同系物——化合物,如CHCH、CHCHCH。
3 3 3 2 3
同分异构体——化合物,如正戊烷、新戊烷。
(4)原子(离子)结构示意图
举例 易错点整理
(1)最外层电子数写错,即原子的结构示意图与离子的结构示意图混
淆;
(2)核电荷数与相对原子质量混淆,如氮元素的核电荷数错误的写成
Cl: S2-:
+14等。【策略2】掌握常考的电子式及注意事项
举例 易错点整理
电子式书写的常见错误:
a、漏写未参与成键的电子,如:
。
b、化合物类型不清楚,漏写或多写[ ]及错写电荷数,如:
, 正 确 应 为
。
c、书写不规范,错写共用电子对,如:
CO 的 电 子 式 为 , 不 能 写 成
2
;N 的电子式为 ,不能写成
2
。
d、原子结合顺序写错,如:
HClO的电子式为 。
e、复杂阳离子与简单阳离子混淆不清,如:
Na+电子式的正确表示应为Na+,误写成 ;
NH电子式的正确表示应为 ,误写成NH。
f、不考虑AB 型离子化合物中2个B是分开写还是一起写,如:
2
CaBr 、CaC 的电子式分别为 、
2 2
。(1)原子的电子式:
氢原子 氯原子 氮原子 钠原子 氧原子 钙原子
O Ca
(2)简单阳离子(单核)的电子式:
钠离子 锂离子 镁离子 铝离子
Na+ Li+ Mg2+ Al3+
(3)简单阴离子(单核)的电子式:
Cl- O2- S2- N3-
— 2— 2— 3—
Cl O S N
(4)原子团的电子式:
NH + HO+ OH- O2- S2- C 2-
4 3 2 2 2
H + + — 2— 2— 2—
H N H H O H O H O O S S C C
H H
(5)共价化合物的电子式(共价分子):
分子 Cl O N HO NH
2 2 2 2 3
电子式 Cl Cl O O N N H O H
结构式 Cl Cl O O N N H O H
分子 CH CO HO HClO C H
4 2 2 2 2 2
H
电子式 H C H O C O H O O H H O Cl
HH
结构式 H C H O C O H O O H H O Cl H—C≡C—H
H
分子 CCl BF PCl PCl
4 3 3 5
Cl
Cl
F B F Cl P Cl
电子式 Cl C Cl Cl P Cl
F Cl
Cl Cl Cl
Cl
Cl
F B F Cl P Cl
结构式 Cl C Cl Cl P Cl
F Cl
Cl Cl
Cl
(6)离子化合物的电子式:
CaO KO CaF NaOH NaClO NaH
2 2
Ca 2+ O 2— K + O 2— K + F — Ca 2+ F — Na + O H — Na + H —
CaC NaO FeS NH Cl NH
2 2 2 2 4 5
Ca 2+ C C 2— Na + O O 2 N — a + Fe 2+ S S 2— H N H H + Cl — H N H H + H —
H H
MgN NaN Al S
3 2 3 2 3
3—
Mg 2+ N 3— Mg 2+ N 3— Mg 2+ Na+ N Na+ S 2— Al 3+ S 2— Al 3+ S 2—
Na+
(7)用电子式表示化合物的形成过程
①用电子式表示共价化合物的形成过程:共价键的形成用电子式表示时,前面写出成键原子的电子式,后
面写出共价分子的电子式,中间用一箭头“→”连起来即可,如:
H: H + H H H
2
Cl + Cl Cl Cl
Cl:
2
HO:
2
HF:②用电子式表示离子化合物的形成过程:离子键的形成用电子式表示式时,前面写出成键原子的电子式,
后面写出离子化合物的电子式,中间用一箭头“→”连起来即可,如:
+ —
Na + Cl Na Cl
NaCl:
CaF :
2
NaS:
2
【策略3】注意区别最简式(实验式)、结构式、结构简式、键线式
最简式(实验式) 乙烯:CH 乙酸:CHO
2 2
结构式
乙醇: 甲烷:
结构简式 乙醇:CHCHOH
3 2
键线式
丙烯: 1,3 -丁二烯:
结构简式的易错点:
①氢原子个数多写(或少些);
②官能团的书写必须注意规范性,例如碳碳双键为“ ”,而不能写成“C===C”,碳碳三键
为“ ”,而不能写成“ ”,醛基应为“—CHO”,而不能写成“—COH”。
③写成结构式或分子式;
④相对位置关系写错,
键线式书写要注意的几个问题:
①一般表示3个及以上碳原子的有机物。
②只忽略C—H键,其余的化学键不能忽略。
③必须表示出 、—C≡C—等官能团。
④碳、氢原子不标注,其余原子必须标注(含羟基、醛基和羧基中氢原子)。
【策略4】注意区别球棍模型和比例模型
(1)注意原子的相对大小
球棍模型
CH: 乙烯: (2)注意微粒的空间构型
4比例(填充)模型
CH: 乙烯:
4
【策略5】原子核外电子的排布表示方法
表示方法 以铁原子为例
电子排布式 1s22s22p63s23p63d64s2
简化电子排布式 [Ar]3d64s2
价电子(外围电子、特征电
3d64s2
子)排布式
最外层电子排布式 4s2
M层电子排布式 3s23p63d6
最高能级电子排布式 3d6
电子排布图(轨道表示式)
价电子排布图
易错点整理:
(1)电子排布式
①原子的核外电子排布式的书写:首先明确原子的核外电子数,然后根据构造原理按顺序填充电子并
检查是否符合洪特规则特例,最后将相同能层的能级写在一起。如Cu:1s22s22p63s23p63d104s1。
②离子核外电子排布式的书写方法:先写出基态原子的核外电子排布式,再失去电子或补充电子(基
态原子失去电子时总是优先失去最外层电子),即得到相应阳离子或阴离子的核外电子排布式。
电子排布式能直观地反映核外电子的能层、能级和各能级上的电子数,但不能表示原子核的情况,
也不能表示各个电子的运动状态。
(2)简化电子排布式
一般用“[稀有气体]+价层电子”的形式表示。如Cu:[Ar]3d104s1。但31号元素(Ga)及以后的主族p区元素书写简化电子排布式时除价层电子外还应加上nd10,如 As:[Ar]3d104s24p3。
33
(3)价层电子排布式
对于主族元素和0族元素,写出最外层电子排布式即可;对于过渡金属元素,其价层电子排布式一
般符合(n-1)d1~10ns1~2(n≥4)。价层电子排布式能反映基态原子的能层数和参与成键的电子数以及最外层电
子数。
(4)电子排布图(轨道表示式)
核外电子排布图能直观地反映出原子的核外电子的自旋情况以及成对的电子对数和未成对电子数。
【策略6】原子轨道及重叠方式
(1)原子轨道模型
符号 s p d
球形 纺锤形(哑铃形) 花瓣形
电子云形状
(2)杂化轨道模型
杂化方式 sp sp2 sp3
杂化轨道构型
(3)轨道重叠方式
a.“头碰头”重叠为σ键,σ键的特征:电子云为轴对称,即是以形成化学键的两个原子核的连线为
轴作旋转操作,σ键电子云的图形不变。利用电子云描述σ键的形成过程:
ss σ键:两个成键原子均提供 s轨道形成的
共价键。
sp σ键:两个成键原子分别提供s轨道和p
轨道形成的共价键。pp σ键:两个成键原子均提供p轨道形成的
共价键。
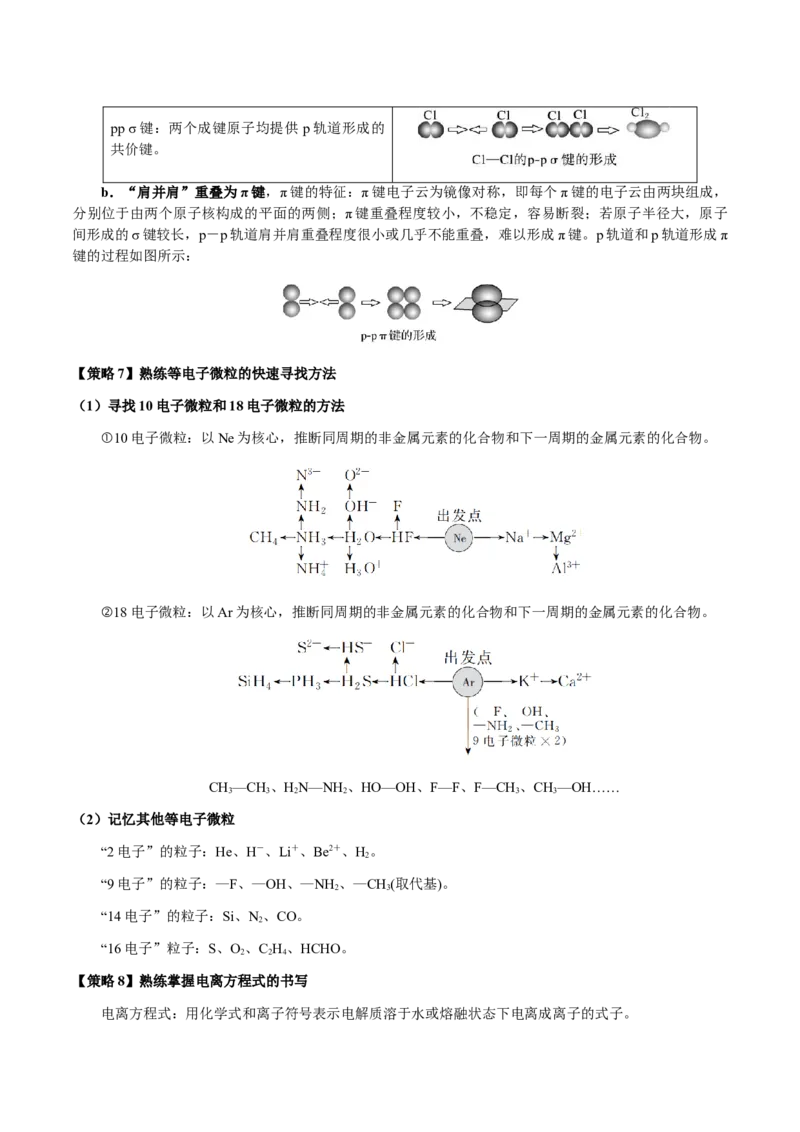
b.“肩并肩”重叠为π键,π键的特征:π键电子云为镜像对称,即每个π键的电子云由两块组成,
分别位于由两个原子核构成的平面的两侧;π键重叠程度较小,不稳定,容易断裂;若原子半径大,原子
间形成的σ键较长,p-p轨道肩并肩重叠程度很小或几乎不能重叠,难以形成π键。p轨道和p轨道形成π
键的过程如图所示:
【策略7】熟练等电子微粒的快速寻找方法
(1)寻找10电子微粒和18电子微粒的方法
①10电子微粒:以Ne为核心,推断同周期的非金属元素的化合物和下一周期的金属元素的化合物。
②18电子微粒:以Ar为核心,推断同周期的非金属元素的化合物和下一周期的金属元素的化合物。
CH—CH、HN—NH、HO—OH、F—F、F—CH 、CH—OH……
3 3 2 2 3 3
(2)记忆其他等电子微粒
“2电子”的粒子:He、H-、Li+、Be2+、H。
2
“9电子”的粒子:—F、—OH、—NH 、—CH(取代基)。
2 3
“14电子”的粒子:Si、N、CO。
2
“16电子”粒子:S、O、C H、HCHO。
2 2 4
【策略8】熟练掌握电离方程式的书写
电离方程式:用化学式和离子符号表示电解质溶于水或熔融状态下电离成离子的式子。(1)强电解质的电离方程式中,用“===”连接,弱电解质(包括弱酸的酸式酸根)的电离方程式中,用“
”连接。例如:
NaSO ===2Na++SO;NaOH===Na++OH-
2 4
HClO H++ClO-;CHCOOH H++CHCOO-
3 3
(2)多元弱酸的电离分步书写,多元弱碱的电离一步写完。例如:
HCO:HCO H++HCO(决定HCO 的酸性),HCO H++CO;
2 3 2 3 2 3
Fe(OH) :Fe(OH) Fe3++3OH-。
3 3
(3)两性氢氧化物:双向电离,如Al(OH) 的电离方程式:
3
H++AlO+HO Al(OH) Al3++3OH-
2 3
(4)酸式盐的电离,强酸酸式盐与弱酸酸式盐的阴离子电离方程式不同。
a.弱酸的酸式盐在溶液中完全电离,生成酸式酸根离子和阳离子,如:NaHCO ===Na++HCO
3
b.强酸的酸式盐在水溶液中完全电离,如:NaHSO===Na++H++SO (水溶液中)
4
c.强酸的酸式盐在熔融状态时,生成酸式酸根离子和阳离子,如:NaHSO===Na++HSO (熔融状态)
4
【策略9】盐类水解方程式的书写
盐类水解的离子方程式一般应用“ ”连接,且一般不标“↑”“↓”等状态符号,且盐类水解
的离子方程式同样遵循质量守恒定律和电荷守恒规律。
盐的离子+HO 弱酸(或弱碱)+OH-(或H+)
2
(1)一元强酸弱碱盐水解:如NH Cl水解的离子方程式为NH+HO NH ·H O+H+。
4 2 3 2
(2)一元强碱弱酸盐水解:如CHCOONa水解的离子方程式为CHCOO-+HO CHCOOH+OH-;
3 3 2 3
(3)多元弱酸盐水解:多元弱酸根离子水解的离子方程式应分步书写,水解是以第一步水解为主。如
NaCO 水解的离子方程式为CO+HO HCO+OH-、HCO+HO HCO+OH-。
2 3 2 2 2 3
(4)多元弱碱盐水解:多元弱碱阳离子的水解比较复杂,一般一步写出。值得注意的是,其最终生成的
弱碱即使是难溶物也不标“↓”等状态符号,因其水解生成的量极少,不会生成沉淀。如AlCl 水解的离
3
子方程式常写成:Al3++3HO Al(OH) +3H+。
2 3
(5)阴、阳离子相互促进的水解(双水解),若水解程度不大,用“ ”表示。如CHCOONH 水解的
3 4
离子方程式为CHCOO-+NH+HO CHCOOH+NH ·H O。
3 2 3 3 2
若双水解程度较大的,书写时用“===”“↑”“↓”。离子方程式书写技巧:书写离子方程式时,一般要根
据水解的特征、水解生成的酸和碱的特点确定反应物和生成物,以离子的电荷守恒和质量守恒相结合的方
法进行配平。如:Al S 水解的离子方程式为2Al3++3S2-+6HO===2Al(OH) ↓+3HS↑。
2 3 2 3 2
AlCl 溶液和NaCO 溶液混合:2Al3++3CO+3HO===2Al(OH) ↓+3CO↑
3 2 3 2 3 2
NH Cl和NaAlO 溶液混合:NH ++AlO-+2HO===Al(OH) ↓+NH ·H O
4 2 4 2 2 3 3 2
1.(2025·河南·模拟预测)下列化学用语或图示正确的是
A.CaO的电子式: B. 的结构示意图:
C.中子数为38的镓原子: D. 的化学名称: 乙基戊烷
【答案】A
【详解】A.CaO是离子化合物,电子式为 ,故A正确;
B. 核外有2个电子,结构示意图 ,故B错误;
C.中子数为38的镓原子,质量数为69: ,故C错误;
D. 主链有6个碳原子,3号碳原子上连有1个甲基,化学名称:3-甲基己烷,故D错误;
选A。
2.(2025·宁夏陕西·模拟预测)下列化学用语表示正确的是
A.氯化氢的电子式:
B. 和 的 模型均为:
C.基态 原子价层电子的轨道表示式:
D.中子数为20的氯原子的核素符号:
【答案】D
【详解】A.氯化氢是共价化合物,其电子式为: ,A错误;
B.二氧化碳的价层电子对是2,没有孤电子对,则其 模型是直线型,B错误;C.Cr是24号元素,价电子排布式为3d54s1,价电子的轨道表示式为: ,C错误;
D.中子数为20的氯原子的质量数为37,可表示为: ,D正确;
故选D。
3.(2025·浙江杭州·模拟预测)下列化学用语或图示正确的是
A.邻羟基苯甲醛分子内氢键:
B.水分子的空间结构模型:
C.基态Br原子核外电子排布式为
D.甲乙醚:
【答案】A
【详解】A.氢键的表达式为X-H···Y,邻羟基苯甲醛分子内氢键: ,A正确;
B.水分子的空间结构为V形,VSEPR模型为: B错误;
C.基态Br原子核外电子排布式为 ,C错误;
D.甲乙醚结构简式为: ,D错误;
答案选A。
4.(2025·内蒙古·模拟预测)下列化学用语或表述正确的是
A.NaO 电子式: B.209Bi和210Bi:互为同素异形体
2 2
C.CH 的空间结构:正方形 D.基态Fe2+的价电子排布式:3d54s1
4
【答案】A
【详解】A.NaO 是由Na+和 构成的离子化合物,电子式为 ,A正确;
2 2
B.209Bi和210Bi的质子数相同,而中子数不同,属于同一种元素的不同的原子,互为同位素,B错误;C.CH 的价层电子对数为 ,其空间结构为正四面体,C错误;
4
D.Fe为26号元素,基态Fe原子的价层电子排布式为3d64s2,失去电子形成阳离子时,从最外层开始失,
因此基态Fe2+的价电子排布式:3d6,D错误;
答案选A。
5.(2024·广东深圳·一模)下列表达正确的是
A. 的电子式为
B. 的电子式可表示为
C.用电子式表示 的形成过程为
D. 的电子式为
【答案】D
【详解】A. 电子式为: ,A错误;
B. 为共价化合物,电子式为: ,B错误;
C. 为离子化合物,用电子式表示 的形成过程为:
,C错误;
D. 为离子化合物,电子式为: ,D正确;
故答案为:D。
6.(2024·四川自贡·一模)化学用语是表达化学思想的专门语言,包括符号语言、文字语言和图表语言。
下列化学用语表达错误的是
A. 的 模型:
B.水合氯离子的示意图:
C. 的结构式:D.“钠与水反应”实验有关图标:
【答案】C
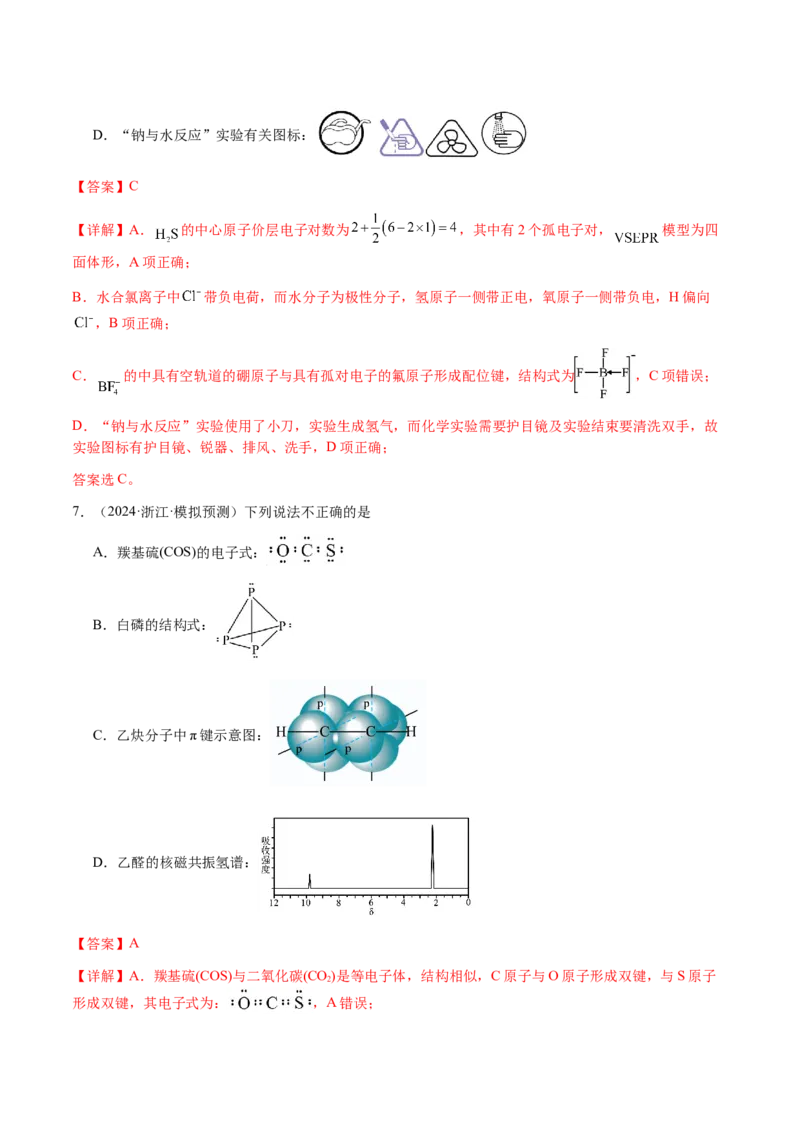
【详解】A. 的中心原子价层电子对数为 ,其中有2个孤电子对, 模型为四
面体形,A项正确;
B.水合氯离子中 带负电荷,而水分子为极性分子,氢原子一侧带正电,氧原子一侧带负电,H偏向
,B项正确;
C. 的中具有空轨道的硼原子与具有孤对电子的氟原子形成配位键,结构式为 ,C项错误;
D.“钠与水反应”实验使用了小刀,实验生成氢气,而化学实验需要护目镜及实验结束要清洗双手,故
实验图标有护目镜、锐器、排风、洗手,D项正确;
答案选C。
7.(2024·浙江·模拟预测)下列说法不正确的是
A.羰基硫(COS)的电子式:
B.白磷的结构式:
C.乙炔分子中π键示意图:
D.乙醛的核磁共振氢谱:
【答案】A
【详解】A.羰基硫(COS)与二氧化碳(CO)是等电子体,结构相似,C原子与O原子形成双键,与S原子
2
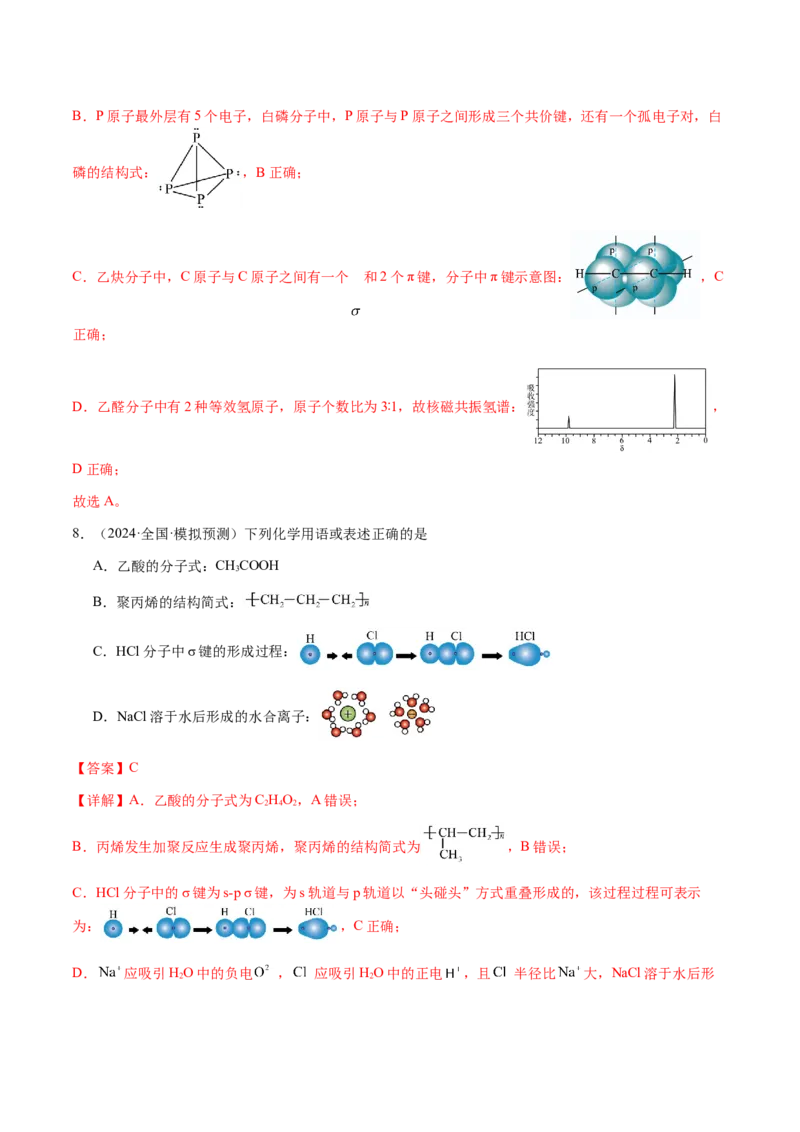
形成双键,其电子式为: ,A错误;B.P原子最外层有5个电子,白磷分子中,P原子与P原子之间形成三个共价键,还有一个孤电子对,白
磷的结构式: ,B正确;
C.乙炔分子中,C原子与C原子之间有一个 和2个π键,分子中π键示意图: ,C
正确;
D.乙醛分子中有2种等效氢原子,原子个数比为3∶1,故核磁共振氢谱: ,
D正确;
故选A。
8.(2024·全国·模拟预测)下列化学用语或表述正确的是
A.乙酸的分子式:CHCOOH
3
B.聚丙烯的结构简式:
C.HCl分子中σ键的形成过程:
D.NaCl溶于水后形成的水合离子:
【答案】C
【详解】A.乙酸的分子式为C HO,A错误;
2 4 2
B.丙烯发生加聚反应生成聚丙烯,聚丙烯的结构简式为 ,B错误;
C.HCl分子中的σ键为s-p σ键,为s轨道与p轨道以“头碰头”方式重叠形成的,该过程过程可表示
为: ,C正确;
D. 应吸引HO中的负电 , 应吸引HO中的正电 ,且 半径比 大,NaCl溶于水后形
2 2成的水合离子应表示为 ,D错误;
答案选C。
9.(2024·广东韶关·一模)下列化学用语中正确的是
A.质量数为127的碘原子:
B.过氧化氢的电子式:
C. 的结构示意图:
D.反-2-丁烯的结构简式:
【答案】D
【详解】A.表示原子时,将质量数表示在元素符号左上角,质子数表示在左下角,质量数为127的碘原
子表示为 ,A错误;
B.过氧化氢为共价化合物,电子式为 ,B错误;
C.S为16号元素,S2−的最外层电子应为8,结构示意图为 ,C错误;
D.反−2−丁烯中两个甲基位于双键的异侧,结构简式为 ,D正确;
答案选D。
10.(2024·吉林长春·一模)实验室制取氮气的一种方法为NH Cl+NaNO NaCl+2H O+N↑。下列有关化
4 2 2 2
学用语表示正确的是
A.离子化合物NH Cl的电子式为:
4
B. 和HO的空间填充模型均为:
2
C.N 中某一个p−pπ键的形成可表示为:
2D.基态氮原子的L层电子的轨道表示式为:
【答案】C
【详解】A.氯化铵是含有离子键和共价键的离子化合物,电子式为 ,A错误;
B. 的价层电子对数为 ,含有1对孤对电子,空间构型为V形,N原子体积大于O原
子,HO的价层电子对数为 ,含有2对孤对电子,空间构型为V形,O原子半径大于H原
2
子,均为中心原子体积较大,B错误;
C.N 中存在一个σ键和两个p−pπ键,p轨道为哑铃形,两个N原子的p轨道以肩并肩的形式进行重叠,
2
符合图示,C正确;
D.基态氮原子的L层电子的排布式为2s22p3,轨道表示式为 ,D错误;
故选C。
11.(2023·陕西延安·一模)牙膏是生活中的常见用品,内含有多种化学成分。下列有关说法错误的是
A.缓冲剂NaOH的电子式:
B.润湿剂甘油(丙三醇)的球棍模型:
C.摩擦剂二氧化硅的化学式:
D.防腐剂苯甲酸钠在水中的电离方程式:
【答案】D
【详解】A.氢氧化钠是含有共价键的离子化合物,电子式为 ,故A项正确;
B.丙三醇的结构简式 ,球根模型为 ,故B项正确;
C.根据二氧化硅晶体的结构可知,二氧化硅的化学式为 ,故C项正确;
D.苯甲酸钠为钠盐,在水中完全电离,其电离方程式为 ,故D
项错误;故本题选D。
12.(2024·广西·模拟预测)中科院研制出一种多功能催化剂,首次将甲烷转化为乙烯:
。下列说法正确的是
A.基态C原子的价层电子排布式为
B. 的电子式为:
C.乙烯的结构简式为:
D.CH 的空间填充模型为:
4
【答案】D
【详解】A.C是第6号元素,基态C原子的价层电子排布式为 ,A错误;
B. 分子中含 双键,故电子式为 ,B错误;
C.乙烯的结构简式为: ,C错误;
D. 分子为正四面体,空间填充模型正确,,D正确;
故选D。
13.(2024·河南·一模)下列化学用语或图示表达正确的是
A.空间填充模型 既可以表示甲烷分子,也可以表示四氯化碳分子
B. 溶液中的水合离子:
C. 的电子式:
D.聚丙烯的结构简式:
【答案】C
【详解】A.原子半径:Cl>C>H,因此该模型可表示甲烷,但不能表示四氯化碳,故A错误;
B. 溶液中存在水合钠离子和水合氯离子,水分子中存在O-H极性键,O带部分负电荷、H带部分正
电荷,氯离子半径大于钠离子,氯离子带负电荷,钠离子带正电荷,则水合钠离子中吸引的是水分子中的
氧原子端、水合氯离子中氯离子吸引的是水分子中的氢原子端,图中显示的错误有:钠离子半径大于氯离
子、钠离子吸引了氢原子、氯离子吸引了氧原子,故B错误;
C. 的结构式和电子式依次为H-O-Cl、 ,故C正确;D.聚丙烯的结构简式: ,故D错误;
故选C。
14.(2024·福建·模拟预测)下列化学用语表达正确的是
A. 的名称:乙二酸乙二酯
B.空间填充模型 既可以表示甲烷分子,也可以表示四氯化碳分子
C. 的价层电子对互斥(VSEPR)模型:
D.基态铍原子最外层电子的电子云轮廓图:
【答案】C
【详解】A. 是由乙二酸和乙醇形成的酯,其名称为乙二酸二乙酯,A错误;
B. 可以表示甲烷分子,但是不能表示CCl 分子,因为Cl原子的半径比C原子大,与比例模型中的
4
原子大小不符,B错误;
C. 的中心原子价层电子对数为 ,其VSEPR模型为平面三角形,C正确;
D.基态铍原子电子排布式为1s22s2,最外层电子在s轨道,电子云轮廓是球形的,D错误;
故选C。
15.(2023·湖南·一模)下列有关化学用语表示正确的是
A.二硫化碳的空间填充模型: B. 是 的原子结构示意图
C.固体 的电子式: D. 的 σ键电子云图形:
【答案】D
【详解】A.二硫化碳分子中碳原子的价层电子对数为2,孤对电子对数为0,分子的空间构型为直线形,
分子的空间填充模型为 ,故A错误;B.选项给出的碳原子结构示意图正确,碳原子的质子数为6,质量数大于6,碳原子符号错误,故B错
误;
C.二氧化硅是呈空间立体网状结构的共价晶体,不是单个的共价分子,故C错误;
D.氯气分子中氯原子的p轨道形成头碰头的p-pσ键,p-pσ键电子云图形为 ,故D正确;
故选D。
16.(2024·湖北·一模)下列化学用语表达正确的是
A.sp2杂化轨道模型:
B.固体HF中的链状结构
C.HO 电子式:
2 2
D.NaCl溶液中的水合离子:
【答案】A
【详解】A.sp2杂化轨道在空间呈平面三角形,键角120o,轨道模型正确,A正确;
B.固体HF中的链状结构应为 ,B错误;
C.HO 为共价化合物,电子式: ,C错误;
2 2
D.钠离子半径小于氯离子,图示中钠离子半径大于氯离子,同时水分子中氢原子呈正电性,氧原子呈负
电性,因此钠离子周围的水分子应该是氧原子对着钠离子,氯离子周围的水分子应该是氢原子对着氯离
子,D错误;
故选A。
17.(2024·浙江·模拟预测)下列表示不正确的是
A.NaOH的电子式: B.NaCl溶液中的水合离子:
C.O 分子的球棍模型: D.环己烷稳定的空间构型的键线式:
3
【答案】D【详解】A.已知NaOH是离子化合物,且OH-中存在共价键,故NaOH的电子式为: ,A
正确;
B.已知HO中H原子一端带正电性,O原子一端带负电性,且Cl-半径比Na+大,故NaCl溶液中的水合离
2
子表示为: ,B正确;
C.已知O 为V形分子,故O 分子的球棍模型为: ,C正确;
3 3
D. 为船式结构,环己烷(C H )稳定的空间构型为椅式结构,即 ,D错误;
6 12
故答案为:D。
18.(2024·四川遂宁·一模)下列化学用语表示正确的是
A.BF 的空间填充模型:
3
B. 的电子式:
C.3,3-二甲基戊烷的键线式:
D. 中共价键的电子云图:
【答案】C
【详解】A.BF 中B形成3个共价键且无孤电子对,为平面三角形,A错误;
3
B. 的电子式: ,B错误;
C.主链上碳原子个数为5,3号碳原子上有2个甲基,名称为3,3-二甲基戊烷,C正确;
D.H原子的轨道为球形, 中共价键的电子云图: ,D错误;
故选C。
19.(2025·广西南宁·模拟预测)实验室制备少量氮气的反应为 。下
列与该反应有关的化学用语表述错误的是
A.基态N原子的价层电子的轨道表示式为
B. 的电子式为
C.NaCl的形成过程可表示为D. 的VSEPR模型为
【答案】B
【详解】A.N元素的原子序数为7,基态原子的价电子排布式为2s22p3,轨道表示式为 ,
A正确;
B.N 的电子式为 ,B错误;
2
C.氯化钠是离子化合物,用电子式表示NaCl的形成过程为 ,C正确;
D.HO中心原子O原子上的价层电子对数为 ,VSEPR模型为四面体形,D正
2
确;
故答案选B。
20.(2025·安徽合肥·模拟预测)下列化学用语或图示正确的是
A.1-氯丙烯的结构简式:
B.基态氮原子电子排布轨道表达式写成 违背了泡利原理
C. 分子的球棍模型:
D. 的电子式:
【答案】D
【详解】A.1-氯丙烯的结构简式:CH-CH=CHCl,A错误;
3
B.基态氮原子电子排布轨道表达式写成 违背了洪特规则,B错误;
C.O 的分子结构如图 ,呈V形,两个键的夹角为116.5°,三个原子以一个O原子
3
为中心,与另外两个O原子分别构成一个共价键;中间O原子提供两个电子,旁边两个O原子各提供一个
电子,构成一个特殊的化学键,所以O 分子的球棍模型不是: ,C错误;
3
D.CO为共价化合物,其电子式为: ,D正确;
故选D。