文档内容
专题 03 物质的分离与提纯
考点一 物质分离、提纯常用的物理方法
考点梳理
1.物质分离、提纯的区别
(1)物质的分离
将混合物的各组分分离开来,获得几种纯净物的过程。
(2)物质的提纯
将混合物中的杂质除去而得到纯净物的过程,又叫物质的净化或除杂。
2.物质分离、提纯常用的物理方法及装置
(1)固体与液体的混合物
装置或
方法 适用条件 实例 说明
主要仪器
①一贴:滤纸紧贴漏斗内壁;
碳酸钙悬 ②二低:滤纸边缘低于漏斗边缘,液面
难溶固体与液
过滤 浊液、泥 低于滤纸边缘;
体混合物
水等 ③三靠:烧杯紧靠玻璃棒,玻璃棒轻靠
三层滤纸处,漏斗下端紧靠烧杯内壁
从 NaCl
溶质的溶解度
溶液中提 NaHCO 、FeCl 、NaSO 等的水溶液在
3 3 2 3
蒸发结晶 受温度变化影
取 NaCl 加热蒸干后得不到原来的溶质
响较小
晶体
(2)固体与固体的混合物
方法 适用条件 实例 说明
沉淀的洗涤方法是沿玻璃棒向过滤器中加
在某种试剂中一种可溶
溶解、 碳酸钠和碳酸 蒸馏水至淹没沉淀,静置,待液体全部流
而另一种溶剂中不溶的
过滤 钙 下,再重复操作2~3次,然后通过检验
固体混合物的分离
洗涤液(滤液),判断是否洗净
用于溶解度随温度变化 除 去 KNO 中
3
若结晶一次纯度达不到要求,则需要重复
结晶 相差较大的可溶性固体 混 有 的 少 量
进行一次,称为重结晶
混合物的分离 NaCl
分离某种组分易升华的 分离 I 和 NaCl 应与物质的分解反应相区分,如:
2
升华
混合物 固体 NH Cl=====NH ↑+HCl↑
4 3
(3)液体与液体的混合物
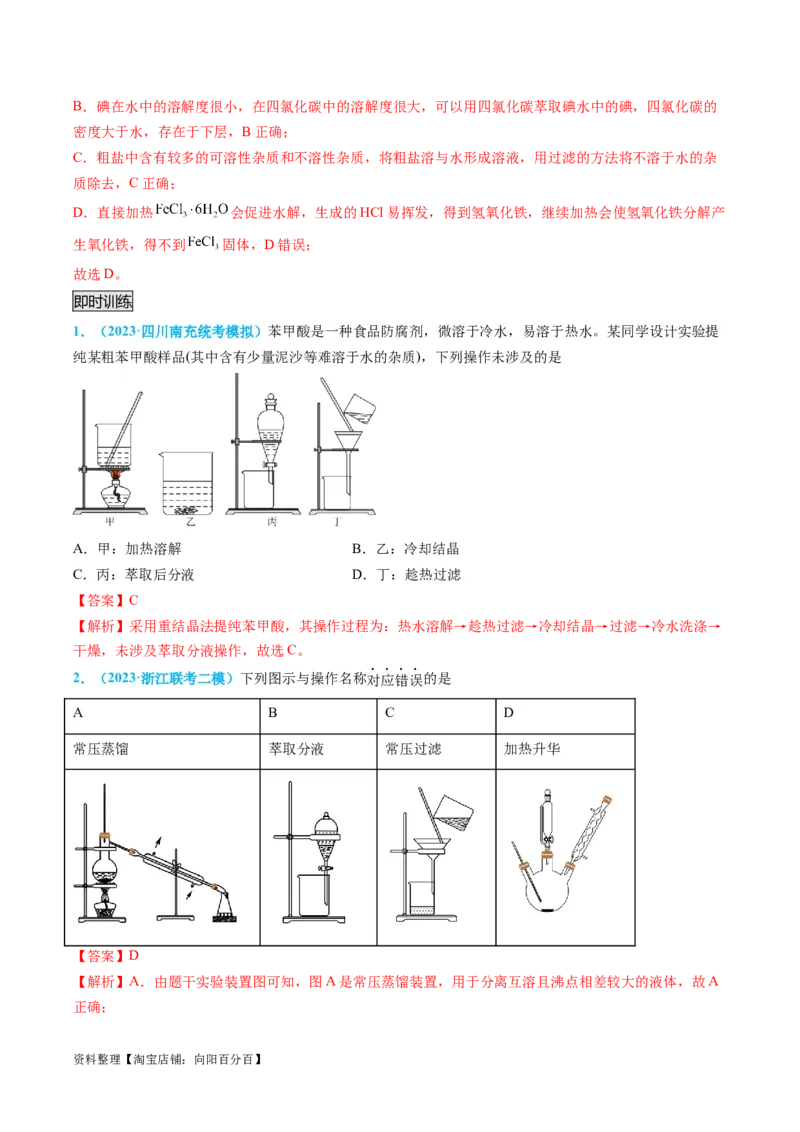
资料整理【淘宝店铺:向阳百分百】方法 萃取、分液 蒸馏
装置或
主要仪器
适用条件 互不相溶的液体混合物 两种或两种以上互溶的液体,沸点相差较
实例 分离CCl 和水等 分离酒精和水
4
蒸馏装置中温度计的水银球要放置在蒸馏烧瓶支
若提取碘水中的碘,分液前要
管口处;为防暴沸,可在蒸馏烧瓶中放几小块沸
说明 先萃取。分液时下层液体从口
石或碎瓷片。冷凝管中水流方向应为“下进上
放出,上层液体从口倒出
出”
3.依据物理性质选择分离、提纯的方法
(1)“固+固”混合物的分离(提纯)
(2)“固+液”混合物的分离(提纯)
(3)“液+液”混合物的分离(提纯)
典例精讲
例1.(2023·湖南卷)下列玻璃仪器在相应实验中选用不合理的是
资料整理【淘宝店铺:向阳百分百】A.重结晶法提纯苯甲酸:①②③ B.蒸馏法分离CHCl 和CCl :③⑤⑥
2 2 4
C.浓硫酸催化乙醇制备乙烯:③⑤ D.酸碱滴定法测定NaOH溶液浓度:④⑥
【答案】A
【解析】A.粗苯甲酸中含有少量氯化钠和泥沙,需要利用重结晶来提纯苯甲酸,具体操作为加热溶解、
趁热过滤和冷却结晶,此时利用的玻璃仪器有漏斗、烧杯、玻璃棒,A选项装置选择不合理;
B.蒸馏法需要用到温度计以测量蒸汽温度、蒸馏烧瓶用来盛装混合溶液、锥形瓶用于盛装收集到的馏分,
B选项装置选择合理;
C.浓硫酸催化制乙烯需要控制反应温度为170℃,需要利用温度计测量反应体系的温度,C选项装置选择
合理;
D.酸碱滴定法测定NaOH溶液浓度是用已知浓度的酸液滴定未知浓度的碱液,酸液盛装在酸式滴定管中,
D选项装置选择合理;
故选A。
变式探究
1.(2022·北京卷)下列实验中,不能达到实验目的的是
萃取碘水中的
由海水制取蒸馏水 分离粗盐中的不溶物 由 制取无水 固体
碘
A B C D
【答案】D
【解析】A.实验室用海水制取蒸馏水用蒸馏的方法制备,蒸馏时用到蒸馏烧瓶、酒精灯、冷凝管、牛角
管、锥形瓶等仪器,注意温度计水银球应处在蒸馏烧瓶的支管口附近,冷凝管应从下口进水,上口出水,
A正确;
资料整理【淘宝店铺:向阳百分百】B.碘在水中的溶解度很小,在四氯化碳中的溶解度很大,可以用四氯化碳萃取碘水中的碘,四氯化碳的
密度大于水,存在于下层,B正确;
C.粗盐中含有较多的可溶性杂质和不溶性杂质,将粗盐溶与水形成溶液,用过滤的方法将不溶于水的杂
质除去,C正确;
D.直接加热 会促进水解,生成的HCl易挥发,得到氢氧化铁,继续加热会使氢氧化铁分解产
生氧化铁,得不到 固体,D错误;
故选D。
即时训练
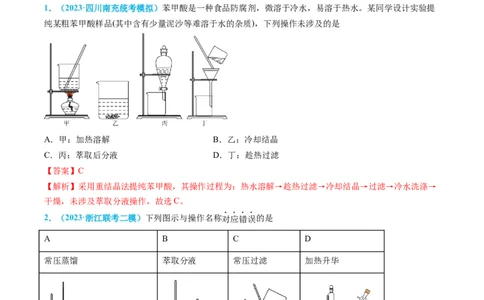
1.(2023·四川南充统考模拟)苯甲酸是一种食品防腐剂,微溶于冷水,易溶于热水。某同学设计实验提
纯某粗苯甲酸样品(其中含有少量泥沙等难溶于水的杂质),下列操作未涉及的是
A.甲:加热溶解 B.乙:冷却结晶
C.丙:萃取后分液 D.丁:趁热过滤
【答案】C
【解析】采用重结晶法提纯苯甲酸,其操作过程为:热水溶解→趁热过滤→冷却结晶→过滤→冷水洗涤→
干燥,未涉及萃取分液操作,故选C。
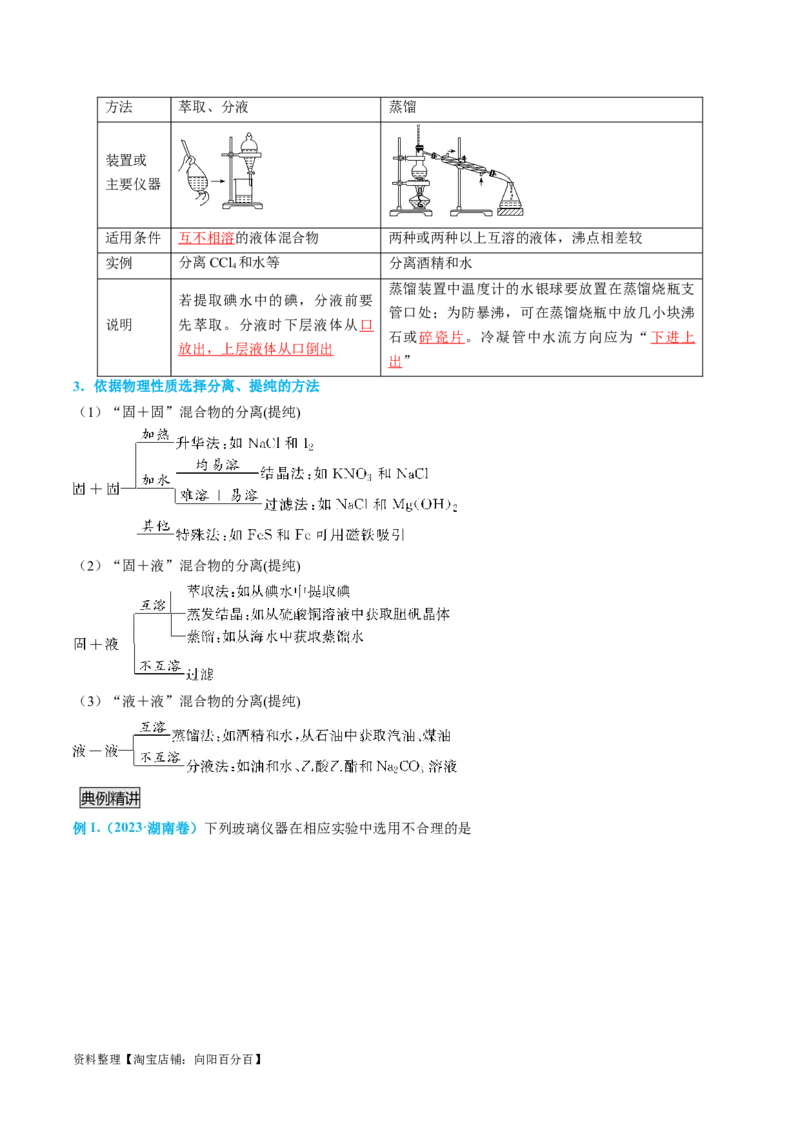
2.(2023·浙江联考二模)下列图示与操作名称对应错误的是
A B C D
常压蒸馏 萃取分液 常压过滤 加热升华
【答案】D
【解析】A.由题干实验装置图可知,图A是常压蒸馏装置,用于分离互溶且沸点相差较大的液体,故A
正确;
资料整理【淘宝店铺:向阳百分百】B.由题干实验装置图可知,图B是萃取分液,用于分离互不相溶的两种液体,故B正确;
C.由题干实验装置图可知,图C是常压过滤,用于分离不溶性固体和液体,故C正确;
D.由题干实验装置图可知,图D不是加热升华装置,而是利用三颈瓶进行的可控温的反应装置,故D错
误;
故选D。
3.(2023·河南郑州外国语学校模拟)工业上常用水蒸气蒸馏的方法(蒸馏装置如图)从植物组织中获取挥
发性成分。这些挥发性成分的混合物统称精油,大都具有令人愉快的香味。从柠檬、橙子和柚子等水果的
果皮中提取的精油90%以上是柠檬烯( )。提取柠檬烯的实验操作步骤如下:
①将1~2块橙子皮剪成细小的碎片,投入乙装置中,加入约30mL水;
②打开活塞K,加热水蒸气发生器至水沸腾,活塞K的支管口有大量水蒸气冒出时旋紧活塞K,接通冷凝
水,水蒸气蒸馏即开始进行,可观察到在馏出液的水面上有一层很薄的油层。
下列说法不正确的是
A.当馏出液无明显油珠且澄清透明时,说明蒸馏完成
B.蒸馏结束后,先打开活塞K,再停止加热
C.为完成实验目的,应将甲中的长导管换成温度计
D.要得到纯精油,还需要用到的分离提纯方法有分液、蒸馏
【答案】C
【解析】A.柠檬烯不溶于水,密度比水小,因此当馏出液无明显油珠,澄清透明时,说明蒸馏完成,故
A项正确;
B.蒸馏结束后,为防止倒吸,先打开活塞K,再停止加热,故B项正确;
C.长玻管可作安全管,平衡气压,防止由于导管堵塞引起爆炸,温度计在甲装置中没啥作用,故C项错
误;
D.因为得到的精油中含有其它成分,所以要想得到柠檬烯,要进行萃取、分液、蒸馏操作才能实现目的,
故D项正确;
故选C。
考点二 物质分离、提纯常用的化学方法
考点梳理
资料整理【淘宝店铺:向阳百分百】1.物质分离、提纯常用的化学方法
方法 原理 杂质成分
沉淀法 将杂质离子转化为沉淀 Cl-、SO、CO及能形成弱碱的阳离子
气化法 将杂质离子转化为气体 CO、HCO、SO、HSO、S2-、NH
杂质中含不同价态的相同元素(用氧化剂或
杂转
将杂质转化为需要提纯的物质 还原剂)、同一种酸的正盐与酸式盐(用对应
纯法
的酸或碱)
氧化 用氧化剂(还原剂)除去具有还原性 如用酸性KMnO 溶液除去CO 中的SO ,
4 2 2
还原法 (氧化性)的杂质 用灼热的铜网除去N 中的O
2 2
热分
加热使不稳定的物质分解除去 如除去NaCl中的NH Cl等
4
解法
酸碱 利用物质与酸或碱溶液反应的差异 如用过量的NaOH溶液可除去Fe O 中的
2 3
溶解法 进行分离 Al O
2 3
含杂质的金属(M)作阳极、纯金属(M)作阴
电解法 利用电解原理除去杂质
极,含M的盐溶液作电解质溶液
如除Cu2+中的Fe3+加入CuO、Cu(OH) 或
2
调 加入试剂调节溶液pH使溶液中某
Cu (OH) CO 等,调节pH使Fe3+转化为
2 2 3
pH法 种成分生成沉淀而分离
Fe(OH) 而除去
3
2.除杂“四原则”
(1)不增,不得引入新的杂质。
(2)不减,尽量不减少被提纯和分离的物质。
(3)易分离,应使被提纯或分离的物质与其他物质易分离。
(4)易复原,被提纯物质转化后要易被复原。
3.除杂操作“四注意”
(1)除杂试剂要过量。
(2)过量试剂需除去。
(3)选择的途径要最佳。
(4)除去多种杂质时要考虑加入试剂的先后顺序。
典例精讲
例2.(2023·海南卷第3题)下列气体除杂(括号里为杂质)操作所选用的试剂合理的是
A. :饱和 溶液
B. :碱石灰
C. :酸性 溶液
D. :
资料整理【淘宝店铺:向阳百分百】【答案】B
【解析】二氧化碳、氯化氢均会和碳酸钠溶液反应,A不符合题意;氨气和碱石灰不反应,水和碱石灰反
应,合理,B符合题意;酸性高锰酸钾会把乙炔氧化,C不符合题意;PO 、二氧化硫均为酸性氧化物,
4 10
不反应,不能除去二氧化硫,D不符合题意;故选B。
【变式探究】(2023·全国甲卷第9题)实验室将粗盐提纯并配制 的 溶液。下列仪器
中,本实验必须用到的有
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A. ①②④⑥ B. ①④⑤⑥ C. ②③⑦⑧ D. ①⑤⑥⑧
【答案】D
【解析】实验室将粗盐提纯时,需要将其溶于一定量的水中,然后将其中的硫酸根离子、钙离子、镁离子
依次用稍过量的氯化钡溶液、碳酸钠溶液和氢氧化钠溶液除去,该过程中有过滤操作,需要用到烧杯、漏
斗和玻璃棒;将所得滤液加适量盐酸酸化后蒸发结晶得到较纯的食盐,该过程要用到蒸发皿和酒精灯;用
提纯后得到的精盐配制溶液的基本步骤有称量、溶解、转移、洗涤、定容、摇匀等操作,需要用到天平、
容量瓶、烧杯、玻璃棒、胶头滴管等。综上所述,本实验必须用到的有①天平、⑤容量瓶、⑥烧杯、⑧酒
精灯,因此本题选D。
即时训练
4.(2023·四川绵阳统考一模)实验室用化学沉淀法除去粗盐中的Ca2+、Mg2+、 获得精制盐。下列叙
述有误的是
A.杂质离子除去顺序可确定为:SO 、Mg2+、Ca2+
B.加入试剂顺序可依次为:NaOH、NaCO、BaCl 、盐酸四种溶液
2 3 2
C.杂质离子沉淀完后,采取的分离操作用到的仪器是a、b、c、d
D.沉淀分离完成后,调整溶液pH时用到的全部仪器为a、c、e、f
【答案】B
【解析】A.要确保碳酸钠在氯化钡之后,杂质离子可依次加入过量的BaCl 、NaOH、NaCO 依次除去
2 2 3
SO 、Mg2+、Ca2+,A正确;
B.加入试剂顺序不可以依次为NaOH、NaCO、BaCl 、盐酸四种溶液,过量的BaCl 未被除去,应确保
2 3 2 2
BaCl 在NaCO 之前,B错误;
2 2 3
C.沉淀后进行过滤,所涉及的仪器有玻璃棒、漏斗、烧杯、铁架台,C正确;
D.沉淀分离完成后,调整溶液pH时用到的全部仪器有烧杯、玻璃棒、胶头滴管和pH试纸,D正确。
故选B。
资料整理【淘宝店铺:向阳百分百】5.(2023·山西晋城第一中学模拟)为除去括号内的杂质,所选用的试剂或方法正确的是
A. :通过饱和碳酸钠溶液的洗气瓶
B. :通入足量的氯气
C. :用点燃的方法除去
D. 溶液 :加入过量 溶液
【答案】B
【解析】A. :通过饱和食盐水的洗气瓶,通入饱和碳酸钠,会产生新的杂质气体 ,A错误;
B. :通入足量的氯气,可以将 氧化为 ,B正确;
C. :不能用点燃的方法除去,应该将混合气体通入灼热的 ,C错误;
D. 溶液 ,加入过量 溶液,除去 ,同时也除去了 ,D错误;
故选B。
6.(2023·江西赣州统考二模)实验探究是化学学科核心素养之一、用下图所示装置能净化和收集气体的
是
选项 气体(杂质) 试剂X
A C H(SO ) NaOH溶液
2 4 2
B Cl(HCl) 饱和食盐水
2
C SO (CO) 饱和碳酸钠溶液
2 2
D C H(C H) 酸性高锰酸钾溶液
3 8 2 4
【答案】B
【解析】A.乙烯中的SO 可以通过装有NaOH的洗气瓶来除杂,也能用浓硫酸进行干燥,但由于乙烯的
2
密度比空气稍小一点,故常用排水法收集而不用排空气法收集(易导致收集的乙烯不纯),A不合题意;
B.除去Cl 中的HCl先通过装有饱和食盐水的洗气瓶,再用浓硫酸进行干燥,且密度大于空气,利用向上
2
排空气法收集氯气,B符合题意;
C.由于SO 和CO 均能与NaCO 溶液反应,故不能用饱和NaCO 溶液来除去SO 中的CO,C不合题意;
2 2 2 3 2 3 2 2
D.乙烯经过酸性高锰酸钾溶液后转化为CO,引入新的杂质,故除去丙烷中的乙烯不能用酸性高锰酸钾
2
溶液,D不合题意;
故选B。
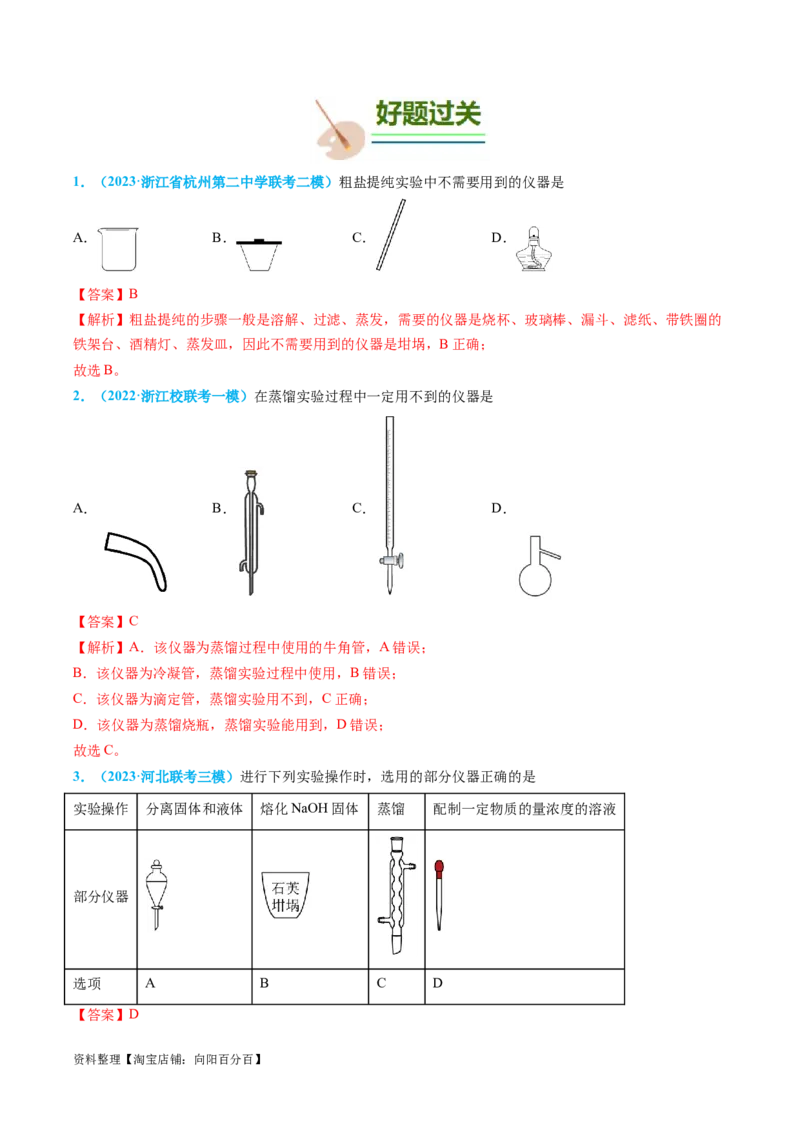
资料整理【淘宝店铺:向阳百分百】1.(2023·浙江省杭州第二中学联考二模)粗盐提纯实验中不需要用到的仪器是
A. B. C. D.
【答案】B
【解析】粗盐提纯的步骤一般是溶解、过滤、蒸发,需要的仪器是烧杯、玻璃棒、漏斗、滤纸、带铁圈的
铁架台、酒精灯、蒸发皿,因此不需要用到的仪器是坩埚,B正确;
故选B。
2.(2022·浙江校联考一模)在蒸馏实验过程中一定用不到的仪器是
A. B. C. D.
【答案】C
【解析】A.该仪器为蒸馏过程中使用的牛角管,A错误;
B.该仪器为冷凝管,蒸馏实验过程中使用,B错误;
C.该仪器为滴定管,蒸馏实验用不到,C正确;
D.该仪器为蒸馏烧瓶,蒸馏实验能用到,D错误;
故选C。
3.(2023·河北联考三模)进行下列实验操作时,选用的部分仪器正确的是
实验操作 分离固体和液体 熔化NaOH固体 蒸馏 配制一定物质的量浓度的溶液
部分仪器
选项 A B C D
【答案】D
资料整理【淘宝店铺:向阳百分百】【解析】A.分离固体和液体使用普通漏斗、烧杯和玻璃棒,不能使用分液漏斗,A项错误;
B.熔化NaOH固体要用铁坩埚,不能使用陶瓷坩埚和石英坩埚,因为NaOH能与其中含有的二氧化硅反
应,会腐蚀陶瓷坩埚和石英坩埚,B项错误;
C.蒸馏时应使用直形冷凝管,不能使用球形冷凝管,若用球形冷凝管,部分冷凝液会残留在球形冷凝管
中,C项错误;
D.配制一定物质的量浓度的溶液,定容时需要使用胶头滴管,D项正确
故选D。
4.(2023·上海统考模拟)下列海带提碘的操作中不合理的是
选项 A B C D
使用仪
器
相关操
灼烧 浸泡海带 过滤海带浸出液 萃取碘
作
【答案】B
【解析】A.灼烧固体物质应该在坩埚中进行,A正确;
B.浸泡海带应该在烧杯中进行而不能用表面皿,B错误;
C.过滤时,应该使用的玻璃仪器有烧杯,漏斗,玻璃棒,C正确;
D.萃取的时候,应该用分液漏斗进行,D正确;
故选B。
5.(2023·广东梅州统考二模)实验室分离CHCl(沸点:40℃)、CCl (沸点:77℃),下列玻璃仪器中不需
2 2 4
要用到的是
A. B. C. D.
【答案】C
【解析】 (沸点:40℃)、 (沸点:77℃)之间沸点差异较大,可通过分馏进行分离,需要用到的
仪器有蒸馏烧瓶(B项仪器名称)、直形冷凝管(A项仪器名称)和锥形瓶(D项仪器名称),不需要用
到分液漏斗,C项符合题意。
故选C。
6.(2023·山东临沂统考二模)实验室提供的玻璃仪器有酒精灯、烧杯、量筒、玻璃棒、胶头滴管、分液
漏斗(非玻璃仪器任选),选用上述仪器不能完成的实验是
资料整理【淘宝店铺:向阳百分百】A.重结晶法提纯苯甲酸
B.分离乙酸乙酯和饱和碳酸钠溶液
C.制备氢氧化铁胶体
D.配制质量分数为20%的氯化钠溶液
【答案】A
【解析】A.用重结晶法提纯苯甲酸的操作环节有溶解、蒸发浓缩、降温结晶和过滤,因此必须使用的仪
器有烧杯、玻璃棒、蒸发皿、酒精灯、普通漏斗,故选A;
B.用分液法分离分离乙酸乙酯和饱和碳酸钠溶液,主要仪器有:分液漏斗、烧杯,故不选B;
C.向盛有沸水的烧杯中滴加少量氯化铁饱和溶液,继续加热至液体呈透明红褐色,制得氢氧化铁胶体,
需要的仪器有烧杯、胶头滴管、酒精灯,故不选C;
D.配制质量分数为20%的氯化钠溶液,步骤有计算、称量、溶解,主要仪器有:天平、烧杯、量筒、玻
璃棒,故不选D;
故选A。
7.(2023·广东广州华南师大附中三模)下列有关气体除杂的试剂选择正确的是
A.除去 中的 :饱和食盐水
B.除去 中的 :硫酸铜溶液
C.除去 中的 :酸性高锰酸钾溶液
D.除去 中的 :饱和碳酸钠溶液
【答案】B
【解析】A.盐酸能与碳酸氢钠溶液反应生成二氧化碳,二氧化碳不溶于饱和碳酸氢钠溶液,则除去二氧
化碳中的氯化氢杂质应选用饱和碳酸氢钠溶液,不能饱和食盐水,故A错误;
B.硫化氢能与硫酸铜溶液反应生成硫化铜沉淀和硫酸,而乙炔与硫酸铜溶液不反应,则除去乙炔中的硫
化氢杂质应选择硫酸铜溶液,故B正确;
C.乙烯与酸性高锰酸钾溶液发生氧化反应生成二氧化碳气体,则除去丙烷中的乙烯杂质不能选用酸性高
锰酸钾溶液,否则会引入新杂质二氧化碳,应选择溴水,故C错误;
D.二氧化碳和二氧化硫电能与碳酸钠溶液反应,所以除去二氧化碳中的二氧化氯杂质不能选用饱和碳酸
钠溶液,应选用饱和碳酸氢钠溶液,故D错误;
故选B。
8.(2023·山东青岛统考三模)实验室从废定影液{含 和 等}中回收 和 的主要步骤:
向废定影液中加入 溶液沉银,过滤、洗涤及干燥,灼烧 制 ;制取 并通入滤液氧化 ,
用苯萃取分液,最后蒸馏分离苯和溴。部分操作的装置如图,下列叙述正确的是
资料整理【淘宝店铺:向阳百分百】A.用装置甲在通风橱中高温灼烧 制取
B.用装置乙制备
C.用装置丙分液时,从下口放出有机相
D.用装置丁分离苯和溴
【答案】B
【分析】甲装置为蒸发结晶,乙不加热制备Cl,丙为萃取分液,丁为蒸馏装置。
2
【解析】A.Ag S在高温灼烧时产生污染的气体SO ,需要在通风橱进行防止污染,灼烧选用坩埚,A项
2 2
错误;
B.高锰酸钾将HCl氧化为Cl,B项正确;
2
C.苯的密度小于水,苯和溴应该在上层,下口放出下层后从上口倒出苯层,C项错误;
D.溴和苯沸点不同,丁蒸馏利用物质沸点不同进行分离,但Br 易挥发污染环境不能敞口收集,D项错误;
2
故选B。
9.(2023·江苏盐城统考三模)下列有关制取、分离和提纯乙酸乙酯实验装置能达到实验目的的是
A.向甲试管中依次加入物质的先后顺序为②①③B.用装置乙制备乙酸乙酯
C.用装置丙分离乙酸乙酯粗品 D.用装置丁提纯乙酸乙酯
【答案】B
【解析】A.由于浓硫酸稀释时放热,所以浓硫酸不能先加,而醋酸的价格较高,为减少醋酸的挥发,冷
却后加入冰醋酸,添加顺序为乙醇、浓硫酸、乙酸,加入物质的先后顺序为③①②,选项A错误;
B.乙醇、乙酸在浓硫酸、加热的条件下可以反应生成乙酸乙酯,饱和碳酸钠溶液可以吸收挥发出来的乙
醇和乙酸,同时降低乙酸乙酯的溶解度,用装置乙可以制备乙酸乙酯且能防止倒吸,选项B正确;
C.在饱和碳酸钠溶液中乙酸乙酯不互溶,分层,应该利用分液分离而不是用过滤,选项C错误;
D.乙酸乙酯分离是利用分液,不是利用蒸馏,选项D错误;
故选B。
资料整理【淘宝店铺:向阳百分百】10.(2023·贵州贵阳统考二模)下列除杂试剂和分离方法都正确的是
选项 物质 杂质 试剂 分离方法
A CuO Cu 稀盐酸 过滤
B CH CH=CH 酸性KMnO 溶液 洗气
4 2 2 4
C 酒精 水 CaO 蒸发
乙酸乙
D 乙酸 饱和碳酸钠溶液 分液
酯
【答案】D
【解析】A.CuO能够和稀盐酸反应,不能用稀盐酸除去CuO中混有的Cu,故A错误;
B.CH=CH 和酸性KMnO 溶液反应会生成CO 引入了新的杂质,故B错误;
2 2 4 2
C.除去酒精中的水,可以加入CaO和水反应后,再蒸馏,故C错误;
D.乙酸能够和饱和碳酸钠溶液反应,而乙酸乙酯在饱和碳酸钠溶液中的溶解度很小且不和碳酸钠反应,
然后通过分液得到乙酸乙酯,故D正确;
故选D。
11.(2023·河北石家庄模拟)溴苯的制备实验的部分实验操作如图所示,其中正确的是
A B C D
制备溴苯 洗涤除溴,放出水层 除去干燥剂 分离苯和溴苯
【答案】C
【解析】A.HBr极易溶于水,故锥形瓶内导管口不能插入水面以下,A项错误;
B.溴苯的密度比水的大,应在下层,B项错误;
C.过滤除去干燥剂CaCl ,C项正确;
2
D.蒸馏时温度计的水银球应放在蒸馏烧瓶的支管口处,需要测量蒸气的温度,而不是液相物质的温度,
D项错误。
故选C。
12.(2023·山东联考模拟)实验室中下列做法或操作分析正确的是
A. 固体保存在广口塑料瓶中
B. 溶液保存时加入少量稀硝酸
资料整理【淘宝店铺:向阳百分百】C.可用热的碳酸钠溶液除去金属表面附着的柴油
D.蒸馏时,若温度计水银球低于蒸馏烧瓶支管口,则收集到的馏分产率更高
【答案】A
【解析】A. 是固体,保存在广口瓶中,同时 属于强碱的碱性氧化物,应保存在塑料瓶中,或者
玻璃瓶和橡胶塞,故A正确;
B.硝酸亚铁溶液保存时加入稀硝酸,能将二价铁氧化成三价铁,引入杂质,故B错误;
C.碳酸钠水解呈碱性,升高温度,水解程度增大,碱性增强,有利于除去酯类油污,但是柴油属于矿物
油,与碱不反应,故C错误;
D.蒸馏时,若温度计水银球低于蒸馏烧瓶支管口时,过早结束收集物质的操作,收集的馏分减少,产率
偏低,故D错误;
故选A。
13.(2023·辽宁丹东统考二模)关于海水综合利用,下列说法正确的是
A.粗盐提纯所加沉淀剂可依次为 溶液、 溶液、 溶液
B.海水提镁过程中将 直接灼烧即可制得无水
C.海水提溴过程中每获得 共需要消耗标准状况下
D.海水淡化常用的主要方法有蒸馏法、电渗析法和离子交换法
【答案】D
【解析】A.粗盐提纯时,为使加入过量的钡离子转化为沉淀除去,碳酸钠溶液必须在氯化钡溶液后加入,
否则会使氯化钠溶液中混有氯化钡杂质,故A错误;
B.氯化镁是强酸弱碱盐,在溶液中会发生水解生成氢氧化镁和氯化氢,若六水氯化镁直接灼烧会导致氯
化镁水解生成氧化镁,不能制得无水氯化镁,故B错误;
C.海水提溴过程中氯气的作用是先将海水中的溴离子转化为溴,经富集(溴转化为溴离子)后再将溴离
子转化为溴,则每获得0.1mol溴共需要消耗标准状况下氯气的体积为0.1mol×2×22.4L/mol=44.8L,故C错
误;
D.从海水中取得淡水的过程为海水淡化,海水淡化常用的主要方法有蒸馏法、电渗析法和离子交换法,
故D正确;
故选D。
14.(2023·重庆统考三模)下列实验中采取的分离或提纯方法能达到实验目的的是
选项 实验目的 分离或提纯方法
A 分离碘的四氯化碳溶液中的碘 用苯萃取
B 除去乙酸乙酯中的乙酸 加入饱和 溶液后分液
C 除去蛋白质溶液中少量NaCl 过滤
D 从高级脂肪酸钠和甘油的混合水溶液中分离出高级脂肪酸钠 加入乙醇和浓硫酸并加热,然后蒸馏
资料整理【淘宝店铺:向阳百分百】【答案】B
【解析】A.苯与四氯化碳互溶,不能用作萃取剂分离溶于四氯化碳中的碘,A错误;
B.乙酸与碳酸钠反应,转化为易溶于水的盐,再通过分液即可提纯乙酸乙酯,B正确;
C.蛋白质溶于水后形成了胶体,胶体离子不能透过半透膜,而氯离子和钠离子能透过半透膜,因此应该
用渗析的方法,C错误;
D.油脂与氢氧化钠溶液反应后即得到高级脂肪酸钠与甘油的混合液,应该加入氯化钠颗粒,发生盐析的
过程,然后过滤,D错误;
故选B。
15.(2023·山东省实验中学校考模拟)为提纯下列物质(括号内的物质为杂质),所选用的除杂试剂和分离
方法均正确的有几项
① ② ③ ④ ⑤
混合物 乙醇(水) 乙酸乙酯(乙酸) 苯(苯酚) 溴苯(溴)
除杂试
饱和 溶液 生石灰 饱和 溶液 溴水 苯
剂
分离方
洗气 蒸馏 分液 过滤 萃取分液
法
A.1 B.2 C.3 D.4
【答案】B
【解析】①二氧化碳和二氧化硫均会和饱和碳酸钠溶液反应,除杂方法错误;
②生石灰和水生成氢氧化钙,然后利于乙醇沸点较低的性质蒸馏出乙醇,正确;
③碳酸钠和乙酸反应生成盐溶液、和乙酸乙酯不反应且分层,能用分液的方法分离出有机层乙酸乙酯,正
确;
④溴和苯酚生成的三溴苯酚溶于苯中,不能过滤分离,错误;
⑤苯与溴苯互溶,不能分液分离,错误;
故选B。
16.(2023·上海嘉定统考二模)制备下列物质过程中,净化除杂的有关操作(括号内是杂质)其中正确的是
A.C H(SO )——气体通过盛有溴水的洗气瓶
2 4 2
B.CHCOOC H(CHCOOH)——用饱和NaCO 溶液洗涤
3 2 5 3 2 3
C.Cl(HCl)——通过水洗,再干燥
2
D.NH (H O)——浓HSO 洗气
3 2 2 4
【答案】B
【解析】A.溴水与乙烯、二氧化硫均能反应,不符合除杂原理,选项A错误;
B.乙酸乙酯不溶于饱和碳酸钠,乙酸的酸性比碳酸强,能与碳酸钠反应生成二氧化碳而被吸收,然后分
液可得到纯净的乙酸乙酯,选项B正确;
C.氯气可与水反应,不能用水洗除去氯气中的氯化氢,选项C错误;
资料整理【淘宝店铺:向阳百分百】D.氨气与硫酸反应生成硫酸铵,不能用浓硫酸干燥氨气,选项D错误;
故选B。
17.(2023·上海长宁统考二模)除去下列物质中所含的少量杂质(括号内为杂质),所用除杂试剂合理的是
A.FeCl 溶液(CuCl )铁粉 B.C H(C H):H/催化剂
3 2 2 6 2 4 2
C.CO(SO ):酸性高锰酸钾溶液 D.乙醛(乙酸):饱和碳酸钠溶液
2 2
【答案】C
【解析】A.铁粉会与FeCl 发生反应,A项不合理;
3
B.C H 和H 反应产生C H 而除杂,但同时引入新杂质H,B项不合理;
2 4 2 2 6 2
C.SO 能与酸性高锰酸钾反应产生硫酸根,而CO 不反应,C项合理;
2 2
D.乙酸与碳酸钠反应,而乙醛溶于饱和碳酸钠溶于而无法分离,D项不合理;
故选C。
18.(2023·福建厦门模拟)从苯甲醛和 溶液反应后的混合液中分离出苯甲醇和苯甲酸的过程如下:
已知甲基叔丁基醚的密度为 。下列说法错误的是
A.“萃取”过程需振荡、放气、静置分层
B.“有机层”从分液漏斗上口倒出
C.“操作X”为蒸馏,“试剂Y”可选用盐酸
D.“洗涤”苯甲酸,用乙醇的效果比用蒸馏水好
【答案】D
【分析】苯甲醛和 溶液反应后的混合液中主要是生成的苯甲醇和苯甲酸钾,加甲基叔丁基醚萃取、
分液后,苯甲醇留在有机层中,加水洗涤、加硫酸镁干燥、过滤,再用蒸馏的方法将苯甲醇分离出来;而
萃取、分液后所得水层主要是苯甲酸钾,要加酸将其转化为苯甲酸,然后经过结晶、过滤、洗涤、干燥得
苯甲酸。
【解析】A.“萃取”过程需振荡、放气、静置分层,故A正确;
B.甲基叔丁基醚的密度为 ,密度比水小,所以要从分液漏斗上口倒出,故B正确;
C.“操作X”是将苯甲醇从有机物中分离出来,可以利用沸点不同用蒸馏的方法将其分离出来;“试剂Y”
的作用是将苯甲酸钾转化为苯甲酸,所以可选用盐酸,故C正确;
D.苯甲酸在乙醇中溶解度大于其在水中溶解度,“洗涤”苯甲酸,用蒸馏水的效果比用乙醇好,故D错
误;故选D。
19.(2023·宁夏银川联考一模)下列除杂方案错误的是
选项 被提纯的物质 杂质 除杂试剂 除杂方法
A 乙酸乙酯 乙酸 氢氧化钠 分液
资料整理【淘宝店铺:向阳百分百】B MgCl (aq) Fe3+(aq) MgO(s) 过滤
2
C CO(g) SO (g) 饱和NaHCO 、浓HSO 洗气
2 2 3 2 4
D NaCO(s) NaHCO (s) / 加热
2 3 3
【答案】A
【解析】A.乙酸乙酯能和强碱氢氧化钠发生反应,导致乙酸乙酯被反应,故A错误;
B.向氯化镁溶液中加入氧化镁,氧化镁能与铁离子水解生成的氢离子反应,使溶液中的氢离子浓度减小,
水解平衡向正反应方向移动,使铁离子转化为氢氧化铁沉淀,则用氧化镁能除去氯化镁溶液中存在的铁离
子,故B正确;
C.亚硫酸的酸性强于碳酸,SO 能与碳酸氢钠溶液反应,而二氧化碳不能与碳酸氢钠溶液反应,得到二氧
2
化碳气体使用浓硫酸干燥得到纯净干燥二氧化碳,则用碳酸氢钠溶液能除去二氧化碳中混有的二氧化硫,
故C正确;
D.碳酸氢钠固体受热分解生成碳酸钠、水和二氧化碳,而碳酸钠受热不分解,则用加热的方法能除去碳
酸钠固体中混有的碳酸氢钠固体,故D正确;
故选A。
20.(2023·山东烟台模拟)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步
分离甲苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是
A.苯胺既可与盐酸也可与 溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
【答案】C
【分析】由题给流程可知,向甲苯、苯胺、苯甲酸的混合溶液中加入盐酸,盐酸将微溶于水的苯胺转化为
易溶于水的苯胺盐酸盐,分液得到水相Ⅰ和有机相Ⅰ;向水相中加入氢氧化钠溶液将苯胺盐酸盐转化为苯
胺,分液得到苯胺粗品①;向有机相中加入水洗涤除去混有的盐酸,分液得到废液和有机相Ⅱ,向有机相
Ⅱ中加入碳酸钠溶液将微溶于水的苯甲酸转化为易溶于水的苯甲酸钠,分液得到甲苯粗品②和水相Ⅱ;向
水相Ⅱ中加入盐酸,将苯甲酸钠转化为苯甲酸,经结晶或重结晶、过滤、洗涤得到苯甲酸粗品③。
【解析】A.苯胺分子中含有的氨基能与盐酸反应,但不能与氢氧化钠溶液反应,故A错误;
B.由分析可知,得到苯胺粗品①的分离方法为分液,得到苯甲酸粗品③的分离方法为结晶或重结晶、过
滤、洗涤,获取两者的操作方法不同,故B错误;
C.由分析可知,苯胺粗品、甲苯粗品、苯甲酸粗品依次由①、②、③获得,故C正确;
资料整理【淘宝店铺:向阳百分百】D.由分析可知,①、②为液相,③为固相,都不是两相混合体系,故D错误;
故选C。
资料整理【淘宝店铺:向阳百分百】