文档内容
浦东一模试卷点评
和往年相比难度变大不少,从单选题最后一题就出现了中档难度的实验探究问题,不定项选择的后
两题都有学生易错点,比如第二题D选项看似考计算,实则往年出现过把“生成”改为“收集”。不定
项的最后一题结合了书本提过的空气中氧气含量测定实验稍作改编,成为了一道非常有水平的选择题。
大题难度更是明显超过往年的浦东一模,前两道比较中规中矩,但是后两题,尤其是最后一题结合
了古代冶炼金属的情境,既考察了计算,又考察了实验探究,难度较大。
初三综合测试期末练习卷
化 学 部 分
相对原子质量:H-1 O-16 Cl-35.5 K-39
五、选择题(共20分)
请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新填涂。
第21~34题,每题均只有一个正确选项。
21.下列工艺属于化学变化的是
A.剪窗花 B.晒海盐 C.酿米酒 D.织衣布
【答案】C ABD都是物理变化,C是从粮食最终变成了乙醇
22.属于非金属元素的是
A.Si B.Al C.Ag D.Fe
【答案】A 硅是非金属元素,元素周期表中名称有金字旁的一定是金属元素,没有金字旁的只有汞是金
属元素
23.属于纯净物的是
A.自来水 B.蒸馏水 C.矿泉水 D.江河水
【答案】B ACD中都有其他物质
24.加入水中形成浊液的是
A.蔗糖 B.食盐 C.酒精 D.汽油
【答案】D ABC都是常见的可溶性物质,D会漂在水上层形成乳浊液
25.三氧化二锑(SbO)主要用于防火涂料,其中Sb的化合价为
2 3
A.-2 B.-3 C.+2 D.+3
【答案】D O是-2价,所以Sb是+3
初三综合测试(化学部分) 第5页 共5页26.维生素泡腾片的水溶液呈酸性,滴入紫色石蕊试液,溶液呈
A.红色 B.紫色 C.蓝色 D.无色
【答案】A 石蕊溶液酸红碱蓝
27.与足球烯(C )互为同素异形体的是
60
A.木炭 B.金刚石 C.一氧化碳 D.碳酸钙
【答案】B 易错的选项A是无定形碳,属于混合物,同素异形体是同种元素不同单质
28.关于硫酸铜(CuSO)说法正确的是
4
A.蓝色晶体 B.属于氧化物
C.俗称胆矾 D.用于检验水
【答案】D 无水硫酸铜是白色固体,遇到水才会变蓝,用于检验水
29.镁带燃烧的化学方程式,书写正确的是
A.Mg+O MgO B.2Mg+O MgO
2 2 2
C.2Mg+O 2MgO D.Mg+O MgO
2 2
【答案】C 产物是氧化镁,考察方程式书写和配平
30.物质的用途主要利用其化学性质的是
A.干冰用于人工降雨 B.氮气用作保护气
C.石墨用于制铅笔芯 D.氦气制作霓虹灯
【答案】B 氮气化学性质稳定不容易反应,这是化学性质,其余都是物理性质
31.2024年我国环境日主题是“全面推进美丽中国建设”。下列做法符合该主题的是
A.分类回收生活垃圾 B.工业废水直接排放
C.推广使用煤炭燃料 D.随意丢弃废旧电池
【答案】A 考察绿色环保相关常识
32.某同学发现实验室里一个久置的酒精灯不易点燃。有同学认为因为酒精蒸发后灯芯上有水,该环节
属于化学实验探究中的
A.提出问题 B.假设猜想 C.收集证据 D.形成结论
【答案】B 问题是为什么不易点燃,现在假设是因为有水,后面做实验是收集证据,最后给结论
33.科学家利用光催化技术实现了绿色制取HO,反应的微观示意图如图所示。下列说法正确的是
2 2
催化剂 氢原子
+
光照 氧原子
甲 乙
A.反应后氧原子个数减少 B.1 mol HO 含6.02×1023个氧分子
2 2
初三综合测试(化学部分) 第5页 共5页C.乙的化学式为HO D.参加反应的甲、乙分子个数比为2∶3
2
【答案】C 通过微观示意图考察质量守恒定律,反应是氧气和水反应生产过氧化氢
34.基于问题设计实验方案是实验探究活动的重要环节。下列实验方案中合理的是
A.除去CO 中少量的CO:将混合气体点燃
2
B.除去MnO 中少量的KCl:加足量的水溶解,过滤,蒸发
2
C.检验CaO中是否有Ca(OH):加水溶解,滴入酚酞溶液
2
D.检验甲烷(CH)中是否有氢元素:点燃甲烷,在火焰上方罩一个干燥的冷烧杯
4
【答案】D A不纯会爆炸 B过滤后就可得到二氧化锰 C氧化钙遇水反应产生氢氧化钙也是碱性
35~37每题有1~2个正确选项。
35.关于氧气说法正确的是
A.氧气具有助燃性,常用作燃料 B.氧气加压降温变成液氧,氧分子变小了
C.可燃物接触氧气不一定能燃烧 D.物质在氧气中的反应一定是化合反应
【答案】 C A可燃物才是燃料 B分子间平均距离变小了 C需要达到着火点 D产物可以不唯一,
比如甲烷燃烧
36.用氯酸钾和二氧化锰制取氧气的装置如图所示。有关说法正确的是
A.试管口略向下倾斜是因为氧气密度比空气大
B.该收集方法得到的氧气较纯净
C.反应前后固体中二氧化锰的质量分数不变
D.生成0.03 mol氧气,需要2.45 g氯酸钾
【答案】BD A 放置冷凝水回流 B 比排空气法收集更纯净 C 反应后二氧化锰质量分数变大 D
2.45g氯酸钾是0.02mol,反应是2:3产生氧气
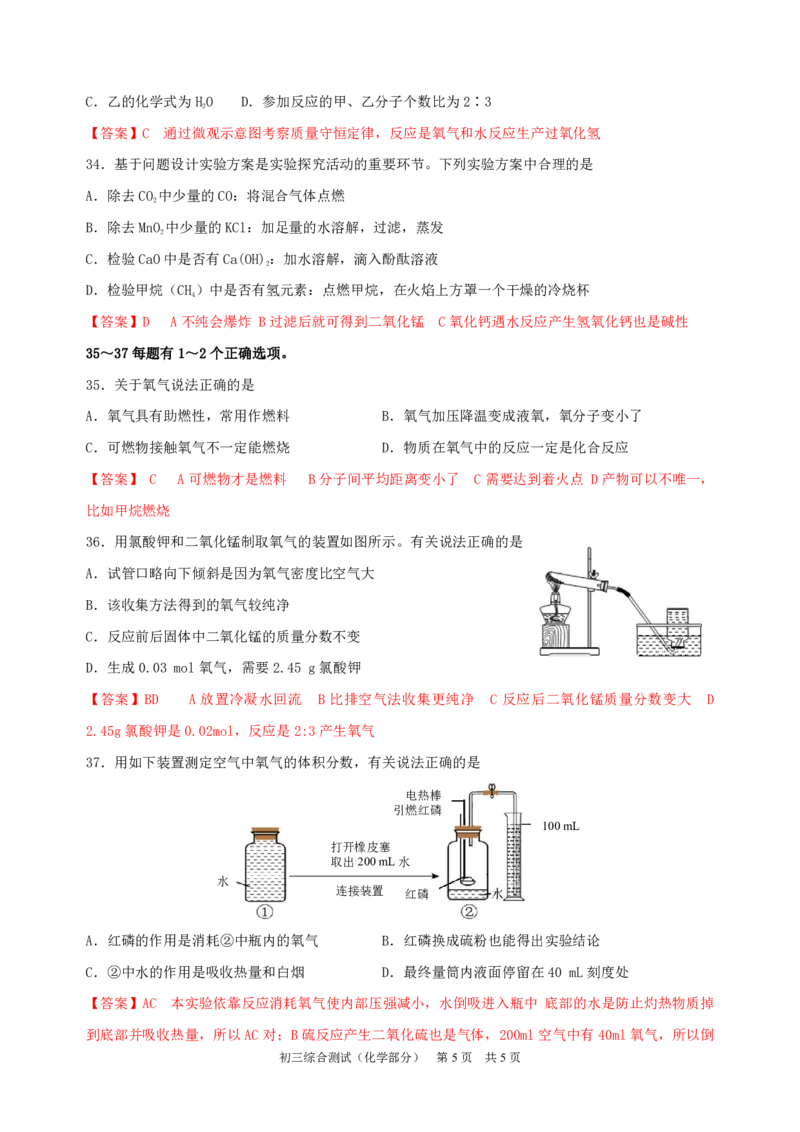
37.用如下装置测定空气中氧气的体积分数,有关说法正确的是
电热棒
引燃红磷
100mL
打开橡皮塞
取出200mL水
水
连接装置 红磷
A.红磷的作用是消耗②中瓶内的氧气 B.红磷换成硫粉也能得出实验结论
C.②中水的作用是吸收热量和白烟 D.最终量筒内液面停留在40 mL刻度处
【答案】AC 本实验依靠反应消耗氧气使内部压强减小,水倒吸进入瓶中 底部的水是防止灼热物质掉
到底部并吸收热量,所以AC对;B硫反应产生二氧化硫也是气体,200ml空气中有40ml氧气,所以倒
初三综合测试(化学部分) 第5页 共5页吸40ml,量筒应该在60ml刻度
六、简答题(共30分)
84消毒液
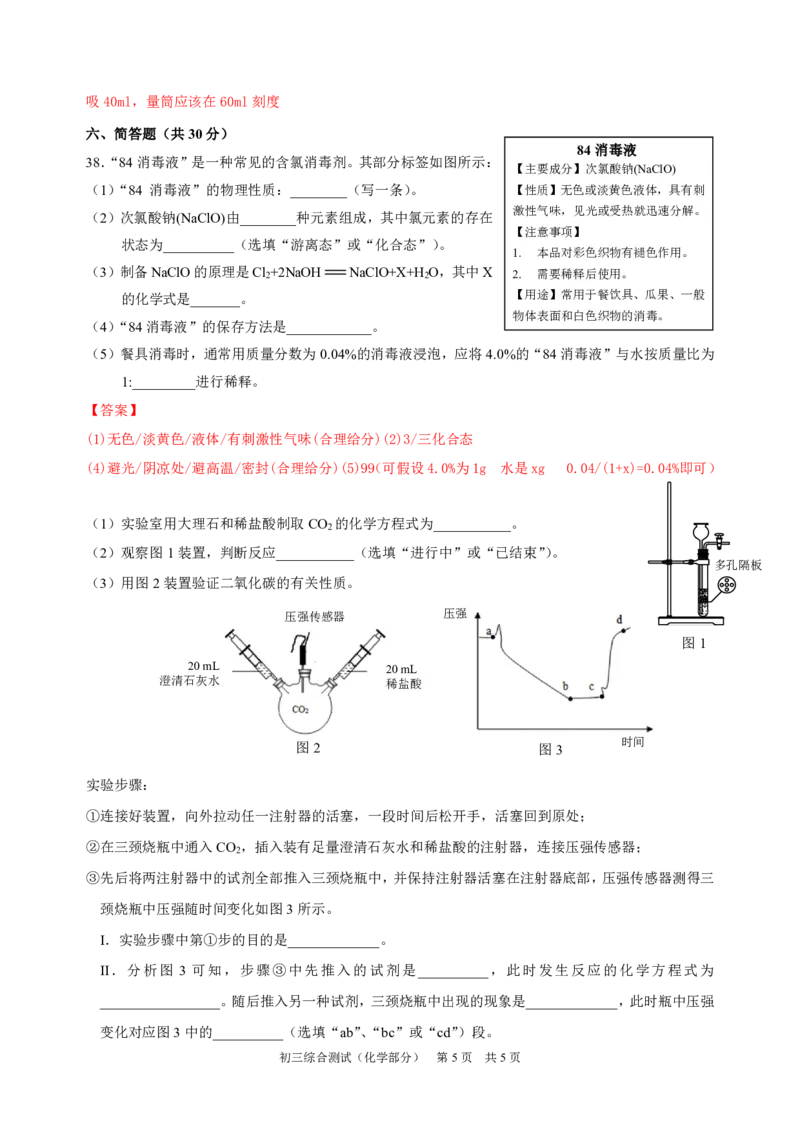
38.“84消毒液”是一种常见的含氯消毒剂。其部分标签如图所示:
【主要成分】次氯酸钠(NaClO)
(1)“84 消毒液”的物理性质:________(写一条)。 【性质】无色或淡黄色液体,具有刺
激性气味,见光或受热就迅速分解。
(2)次氯酸钠(NaClO)由________种元素组成,其中氯元素的存在
【注意事项】
状态为__________(选填“游离态”或“化合态”)。
1. 本品对彩色织物有褪色作用。
(3)制备NaClO的原理是Cl 2 +2NaOH NaClO+X+H 2 O,其中X 2. 需要稀释后使用。
的化学式是_______。 【用途】常用于餐饮具、瓜果、一般
物体表面和白色织物的消毒。
(4)“84消毒液”的保存方法是____________。
(5)餐具消毒时,通常用质量分数为0.04%的消毒液浸泡,应将4.0%的“84消毒液”与水按质量比为
1:_________进行稀释。
【答案】
(1)无色/淡黄色/液体/有刺激性气味(合理给分)(2)3/三化合态
(4)避光/阴凉处/避高温/密封(合理给分)(5)99(可假设4.0%为1g 水是xg 0.04/(1+x)=0.04%即可)
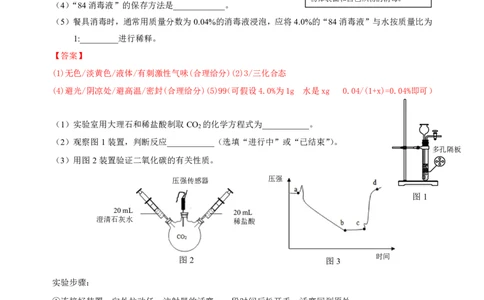
(1)实验室用大理石和稀盐酸制取CO 的化学方程式为___________。
2
(2)观察图1装置,判断反应___________(选填“进行中”或“已结束”)。
多孔隔板
(3)用图2装置验证二氧化碳的有关性质。
压压强强传传感感器器 压强
图1
20mL 20mL
澄清石灰水 稀盐酸
时间
图2 图3
实验步骤:
①连接好装置,向外拉动任一注射器的活塞,一段时间后松开手,活塞回到原处;
②在三颈烧瓶中通入CO ,插入装有足量澄清石灰水和稀盐酸的注射器,连接压强传感器;
2
③先后将两注射器中的试剂全部推入三颈烧瓶中,并保持注射器活塞在注射器底部,压强传感器测得三
颈烧瓶中压强随时间变化如图3所示。
Ⅰ.实验步骤中第①步的目的是_____________。
Ⅱ.分析图 3 可知,步骤③中先推入的试剂是__________,此时发生反应的化学方程式为
_________________。随后推入另一种试剂,三颈烧瓶中出现的现象是_____________,此时瓶中压强
变化对应图3中的__________(选填“ab”、“bc”或“cd”)段。
初三综合测试(化学部分) 第5页 共5页【答案】(1)CaCO+2HC1=CaCl+HO+CO↑ (2) 进行中(液面未降到与反应物脱离)
3 2 2 2
(3)检查装置气密性 氢氧化钙/Ca(0H)/澄清石灰水 Ca(0H)+C0=CaC0↓+H0
2 2 2 2 2
沉淀消失、产生气泡 cd(反应产生气体,压强变大)
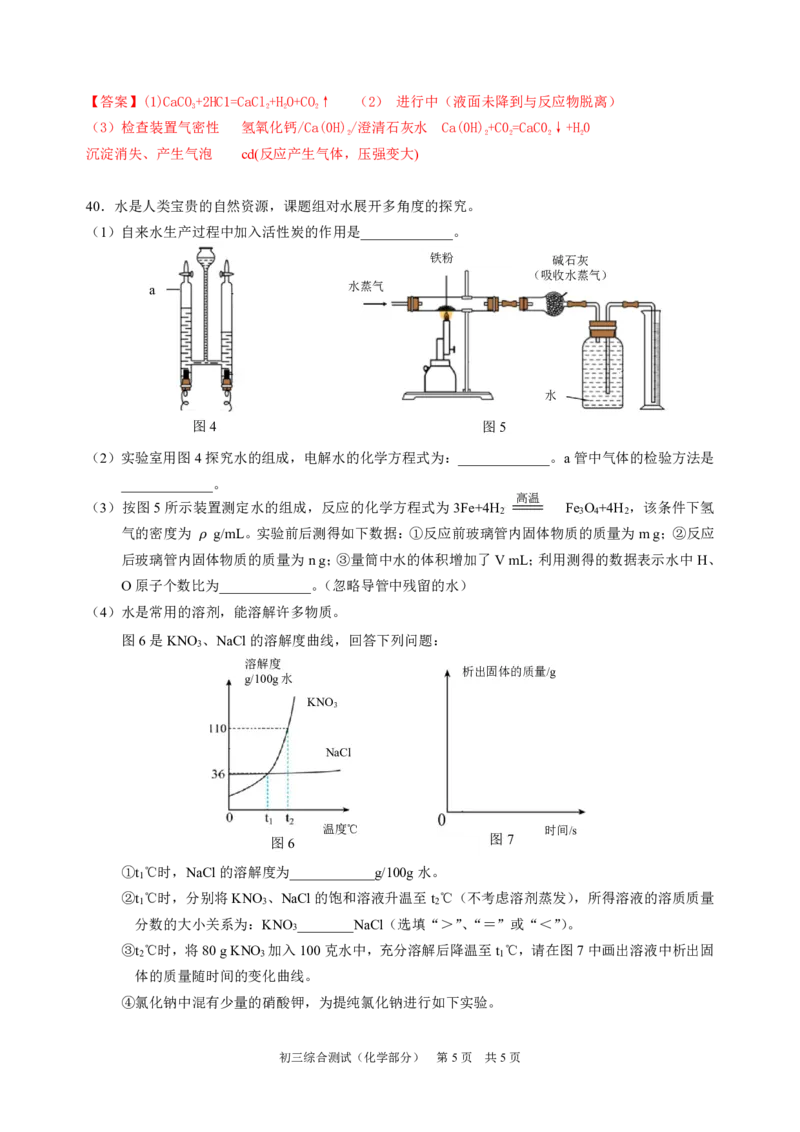
40.水是人类宝贵的自然资源,课题组对水展开多角度的探究。
(1)自来水生产过程中加入活性炭的作用是_____________。
铁粉 碱石灰
(吸收水蒸气)
水蒸气
a
水
图4 图5
(2)实验室用图4探究水的组成,电解水的化学方程式为:_____________。a管中气体的检验方法是
_____________。
高温
(3)按图5所示装置测定水的组成,反应的化学方程式为3Fe+4H O Fe O +4H ,该条件下氢
2 3 4 2
气的密度为 g/mL。实验前后测得如下数据:①反应前玻璃管内固体物质的质量为mg;②反应
后玻璃管内固
体物质的质量为ng;③量筒中水的体积增加了VmL;利用测得的数据表示水中H、
O原子个数比为_____________。(忽略导管中残留的水)
(4)水是常用的溶剂,能溶解许多物质。
图6是KNO 、NaCl的溶解度曲线,回答下列问题:
3
溶解度
析出固体的质量/g
g/100g水
KNO3
NaCl
温度℃ 时间/s
图6 图7
①t ℃时,NaCl的溶解度为____________g/100g水。
1
②t ℃时,分别将KNO 、NaCl的饱和溶液升温至t ℃(不考虑溶剂蒸发),所得溶液的溶质质量
1 3 2
分数的大小关系为:KNO ________NaCl(选填“>”、“=”或“<”)。
3
③t ℃时,将80gKNO 加入100克水中,充分溶解后降温至t ℃,请在图7中画出溶液中析出固
2 3 1
体的质量随时间的变化曲线。
④氯化钠中混有少量的硝酸钾,为提纯氯化钠进行如下实验。
初三综合测试(化学部分) 第5页 共5页氯化钠
加一定量水 边搅拌边加热 趁热过滤
固体混合物 悬浊液
滤液
实验操作中加热的原因____________。
若要确定滤液是否为硝酸钾的饱和溶液,可进行的实验是____________。
【答案】(1)吸附 (2) 2H O通电2H 个+O ↑ 打开a管活塞,用带火星的木条靠近a管口复燃
2 2 2
(3)ρV÷[(n-m)/16]=16ρV/(n-m) (4)36 =(看图)(5)
41.铜是重要的金属材料。
(1)三千多年前我国就掌握了“火法炼铜”,其原理是用木炭和氧化铜在高温的条件下生成铜和二氧化
碳,该反应的化学方程式为____________。
(2)课题组用铜丝和碳粉探究碳还原氧化铜的实验。
①把mg铜丝的一端卷成螺旋状,在酒精灯上加热(见图8),生成_____色的氧化铜。
②把加热后的铜丝插入碳粉中,按图9连接装置。点燃酒精灯,反应一段时间后熄灭酒精灯,待装置冷
却到室温后,将注射器1中20mL氮气全部注入,关闭注射器上的弹簧夹。最终注射器2的活塞停留
在amL处,取出铜丝称量为ng。(装置气密性良好,试管、导管和干燥管的体积约为20mL,空气中
的二氧化碳忽略不计)
注射器1
内装20mL氮
气
注射器2
初始刻度为 0
mL
干燥管
足量澄清石灰水
图8 图9
Ⅰ.铜丝卷成螺旋状的原因是____________。
Ⅱ.能证明该实验还生成了一氧化碳的现象是____________。
Ⅲ.比较m与n的大小,并说明理由____________。
Ⅳ.该实验选用铜丝的优点:一是新制的氧化铜更容易与碳粉反应;二是______________。
【答案】(1)C+2CuO高温2Cu+CO ↑(2)黑 增大与反应物的接触面积 注射器2的活塞停留在a处的
2
刻度大于 20ml(合理给分) 当氧化铜完全反应则 m=n,当氧化铜部分反应则 m