文档内容
专题 03 离子反应
(考试时间:75分钟 试卷满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一项是符合题目要求的)
1.下列属于非电解质的是( )
A. 氢气 B. 蔗糖溶液 C. 已烷 D. 硫化钠
2.下列离子方程式书写错误的是
A.将HO 溶液滴入酸性高锰酸钾溶液中:HO+ 2MnO-+6H+=2Mn2++4H O+3O↑
2 2 2 2 4 2 2
B.小苏打溶液显碱性的主要原因:HCO -+H O HCO+OH-
3 2 2 3
C.向新制氢氧化铜悬浊液中加入乙醛溶液并加热:CHCHO+2 Cu(OH)+OH- CHCOO-+
3 2 3
CuO↓+3H O
2 2
D.少量二氧化碳通入偏铝酸钠溶液中:CO+2AlO -+3H O=CO2-+2Al(OH)↓
2 2 2 3 3
3.下列反应对应的离子方程式书写正确的是( )
A.向NaAlO 溶液中通入过量CO 制Al(OH) :AlO-+CO +2H O=Al(OH) ↓+HCO-
2 2 3 2 2 2 3 3
B.将Na单质放入HO中:Na+HO=Na++H ↑+OH-
2 2 2
C.Cr(OH) 的悬浊液中同时加入NaOH溶液和HO 制NaCrO :2Cr3++3H O+10OH-=2CrO -+8H O
3 2 2 2 4 2 2 4 2
D.用惰性电极电解NaCl溶液:2Cl-+2H+ Cl↑+H ↑
2 2
4.室温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=12的溶液:Na+、K+、NO、ClO-
B.能使甲基橙变红的溶液:Na+、NH、Cl-、CHCOO-
3
C.1.0 mol·L-1的KNO 溶液:Fe2+、H+、SO、I-
3
D.0.1 mol·L-1 NaAlO 溶液:NH、Al3+、Cl-、CO
2
5.常温下,下列各组离子在指定溶液中能大量共存的是( )
A.0.1 mol·L-1 FeSO 溶液:Na+、K+、Cl-、NO
4
B.滴入酚酞变红色的溶液:K+、Ca2+、HCO、CO
C.加入铁粉放出氢气的溶液:NH、Fe3+、ClO-、SO
D.水电离的c(H+)=1×10-13mol·L-1的溶液:K+、Mg2+、I-、C HO-
6 5
6.(2024·浙江强基联盟高三联考)下列反应的离子方程式正确的是( )
A.向FeBr 溶液中通入足量Cl:2Fe2++2Br - +2Cl= 2Fe3++Br+4Cl-
2 2 2 2
B.向CaCl 溶液中通入CO:Ca2++CO+H O= CaCO ↓+2H+
2 2 2 2 3
C.向NH Al(SO ) 溶液中滴入Ba(OH) 溶液使SO 2-完全沉淀:NH ++Al3++2SO2+4OH-=2BaCO ↓+
4 4 2 2 4 4 4 3
Al(OH) ↓+ NH ·H O
3 3 2
D.实验室用FeS制取少量HS:S2-+2H+= H S↑
2 2
7.(2024·浙江省 A9 协作体高三联考)能正确表示下列反应的离子方程式是( )
A.硝酸银溶液中滴入少量氨水:Ag++2NH=[Ag(NH )]+
3 3 2
B.二氧化锰与浓盐酸共热:MnO +4HCl Mn2++2Cl-+Cl↑+2H O
2 2 2
C.乙酰甲胺在稀盐酸中水解:CHCONHCH +H O+H+ CHCOOH+CH NH +
3 3 2 3 3 3D.次氯酸钙溶液中通入少量二氧化硫:Ca2++ClO-+SO+H O=CaSO↓+Cl-+2H+
2 2 4
8.(2024·浙江省百校高三起点联考)下列反应的离子方程式正确的是( )
A.工业上生产漂白粉:2OH-+Cl=Cl-+ClO-+H O
2 2
B.用惰性电极电解饱和ZnCl 溶液:Zn2++2Cl-+2H O Zn(OH) ↓+Cl↑+H ↑
2 2 2 2 2
C.二氧化硫通入氯化铁溶液中:SO +2Fe3++2H O=2Fe2++4H++SO2-
2 2 4
D.NaHSO 溶液与Ba(OH) 溶液反应恰好呈中性:H++SO2-+Ba2++OH-=BaSO ↓+H O
4 2 4 4 2
9.下列离子方程式书写正确的是( )
A.2.24LCO 通入250 mL 0.5 mol/L的 NaOH溶液中:4CO+5OH-=CO 2-+3HCO -+HO
2 2 3 3 2
B.在100 mL 2 mol/L的FeI 的溶液中通入标准状况下5.6 L的Cl:4Fe2++6I-+5Cl=4Fe3++3I+
2 2 2 2
10Cl-
C.100 mL 0.1 mol/L的NaCO 溶液中加入0.01 molCH COOH:CO2- +2 CHCOOH=HO+CO↑+
2 3 3 3 3 2 2
CHCOO-
3
D.4 mol/L的NaAlO 溶液和7 mol/L的盐酸等体积均匀混合:4AlO- + 7H+ + H O=3Al(OH) ↓+ Al3+
2 2 2 3
10.某强酸性溶液中可能存在Al3+、Fe2+、NH、Ba2+、Cl-、CO、SO、NO中的若干种,为确定溶液
组成进行如下实验:
(1)取100 mL原溶液,加入足量Ba(NO ) 溶液,有白色沉淀a和无色气体b生成,过滤得滤液c。
3 2
(2)往(1)所得滤液c中加入足量的NaOH溶液并加热,可得气体d和沉淀e,过滤。
(3)取(2)中过滤所得滤液,通入少量的CO,有白色沉淀f生成。
2
下列有关判断正确的是( )
A.试液中一定没有Ba2+、CO、NO、Cl-
B.试液中一定有Fe2+、NH、Al3+、SO
C.气体b和气体d在一定条件下能发生反应生成一种单质和一种无色液体
D.沉淀f一定含有Al(OH) ,可能含有BaCO
3 3
11.下列各组微粒在溶液中可以大量共存,且在加入试剂X后发生反应的离子方程式书写也正确的是(
)
选项 微粒组 试剂X 发生反应的离子方程式
Al3++3HCO===3CO ↑+
A Cl-、NO、Al3+、NH 少量NaHCO 溶液 2
3
Al(OH) ↓
3
B NH、Fe2+、I-、SO 少量氯水 2Fe2++Cl===2Fe3++2Cl-
2
C Al3+、Ba2+、AlO、NO 适量的NaSO Ba2++SO===BaSO ↓
2 4 4
SO+S2-+4H+===2S↓+
D Na+、SO、S2-、Cl- 适量HCl
2HO
2
12.下表第Ⅰ栏与第Ⅱ栏中的化学反应,都可以用第Ⅲ栏中的离子方程式表示的是( )
选项 第Ⅰ栏 第Ⅱ栏 第Ⅲ栏
向少量NaOH溶液中投入 向过量NaOH溶液中投入 2Al+6HO===2Al(OH) +
2 3
A
铝片 铝片 3H↑
2
向Fe (SO ) 溶液中滴入 向Fe (SO ) 溶液中滴入
B 2 4 3 2 4 3 Fe3++3OH-===Fe(OH) ↓
3
NaOH溶液 Ba(OH) 溶液
2向Ca(HCO ) 溶液中滴入 向Ca(HCO ) 溶液中滴入 Ca2++OH-+
3 2 3 2
C
Ca(OH) 溶液 少量的NaOH溶液 HCO===CaCO ↓+HO
2 3 2
向NaOH溶液中通入过量 向NaOH溶液中通入少量
D CO+OH-===HCO
2
CO 气体 CO 气体
2 2
13.下列各组离子能大量共存,且当加入相应试剂后发生反应的离子方程式书写正确的是
选项 离子组 加入试剂 现象或离子方程式
A NH +、Fe2+、SO 2- 少量Ba(OH) 溶液 2NH ++SO2-+Ba2++2OH-=BaSO ↓+2NH·H O
4 4 2 4 4 4 3 2
K+、Cr O2- (橙色)、
B 2 7 滴加少量浓HSO 溶液橙色加深,Cr O2-+2OH- 2CrO2-+H O
CrO2-(黄色) 2 4 2 7 4 2
4
⇌
C H+、MnO -、Cl- 滴加少量HO 2MnO -+6H++5H O=2Mn2++5O ↑+8H O
4 2 2 4 2 2 2 2
Mg2+、HCO -、Cl-(物质
D 3 过量NaOH溶液 Mg2++HCO +3OH-=H O+Mg(OH)↓+CO 2-
的量比1:1:1) 2 2 3
14.室温下,通过下列实验探究0.1mol·L−1NaHCO 和0.1mol·L−1NaCO 溶液的性质。
3 2 3
实验1: 用pH试纸测得0.1mol·L−1NaCO 溶液pH约为12
2 3
实验2: 两溶液中分别加入等体积的0.1mol·L−1CaCl 溶液,都产生白色沉淀
2
实验3: 0.1mol·L−1NaHCO 与0.1mol·L−1Ba(OH) 溶液等体积混合,产生白色沉淀
3 2
实验4: 向两溶液中不断滴加0.1mol·L−1HCl溶液,至不再产生气体
下列说法正确的是( )
A.0.1mol·L−1NaCO 溶液中存在c(OH-)=c(H+)+c(HCO-)+c(H CO)
2 3 3 2 3
B.实验2中CaCl 溶液滴入后,两试管中溶液pH均降低
2
C.实验3中的离子方程式为:Ba2++2OH-+2HCO-=BaCO ↓+ CO2-+2H O
3 3 3 2
D.实验4中完全反应后,两试管中溶液中都存在:c(H+)+c(Na+)=c(Cl-)+c(OH-)+c(CO 2-)+c(HCO-)
3 3
15.(2024·山东淄博高三模拟)为探究FeCl 的性质,进行了如下实验(已知:FeCl 和NaSO 溶液浓度
3 3 2 3
均为0.1mol/L,[Fe(H O) ]3+呈浅紫色,[Fe(H O) OH]2+呈棕黄色)。
2 6 2 5
实
操作与现象
验
① 在5mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色。
3
在5 mL FeCl 溶液中滴加2滴NaSO 溶液,溶液变红褐色;再滴加K[Fe(CN) ]溶液,产生蓝色沉
② 3 2 3 3 6
淀。
在5 mL Na SO 溶液中滴加2滴FeCl 溶液,溶液变红褐色;将上述混合液分成两份,一份滴加
③ 2 3 3
K[Fe(CN) ]溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色沉淀。
3 6
依据上述实验现象,方程式或结论不合理的是( )
A.实验①的“煮沸”反应方程式为:[Fe(H O) OH]2+=Fe(OH) +2H O++H O
2 5 3 3 2
B.实验②溶液中只发生反应2Fe3++SO2-+H O=2Fe2++SO2-+2H+
3 2 4C.实验③“变红褐色”反应方程式为:Fe3++3SO2-+3H O= Fe(OH) +3HSO -
3 2 3 3
D.整个实验说明 对 的水解反应和还原反应均有影响
二、非选择题(本题包括4小题,共55分)
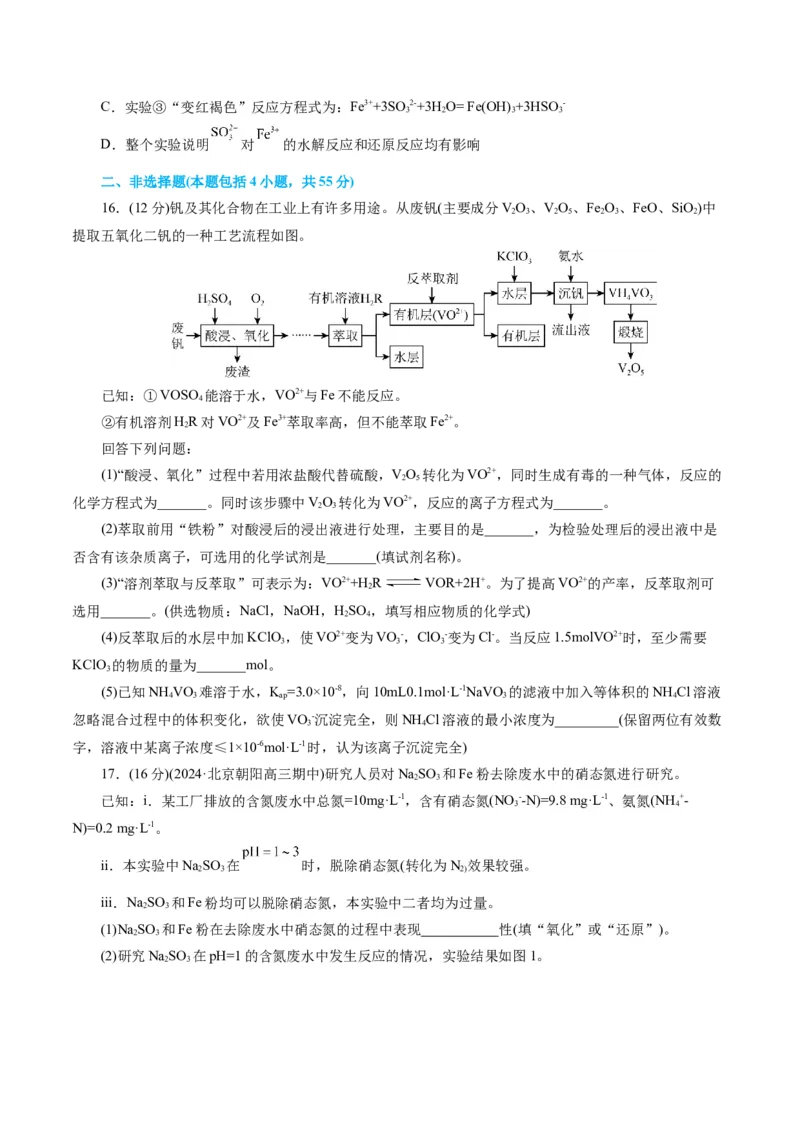
16.(12分)钒及其化合物在工业上有许多用途。从废钒(主要成分VO、VO、Fe O、FeO、SiO)中
2 3 2 5 2 3 2
提取五氧化二钒的一种工艺流程如图。
已知:①VOSO 能溶于水,VO2+与Fe不能反应。
4
②有机溶剂HR对VO2+及Fe3+萃取率高,但不能萃取Fe2+。
2
回答下列问题:
(1)“酸浸、氧化”过程中若用浓盐酸代替硫酸,VO 转化为VO2+,同时生成有毒的一种气体,反应的
2 5
化学方程式为_______。同时该步骤中VO 转化为VO2+,反应的离子方程式为_______。
2 3
(2)萃取前用“铁粉”对酸浸后的浸出液进行处理,主要目的是_______,为检验处理后的浸出液中是
否含有该杂质离子,可选用的化学试剂是_______(填试剂名称)。
(3)“溶剂萃取与反萃取”可表示为:VO2++H R VOR+2H+。为了提高VO2+的产率,反萃取剂可
2
选用_______。(供选物质:NaCl,NaOH,HSO ,填写相应物质的化学式)
2 4
(4)反萃取后的水层中加KClO,使VO2+变为VO -,ClO -变为Cl-。当反应1.5molVO2+时,至少需要
3 3 3
KClO 的物质的量为_______mol。
3
(5)已知NH VO 难溶于水,K =3.0×10-8,向10mL0.1mol·L-1NaVO 的滤液中加入等体积的NH Cl溶液
4 3 ap 3 4
忽略混合过程中的体积变化,欲使VO -沉淀完全,则NH Cl溶液的最小浓度为_________(保留两位有效数
3 4
字,溶液中某离子浓度≤1×10-6mol·L-1时,认为该离子沉淀完全)
17.(16分)(2024·北京朝阳高三期中)研究人员对NaSO 和Fe粉去除废水中的硝态氮进行研究。
2 3
已知:i.某工厂排放的含氮废水中总氮=10mg·L-1,含有硝态氮(NO --N)=9.8 mg·L-1、氨氮(NH +-
3 4
N)=0.2 mg·L-1。
ii.本实验中NaSO 在 时,脱除硝态氮(转化为N 效果较强。
2 3 2)
iii.NaSO 和Fe粉均可以脱除硝态氮,本实验中二者均为过量。
2 3
(1)Na SO 和Fe粉在去除废水中硝态氮的过程中表现 性(填“氧化”或“还原”)。
2 3
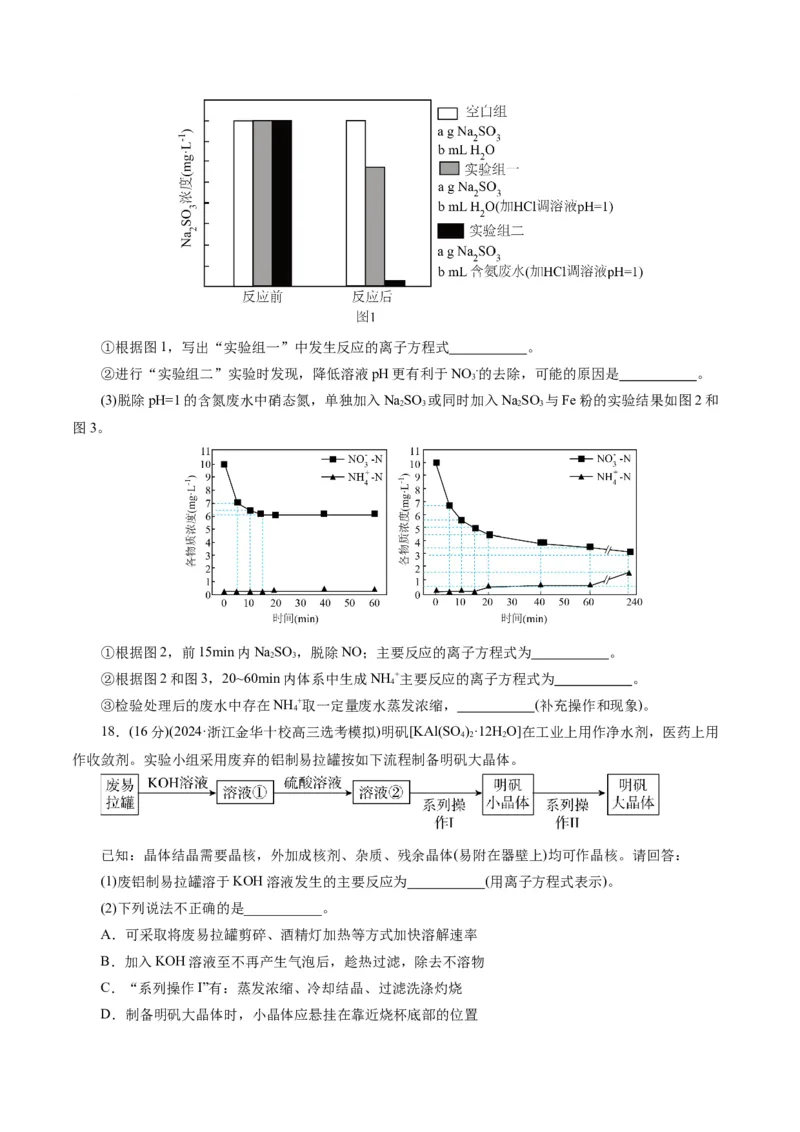
(2)研究NaSO 在pH=1的含氮废水中发生反应的情况,实验结果如图1。
2 3①根据图1,写出“实验组一”中发生反应的离子方程式 。
②进行“实验组二”实验时发现,降低溶液pH更有利于NO -的去除,可能的原因是 。
3
(3)脱除pH=1的含氮废水中硝态氮,单独加入NaSO 或同时加入NaSO 与Fe粉的实验结果如图2和
2 3 2 3
图3。
①根据图2,前15min内NaSO ,脱除NO;主要反应的离子方程式为 。
2 3
②根据图2和图3,20~60min内体系中生成NH +主要反应的离子方程式为 。
4
③检验处理后的废水中存在NH +取一定量废水蒸发浓缩, (补充操作和现象)。
4
18.(16分)(2024·浙江金华十校高三选考模拟)明矾[KAl(SO )·12H O]在工业上用作净水剂,医药上用
4 2 2
作收敛剂。实验小组采用废弃的铝制易拉罐按如下流程制备明矾大晶体。
已知:晶体结晶需要晶核,外加成核剂、杂质、残余晶体(易附在器壁上)均可作晶核。请回答:
(1)废铝制易拉罐溶于KOH溶液发生的主要反应为 (用离子方程式表示)。
(2)下列说法不正确的是___________。
A.可采取将废易拉罐剪碎、酒精灯加热等方式加快溶解速率
B.加入KOH溶液至不再产生气泡后,趁热过滤,除去不溶物
C.“系列操作I”有:蒸发浓缩、冷却结晶、过滤洗涤灼烧
D.制备明矾大晶体时,小晶体应悬挂在靠近烧杯底部的位置(3)“系列操作II”的装置如图所示,烧杯上方所盖的纸片的作用是 。
(4) Al3+是一种慢性神经毒素,长期积累会导致神经结节。实验室可采用置换滴定法测定天然水体样品
中的Al3+浓度。简要过程如下:
有关反应如下(试剂EDTA用 表示):
步骤①:Al3++Y4-=AlY-
步骤②:Zn2++Y4-= ZnY2-
步骤③: AlY- +6F-=AlF 3-+Y4-
6
①下列有关说法不正确的是 。
A.碱式滴定管有气泡时,将橡皮塞向上弯曲,两手指挤压橡皮管中玻璃珠的下方(图所示位置),将气
泡从管尖排出
B.天然水体样品中的Ca2+ ( CaY2-不与F反应)不影响 含量的测定
C.步骤①所加试剂EDTA,实验前不需要标定其浓度
D.如果步骤②所加Zn2+标准溶液偏少,会导致 浓度的测定值小于真实值
②根据检测过程,请给出配合离子ZnY2-、AlY-、AlF3-的稳定性由弱到强的顺序: 。
6
③要准确计算水样中 浓度,须利用水样1的体积以及步骤 的实验数据(选填:①、②、③、
④)
19.(13分)碘化亚铜( )可用作有机反应催化剂。某化学兴趣小组以黄铜矿(主要成分为CuFeS,其
2
中Cu的化合价为+2)为原料制备CuI的流程如下:已知:CuI是白色粉末,不溶于水,能与过量 继续反应:CuI(s)+I- [ CuI ]-,从而溶于KI溶液
2
中。
回答下列问题:
(1)“浸取”时,反应的化学方程式为_______;该步骤使用的FeCl 溶液的浓度为560 g ·L-1,则其物质
3
的量浓度为_______ mol·L-1 (保留2位小数)。
(2)“滤渣处理”过程中发生的基本反应类型为_______。
(3)“溶解”时,NO -被还原为NH +,写出该反应的离子方程式:_______。
3 4
(4)“转化”时生成CuI的离子方程式为_______,该步骤需要控制KI溶液的用量,其原因是_______。
(5)用NaSO 溶液洗涤沉淀的目的是_______。
2 3
(6)已知:K (CuBr)= 6.2×10-9,K (CuI)= 1.24×10-12,取2.00gCuI放入锥形瓶中,加入100mLa mol·L-1NaBr
sp sp
溶液,充分振荡后,测得溶液中c(I-)=1.0×10-4mol·L-1,则a约为_______(保留1位小数,溶液体积变化忽
略不计)。