文档内容
易错题 04 氧化还原反应
1.明兰做实验时不小心沾了一些KMnO ,皮肤上的黑斑很久才能消除,如果用草酸的稀溶液洗涤马上可以
4
复原,其离子方程式为:MnO -+H C O+H+→CO↑+Mn2++____(未配平)。关于此反应的叙述正确的是( )
4 2 2 4 2
A.该反应的氧化产物是Mn2+
B.1 mol MnO -在反应中失去5 mol电子
4
C.该反应右横线上的产物是OH-
D.配平该反应后,H+的计量数是6
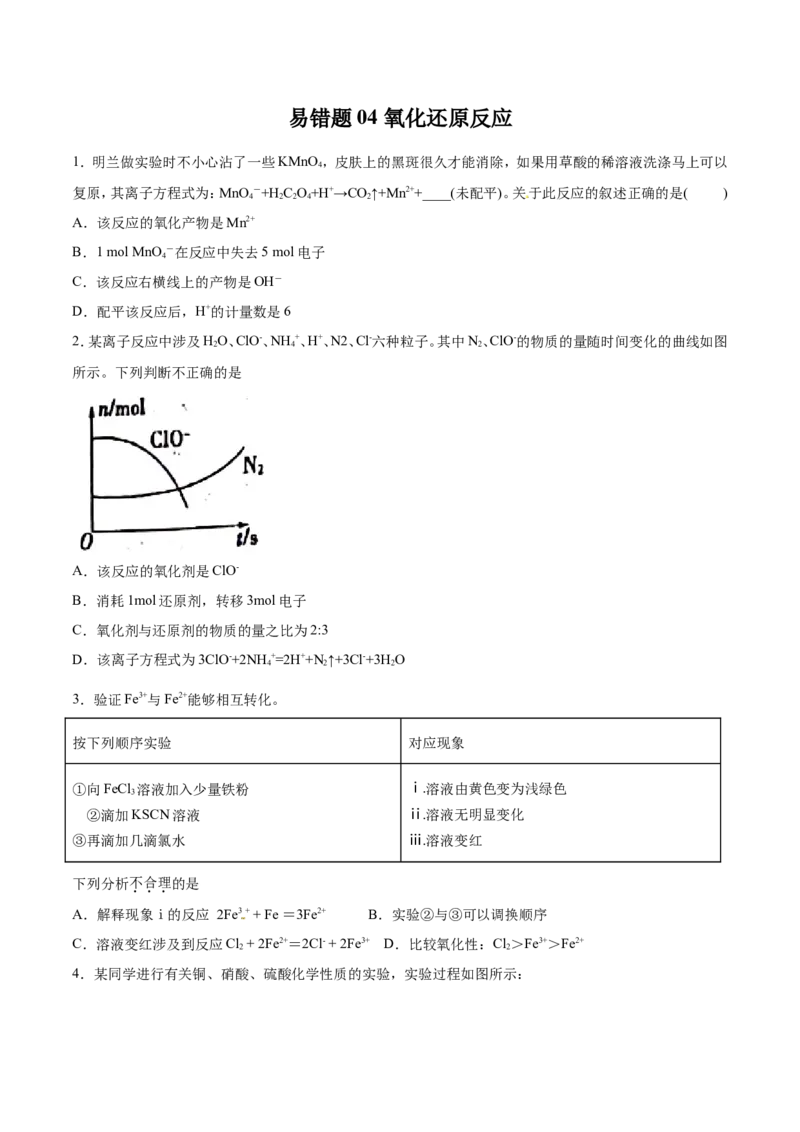
2.某离子反应中涉及HO、ClO-、NH +、H+、N2、Cl-六种粒子。其中N、ClO-的物质的量随时间变化的曲线如图
2 4 2
所示。下列判断不正确的是
[来源:学科网ZXXK]
A.该反应的氧化剂是ClO-
B.消耗1mol还原剂,转移3mol电子
C.氧化剂与还原剂的物质的量之比为2:3
D.该离子方程式为3ClO-+2NH+=2H++N ↑+3Cl-+3H O
4 2 2
3.验证Fe3+与Fe2+能够相互转化。
按下列顺序实验 对应现象
①向FeCl 溶液加入少量铁粉 ⅰ.溶液由黄色变为浅绿色
3
②滴加KSCN溶液 ⅱ.溶液无明显变化
③再滴加几滴氯水 ⅲ.溶液变红
[来源:Z#xx#k.Com]
下列分析不合理的是
[来源:Zxxk.Com]
A.解释现象ⅰ的反应 2Fe3+ + Fe =3Fe2+ B.实验②与③可以调换顺序
C.溶液变红涉及到反应Cl + 2Fe2+=2Cl- + 2Fe3+ D.比较氧化性:Cl>Fe3+>Fe2+
2 2
4.某同学进行有关铜、硝酸、硫酸化学性质的实验,实验过程如图所示:①、③均观察到实验现象:溶液呈蓝色,试管口有红棕色气体产生。下列说法正确的是
A.①试管口有红棕色气体产生,原因是硝酸被还原为NO
2
B.由③的现象可得出结论:Cu可与稀硫酸反应
C.③中反应的离子方程式:3Cu+2NO -+8H+=== 3Cu2++2NO↑+4HO
3 2
D.③中可能产生SO
2
5.氧化性:Fe3+>Cu2+,向物质的量浓度均为2mol· Lˉ1的Fe (SO ) 和CuSO 的500mL混合液中加入a mol 铁
2 4 3 4
粉,充分反应后,下列说法不正确的是
A.当 a≤1时,发生的反应为:2Fe3++Fe=3Fe2+
B.当 a≥2 时,发生的反应为:2Fe3++2Cu2++3Fe=5Fe2++2Cu
C.当 1≤a<2 时,溶液中n(Fe2+ )=(2+ a)mol
D.若有固体剩余,则可能是铜或铁和铜
6.ClO 是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得2KClO+HC O+
2 3 2 2 4
HSO 2ClO ↑+KSO +2CO↑+2HO。据此,下列说法不正确的( )
2 4 2 2 4 2 2
A.KClO 发生还原反应
3
B.HC O 在反应中被氧化
2 2 4
C.HC O 的氧化性强于ClO 的氧化性
2 2 4 2
D.每生成1 mol ClO,转移的电子数约为6.02×1023
2 [来源:Z|xx|k.Com]
7.已知5KCl + KClO +3H SO ==3Cl + 3K SO + 3H O ,下列说法不正确的是 ( )
3 2 4 2 2 4 2
A.HSO 既不是氧化剂又不是还原剂
2 4
B.1mol KClO 参加反应时有5mol电子转移
3
C.KClO 是氧化剂
3
D.被氧化与被还原的氯元素的质量比为1:5
8.C1O 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得C1O:
2 2
2KClO+H C O+H SO 2ClO ↑+K SO +2CO ↑+2H O,下列说法中正确的是
3 2 2 4 2 4 2 2 4 2 2
A.在反应中HC O 既不是氧化剂也不是还原剂
2 2 4 [来源:学科网ZXXK]
B.1 mol KClO 参加反应,在标准状况下能得到22.4 L气体
3
C.1 mol KClO 参加反应有2 mol电子转移
3D.KClO 在反应中是氧化剂
3
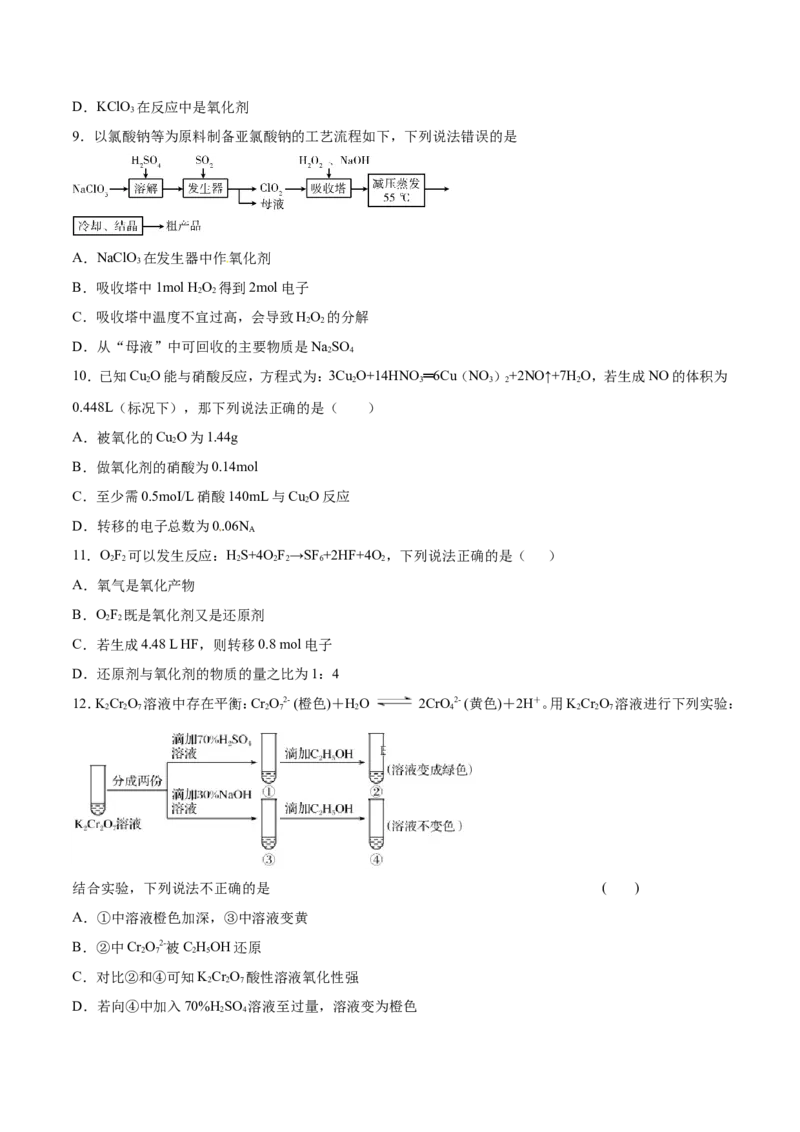
9.以氯酸钠等为原料制备亚氯酸钠的工艺流程如下,下列说法错误的是
A.NaClO 在发生器中作氧化剂
3
B.吸收塔中1mol HO 得到2mol电子
2 2
C.吸收塔中温度不宜过高,会导致HO 的分解
2 2
D.从“母液”中可回收的主要物质是NaSO
2 4
10.已知Cu O能与硝酸反应,方程式为:3Cu O+14HNO ═6Cu(NO )+2NO↑+7HO,若生成NO的体积为
2 2 3 3 2 2
0.448L(标况下),那下列说法正确的是( )
A.被氧化的Cu O为1.44g
2
B.做氧化剂的硝酸为0.14mol
C.至少需0.5moI/L硝酸140mL与Cu O反应
2
D.转移的电子总数为0.06N
A
11.OF 可以发生反应:HS+4OF→SF +2HF+4O,下列说法正确的是( )
2 2 2 2 2 6 2
A.氧气是氧化产物
B.OF 既是氧化剂又是还原剂
2 2
C.若生成4.48 L HF,则转移0.8 mol电子
D.还原剂与氧化剂的物质的量之比为1:4
12.KCr O 溶液中存在平衡:Cr O2- (橙色)+HO 2CrO2- (黄色)+2H+。用KCr O 溶液进行下列实验:
2 2 7 2 7 2 4 2 2 7
结合实验,下列说法不正确的是 ( )
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr O2-被C HOH还原
2 7 2 5
C.对比②和④可知KCr O 酸性溶液氧化性强
2 2 7
D.若向④中加入70%H SO 溶液至过量,溶液变为橙色
2 413.为探讨化学平衡移动原理与氧化还原反应规律的联系,实验如下。
下列说法不正确的是
A.试管i溶液变蓝证明有I 生成
2
B.结合试管i、ii中现象,可知2Fe3++2I- 2Fe2++I
2
C.试管iii中溶液褪色说明I 转化为I-,此时I-还原性强于Fe2+
2
D.对比实验I和试管iii中现象,说明物质的氧化性与还原性强弱受浓度影响
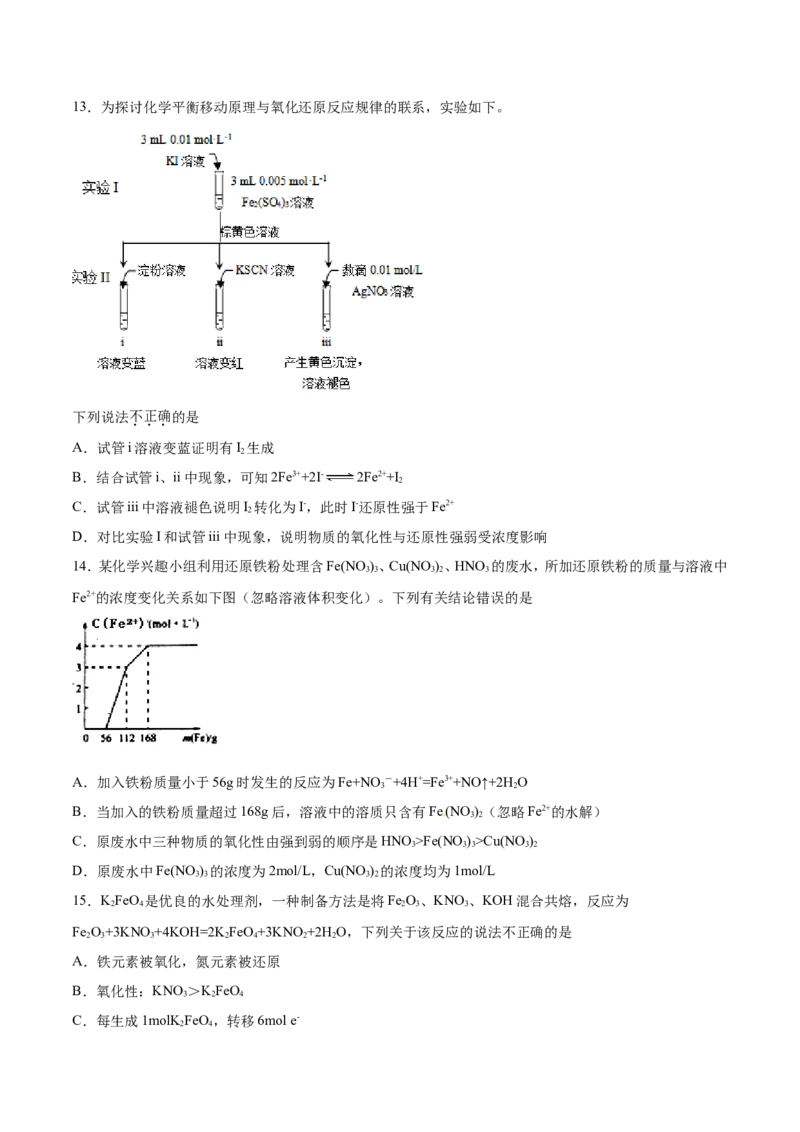
14.某化学兴趣小组利用还原铁粉处理含Fe(NO )、Cu(NO )、HNO 的废水,所加还原铁粉的质量与溶液中
3 3 3 2 3
Fe2+的浓度变化关系如下图(忽略溶液体积变化)。下列有关结论错误的是
A.加入铁粉质量小于56g时发生的反应为Fe+NO-+4H+=Fe3++NO↑+2HO
3 2
B.当加入的铁粉质量超过168g后,溶液中的溶质只含有Fe(NO )(忽略Fe2+的水解)
3 2
C.原废水中三种物质的氧化性由强到弱的顺序是HNO>Fe(NO)>Cu(NO)
3 3 3 3 2
D.原废水中Fe(NO ) 的浓度为2mol/L,Cu(NO ) 的浓度均为1mol/L
3 3 3 2
15.KFeO 是优良的水处理剂,一种制备方法是将Fe O、KNO、KOH混合共熔,反应为
2 4 2 3 3
Fe O+3KNO +4KOH=2K FeO+3KNO +2H O,下列关于该反应的说法不正确的是
2 3 3 2 4 2 2
A.铁元素被氧化,氮元素被还原
B.氧化性:KNO>KFeO
3 2 4
C.每生成1molK FeO,转移6mol e-
2 4D.KFeO 具有氧化杀菌作用
2 4
16.叠氮酸钠(NaN )是汽车安全气囊的产气剂,Fe O 是主氧化剂,NaHCO 作冷却剂。当汽车发生剧烈碰撞时,
3 2 3 3
分解产生大量气体使安全气囊迅速打开,从而起到安全保护作用[已知K(HN )=1.8×10-5]。下列有关说法正
a 3
确的是
A.NaHCO 的冷却原理是它发生分解,消耗体系的热量
3
B.Fe O 和Na反应的氧化产物是NaO
2 3 2 2
C.等物质的量的NaN 和HN 混合溶液显碱性
3 3
D.若有6.5 gNaN 分解产生N,则转移0.9 mol电子
3 2
17.有一瓶NaSO 溶液,由于它可能部分被氧化,某同学进行如下实验:取少量溶液,滴入Ba(NO ) 溶液,产
2 3 3 2
生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。对此实验下述结论正确的是
A.加硝酸后的不溶性沉淀一定是BaSO
4
B.NaSO 已部分被空气中的氧气氧化
2 3
C.加入Ba(NO ) 溶液后,生成的沉淀中一定含有BaSO
3 2 4
D.此实验能确定NaSO 是否被部分氧化
2 3
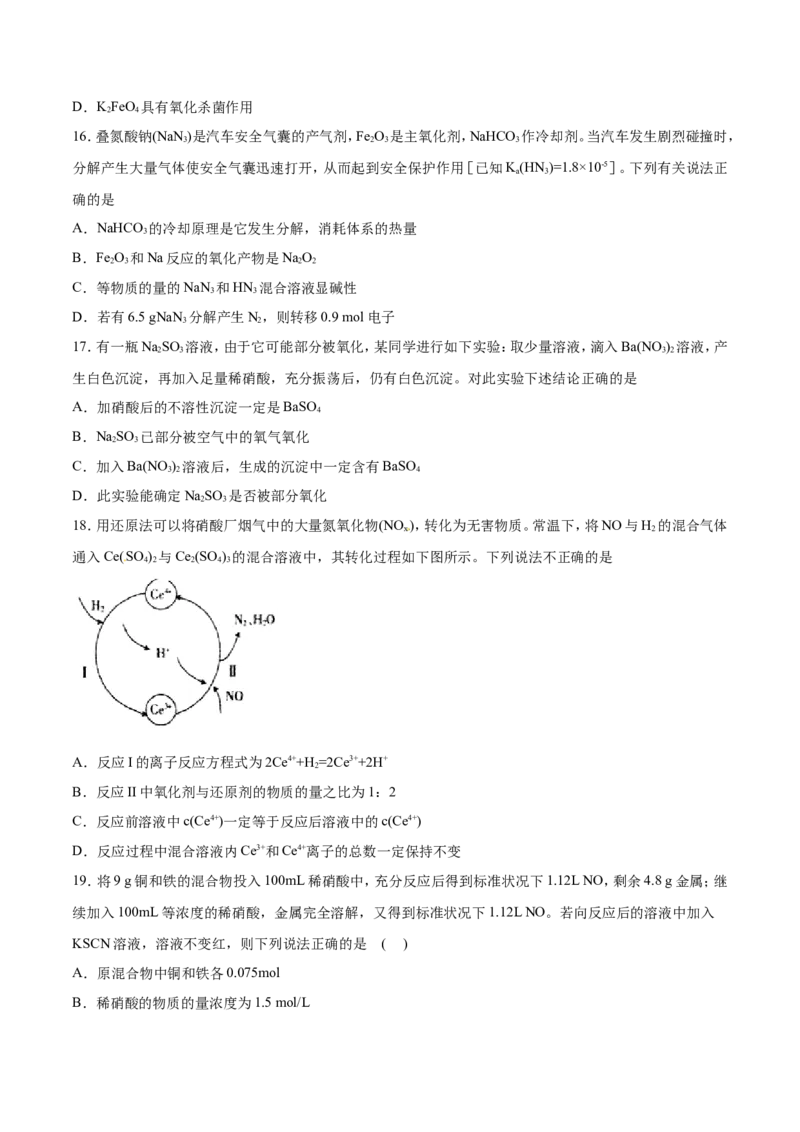
18.用还原法可以将硝酸厂烟气中的大量氮氧化物(NO ),转化为无害物质。常温下,将NO与H 的混合气体
x 2
通入Ce(SO ) 与Ce (SO ) 的混合溶液中,其转化过程如下图所示。下列说法不正确的是
4 2 2 4 3
A.反应I的离子反应方程式为2Ce4++H =2Ce3++2H+
2
B.反应II中氧化剂与还原剂的物质的量之比为1:2
C.反应前溶液中c(Ce4+)一定等于反应后溶液中的c(Ce4+)
D.反应过程中混合溶液内Ce3+和Ce4+离子的总数一定保持不变
19.将9 g铜和铁的混合物投入100mL稀硝酸中,充分反应后得到标准状况下1.12L NO,剩余4.8 g金属;继
续加入100mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下1.12L NO。若向反应后的溶液中加入
KSCN溶液,溶液不变红,则下列说法正确的是 ( )
A.原混合物中铜和铁各0.075mol
B.稀硝酸的物质的量浓度为1.5 mol/LC.第一次剩余的4.8g金属为铜和铁
D.向反应后的溶液中再加入该稀硝酸100mL,又得到NO在标准状况下的体积为1.12L
20.根据下表中的信息判断,下列说法错误的是
A.第①组反应的氧化产物为O
2
B.第②组反应中C1 与FeBr 的物质的量之比小于或等于1:2
2 2
C.第③组反应中生成3mol C1 ,转移6mol电子
2
D.氧化性由强到弱的顺序为C1O- >C1 >Fe3+
3 2
21.锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量为世界第一,从硫化物中提取单质锑一般是
先在高温下将硫化物转化为氧化物,再用碳还原:
①2Sb S+3O +6Fe Sb O+6FeS②Sb O+6C 4Sb+6CO↑,关于反应①、②的说法正确的是( )
2 3 2 4 6 4 6
A.反应①②中的氧化剂分别是Sb S、Sb O
2 3 4 6
B.反应①中每生成3mol FeS时,共转移6mol电子
C.反应②说明C的还原性比Sb弱
D.每生成4mol Sb时,反应①与反应②中还原剂的物质的量之比为4:3
22.著名化学家徐光宪获得“国家最高科学技术奖”,以表彰他在稀土萃取理论方面作出的贡献。稀土铈
(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化
合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法不正确的是
A.铈(Ce)元素在自然界中主要以化合态形式存在
B.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI +2H ↑
4 2
C.用Ce(SO) 溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+
4 2
D.四种稳定的核素136Ce、138Ce、140Ce、142Ce,它们互称为同位素
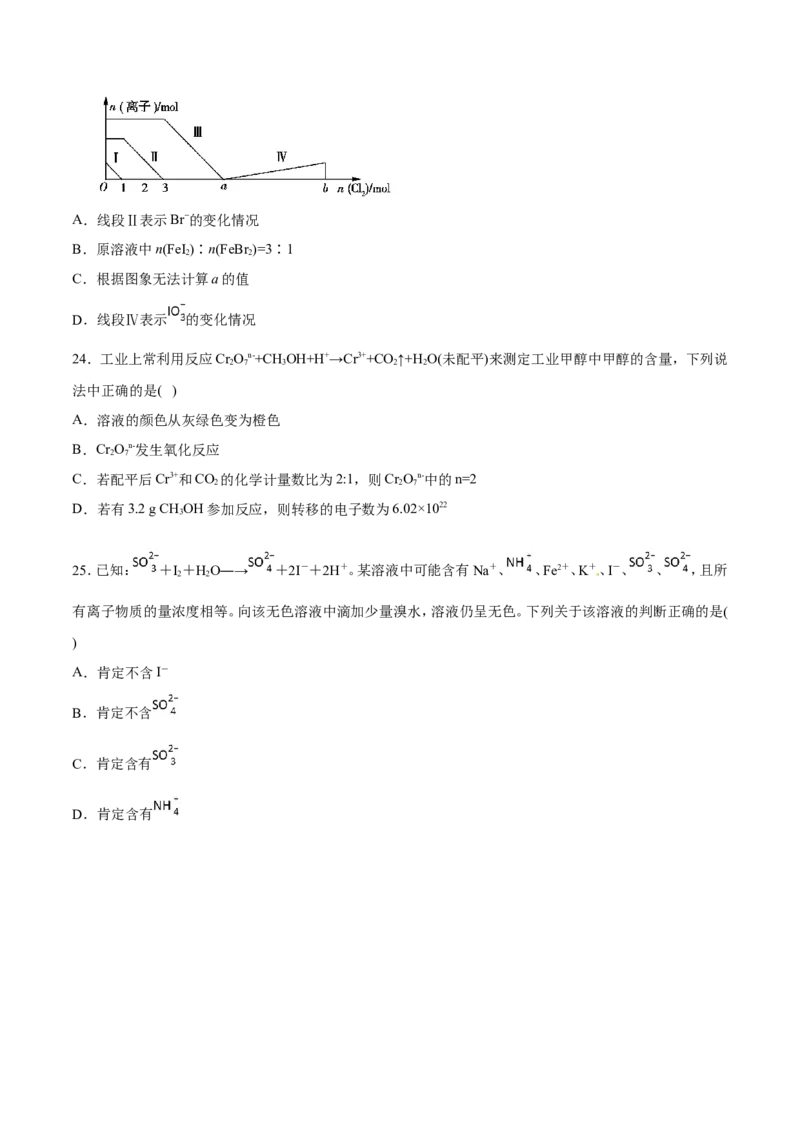
23.向含Fe2+、I−、Br−的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b−a=5,线段
Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法正确的是A.线段Ⅱ表示Br−的变化情况
B.原溶液中n(FeI )∶n(FeBr)=3∶1
2 2
C.根据图象无法计算a的值
D.线段Ⅳ表示 的变化情况
24.工业上常利用反应Cr On-+CH OH+H+→Cr3++CO ↑+H O(未配平)来测定工业甲醇中甲醇的含量,下列说
2 7 3 2 2
法中正确的是( )
A.溶液的颜色从灰绿色变为橙色
B.Cr On-发生氧化反应
2 7
C.若配平后Cr3+和CO 的化学计量数比为2:1,则Cr On-中的n=2
2 2 7
D.若有3.2 g CH OH参加反应,则转移的电子数为6.02×1022
3
25.已知: +I+HO―→ +2I-+2H+。某溶液中可能含有Na+、 、Fe2+、K+、I-、 、 ,且所
2 2
有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是(
)
A.肯定不含I-
B.肯定不含
C.肯定含有
D.肯定含有