文档内容
专题 04 氧化还原反应
一、选择题(每小题只有一个选项符合题意)
1.(2022·北京四中高三期中)下列装置工作原理与氧化还原反应无关的是( )
A.臭氧消毒柜 B.甲烷燃料电池 C.太阳能集热器 D.燃气灶
2.(2022·山东省菏泽一中高三期中考试)下列化学变化过程中,有气体被还原的是( )
A.用酒精检测仪(内有酸性KCr O)测出某司机酒驾
2 2 7
B.在潜水中用NaO 作供氧剂
2 2
C.用氨水吸收硫酸工业的尾气
D.海水提溴过程中将溴蒸气吹入存在吸收剂SO 的吸收塔中
2
3.(2022·浙江省缙云中学等三校高三联考)已知反应:O + 2I− + H O=O + I + 2OH−,下列说法不正确的
3 2 2 2
是( )
A.I 为氧化产物 B.氧化性:O >I
2 3 2
C.HO既不是氧化剂也不是还原剂 D.反应生成1molO 时转移4mol电子
2 2
6.(2022·辽宁省六校高三期中联考)关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是( )
2 3 6 2 2
A.KHIO 中I元素的化合价为+7价 B.HI在反应中只表现还原性
2 3 6
C.常温下,生成25.4g I 时,转移0.2mol电子 D.氧化产物与还原产物的物质的量之比为1:7
2
4.(2023·浙江省十校联盟高三10月月考)下列关于反应MnO -+Cu S+H+→Mn2++Cu2++SO↑+H O (未配平)的
4 2 2 2
说法中正确的是( )
A.氧化产物仅是SO B.还原性的强弱关系是:Mn2+>Cu S
2 2
C.氧化剂与还原剂的物质的量之比为5∶8 D.生成 (标况下) SO,转移电子的物质的量是
2
5.(2023·浙江省嘉兴市高三上学期检测)制硫酸过程中有以下反应发生:FeS+11O 2Fe O+8SO,下
2 2 2 3 2
列说法正确的是( )
A.FeS 既是氧化剂又是还原剂 B.还原剂与氧化剂的物质的量之比为4:11
2
C.SO 只是氧化产物 D.每消耗1.1mol氧气,反应中转移2.2mol电子
26.(2023·安徽省阜阳江准十校高三第二次联考)等物质的量的NaO 与FeSO 溶液混合,反应过程中有沉
2 2 4
淀和气体生成,恰好完全反应时,生成气体22.4L(换算成标准状况),对该反应分析正确的是( )
A.氧化剂是NaO,还原剂是FeSO B.反应过程中转移电子4mol
2 2 4
C.被FeSO 还原的NaO 为2mol D.反应后溶液的pH减小
4 2 2
7.(2022·吉林省东北师大附中一模)KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的
3
第一步反应为 。下列说法错误的是( )
A.反应中氧化剂和还原剂的物质的量之比为11:6 B.产生22.4LCl 时,反应中转移
2
C.可用石灰乳吸收反应产生的Cl 制备漂白粉 D.可用酸化的淀粉碘化钾溶液检验食盐中IO -的存
2 3
在
8.(2022·吉林省东北师大附中一模)(NH )SO 具有强氧化性,在酸性溶液中,可将Mn2+氧化为MnO-,
4 2 2 8 4
但一般情况下,该反应进行的非常缓慢,而加入几滴AgNO 溶液后,混合液迅速变为紫红色。下列说法错误
3
的是( )
A.AgNO 为该反应的催化剂 B.SO 2-为还原产物
3 4
C.SO2-中存在一个过氧键 D.反应中氧化剂与还原剂物质的量之比为2∶5
2 8
9.(2022·浙江省9+1高中联盟高三期中联考)超氧化钾(KO )在加热条件下可以将CuO氧化成Cu(Ⅲ)的化
2
合物,化学方程式如下:2CuO+2KO O↑+2KCuO,则下列说法不正确的是( )
2 2 2
A.该反应中化合价升高的元素是Cu和O
B.KCuO 既是氧化产物,又是还原产物
2
C.当反应中转移的电子数为0.3N 时,则有0.2molCuO被氧化
A
D.标准状况下,生成6.72LO 时,被还原的超氧化钾(KO )为0.6mol
2 2
10.(2022·江西省七校高三第一次联考)工业上用硫酸铁溶液溶解黄铜矿精矿工艺中,发生主要反应的离子
方程式为:CuFeS+4Fe3+=Cu2++5Fe2++2S。下列关于该反应说法正确的是( )
2
A.CuFeS 中Cu为+1价,Fe为+3价 B.反应中硫元素被氧化,所有铁元素均被还原
2
C.反应中氧化产物与还原产物物质的量之比为2:5 D.当转移1 mol e-时,有46 g CuFeS 参加反应
2
11.(2022·浙江省S9联盟期中联考)食盐中的碘以碘酸钾(KIO )形式存在,可根据反应:IO -+5I-
3 3
+6H+=3I +3H O验证食盐中存在IO -。根据上述反应,下列说法错误的是( )
2 2 3
A.IO -作氧化剂,发生还原反应 B.I 既是氧化产物又是还原产物
3 2
C.该条件下氧化性:IO ->I D.被氧化的I原子和被还原的I原子个数比1:5
3 2
12.(2022·浙江省绿谷高中联盟期中联考)已知:①2KMnO +16HCl=2KCl+2MnCl +5Cl↑+8H O;
4 2 2 2②Cl+2FeCl =2FeCl ;③2KI+2FeCl =2KCl+I +2FeCl 。则下列判断正确的是( )
2 2 3 3 2 2
A.氧化性:MnO ->Fe3+>Cl B.还原性:Cl->I->Fe2+
4 2
C.Fe3+只有氧化性,Fe2+只有还原性 D.由信息推测:Cl+2I-=2Cl-+I 反应可以进行
2 2
13.(2022·浙江省诸暨市教育研究中心高三选考诊断性考试)已知反应
10AgF+5Cl +5H O=9AgCl+AgClO +10HF+O,下列说法正确的是( )
2 2 3 2
A.AgCl是氧化产物 B.AgF是氧化剂
C.有1molO 生成时反应所转移的电子总数为9mol D.被氧化的氯与被还原的氯物质的量之比为9∶1
2
14.(2022·浙江省嘉兴市选考模拟预测)误服白磷(P ),应立即用2%硫酸铜溶液洗胃,其反应是
4
11P+60CuSO+96H O=20Cu P↓+24HPO +60 H SO ,下列说法正确的是( )
4 4 2 3 3 4 2 4
A.白磷(P )只发生了氧化反应 B.HSO 是还原产物
4 2 4
C.氧化产物和还原产物的物质的量之比为5:6 D.1mol CuSO 能氧化0.05mol P
4 4
10.(2023·浙江省普通高校招生高三选考模拟)关于反应5NaClO+ xHCl=yClO +5NaClO +zHO,下列说法
2 2 2 2
不正确的是( )
A.x =4,y=4 B.该化学反应中HCl仅体现出了酸性
C.通过该反应可知氧化性:ClO >NaClO D.该反应生成1mol水,转移2N 个电子
2 2 A
15.(2022·浙江省金华十校高三选考模拟)关于反应Ⅰ:6NaOH+3S=2Na S+ Na SO +3H O和反应Ⅱ:
2 2 3 2
S+6HNO (浓)=H SO +6NO+2H O,下列说法正确的是( )
3 2 4 2 2
A.NaS和NO 均为还原产物 B.反应Ⅰ中还原剂与氧化剂的物质的量之比为2:1
2 2
C.两反应中S都只发生了氧化反应 D.两反应中消耗64gS时,转移电子数目相同
16.(2022·湘豫名校高三联考)2021年6月搭载神舟十二号载人飞船的长征二号F遥十二火箭在酒泉卫星
发射中心发射成功。火箭用NH 作燃料,发生反应:NH+NO→N+H O (未配平)。下列说法正确的是( )
2 4 2 4 2 2 2
A.2mol NH 燃料参与反应,生成3mol氧化产物
2 4
B.标准状况下22.4LNO 的质量为46g
2
C.1mol NH 有5mol极性共价键
2 4
D.NO 可用于工业上制硝酸,1molNO 最多可以得到1mol硝酸
2 2
17.(2023·浙江省强基联盟高三上学期10月统测)科学家发现金星大气中存在PH ,据此推断金星大气层
3
或许存在生命。利用P 与足量的浓KOH溶液反应可制备PH :P+3KOH(浓)+3H O 3KH PO + PH ↑;下列说
4 3 4 2 2 2 3
法正确的是( )
A. PH 的电子式为 B.1mol P 参与反应,转移3mol电子
3 4
C.KH PO 是酸式盐 D.氧化剂与还原剂的物质的量之比为1∶1
2 218.(2023·浙江省Z20名校新高考研究联盟高三第一次联考)工业制硅第二步反应为SiHCl +H
3 2
Si+3HCl,下列说法不正确的是( )
A.SiHCl 中的Si呈+4价,分子空间结构为四面体形
3
B.该反应中SiHCl 既是氧化剂又是还原剂
3
C.该反应说明在该温度下氢气的还原性强于硅单质
D.当1 mol H 完全反应时,该反应转移2 mol电子
2
19.(2023·浙江省浙里卷天下高三上学期10月联考)高铁酸钠(Na FeO)是一种绿色消毒剂,可用于饮用水
2 4
处理。制备高铁酸钠的离子方程式为3ClO-+2Fe3++10OH-=2FeO 2-+3Cl-+5H O,则下列说法不正确的是( )
4 2
A.在反应中Fe3+被还原,发生氧化反应
B.氧化剂与还原剂的物质的量之比为3:2
C.上述反应生成1mol高铁酸根离子,转移3mol电子
D.高铁酸根离子具有强氧化性,溶于水能生成氢氧化铁胶体和氧气
20.(2023·浙江省浙南名校联盟高三上学期第一次联考)三氟化溴有强氧化性和强反应活性,是一种良好的
非水溶剂,遇水立即发生如下反应:3BrF+5H O=HBrO +Br +9HF+O↑,下列有关该反应的说法不正确的是(
3 2 3 2 2
)
A.当0.5molHO被氧化时,生成0.1mol氧气
2
B.氧化剂与还原剂的物质的量之比为2∶3
C.当转移电子6mol时,生成的还原产物为1mol
D.当生成2.7molHF时,被BrF 还原的BrF 为0.2mol
3 3
21.(2023届•浙江省舟山市普陀中学高三返校考试)工业废水中含有重铬酸根离子(CrO2-)有毒,必须处理
2 7
达标后才能排放。工业上常用绿矾(FeSO ·7H O)做处理剂,反应的离子方程式为:6Fe2++Cr O2-+14H O=6Fe3+
4 2 2 7 2
+2Cr3++7H O,下列说法不正确的是( )
2
A.将绿矾水溶液久置于空气中,滴加几滴KSCN溶液,溶液出现血红色
B.配制好的FeSO 溶液,为防止变质可向溶液中加入少量铁粉
4
C.每处理1mol Cr O2-转移 电子
2 7
D.向FeSO 溶液中加入NaOH溶液一段时间后,沉淀会变成红褐色
4
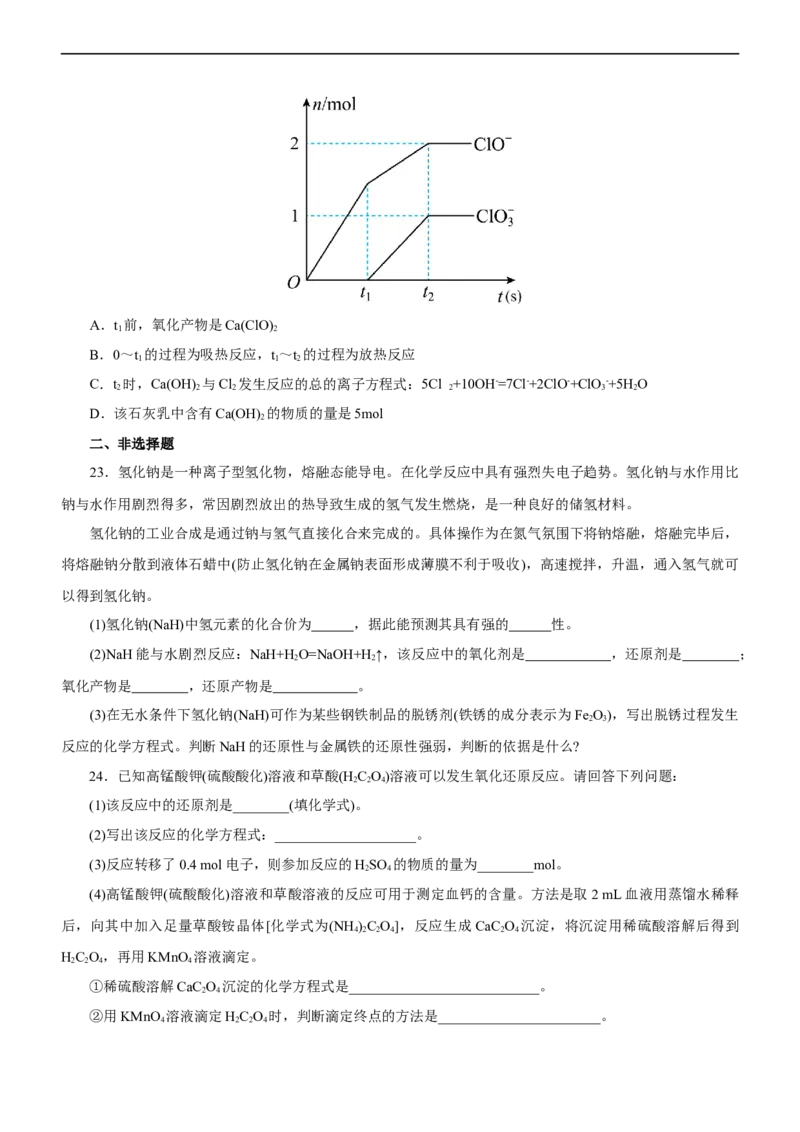
22.(2023·天津市部分区高三期中)已知Ca(OH) 与Cl 反应的氧化产物与温度有关,在一定量的石灰乳中
2 2
通入一定量的氯气,二者恰好完全反应。生成物中含有C l-、ClO-和ClO -三种含氯元素的离子,其中ClO-和
3
ClO - 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。下列说法不正确的是( )
3A.t 前,氧化产物是Ca(ClO)
1 2
B.0~t 的过程为吸热反应,t~t 的过程为放热反应
1 1 2
C.t 时,Ca(OH) 与Cl 发生反应的总的离子方程式:5Cl +10OH-=7Cl-+2ClO-+ClO -+5H O
2 2 2 2 3 2
D.该石灰乳中含有Ca(OH) 的物质的量是5mol
2
二、非选择题
23.氢化钠是一种离子型氢化物,熔融态能导电。在化学反应中具有强烈失电子趋势。氢化钠与水作用比
钠与水作用剧烈得多,常因剧烈放出的热导致生成的氢气发生燃烧,是一种良好的储氢材料。
氢化钠的工业合成是通过钠与氢气直接化合来完成的。具体操作为在氮气氛围下将钠熔融,熔融完毕后,
将熔融钠分散到液体石蜡中(防止氢化钠在金属钠表面形成薄膜不利于吸收),高速搅拌,升温,通入氢气就可
以得到氢化钠。
(1)氢化钠(NaH)中氢元素的化合价为 ,据此能预测其具有强的 性。
(2)NaH能与水剧烈反应:NaH+H O=NaOH+H ↑,该反应中的氧化剂是 ,还原剂是 ;
2 2
氧化产物是 ,还原产物是 。
(3)在无水条件下氢化钠(NaH)可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe O),写出脱锈过程发生
2 3
反应的化学方程式。判断NaH的还原性与金属铁的还原性强弱,判断的依据是什么?
24.已知高锰酸钾(硫酸酸化)溶液和草酸(H C O)溶液可以发生氧化还原反应。请回答下列问题:
2 2 4
(1)该反应中的还原剂是________(填化学式)。
(2)写出该反应的化学方程式:____________________。
(3)反应转移了0.4 mol电子,则参加反应的HSO 的物质的量为________mol。
2 4
(4)高锰酸钾(硫酸酸化)溶液和草酸溶液的反应可用于测定血钙的含量。方法是取2 mL血液用蒸馏水稀释
后,向其中加入足量草酸铵晶体[化学式为(NH )C O],反应生成CaC O 沉淀,将沉淀用稀硫酸溶解后得到
4 2 2 4 2 4
HC O,再用KMnO 溶液滴定。
2 2 4 4
①稀硫酸溶解CaC O 沉淀的化学方程式是___________________________。
2 4
②用KMnO 溶液滴定HC O 时,判断滴定终点的方法是_______________________。
4 2 2 4③若消耗了1.0×10-4 mol·L-1的KMnO 溶液20.00 mL,则100 mL该血液中含钙________ g。
4
25.(2022·浙江省绿谷高中联盟高一期中联考)Ⅰ.我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和
木炭粉按一定比例混合而成,爆炸时发生的反应为:S+2KNO +3C=K S+N↑+3X↑请回答:
3 2 2
(1)X的化学式是_______,按照物质的组成和性质分类,属于______ (填字母)。
A.单质 B.酸性氧化物 C.化合物 D.盐
(2)在上述反应中,氧化剂是(填化学式)_______________。
(3)写出在NaOH溶液中通入过量的X气体发生反应的化学方程式____________。
(4)高铁酸钠(Na FeO)是一种新型绿色消毒剂,主要用于饮用水处理。工业制备高铁酸钠有多种方法。其
2 4
中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2FeO 2-+3Cl-+5H O。用单线桥标出上述方
4 2
程式的电子转移方向和数目___________________________。
26.(2023·辽宁省六校高三期中联考)化学反应原理在日常的生产生活中都有广泛的应用,按要求回答下列
问题:
(1)次磷酸(H PO )为一元中强酸,是一种精细磷化工产品,具有较强的还原性。化工生产中用次磷酸钠
3 2
(NaH PO )进行化学镀铜,具有体系稳定性好、无毒性等优点,反应原理为2NaH PO + NaOH+
2 2 2 2
CuSO =2NaHPO + Na SO + Cu+H ↑。
4 2 3 2 4 2
①NaH PO 在物质类别中属于____________(填“正盐”或“酸式盐”)。
2 2
②上述化学反应中每生成H 5.6L(标准状况),则转移电子数为___________。
2
(2) Na SO 是化工生产中的强氧化剂,SO2-的结构式为 ,其中S元素的化合价为
2 2 8 2 8
___________。在Ag+催化下,SO2-能使含Mn2+的溶液变成紫红色,氧化产物是___________(填离子符号)。
2 8
(3)化学工艺处理废水中也发挥了重要作用
①用KFeO 处理中性废水时与水反应生成氢氧化铁胶体,并放出无色无味的气体和其它物质,写出反应
2 4
的离子反应方程式________,处理废水时既利用KFeO 强氧化性,又利用生成氢氧化铁胶体的___________作
2 4
用。
②NaS也是一种重要的水处理剂用于除去水体中的汞盐,写出对应的离子反应方程________。
2
27.(2023·江苏省无锡市高三教学质量调研测试)聚合硫酸铁 是一种应用广泛
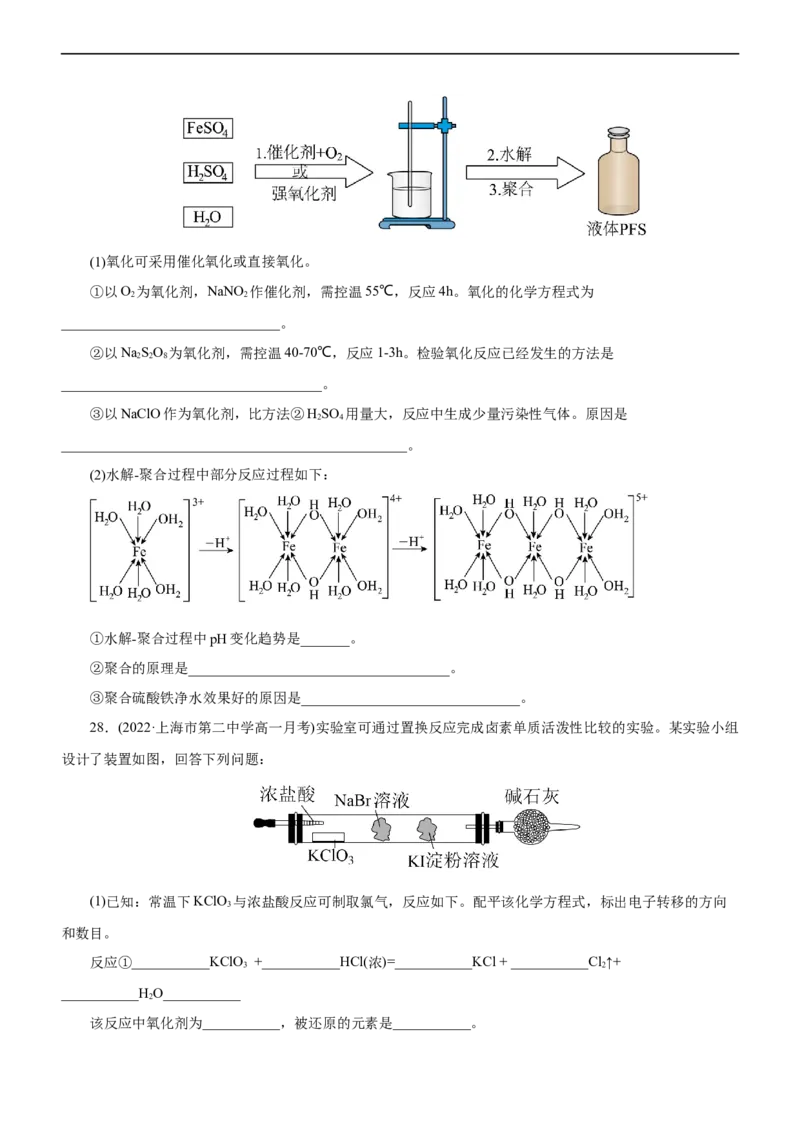
的水处理剂。制备方法如下:(1)氧化可采用催化氧化或直接氧化。
①以O 为氧化剂,NaNO 作催化剂,需控温55℃,反应4h。氧化的化学方程式为
2 2
_______________________________。
②以NaSO 为氧化剂,需控温40-70℃,反应1-3h。检验氧化反应已经发生的方法是
2 2 8
_____________________________________。
③以NaClO作为氧化剂,比方法②HSO 用量大,反应中生成少量污染性气体。原因是
2 4
_________________________________________________。
(2)水解-聚合过程中部分反应过程如下:
①水解-聚合过程中pH变化趋势是_______。
②聚合的原理是_____________________________________。
③聚合硫酸铁净水效果好的原因是_______________________________。
28.(2022·上海市第二中学高一月考)实验室可通过置换反应完成卤素单质活泼性比较的实验。某实验小组
设计了装置如图,回答下列问题:
(1)已知:常温下KClO 与浓盐酸反应可制取氯气,反应如下。配平该化学方程式,标出电子转移的方向
3
和数目。
反应①___________KClO +___________HCl(浓)=___________KCl + ___________Cl ↑+
3 2
___________HO___________
2
该反应中氧化剂为___________,被还原的元素是___________。(2)该装置中,吸有KI淀粉溶液的棉球颜色变为___________。吸有NaBr溶液的棉球中发生反应的离子方
程式为___________。
(3)由反应现象能否得出活泼性Br >I 的结论?回答并说明理由___________。
2 2
(4)实验室还可通过以下反应制取氯气:
反应② 2KMnO +16HCl=2KCl + 2MnCl +5Cl ↑+ 8H O;
4 2 2 2
反应③ MnO +4HCl(浓) MnCl +Cl ↑+ 2H O;
2 2 2 2
若要制得相同质量的氯气,反应②和③中电子转移的数目之比为___________。
(5)通过反应①~③,比较反应中氧化剂的氧化性强弱___________,(用“>”、“<”或“=”连接)说明判
断依据:___________。
(6)通过反应①~③,可以知道HCl的还原性强弱与___________、___________等因素有关。
29.柠檬酸亚铁(FeC HO)是一种易吸收的高效铁制剂,可由绿矾(FeSO ·7H O)通过下列反应制备:FeSO
6 6 7 4 2 4
+NaCO===FeCO ↓+NaSO 、FeCO+C HO===FeC HO+CO↑+HO。某实验小组用下列方法测定产品中
2 3 3 2 4 3 6 8 7 6 6 7 2 2
柠檬酸亚铁晶体的质量分数:取 25.00 g柠檬酸亚铁晶体(摩尔质量为246 g·mol-1),配成100 mL溶液,取
20.00 mL至锥形瓶中,另取0.200 0 mol·L-1的酸性KMnO 标准溶液装入酸式滴定管中,用氧化还原法测定柠
4
檬酸亚铁晶体的质量分数,杂质不与酸性KMnO 标准溶液反应,经4次滴定,每次消耗KMnO 溶液的体积如
4 4
下:
实验序号 1 2 3 4
消耗KMnO 溶液体积 20.00 mL 19.98 mL 21.38 mL 20.02 mL
4
滴定终点时现象为:________________________,柠檬酸亚铁的质量分数为________。