文档内容
专题 06 水溶液中的离子平衡
内容 弱电解质的电离平衡、水的电离、溶液的酸碱性、盐类水解、沉淀溶解平衡
1.理解弱电解质在水中的电离平衡 6.掌握中和滴定实验的基本操作
课
2.了解强电解质和弱电解质的概念 7.了解中和滴定实验主要仪器的使用方法
标
3.理解电解质在水中的电离以及电解 8.盐类水解及其应用
解 解读 质溶液的导电性
9. 离子浓度大小比较
读 4.了解水的电离、离子积常数
10.沉淀溶解平衡
5.了解溶液 pH 的含义及其测定方
法,能进行pH的简单计算 11.溶度积常数及其应用
该专题内容是近几年的必考内容。主要考查影响弱电解质电离平衡的因素,通过图
像判断强、弱电解质,计算电离常数,比较微粒浓度大小,进行pH的相关计算和中
考情分析
和滴定的迁移应用等,命题时与水解相结合又增加了试题难度,预计在今后的高考
中出现的概率仍较大。
备考时应重点关注数形结合与分析推理型选择题、滴定终点判断的规范表达,同时
备考策略 要了解水溶液中的离子反应与平衡在物质检测、化学反应规律研究、沉淀溶解平衡
及其转化等。
核心素养 变化观念与平衡思想 证据推理与模型认知
高频考点一 弱电解质电离以及溶液的酸碱性
1.溶液中水电离出的c(H+)H O或c(OH-)H O计算
2 2
(1)酸或碱溶液:c(H+)H O=c(OH-)H O=c(OH-)或c(H+)。
2 2
(2)水解呈酸性或碱性的盐溶液:c(H+)H O=c(OH-)H O=c(H+)或c(OH-)。
2 2
2.酸碱混合液性质的两种判断
(1)同浓度同体积的HA与BOH混合,溶液的性质决定谁强显谁性。
(2)25 ℃,pH之和为14的HA与BOH等体积混合,溶液的性质决定于谁弱谁过量显谁性。
3.溶液pH的计算
(1)单一溶液的pH计算
强酸溶液:如HA,设浓度为c mol·L-1,c(H+)=nc mol·L-1,pH=-lg c(H+)=-lg(nc)。
n
强碱溶液(25 ℃):如B(OH) ,设浓度为c mol·L-1,c(H+)= mol·L-1,pH=-lg c(H+)=14+lg(nc)。
n
(2)混合溶液pH的计算类型①两种强酸混合:先求出c (H+),再根据c (H+)求pH。
混 混
c (H+)=。
混
②两种强碱混合:先求出c (OH-),再根据K 求出c (H+),最后求pH。
混 w 混
c (OH-)=。
混
③强酸、强碱混合:先判断哪种物质过量,再由下式求出溶液中H+或OH-的浓度,最后求pH。
c (H+)或c (OH-)=。
混 混
(3)酸、碱溶液稀释时pH的变化
酸(pH=a) 碱(pH=b)
弱酸 强酸 弱碱 强碱
稀释10n倍 <a+n a+n >b-n b-n
无限稀释 pH趋向于7
4.外界条件对弱电解质电离平衡的影响
(1)浓度:在一定温度下,同一弱电解质溶液,浓度越小,越易电离。
(2)温度:温度越高,电离程度越大。
(3)同离子效应:加入与弱电解质具有相同离子的电解质时,可使电离平衡向结合成弱电解质分子的方向
移动。
如:以0.1 mol·L-1 CHCOOH溶液为例,填写外界条件对CHCOOHCH COO-+H+ ΔH>0的影响。
3 3 3
移动 电离
改变条件 n(H+) c(H+) c(CHCOO-)
3
方向 程度
加水稀释 正向 增大 减小 减小 增大
加冰醋酸 正向 增大 增大 增大 减小
通入HCl(g) 逆向 增大 增大 减小 减小
加醋酸钠固体 逆向 减小 减小 增大 减小
升高温度 正向 增大 增大 增大 增大
例1.(2022·浙江卷)已知25℃时二元酸HA的K =1.3×10-7,K =7.1×10-15。下列说法正确的是
2 a1 a2
A.在等浓度的NaA、NaHA溶液中,水的电离程度前者小于后者
2
B.向0.1mol·L-1的HA溶液中通入HCl气体(忽略溶液体积的变化)至pH=3,则HA的电离度为0.013%
2 2
C.向HA溶液中加入NaOH溶液至pH=11,则c(A2-)>c(HA-)
2
D.取pH=a的HA溶液10mL,加蒸馏水稀释至100mL,则该溶液pH=a+1
2
【变式探究】(2022·浙江卷)25℃时,苯酚 的 ,下列说法正确的是
A.相同温度下,等 的 和 溶液中,B.将浓度均为 的 和 溶液加热,两种溶液的 均变大
C. 时, 溶液与 溶液混合,测得 ,则此时溶液中
D. 时, 的 溶液中加少量 固体,水的电离程度变小
高频考点二 水溶液中的三大平衡
1.电离平衡与水解平衡的比较
电离平衡(如CHCOOH溶液) 水解平衡(如CHCOONa溶液)
3 3
实质 弱电解质的电离 盐促进水的电离
升高温度 促进电离,离子浓度增大,K 增大 促进水解,水解常数K 增大
a h
促进水解,离子浓度(除H+外)减小,水解
加水稀释 促进电离,离子浓度(除OH-外)减小,K 不变
a 常数K 不变
h
加入相 加入CHCOOH或NaOH,抑制水解,水
加入CHCOONa固体或盐酸,抑制电离,K 不变 3
应离子 3 a 解常数K h 不变
加入反
加入NaOH,促进电离,K 不变 加入盐酸,促进水解,水解常数K 不变
a h
应离子
2.沉淀溶解平衡的影响
(1)升高温度,沉淀、溶解平衡大部分右移,少部分左移。
(2)加少量水,溶解平衡右移,但离子浓度一般不变。
(3)加沉淀本身,溶解平衡不移动。
(4)加同离子可溶物,抑制溶解,溶解度减小,但K 不变。
sp
(5)加反应离子,促进溶解,溶解度增大,但K 不变。
sp
3.沉淀、溶解平衡的三种应用
(1)沉淀生成:除去CuCl 溶液中的FeCl ,可调节pH=3~4,使Fe3+转化为Fe(OH) 沉淀而除去。
2 3 3
(2)沉淀溶解:向浓的NH Cl溶液中加入Mg(OH) ,现象为Mg(OH) 逐渐溶解,其反应方程式为2NH Cl+
4 2 2 4
Mg(OH) ===MgCl +2NH ·H O。
2 2 3 2
(3)沉淀转化:向MgCl 溶液中加入少量NaOH溶液,然后再加入FeCl 溶液,现象为先生成白色沉淀,然
2 3
后又转化为红褐色沉淀。有关离子方程式为Mg2++2OH-===Mg(OH) ↓,3Mg(OH) (s)+2Fe3+
2 2
2Fe(OH) (s)+3Mg2+。
3
4.水溶液中的三大平衡常数(1)明确各种平衡常数表达式。
(2)平衡常数都只与温度有关,温度不变,平衡常数不变。升高温度,K、K 、K 、K 均增大。
a b W h
(3)K、K 、K 三者的关系式为K =;K 、K 、K 三者的关系式为K =。
a h W h b h W h
(4)对二元酸的K 、K 与相应酸根离子的K 、K 的关系式为K ·K =K ,K ·K =K 。
a1 a2 h1 h2 a1 h2 W a2 h1 W
(5)反应CdS(s)+2H+(aq) Cd2+(aq)+HS(aq)的平衡常数K,则K=。
2
(6)反应3Mg(OH) (s)+2Fe3+(aq) 2Fe(OH) (s)+3Mg2+(aq)的平衡常数K==。
2 3
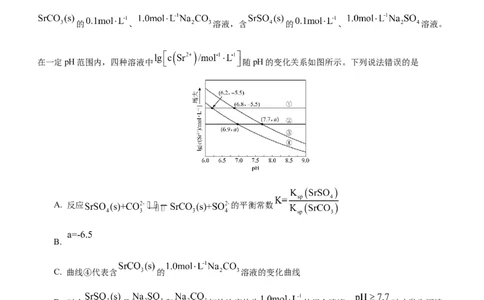
例2.(2022·山东卷)工业上以 为原料生产 ,对其工艺条件进行研究。现有含
的 、 溶液,含 的 、 溶液。
在一定pH范围内,四种溶液中 随pH的变化关系如图所示。下列说法错误的是
A. 反应 的平衡常数
B.
C. 曲线④代表含 的 溶液的变化曲线
D. 对含 且 和 初始浓度均为 的混合溶液, 时才发生沉淀
转化
【变式探究】(2022·湖南卷)为探究 的性质,进行了如下实验( 和 溶液浓度均为
)。
实验 操作与现象① 在 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。
在 溶液中滴加2滴 溶液,变红褐色;再滴加 溶液,产生蓝
②
色沉淀。
在 溶液中滴加2滴 溶液,变红褐色;将上述混合液分成两份,一份滴加
③
溶液,无蓝色沉淀生;另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是
A. 实验①说明加热促进 水解反应
B. 实验②说明 既发生了水解反应,又发生了还原反应
C. 实验③说明 发生了水解反应,但没有发生还原反应
D. 整个实验说明 对 的水解反应无影响,但对还原反应有影响
高频考点三 溶液中粒子浓度的比较
1.三大守恒规律
(1)电荷守恒:电解质溶液中所有阳离子的正电荷总数与所有阴离子的负电荷总数相等。
(2)物料守恒:电解质溶液中由于电离或水解因素,离子会发生变化,变成其他离子或分子等,但离子或
分子中某些特定元素的原子的总数存在确定的比例关系。
(3)质子守恒:即HO电离出的氢离子和氢氧根离子总数相等。一般根据电荷守恒式和物料守恒式整理得
2
到。
2.溶液中粒子浓度比较
(1)MCl(强酸弱碱盐)溶液
①电荷守恒:c(M+)+c(H+)=c(Cl-)+c(OH-)
②物料守恒:c(M+)+c(MOH)=c(Cl-)
③粒子浓度:c(Cl-)>c(M+)>c(H+)>c(MOH)>c(OH)
(2)Na A(强碱弱酸盐)溶液
2
①电荷守恒:c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-)
②物料守恒:c(Na+)=2[c(H A)+c(HA-)+c(A2-)]
2
③粒子浓度:c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H A)>c(H+)
2(3)NaHA(a:水解为主,b:电离为主)
①电荷守恒:c(Na+)+c(H+)=2c(A2-)+c(HA-)+c(OH-)
②物料守恒:c(Na+)=c(H A)+c(HA-)+c(A2-)
2
③粒子浓度:
(4)HA(弱酸)与NaA混合液(同浓度同体积)(a:pH<7,b:pH>7)
①电荷守恒:c(Na+)+c(H+)=c(A-)+c(OH-)
②物料守恒:2c(Na+)=c(HA)+c(A-)
③粒子浓度:
(5)MOH(弱碱)与MCl混合液(同浓度、同体积)
(a:pH>7,b:pH<7)
①电荷守恒:c(M+)+c(H+)=c(Cl-)+c(OH-)
②物料守恒:2c(Cl-)=c(MOH)+c(M+)
③粒子浓度:
例3.(2022·海南卷)NaClO溶液具有漂白能力,已知25℃时, 。下列关于NaClO
溶液说法正确的是
A. 0.01mol/L溶液中,
B. 长期露置在空气中,释放 ,漂白能力减弱
C. 通入过量 ,反应的离子方程式为
D. 25℃, 的NaClO和HClO的混合溶液中,
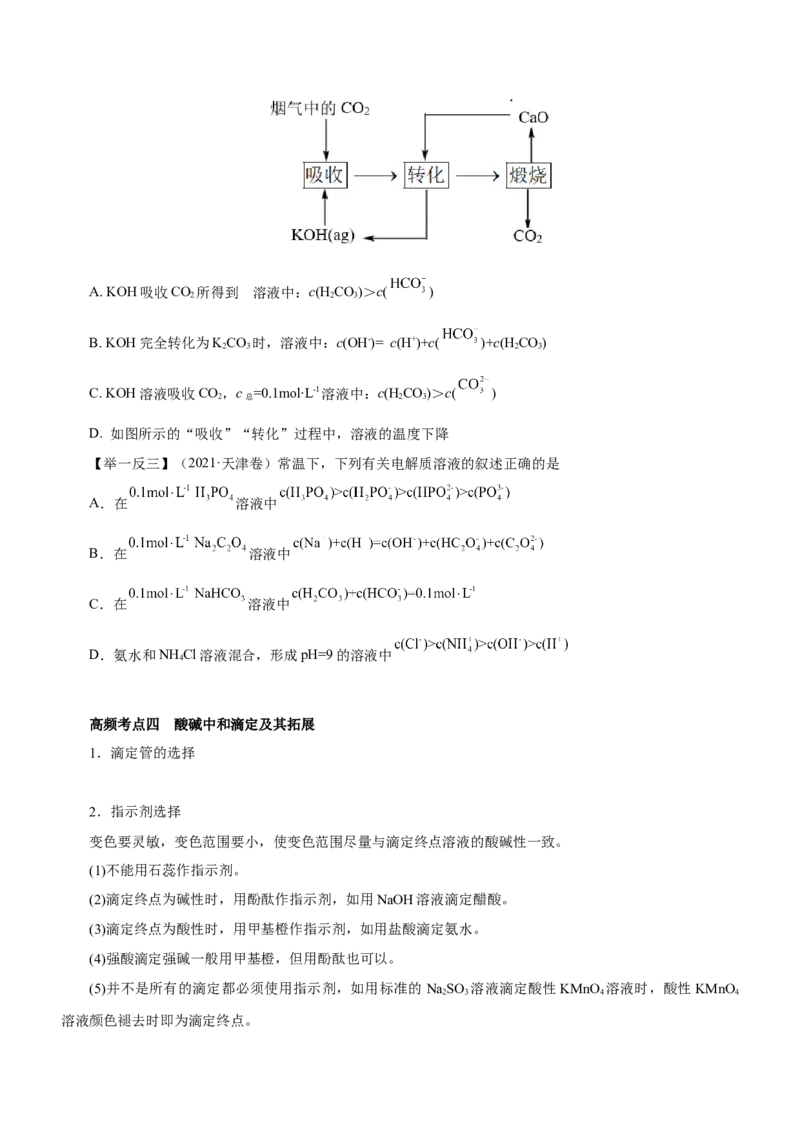
【变式探究】(2022·江苏卷)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收
2
CO,若通入CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c( )
2 2 2 总 2 3
+c( )。HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是
2 3 a1 a2的
A. KOH吸收CO 所得到 溶液中:c(H CO)>c( )
2 2 3
B. KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c( )+c(H CO)
2 3 2 3
C. KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c( )
2 总 2 3
D. 如图所示的“吸收”“转化”过程中,溶液的温度下降
【举一反三】(2021·天津卷)常温下,下列有关电解质溶液的叙述正确的是
A.在 溶液中
B.在 溶液中
C.在 溶液中
D.氨水和NH Cl溶液混合,形成pH=9的溶液中
4
高频考点四 酸碱中和滴定及其拓展
1.滴定管的选择
2.指示剂选择
变色要灵敏,变色范围要小,使变色范围尽量与滴定终点溶液的酸碱性一致。
(1)不能用石蕊作指示剂。
(2)滴定终点为碱性时,用酚酞作指示剂,如用NaOH溶液滴定醋酸。
(3)滴定终点为酸性时,用甲基橙作指示剂,如用盐酸滴定氨水。
(4)强酸滴定强碱一般用甲基橙,但用酚酞也可以。
(5)并不是所有的滴定都必须使用指示剂,如用标准的NaSO 溶液滴定酸性KMnO 溶液时,酸性KMnO
2 3 4 4
溶液颜色褪去时即为滴定终点。3.误差分析
c =V
测 标
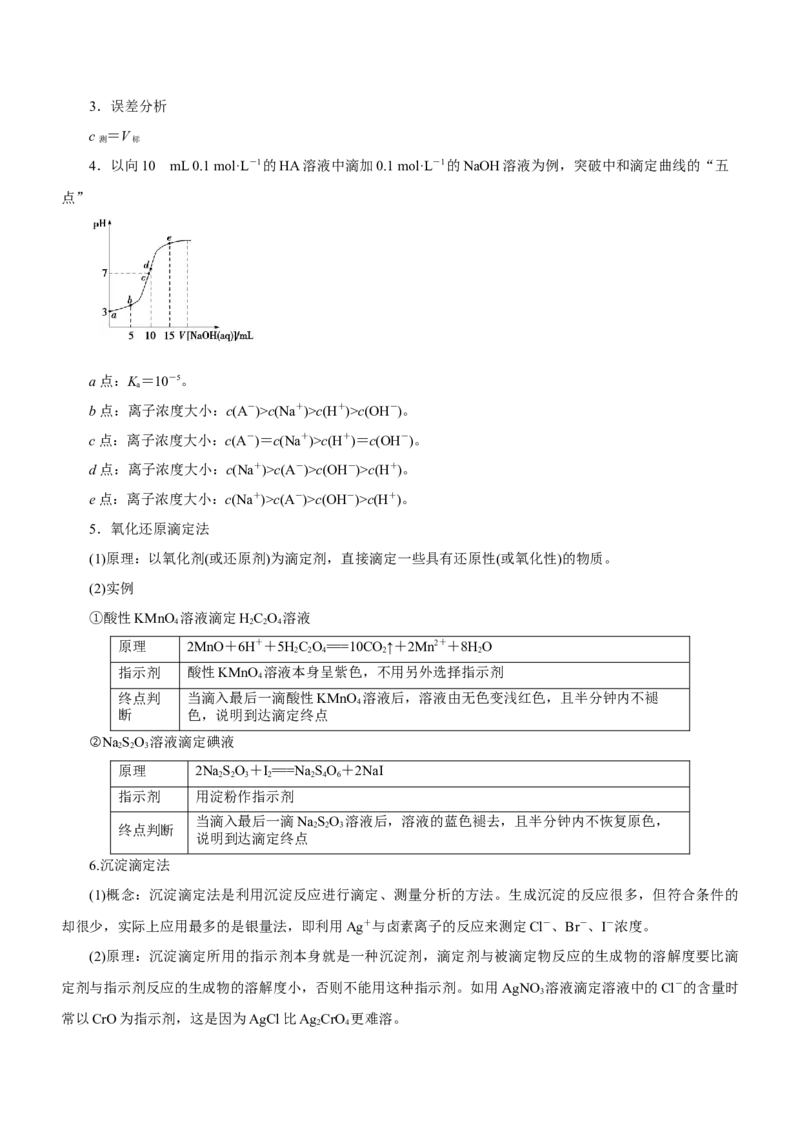
4.以向10 mL 0.1 mol·L-1的HA溶液中滴加0.1 mol·L-1的NaOH溶液为例,突破中和滴定曲线的“五
点”
a点:K=10-5。
a
b点:离子浓度大小:c(A-)>c(Na+)>c(H+)>c(OH-)。
c点:离子浓度大小:c(A-)=c(Na+)>c(H+)=c(OH-)。
d点:离子浓度大小:c(Na+)>c(A-)>c(OH-)>c(H+)。
e点:离子浓度大小:c(Na+)>c(A-)>c(OH-)>c(H+)。
5.氧化还原滴定法
(1)原理:以氧化剂(或还原剂)为滴定剂,直接滴定一些具有还原性(或氧化性)的物质。
(2)实例
①酸性KMnO 溶液滴定HC O 溶液
4 2 2 4
原理 2MnO+6H++5HC O===10CO ↑+2Mn2++8HO
2 2 4 2 2
指示剂 酸性KMnO 溶液本身呈紫色,不用另外选择指示剂
4
终点判 当滴入最后一滴酸性KMnO 溶液后,溶液由无色变浅红色,且半分钟内不褪
4
断 色,说明到达滴定终点
②Na SO 溶液滴定碘液
2 2 3
原理 2NaSO+I===Na SO+2NaI
2 2 3 2 2 4 6
指示剂 用淀粉作指示剂
当滴入最后一滴NaSO 溶液后,溶液的蓝色褪去,且半分钟内不恢复原色,
终点判断 2 2 3
说明到达滴定终点
6.沉淀滴定法
(1)概念:沉淀滴定法是利用沉淀反应进行滴定、测量分析的方法。生成沉淀的反应很多,但符合条件的
却很少,实际上应用最多的是银量法,即利用Ag+与卤素离子的反应来测定Cl-、Br-、I-浓度。
(2)原理:沉淀滴定所用的指示剂本身就是一种沉淀剂,滴定剂与被滴定物反应的生成物的溶解度要比滴
定剂与指示剂反应的生成物的溶解度小,否则不能用这种指示剂。如用AgNO 溶液滴定溶液中的Cl-的含量时
3
常以CrO为指示剂,这是因为AgCl比Ag CrO 更难溶。
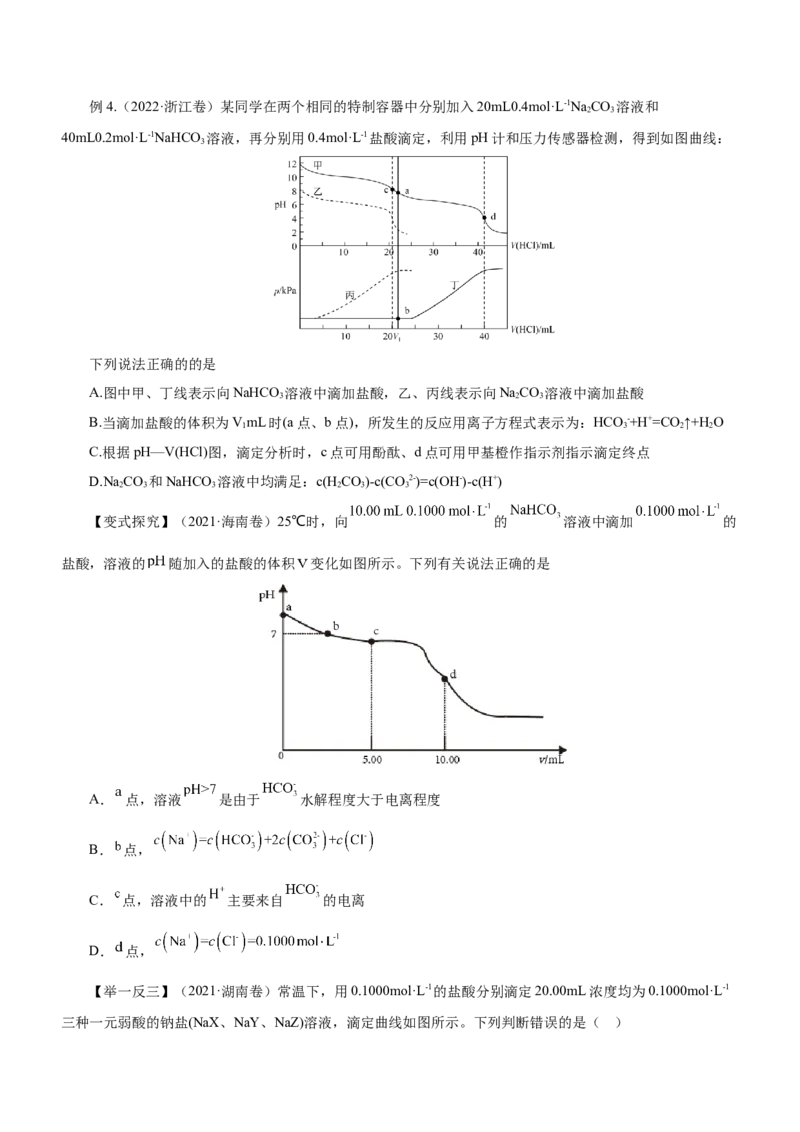
2 4例4.(2022·浙江卷)某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
3
下列说法正确的的是
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO -+H+=CO ↑+H O
1 3 2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO2-)=c(OH-)-c(H+)
2 3 3 2 3 3
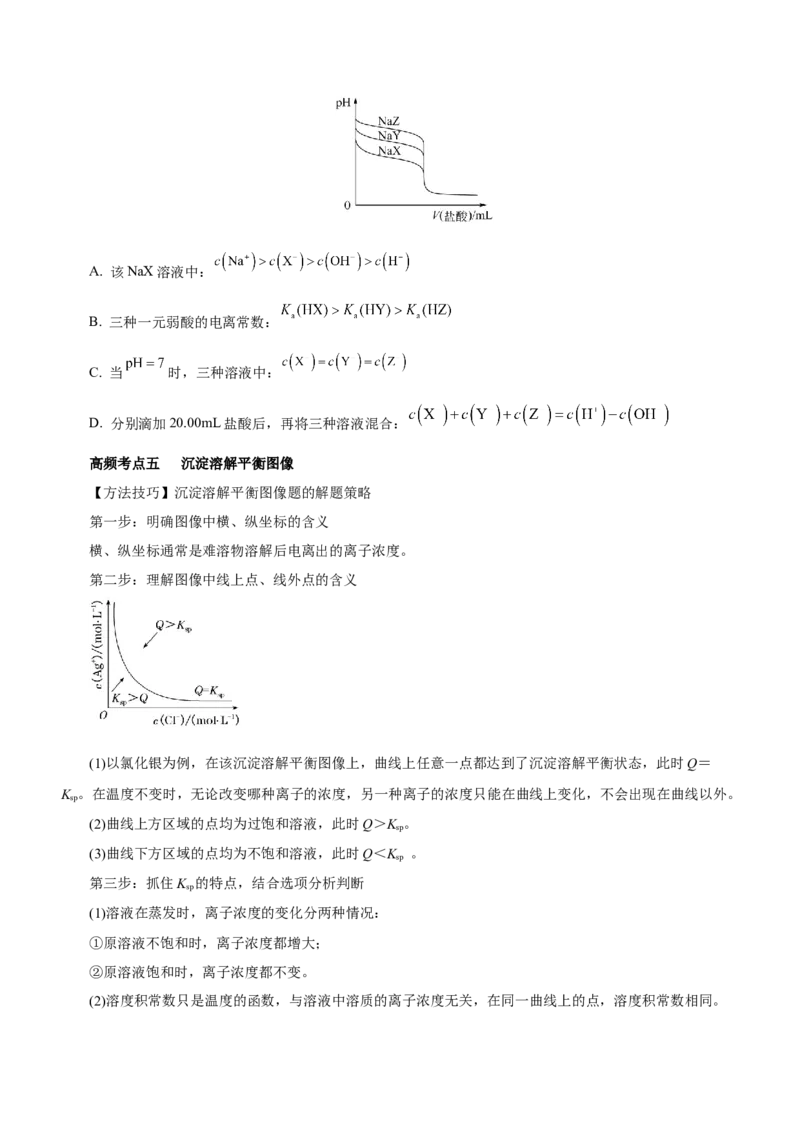
【变式探究】(2021·海南卷)25℃时,向 的 溶液中滴加 的
盐酸,溶液的 随加入的盐酸的体积 变化如图所示。下列有关说法正确的是
A. 点,溶液 是由于 水解程度大于电离程度
B. 点,
C. 点,溶液中的 主要来自 的电离
D. 点,
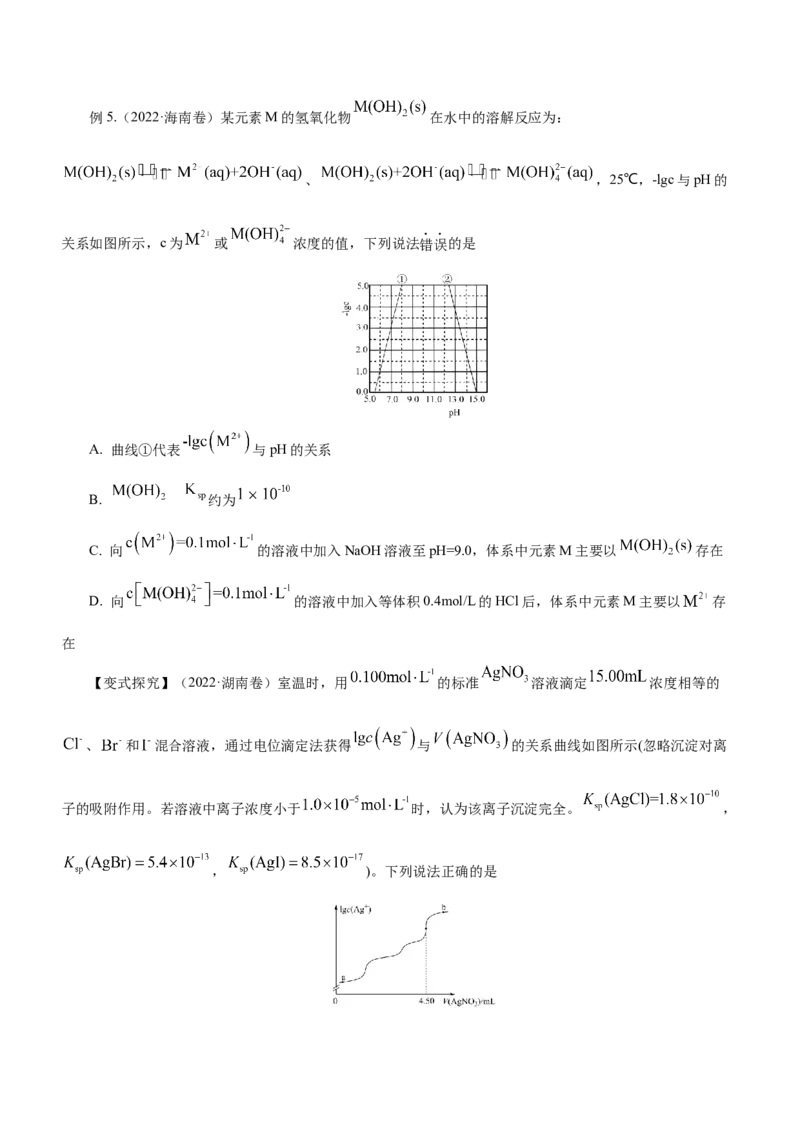
【举一反三】(2021·湖南卷)常温下,用0.1000mol·L-1的盐酸分别滴定20.00mL浓度均为0.1000mol·L-1
三种一元弱酸的钠盐(NaX、NaY、NaZ)溶液,滴定曲线如图所示。下列判断错误的是( )A. 该NaX溶液中:
B. 三种一元弱酸的电离常数:
C. 当 时,三种溶液中:
D. 分别滴加20.00mL盐酸后,再将三种溶液混合:
高频考点五 沉淀溶解平衡图像
【方法技巧】沉淀溶解平衡图像题的解题策略
第一步:明确图像中横、纵坐标的含义
横、纵坐标通常是难溶物溶解后电离出的离子浓度。
第二步:理解图像中线上点、线外点的含义
(1)以氯化银为例,在该沉淀溶解平衡图像上,曲线上任意一点都达到了沉淀溶解平衡状态,此时Q=
K 。在温度不变时,无论改变哪种离子的浓度,另一种离子的浓度只能在曲线上变化,不会出现在曲线以外。
sp
(2)曲线上方区域的点均为过饱和溶液,此时Q>K 。
sp
(3)曲线下方区域的点均为不饱和溶液,此时Q<K 。
sp
第三步:抓住K 的特点,结合选项分析判断
sp
(1)溶液在蒸发时,离子浓度的变化分两种情况:
①原溶液不饱和时,离子浓度都增大;
②原溶液饱和时,离子浓度都不变。
(2)溶度积常数只是温度的函数,与溶液中溶质的离子浓度无关,在同一曲线上的点,溶度积常数相同。例5.(2022·海南卷)某元素M的氢氧化物 在水中的溶解反应为:
、 ,25℃,-lgc与pH的
关系如图所示,c为 或 浓度的值,下列说法错误的是
A. 曲线①代表 与pH的关系
的
B. 约为
C. 向 的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以 存在
D. 向 的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 存
在
【变式探究】(2022·湖南卷)室温时,用 的标准 溶液滴定 浓度相等的
、 和 混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离
子的吸附作用。若溶液中离子浓度小于 时,认为该离子沉淀完全。 ,
, )。下列说法正确的是A. a点:有白色沉淀生成 B. 原溶液中 的浓度为
C. 当 沉淀完全时,已经有部分 沉淀 D. b点:
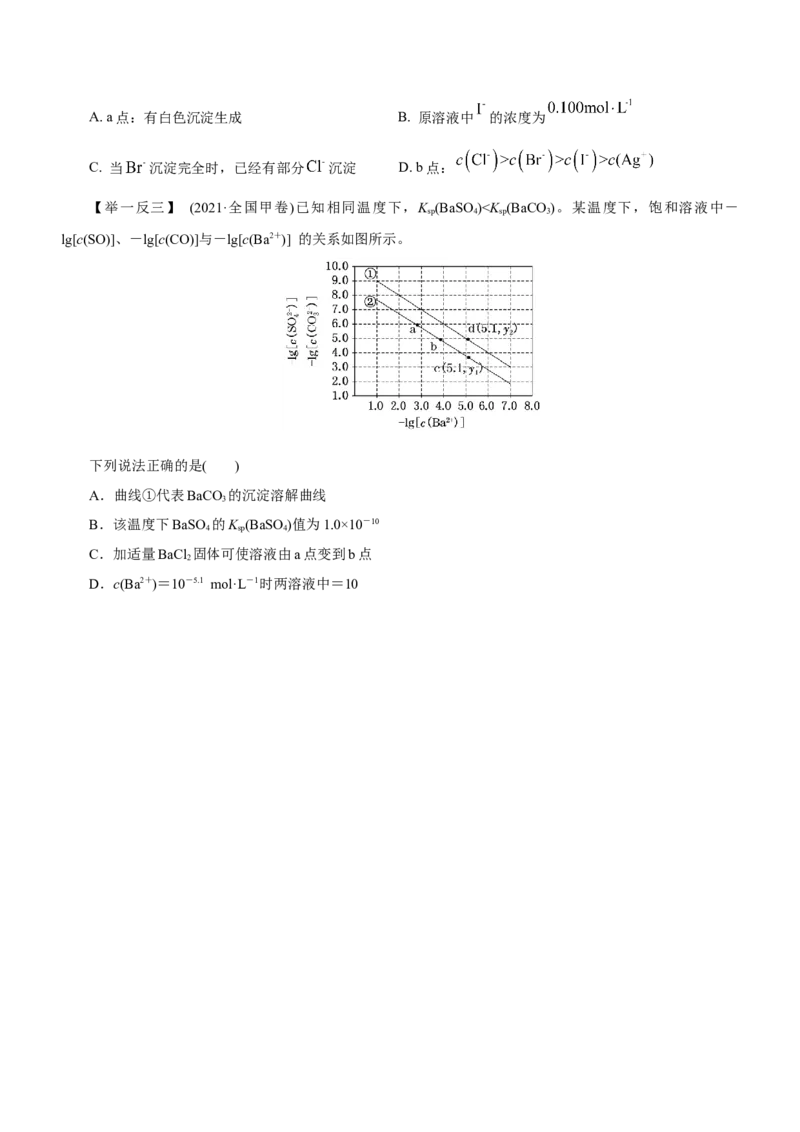
【举一反三】 (2021·全国甲卷)已知相同温度下,K (BaSO)