文档内容
专题 08 水溶液中的离子反应与平衡
目 录
01 弱电解质的电离平衡
02 水的电离和溶液的酸碱性
03 酸碱中和滴定
04 盐类水解和粒子浓度大小比较
05 难溶电解质的溶解平衡
01 弱电解质的电离平衡
1.已知NH ·H O为弱碱,下列实验事实能证明某酸HA为弱酸的是( )
3 2
A.浓度为0.1 mol·L-1HA的导电性比浓度为0.1 mol·L-1硫酸的导电性弱
B.0.1 mol·L-1 NH A溶液的pH等于7
4
C.0.1 mol·L-1的HA溶液能使甲基橙变红色
D.等物质的量浓度的NaA和HA混合溶液pH小于7
2.已知25 ℃时有关弱酸的电离平衡常数如下表:
弱酸化学式 HX HY HCO
2 3
K =4.4×10-7
电离平衡常数/mol·L-1 7.8×10-9 3.7×10-15 1
K =4.7×10-11
2
下列推断正确的是( )
A.HX、HY两种弱酸的酸性:HX>HY
B.相同条件下溶液的碱性:NaX>NaCO>NaY>NaHCO
2 3 3
C.结合H+的能力:CO>Y->X->HCOD.HX和HY酸性相同,都比HCO 弱
2 3
3.根据下表提供的数据,判断下列离子方程式或化学方程式正确的是( )
化学式 电离常数
HClO K=3×10-8
HCO K =4×10-7 K =6×10-11
2 3 a1 a2
A.向NaCO 溶液中滴加少量氯水:CO+2Cl+HO===2Cl-+2HClO+CO↑
2 3 2 2 2
B.向NaHCO 溶液中滴加少量氯水:2HCO+Cl===Cl-+ClO-+2CO↑+HO
3 2 2 2
C.向NaClO溶液中通入少量CO:CO+NaClO+HO===NaHCO+HClO
2 2 2 3
D.向NaClO溶液中通入过量CO:CO+2NaClO+HO===Na CO+2HclO
2 2 2 2 3
4.(2023·北京市牛栏山一中高三检测)室温下,对于1L 醋酸溶液,下列判断正确的是( )
A.该溶液中CHCOO-的粒子数为 个
3
B.加入少量CHCOONa固体后,溶液的pH升高
3
C.滴加NaOH溶液过程中,c(CHCOO-)与c(CHCOOH)之和始终为0.1mol/L
3 3
D.与NaCO 溶液反应的离子方程式为CO2-+2H+=H O+CO↑
2 3 3 2 2
5.醋酸溶液中存在电离平衡:CHCOOH H++CHCOO-,下列叙述不正确的是
3 3
A.0.1 mol/L 的CHCOOH 溶液加水稀释或加热均可使CHCOO-的物质的量增多
3 3
B.0.1 mol/L 的CHCOOH 溶液加水稀释,c(CHCOO-)/[c(CHCOOH) ·c(OH-)]不变
3 3 3
C.向0.1 mol/L CH COOH溶液中加入少量纯醋酸,平衡向右移动,电离程度增大
3
D.0.1 mol/L CH COOH溶液加水稀释后,溶液中c(CHCOOH)/c(CHCOO-)的值减小
3 3 3
6.(2023·浙江省宁波市高三选考模拟考试)下列说法正确的是( )
A.25℃时,将pH=5的醋酸溶液与pH=5的盐酸等体积混合,混合后溶液pH>5
B.25℃时,等浓度的盐酸与醋酸分别稀释相同倍数,稀释后溶液pH:盐酸<醋酸
C.25℃时,等体积、等pH的盐酸与醋酸分别用等浓度的NaOH溶液中和,盐酸消耗NaOH溶液多
D.25℃时,pH=3的一元酸HA溶液与pH=11的一元碱MOH溶液等体积混合后溶液呈酸性,则HA
是强酸
7.已知某温度下 CHCOOH 和 NH ·H O 的电离常数相等,现向 10 mL 浓度为 0.1 mol·L-1的
3 3 2
CHCOOH溶液中滴加相同浓度的氨水,在滴加过程中( )
3
A.水的电离程度始终增大
B.c(NH)/c(NH ·H O)先增大再减小
3 2
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3
D.当加入氨水的体积为10 mL时,c(NH)=c(CHCOO-)
3
8.(2023·浙江省诸暨市高三适应性考试)已知HR为二元弱酸,K (H R)=5.4×10-2,K (H R)=5.4×10-
2 a1 2 a2 2
5。室温下,下列说法不正确的是( )
A.0.1mol/L NaHR溶液pH<7B.用NaOH溶液中和一定量的HR溶液至呈中性时,溶液中c(HR-)<c(R2-)
2
C.0.1mol/L H R溶液:.2mol/L+c(OH-)=c(H+)+c(H R)+c(HR-)
2 2
D.0.01mol/L的HR溶液与pH=12的NaOH溶液完全中和时,消耗酸与碱溶液的体积比为1∶2
2
9.(2024·山西吕梁高三阶段性测试)草酸(乙二酸)存在于自然界的植物中,其K =5.2×10-2,K =5.4×10-
a1 a2
5。草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(HC O·2H O)无色,熔点为101℃,易溶于
2 2 4 2
水,受热脱水、升华,170℃以上分解。有关草酸性质说法错误的是( )
A.草酸晶体(HC O·2H O)受热时先熔化后分解
2 2 4 2
B.草酸与澄清石灰水反应的离子方程式为:Ca2++2OH-+H C O =CaC O↓+2H O
2 2 4 2 4 2
C.草酸溶液中加入少量NaHCO 溶液,产生气泡:HC O+NaHCO=NaHC O+2CO +2H O
3 2 2 4 3 2 4 2 2
D.HC O 具有还原性,把草酸滴入酸性高锰酸钾溶液,溶液褪色,发生的反应为:2 MnO -+5C O2-
2 2 4 4 2 4
+16H+=2 Mn2++10CO ↑+8H O
2 2
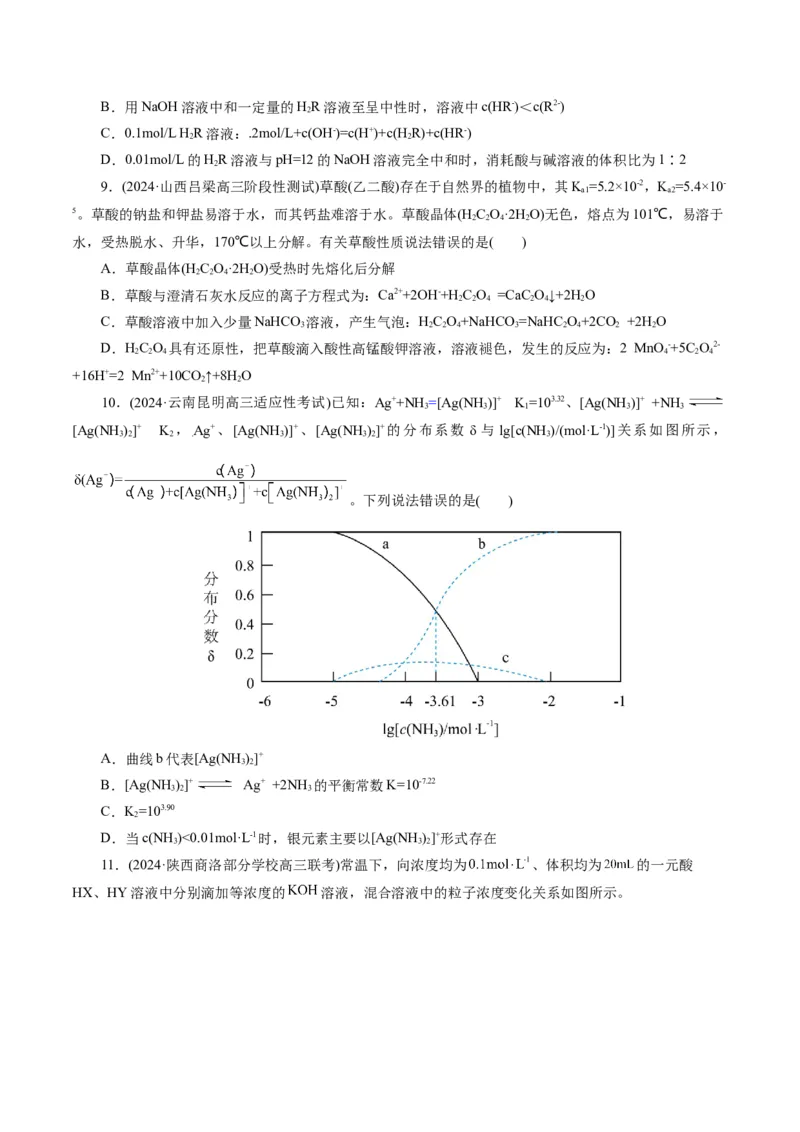
10.(2024·云南昆明高三适应性考试)已知:Ag++NH=[Ag(NH)]+ K=103.32、[Ag(NH)]+ +NH
3 3 1 3 3
[Ag(NH)]+ K ,Ag+、[Ag(NH)]+、[Ag(NH)]+的分布系数 δ 与 lg[c(NH)/(mol·L-1)]关系如图所示,
3 2 2 . 3 3 2 3
。下列说法错误的是( )
A.曲线b代表[Ag(NH)]+
3 2
B.[Ag(NH)]+ Ag+ +2NH 的平衡常数K=10-7.22
3 2 3
C.K=103.90
2
D.当c(NH )<0.01mol·L-1时,银元素主要以[Ag(NH)]+形式存在
3 3 2
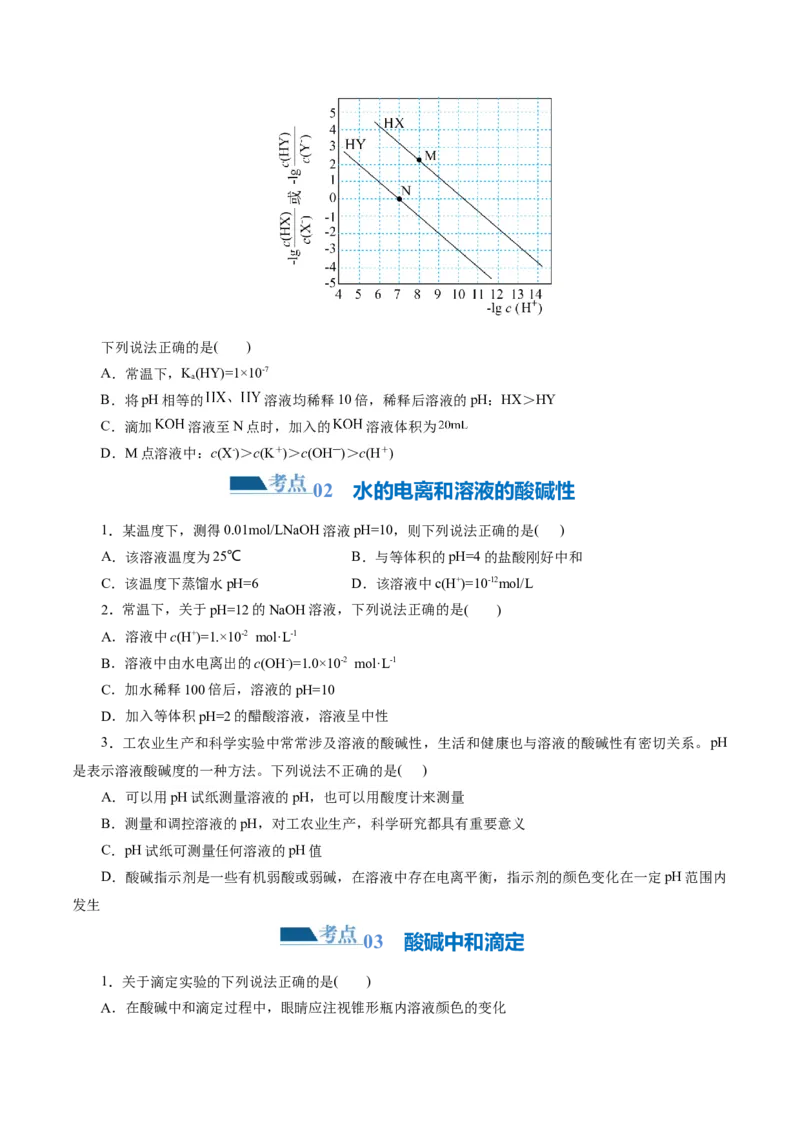
11.(2024·陕西商洛部分学校高三联考)常温下,向浓度均为 、体积均为 的一元酸
HX、HY溶液中分别滴加等浓度的 溶液,混合溶液中的粒子浓度变化关系如图所示。下列说法正确的是( )
A.常温下,K(HY)=1×10-7
a
B.将pH相等的 溶液均稀释10倍,稀释后溶液的pH:HX>HY
C.滴加 溶液至N点时,加入的 溶液体积为
D.M点溶液中:c(X-)>c(K+)>c(OH―)>c(H+)
02 水的电离和溶液的酸碱性
1.某温度下,测得0.01mol/LNaOH溶液pH=10,则下列说法正确的是( )
A.该溶液温度为25℃ B.与等体积的pH=4的盐酸刚好中和
C.该温度下蒸馏水pH=6 D.该溶液中c(H+)=10-12mol/L
2.常温下,关于pH=12的NaOH溶液,下列说法正确的是( )
A.溶液中c(H+)=1.×10-2 mol·L-1
B.溶液中由水电离出的c(OH-)=1.0×10-2 mol·L-1
C.加水稀释100倍后,溶液的pH=10
D.加入等体积pH=2的醋酸溶液,溶液呈中性
3.工农业生产和科学实验中常常涉及溶液的酸碱性,生活和健康也与溶液的酸碱性有密切关系。pH
是表示溶液酸碱度的一种方法。下列说法不正确的是( )
A.可以用pH试纸测量溶液的pH,也可以用酸度计来测量
B.测量和调控溶液的pH,对工农业生产,科学研究都具有重要意义
C.pH试纸可测量任何溶液的pH值
D.酸碱指示剂是一些有机弱酸或弱碱,在溶液中存在电离平衡,指示剂的颜色变化在一定pH范围内
发生
03 酸碱中和滴定
1.关于滴定实验的下列说法正确的是( )
A.在酸碱中和滴定过程中,眼睛应注视锥形瓶内溶液颜色的变化B.用NaOH标准溶液滴定未知浓度的盐酸,达到滴定终点时发现滴定管尖嘴部分有悬滴,会使测定
结果偏小
C.用KMnO 标准溶液滴定草酸时,KMnO 标准溶液盛装在碱式滴定管中
4 4
D.所有的滴定实验都需要加入指示剂
2.实验室用标准盐酸测定某NaOH溶液的浓度,用甲基橙作指示剂,下列对测定结果的评价错误的
是( )
选项 操作 测定结果的评价
A 酸式滴定管在装液前未用标准盐酸润洗2~3次 偏高
B 开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 偏高
C 锥形瓶未干燥 无影响
D 盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 偏低
3.下列实验操作不会引起误差的是( )
A.酸碱中和滴定时,用待测液润洗锥形瓶
B.酸碱中和滴定时,用冲洗干净的滴定管盛装标准溶液
C.用NaOH标准溶液测定未知浓度的盐酸时,选用酚酞作指示剂,实验时不小心多加了几滴
D.用标准盐酸测定未知浓度NaOH溶液,开始实验时,酸式滴定管尖嘴部分无气泡,实验结束时有
气泡
4.(2024·山东烟台高三期中)在含单质碘的KI溶液中存在可逆反应:I(aq)+I-(aq) I-(aq),为测定
2 3
该反应的平衡常数K进行如下实验,实验步骤如下:
①在装有 的KI溶液的碘量瓶中加入足量I,充分搅拌溶解,待过量的固体碘沉于瓶
2
底后,取42.5mL上层清液,用5 mL CCl 萃取,充分振荡、静置、分液,得到42.5mL萃取后的水溶液、
4
5 mLI ~ CCl 溶液。
2 4
②取萃取后的5 mLI ~ CCl 溶液于碘量瓶中,加水充分振荡,再加入质量分数为0.01%KI溶液,充分
2 4
振荡后,静置5分钟,注入4mL0.2%的淀粉溶液,用cmol·L-1的NaSO 标准溶液滴定,平行滴定3次,平
2 2 3
均消耗V mL NaSO 溶液。
1 2 2 3
③将萃取后的水溶液42.5mL移入碘量瓶中,注入4mL0.2%的淀粉溶液,用 的NaSO 标准溶
2 2 3
液滴定,平行滴定3次,平均消耗V mL NaSO 溶液。
2 2 2 3
已知:(1)2 Na SO+I =2Na SO+2NaI;(2)I-与I-难溶于CCl;(3)达到溶解平衡后,I 在CCl 层和水层
2 2 3 2 2 4 6 3 4 2 4
中的分配比 为85:1I(aq)+I-(aq) I-(aq)的平衡常数K计算正确的是( )
2 3
A. B.
C. D.
5.(2024·北京丰台高三期中)某实验小组用如下实验测定海带预处理后所得溶液的碘含量,实验步骤
及现象如下:
已知:I+2Na SO=2NaI+Na SO,下列说法不正确的是( )
2 2 2 3 2 4 6
A.溶液b为蓝色是因为发生了反应:HO+2I-+2H+=I +2H O
2 2 2 2
B.该实验可证明蓝色恢复与空气无关
C.溶液反复由无色变蓝的原因可能是HO 氧化I-的反应速率比NaSO 还原I 的反应速率快
2 2 2 2 3 2
D.上述实验不能准确测定待测液中的碘含量,应补充实验步骤:滴定前向溶液b中加少量MnO ,反
2
应至不再产生气泡,过滤,对滤液进行滴定
6.(2024·山东潍坊五县区高三阶段监测)乙二胺四乙酸(EDTA)可与金属离子形成稳定的配合物。常用
EDTA测定水中钙含量(EDTA与钙反应时物质的量之比均为1∶1)。基本步骤如下:
①EDTA标定:取10.00 mL 0.1 mol·L-1标准CaCl 溶液,加入3滴甲基橙溶液作指示剂,用已配制好
2
的EDTA溶液滴定至终点,消耗EDTA溶液V mL。
1
②钙提取:取一定质量的有机物,并用酸性KMnO 溶液氧化,再经萃取、反萃取将金属转移到水中,
4
得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。
③EDTA滴定:取20.00mL提取液,加入指示剂钙黄绿素(钙与钙黄绿素生成能发出绿色荧光的配合物),在黑色背景下用标定后的EDTA溶液滴定至终点,消耗EDTA溶液V mL。
2
提取液中钙含量(浓度单位为 )的计算结果正确的是( )
A. B. C. D.
7.(2023·山东省高三联考)一定条件下,乙酸酐[(CH CO) O]醇解反应
3 2
[(CH CO) O+ROH→CH COOR+CH COOH]可进行完全,利用此反应定量测定有机醇(ROH)中的羟基含
3 2 3 3
量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入 样品,充分反应后,加适量水使剩余乙酸
酐完全水解:(CHCO) O+HO→2CH COOH。
3 2 2 3
③加指示剂并用cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol·L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。根据上述实验原理,下列说法正确的是(
2
)
A.可以用乙酸代替乙酸酐进行上述实验
B.若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D.步骤④中,若加水量不足,将导致测定结果偏大
8.使用硫酸亚铁铵晶体[(NH )Fe(SO )·6H O]滴定法可以测定青铜中铬元素的含量。实验步骤如下:
4 2 4 2 2
步骤1:称量硫酸亚铁铵晶[(NH )Fe(SO )·6H O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L
4 2 4 2 2
(NH )Fe(SO ) 标准溶液。
4 2 4 2
步骤2:称取1.00 g青铜样品于250 mL维形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过硫酸
[(NH )SO]溶液,加热煮沸,使样品中的铬元素完全转化为HCrO,冷却后加蒸馏水配制成250 mL溶液,
4 2 2 8 2 4
摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用
(NH )Fe(SO ) 标准溶液满淀至终点。重复上述操作3次。测得消耗(NH )Fe(SO ) 标准溶液的体积分别为
4 2 4 2 4 2 4 2
18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:HCrO+Fe2++H+→Cr3++Fe3++H O (未配平)
2 4 2
下列说法不正确的是( )
A.在“步骤1”中,用到的玻璃仪器有1000 mL容量瓶、烧杯、玻璃棒、胶头滴管
B.在“步骤2”中,铜与硝酸反应的离子方程式为:3Cu+2NO-+8H+=3Cu2++2NO↑+4HO
3 2
C.青铜中铬元素的质量分数为6.344%
D.实验中,如果盛放(NH )Fe(SO ) 标准溶液的滴定管没有润洗,则测量结果将偏大
4 2 4 204 盐类水解和粒子浓度大小比较
1.(2024·江西宜春高三期末)(双选)某同学拟用 计测定溶液 以探究某酸HR是否为弱电解质。下
列说法正确的是( )
A.25℃时,若测得0.01mol·L-1NaR溶液PH>7,则HR是弱酸
B.25℃时,若测得0.01mol·L-1HR溶液 且 ,则HR是弱酸
C.25℃时,若测得HR溶液 ,取该溶液 ,加蒸馏水稀释至 ,测得 ,
则HR是弱酸
D.25℃时,若测得NaR溶液 ,取该溶液 ,升温至50℃,测得 , ,则HR是弱
酸
2.将去掉氧化膜的铝片放入足量NaCO 溶液中,铝片表面产生气泡,充分反应后得到无色溶液M。
2 3
下列分析错误的是( )
A.产生的气体中有H B.反应与CO2-水解有关
2 3
C.Al(OH) 向酸式电离方向移动 D.M中含大量:Na+、Al3+、HCO -
3 3
3.甲胺[(CH )NH ·H O]在水中电离与氨相似,常温下,K [(CH )NH ·H O]=2.0×10-5。已知lg2=0.3。下
3 2 2 b 3 2 2
列说法错误的是( )
A.(CH)NH NO 溶液显酸性
3 3 3
B.甲胺溶液中c(OH-)随温度升高而增大
C.常温下,0.1mol/L的甲胺溶液的pH=11.3
D.0.1mol/L(CH )NH Cl溶液中离子浓度大小关系为:c(Cl-)>c[(CH )NH )+]>c(H+)>c(OH-)
3 3 3 3
4.含SO 的烟气会形成酸雨,工业上常利用NaSO 溶液作为吸收液脱除烟气中的SO ,随着SO 的吸
2 2 3 2 2
收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是( )
A.NaSO 溶液中存在:c(Na+)>c(SO)>c(H SO )>c(HSO)
2 3 2 3
B.已知NaHSO 溶液pH<7,该溶液中:c(Na+)>c(HSO)>c(H SO )>c(SO)
3 2 3
C.当吸收液呈酸性时:c(Na+)=c(SO)+c(HSO)+c(H SO )
2 3
D.当吸收液呈中性时:c(Na+)=2c(SO)+c(HSO)
5.室温下,有a mol·L-1NaX和b mol·L-1NaY两种盐溶液。下列说法正确的是( )
A.若a=b且c(X-) +c(HX)=c(Y-),则酸性HX>HY
B.若a>b且c(X-)=c(Y-),则酸性HX>HY
C.若 且 ,则酸性HX<HY
D.若a<b且c(X-)<c(Y-),则酸性HX<HY
6.(2023·广东省百校高三联考)苯甲酸钠(PhCOONa)是一种常用食品防腐剂。已知25℃,PhCOOH的
K=1.0×10-4.2。下列有关PhCOONa溶液说法不正确的是( )
a
A.PhCOONa溶液呈碱性B.0.1mol/L PhCOONa溶液中: c(PhCOO-)<0.1mol/L
C. 25℃,pH=7的PhCOONa和PhCOOH的混合溶液中:c(PhCOOH)>c(PhCOO-) = c(Na+)
D.PhCOONa溶液加水稀释时,溶液中c(PhCOO-)减小
7.已知:常温下,CN-的水解常数K =1.6×10-5。该温度下,将浓度均为0.1 mol•L-1的HCN溶液和
h
NaCN溶液等体积混合。下列说法正确的是( )
A.混合溶液的
B.混合液中水的电离程度小于纯水的
C.混合溶液中存在c(CN-)>c(Na+)>c(HCN)>c(OH-)>c(H+)
D.若c 盐酸与0.6 mol•L-1 NaCN溶液等体积混合后溶液呈中性,则
8.将标准状况下1.68LCO 通入含有2gNaOH的水溶液中,完全反应并得到2L碱性溶液。则对于该溶
2
液表述正确的是( )
A.2c(Na+)=3[c(HCO-)+c(CO 2-)+c(H CO)]
3 3 2 3
B.c(Na+)+c(H+)=c(HCO-)+2c(CO 2-)+c(OH-)
3 3
C.HCO -的电离程度大于HCO -的水解程度
3 3
D.存在的平衡体系只有:HCO -+H O HCO+OH-,HCO - H++ CO2-
3 2 2 3 3 3
9.(2024·江浙高中发展共同体高三联考)室温下,通过下列实验探究NaHSO 溶液的性质。下列有关说
3
法正确的是( )
实验 实验操作和现象或结论
1 用 试纸测量0.1mol·L-1NaHSO 溶液的 ,测得 约为5
3
向10 mL 0.1mol·L-1NaHSO 溶液中加入等体积0.1mol·L-1氨水溶液,充分混合,溶液
2 3
约为9
3 向10 mL 0.1mol·L-1NaCO 溶液中滴加几滴0.1mol·L-1NaHSO 溶液,无明显现象
2 3 3
4 向10 mL 0.1mol·L-1NaHSO 溶液中加入10 mL 0.05mol·L-1Ba(ClO) 溶液,产生白色沉淀
3 2
A.实验1可得出:K (H SO ) · K (H SO ) <K
a1 2 3 a2 2 3 W
B.实验2所得溶液中存在:c(H+)+c(HSO ) +c(HSO -)= c(OH―)+c(NH ·H O)
2 3 3 3 2
C.实验3可得出:K (H SO )<K (H CO)
a2 2 3 a1 2 3
D.实验4两溶液混合时有:
10.(2024·江苏常州高三期中)室温下,通过下列实验探究NaHCO 、NaCO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1mol•L-1NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1mol•L-1NaHCO 溶液与0.1mol•L-1CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:饱和NaCO 溶液中通入CO 产生白色沉淀,溶液pH从12下降到约为9
2 3 2实验4:0.1mol•L-1NaHCO 溶液中滴加新制饱和氯水,氯水颜色褪去并有气泡
3
下列说法正确的是( )
A.由实验1可得出:K (H CO)∙K (H CO)<10-16
a1 2 3 a2 2 3
B.实验2中两溶液混合时有:K (CaCO)>2.5×10-3
sp 3
C.实验3中发生反应的离子方程式为CO2-+H O+CO=2 HCO -
3 2 2 3
D.实验4所得溶液中c(Na+)=c(HCO -)+c(CO2-)+c(H CO)
3 3 2 3
11.(2024·江苏南通海安高三联考)室温下:K(CHCOOH)=1.8×10-5、K (H SO )= 10-1.85、
a 3 a1 2 3
K (H SO )=10-7.22 、K(NH ·H O)=1.8×10-5。本小组同学进行如下实验:
a2 2 3 b 3 2
实验 实验操作和现象
1 测定0.10mol·L-1 NaHSO 溶液的
3
2 向0.10mol·L-1CHCOONa溶液中通入少量SO
3 2
3 向20mL0.10mol·L-1CHCOOH溶液中逐滴加入等浓度NaOH溶液10mL
3
4 配制0.10mol·L-1的(NH )SO 、CHCOONH、NH HSO 三种溶液
4 2 3 3 4 4 3
下列所得结论正确的是( )
A.实验1溶液中存在:c(Na+)>c(HSO -)>c(H SO )>c(SO 2-)
3 2 3 3
B.实验2反应的离子方程式:2CHCOO-+SO+H O=2CHCOOH+SO 2-
3 2 2 3 3
C.实验3反应后的溶液中存在:c(CHCOOH)-c(CHCOO-)=c(OH―)-c(H+)
3 3
D.实验4中各溶液pH大小:c(NH HSO )<c(CHCOONH)<c[(NH )SO ]
4 3 3 4 4 2 3
12.下列溶液中粒子的物质的量浓度关系正确的是( )
A.0.1 mol·L-1 NaHCO 溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO)>
3
c(HCO)>c(OH-)
B.20 mL 0.1 mol·L-1 CHCOONa溶液与10 mL 0.1 mol·L-1 HCl溶液混合后溶液呈酸性,所得溶液中:
3
c(CHCOO-)>c(Cl-)>c(CHCOOH)>c(H+)
3 3
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH)+c(OH
-)
D.0.1 mol·L-1 CHCOOH溶液与0.1 mol·L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)
3
+c(CHCOOH)
3
13.下列有关溶液(室温下)的说法正确的是( )
A.NaCO 和NaHCO 形成的混合溶液中:2c(Na+)=3[c(CO 2-)+c(HCO-)+c(H CO)]
2 3 3 3 3 2 3
B.0.10mol•L-1NaHSO 溶液中通入NH 至溶液pH=7:c(Na+)>c(NH+)>c(SO2-)
3 3 4 3
C.物质的量浓度相等的①(NH )SO 溶液、②NH HCO 溶液、③NH Cl溶液、④(NH )Fe(SO ) 溶液
4 2 4 4 3 4 4 2 4 2
中,c(NH +)的大小关系:④>①>②>③
4
D.0.10mol•L-1CHCOONa溶液中通入HCl至溶液pH=7:c(Na+)>c(CH COOH)>c(Cl-)
3 3
14.(2023·浙江省宁波市高三下学期高考模拟)常温下,K (HCOOH)=1.77×10-4,K (HCOOH)=1.75×10-
a1 a2
5,K(NH ·H O)=1.76×10-5,下列说法不正确的是( )
a 3 2A.浓度均为0.1 mol/L的HCOONa和NH Cl溶液中阳离子的物质的量浓度之和:前者>后者
4
B.用相同浓度的NaOH溶液分别滴定等体积、pH均为3的HCOOH和CHCOOH溶液至终点,消耗
3
NaOH溶液的体积:前者<后者
C.0.2mol/L CH COONa与0.1 mol/L盐酸等体积混合后,溶液中微粒浓度:c(Na+)>c(CHCOO-)>
3 3
c(Cl-)>c(CHCOOH)>c(H+)>c(OH-)
3
D.0.2mol/L HCOONa 溶液与 0.1mol/L NaOH 溶液等体积混合后的溶液中:c(HCOO-)+ c(OH-)=
c(HCOOH)+c(H+)
15.室温下,通过下列实验探究NaHCO 溶液的性质。下列有关说法正确的是( )
3
实验 实验操作和现象
1 用pH计测定0.05 mol∙L−1 NaHCO 溶液,测得pH约为8.3
3
向10 mL 0.05 mol∙L−1 NaHCO 溶液中滴加10 mL 0.05 mol∙L−1 NaOH溶液,反应
2 3
结束后测得溶液pH约为10.3
向10 mL 0.05 mol∙L−1 NaHCO 溶液中滴加10 mL 0.05 mol∙L−1 HCl,反应结束后
3 3
测得溶液pH约为5.6
4 向0.05 mol/L NaHCO 溶液中滴加过量0.1 mol∙L−1 Ca(OH) 溶液,产生白色沉淀
3 2
A.NaHCO 溶液中HCO -的电离程度大于水解程度
3 3
B.实验2滴加结束后:c(H+) + 2c(H CO) + c(HCO -) =c(OH-)
2 3 3
C.实验3滴加过程中:c(Na+) = c(CO2-) + c(HCO -) + c(H CO)
3 3 2 3
D.实验4反应静置后的上层清液中:c(Ca2+)∙c(CO2-)< K (CaCO)
3 sp 3
16.(2024·江苏苏州高三期中)室温下,用0.1mol·L-1NaSO 溶液吸收废气中的SO ,并获得BaSO 的过
2 3 2 3
程如图所示。忽略吸收废气所引起的溶液体积变化和HO的挥发,溶液中含硫物种的浓度c=c(H SO )+
2 2 3
2c(SO 2-)+c(HSO -)。已知:K (H SO )=1.54×10-2,K (H SO )=1.02×10-7 。下列说法正确的是( )
3 3 a1 2 3 a2 2 3
A.0.1mol·L-1NaSO 溶液吸收SO 至 的溶液:c(HSO -)<c(SO 2-)
2 3 2 3 3
B.吸收SO 后 的溶液:c(H+)+c(SO 2-)=c(OH―)+c(HSO )
2 3 2 3
C.沉淀后的上层清液:
D.沉淀后的上层清液久置:2c(Ba2+)+c(Na+)+c(H+)= c(OH―)+2c(SO 2-)+c(HSO -)
3 3
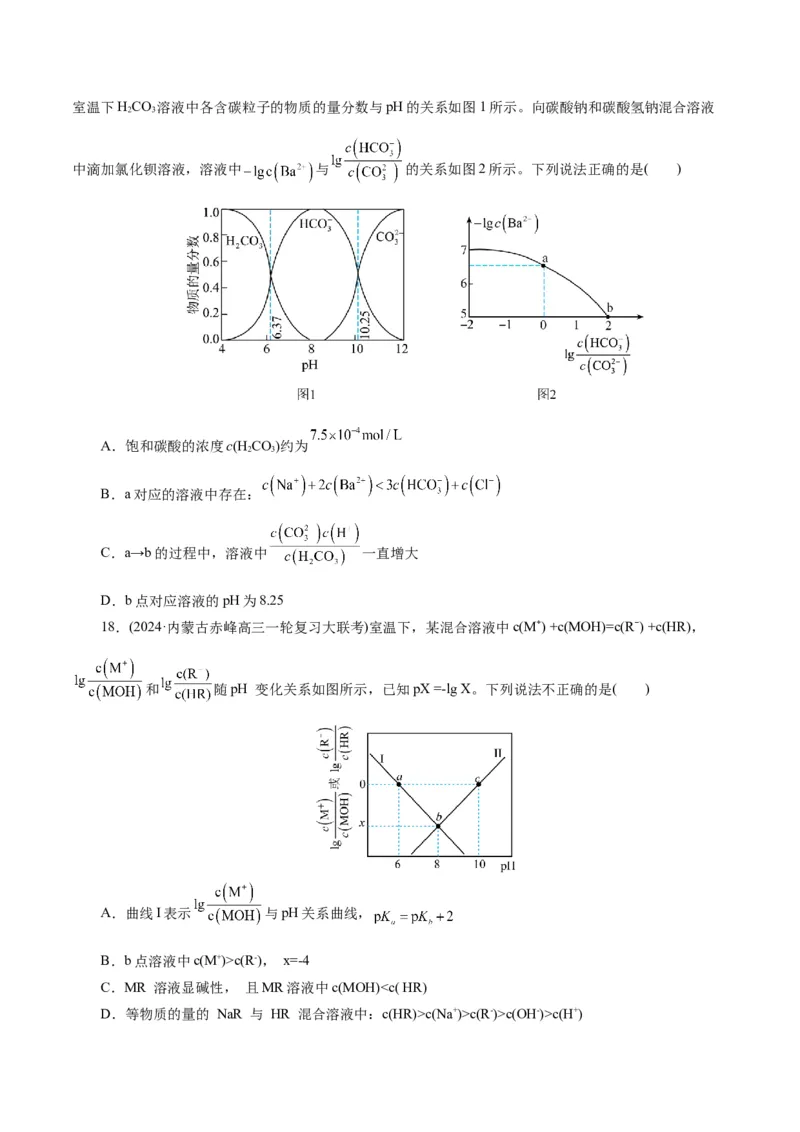
17.(2024·山东德州高三期中)标况下,CO 的溶解度约为1∶1,HO+CO HCO, 。
2 2 2 2 3室温下HCO 溶液中各含碳粒子的物质的量分数与pH的关系如图1所示。向碳酸钠和碳酸氢钠混合溶液
2 3
中滴加氯化钡溶液,溶液中 与 的关系如图2所示。下列说法正确的是( )
A.饱和碳酸的浓度c(HCO)约为
2 3
B.a对应的溶液中存在:
C.a→b的过程中,溶液中 一直增大
D.b点对应溶液的pH为8.25
18.(2024·内蒙古赤峰高三一轮复习大联考)室温下,某混合溶液中c(M⁺) +c(MOH)=c(R⁻) +c(HR),
和 随pH 变化关系如图所示,已知pX =-lg X。下列说法不正确的是( )
A.曲线I表示 与pH关系曲线,
B.b点溶液中c(M+)>c(R-), x=-4
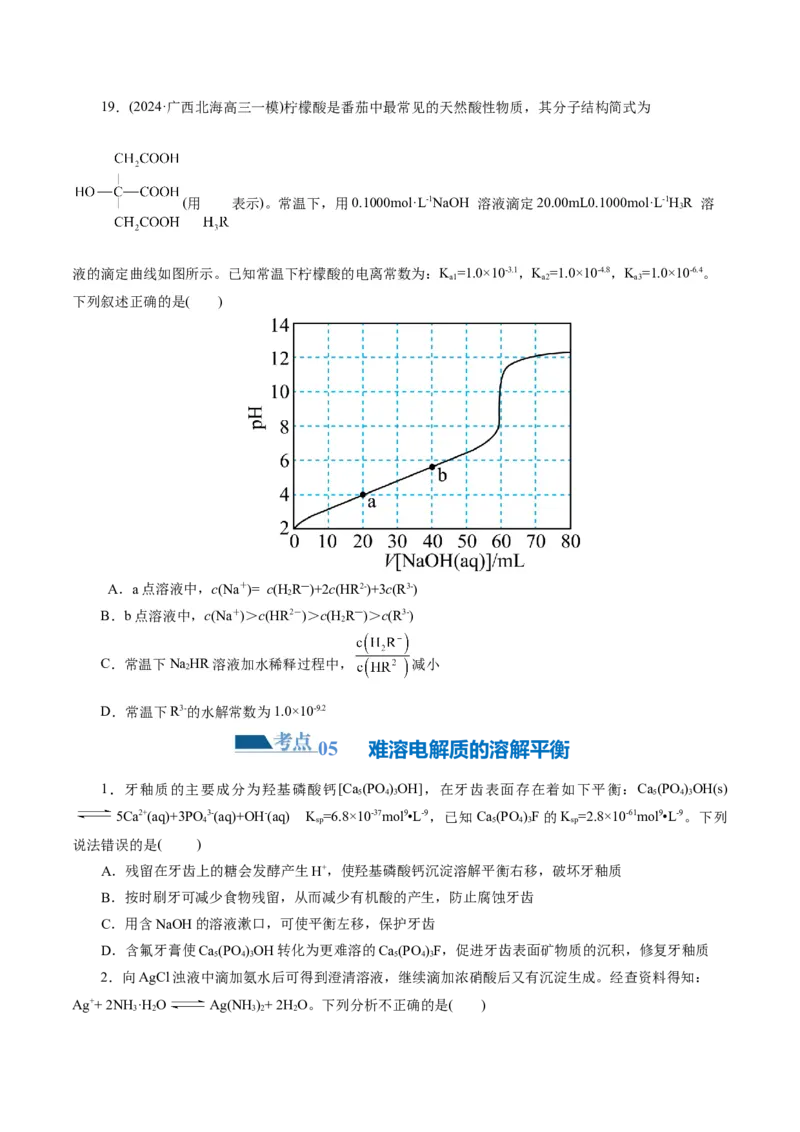
C.MR 溶液显碱性, 且MR溶液中c(MOH)c(Na+)>c(R-)>c(OH-)>c(H+)19.(2024·广西北海高三一模)柠檬酸是番茄中最常见的天然酸性物质,其分子结构简式为
(用 表示)。常温下,用0.1000mol·L-1NaOH 溶液滴定20.00mL0.1000mol·L-1HR 溶
3
液的滴定曲线如图所示。已知常温下柠檬酸的电离常数为:K =1.0×10-3.1,K =1.0×10-4.8,K =1.0×10-6.4。
a1 a2 a3
下列叙述正确的是( )
A.a点溶液中,c(Na+)= c(H R―)+2c(HR2-)+3c(R3-)
2
B.b点溶液中,c(Na+)>c(HR2-)>c(H R―)>c(R3-)
2
C.常温下NaHR溶液加水稀释过程中, 减小
2
D.常温下R3-的水解常数为1.0×10-9.2
05 难溶电解质的溶解平衡
1.牙釉质的主要成分为羟基磷酸钙[Ca (PO )OH],在牙齿表面存在着如下平衡:Ca (PO )OH(s)
5 4 3 5 4 3
5Ca2+(aq)+3PO3-(aq)+OH-(aq) K =6.8×10-37mol9•L-9,已知Ca (PO )F的K =2.8×10-61mol9•L-9。下列
4 sp 5 4 3 sp
说法错误的是( )
A.残留在牙齿上的糖会发酵产生H+,使羟基磷酸钙沉淀溶解平衡右移,破坏牙釉质
B.按时刷牙可减少食物残留,从而减少有机酸的产生,防止腐蚀牙齿
C.用含NaOH的溶液漱口,可使平衡左移,保护牙齿
D.含氟牙膏使Ca (PO )OH转化为更难溶的Ca (PO )F,促进牙齿表面矿物质的沉积,修复牙釉质
5 4 3 5 4 3
2.向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:
Ag++ 2NH ·H O Ag(NH)+ 2H O。下列分析不正确的是( )
3 2 3 2 2A.浊液中存在沉淀溶解平衡:AgCl (s) Ag+(aq)+Cl-(aq)
B.实验可以证明NH 结合Ag+能力比Cl-强
3
C.实验表明实验室可用氨水洗涤银镜反应后的试管
D.由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
3.往锅炉注入NaCO 溶液浸泡,将水垢中的CaSO 转化为CaCO ,再用盐酸去除,下列叙述中正确
2 3 4 3
的是( )
A.温度升高,NaCO 溶液的K 和c(H+)均会增大
2 3 w
B.CaSO 能转化为CaCO ,说明K (CaCO)>K (CaSO)
4 3 sp 3 sp 4
C.CaCO 溶解于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为CO(aq)+CaSO(s) CaCO (s)+SO(aq)
4 3
4.工业上用化学法除锅炉的水垢时,先向锅炉中注入饱和NaCO 溶液浸泡,将水垢中的CaSO 转化
2 3 4
为CaCO ,再用盐酸除去[已知:K (CaCO)=1×10-10,K (CaSO)=9×10-6]。下列说法不正确的是( )
3 sp 3 sp 4
A.温度升高,NaCO 溶液的K 和c(OH-)均会增大
2 3 w
B.沉淀转化的离子方程式为CO(aq)+CaSO(s) CaCO (s)+SO(aq)
4 3
C.该条件下,CaCO 的溶解度小于CaSO
3 4
D.CaCO 和CaSO 共存的悬浊液中,c(SO 2-)/c(CO 2-)=1 105
3 4 4 3
5.(2023·江苏省高三第二次大联考)室温下,通过下列实验探究有关AgNO 的性质[已知:
3
]。
实验1:向 0.1mol·L-1的AgNO 溶液中滴加 0.1mol·L-1的NaCl溶液,产生白色沉淀,过滤,
3
实验2:向实验1所得滤液中滴加 0.1mol·L-1 溶液,产生淡黄色沉淀,过滤。
实验3:向实验2所得滤液中逐滴滴加氨水,产生沉淀先变多后变少,直至消失。
下列说法正确的是( )
A.实验1过滤后滤液中c(Ag+)=10-4.9mol·L-1
B.通过实验1和实验2可得出
C.实验2所得滤液中c(Ag+)+c(H+)=c(Cl-)+c(Br-)+ c(OH-)
D.实验3滴加氨水过程中,c(Ag+)一直减小
6.(2023·浙江省临海、新昌两地高三适应性考试5月模考)印尼苏拉威西岛特产的椰子蟹具有异常坚
硬的甲壳,这归功于摄入的椰子中的月桂酸(C H COOH),在表面的角质层中形成难溶的月桂酸磷酸钙,
11 23
存在如下平衡:Ca PO (OOCC H )(s) 3Ca2+(aq)+PO (aq)+3C H COO-(aq) K =7.3×10-35,已知
3 4 11 23 3 11 23 sp
CaCO 的K =2.8×10-9。下列说法不正确的是( )
3 sp
A.椰子蟹摄入月桂酸含量较高的椰肉有助于形成更加坚硬的甲壳
B.弱碱性的海水可以保护椰子蟹外壳,使其不易被腐蚀
C.将少量月桂酸磷酸钙投入适量1mol•L-1碳酸钠溶液中,可实现其与碳酸钙的转化D.海水中CO 浓度升高,会腐蚀椰子蟹的外壳,使K 增大
2 sp
7.(2023·浙江省杭州地区(含周边)重点中学高三联考化)可溶性钡盐有毒,医院中常用硫酸钡这种钡盐
作为内服造影剂。已知:K (BaCO)=5.0×10-9;K (BaSO)=1.0×10-10。下列推断正确的是( )
sp 3 sp 4
A.饱和BaCO 溶液中存在:c(Ba2+)=c(HCO -)+c(CO2-)
3 3 3
B.向BaCO 、BaSO 的饱和混合溶液中加入少量BaCl ,溶液中 减小
3 4 2
C.不用碳酸钡作为内服造影剂,是因为K (BaCO)>K (BaSO)
sp 3 sp 4
D.若每次加入1 L2mol·L-1的NaCO 溶液,至少需要6次可将0.2mol BaSO 转化为BaCO
2 3 4 3
8.室温下,将0.1mol·L-1AgNO 溶液和0.1mol·L-1NaCl溶液等体积充分混合,一段时间后过滤,得滤
3
液a和沉淀b。取等量的滤液a于两支试管中,分别滴加相同体积、浓度均为 0.1mol·L-1的NaS溶液和
2
NaSO 溶液,前者出现浑浊,后者溶液仍澄清;再取少量的沉淀b,滴加几滴氨水,沉淀逐渐溶解。下列
2 4
说法正确的是( )
A.0.1mol·L-1NaS溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H S)
2 2
B.过滤后所得清液中一定存在:c(Ag+)= 且c(Ag+)>
C.沉淀b中滴加氨水发生反应的离子方程式:AgCl+2NH∙HO=[Ag(NH)]++Cl-+2H O
3 2 3 2 2
D.从实验现象可以得出该温度下K (Ag S)>K (Ag SO )
sp 2 sp 2 4
9.取1.0L浓缩卤水(Cl-、I-浓度均为 )进行实验:滴加一定量AgNO 溶液,产生黄色沉
3
淀;继续滴加,产生白色沉淀。已知: 、 。下列分析不正确的是(
)
A.黄色沉淀是AgI,白色沉淀是AgCl
B.产生白色沉淀时,溶液中存在AgI(s) Ag+(sq)+ I-(aq)
C.若起始时向卤水中滴加2滴(0.1 ) AgNO,能产生沉淀
3
D.白色沉淀开始析出时,
10.(2024·河北承德高三一轮复习联考)工业生产中常通过生成氟化物沉淀除去Ca2+、Mg2+,为探究溶
液酸碱性对沉淀的影响,用盐酸分别调节CaF 和MgF 浊液的pH,在不同pH条件下,测得体系中
2 2
与 为Ca2+、Mg2+、F-)的变化关系如图所示。已知K (CaF )<K (MgF ),下列说法正确
sp 2 sp 2
的是( )A.L 表示 与 的变化曲线
1
B.K (CaF )=10-9.8
sp 2
C.c点溶液中: (不考虑水的电离因素)
D.e点浊液中加入 固体,阳离子 沿 向d点移
11.(2024·湖北省鄂东南省级示范高中教学改革联盟高三联考)25℃时,用 溶液分别滴定弱酸
、CuSO 、FeSO 三种溶液, 随 变化关系如图所示[p表示负对数,M表示 、 、
4 4
等],已知 ,下列有关分析正确的是( )
A.①代表滴定 溶液的变化关系
B.①与③直线交点对应的pH=3.4
C.调整溶液的pH=5,可使工业废水中的 沉淀完全
D.Fe(OH) 固体比Cu(OH) 固体难溶解于 溶液
2 2
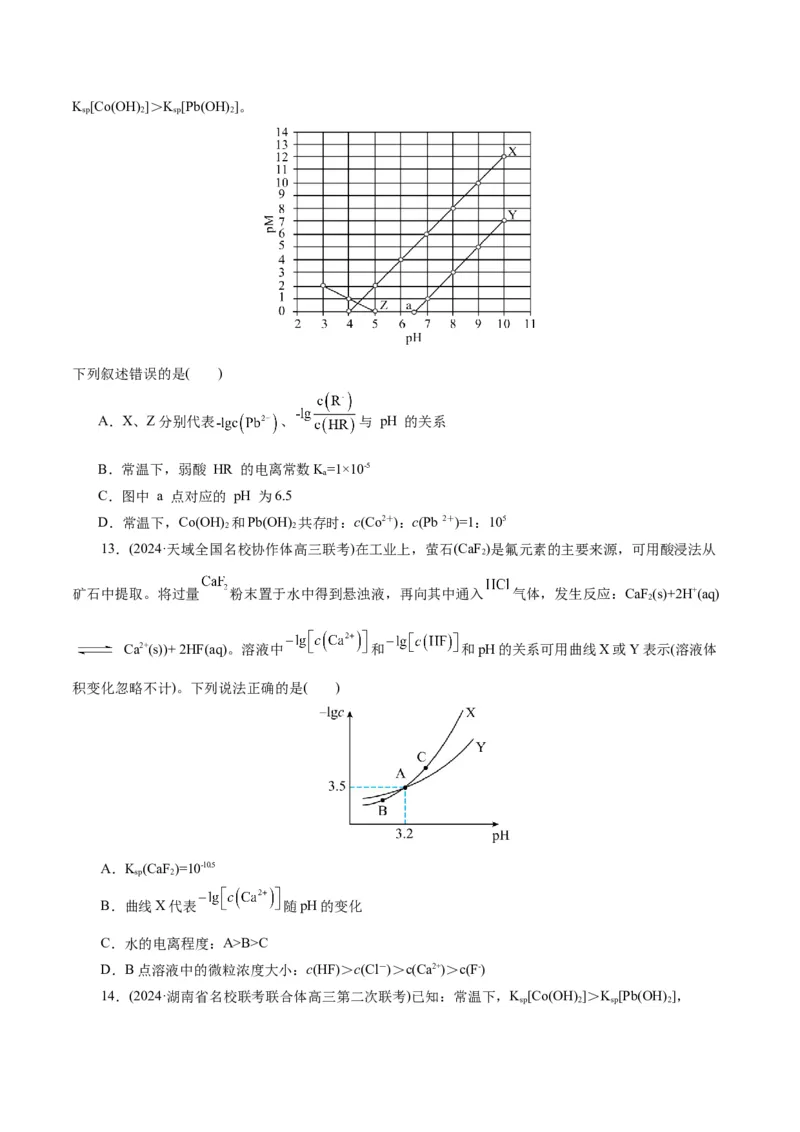
12.(2024·河南省部分名校高三联考)常温下,向Co(NO )、Pb(NO ) 和 HR 的混合液中滴加 NaOH
3 2 3 2
溶液,pM 与 pH 的关系如图所示。已知:pM=-lgc(M),c(M)代表c(Co2+)、c(Pb 2+)或 ,K [Co(OH) ]>K [Pb(OH) ]。
sp 2 sp 2
下列叙述错误的是( )
A.X、Z分别代表 、 与 pH 的关系
B.常温下,弱酸 HR 的电离常数K=1×10-5
a
C.图中 a 点对应的 pH 为6.5
D.常温下,Co(OH) 和Pb(OH) 共存时:c(Co2+):c(Pb 2+)=1:105
2 2
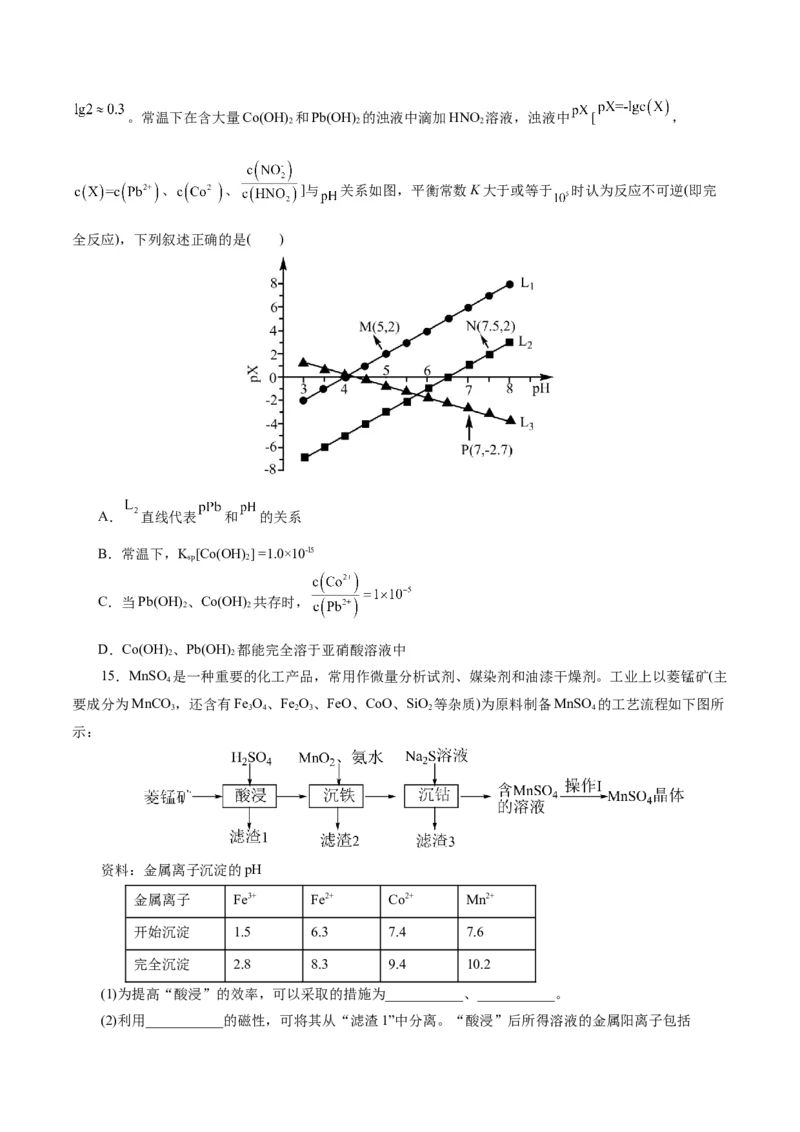
13.(2024·天域全国名校协作体高三联考)在工业上,萤石(CaF )是氟元素的主要来源,可用酸浸法从
2
矿石中提取。将过量 粉末置于水中得到悬浊液,再向其中通入 气体,发生反应:CaF (s)+2H+(aq)
2
Ca2+(s))+ 2HF(aq)。溶液中 和 和pH的关系可用曲线X或Y表示(溶液体
积变化忽略不计)。下列说法正确的是( )
A.K (CaF )=10-10.5
sp 2
B.曲线X代表 随pH的变化
C.水的电离程度:A>B>C
D.B点溶液中的微粒浓度大小:c(HF)>c(Cl-)>c(Ca2+)>c(F-)
14.(2024·湖南省名校联考联合体高三第二次联考)已知:常温下,K [Co(OH) ]>K [Pb(OH) ],
sp 2 sp 2。常温下在含大量Co(OH) 和Pb(OH) 的浊液中滴加HNO 溶液,浊液中 [ ,
2 2 2
、 、 ]与 关系如图,平衡常数K大于或等于 时认为反应不可逆(即完
全反应),下列叙述正确的是( )
A. 直线代表 和 的关系
B.常温下,K [Co(OH) ] =1.0×10-15
sp 2
C.当Pb(OH) 、Co(OH) 共存时,
2 2
D.Co(OH) 、Pb(OH) 都能完全溶于亚硝酸溶液中
2 2
15.MnSO 是一种重要的化工产品,常用作微量分析试剂、媒染剂和油漆干燥剂。工业上以菱锰矿(主
4
要成分为MnCO ,还含有Fe O、Fe O、FeO、CoO、SiO 等杂质)为原料制备MnSO 的工艺流程如下图所
3 3 4 2 3 2 4
示:
资料:金属离子沉淀的pH
金属离子 Fe3+ Fe2+ Co2+ Mn2+
开始沉淀 1.5 6.3 7.4 7.6
完全沉淀 2.8 8.3 9.4 10.2
(1)为提高“酸浸”的效率,可以采取的措施为___________、___________。
(2)利用___________的磁性,可将其从“滤渣1”中分离。“酸浸”后所得溶液的金属阳离子包括Mn2+、Co2+、___________、___________。
(3)“沉铁”过程中,先加MnO 充分反应后再加氨水。则加MnO 时发生反应的离子方程式为
2 2
___________。
(4)“沉钴”中,不能用NaOH代替含硫沉淀剂,原因是___________。
(5)已知K (MnS)= 2.5×10-13,K (CoS)= 4.0×10-21,“沉铁”后溶液中c(Mn2+)=2 mol·L-1,当金属阳离
sp sp
子浓度小于1.0×10-5 mol·L-1时沉淀完全,此时“滤渣3”中是否含有MnS沉淀?__(列式计算)。
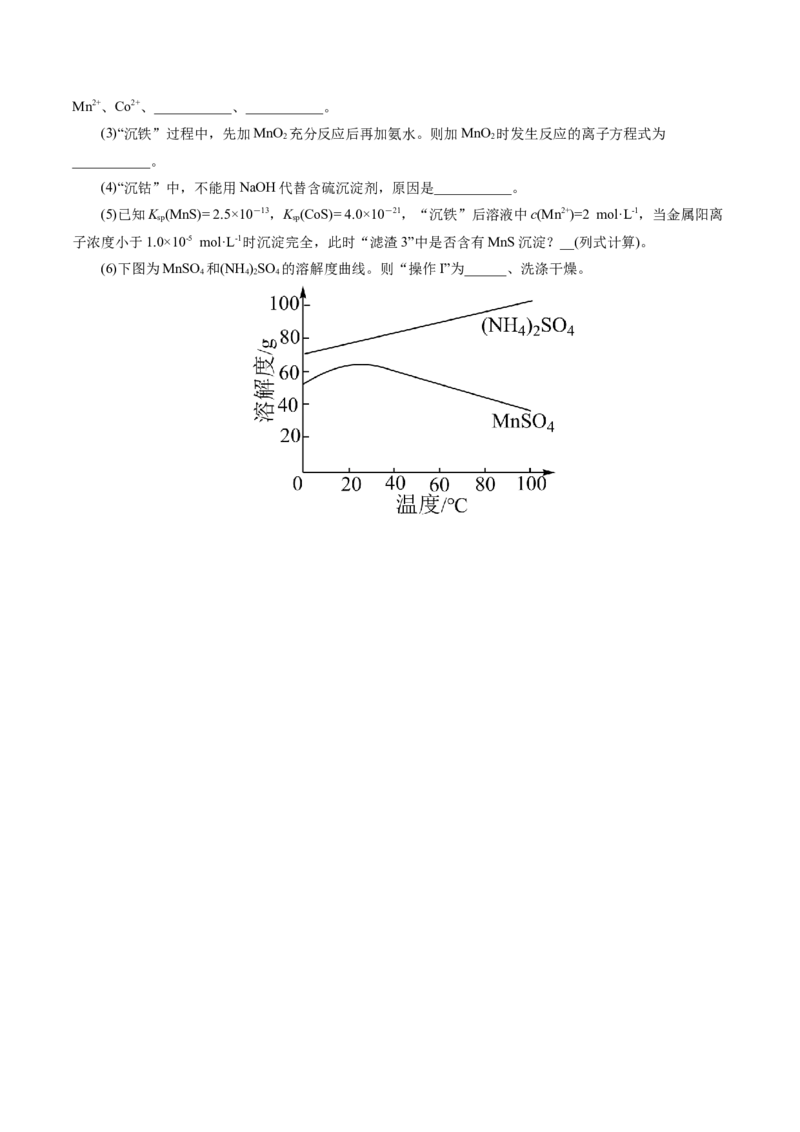
(6)下图为MnSO 和(NH )SO 的溶解度曲线。则“操作I”为______、洗涤干燥。
4 4 2 4