文档内容
专题 08 水溶液中的离子反应与平衡
目录
01 模拟基础练
【题型一】电离平衡、水解平衡、沉淀溶解平衡及其应用
【题型一】电离常数、水解常数、溶度积常数的综合应用
【题型一】中和滴定及其拓展应用
02 重难创新练
03 真题实战练
题型一 电离平衡、水解平衡、沉淀溶解平衡及其应用
1.已知25 ℃时有关弱酸的电离平衡常数如下表:
弱酸化学式 HX HY HCO
2 3
K =4.4×10-7
1
电离平衡常数/mol·L-1 7.8×10-9 3.7×10-15
K =4.7×10-11
2
下列推断正确的是( )
A.HX、HY两种弱酸的酸性:HX>HY
B.相同条件下溶液的碱性:NaX>NaCO>NaY>NaHCO
2 3 3
C.结合H+的能力:CO>Y->X->HCO
D.HX和HY酸性相同,都比HCO 弱
2 3
【答案】A
【解析】根据电离平衡常数可知酸性:HCO >HX>HCO>HY,则结合H+的能力:Y->CO>X->
2 3
HCO,故A正确、C、D错误;酸越弱,其对应的盐的水解能力越强,故相同条件下溶液的碱性:NaY>
NaCO>NaX>NaHCO ,故B错误。
2 3 3
2.根据下表提供的数据,判断下列离子方程式或化学方程式正确的是( )
化学式 电离常数
HClO K=3×10-8
HCO K =4×10-7 K =6×10-11
2 3 a1 a2
A.向NaCO 溶液中滴加少量氯水:CO+2Cl+HO===2Cl-+2HClO+CO↑
2 3 2 2 2
B.向NaHCO 溶液中滴加少量氯水:2HCO+Cl===Cl-+ClO-+2CO↑+HO
3 2 2 2
C.向NaClO溶液中通入少量CO:CO+NaClO+HO===NaHCO+HClO
2 2 2 3D.向NaClO溶液中通入过量CO:CO+2NaClO+HO===Na CO+2HclO
2 2 2 2 3
【答案】C
【解析】HClO的电离常数小于HCO 的第一步电离,向NaCO 溶液中滴加少量氯水,不能生成二氧
2 3 2 3
化碳,应该生成碳酸氢根,A项错误;向NaHCO 溶液中滴加少量氯水,氯水中的氯化氢和碳酸氢钠反应
3
生成氯化钠、二氧化碳和水,次氯酸不能和碳酸氢钠反应,产物应为次氯酸,B项错误;向NaClO溶液中
通入过量CO,反应生成碳酸氢钠和次氯酸,D项错误。
2
3.甲胺[(CH )NH ·H O]在水中电离与氨相似,常温下,K [(CH )NH ·H O]=2.0×10-5。已知lg2=0.3。下
3 2 2 b 3 2 2
列说法错误的是( )
A.(CH)NH NO 溶液显酸性
3 3 3
B.甲胺溶液中c(OH-)随温度升高而增大
C.常温下,0.1mol/L的甲胺溶液的pH=11.3
D.0.1mol/L(CH )NH Cl溶液中离子浓度大小关系为:c(Cl-)>c[(CH )NH )+]>c(H+)>c(OH-)
3 3 3 3
【答案】C
【解析】A项,(CH)NH NO 为强酸弱碱盐,其溶液显酸性,A项正确;B项,温度升高,促进甲胺
3 3 3
电离,溶液中c(OH-)增大,B项正确;C项,0.1mol/L的甲胺溶液中,
, ,
,C项错误;D项,由于(CH)NH )+水解,溶液显酸性,故有:
3 3
c(Cl-)>c[(CH )NH )+]>c(H+)>c(OH-),D项正确。故选C。
3 3
4.(2024·江苏常州高三期中)室温下,通过下列实验探究NaHCO 、NaCO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1mol•L-1NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1mol•L-1NaHCO 溶液与0.1mol•L-1CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:饱和NaCO 溶液中通入CO 产生白色沉淀,溶液pH从12下降到约为9
2 3 2
实验4:0.1mol•L-1NaHCO 溶液中滴加新制饱和氯水,氯水颜色褪去并有气泡
3
下列说法正确的是( )
A.由实验1可得出:K (H CO)∙K (H CO)<10-16
a1 2 3 a2 2 3
B.实验2中两溶液混合时有:K (CaCO)>2.5×10-3
sp 3
C.实验3中发生反应的离子方程式为CO2-+H O+CO=2 HCO -
3 2 2 3D.实验4所得溶液中c(Na+)=c(HCO -)+c(CO2-)+c(H CO)
3 3 2 3
【答案】A
【解析】A项,实验1中,K (H CO)∙K (H CO)= ∙ =
a1 2 3 a2 2 3
,0.1mol•L-1NaHCO 溶液的pH约为8,表明溶液中HCO -水解是主要的,电离是次要的,c(CO2-)<
3 3 3
c(H CO),所以 <c2(H+)=10-16,A正确;B项,实验2中两溶液混合时,c(Ca2+)=0.05
2 3
mol•L-1,c(HCO -)<0.05 mol•L-1,则有:K (CaCO)=c(Ca2+)∙c(HCO -)=(0.05 mol•L-1)∙(<0.05 mol•L-1)<
3 sp 3 3
2.5×10-3,B不正确;C项,实验3中发生反应的离子方程式为2Na++ CO2-+H O+CO=2NaHCO↓,C不正
3 2 2 3
确;D项,实验4中,0.1mol•L-1NaHCO 溶液中滴加新制饱和氯水,氯水颜色褪去并有气泡,则有一部分
3
HCO 发生分解,生成CO,所得溶液中c(Na+)=c(HCO -)+c(CO2-)+c(H CO)+ c(CO),则c(Na+)>c(HCO -)
2 3 2 3 3 2 3 2 3
+c(CO2-)+c(H CO),D不正确;故选A。
3 2 3
5.工业上用化学法除锅炉的水垢时,先向锅炉中注入饱和NaCO 溶液浸泡,将水垢中的CaSO 转化
2 3 4
为CaCO ,再用盐酸除去[已知:K (CaCO)=1×10-10,K (CaSO)=9×10-6]。下列说法不正确的是( )
3 sp 3 sp 4
A.温度升高,NaCO 溶液的K 和c(OH-)均会增大
2 3 w
B.沉淀转化的离子方程式为CO(aq)+CaSO(s) CaCO (s)+SO(aq)
4 3
C.该条件下,CaCO 的溶解度小于CaSO
3 4
D.CaCO 和CaSO 共存的悬浊液中,c(SO 2-)/c(CO 2-)=1 105
3 4 4 3
【答案】D
【解析】A项,水电离、盐水解都吸热,温度升高,NaCO 溶液的K 和c(OH-)均会增大,故A正确;
2 3 w
B项,加入碳酸钠溶液,把硫酸钙转化为碳酸钙:CO+CaSO CaCO +SO 2-,故B正确;C项,该
4 3 4
条件下,设溶液为1L,由c(CO2-)=c(Ca2+)= =10-5 mol·L-1,则 =
3
=1 10-4g,CaCO 的溶解度约为1×10-4,显然,CaCO 的溶解度小于CaSO,故C正确;D项,CaCO 和
3 3 4 3
CaSO 共存的悬浊液中, =9 104,故D错误;故选D。
46.室温下,通过下列实验探究有关AgNO 的性质[已知: ]。
3
实验1:向 0.1mol·L-1的AgNO 溶液中滴加 0.1mol·L-1的NaCl溶液,产生白色沉淀,过滤,
3
实验2:向实验1所得滤液中滴加 0.1mol·L-1 溶液,产生淡黄色沉淀,过滤。
实验3:向实验2所得滤液中逐滴滴加氨水,产生沉淀先变多后变少,直至消失。
下列说法正确的是( )
A.实验1过滤后滤液中c(Ag+)=10-4.9mol·L-1
B.通过实验1和实验2可得出
C.实验2所得滤液中c(Ag+)+c(H+)=c(Cl-)+c(Br-)+ c(OH-)
D.实验3滴加氨水过程中,c(Ag+)一直减小
【答案】D
【解析】A项, 向10mL0.1mol/L的AgNO 溶液中滴加1mL0.1mol/L的NaCl溶液,发生反应
3
AgNO+NaCl=AgCl↓+NaNO ,反应后AgNO 过量,过滤后所得滤液中c(Ag+)=
3 3 3
=0.082mol/L,A项错误;B项,实验1所得滤液中含过量的AgNO、
3
NaNO 和饱和AgCl,滴加1mL0.1mol/LNaBr溶液,AgNO 直接与NaBr发生沉淀反应生成淡黄色的AgBr
3 3
沉淀,不能说明发生了沉淀的转化,不能比较AgCl、AgBr的K ,B项错误;C项,实验2中发生的反应
sp
为AgNO+NaBr=AgBr↓+NaNO ,反应后AgNO 仍然过量,过滤所得滤液中含过量的AgNO、NaNO 、饱
3 3 3 3 3
和AgCl和AgBr,滤液中NO -物质的量为0.1mol/L×0.01L=0.001mol、Na+物质的量为0.1mol/
3
L×0.001L+0.1mol/L×0.001L=0.0002mol,溶液中的电荷守恒为c(Ag+)+c(H+)+c(Na+)=c(Cl-)+c(Br-)+c(NO -)
3
+c(OH-),C项错误;D项,向实验2所得滤液中逐滴滴加氨水,随着氨水的滴入,依次发生反应:
AgNO+NH∙HO=AgOH↓+NH NO 、AgOH+2NH∙HO=[Ag(NH)]OH+2H O,故产生沉淀先变多后变少,
3 3 2 4 3 3 2 3 2 2
直至消失,c(Ag+)一直减小,D项正确;故选D。
7.已知K、K、K 、K 、K 分别表示化学平衡常数、弱酸的电离平衡常数、水的离子积常数、盐的
a w h sp
水解平衡常数、难溶电解质的溶度积常数。
(1)有关上述常数的说法正确的是________。
a.它们都能反映一定条件下对应变化进行的程度
b.它们的大小都随温度的升高而增大
c.常温下,CHCOOH在水中的K 大于在饱和CHCOONa溶液中的K
3 a 3 a
d.一定温度下,在CHCOONa溶液中,K =K·K
3 w a h
(2)25 ℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合所得溶液中c(NH)=c(Cl-),则溶液显________(填“酸”、“碱”或“中”)性;用含a的代数式表示NH ·H O的电离平衡常数K =
3 2 b
________。
(3)25 ℃时,HSO HSO+H+的电离常数K=1×10-2 mol·L-1,则该温度下pH=3、c(HSO)=
2 3 a
0.1 mol·L-1的NaHSO 溶液中c(H SO )=________。
3 2 3
(4)已知常温下Fe(OH) 和Mg(OH) 的K 分别为8.0×10-38、1.0×10-11,向浓度均为0.1 mol/L的FeCl 、
3 2 sp 3
MgCl 的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液pH的范围是________。
2
(已知lg 2=0.3)
【答案】(1)ad (2)中 (3)0.01 mol/L (4)[3.3,9]
【解析】(1)对于正反应为放热反应的化学平衡,升高温度,平衡逆向移动,平衡常数减小,b选项错
误;温度不变,CHCOOH的电离平衡常数不变,c选项错误。(2)根据电荷守恒得c(H+)+c(NH)=c(Cl-)+
3
c(OH-),因为c(NH)=c(Cl-),所以c(H+)=c(OH-),故溶液显中性。K = ==。(3)由
b
,代入数据得c(H SO )=0.01 mol/L。(4)K [Fe(OH) ]=c(Fe3+)·c3(OH-),Fe3+完全沉淀
2 3 sp 3
时c3(OH-)=,得c(OH-)=2×10-11 mol/L,pH=3.3,Mg(OH) 开始沉淀时c2(OH-)==1.0×10-10,得c(OH
2
-)=1×10-5 mol/L,pH=9,调节pH范围为[3.3,9]。
题型二 电离常数、水解常数、溶度积常数的综合应用
8.(2024·江苏淮安市5校高三联考)室温下: K (H C O)=5×10 -2,K (H C O)=1×10-4,
a1 2 2 4 a2 2 2 4
Ksp(CaC O)=2.5×10 -9。通过下列实验探究某些草酸盐的性质。
2 4
实验①:用pH计测得 0.10mol/L K C O 溶液的 pH=8
2 2 4
实验②:向0.10mol/LKHC O 溶液中滴入少量酸性高锰酸钾溶液,振荡后溶液紫色褪去
2 4
实验③:向0.10mol/L KHC O 溶液加入一定体积的等浓度CaCl 溶液产生白色沉淀,测得上层清液
2 4 2
pH=4, (Ca2+)=10-4mol/L
实验④:向0.10mol/L K C O 溶液中滴加一定浓度的稀盐酸后,混合溶液的 pH=7,下列说法正确的
2 2 4
是( )
A.实验①溶液中: =2×10-3
B.实验②说明 KHC O 溶液具有漂白性
2 4
C.实验③所得上层清液中的c(HC O-)=2.5×10-5mol/L
2 4
D.实验④反应所得溶液中存在:c(K+)=2c(C O2-)+c(HC O-)
2 4 2 4
【答案】C
【解析】A项,0.100mol•L-1KC O 溶液的pH=8,c(H+)=10-8mol•L-1,K (H C O)•K (H C O)==5×10-
2 2 4 a1 2 2 4 a2 2 2 42×1×10-4=5×10-6, = =2×10-11,A错误;B项,向0.10mol•L-1KHC O 溶液中滴入少量酸性
2 4
高锰酸钾溶液,振荡后溶液紫色褪去,高锰酸钾与KHC O 发生氧化还原反应,体现KHC O 具有还原性,
2 4 2 4
B错误;C项,向0.10mol•L-1KHC O 溶液加入一定体积的等浓度CaCl 溶液产生白色沉淀,测得上层清液
2 4 2
pH=4,c(Ca2+)=10-4mol•L-1,则c(C O2-)=2.5×10-5mol•L-1,K (H C O)= 1×10-4,解得c(HC O-)=2.5×10-
2 4 a2 2 2 4 2 4
5mol•L-1,C正确;D项,向0.10mol•L-1KC O 溶液中滴加一定浓度的稀盐酸后,由电荷守恒可知c(K+)
2 2 4
+c(H+)=2c(C O2-)+c(HC O-)+c(Cl-)+c(OH-),混合溶液的pH=7,则c(H+)=c(OH-),则c(K+)=2c(C O2-)
2 4 2 4 2 4
+c(HC O-)+c(Cl-),D错误;故选C。
2 4
9.(2024·辽宁沈阳高三期中)SO 是引发酸雨的主要污染物,将工业废气中的 吸收能有效减少对大
2
气的污染、并实现资源化利用。下列离子方程式正确的是( )
已知常温下亚硫酸的电离平衡常数(K =1.3×10-2,K =6.3×10-8)碳酸的电离平衡常数(K =4.3×10-7,
a1 a2 a1
K =5.6×10-11)
a2
A.硫酸型酸雨露置于空气中一段时间后溶液酸性增强:HSO +O =2H++SO2-
2 3 2 4
B.用过量Ca(ClO) 溶液吸收废气中的SO : Ca2++ClO- +SO+H O= CaSO↓+ Cl-+2H+
2 2 2 2 4
C.用过量氨水吸收废气中的SO : NH ·H O +SO=NH++HSO -
2 3 2 2 4 3
D.用过量NaCO 溶液吸收废气中的SO : 2CO2- +SO+H O=SO 2-+HCO-
2 3 2 3 2 2 3 3
【答案】D
【解析】A项,硫酸型酸雨露置于空气中一段时间后溶液酸性增强:2HSO +O H++2SO2-,A错误;B
2 3 4 4
项,用过量Ca(ClO) 溶液吸收废气中的SO 发生反应的离子方程式为Ca2++3ClO- +SO+H O= CaSO↓+ Cl-
2 2 2 2 4
+2HClO,B错误;C项,用过量氨水吸收废气中的SO 发生反应的离子方程式为2NH ·H O +SO=2NH+
2 3 2 2 4
+SO2-+H O,C错误;D项,用过量NaCO 溶液吸收废气中的SO 发生反应的离子方程式为2CO2-
3 2 2 3 2 3
+SO+H O=SO 2-+HCO-,D正确;故选D。
2 2 3 3
10.(2025·浙江省第二届辛愉杯高三线上模拟考试)氢硫酸(H S)是二元弱酸,常温下,某同学做了如下
2
三组实验:
实验I:向20mL0.1mol·L-1NaHS溶液中滴加0.1mol·L-1 ZnCl 溶液
2
实验II:向20mL0.1mol·L-1NaHS溶液中滴加0.1mol·L-1 HCl溶液
实验III:向20mL0.1mol·L-1HS溶液中滴加0.1mol·L-1 CuSO 溶液
2 4
已知:HS的电离平衡常数K =1.1×10-7,K =1.3×10-13,K (ZnS)= 1.6×10-24,K (CuS)= 6.3×10-36。忽
2 a1 a2 sp sp
略溶液混合后体积变化。
下列说法不正确的是( )A.实验I中ZnCl 溶液体积为60mL时,溶液中c(S2-)=3.2×10-23mol·L-1
2
B.实验I中ZnCl 溶液体积小于00mL时,会发生反应2HS-+Zn2+=ZnS↓+H S↑
2 2
C.实验II不可以选用甲基橙作为指示剂
D.实验III中CuSO 溶液体积为20mL时,溶液pH等于1
4
【答案】C
【 解 析 】 A 项 , 加 入 ZnCl 溶 液 体 积 为 60mL 时 ,
2
,
,A正确;B项,由于开始滴加的ZnCl 量较少而NaHS
2
过量,因此该反应在初始阶段发生的是2HS-+Zn2+=ZnS↓+H S↑,B正确;C项,实验II发生的反应:HS-
2
+H+= H S↑,若恰好完全反应溶液中溶质是氯化钠,若盐酸过量时,因甲基橙变色范围是3.1(红)~4.4(黄),
2
可以选用甲基橙作为指示剂,C错误;D项,实验III中向20mL0.1mol·L-1HS溶液中滴加0.1mol·L-1 CuSO
2 4
溶 液 , CuSO 溶 液 体 积 为 20mL 时 , HS+CuSO = CuS↓+H SO ,
4 2 4 2 4
, ,溶液pH等于1,D
正确; 故选C。
11.(2025·浙江省名校协作体高三联考)氢硫酸(H S)是二元弱酸,常温下,某同学做了如下三组实验:
2
实验I:向20mL0.1mol·L-1NaHS溶液中滴加0.1mol·L-1 ZnCl 溶液
2
实验II:向20mL0.1mol·L-1NaHS溶液中滴加0.1mol·L-1 HCl溶液
实验III:向20mL0.1mol·L-1HS溶液中滴加0.1mol·L-1 CuSO 溶液
2 4
已知:HS的电离平衡常数K =1.1×10-7,K =1.3×10-13,K (ZnS)= 1.6×10-24,K (CuS)= 6.3×10-36。
2 a1 a2 sp sp
忽略溶液混合后体积变化。
下列说法不正确的是( )
A.实验I中ZnCl 溶液体积为60mL时,溶液中c(S2-)=3.2×10-23mol·L-1
2
B.实验I中ZnCl 溶液体积小于10mL时,会发生反应Zn2++2HS-=ZnS↓+H S↑
2 2
C.实验II不可以选用甲基橙作为指示剂D.实验III中CuSO 溶液体积为20mL时,溶液 等于1
4
【答案】C
【解析】A项,加入ZnCl 溶液体积为60 mL时,
2
,
,A正确;B项,由于开始滴加的ZnCl 量较少而NaHS
2
过量,因此该反应在初始阶段发生的是Zn2++2HS-=ZnS↓+H S↑,B正确;C项,实验II发生的反应:H+
2
+HS-=HS↑,若恰好完全反应溶液中溶质是氯化钠,若盐酸过量时,因甲基橙变色范围是3.1(红)~4.4(黄),
2
可以选用甲基橙作为指示剂,C错误;D项,实验III中向20mL0.1mol·L-1HS溶液中滴加0.1mol·L-1 CuSO
2 4
溶液,CuSO 溶液体积为20mL时,CuSO +H S= CuS↓+H SO ,
4 4 2 2 4
,c(H+)=2×0.05mol·L-1 =0.1mol·L-1,溶液pH等于1,D正
确;故选C。
12.常温下,向20mL0.1mol/LNaHCO 溶液中再加入少量的NaHCO 固体,一段时间后,少量气体X
3 3
从溶液底部固体中缓慢逸出,最终固体全部溶解,得到溶液Y,pH值为8.7。
已知:K (CaCO)=4.96×10-9 K (MgCO )=6.82×10-6,K [Mg(OH) ]=1.8×10-11
sp 3 sp 3 sp 2
HCO:pK =6.3、pK =10.3;Mg(OH) 沉淀范围:pH9.4~12.4。
2 3 a1 a2 2
下列说法正确的是( )
A.X气体是CO,饱和NaHCO 溶液的
2 3
B.因为K (MgCO )>K [Mg(OH) ],Mg(OH) 更难溶
sp 3 sp 2 2
C.向溶液Y中滴加MgCl 溶液,有Mg(OH) 生成
2 2
D.向0.1mol/L NaHCO 溶液中加入MgCl 溶液,无明显现象,但改为同浓度的CaCl 溶液,可生成沉
3 2 2
淀。
【答案】D
【解析】A项,在NaHCO 3 溶液中既存在水解平衡HCO 3 -+H 2 O⇌H 2 CO 3 +OH-、又存在电离平衡HCO 3 - ⇌H++ CO 2-,HCO -的水解平衡常数K = = =10-7.7>10-10.3,NaHCO 溶液呈碱性,向其中加入少量
3 3 h 3
NaHCO 固体,上述平衡正向移动,生成的HCO 分解产生少量气体CO ,即X气体是CO ,同时有CO2-
3 2 3 2 2 3
生成,即溶液Y中含CO2-,由HCO 的K 、K 可知CO2-的水解能力大于HCO -,溶液Y的pH为8.7,
3 2 3 a1 a2 3 3
则饱和NaHCO 溶液的pH<8.7,A项错误;B项,MgCO 、Mg(OH) 不属于同类型的难溶电解质,不能直
3 3 2
接由 K 的大小判断溶解度的大小,K (MgCO )=6.82×10-6,饱和 MgCO 溶液的浓度 c(MgCO )=
sp sp 3 3 3
= mol/L= ×10-3mol/L,K [Mg(OH) ]=1.8×10-11,饱和 Mg(OH) 溶液的浓度
sp 2 2
c[Mg(OH) ]= = mol/L= ×10-4mol/L< ×10-3mol/L,Mg(OH) 更难溶,B
2 2
项错误;C项,Mg(OH) 沉淀的范围:pH9.4~12.4,即pH=9.4时Mg2+开始形成Mg(OH) 沉淀,Y溶液的
2 2
pH为8.7,故向溶液Y中滴加MgCl 溶液,没有Mg(OH) 生成,C项错误;D项,NaHCO 溶液中存在平
2 2 3
衡 HCO
3
- ⇌H++ CO
3
2-,由于 K
sp
(CaCO
3
) <K
sp
(MgCO
3
),说明 Ca2+结合 CO
3
2-的能力比 Mg2+强,故
向0.1mol/LNaHCO 溶液中加入MgCl 溶液,无明显现象,但改为同浓度的CaCl 溶液,可生成沉淀,D项
3 2 2
正确;故选D。
13.草酸钙是常见的难溶物。将过量草酸钙粉末置于水中达到溶解平衡:CaC O (s) Ca2+ (aq)
2 4
+ C O2- (aq)[已知 K (CaC O)=2.3×10-9,K(CHCOOH)=1.75×10-5,HC O 的电离常数 K =5.6×10-2,
2 4 sp 2 4 a 3 2 2 4 a1
K =1.5×10-4,下列有关说法不正确的是( )
a2
A.上层清液中含碳微粒最主要以C O2-形式存在
2 4
B.上层清液中存在:c(Ca2+)=c(C O2-)+c(HC O-)+c(H C O)
2 4 2 4 2 2 4
C.HC O 加入CaCl 溶液时,加入适量醋酸钠粉末,有利于生成CaC O 沉淀
2 2 4 2 2 4
D.向上层清液中通入 至pH=1,则:2c(Ca2+)-2c(C O2-)-c(HC O-)- c(OH―)= 0.1mol·L-1
2 4 2 4
【答案】D
【解析】A项,溶解在水中的草酸钙电离出草酸根离子,草酸根离子能水解,但程度很小,故含碳的
微粒最主要的是草酸根离子,A正确;B项,根据物料守恒钙原子和碳原子物质的量浓度相等,故有
c(Ca2+)=c(C O2-)+c(HC O-)+c(H C O),B正确;C项,草酸加入氯化钙中反应生成草酸钙,加入醋酸钠粉
2 4 2 4 2 2 4
末,根据电离平衡常数分析,醋酸根离子水解程度大于草酸根离子,故醋酸钠的碱性抑制草酸根离子水解,
有利于生成草酸钙,C正确;D项,向上层清液中通入HCl至pH=1,则有电荷守恒:2c(Ca2+)+c(H+)=2c(C O2-)+c(HC O-)+c(OH―)+c(Cl-),根据氢离子浓度为0.1mol/L分析,2c(Ca2+)-2c(C O2-)-c(HC O-)-
2 4 2 4 2 4 2 4
c(OH―)=c(Cl-)-c(H+),不能确定氯离子浓度,故D错误;故选D。
14.HS是常见的二元弱酸(电离常数K (H S)=1.1×10-7,K (H S)=1.3×10-13)。氢氧化铁[K = 2.8×10-
2 a1 2 a2 2 sp
39]、氢氧化锌[K = 3.0×10-17]均为难溶多元弱碱,硫化锌[K = 1.6×10-24]为难溶盐。所有数据均为25℃的值。
sp sp
下列有关说法不正确的是( )
A.因为HS的K >>K ,所以c(S2-)≈K =1.3×10-13mol/L
2 a1 a2 a2
B.Fe(OH) 饱和溶液中的c(Fe3+)≈1×10-10mol/L
3
C.分别向等体积等浓度的(CHCOO) Zn、ZnSO 溶液中通入等物质的量的HS沉淀ZnS后,前者
3 2 4 2
c(Zn2+)更小
D.pH=13的NaS溶液与相同物质的量的ZnSO 反应,只沉淀ZnS
2 4
【答案】D
【解析】A项,HS在水溶液中的电离方程式为:HS H++HS-、HS H++S2-,K =
2 2 a1
,K = ,因为HS的K >>K ,可以任务c(H+)≈c(HS-),所以c(S2-)≈K =1.3×10-
a2 2 a1 a2 a2
13mol/L,故A正确;B项,Fe(OH) 溶于水所得饱和溶液中存在平衡:Fe(OH) Fe3++3OH-,设
3 3
c(Fe3+)=amol/L,则c(OH-)=3amol/L,K [Fe(OH) ]=c(Fe3+)c3(OH-)=a×(3a)3=2.8×10-39,解得a 1×10-10mol/L,
sp 3
故B正确;C项,(CHCOO) Zn是强碱弱酸盐,其水溶液呈碱性,抑制HS的电离,c(S2-)更大,沉淀
3 2 2
Zn2+更加彻底,c(Zn2+)更小,故C正确;D项,氢氧化锌的K = 3.0×10-17,则当0.1mol/L的ZnSO 溶液中
sp 4
Zn2+开始沉淀时,c(OH-)= ,pH=
,则pH=13的NaS溶液与相同物质的量的ZnSO 反应,除了
2 4
沉淀ZnS还会生成Zn(OH) ,故D错误;故选D。
2
15.常温下,向20mL0.1mol/LNaHCO 溶液中再加入少量的NaHCO 固体,一段时间后,少量气体X
3 3
从溶液底部固体中缓慢逸出,最终固体全部溶解,得到溶液Y,pH值为8.7。
已知:K (CaCO)=4.96×10-9 K (MgCO )=6.82×10-6,K [Mg(OH) ]=1.8×10-11
sp 3 sp 3 sp 2
HCO:pK =6.3、pK =10.3;Mg(OH) 沉淀范围:pH9.4~12.4。
2 3 a1 a2 2下列说法正确的是( )
A.X气体是CO,饱和NaHCO 溶液的
2 3
B.因为K (MgCO )>K [Mg(OH) ],Mg(OH) 更难溶
sp 3 sp 2 2
C.向溶液Y中滴加MgCl 溶液,有Mg(OH) 生成
2 2
D.向0.1mol/L NaHCO 溶液中加入MgCl 溶液,无明显现象,但改为同浓度的CaCl 溶液,可生成沉
3 2 2
淀。
【答案】D
【解析】A项,在NaHCO 3 溶液中既存在水解平衡HCO 3 -+H 2 O⇌H 2 CO 3 +OH-、又存在电离平衡HCO 3 - ⇌
H++ CO2-,HCO -的水解平衡常数K = = =10-7.7>10-10.3,NaHCO 溶液呈碱性,向其中加入少量
3 3 h 3
NaHCO 固体,上述平衡正向移动,生成的HCO 分解产生少量气体CO,即X气体是CO,同时有CO2-
3 2 3 2 2 3
生成,即溶液Y中含CO2-,由HCO 的K 、K 可知CO2-的水解能力大于HCO -,溶液Y的pH为8.7,
3 2 3 a1 a2 3 3
则饱和NaHCO 溶液的pH<8.7,A项错误;B项,MgCO 、Mg(OH) 不属于同类型的难溶电解质,不能直
3 3 2
接由K 的大小判断溶解度的大小,K (MgCO )=6.82×10-6,饱和MgCO 溶液的浓度c(MgCO )=
sp sp 3 3 3
= mol/L= ×10-3mol/L,K [Mg(OH) ]=1.8×10-11,饱和Mg(OH) 溶液的浓度
sp 2 2
c[Mg(OH) ]= = mol/L= ×10-4mol/L< ×10-3mol/L,Mg(OH) 更难溶,B
2 2
项错误;C项,Mg(OH) 沉淀的范围:pH9.4~12.4,即pH=9.4时Mg2+开始形成Mg(OH) 沉淀,Y溶液的
2 2
pH为8.7,故向溶液Y中滴加MgCl 溶液,没有Mg(OH) 生成,C项错误;D项,NaHCO 溶液中存在平
2 2 3
衡HCO
3
- ⇌H++ CO
3
2-,由于K
sp
(CaCO
3
) <K
sp
(MgCO
3
),说明Ca2+结合CO
3
2-的能力比Mg2+强,故
向0.1mol/LNaHCO 溶液中加入MgCl 溶液,无明显现象,但改为同浓度的CaCl 溶液,可生成沉淀,D项
3 2 2
正确;故选D。
16.(2024·江苏淮安高三开学考试)室温下,用FeSO 溶液制备FeCO 的过程如图所示。已知:
4 3
K(NH ·H O)=1.8×10-5,K (H CO)=4.5×10-7,K (H CO)=4.7×10-11,K [Fe(OH) ]=8.0×10-16,
b 3 2 a1 2 3 a2 2 3 sp 2
K (FeCO)=3.1×10-11。下列说法正确的是( )
sp 3A.0.1 mol·L-1NH HCO 溶液中:c(NH ·H O)>c(H CO)
4 3 3 2 2 3
B.(NH )SO 溶液中:c(H+)=2 c(NH ·H O)+ c(OH―)
4 2 4 3 2
C.制备FeCO 的离子方程式为:Fe2++ NH ·H O +HCO-=FeCO ↓+NH++H O
3 3 2 3 3 4 2
D.c(Fe2+)=0.08mol·L-1时,应控制
【答案】C
【解析】A项,由于NH +的水解常数 5.56 10-10,HCO -的水解常数
4 3
10-8,所以HCO -的水解程度比NH +的水解程度大,c(NH ·H O)<c(H CO),
3 4 3 2 2 3
故A错误;B项,(NH )SO 为强酸弱碱盐,溶液中根据质子守恒可知:c(H+)= c(NH ·H O)+ c(OH―),故
4 2 4 3 2
B错误;C项,HCO -与NH ·H O反应产生的CO2-再与Fe2+结合生成FeCO,反应的离子方程式为:Fe2++
3 3 2 3 3
NH ·H O +HCO-=FeCO ↓+NH++H O,故C正确;D项,当混合液中c(Fe2+)=0.08mol·L-1时,为防止生成
3 2 3 3 4 2
Fe(OH) , ,即 ,故D错误;故选C。
2
题型三 中和滴定及其拓展应用
17.下列滴定反应中,指示剂使用正确的是( )
A.用HO 溶液滴定KI溶液,淀粉做指示剂
2 2
B.用酸性KMnO 标准溶液滴定NaHSO 溶液以测量其浓度,用甲基橙做指示剂
4 3
C.用标准FeCl 溶液滴定KI溶液,KSCN溶液做指示剂
3
D.用强酸标准溶液滴定测量弱碱浓度,用酚酞做指示剂
【答案】C
【解析】A项,用过氧化氢滴定碘化钾溶液,若用淀粉作指示剂,反应开始生成的碘遇淀粉使溶液就
变为蓝色,继续滴加时,溶液蓝色的变化无法确定滴定终点,故A错误;B项,酸性高锰酸钾溶液与亚硫
酸氢钠溶液完全反应时,再滴入酸性高锰酸钾溶液,过量的酸性高锰酸钾会使溶液会变为浅紫色,则滴定
时不需要指示剂即可完成测量实验,故B错误;C项,氯化铁溶液与碘化钾溶液完全反应时,若用硫氰化钾溶液做指示剂,过量的氯化铁溶液与硫氰化钾溶液反应生成硫氰化铁溶液,使溶液变为红色,可以确定
滴定达到终点,故C正确;D项,强酸溶液与弱碱溶液完全反应时生成强酸弱碱盐,强酸弱碱盐使溶液呈
酸性,若用酚酞作指示剂无法判断反应的终点,应选用甲基橙做指示剂,故D错误;故选C。
18.(2024·河北石家庄高三第二次调研)某活动小组为测定样品中NaBH 的纯度,设计了如下的实验步
4
骤:
步骤l:取5.0gNaBH 样品(杂质不参与反应),将样品溶于NaOH溶液后配成500mL溶液,取25.00mL
4
置于碘量瓶中,加入60.00mL0.1000mol/L的KIO 溶液充分反应(反应为
3
3NaBH +4KIO=3NaBO +4KI+6H O);
4 3 2 2
步骤2:向步骤1所得溶液中加入过量的KI溶液,用稀硫酸调节pH,使过量KIO 转化为I,冷却后
3 2
在暗处放置数分钟;
步骤3:向步骤2所得溶液中加入某种缓冲溶液调pH至5.0,加入几滴指示剂,用0.1000mol/L的
NaSO 标准溶液滴定至终点,消耗标准溶液的体积为20.70mL(反应为I+2Na SO=2NaI+Na SO)。
2 2 3 2 2 2 3 2 4 6
下列说法正确的是( )
A.NaBH 中H元素化合价为+1价
4
B.步骤2反应的离子方程式为IO -+I-+6H+=I +3H O
3 2 2
C.步骤3中加入几滴酚酞作指示剂
D.样品中NaBH 的纯度为64.47%
4
【答案】D
【解析】A项,NaBH 具有强还原性,H元素化合价为-1价,故A错误;B项,步骤2的反应为KI和
4
KIO 在酸性条件下生成I,离子方程式为:IO -+5I-+6H+=I +3H O;故B错误;C项,步骤3用NaSO 标
3 2 3 2 2 2 2 3
准溶液滴定碘单质溶液,用淀粉溶液坐指示剂,故C错误;D项,根据方程式
I+2Na SO=2NaI+Na SO,n(Na SO)=0.00207mol,则n(I)=0.001035mol,再根据IO -+5I-
2 2 2 3 2 4 6 2 2 3 2 3
+6H+=I +3H O,可以计算出n(KIO )=0.000345mol,这是剩余的KIO ,与NaBH 反应的KIO 为
2 2 3 3 4 3
0.006mol-0.000345mol=0.005655mol,根据3NaBH +4KIO=3NaBO +4KI+6H O可以计算出
4 3 2 2
n(NaBH )=0.00424125mol,则原样品中n(NaBH )=0.00424125mol =0.084825mol,NaBH 的纯度为
4 4 4
=64.47%,故D正确。
19.(2025·湖北省鄂东南省级示范高中教革联盟高三联考,节选)亚硝酰硫酸(NOSOH,相对分子质量
4
为127)是一种浅黄色或蓝紫色液体,遇水分解,溶于浓硫酸不分解,主要用于染料、医药等领域。(4)测定亚硝酰硫酸的纯度:准确称取1.800 g产品放入250 mL碘量瓶中,加入
的高锰酸钾溶液和 的硫酸溶液,摇匀。用 草酸钠标准溶液滴定,消耗草酸钠溶
液的体积为10.00 mL。已知该测定过程中只发生以下两步反应:
2KMnO +5NOSO H+2HO=KSO +2MnSO +5HNO +2H SO
4 4 2 2 4 4 3 2 4
5C O2-+2MnO-+16H+=10CO ↑+2Mn2++8H O
2 4 4 2 2
则产品中亚硝酰硫酸的纯度为: (精确到0.1%),在实验过程中,下列操作可能会导致亚硝酰
硫酸的纯度偏大的是 。
A.滴加草酸钠标准溶液时,滴定前俯视读数,滴定后仰视读数
B.滴加草酸钠标准溶液时,滴定开始时尖嘴处无气泡,滴定结束时出现气泡
C.滴定过程中,将挂在锥形瓶内壁上的草酸钠标准溶液用蒸馏水冲进瓶内
D.当溶液由浅紫红色刚好变无色时,立即停止滴加草酸钠溶液
【答案】(4) 88.2% BD
【解析】(4)根据滴定实验操作,用0.2500 mol·l-l的草酸钠标准溶液滴定过量的KMnO 标准溶液,草酸
4
钠与KMnO 发生氧化还原反应,根据氧化还原反应规律,配平该反应的离子反应为:5C O2-+2MnO-
4 2 4 4
+16H+=10CO ↑+2Mn2++8H O。由反应可知,过量的KMnO 标准溶液的物质的量n(KMnO)= n ( )=
2 2 4 4
×0.2500×0.01 mol=0.001mol,则与NOSOH溶液反应的KMnO 标准溶液的物质的量n(KMnO)=0.06
4 4 4
L×0.1000 mol/L -0.001 mol=0.005 mol,据已知反应
2KMnO +5NOSO H+2HO=KSO +2MnSO +5HNO +2H SO 可知:产品中NOSOH的物质的量
4 4 2 2 4 4 3 2 4 4
n(NOSOH)=0.005× mol=0.0125 mol,则亚硝酰硫酸的纯度为 ×100%≈88.2%;A项,
4
加草酸钠标准溶液时,滴定前俯视读数,滴定后仰视读数,标准液体积偏大,测定结果偏小,A错误;B
项,滴加草酸钠标准溶液时,滴定开始时尖嘴处无气泡,滴定结束时出现气泡,标准液体积偏小,测定结
果偏大,B正确;C项,滴定过程中,将挂在锥形瓶内壁上的草酸钠标准溶液用蒸馏水冲进瓶内,属于规
范操作,对测定结果没影响,C错误;D项,当溶液由浅紫红色刚好变无色时,未达到30s稳定时间,还
会有额外的草酸钠消耗,故标准液体积偏小,测定结果偏大,D正确;故选BD。
20.中华人民共和国国家标准(GB 27602011)规定葡萄酒中SO 最大使用量为0.25 g·L-1。某兴趣小组
2
用图1装置(夹持装置略)收集某葡萄酒中SO ,并对其含量进行测定。
2图1 图2
(1)仪器A的名称是____________,水通入A的进口为______。
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO 全部逸出并与C中HO 完全反应,其化学方程
2 2 2
式为__________________________________。
(3)除去C中过量的HO ,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择
2 2
图2中的________;若滴定终点时溶液的pH=8.8,则选择的指示剂为________;若用50 mL滴定管进行
实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)________(①=10 mL,②=40 mL,
③<10 mL,④>40 mL)。
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO 含量为________g·L-1。
2
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施:_____________________。
【答案】(1)冷凝管(或冷凝器) b (2)SO +HO===H SO (3)③ 酚酞 ④ (4)0.24
2 2 2 2 4
(5)原因:盐酸的挥发;改进措施:用不挥发的强酸如硫酸代替盐酸(或用蒸馏水代替葡萄酒进行对比
实验,扣除盐酸挥发的影响)
【解析】(1)A仪器的名称为冷凝管或冷凝器;为使冷却效果好,应将冷却水从处于低处的b口通入。
(2)SO 具有强还原性,HO 具有强氧化性,二者发生氧化还原反应:SO +HO===H SO 。(3)NaOH盛装
2 2 2 2 2 2 2 4
在碱式滴定管中,应将橡皮管向上弯曲以排出气泡,选③。滴定至终点时溶液的pH=8.8,在酚酞的变色
范围内,故可选用酚酞作指示剂。液面在10 mL时滴定管中有刻度的液体为40 mL,因滴定管的下端有一
段无刻度,故管内液体的体积大于40 mL。(4)SO 与NaOH存在如下关系:
2
SO ~ HSO ~ 2NaOH
2 2 4
64 g 2 mol
m(SO ) 0.090 0 mol·L-1×0.025 L
2
解得:m(SO )==0.072 g,故葡萄酒中SO 的含量为=0.24 g·L-1。(5)盐酸为挥发性酸,挥发出的HCl
2 2
消耗NaOH,使测量值偏大。可以用难挥发的稀硫酸代替盐酸进行该实验。
21.某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛
________________________________。
(2)滴定终点的判断:____________________________________________。
(3)某学生根据3次实验分别记录有关数据如表:
0.1000mol/L盐酸的体积/mL
待测NaOH
滴定次数 溶液的体
积/mL 滴定前刻度 滴定后刻度 溶液体积/mL
第一次 25.00 0.00 26.11 26.11
第二次 25.00 1.56 30.30 28.74
第三次 25.00 0.22 26.31 26.09
根据表中数据该NaOH溶液的物质的量浓度为______________。
(4)以下操作会导致测得的NaOH溶液浓度偏高的是______________。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.盛放碱液的碱式滴定管开始俯视读数,后来仰视读数
(5)氧化还原滴定实验的原理与中和滴定相同(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或
反之)。为测定某样品中所含晶体FeSO •7H O的质量分数,取晶体样品ag,溶于稀硫酸配成100.00mL溶
4 2
液,取出20.00mL溶液,用KMnO 溶液滴定(杂质与KMnO 不反应)。若消耗0.2000mol•L-1KMnO 溶液
4 4 4
20.00mL,所得晶体中FeSO •7H O的质量分数为_______________(用a表示)。
4 2
【答案】(1)注视锥形瓶内颜色变化 (2)浅红色变为无色且半分钟内不恢复原色
(3)0.1044mol/L (4)AC (5) ×100%
【解析】(1) 用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,
眼睛注视锥形瓶内颜色变化;(2)用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选
择酚酞作指示剂,滴定前溶液为红色,滴定后呈中性,溶液为无色,则滴定终点的判断依据是浅红色变为
无色且半分钟内不恢复原色;(3)根据表中数据,第二次实验数据明显偏大,舍去,根据第一次、第三次实验数据,平均消耗盐酸的体积是 =26.10ml,则c()= =
=0.1044mol/L;(4) A项,酸式滴定管未用标准盐酸润洗就直接注入标准盐酸,盐
酸浓度偏小,消耗盐酸体积偏大,测定氢氧化钠溶液浓度偏高;B项,滴定前盛放NaOH溶液的锥形瓶用
蒸馏水洗净后没有干燥,氢氧化钠的物质的量不变,消耗盐酸体积不变,测定氢氧化钠溶液的浓度无影响;
C项,酸式滴定管在滴定前有气泡,滴定后气泡消失,消耗盐酸体积偏大,测定氢氧化钠溶液浓度偏高;
D项,读取盐酸体积时,开始仰视读数,滴定结束时俯视读数,消耗盐酸体积偏小,测定氢氧化钠溶液浓
度偏低;E项,盛放碱液的碱式滴定管开始俯视读数,后来仰视读数,氢氧化钠溶液体积偏小,消耗盐酸
体积偏小,测定氢氧化钠溶液的浓度偏低;故选AC。(5)亚铁离子会被高锰酸钾溶液氧化为铁离子,高锰
酸钾被还原成锰离子,根据电子守恒,即5FeSO •7H O~ KMnO,所以晶体中FeSO •7H O的质量分数为
4 2 4 4 2
= ×100%。
1.(2025·浙江省富阳中学高三选考模拟)在化学实践中,科研工作者会使用许多缓冲溶液。在缓冲溶液
中发挥作用的物质称为缓冲对,一个缓冲对包含2个相差1个H+的分子或离子。在人体的血液(pH约7.35-
7.45)中也有HCO/HCO-,HPO -/HPO 2-/等缓冲对。下图为参考数据。关于缓冲溶液相关实验,下列说法
2 3 3 2 4 4
正确的是( )
物质 HCO HCO - CHCOOH NH HC O HC O-
2 3 3 3 3 2 2 4 2 4
pKa/pK 6.4 10.3 4.7 4.7 1.3 4.3
b
A.为构建pH=3的缓冲溶液,可采用HCO/HCO-缓冲对
2 3 3
B.某缓冲溶液仅由HC O/NaHC O 配制而成,且该溶液pH=1,则配制时可将0.2mol/L的HC O 溶
2 2 4 2 4 2 2 4
液与0.1mol/L的NaHC O 溶液等体积混合
2 4
C.将浓度均为2mol/L的CHCOONH/ Na C O 溶液混合,则c(OH-)>c(HC O-)
3 4 2 2 4 2 4
D.将浓度均为0.2mol/L的1L MgCl 溶液与2L Na CO 溶液混合,此时Mg2+可视为完全沉淀,且沉淀
2 2 3质量为14.2g,则此时溶液pH约为10
【答案】D
【解析】A项,由表可知,HCO/HCO-缓冲对形成的溶液的pH大于3,A错误;B项,0.2mol/L的
2 3 3
HC O 溶液与0.1mol/L的NaHC O 溶液等体积混合,则得到0.1mol/L的HC O 与0.05mol/L的NaHC O 的
2 2 4 2 4 2 2 4 2 4
混合溶液,则 , c(H+)=20×10-2.3mol·L-1 mol/L,pH≠1,B错误;
C项,由表知,铵根离子、乙酸根离子水解程度相等,而铵根离子水解程度大于草酸根离子,铵根离子水
解的氢离子结合了草酸根离子水解的氢氧根离子生成水,使得草酸氢根离子浓度大于氢氧根离子浓度,C
错误;D项,设生成氢氧化镁、碳酸镁分别为amol、(0.2-a)mol,则58a+84×(0.2-a)=14.2,a=0.1mol,CO2-
3
+H O HCO -+OH-,0.2mol碳酸根离子水解生成0.2mol碳酸氢根离子、0.2mol氢氧根离子,氢氧根离
2 3
子转化为氢氧化镁沉淀,结合碳质量守恒,反应后碳酸根离子为0.2mol、碳酸氢根离子为0.2mol,则
, c(OH-)=10-3.7mol·L-1,pOH≈4,pH≈10,D正确;故选D。
2.(2025·浙江省稽阳联谊学校高三联考)某小组做如下两组实验:
实验Ⅰ:往10mL0.1mol/L氨水中滴加0.1mol/L的草酸溶液。
实验Ⅱ:往10mL0.1mo/L氨水中滴加0.1mol/L的氢氟酸。
已知:溶液混合后体积变化忽略不计。溶液中某离子的浓度小于1.0×10-5mol·L-1时,可认为该离子已
沉淀完全。25℃时,相关常数如下表。
NH ·H O HF HC O CaF CaC O
3 2 2 2 4 2 2 4
电
离
1.8×10-5 6.3×10-4 K =5.6×10-2,K =1.5×10-4 溶度积K 4.0×10-11 2.5×10-9
a1 a2 sp
常
数
下列说法正确的是( )
A.实验Ⅰ,滴加过程中始终满足cC O2-+cHC O-+cHC O=0.1mol·L-1
2 4 2 4 2 2 4
B.实验Ⅱ中 时,因NH +和F-水解相互促进,导致所得溶液中含氟微粒的主要形式
4
为HF分子
C.相同温度下,CaC O 在NH Cl溶液中的溶解度比水中要小
2 4 4D.用Ca(NO ) 溶液,无法将混合液中相同浓度的C O2-和F-先后沉淀而分离
3 2 2 4
【答案】D
【解析】A项,滴加过程中溶液体积逐渐变大,cC O2-+cHC O-+cHC O逐渐减小,A错误;B
2 4 2 4 2 2 4
项,实验Ⅱ中 时,恰好生成NH F溶液。NH ++F-+H O HF+NH ·H O的
4 4 2 3 2
,故尽管NH +和F-水解相互促进,但水解仍然微弱,所得溶液中含氟微
4
粒的主要形式为F-,B错误;C项,NH Cl溶液呈酸性,使溶解平衡CaC O(s) Ca2+ (aq)+ C O2-(aq)
4 2 4 2 4
右移,CaC O 在NH Cl溶液中的溶解度比水中要大,C错误;D项,当F-浓度等于1.0×10-5mol·L-1时,
2 4 4
Ca2+浓度等于0.4mol/L,此时C O2-的最大浓度为6.25×10-9mol·L-1,即C O2-也沉淀完全;反之,当C O2-浓
2 4 2 4 2 4
度等于1.0×10-5mol·L-1时,Ca2+浓度等于2.5×10-4mol·L-1,此时F-的最大浓度为4.0×10-4mol·L-1,即F-也几乎
沉淀完全;综上,用Ca(NO ) 溶液,无法将混合液中相同浓度的C O2-和F-先后沉淀而分离,D正确;故
3 2 2 4
选D。
3.(2025·浙江省金丽衢十二校高三第一次联考)已知K (CaCO )=2.8×10-9,K (H CO)=4.5×10-7,
sp 3 a1 2 3
K (H CO)=4.7×10-11,K(HClO)=2.9×10-8。下列说法正确的是( )
a2 2 3 a
A.向漂白粉溶液中通入少量CO 气体的离子方程式为ClO-+CO +H O= HClO+HCO -
2 2 2 3
B.向0.2mol·L-1的CaCl 溶液中加入等体积的0.2mol·L-1的NaHCO 溶液可生成白色沉淀
2 3
C.室温下,向NaOH溶液中通入CO 气体至pH=11,此时溶液中的cHCO -=4.7cCO2-
2 3 3
D.向物质的量浓度均为0.1mol·L-1的NaCO 和NaHCO 的混合溶液中无论滴加少量的HCl还是
2 3 3
NaOH溶液,均可导致溶液的pH值出现较大变化
【答案】B
【解析】根据电离常数可知酸性HCO>HClO>HCO -。A项,酸性HCO>HClO>HCO -,向漂白
2 3 3 2 3 3
粉溶液中通入少量CO 气体生成碳酸钙沉淀、次氯酸,对应的离子方程式为Ca2++2ClO-+H O+CO=2HClO+
2 2 2
CaCO ↓,A错误;B项,向0.2mol·L-1的CaCl 溶液中加入等体积的0.2mol·L-1的NaHCO 溶液混合后溶液
3 2 3
中 , ,根据HCO-+H O HCO+OH-可知
3 2 2 3, , ,
, ;根据K (H CO)=4.7×10-11可知
a2 2 3
,溶液中 , ,计算可得
,此时溶液中 ,
,有白色沉淀生成,B正确;C项,向NaOH溶液中通入CO 气体至
2
pH=11, , , ,即
4.7cHCO -=cCO2-,C错误;D项,物质的量浓度均为0.1mol·L-1的NaCO 和NaHCO 的混合溶液存在
3 3 2 3 3
CO2-+H O HCO -+OH- 、HCO-+H O HCO+OH-、HCO HCO -+H+,使得溶液具有缓冲
3 2 3 3 2 2 3 2 3 3
能力,滴加少量的HCl还是NaOH溶液,均可导致溶液的pH值变化不大,D错误;故选B。
4.(2025·浙江省五校高三联考)已知:常温下,氢硫酸HS的电离常数K =1.1×10-7,K =1.3×10-13,
2 a1 a2
K (FeS)= 6.3×10-18,K (HgS)= 1.6×10-52。往10mL0.1mol/LH S(pH约为4.1)溶液中加
sp sp 2
入10mL0.1mol/LNaOH溶液,然后再滴加入0.1mol/LFeSO 溶液。溶液混合后体积变化忽略不计,下列说
4
法不正确的是( )
A.0.1mol/LH S溶液中存在c(H+)>c(HS-)>c(OH―)>c(S2-)
2
B.HS与NaOH溶液反应至溶液呈中性时,cNa++cHS- c(S2-)=0.1mol·L-1
2 2
C.滴加入0.1mol/LFeSO 溶液时,会产生FeS沉淀
4
D.FeS固体能用于去除工业废水中的Hg2+
【答案】B
【解析】A项,0.1mol/LH S溶液中存在电离平衡HS SH-+H+ (H S以第一步电离为主)、H -
2 2 2 S
S2-+H+、HO OH-+H+,0.1mol/LH S溶液的pH约为4.1,则c(OH-)=1.0×10-9.9mol·L-1,
2 2, ,则
,故c(H+)>c(HS-)>
c(OH―)>c(S2-),故A正确;B项,溶液中存在电荷守恒cNa++cH+=cOH-+cHS-+2cS2-,HS与
2
NaOH溶液反应至溶液呈中性时,c(OH―)=c(H+),则cNa+=cHS-+2c(S2-),则cNa++ cHS=cHS-+
2
2cS2-+ cHS,cNa++ cHS- cS2-=cHS-+cS2-+ cHS= cS溶液体积变大,故,c(S2-)<
2 2 2
0.1mol·L-1,cNa++cHS- c(S2-)<0.1mol·L-1,故B错误;C项,往10mL0.1mol/LH S溶液中加入
2 2
10mL0.1mol/LNaOH溶液,恰好发生反应生成NaHS,滴加入0.1mol/LFeSO 溶液时,发生反应HS-
4
+Fe2+=FeS+H+,该反应的平衡常数为
,会产生FeS沉淀,故 C正确;D
项,FeS的溶度积比HgS的溶度积大,难溶电解质易转化为更难溶的电解质,则FeS固体能用于去除工业
废水中的Hg2+,故 D正确;故选B。
5.(2024·山东潍坊五县区高三阶段监测)乙二胺四乙酸(EDTA)可与金属离子形成稳定的配合物。常用
EDTA测定水中钙含量(EDTA与钙反应时物质的量之比均为1∶1)。基本步骤如下:
①EDTA标定:取10.00 mL 0.1 mol·L-1标准CaCl 溶液,加入3滴甲基橙溶液作指示剂,用已配制好
2
的EDTA溶液滴定至终点,消耗EDTA溶液V mL。
1
②钙提取:取一定质量的有机物,并用酸性KMnO 溶液氧化,再经萃取、反萃取将金属转移到水中,
4
得到提取液。加入掩蔽剂(掩蔽除钙之外的金属)并将pH调至11.3。
③EDTA滴定:取20.00mL提取液,加入指示剂钙黄绿素(钙与钙黄绿素生成能发出绿色荧光的配合
物),在黑色背景下用标定后的EDTA溶液滴定至终点,消耗EDTA溶液V mL。
2
根据上述实验原理,下列说法错误的是( )
A.若对提取液的其他金属不进行掩蔽,测定的钙含量结果偏高
B.EDTA标定时,滴定管尖嘴开始有气泡终点无气泡,会使钙含量测定结果偏高
C.EDTA滴定若选用其他物质作指示剂,提取液的pH可能发生变化
D.pH为11.3时,EDTA与钙的配合能力强于钙黄绿素与钙的配合能力
【答案】B【解析】A项,EDTA可与金属离子形成稳定的配合物,若对提取液的其他金属不进行掩蔽,测定的
钙含量结果偏高,A正确;B项,EDTA标定时,滴定管尖嘴开始有气泡终点无气泡,则V 数值增大,故
2
钙含量偏低,B错误;C项,EDTA滴定时,指示剂的选用与体系pH有关,同时滴定时应保证体系的酸碱
性,保证钙不会变成沉淀,故改变指示剂的种类,提取液的pH会发生变化,C正确;D项,由③可知pH
为11.3时,EDTA与钙的配合能力强于钙黄绿素与钙的配合能力,D正确; 故选B。
6.(2025·浙江省名校协作体三开学测试,节选)探究NaBiO 的应用:利用NaBiO 测定溶液中 含
3 3
量
(4)在试管中加入VmLMnSO 和HSO 的混合液,然后加入一定量的NaBiO,充分反应分离出剩余的
1 4 2 4 3
NaBiO,向所得滤液中加入足量KI溶液,充分反应后转移至碘量瓶中,用cmol·L-1NaSO 溶液滴定至浅
3 2 2 3
黄色,加入淀粉溶液,继续用cmol·L-1NaSO 溶液滴定至终点,共消耗NaSO 溶液VmL。
2 2 3 2 2 3 2
(已知:I-+MnO-+H+→I+Mn2++H O、I+S O2-→SO2-+I-,均未配平)
4 2 2 2 2 3 4 6
①混合液中Mn2+的含量为 mg·mL-1 (用含V、V、c的代数式表示);
1 2
②在滴定过程中,下列实验操作会使测定结果偏高的是 (填标号)。
a.滴定前平视读数,滴定终点时俯视读数
b.滴定时碘量瓶中溶液酸性太强
c.碘量瓶用蒸馏水洗涤后未干燥
d.滴定前滴定管尖嘴内无气泡,达到终点有气泡
e.没有分离出剩余的NaBiO,直接加入足量 溶液
3
【答案】(1)Bi(OH) +3OH-+Na++ Cl=NaBiO+2Cl-+3H O
3 2 3 2
(2)防止氯气过量使溶液呈酸性,导致NaBiO 分解 吸收多余的氯气
3
(3)efad (4) be
【解析】用浓盐酸和高锰酸钾反应制备氯气,其中混有挥发出的氯化氢气体,要用饱和食盐水进行除
杂,然后利用氯气的强氧化性,在碱性环境下将Bi(OH) 氧化为NaBiO。(1)丙中发生反应为碱性环境下氯
3 3
气将Bi(OH) 氧化为NaBiO,氯化合价由0变为-1、Bi化合价由+3变为+5,结合电子守恒可知,离子方程
3 3
式为Bi(OH) +3OH-+Na++Cl=NaBiO+2Cl-+3H O;(2)铋酸钠在酸中会逐渐分解,氯气和水会生成盐酸和和
3 2 3 2
次氯酸,当丙中白色固体消失时,可以初步判断丙中反应已完成,此时应立即进行的操作是关闭K 和
3
K、打开K,以防止NaBiO 分解,同时不产生过量氯气,多余的氯气被NaOH吸收;(3)据已知信息,不
1 2 3
溶于冷水,在空气或热水中逐渐分解,为从丙中获取粗产品应该:e.在冰水中冷却,析出晶体;f.用布
氏漏斗抽滤,加快过滤速率;a.冷水洗涤,减少溶解损失;d.在干燥器中干燥,防止其分解;故选efad;(4)①根据反应原理可知最后生成碘单质,碘单质被c mol·L-1NaSO 反应,碘单质被反应完,
2 2 3
NaSO 的物质的量为 ,I+2S O2-=S O2-+2I-,NaSO 的物质的量为碘单质的物质的量2倍,
2 2 3 2 2 3 4 6 2 2 3
根据10I-+2MnO-+16H+=5I +2Mn2++8H O,锰离子的物质的量为碘单质的2.5倍,故硫酸锰的质量为
4 2 2
,故含量为 ;②a项,滴定终点时俯视读数,则读数偏小,则体积偏小,
故碘单质偏小,故结果偏小,a不符合题意;b项,碘量瓶中溶液酸性太强,NaSO 发生歧化反应,导致
2 2 3
消耗的碘的含量偏小,碘单质偏高,b符合题意;c项,锥形瓶用蒸馏水洗涤后未干燥 ,对结果无影响,
故c不符合题意;d.滴定前滴定管尖嘴内无气泡,达到终点有气泡,读数偏小,则体积偏小,结果偏低,
d不符合题意;e项,没有分离出剩余的NaBiO 与KI反应,生成碘单质,则最终测定的碘含量偏高,e符
3
合题意;故选be。
7.(2025·河南省南阳市高三联考,节选)某小组设计实验制备FeCl 并测定产品纯度。
3
(二)测定FeCl 样品的纯度
3
已知:Fe3++6F- [FeF ]3- (无色,很稳定),AgF易溶于水且完全电离。
6
(4)实验步骤如下(已知杂质均不溶于水或不参与反应):
步骤1:准确称取mg样品,溶于水,滤去不溶物后,配成1000mL溶液,取10.00mL置于锥形瓶中;
步骤2:向锥形瓶中加入适量NaF溶液(恰好与铁离子完全反应),用力振荡,再加入
VmL0.1000mol·L-1 AgNO 溶液(过量)使Cl-完全沉淀;
1 3
步骤3:向其中加入硝基苯(不溶于水,密度比水大),用力振荡;
步骤4:加入几滴Fe(NO ) 溶液,用0.1000mol·L-1NH SCN溶液滴定过量的Ag+至终点,消耗NH SCN
3 3 4 4
溶液的体积为VmL。
2
(已知:常温下,K (AgCl)= 1.8×10-10,K (AgSCN)= 2.0×10-12。FeCl 的摩尔质量用M表示)
sp sp 3
①滴定终点时锥形瓶内现象为 。
②步骤3加入硝基苯的目的是 ,若省略步骤3,测定结果将 。(填“偏大”、“偏小”
或“无影响”)。
③测得样品中FeCl 的质量分数为 %(用含m、V、V、M的式子表示)。
3 1 2
【答案】(4)滴入最后半滴NH SCN标准溶液,锥形瓶内液体变为血红色,且半分钟不恢复原色
4
覆盖氯化银沉淀,保护氯化银沉淀不转化为溶解度更小的AgSCN沉淀(合理即可) 偏小【解析】(1)盛放MnO 的仪器名称为蒸馏烧瓶;由分析可知,图中各装置连接顺序是
2
A→C→E→B→D→E→F;(2)装置A中发生反应为浓盐酸与二氧化锰制备氯气,其离子方程式为
MnO +4H++2Cl- MnCl +Cl↑+2H O;(3)装置F用来吸收多余的尾气,所以其离子方程式为Cl+2OH—=ClO
2 2 2 2 2
—+Cl—+H O;D装置用来收集FeCl ,FeCl 遇水蒸气易水解而生成Fe(OH) ,若D和F直接相连,则F中的
2 3 3 3
水蒸气会进入D中使FeCl 水解,所以制得产品中会含有杂质Fe(OH) ;(4)①硫氰根与银离子结合生成沉
3 3
淀,当银离子恰好被反应完时,滴入最后半滴NH SCN,硫氰根与三价铁结合生成硫氰化铁锥形瓶内液体
4
变为红色,且半分钟不恢复原色,故答案为:滴入最后半滴NH SCN标准溶液,锥形瓶内液体变为血红色,
4
且半分钟不恢复原色;②步骤3加入硝基苯的目的是为了让有机物覆盖氯化银沉淀,保护氯化银沉淀不会
转化为溶解度更小的AgSCN沉淀,若省略步骤三,会使得氯离子测定结果偏小使得氯化铁测定结果偏小;
③由Ag++Cl- = AgCl↓、Ag++SCN- = AgSCN↓根据可知n(SCN-) =0.1000mol/L×V×10-3 L =V×10-4mol,与
2 2
硫氰根反应的n(Ag+) =V×10-4mol,由于n (Ag+)= V ×10-3 L×0.1000mol/L=V×10-4mol,所以与氯离子反
2 总 1 1
应的n(Ag+)=V×10-4-1V×10-4=(V-V)×10-4mol,故氯离子的物质的量为(V-V)×10-4mol,根据元素物
1 2 1 2 1 2
质的量守恒可知n(FeCl )= ,m(FeCl )=n×M= ,所以氯化铁的质量分数
3 3
= 。
8.滴定法可用于测定样品纯度。
I.双指示剂法测定烧碱样品(含NaCO)纯度:
2 3
[实验步骤]
a.迅速称取烧碱样品1.2 g,溶解后配制成250 mL溶液,备用:
b.将0.1000 mo/L HCl标准溶液装入酸式滴定管,调零,记录起始读数V =0.10mL;
0
c.用碱式滴定管取20.00 mL样品溶液于锥形瓶中,滴加2滴酚酞;以HCl标准溶液滴定至第一终点(此
时溶质为NaCl和NaHCO ),记录酸式滴定管的读数V =21.8mL;
3 1
d.然后再向锥形瓶内滴加2滴甲基橙,继续用HCl标准溶液滴定至第二终点,记录酸式滴定管的读数
V =23.50mL。
2
(1)滴定至第一终点的过程中,发生反应的离子方程式为_______。(2)判断滴定至第二终点的现象是溶液由_______色变为橙色。
(3)样品中NaOH的质量分数 _______%(计算结果保留小数点后1位)。
(4)下列操作会导致测得的NaOH质量分数偏高的是_______(填字母序号)。
a.滴定前有气泡,滴定至第一终点时气泡消失
b.达到第一终点前,锥形瓶中有气泡产生
c.第一终点后继续滴定时,锥形瓶中有少许液体溅出
d.记录酸式滴定管读数V 时,仰视标准液液面
2
II.测定三草酸合铁酸钾K[Fe(C O)]·3H O中铁的含量:
3 2 4 3 2
第一步,称量m g样品于锥形瓶中,溶解后加稀HSO 酸化,用c mol/L KMnO 溶液滴定至终点,消
2 4 4
耗KMnO 溶液V mL。
4 1
第二步,向上述溶液中加入过量锌粉将Fe3+转化为Fe2+,过滤、洗涤,将滤液及洗涤液全部收集到锥
形瓶中。加稀HSO 酸化,用c mol/L KMnO 溶液滴定至终点,消耗KMnO 溶液V mL。
2 4 4 4 2
(5)该晶体中铁的质量分数的表达式是_______。
【答案】(1)OH-+H+=H O、CO2-+H+=HCO- (2)黄
2 3 3
(3)83.3% (4)abc (5)
【解析】(1)滴定至第一终点的过程中,盐酸与氢氧化钠、碳酸钠依次发生反应,反应的离子方程式是:
OH-+H+=H O、CO2-+H+=HCO-;(2)甲基橙的变色范围为:pH<3.1时红色,3.1<pH<4.4橙色,pH>4.4
2 3 3
黄色,根据其变色范围可知,滴定至第二终点的现象是溶液由黄色变为橙色;(3)根据已知信息,可知实验
中NaHCO 生成CO 消耗盐酸的体积为23.50mL-21.80mL=1.70mL,NaOH消耗盐酸的体积是
3 2
21.80mL-1.70mL-0.10mL=20.00mL,故20.00mL样品溶液中NaOH的物质的量是0.1000mol/
L×0.020L=0.0020mol,氢氧化钠的质量为0.0020mol×40g/mol=0.080g,样品中氢氧化钠的质量分数
w(NaOH) = ;(4)a项,滴定前有气泡,滴定至第一终点时气泡消失,说明达到
第一终点消耗的盐酸多,测得的氢氧化钠质量分数偏高,故a正确;b项,达到第一终点前,锥形瓶中有
气泡产生,说明达到第一终点消耗的盐酸多,测得的氢氧化钠质量分数偏高,故b正确;c项,第一终点
后继续滴定时,锥形瓶中有少许液体溅出,导致第二次滴定消耗的盐酸少,测得的氢氧化钠质量分数偏高,
故c正确;d项,记录酸式滴定管读数V 时,仰视标准液液面,说明计算出的达到第二终点消耗的盐酸多,
2
测得的氢氧化钠质量分数偏低,故d错误;故选abc;(5)加入过量锌粉能将溶液中Fe3+转化为Fe2+,酸化后Fe2+与KMnO 溶液反应,根据化合价变化可找出关系式为5 Fe2+~ MnO -,根据消耗KMnO 溶液的浓度和体
4 4 4
积可知溶液中n(Fe2+)=cmol/L×V×10-3L×5=5×10-3cVmol,则该晶体中铁元素的质量分数为
2 2
= 。
9.用氧化还原滴定法可以测定市售双氧水中过氧化氢的浓度(单位g∙L−1),实验过程包括标准溶液的准
备和滴定待测溶液。
I.准备KMnO 标准溶液
4
a.配制100.00mLKMnO 溶液备用;
4
b.准确称取NaC O 基准物质3.35g(0.025mol),配制成250.00mL标准溶液。取出25.00mL于锥形瓶
2 2 4
中,加入适量3 mol∙L−1硫酸酸化后,用待标定的KMnO 溶液滴定至终点,记录数据,计算KMnO 溶液的
4 4
浓度。
II.滴定主要步骤
a.取待测双氧水10.00mL于锥形瓶中;
b.锥形瓶中加入30.00mL蒸馏水和30.00mL3 mol∙L−1硫酸,然后用已标定的KMnO 溶液(0.1000
4
mol∙L−1)滴定至终点;
c.重复上述操作两次,三次测定的数据如表:
组别 1 2 3
消耗标准溶液体积(mL) 25.00 25.02 24.98
d.数据处理。
请回答下列问题:
(1)将称得的NaC O 配制成250.00mL标准溶液,所使用的仪器除烧杯和玻璃棒外还有___。
2 2 4
(2)标定KMnO 溶液时,能否用稀硝酸调节溶液酸度____(填“能”或“不能”),简述理由___。写出
4
标定过程中发生反应的离子方程式____。
(3)滴定待测双氧水时,标准溶液应装入____滴定管,滴定至终点的现象是____。
(4)计算此双氧水的浓度为____g∙L−1。
(5)误差分析:在第II步滴定主要步骤中,下列操作会使双氧水浓度测定结果偏高的是____。A.锥形
瓶洗净后用双氧水润洗
B.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
C.观察读数时,滴定前仰视,滴定后俯视D.振荡锥形瓶时部分液体溅出
【答案】(1)250mL容量瓶、胶头滴管
(2)不能 稀硝酸有氧化性,也会与NaC O 反应,影响KMnO 溶液浓度的标
2 2 4 4
定 2MnO -+2C O2-+16H+=2Mn2++10CO ↑+8H O
4 2 4 2 2
(3) 酸式 滴入最后一滴标准溶液,锥形瓶中的液体变为浅紫色(红色),且半分钟不变色
(4)21.25 (5)AB
【解析】配置基准物质溶液,通过溶解、冷却、转移、洗涤、定容、摇匀等操作,用待标定的高锰酸
钾溶液进行滴定,标定高锰酸钾溶液的浓度,用高锰酸钾溶液来滴定双氧水溶液测定双氧水的浓度,取
10.00mL的双氧水与锥形瓶,用酸式滴定管滴定高锰酸钾溶液至终点,重复实验2~3次。(1)将称得的
NaC O 配制成250.00mL标准溶液,先在烧杯中溶解,冷却后转移到250mL容量瓶中,洗涤烧杯和玻璃棒,
2 2 4
洗涤液也转移到容量瓶中,先直接加蒸馏水至刻度线下1~2cm处改用胶头滴管滴加至溶液凹液面与刻度
线相切为止,所使用的仪器除烧杯和玻璃棒外还有250mL容量瓶、胶头滴管;(2)稀硝酸有氧化性,也会
与NaC O 反应,影响KMnO 溶液浓度的标定,因此不能用稀硝酸调节溶液酸度;标定过程中草酸根被氧
2 2 4 4
化为二氧化碳,高锰酸根被还原为锰离子,发生反应的离子方程式2MnO -+2C O2-+16H+=2Mn2+
4 2 4
+10CO ↑+8H O;(3)滴定待测双氧水时,高锰酸钾溶液具有氧化性,因此标准溶液应装入酸式滴定管,双
2 2
氧水是无色,高锰酸钾是紫色,因此滴定至终点的现象是滴入最后一滴标准溶液,锥形瓶中的液体变为浅
紫色(红色),且半分钟不变色;(4)三次消耗高锰酸钾溶液的平均值为25.00mL,根据题意得到关系式5HO
2 2
~2MnO -,则HO 的物质的量为n(H O)= 0.1000 mol∙L−1×0.025L× ,则此双氧水的浓度为
4 2 2 2 2
;(5)A项,锥形瓶洗净后用双氧水润洗,双氧水待测液
增多,消耗标准液体积增多,计算双氧水浓度偏高,故A符合题意;B项,滴定前滴定管尖嘴部分有气泡,
滴定后气泡消失,读出数据偏大,测定结果偏高,故B符合题意;C项,观察读数时,滴定前仰视,滴定
后俯视,读书数据偏小,测定结果偏低,故C不符合题意;D项,振荡锥形瓶时部分液体溅出,消耗标准
液体积减小,测定结果偏低,故D不符合题意;故选AB。
1.(2023•浙江省1月选考,15)碳酸钙是常见难溶物,将过量碳酸钙粉末置于水中达到溶解平衡:CaCO (s) Ca2+(aq)+CO 2-(aq)[已知Ksp(CaCO)=3.4×10-9,Ksp(CaSO )=4.9×10-5,HCO 的电离常数
3 3 3 4 2 3
K =4.5×10-7,K =4.7×10-11],下列有关说法正确的是( )
a1 a2
A.上层清液中存在c(Ca2+)=c(CO2-)
3
B.上层清液中含碳微粒最主要以HCO -形式存在
3
C.向体系中通入CO 气体,溶液中c(Ca2+)保持不变
2
D.通过加NaSO 溶液可实现CaCO 向CaSO 的有效转化
2 4 3 4
【答案】B
【解析】A项,上层清液为碳酸钙的饱和溶液,碳酸根离子水解生成碳酸氢根离子,因此 c(Ca2+)>
c(CO2-),A错误;B项,根据K =4.7×10-11可得 ,则碳酸根的水解平衡常数为
3 a2
,说明碳酸根的水解程度较大,则上层清液中含碳微粒主要为碳酸氢
根离子,B正确;C项,向体系中通入CO ,碳酸钙与CO 反应生成碳酸氢钙,碳酸氢钙易溶于水,则溶
2 2
液中钙离子浓度增大,C错误;D项,由题干可知,Ksp(CaCO)=3.4×10-9,Ksp(CaSO )=4.9×10-5,碳酸钙比
3 4
硫酸钙更难溶,加入硫酸钠后碳酸钙不会转化成硫酸钙,D错误;故选B。
2.(2023•山东卷,15)在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系:HgI (s)
2 2
HgI (aq);HgI (aq) Hg2++2I-;HgI (aq) HgI++I-;HgI (aq)+I- HgI --;HgI (aq)+2I-
2 2 2 2 3 2
HgI 2-,平衡常数依次为K、K、K、K、K。已知lgc(Hg2+)、lgc(HgI+)、lgc(HgI -)、lgc(HgI 2-)随lgc(I-)的
4 0 1 2 3 4 3 4
变化关系如图所示,下列说法错误的是( )
A.线 表示lgc(HgI 2-)的变化情况
4
B.随c(I-)增大,c[HgI (aq)]先增大后减小
2C.
D.溶液中I元素与 元素的物质的量之比始终为2:1
【答案】B
【解析】由题干反应方程式HgI (aq) Hg2++2I-可知,K= ,则有c(Hg2+)=
2 1
,则有lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-),同理可得:lgc(HgI+)=lgK +lgc(HgI )-lgc(I-),lgc(HgI -)
1 2 2 2 3
=lgK +lgc(HgI )+ lgc(I-),lgc(HgI 2-) ==lgK +lgc(HgI )+ 2lgc(I-),且由HgI (s) HgI (aq)可知
3 2 4 4 2 2 2
K=c[HgI (aq)]为一定值,故可知图示中 曲线1、2、3、4即L分别代表
0 2
lgc(HgI+)、lgc(Hg2+)、lgc(HgI -)、lgc(HgI 2-)。A项,线L表示lgc(HgI 2-)的变化情况,A正确;B项,已知
3 4 4
HgI (s) HgI (aq)的化学平衡常数K= c[HgI (aq)],温度不变平衡常数不变,故随c(I-)增大,c[HgI (aq)]
2 2 0 2 2
始终保持不变,B错误;C项,曲线1方程为:lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-),曲线2方程为:
1 2
lgc(HgI+)=lgK +lgc(HgI )-lgc(I-)即有①b= lgK+lgc(HgI )-2a,②b= lgK+lgc(HgI )-a,联合①②可知得:
2 2 1 2 2 2
,C正确;D项,溶液中的初始溶质为HgI ,根据原子守恒可知,该溶液中I元素与Hg
2
元素的物质的量之比始终为2:1,D正确;故选B。
3.(2023•江苏卷,12,3分)室温下,用含少量Mg2+的MnSO 溶液制备MnCO 的过程如题图所示。已
4 3
知K (MgF)=5.2×10-11,K(HF)=6.3×10-4。下列说法正确的是( )
sp 2 aA.0.1mol·L-1NaF溶液中:c(F-)= c(Na+)+c(H+)
B.“除镁”得到的上层清液中:
C.0.1mol·L-1NaHCO 溶液中:c(CO2―)=c(H+)+c(H CO)-c(OH―)
3 3 2 3
D.“沉锰”后的滤液中:(Na+)+c(H+)= c(OH―)+c(HCO -)+2c(CO2―)
3 3
【答案】C
【解析】A项,0.1mol·L-1NaF溶液中存在电荷守恒:c(OH―)+c(F-)= c(Na+)+c(H+),A错误;B项,
“除镁”得到的上层清液中为MgF 的饱和溶液,有K (MgF)=c(Mg2+)·c2(F―),故 ,
2 sp 2
B 错误;C 项,0.1mol·L-1NaHCO 溶液中存在质子守恒:c(CO2―)+c(OH―)=c(H+)+c(H CO),故
3 3 2 3
c(CO2―)=c(H+)+c(H CO)-c(OH―),C正确;D项,“沉锰”后的滤液中还存在F-、SO 2-等离子,故电荷守
3 2 3 4
恒中应增加其他离子使等式成立,D错误。 故选C。
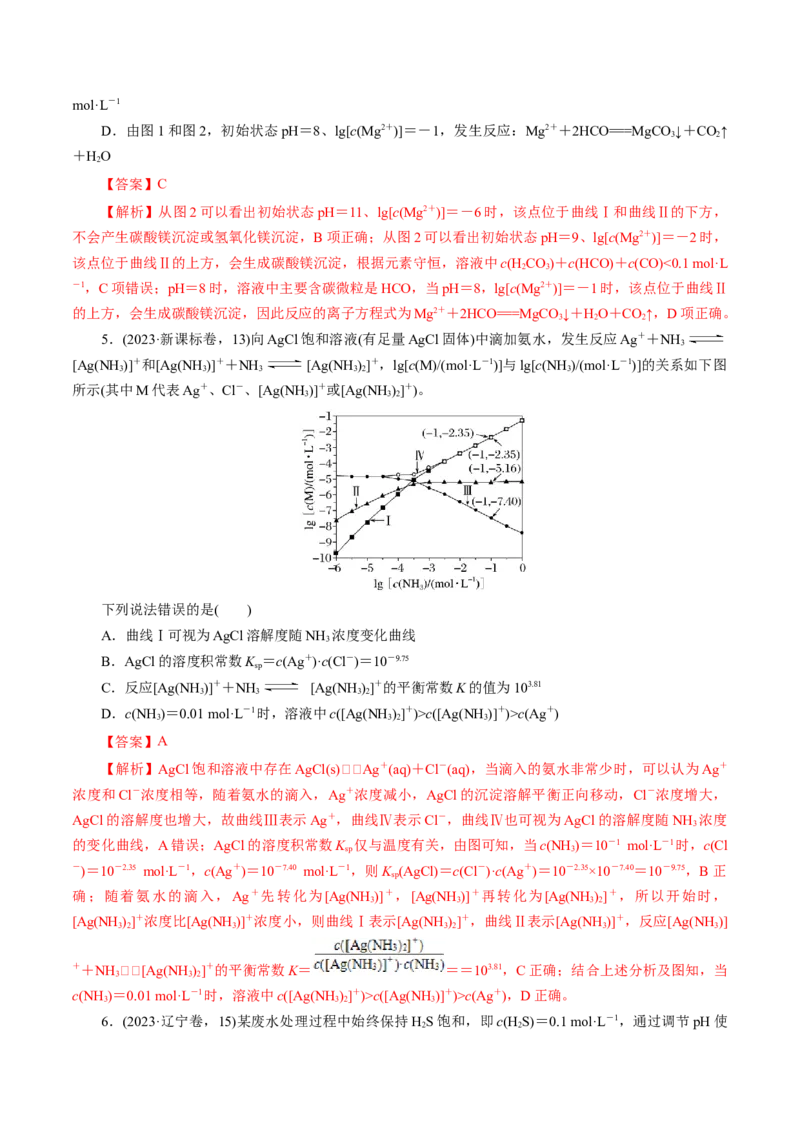
4.(2023·北京卷,14)利用平衡移动原理,分析一定温度下Mg2+在不同pH的NaCO 体系中的可能产
2 3
物。
已知:i.图1中曲线表示NaCO 体系中各含碳粒子的物质的量分数与pH的关系。
2 3
ii.图2中曲线Ⅰ的离子浓度关系符合c(Mg2+)·c2(OH-)=K [Mg(OH) ];曲线Ⅱ的离子浓度关系符合
sp 2
c(Mg2+)·c(CO)=K (MgCO )[注:起始c(Na CO)=0.1 mol·L-1,不同pH下c(CO)由图1得到]。
sp 3 2 3
下列说法不正确的是( )
A.由图1,pH=10.25,c(HCO)=c(CO)
B.由图2,初始状态pH=11、lg[c(Mg2+)]=-6,无沉淀生成
C.由图2,初始状态pH=9、lg[c(Mg2+)]=-2,平衡后溶液中存在c(H CO)+c(HCO)+c(CO)=0.1
2 3mol·L-1
D.由图1和图2,初始状态pH=8、lg[c(Mg2+)]=-1,发生反应:Mg2++2HCO===MgCO↓+CO↑
3 2
+HO
2
【答案】C
【解析】从图2可以看出初始状态pH=11、lg[c(Mg2+)]=-6时,该点位于曲线Ⅰ和曲线Ⅱ的下方,
不会产生碳酸镁沉淀或氢氧化镁沉淀,B项正确;从图2可以看出初始状态pH=9、lg[c(Mg2+)]=-2时,
该点位于曲线Ⅱ的上方,会生成碳酸镁沉淀,根据元素守恒,溶液中c(H CO)+c(HCO)+c(CO)<0.1 mol·L
2 3
-1,C项错误;pH=8时,溶液中主要含碳微粒是HCO,当pH=8,lg[c(Mg2+)]=-1时,该点位于曲线Ⅱ
的上方,会生成碳酸镁沉淀,因此反应的离子方程式为Mg2++2HCO===MgCO↓+HO+CO↑,D项正确。
3 2 2
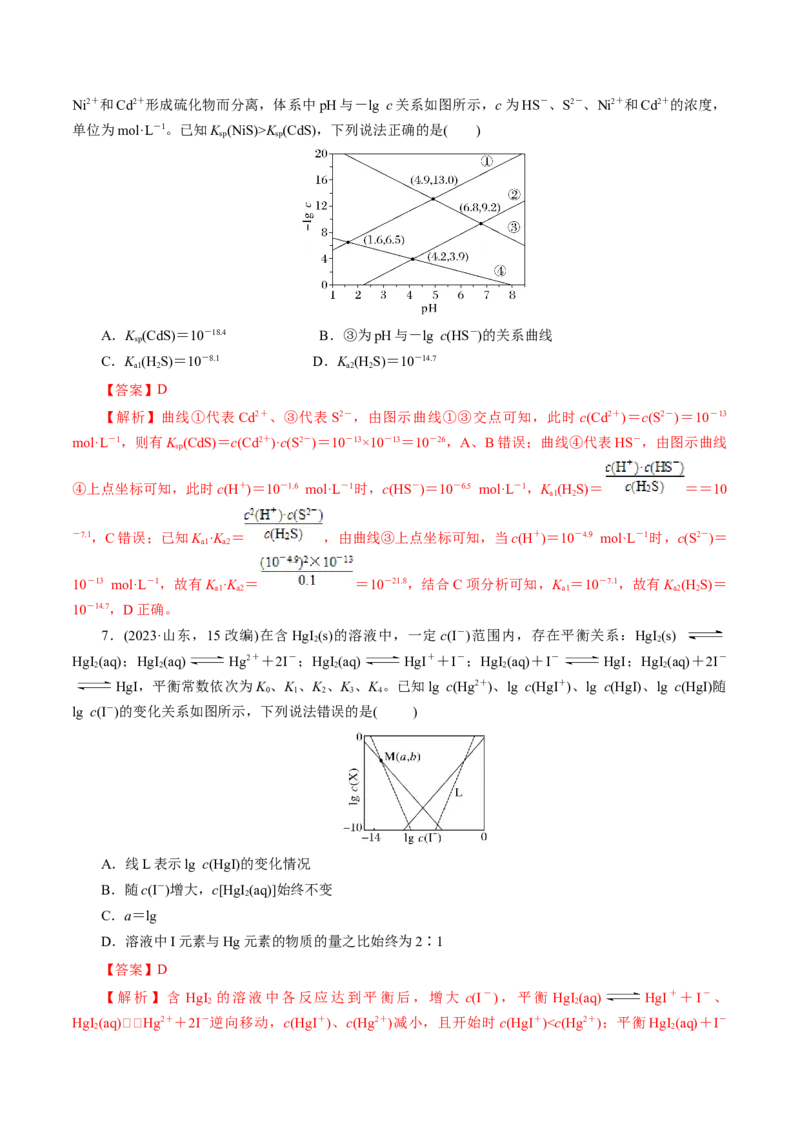
5.(2023·新课标卷,13)向AgCl饱和溶液(有足量AgCl固体)中滴加氨水,发生反应Ag++NH
3
[Ag(NH)]+和[Ag(NH)]++NH [Ag(NH)]+,lg[c(M)/(mol·L-1)]与lg[c(NH )/(mol·L-1)]的关系如下图
3 3 3 3 2 3
所示(其中M代表Ag+、Cl-、[Ag(NH)]+或[Ag(NH)]+)。
3 3 2
下列说法错误的是( )
A.曲线Ⅰ可视为AgCl溶解度随NH 浓度变化曲线
3
B.AgCl的溶度积常数K =c(Ag+)·c(Cl-)=10-9.75
sp
C.反应[Ag(NH)]++NH [Ag(NH)]+的平衡常数K的值为103.81
3 3 3 2
D.c(NH )=0.01 mol·L-1时,溶液中c([Ag(NH)]+)>c([Ag(NH)]+)>c(Ag+)
3 3 2 3
【答案】A
【解析】AgCl饱和溶液中存在AgCl(s)Ag+(aq)+Cl-(aq),当滴入的氨水非常少时,可以认为Ag+
浓度和Cl-浓度相等,随着氨水的滴入,Ag+浓度减小,AgCl的沉淀溶解平衡正向移动,Cl-浓度增大,
AgCl的溶解度也增大,故曲线Ⅲ表示Ag+,曲线Ⅳ表示Cl-,曲线Ⅳ也可视为AgCl的溶解度随NH 浓度
3
的变化曲线,A错误;AgCl的溶度积常数K 仅与温度有关,由图可知,当c(NH )=10-1 mol·L-1时,c(Cl
sp 3
-)=10-2.35 mol·L-1,c(Ag+)=10-7.40 mol·L-1,则K (AgCl)=c(Cl-)·c(Ag+)=10-2.35×10-7.40=10-9.75,B正
sp
确;随着氨水的滴入,Ag+先转化为[Ag(NH)]+,[Ag(NH)]+再转化为[Ag(NH)]+,所以开始时,
3 3 3 2
[Ag(NH)]+浓度比[Ag(NH)]+浓度小,则曲线Ⅰ表示[Ag(NH)]+,曲线Ⅱ表示[Ag(NH)]+,反应[Ag(NH)]
3 2 3 3 2 3 3
++NH [Ag(NH )]+的平衡常数K= ==103.81,C正确;结合上述分析及图知,当
3 3 2
c(NH )=0.01 mol·L-1时,溶液中c([Ag(NH)]+)>c([Ag(NH)]+)>c(Ag+),D正确。
3 3 2 3
6.(2023·辽宁卷,15)某废水处理过程中始终保持HS饱和,即c(H S)=0.1 mol·L-1,通过调节pH使
2 2Ni2+和Cd2+形成硫化物而分离,体系中pH与-lg c关系如图所示,c为HS-、S2-、Ni2+和Cd2+的浓度,
单位为mol·L-1。已知K (NiS)>K (CdS),下列说法正确的是( )
sp sp
A.K (CdS)=10-18.4 B.③为pH与-lg c(HS-)的关系曲线
sp
C.K (H S)=10-8.1 D.K (H S)=10-14.7
a1 2 a2 2
【答案】D
【解析】曲线①代表Cd2+、③代表S2-,由图示曲线①③交点可知,此时c(Cd2+)=c(S2-)=10-13
mol·L-1,则有K (CdS)=c(Cd2+)·c(S2-)=10-13×10-13=10-26,A、B错误;曲线④代表HS-,由图示曲线
sp
④上点坐标可知,此时c(H+)=10-1.6 mol·L-1时,c(HS-)=10-6.5 mol·L-1,K (H S)= ==10
a1 2
-7.1,C错误;已知K ·K = ,由曲线③上点坐标可知,当c(H+)=10-4.9 mol·L-1时,c(S2-)=
a1 a2
10-13 mol·L-1,故有K ·K = =10-21.8,结合C项分析可知,K =10-7.1,故有K (H S)=
a1 a2 a1 a2 2
10-14.7,D正确。
7.(2023·山东,15改编)在含HgI (s)的溶液中,一定c(I-)范围内,存在平衡关系:HgI (s)
2 2
HgI (aq);HgI (aq) Hg2++2I-;HgI (aq) HgI++I-;HgI (aq)+I- HgI;HgI (aq)+2I-
2 2 2 2 2
HgI,平衡常数依次为K 、K 、K 、K 、K 。已知lg c(Hg2+)、lg c(HgI+)、lg c(HgI)、lg c(HgI)随
0 1 2 3 4
lg c(I-)的变化关系如图所示,下列说法错误的是( )
A.线L表示lg c(HgI)的变化情况
B.随c(I-)增大,c[HgI (aq)]始终不变
2
C.a=lg
D.溶液中I元素与Hg元素的物质的量之比始终为2∶1
【答案】D
【解析】含 HgI 的溶液中各反应达到平衡后,增大 c(I-),平衡 HgI (aq) HgI++I-、
2 2
HgI (aq)Hg2++2I-逆向移动,c(HgI+)、c(Hg2+)减小,且开始时c(HgI+)c(HgI)。分析可知,
2
线L表示lg c(HgI)的变化情况,A正确;HgI (s) HgI (aq)的化学平衡常数K =c[HgI (aq)],温度不变
2 2 0 2
平衡常数不变,故随c(I-)增大,c[HgI (aq)]始终保持不变,B正确; , ,
2
带入M点值可得 , ,则可得a=lg,C正确;需要外加I-调节,则I元素与
Hg元素的物质的量之比无法确定,D错误。
8.(2021·广东,18节选)对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝(Al)、钼
(Mo)、镍(Ni)等元素的氧化物,一种回收利用工艺的部分流程如下:
已知:25 ℃时,HCO 的K =4.5×10-7,K =4.7×10-11;K (BaMoO )=3.5×10-8;K (BaCO)=
2 3 al a2 sp 4 sp 3
2.6×10-9;该工艺中,pH>6.0时,溶液中Mo元素以MoO的形态存在。
(1)“焙烧”中,有NaMoO 生成,其中Mo元素的化合价为__________。
2 4
(2)“沉铝”中,生成的沉淀X为________。
(3)“沉钼”中,pH为7.0。
①生成BaMoO 的离子方程式为__________________________________________。
4
②若条件控制不当,BaCO 也会沉淀。为避免BaMoO 中混入BaCO 沉淀,溶液中c(HCO)∶c(MoO)
3 4 3
=_________________(列出算式)时,应停止加入BaCl 溶液。
2
【答案】(1)+6 (2)Al(OH) (3)①MoO+Ba2+===BaMoO ↓ ②
3 4
【解析】(3)②若开始生成BaCO 沉淀,则体系中恰好建立如下平衡:HCO+BaMoO BaCO +
3 4 3
MoO+H+,该反应的化学平衡常数K===。为避免BaMoO 中混入BaCO 沉淀,必须满足≤,由于“沉
4 3
钼”中 pH 为 7.0,c(H+)=1×10-7 mol·L-1,所以溶液中=时,开始生成 BaCO 沉淀,因此,
3
c(HCO)∶c(MoO)==时,应停止加入BaCl 溶液。
2
9.(2022•辽宁省选择性,17节选) H O 作为绿色氧化剂应用广泛,氢醌法制备HO。
2 2 2 2
(7)取 产品,加蒸馏水定容至 摇匀,取 于锥形瓶中,用0.0500mol·L-1酸性
KMnO 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为19.98mL、20.90mL、20.02mL。假设其他
4
杂质不干扰结果,产品中HO 质量分数为___________。
2 2
【答案】(7)17%
【解析】(7)滴定反应的离子方程式为2 MnO-+5H O+6H+=2 Mn2++5O ↑+8H O,可得关系式:2
4 2 2 2 2
KMnO ~5H O。三组数据中20.90mL偏差较大,舍去,故消耗酸性高锰酸钾标准溶液的平均体积为
4 2 220.00mL,HO 的质量分数 。
2 2