文档内容
专题 08 电化学及其应用
1.(2022·广东卷)以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,实现 的再生。
该过程中
A.阴极发生的反应为 B.阴极上 被氧化
C.在电解槽底部产生含 的阳极泥 D.阳极和阴极的质量变化相等
【答案】C
【解析】根据电解原理可知,电解池中阳极发生失电子的氧化反应,阴极发生得电子的还原反应,该题中
以熔融盐为电解液,含 和 等的铝合金废料为阳极进行电解,通过控制一定的条件,从而可使阳
极区Mg和Al发生失电子的氧化反应,分别生成Mg2+和Al3+,Cu和Si不参与反应,阴极区Al3+得电子生
成Al单质,从而实现Al的再生,据此分析解答。
A.阴极应该发生得电子的还原反应,实际上Mg在阳极失电子生成Mg2+,A错误;
B.Al在阳极上被氧化生成Al3+,B错误;
C.阳极材料中Cu和Si不参与氧化反应,在电解槽底部可形成阳极泥,C正确;
D.因为阳极除了铝参与电子转移,镁也参与了电子转移,且还会形成阳极泥,而阴极只有铝离子得电子
生成铝单质,根据电子转移数守恒及元素守恒可知,阳极与阴极的质量变化不相等,D错误;
故选C。
2.(2022·全国甲卷)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示(KOH溶液中,Zn2+以Zn(OH)
2
存在)。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C. MnO 电极反应:MnO +2e-+4H+=Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O
2 2
【答案】A
【解析】根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-2e-+4OH-
=Zn(OH) ,Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+=Mn2++2H O;电池在工作过程中,由于
2 2 2
两个离子选择隔膜没有指明的阳离子隔膜还是阴离子隔膜,故两个离子隔膜均可以通过阴、阳离子,因此
可以得到Ⅰ区消耗H+,生成Mn2+,Ⅱ区的K+向Ⅰ区移动或Ⅰ区的SO 向Ⅱ区移动,Ⅲ区消耗OH-,生成
Zn(OH) ,Ⅱ区的SO 向Ⅲ区移动或Ⅲ区的K+向Ⅱ区移动。据此分析答题。
A.根据分析,Ⅱ区的K+只能向Ⅰ区移动,A错误;
B.根据分析,Ⅰ区的SO 向Ⅱ区移动,B正确;
C.MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;
2 2 2
D.电池的总反应为Zn+4OH-+MnO+4H+=Zn(OH) +Mn2++2H O,D正确;
2 2
故答案选A。
3.(2022·全国乙卷) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究了
一种光照充电 电池(如图所示)。光照时,光催化电极产生电子 和空穴 ,驱动阴极反应
和阳极反应(Li O+2h+=2Li++O )对电池进行充电。下列叙述错误的是
2 2 2A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
【答案】C
【解析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应(Li O+2h+=2Li+
2 2
+O ),则充电时总反应为LiO=2Li+O ,结合图示,充电时金属Li电极为阴极,光催化电极为阳极;则放
2 2 2 2
电时金属Li电极为负极,光催化电极为正极;据此作答。
A.光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳
极反应,充电时电池的总反应为LiO=2Li+O ,A正确;
2 2 2
B.充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率
与光照产生的电子和空穴量有关,B正确;
C.放电时,金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;
D.放电时总反应为2Li+O=Li O,正极反应为O+2Li++2e-=Li O,D正确;
2 2 2 2 2 2
答案选C。
4.(2022·浙江卷)通过电解废旧锂电池中的 可获得难溶性的 和 ,电解示意图如下(其
中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法不正
确的是A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中 浓度保持不变
D.电解结束,可通过调节 除去 ,再加入 溶液以获得
【答案】C
【解析】A.由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则电极B
2
为阳极,电极A为阴极,得电子,发生还原反应,A正确;
B.由电解示意图可知,电极B上Mn2+失电子转化为了MnO ,电极反应式为:2HO+Mn2+-2e-
2 2
=MnO+4H+,B正确;
2
C.电极A为阴极, LiMn O 得电子,电极反应式为:2LiMn O+6e-+16H+=2Li++4Mn2++8H O,依据得失
2 4 2 4 2
电子守恒,电解池总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,反应生成了Mn2+,Mn2+浓度增大,
2 4 2 2
C错误;
D.电解池总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,电解结束后,可通过调节溶液pH将锰离
2 4 2 2
子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确;
答案选C。
5.(2022·湖南卷)海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的
是A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
【答案】B
【解析】锂海水电池的总反应为2Li+2HO═2LiOH+H ↑, M极上Li失去电子发生氧化反应,则M电极为
2 2
负极,电极反应为Li-e-=Li+,N极为正极,电极反应为2HO+2e-=2OH-+H ↑,同时氧气也可以在N极得电
2 2
子,电极反应为O+4e-+2H O=4OH-。
2 2
A.海水中含有丰富的电解质,如氯化钠、氯化镁等,可作为电解质溶液,故A正确;
B.由上述分析可知,N为正极,电极反应为2HO+2e-=2OH-+H ↑,和反应O+4e-+2H O=4OH-,故B错误;
2 2 2 2
C.Li为活泼金属,易与水反应,玻璃陶瓷的作用是防止水和Li反应,并能传导离子,故C正确;
D.该电池不可充电,属于一次电池,故D正确;
答案选B。
6.(2022·广东卷)科学家基于 易溶于 的性质,发展了一种无需离子交换膜的新型氯流电池,可作储
能设备(如图)。充电时电极a的反应为: 。下列说法正确的是
A.充电时电极b是阴极
B.放电时 溶液的 减小
C.放电时 溶液的浓度增大
D.每生成 ,电极a质量理论上增加
【答案】C
【解析】A.由充电时电极a的反应可知,充电时电极a发生还原反应,所以电极a是阴极,则电极b是阳
极,故A错误;B.放电时电极反应和充电时相反,则由放电时电极a的反应为 可
知,NaCl溶液的pH不变,故B错误;
C.放电时负极反应为 ,正极反应为 ,反应后
Na+和Cl-浓度都增大,则放电时NaCl溶液的浓度增大,故C正确;
D.充电时阳极反应为 ,阴极反应为 ,由得失电
子守恒可知,每生成1molCl ,电极a质量理论上增加23g/mol 2mol=46g,故D错误;
2
答案选C。
1.(2022·云南曲靖·二模)科学家设计了一种高效、低能耗制备HO 的装置,装置如图所示。下列有关说法
2 2
不正确的是
A.阴极区产生2molOH-时,参加反应的O 在标准状况下的体积为11.2L
2
B.a为电源的正极
C.阳极区反应为 −2e-+3OH-=2H O+
2
D.该装置中,离子交换膜为阴离子交换膜
【答案】A
【解析】右边氧气变双氧水,氧化合价降低,说明右边是阴极,则b为负极,a为正极,左边为阳极。
A.阴极电极反应式O+2e-+2HO=HO+2OH-,则阴极区产生2molOH-时,参加反应的O 为
2 2 2 2 21mol,在标准状况下的体积为22.4L,故A错误;
B.根据前面分析a为电源的正极,故B正确;
C.根据前面得到左边是阳极, 被氧化,因此阳极区反应式为 −2e-
+3OH-=2H O+ ,故C正确;
2
D.该装置中,氢氧根在阳极消耗,因此阴极产生的氢氧根要转移到阳极区域,则离子交换膜为阴离子交
换膜,故D正确。
综上所述,答案为A。
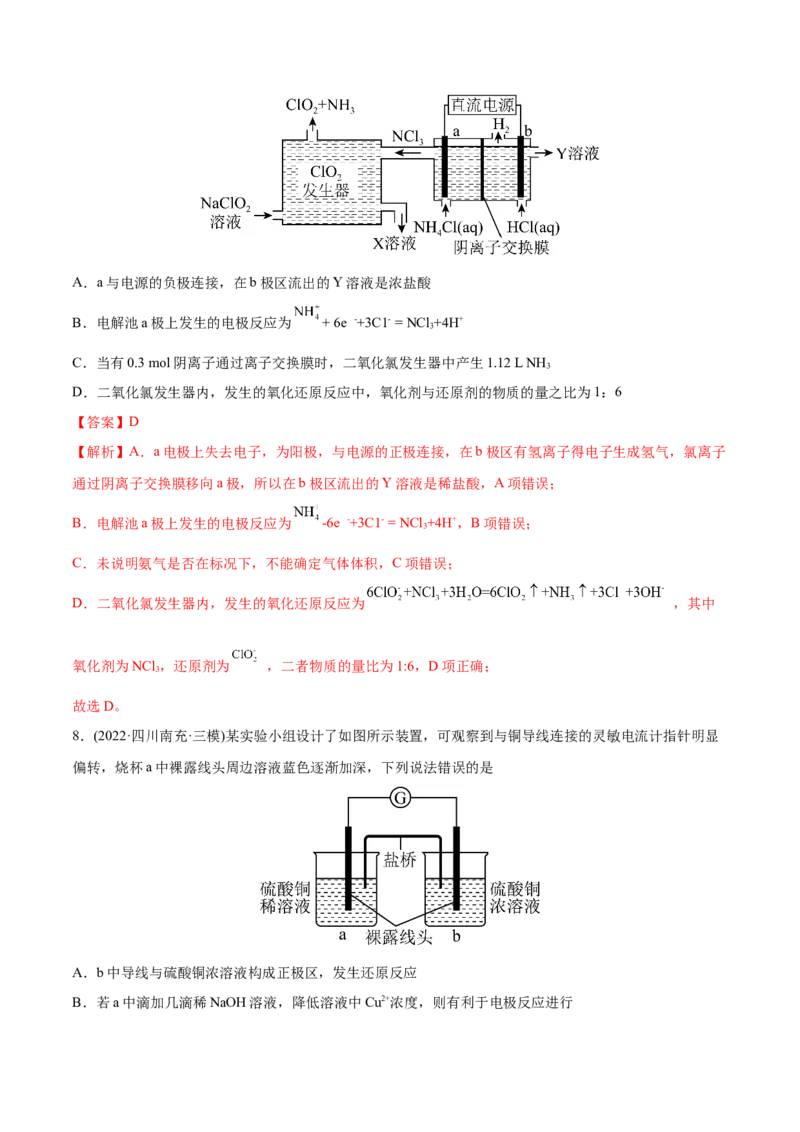
2.(2022·贵州遵义·二模)镍镉电池是一种新型的封闭式体积小的充电电池。其工作原理如图所示,下列说
法错误的是
A.放电时b极为正极
B.放电时a极的反应
C.充电时电流的方向:外电源正极→b极→电解质溶液→a极
D.用该电池提供的电能电解饱和食盐水,电路中通过0.2mol e-,阴极生成0.2gH
2
【答案】B
【解析】根据化合价升降,左边化合价升高,失去电子,作负极,右边化合价降低,得到电子,作正极。
A.根据图中信息电子从左转移到右边,因此放电时a极为负极, b极为正极,故A正确;
B.根据图中负极Cd变为Cd(OH) ,则放电时a极的反应 ,故B错误;
2
C.充电时电流的方向从:外电源正极→阳极(b极)→电解质溶液→阴极(a极)→外电源负极,故C正确;
D.用该电池提供的电能电解饱和食盐水,阴极反应式为HO+2e-=H↑+2OH-,电路中通过0.2mol e
2 2
-,则阴极生成氢气物质的量为0.1mol,质量为0.2g,故D正确;综上所述,答案为B。
3.(2022·云南昆明·一模)间接电氧化苯甲醇(C HCHOH)合成苯甲醛(C HCHO)是一种绿色生产工艺。我国
6 5 2 6 5
学者利用Ce4+/Ce3+为媒介在酸性水溶液中合成苯甲醛,工作原理如图所示。下列说法正确的是
A.电极b与电源正极相连
B.一段时间后,体系中Ce3+浓度逐渐减小
C.生成0.2molC HCHO时,电极b上生成H4.48L(标准状况)
6 5 2
D.阳极的电极反应式为C HCHOH-2e-=C HCHO+2H+
6 5 2 6 5
【答案】C
【解析】电极a上Ce元素化合价升高,发生氧化反应,则a为阳极,电极反应式为Ce3+-e-=Ce4+,电极b为
阴极,在酸性水溶液中氢离子得到电子生成氢气,电极反应式为2H++2e-=H ;
2
A.由电极a上Ce元素化合价升高,则a为阳极,b为阴极,阴极与电源负极相连,A错误;
B.由于Ce3+和 Ce4+之间是循环反应,则体系中Ce3+浓度保持不变,B错误;
C. C HCHOH→ C HCHO过程中失去2个电子,生成0.2molC HCHO时,转移0.4mol电子,电极b上
6 5 2 6 5 6 5
电极反应式为2H++2e-=H ,则生成0.2mol氢气,标准状况下生成H 体积为V=nVm=0.2mol×22.4L/
2 2
mol=4.48L,C正确;
D.分析可知,电极a上Ce元素化合价升高,阳极的电极反应式为Ce3+-e-=Ce4+,D错误;
故选:C。
4.(2022·广西·一模)在一种微生物细菌作用下苯酚可以转化为CO,目前,某研究团队利用电化学原理来
2
模拟处理废水中的苯酚(C HOH),其工作原理如图所示。下列说法错误的是
6 5A.a极为正极,M为阳离子交换膜
B.b极的电极反应式为 C HOH-28e-+11H O = 6CO ↑+28H+
6 5 2 2
C.NaCl溶液的作用是增强导电性
D.电池工作过程中,a极室的pH升高
【答案】A
【解析】由题可知,此装置为原电池,a极物质由Cr O 转化为Cr(OH) 化合价降低,为正极,则b极为负
2 3
极,据此解答。
A.由图可知,a极发生还原反应Cr O 转化为Cr(OH) 同时生成氢氧根,则 M为阴离子交换膜,使氢氧
2 3
根通过,故A错误;
B.b极苯酚发生氧化反应生成CO,电极反应式为C HOH-28e-+11H O = 6CO ↑+28H+,故B正确;
2 6 5 2 2
C.氯化钠溶液的作用是增强溶液导电性,故C正确;
D.电池工作过程中,a极室发生反应Cr O +6e-+7H O=2Cr(OH) ↓+8OH-,a极室的pH升高,故D正确;
2 2 3
故答案选A。
5.(2022·广西南宁·二模)KIO 广泛用于化工、医学和生活中,工业上制备KIO 的工作原理如图所示,下列
3 3
说法正确的是A.a为正极,B极上发生氧化反应
B.电子流向:A→a→b→B
C.X气体是H,每转移2mole-,可产生22.4LX气体
2
D.A极的电极反应式为:I-+6OH--6e-=IO +3H O
2
【答案】D
【解析】根据图示,该装置为电解池,A电极上I-发生失电子的氧化反应生成 ,A电极为阳极,则a为
电源的正极,b为电源的负极,B电极为阴极;据此分析作答。
A.a为电源的正极,B电极为阴极,B极上发生得电子的还原反应,A错误;
B.A电极为阳极,a为电源的正极,b为电源的负极,B电极为阴极,电子流向为:A→a、b→B,电子不
通过电源的内电路,B错误;
C.B极电极反应式为2HO+2e-=H ↑+2OH-,X气体是H,每转移2mole-生成1molH ,由于H 所处温度和
2 2 2 2 2
压强未知,不能计算H 的体积,C错误;
2
D.A电极上I-发生失电子的氧化反应生成 ,电极反应式为I-+6OH--6e-= +3H O,D正确;
2
答案选D。
6.(2022·广西柳州·二模)实现“碳中和”的重要方式之一是将 重新转化成能源,在金属氧化物电解池,
高温下电解 的混合气体制备 和CO是一种新的能源利用方式,基本原理如图所示。下列说法
错误的是A.Y是电源的正极
B.阳极的电极反应式是
C.总反应可表示为
D.阴阳两极生成的气体的物质的量之比是1:2
【答案】D
【解析】由图可知产生氢气和CO的电极H、C化合价降低,发生还原反应,为电解池阴极,则X是电源
的负极,Y为正极。
A.由分析知A正确;
B.金属氧化物为电解质,则阳极的反应式为2O2--4e-=O ↑,B正确;
2
C.由图可知反应物为水和二氧化碳,生成物为氢气、一氧化碳、氧气,则该电解池的总反应可表示为
,C正确;
D.结合总反应 可知阴极每产生1 mol H 和1 mol CO的同时阳极产生1 mol O ,则
2 2
阴、阳两极生成的气体的物体的量之比是2:1,D错误;
故答案选D。
7.(2022·四川自贡·三模)应对新冠肺炎疫情时所采取的措施是对环境进行彻底消毒,二氧化氯(C1O,黄绿
2
色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制
备ClO 的原理如图所示。下列说法正确的
2A.a与电源的负极连接,在b极区流出的Y溶液是浓盐酸
B.电解池a极上发生的电极反应为 + 6e -+3C1- = NCl +4H+
3
C.当有0.3 mol阴离子通过离子交换膜时,二氧化氯发生器中产生1.12 L NH
3
D.二氧化氯发生器内,发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为1:6
【答案】D
【解析】A.a电极上失去电子,为阳极,与电源的正极连接,在b极区有氢离子得电子生成氢气,氯离子
通过阴离子交换膜移向a极,所以在b极区流出的Y溶液是稀盐酸,A项错误;
B.电解池a极上发生的电极反应为 -6e -+3C1- = NCl +4H+,B项错误;
3
C.未说明氨气是否在标况下,不能确定气体体积,C项错误;
D.二氧化氯发生器内,发生的氧化还原反应为 ,其中
氧化剂为NCl ,还原剂为 ,二者物质的量比为1:6,D项正确;
3
故选D。
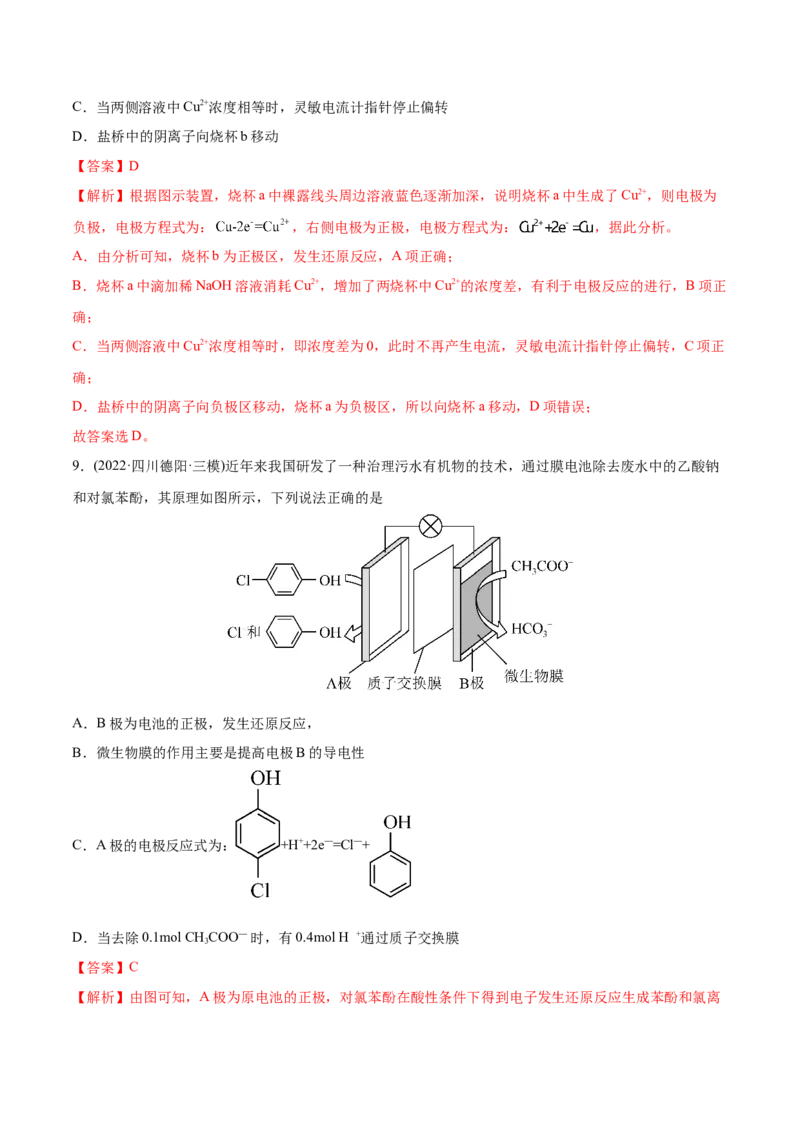
8.(2022·四川南充·三模)某实验小组设计了如图所示装置,可观察到与铜导线连接的灵敏电流计指针明显
偏转,烧杯a中裸露线头周边溶液蓝色逐渐加深,下列说法错误的是
A.b中导线与硫酸铜浓溶液构成正极区,发生还原反应
B.若a中滴加几滴稀NaOH溶液,降低溶液中Cu2+浓度,则有利于电极反应进行C.当两侧溶液中Cu2+浓度相等时,灵敏电流计指针停止偏转
D.盐桥中的阴离子向烧杯b移动
【答案】D
【解析】根据图示装置,烧杯a中裸露线头周边溶液蓝色逐渐加深,说明烧杯a中生成了Cu2+,则电极为
负极,电极方程式为: ,右侧电极为正极,电极方程式为: ,据此分析。
A.由分析可知,烧杯b为正极区,发生还原反应,A项正确;
B.烧杯a中滴加稀NaOH溶液消耗Cu2+,增加了两烧杯中Cu2+的浓度差,有利于电极反应的进行,B项正
确;
C.当两侧溶液中Cu2+浓度相等时,即浓度差为0,此时不再产生电流,灵敏电流计指针停止偏转,C项正
确;
D.盐桥中的阴离子向负极区移动,烧杯a为负极区,所以向烧杯a移动,D项错误;
故答案选D。
9.(2022·四川德阳·三模)近年来我国研发了一种治理污水有机物的技术,通过膜电池除去废水中的乙酸钠
和对氯苯酚,其原理如图所示,下列说法正确的是
A.B极为电池的正极,发生还原反应,
B.微生物膜的作用主要是提高电极B的导电性
C.A极的电极反应式为: +H++2e—=Cl—+
D.当去除0.1mol CH COO— 时,有0.4mol H +通过质子交换膜
3
【答案】C
【解析】由图可知,A极为原电池的正极,对氯苯酚在酸性条件下得到电子发生还原反应生成苯酚和氯离子,电极反应式为 +H++2e—=Cl—+ ,B极为负极,乙酸根离子在微生物膜做催化剂的作用下
失去电子发生氧化反应生成碳酸氢根离子和氢离子,电极反应式为CHCOO——8e—+4H O=2HCO +9H+。
3 2
A.由分析可知,B极为负极,乙酸根离子在微生物膜做催化剂的作用下失去电子发生氧化反应生成碳酸
氢根离子和氢离子,故A错误;
B.由分析可知,微生物膜的作用主要是做催化剂,使乙酸根离子失去电子发生氧化反应生成碳酸氢根离
子和氢离子,故B错误;
C.由分析可知,A极为原电池的正极,对氯苯酚在酸性条件下得到电子发生还原反应生成苯酚和氯离子,
电极反应式为 +H++2e—=Cl—+ ,故C正确;
D.负极反应式为CHCOO——8e—+4H O=2HCO +9H+,消耗0.1mol乙酸根离子时,转移电子的物质的量
3 2
为0.8mol,整个电路中通过的电量相同,因此去除0.1mol乙酸根离子时,有0.8mol氢离子通过质子交换膜,
故D错误;
故选C。
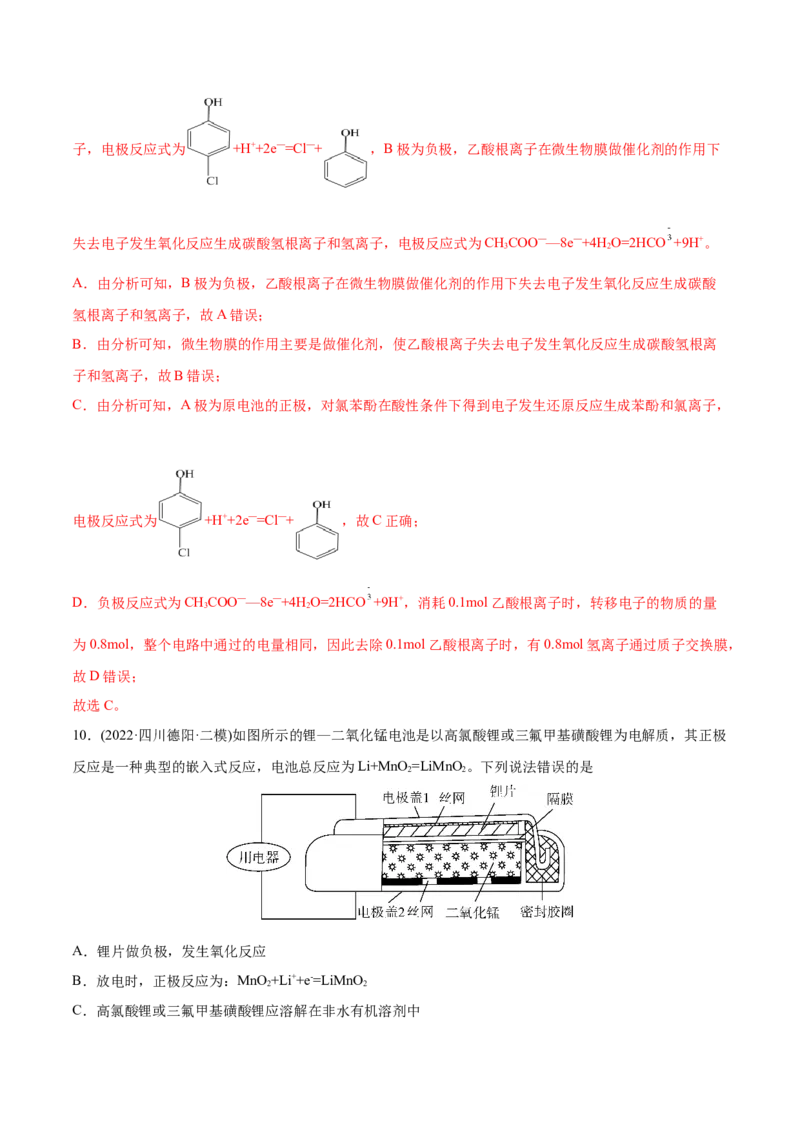
10.(2022·四川德阳·二模)如图所示的锂—二氧化锰电池是以高氯酸锂或三氟甲基磺酸锂为电解质,其正极
反应是一种典型的嵌入式反应,电池总反应为Li+MnO =LiMnO 。下列说法错误的是
2 2
A.锂片做负极,发生氧化反应
B.放电时,正极反应为:MnO +Li++e-=LiMnO
2 2
C.高氯酸锂或三氟甲基磺酸锂应溶解在非水有机溶剂中D.放电时,电子移动方向为:电极盖1→用电器→电极盖2→内电路→电极盖1
【答案】D
【解析】由电池总反应Li+MnO =LiMnO 可知Li失电子,MnO 得电子,负极反应式为Li-e-=Li+,Li+向正
2 2 2
极移动,正极反应式为MnO +Li++e-=LiMnO 。
2 2
A.Li失电子,作负极,发生氧化反应,A正确;
B.放电时,MnO 在正极得电子,正极反应为:MnO +Li++e-=LiMnO ,B正确;
2 2 2
C.负极Li是活泼金属,能与水反应,故高氯酸锂或三氟甲基磺酸锂应溶解在非水有机溶剂中,C正确;
D.放电时属于原电池装置,电子从负极经用电器流向正极,不在电解质中移动,故放电时,电子移动方
向为:电极盖1→用电器→电极盖2,D错误;
答案选D。
11.(2022·四川南充·二模)污水资源化利用既可以缓解水的供需矛盾,又可以减少水污染。化学工作者提出
采用电解法除去工业污水中的NaCN,其原理如图所示,通电前先向污水中加入适量食盐并调整其pH维持
碱性(CN-不参与电极反应)。下列说法正确的是
A.b为电源的负极
B.隔膜I为阴离子交换膜
C.x为H,电极反应为:2HO+2e-=H ↑+2OH-
2 2 2
D.当生成2.24LN 时,电路中通过1mol电子
2
【答案】C
【解析】A.右侧氯离子放电得到次氯酸根离子,次氯酸根离子再氧化CN-为氮气,所以右侧电极为阳极,
b为电源的正极,故A错误;
B.由A知b为电源的正极,则a为电源的负极,左侧电极为阴极,发生2HO+2e-=H ↑+2OH-,阴离子增加,
2 2
污水中的钠离子会通过隔膜I进入左侧,形成氢氧化钠溶液,所以隔膜I为阳离子交换膜,故B错误;
C.由A、B可知左侧电极反应为:2HO+2e-=H ↑+2OH-,则x为H,故C正确;
2 2 2
D.生成的2.24LN 未标明条件,无法求得电路中通过电子的量,故D错误;
2故答案为:C。
12.(2022·四川成都·二模)钠离子电池易获取,正负极材料均采用铝箔(可减少铜箔用量),因此钠离子电池
理论成本低于锂离子电池。现有一种正极材料为KFe (CN) ,固体电解质为NaPS ,负极材料为NaTi O
2 6 3 4 2 3 7
的钠离子电池。下列有关叙述错误的是
A.正极KFe (CN) 中Fe的化合价为+2、+3
2 6
B.放电时,正极可能发生Fe (CN) +e-=Fe (CN)
2 2
C.放电时,电子从负极流经固体电解质到达正极
D.充电时,负极区发生还原反应,并且Na+增多
【答案】C
【解析】A.钾离子呈+1价、CN-为-1价,化合物中元素的正负化合价代数和为0,则正极KFe (CN) 中Fe
2 6
的化合价为+2、+3,A正确;
B. 放电时,正极发生还原反应,可能发生Fe (CN) +e-=Fe (CN) ,B正确;
2 2
C. 放电时,电子从负极流经导线到达正极,电子不流经固体电解质,C不正确;
D. 充电时,负极区即阴极发生还原反应,阳离子向阴极移动,则Na+增多,D正确;
答案选C。
13.(2022·四川绵阳·二模)科学家利用质子导体反应器实现了电化学合成NH ,证明了HO作为氢源的可行
3 2
性。以HO替换H 作为氢源,可以免除H 的生产和提纯成本,进一步降低氨的生产成本,且可以以最小
2 2 2
的成本生产纯O,其工作原理如图所示。下列说法错误的是
2A.氨电极为阴极,电极反应为N+6H++6e-=2NH
2 3
B.在外电场作用下,H+由氢电极经固体电解质移
C.每制得1molNH ,理论上消耗1.5mol H 同时得到48g氧气
3 2
D.若在氢电极通入水蒸气和甲烷,电极反应为CH+2H O-8e-=CO +8H+
4 2 2
【答案】C
【解析】氨电极上N元素化合价降低,为阴极,电极反应为N+6H++6e-=2NH,氢电极上O元素化合价升
2 3
高,为阳极,电极反应为2HO-4e-=O ↑+4H+;
2 2
A.氨电极上N元素化合价降低,发生还原反应,为阴极,电极反应为N+6H++6e-=2NH,故A正确;
2 3
B.氨电极为阴极,氢电极为阳极,阳离子移向阴极,H+由氢电极经固体电解质移向氨电极,故B正确;
C.阳极反应式为2HO-4e-=O +4H+,不消耗氢气,故C错误;
2 2
D.氢电极为阳极,通入水蒸气和甲烷,C元素化合价升高,电极反应为CH+2H O-8e-=CO +8H+,故D正
4 2 2
确;
故选:C。
14.(2022·河南洛阳·三模)我国科研团队开发了一种新型铠甲催化剂Ni/Co@石墨烯,可以高效去除合成气
中的HS杂质并耦合产氢,其工作原理如图所示。下列说法错误的是
2
A.M电极为阴极,电极上发生还原反应
B.生成H 和S 的物质的量之比为1:x
2 x
C.阳极的电极反应式为xHS- 2xe- =S +2xH+
2 x
D.铠甲催化剂表面的石墨烯可以保护内部金属核免受环境的影响
【答案】B
【解析】由题干电解池装置图可知,Na+由右侧电极室进入左侧电极室,说明n为电源的正极,铠甲催化剂
电极为阳极发生氧化反应,电极反应式为:xHS-2xe-=S +2xH+,m为电源的负极,M电极为阴极发生还原
2 x
反应,电极反应为:2H++2e-=H ↑,据此分析解题。
2
A.由分析可知,M电极为阴极,电极上发生还原反应,A正确;
B.根据电子守恒并结合阳极反应式:xHS-2xe-=S +2xH+和阴极反应式2H++2e-=H ↑可知,生成H 和S 的
2 X 2 2 x
物质的量之比为x:1,B错误;
C.由分析可知,阳极的电极反应式为xHS- 2xe- =S +2xH+,C正确;
2 xD.由分析可知,铠甲催化剂电极为阳极,若没有表面的石墨烯则容易内部金属放电,故铠甲催化剂表面
的石墨烯可以保护内部金属核免受环境的影响,D正确;
故答案为:B。
15.(2022·河南商丘·三模)某科研团队研制了一种基于阳离子型活性分子的中性水系有机液流电池,以[Pyr-
TEMPO]和[Pyr-PV]Cl 作中性水系有机液流电池的电极材料,已知放电时[Pyr-PV]2+先转化为[Pyr-PV]3+,后
4
转化为[Pyr-PV]4+,电池工作原理如图所示。下列说法正确的是
A.放电的过程中,氯离子由b电极向a电极移动
B.放电时,负极的电极反应之一为[Pyr-PV]3+- =[Pyr-PV]4+
C.a电极的电势比b电极的低
D.充电时,b电极为阳极,发生氧化反应
【答案】B
【解析】已知放电时 先转化为 ,后转化为 ,可知b电极失电子,发生氧
化反应,为电源负极,则a电极为正极,即放电时,a电极为正极,b电极为负极。
A.由分析可知,放电时,a电极为正极,b电极为负极,则氯离子由a电极向b电极移动,A错误:
B.已知放电时 先转化为 ,后转化为 ,则负极的电极反应之一为
,B正确;
C.由分析可知,放电时,a电极为正极,b电极为负极,则充电时,a电极为阳极,b电极为阴极,故无论
放电或充电,a电极的电势均比b电极的高,C错误;D.由C选项可知,充电时,b电极为阴极,发生还原反应,D错误;
故选B。
16.(2022·河南新乡·三模)我国科学家研发出一种绿色锌碘单液流二次电池,工作原理如图所示。下列说法
错误的是
A.放电时,聚烯烃多孔电极上发生氧化反应
B.放电时,K+向多孔石墨电极迁移
C.充电时,阳极反应式为2I--2e-=I
2
D.充电时,阴极净增65g时a区净增2mol离子
【答案】D
【解析】装置连接用电器时,该装置为电池装置,连接光伏电池时,该装置为电解装置,若为电池时,根
据原电池工作原理,以及装置图可知,聚烯烃多孔电极为负极,电极反应式为Zn-2e-=Zn2+,多孔石墨电极
为正极,电极反应式为I+2e-=2I-,据此分析。
2
A.根据上述分析,放电时,聚烯烃多孔电极作负极,化合价升高,发生氧化反应,故A正确;
B.根据原电池工作原理,阳离子向正极移动,即放电时,K+向多孔石墨电极迁移,故B正确;
C.充电时,电池正极接电源的正极,阳极的电极反应式为2I--2e-=I ,故C正确;
2
D.充电时,阴极电极反应式为Zn2++2e-=Zn,增加65g锌,转移电子物质的量2mol,所以C区增加
2molK+、2molCl-,离子总数为4mol,故D错误;
答案为D。
17.(2022·河南郑州·二模)钛铁合金具有优异的性能,在航天和生物医学等领域有广泛的应用。下图是以二
氧化钛、氧化亚铁混合粉末压制的块体和石墨坩埚分别做电极材料,以CaCl 熔盐为离子导体(不参与电极
2
反应)制备钛铁合金的电解装置示意图。下列相关说法正确的是A.石墨坩埚连接直流电源的负极
B.通入Ar气主要是为了保护石墨坩埚不被氧化
C.TiO 发生的电极反应为:TiO-4e-=Ti+2O2-
2 2
D.每生成16.0g TiFe 时,流出气体在标准状况下的体积大于4.48L
2
【答案】D
【解析】该装置的目的是制备钛铁合金,所以需要Fe2+、Ti4+发生还原反应,而CaCl 熔盐不参与电极反应,
2
所以阳极应是O2-被氧化生成氧气。
A.电解过程中需要Fe2+、Ti4+发生还原反应,所以以二氧化钛、氧化亚铁混合粉末压制的块体应为阴极,
连接电源的负极,A错误;
B.Ti、Fe性质活泼,容易被生成的氧气氧化,所以通入Ar气主要是为了保护钛铁合金不被氧化,B错误;
C.TiO 得电子发生还原反应,电极反应应为TiO+4e-=Ti+2O2-,C错误;
2 2
D.16.0g TiFe ,即 =0.1mol,需生成0.1mol Ti、0.2mol Fe,根据电极反应TiO+4e-=Ti+2O2-、
2 2
FeO+2e-=Fe+O2-可知,共转移0.8mol电子,O2-在阳极被还原,电极反应为2O2--4e-=O ↑,所以生成
2
0.2mol氧气,标况下体积为0.2mol×22.4L/mol=4.48L,但同时流出的气体还有Ar,所以流出气体在标准状
况下的体积大于4.48L,D正确;
综上所述答案为D。
18.(2022·山西太原·三模)某微生物燃料电池在废水处理和新能源开发领域具有广阔的应用前景,其工作原
理如图所示。下列说法正确的是A.电极电势a< b,电极b上发生氧化反应
B.HS-在硫氧化菌作用下发生反应 HS-+ 4H O- 8e- = +9H+
2
C.若该电池外电路有0.4 mol电子转移,则 有0.45molH+迁移到b极。
D.该燃料电池在高温下进行效率更高
【答案】B
【解析】由图可知,b极为正极,电极反应式为O+4e-+4H+=2H O,a极为负极,电极反应式为HS-
2 2
+4H O-8e-= +9H+,据此作答。
2
A.a极为负极,b极为正极,发生还原反应,电极电势a<b,A错误;
B.a极为负极,电极反应式为HS-+4H O-8e-= +9H+,B正确;
2
C.该电池外电路有0.4mol电子转移,由电荷守恒可知,有0.4molH+迁移到b极,C错误;
D.微生物在高温下会死亡,降低电池效率,D错误;
故答案为:B。
19.(2022·山西临汾·三模)酸性水系锌锰电池在放电时电极上的MnO 部分脱落,会造成电池效率“损失”。
2
最新研究表明,向体系中加入少量KI固体能使电池持续大电流放电,提高电池的工作效率,原理如图所
示。下列说法错误的是
A.加入KI降低了正极反应的活化能
B.I-与剥落的MnO 反应生成的 能恢复“损失”的能量
2
C.放电时,正极区溶液的pH减小
D.放电时,若消耗1molZn,正极区电解质溶液理论上增重89g
【答案】C
【解析】由题干中原电池装置图示可知,Zn所在石墨电极为负极,电极反应为:Zn-2e-=Zn2+,MnO 所在
2的石墨电极为正极,电极反应为:MnO +2e-+4H+=Mn2++2H O,加入KI后的反应机理为:MnO +3I-
2 2 2
+4H+=Mn2++ +2H O, +2e-=3I-,据此分析解题。
2
A.由分析可知,KI参与正极电极反应,且加入少量KI固体后能使电池持续大电流放电,说明反应速率加
快,故降低了正极反应的活化能,A正确;
B.由分析可知,I-与剥落的MnO 反应生成的I ,然后 能继续从正极上得到电子转化为I-,故能恢复
2
“损失”的能量,B正确;
C.由分析可知,放电时,正极反应式为:MnO +2e-+4H+=Mn2++2H O,故正极区溶液的pH增大,C错误;
2 2
D.根据得失电子总数相等,结合正极反应式:MnO +2e-+4H+=Mn2++2H O可知,放电时,消耗1molZn时,
2 2
正极区电解质溶液增重1molMnO ,同时向正极移动2mol电子,故增重87+2=89g,D正确;
2
故答案为:C。