文档内容
专题 09 化学反应的热效应
1.下列有关能量的说法不正确的是( )
A.化学能可转变为电能 B.化学反应伴随能量变化是化学反应基本特征之一
C.化学反应能量转换遵守能量守恒定律D.化学变化时断裂化学键需放出能量
2.下列关于反应热的说法正确的是 ( )
A.化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关
B.已知C(s)+ O(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJ
2
C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D.当∆H为“-”时,表示该反应为吸热反应
3.下列关于反应热的说法正确的是( )
A.当ΔH为小于0时,表示该反应为吸热反应
B.已知C(s)+ O(g)=CO(g) ΔH=-110.5 kJ·mol-1,说明碳的燃烧热为110.5 kJ·mol-1
2
C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D.化学反应反应热只与反应体系的始态和终态有关,而与反应的途径无关
4.在测定中和反应反应热的实验中,下列说法正确的是( )
A.使用玻璃搅拌器是为了加快反应速率,减小实验误差
B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触
C.用0.5 mol·L-1 NaOH溶液分别与0.5 mol·L-1的盐酸、醋酸溶液反应,若所取的溶液体积都相等,
则测得的中和反应反应热数值相同
D.在测定中和反应反应热的实验中,需要使用的仪器有天平、量筒、烧杯、滴定管、温度计、玻璃
搅拌器
5.关于热化学方程式S(s)+O (g)=SO(g) ΔH=-296 kJ·mol-1,下列分析正确的是( )。
2 2
A.1 mol S(s)与1 mol O (g)的总能量比1 mol SO (g)的能量低296 kJ
2 2
B.1 mol S(g)与1 mol O (g)生成1 mol SO (g)放出296 kJ的热量
2 2
C.反应S(g)+O(g)=SO(g)的ΔH小于-296 kJ·mol-1
2 2
D.反应物的总键能大于生成物的总键能
6.下列关于热化学反应的描述中正确的是( )
A.需要加热才能发生的反应一定是吸热反应B.在一定的条件下将1molSO 和0.5molO 置于密闭容器中充分反应,放出热量79.2kJ,则反应的热
2 2
化学方程式为2SO (g)+O(g) 2SO (g) ΔH=-158.4 kJ•mol-1
2 2 3
C.HCl和NaOH反应的中和热ΔH=-57.3 kJ•mol-1,则HSO 和Ca(OH) 反应的中和热ΔH=2×(-57.3)
2 4 2
kJ•mol-1
D.CO(g)的燃烧热是283.0kJ/mol,则2CO(g)=2CO(g)+O(g)反应的ΔH=+2×283.0 kJ•mol-1
2 2
7.下列关于热化学反应的描述中正确的是( )
A.已知H+(aq)+OH-(aq)=H O(l)ΔH=-57.3kJ·mol-1,则HSO 和Ba(OH) 反应的ΔH=2×(-57.
2 2 4 2
3)kJ·mol-1
B.将甲醇蒸气转化为氢气的热化学方程式是 CHOH(g)+ O(g)=CO (g)+2H(g)ΔH=-192.
3 2 2 2
9kJ·mol-1,则CHOH(g)的燃烧热为192.9kJ·mol-1
3
C.H(g)的燃烧热为285.8kJ·mol-1,则2HO(g)=2H (g)+O(g) ΔH=+571.6kJ·mol-1
2 2 2 2
D.葡萄糖的燃烧热是2800kJ·mol-1,则 C H O(s)+3O(g)=3CO (g)+3HO(l) ΔH=-1400kJ·mol-1
6 12 6 2 2 2
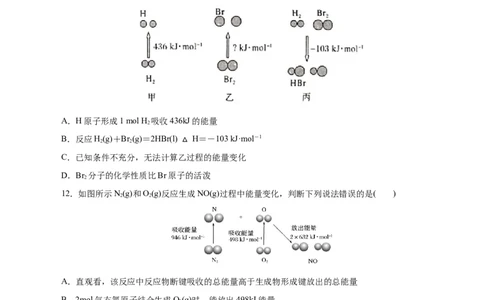
8.下列依据热化学方程式得出的结论正确的是( )
选项 热化学方程式 结论
2H(g)+O(g)=2HO(g) H=-483 . 6
A 2 2 2 H 的燃烧热为483.6 kJ/mol
kJ/mol 2
△
OH-(aq)+H+(aq)= HO(g) H=-57 . 3 含1mol NaOH的稀溶液与浓 HSO
B 2 2 4
kJ/mol 完全中和,放出热量小于57.3 kJ
△
2C(s)+2O(g)=2CO (g) H=-a kJ/mol
2 2
C b<a
2C(s)+O(g)=2CO(g) H=-b kJ/mol
2 △
△
C(石墨,s)=C(金刚石,s) H=+1.5
D 金刚石比石墨稳定
kJ/mol
△
9.热化学方程式C(s)+HO(g)===CO(g)+H(g)
2 2
H=+131.3kJ•mol﹣1 表示( )
△A.碳和水反应吸收131.3 kJ能量
B.1 mol碳和1 mol水反应生成1 mol一氧化碳和1 mol氢气并吸收131.3 kJ热量
C.1 mol固态碳和1 mol水蒸气反应生成1 mol一氧化碳气体和1 mol氢气并吸收131.3 kJ热量
D.1个固态碳原子和1分子水蒸气反应吸热131.3 kJ
10.已知25℃、101kPa时,以下反应的热化学方程式为:Fe O(s)+3C(s)=2Fe(s)+3CO(g) ΔH =+489kJ·mol-1
2 3 1
2CO(g)+O(g)=2CO (g) ΔH =-564kJ·mol-1
2 2 2
C(s)+O(g)=CO (g) ΔH =-393kJ·mol-1
2 2 3
则 的ΔH为( )
A.-822kJ·mol-1 B.-468kJ·mol-1 C.-186kJ·mol-1 D.+468kJ·mol-1
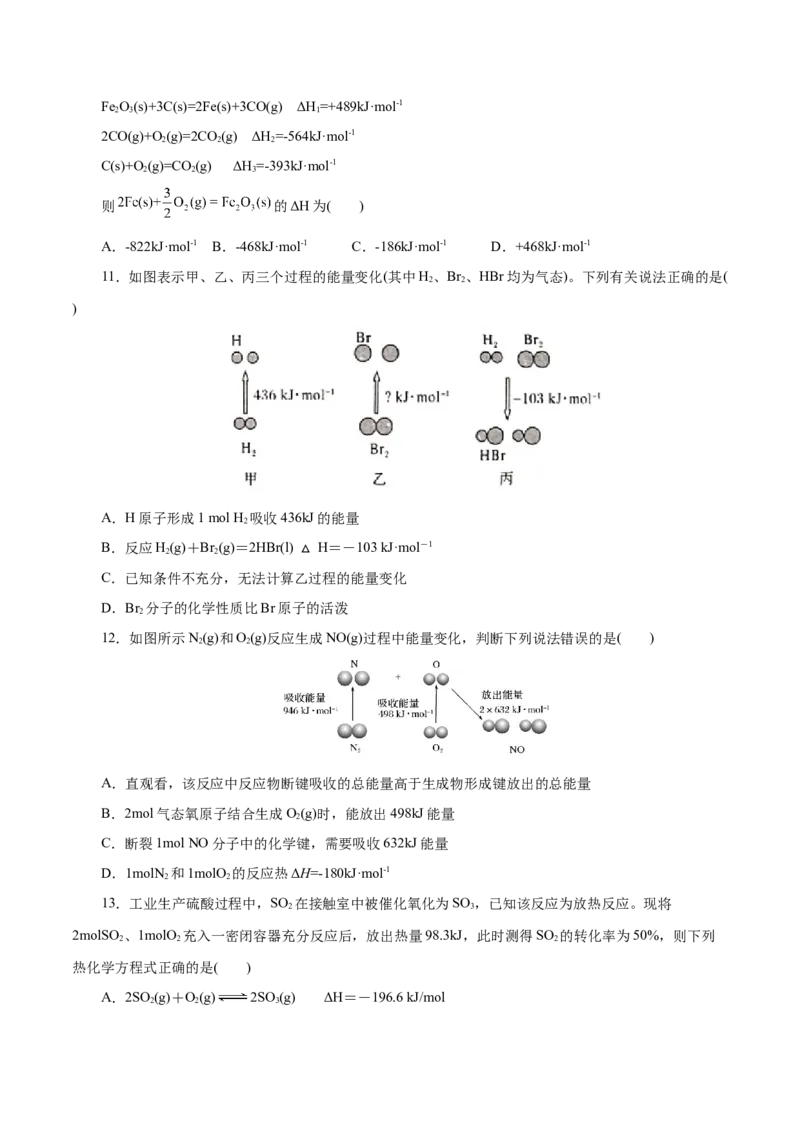
11.如图表示甲、乙、丙三个过程的能量变化(其中H、Br 、HBr均为气态)。下列有关说法正确的是(
2 2
)
A.H原子形成1 mol H 吸收436kJ的能量
2
B.反应H(g)+Br (g)=2HBr(l) H=-103 kJ·mol-1
2 2
C.已知条件不充分,无法计算乙△过程的能量变化
D.Br 分子的化学性质比Br原子的活泼
2
12.如图所示N(g)和O(g)反应生成NO(g)过程中能量变化,判断下列说法错误的是( )
2 2
A.直观看,该反应中反应物断键吸收的总能量高于生成物形成键放出的总能量
B.2mol气态氧原子结合生成O(g)时,能放出498kJ能量
2
C.断裂1mol NO分子中的化学键,需要吸收632kJ能量
D.1molN 和1molO 的反应热ΔH=-180kJ·mol-1
2 2
13.工业生产硫酸过程中,SO 在接触室中被催化氧化为SO ,已知该反应为放热反应。现将
2 3
2molSO 、1molO 充入一密闭容器充分反应后,放出热量98.3kJ,此时测得SO 的转化率为50%,则下列
2 2 2
热化学方程式正确的是( )
A.2SO (g)+O(g) 2SO (g) ΔH=-196.6 kJ/mol
2 2 3B.2SO (g)+O(g) 2SO (g) ΔH=-98.3 kJ/mol
2 2 3
C.SO (g)+ O(g) SO (g) ΔH=+98.3 kJ/mol
2 2 3
D.SO (g)+ O(g) SO (g) ΔH=-196.6 kJ/mol
2 2 3
14.下列关于热化学反应的描述中正确的是( )
A.已知H+(aq)+OH-(aq)=H O(l)ΔH=-57.3kJ·mol-1,则HSO 和Ba(OH) 反应的ΔH=2×(-
2 2 4 2
57.3)kJ·mol-1
B.将甲醇蒸气转化为氢气的热化学方程式是CHOH(g)+ O(g)=CO (g)+2H(g)ΔH=-192.9kJ·mol
3 2 2 2
-1,则CHOH(g)的燃烧热为192.9kJ·mol-1
3
C.H(g)的燃烧热为285.8kJ·mol-1,则2HO(g)=2H (g)+O(g) ΔH=+571.6kJ·mol-1
2 2 2 2
D.葡萄糖的燃烧热是2800kJ·mol-1,则 C H O(s)+3O(g)=3CO (g)+3HO(l) ΔH=-1400kJ·mol-1
6 12 6 2 2 2
15.已知H(g)+ O(g)=HO(g) ΔH=-242kJ·mol-1,断开1molO=O键和1mol H—O键所吸收的能量分
2 2 2
别为496kJ和463kJ,则断开1molH—H键所吸收的能量为( )
A.920kJ B.557kJ C.436kJ D.188kJ
16.已知:N(g) +3H (g) 2NH (g) H=-92.4 kJ/mo1.若断裂1 mol H-H、1 molN≡N需要吸收的
2 2 3
能量分别为akJ、b kJ。则生成1 mol N-H放出△能量的数值为( )
A. B.
C. D.
11.(2021·河北高三开学考试)用HO 和HSO 的混合溶液可溶出废旧印刷电路板上的铜。已知:
2 2 2 4
Cu(s)+2H+(aq)=Cu2+(aq)+H (g) ΔH=+64.39kJ·mol-1
2
2HO(l)=2H O(l)+O(g) ΔH=-196.46kJ·mol-1
2 2 2 2
H(g)+ O(g)=H O(l) ΔH=-285.84kJ·mol-1
2 2 2在HSO 溶液中,1molCu与1molH O 完全反应生成Cu2+(aq)和HO(l)的反应热ΔH等于( )
2 4 2 2 2
A.-417.91kJ·mol-1 B.-319.68kJ·mol-1
C.+546.69kJ·mol-1 D.-448.46kJ·mol-1
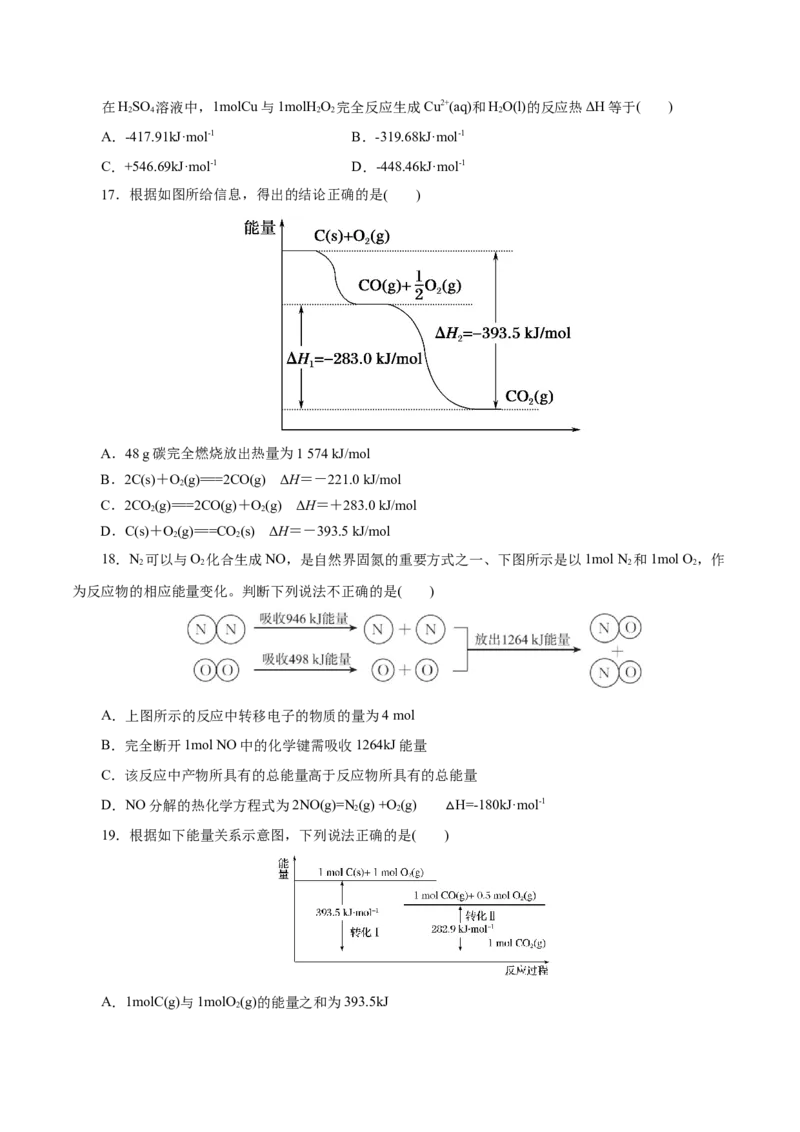
17.根据如图所给信息,得出的结论正确的是( )
A.48 g碳完全燃烧放出热量为1 574 kJ/mol
B.2C(s)+O(g)===2CO(g) ΔH=-221.0 kJ/mol
2
C.2CO(g)===2CO(g)+O(g) ΔH=+283.0 kJ/mol
2 2
D.C(s)+O(g)===CO (s) ΔH=-393.5 kJ/mol
2 2
18.N 可以与O 化合生成NO,是自然界固氮的重要方式之一、下图所示是以1mol N 和1mol O,作
2 2 2 2
为反应物的相应能量变化。判断下列说法不正确的是( )
A.上图所示的反应中转移电子的物质的量为4 mol
B.完全断开1mol NO中的化学键需吸收1264kJ能量
C.该反应中产物所具有的总能量高于反应物所具有的总能量
D.NO分解的热化学方程式为2NO(g)=N (g) +O (g) H=-180kJ·mol-1
2 2
19.根据如下能量关系示意图,下列说法正确的是( )△
A.1molC(g)与1molO (g)的能量之和为393.5kJ
2B.反应2CO(g)+O(g)=2CO (g)中,生成物的总能量大于反应物的总能量
2 2
C.由C→CO的热化学方程式为:2C(s)+O(g)=2CO(g) ΔH=-221.2kJ·mol-1
2
D.热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH=-10.1 kJ·mol-1
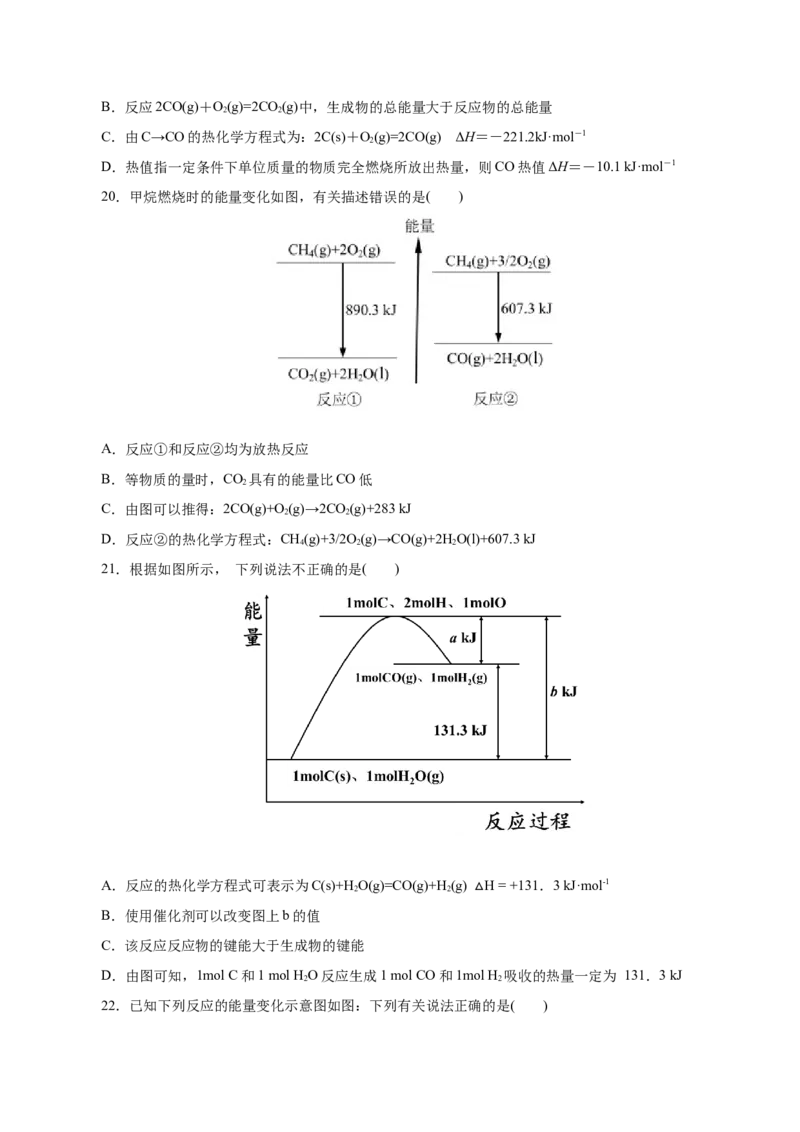
20.甲烷燃烧时的能量变化如图,有关描述错误的是( )
A.反应①和反应②均为放热反应
B.等物质的量时,CO 具有的能量比CO低
2
C.由图可以推得:2CO(g)+O(g)→2CO (g)+283 kJ
2 2
D.反应②的热化学方程式:CH(g)+3/2O (g)→CO(g)+2H O(l)+607.3 kJ
4 2 2
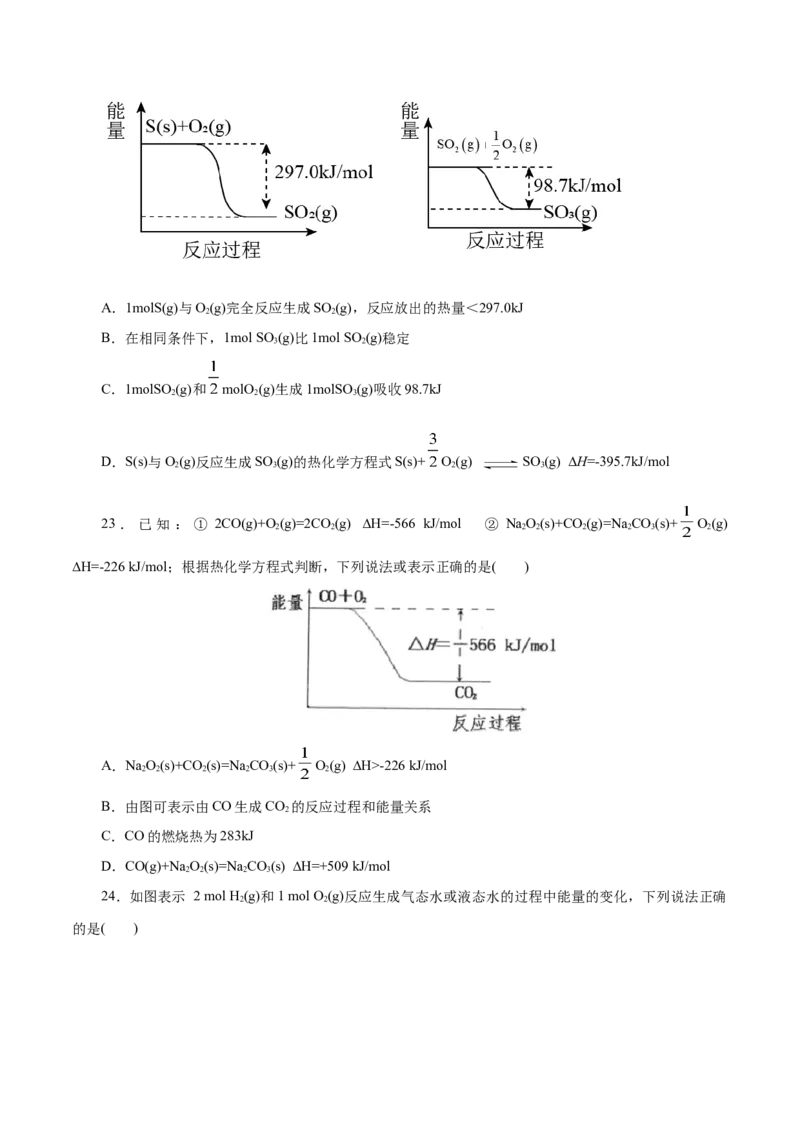
21.根据如图所示, 下列说法不正确的是( )
A.反应的热化学方程式可表示为C(s)+HO(g)=CO(g)+H (g) H = +131.3 kJ·mol-1
2 2
B.使用催化剂可以改变图上b的值 △
C.该反应反应物的键能大于生成物的键能
D.由图可知,1mol C和1 mol H O反应生成1 mol CO和1mol H 吸收的热量一定为 131.3 kJ
2 2
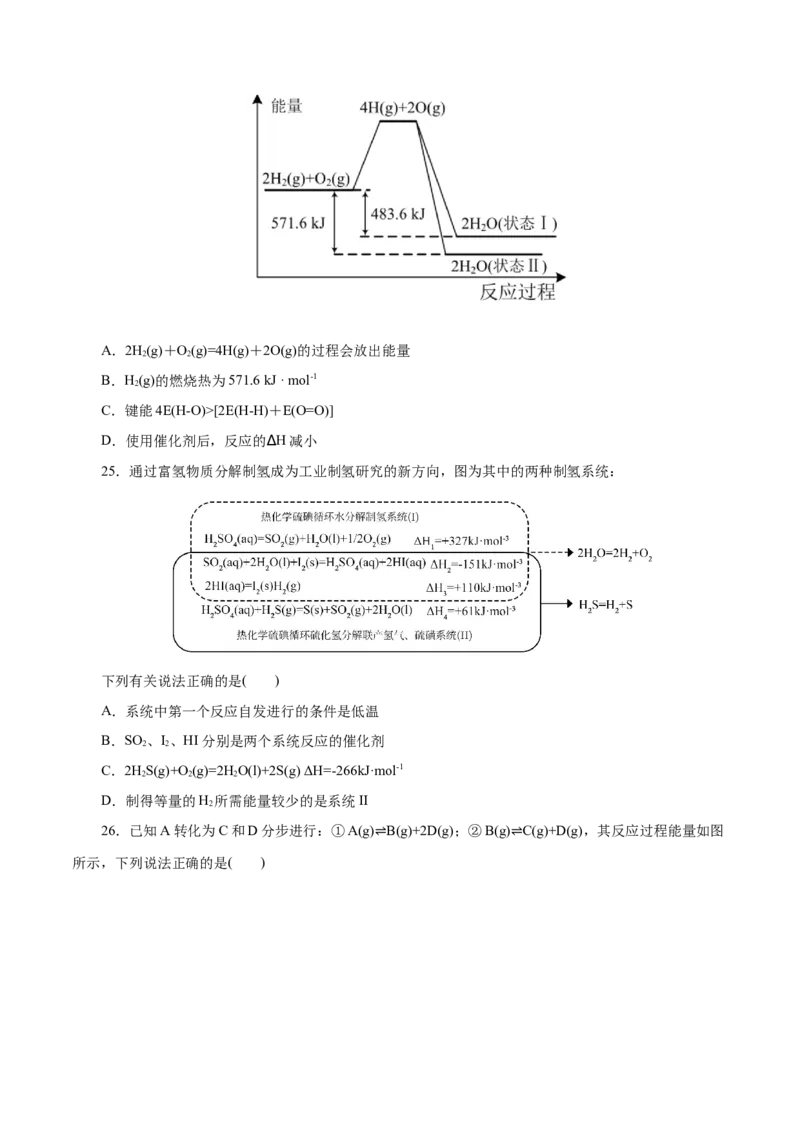
22.已知下列反应的能量变化示意图如图:下列有关说法正确的是( )A.1molS(g)与O(g)完全反应生成SO (g),反应放出的热量<297.0kJ
2 2
B.在相同条件下,1mol SO (g)比1mol SO (g)稳定
3 2
C.1molSO (g)和 molO (g)生成1molSO (g)吸收98.7kJ
2 2 3
D.S(s)与O(g)反应生成SO (g)的热化学方程式S(s)+ O(g) SO (g) ∆H=-395.7kJ/mol
2 3 2 3
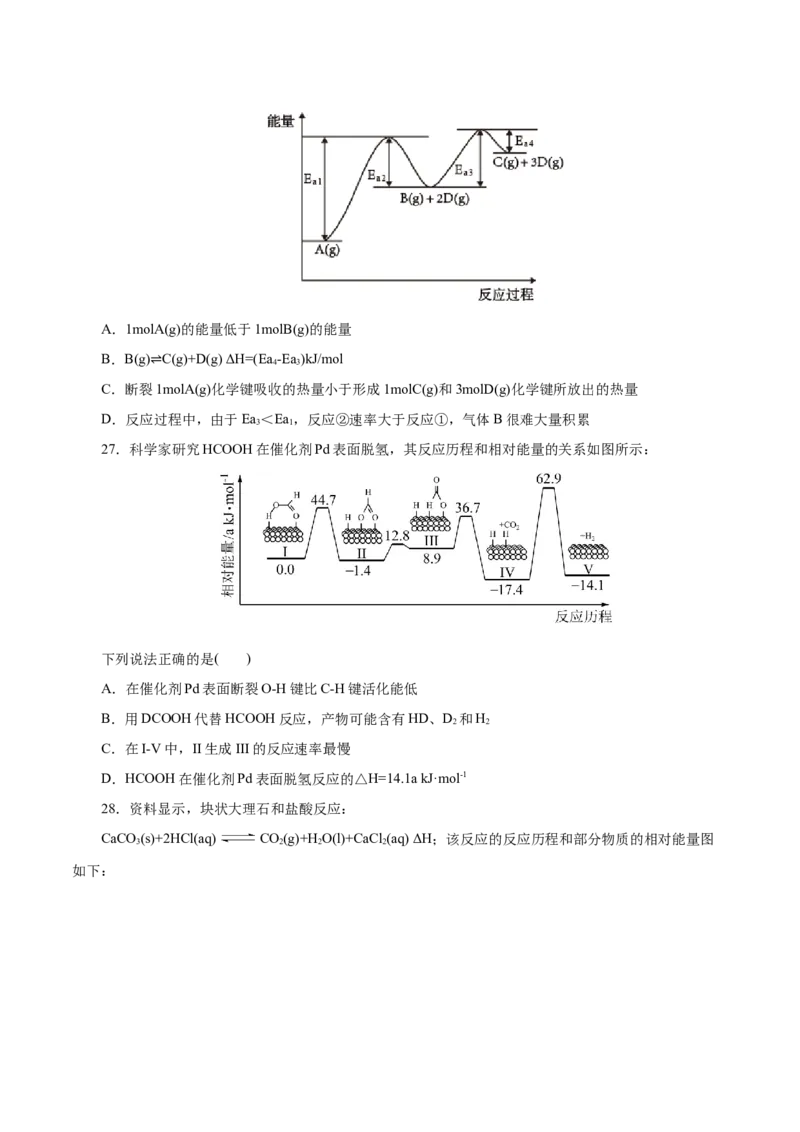
23 . 已 知 : ① 2CO(g)+O(g)=2CO (g) ∆H=-566 kJ/mol ② NaO(s)+CO(g)=Na CO(s)+ O(g)
2 2 2 2 2 2 3 2
∆H=-226 kJ/mol;根据热化学方程式判断,下列说法或表示正确的是( )
A.NaO(s)+CO(s)=Na CO(s)+ O(g) ∆H>-226 kJ/mol
2 2 2 2 3 2
B.由图可表示由CO生成CO 的反应过程和能量关系
2
C.CO的燃烧热为283kJ
D.CO(g)+Na O(s)=Na CO(s) ∆H=+509 kJ/mol
2 2 2 3
24.如图表示 2 mol H (g)和1 mol O (g)反应生成气态水或液态水的过程中能量的变化,下列说法正确
2 2
的是( )A.2H(g)+O(g)=4H(g)+2O(g)的过程会放出能量
2 2
B.H(g)的燃烧热为571.6 kJ · mol-1
2
C.键能4E(H-O)>[2E(H-H)+E(O=O)]
D.使用催化剂后,反应的∆H减小
25.通过富氢物质分解制氢成为工业制氢研究的新方向,图为其中的两种制氢系统:
下列有关说法正确的是( )
A.系统中第一个反应自发进行的条件是低温
B.SO 、I、HI分别是两个系统反应的催化剂
2 2
C.2HS(g)+O(g)=2HO(l)+2S(g) ΔH=-266kJ·mol-1
2 2 2
D.制得等量的H 所需能量较少的是系统II
2
26.已知A转化为C和D分步进行:①A(g) B(g)+2D(g);②B(g) C(g)+D(g),其反应过程能量如图
所示,下列说法正确的是( ) ⇌ ⇌A.1molA(g)的能量低于1molB(g)的能量
B.B(g) C(g)+D(g) ΔH=(Ea -Ea )kJ/mol
4 3
C.断裂⇌1molA(g)化学键吸收的热量小于形成1molC(g)和3molD(g)化学键所放出的热量
D.反应过程中,由于Ea<Ea,反应②速率大于反应①,气体B很难大量积累
3 1
27.科学家研究HCOOH在催化剂Pd表面脱氢,其反应历程和相对能量的关系如图所示:
下列说法正确的是( )
A.在催化剂Pd表面断裂O-H键比C-H键活化能低
B.用DCOOH代替HCOOH反应,产物可能含有HD、D 和H
2 2
C.在I-V中,II生成III的反应速率最慢
D.HCOOH在催化剂Pd表面脱氢反应的△H=14.1a kJ·mol-1
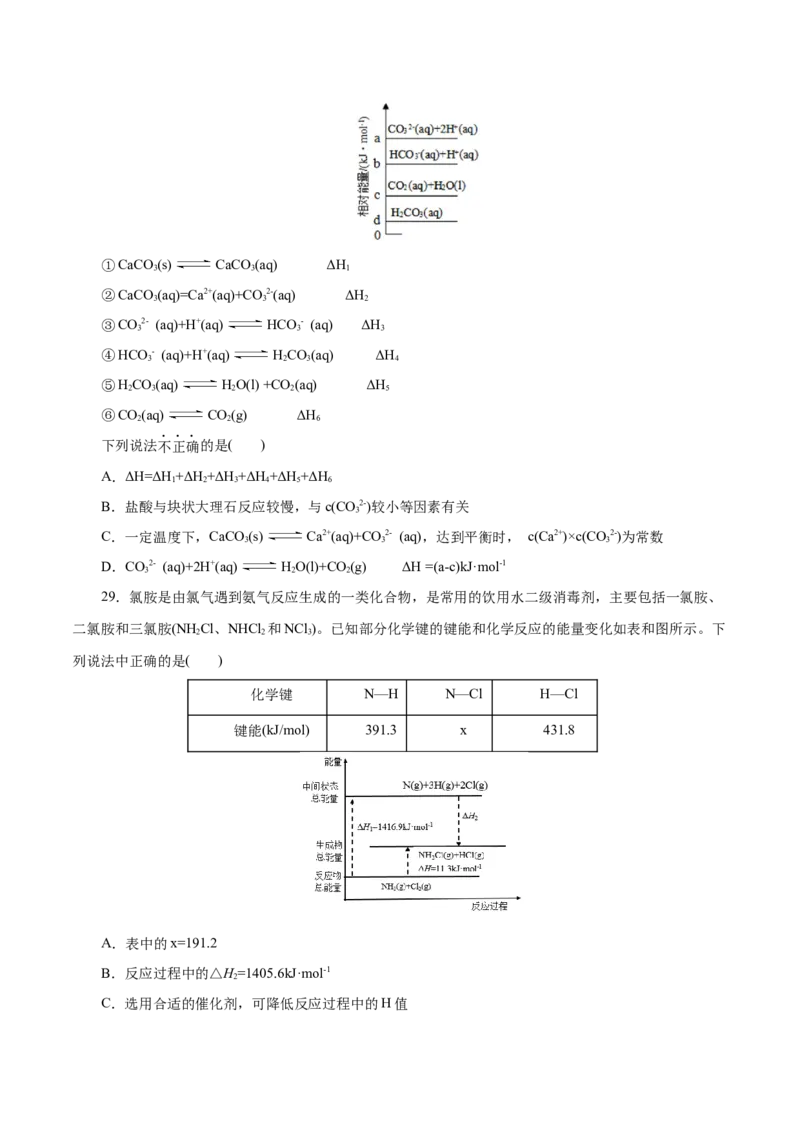
28.资料显示,块状大理石和盐酸反应:
CaCO (s)+2HCl(aq) CO(g)+HO(l)+CaCl (aq) ΔH;该反应的反应历程和部分物质的相对能量图
3 2 2 2
如下:①CaCO (s) CaCO (aq) ΔH
3 3 1
②CaCO (aq)=Ca2+(aq)+CO 2-(aq) ΔH
3 3 2
③CO2- (aq)+H+(aq) HCO - (aq) ΔH
3 3 3
④HCO - (aq)+H+(aq) HCO(aq) ΔH
3 2 3 4
⑤HCO(aq) HO(l) +CO (aq) ΔH
2 3 2 2 5
⑥CO(aq) CO(g) ΔH
2 2 6
下列说法不正确的是( )
A.ΔH=ΔH+ΔH +ΔH +ΔH +ΔH +ΔH
1 2 3 4 5 6
B.盐酸与块状大理石反应较慢,与c(CO2-)较小等因素有关
3
C.一定温度下,CaCO (s) Ca2+(aq)+CO 2- (aq),达到平衡时, c(Ca2+)×c(CO 2-)为常数
3 3 3
D.CO2- (aq)+2H+(aq) HO(l)+CO (g) ΔH =(a-c)kJ·mol-1
3 2 2
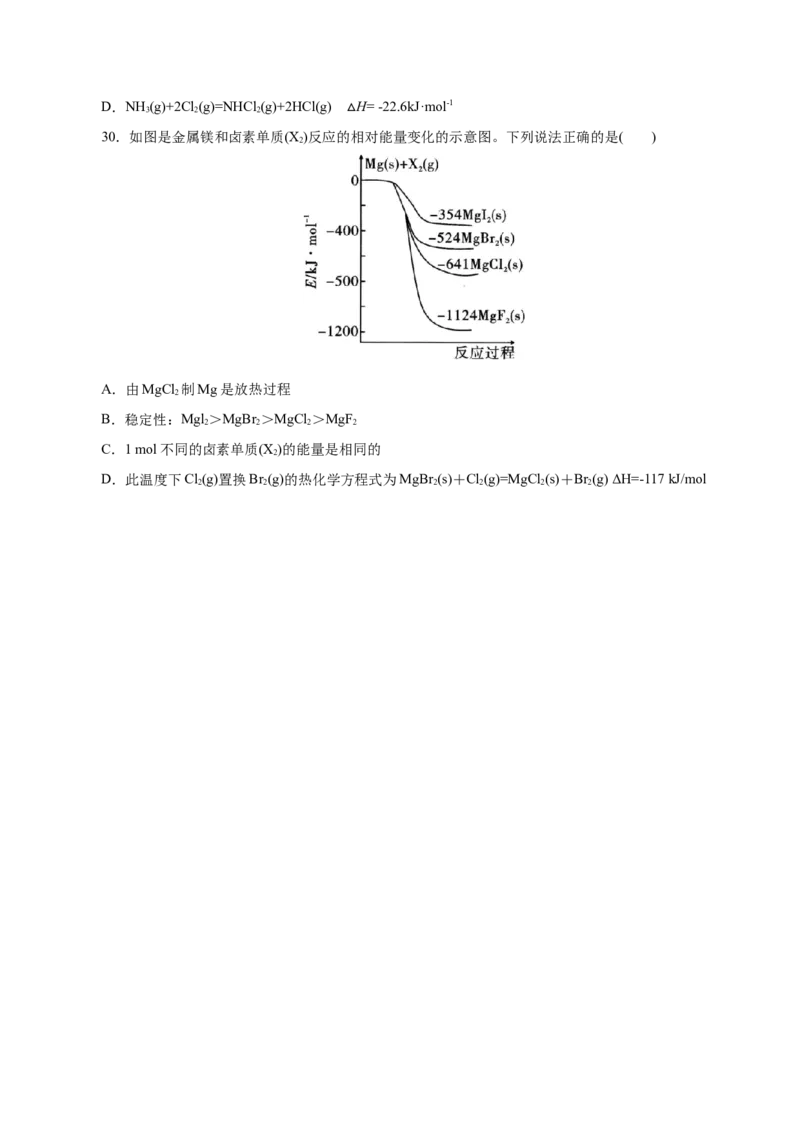
29.氯胺是由氯气遇到氨气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺、
二氯胺和三氯胺(NH Cl、NHCl 和NCl )。已知部分化学键的键能和化学反应的能量变化如表和图所示。下
2 2 3
列说法中正确的是( )
化学键 N—H N—Cl H—Cl
键能(kJ/mol) 391.3 x 431.8
A.表中的x=191.2
B.反应过程中的△H=1405.6kJ·mol-1
2
C.选用合适的催化剂,可降低反应过程中的H值D.NH (g)+2Cl (g)=NHCl (g)+2HCl(g) H= -22.6kJ·mol-1
3 2 2
30.如图是金属镁和卤素单质(X )反应的△相对能量变化的示意图。下列说法正确的是( )
2
A.由MgCl 制Mg是放热过程
2
B.稳定性:Mgl >MgBr >MgCl >MgF
2 2 2 2
C.1 mol不同的卤素单质(X )的能量是相同的
2
D.此温度下Cl(g)置换Br (g)的热化学方程式为MgBr (s)+Cl(g)=MgCl (s)+Br (g) ΔH=-117 kJ/mol
2 2 2 2 2 2