文档内容
专题 09 金属和非金属元素及其化合物
1.《本草纲目》中“石碱”条目下写到:“采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发
面,亦去垢发面”。这里的“石碱”是指( )
A.KOH B.KAl(SO )
4 2
C.KHCO D.KCO
3 2 3
2.下列有关物质的性质与用途具有对应关系的是( )
A.NaS具有还原性,可用于去除水体中Hg2+
2
B.O 具有氧化性,可用于自来水的消毒杀菌
3
C.葡萄糖易溶于水,可用作制镜工业的原料
D.Al O 具有两性,可用作耐高温材料
2 3
3.分别用等量的铁与足量的稀硫酸和足量的CuO制备单质铜,有人设计了以下两种方案:
①Fe――→H――→Cu,②CuO――→CuSO ――→Cu。
2 4
对制备得到Cu的量,下列判断正确的是( )
A.一样多 B.①多 C.②多 D.无法判断
4.A~G各物质间的关系如图所示,其中B、D为气体单质。则下列说法错误的是( )
――→――→――→
――→――→
A.已知C的浓溶液在催化存在的条件下加热,能与B反应生成D,由此可以推断B的氧化性比MnO 强
2
B.反应②的离子方程式为MnO +4H++2Cl-=====Cl↑+Mn2++2HO
2 2 2
C.新配制的F溶液一般需要加入铁屑和稀盐酸,前者用于防止 Fe2+被空气氧化成Fe3+,后者可抑制Fe2+
的水解
D.若反应①在常温下进行,则1 mol A在反应中能转移1 mol电子
5.工业上利用无机矿物资源生产部分材料的流程示意图如下。下列说法正确的是( )
(注:铝土矿中含有Al O、SiO、Fe O)
2 3 2 2 3
A.在铝土矿制备较高纯度Al的过程中只用到NaOH溶液、CO 气体、冰晶石
2
B.石灰石、纯碱、石英、玻璃都属于盐,都能与盐酸反应C.在制粗硅时,氧化剂与还原剂的物质的量之比为1:2
D.黄铜矿(CuFeS)与O 反应产生的Cu S、SO 均是还原产物
2 2 2 2
6.研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如图所示)。下列叙述错误的是( )
A.雾和霾的分散剂相同
B.雾霾中含有硝酸铵和硫酸铵
C.NH 是形成无机颗粒物的催化剂
3
D.雾霾的形成与过度施用氮肥有关
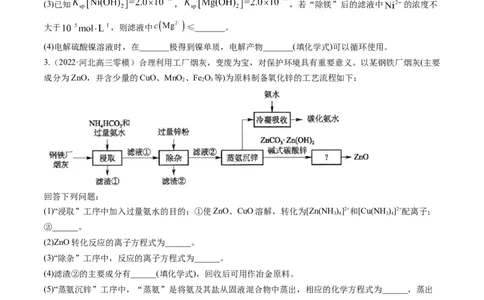
1.(2022·辽宁高三模拟)Ni O 是一种灰黑色有光泽的块状物质,常用作着色颜料或镍电池的电极材料。
2 3
某工厂以废弃的含镍催化剂(主要成分为NiO,含Fe O、CaO、CuO、BaO等杂质)为主要原料生产Ni O,
2 3 2 3
工艺流程如下:
(1)流程中得到的副产品的化学式是_______,该物质的用途有_______(任写一种)。
(2)操作A中通入HS生成CuS的离子方程式为_______。
2
(3)操作B的目的是除铁元素,具体操作是向操作A的滤液中加入足量HO,然后加NaOH溶液调节pH为
2 2
4~7,静置、过滤。pH调至4~7的原因是_______。
(4)操作C中加入NaF的目的是除去溶液中的Ca2+,已知K (CaF )=1.6×10-10,当Ca2+完全沉淀(离子浓度小
sp 2
于1×10-5 mol·L-1时,即可认为是完全沉淀),溶液中的c(F-)至少为_______。
(5)电解产生2NiOOH·H O的原理是阳极Cl-先放电得到ClO-,ClO-再把Ni2+氧化为2NiOOH·H O。电解的阳
2 2
极反应式和阴极反应式依次为_______、_______。
2.(2022河北石家庄二中模拟)硫化镍矿的主要成分是 ,还含有 、 、一些不溶性物质等,
工业上用硫化镍矿制备金属镍的工艺流程如图所示:(1)硫化镍矿粉磨的目的是_______,“酸浸”时,硫化镍与稀盐酸反应的化学方程式为_______。
(2)“氧化、除铁”过程中加入 溶液时,发生反应的离子方程式为_______;加入氧化镍的目的是除去
铁元素,用化学平衡移动原理解释除去铁元素的原因_______。
(3)已知 , ,若“除镁”后的滤液中 的浓度不
大于 ,则滤液中 ≤_______。
(4)电解硫酸镍溶液时,在_______极得到镍单质,电解产物_______(填化学式)可以循环使用。
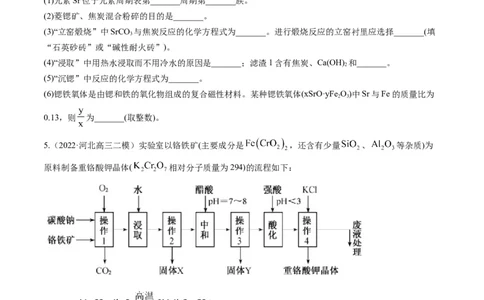
3.(2022·河北高三零模)合理利用工厂烟灰,变废为宝,对保护环境具有重要意义。以某钢铁厂烟灰(主要
成分为ZnO,并含少量的CuO、MnO 、Fe O 等)为原料制备氧化锌的工艺流程如下:
2 2 3
回答下列问题:
(1)“浸取”工序中加入过量氨水的目的:①使ZnO、CuO溶解,转化为[Zn(NH )]2+和[Cu(NH )]2+配离子;
3 4 3 4
②______。
(2)ZnO转化反应的离子方程式为______。
(3)“除杂”工序中,反应的离子方程式为______。
(4)滤渣②的主要成分有______(填化学式),回收后可用作冶金原料。
(5)“蒸氨沉锌”工序中,“蒸氨”是将氨及其盐从固液混合物中蒸出,相应的化学方程式为______,蒸出
物冷凝吸收后得到的碳化氨水可返回______工序循环使用。
(6)从碱式碳酸锌得到氧化锌的工序名称为______。
(7)将滤渣①用HSO 溶液处理后得到______溶液和______固体(均填化学式)。
2 4
4.(2022·重庆高三零模)碳酸锶(SrCO )是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以
3
菱锶矿(含80~90% SrCO ,少量MgCO 、CaCO 、BaCO 等)制备高纯碳酸锶的工艺流程如下:
3 3 3 3Sr(OH) 在水中的溶解度
2
温度/℃ 10 20 30 40 60 80 90 100
溶解度/(g/100g) 1.25 1.77 2.64 3.95 8.42 20.2 44.5 91.2
(1)元素Sr位于元素周期表第_______周期第_______族。
(2)菱锶矿、焦炭混合粉碎的目的是_______。
(3)“立窑煅烧”中SrCO 与焦炭反应的化学方程式为_______。进行煅烧反应的立窑衬里应选择_______(填
3
“石英砂砖”或“碱性耐火砖”)。
(4)“浸取”中用热水浸取而不用冷水的原因是_______;滤渣1含有焦炭、Ca(OH) 和_______。
2
(5)“沉锶”中反应的化学方程式为_______。
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe O)中Sr与Fe的质量比为
2 3
0.13,则 为_______(取整数)。
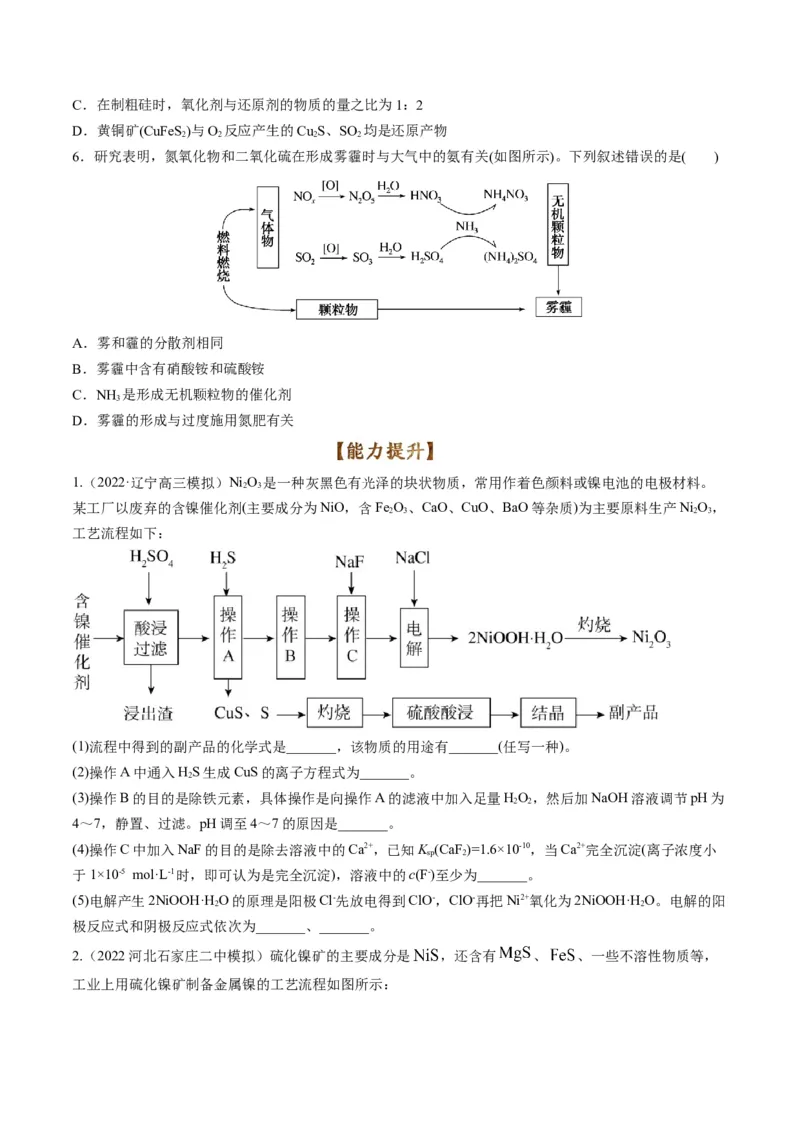
5.(2022·河北高三二模)实验室以铬铁矿(主要成分是 ,还含有少量 、 等杂质)为
原料制备重铬酸钾晶体( 相对分子质量为294)的流程如下:
已知:①
② 时, 含量极小
请回答下列问题:
(1)① 中各元素化合价均为整数,则 为_______价,将它用氧化物的形式表示为_______。
②“操作1”的反应条件是高温,写出主要的化学反应化学方程式_______。
③“操作1”中的反应,在常温下的反应速率较慢,为使反应速率增大,除升高温度外,还可采取的措施为
_______、_______(写出两条)。(2)固体X中主要含有_______(填写化学式),固体Y中主要含有_______(填写化学式)。
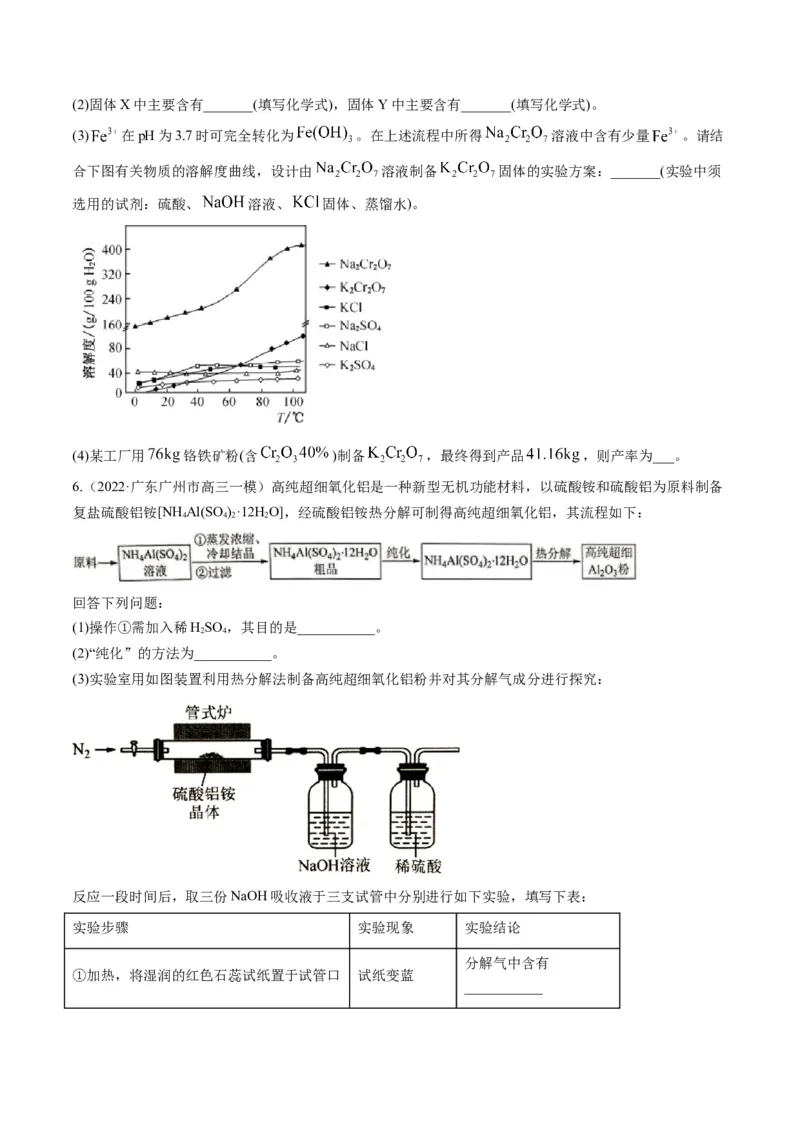
(3) 在pH为3.7时可完全转化为 。在上述流程中所得 溶液中含有少量 。请结
合下图有关物质的溶解度曲线,设计由 溶液制备 固体的实验方案:_______(实验中须
选用的试剂:硫酸、 溶液、 固体、蒸馏水)。
(4)某工厂用 铬铁矿粉(含 )制备 ,最终得到产品 ,则产率为___。
6.(2022·广东广州市高三一模)高纯超细氧化铝是一种新型无机功能材料,以硫酸铵和硫酸铝为原料制备
复盐硫酸铝铵[NH Al(SO )·12H O],经硫酸铝铵热分解可制得高纯超细氧化铝,其流程如下:
4 4 2 2
回答下列问题:
(1)操作①需加入稀HSO ,其目的是___________。
2 4
(2)“纯化”的方法为___________。
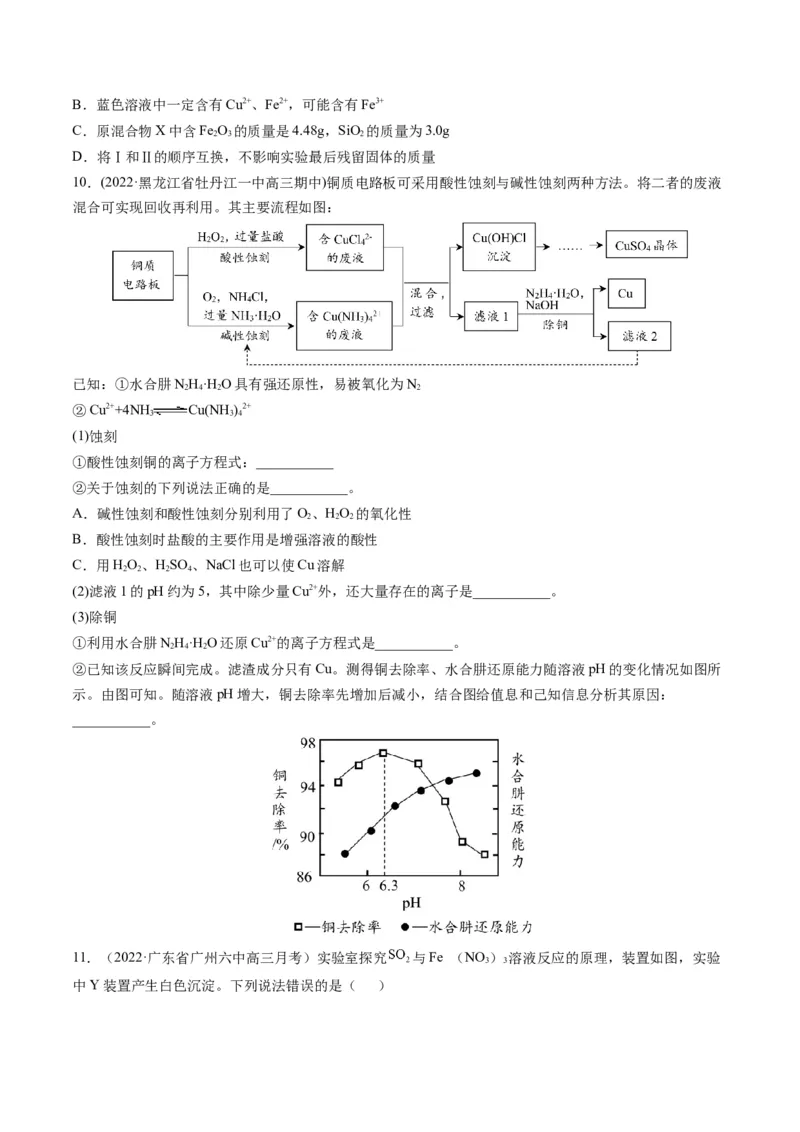
(3)实验室用如图装置利用热分解法制备高纯超细氧化铝粉并对其分解气成分进行探究:
反应一段时间后,取三份NaOH吸收液于三支试管中分别进行如下实验,填写下表:
实验步骤 实验现象 实验结论
分解气中含有
①加热,将湿润的红色石蕊试纸置于试管口 试纸变蓝
___________②加入盐酸酸化,再滴加氯化钡溶液 产生白色沉淀 分解气中___________
③___________ ___________ 分解气中不含有SO
2
写出硫酸铝铵晶体高温分解的化学方程式___________。
(4)为了测定高纯超细氧化铝粉中Al O 的质量分数,可用EDTA(简写为HY)标准溶液滴定。取mg氧化铝
2 3 4
粉溶于盐酸,加入过量的VmLcmol·L-1EDTA标准溶液,充分反应后,再用cmol·L-1的Zn2+标准溶液滴定
1 1 2
过量的EDTA至终点,消耗Zn2+标准溶液体积为VmL。反应的离子方程式:Al3++Y4-=AlY-、zn2++Y4-=ZnY
2
。Al O 的质量分数为___________。
2 3
7.(2022·山东省泰安教育发展中心高三期中)黄铜灰渣(含有Cu 、Zn、CuO、ZnO及少量FeO、Fe O)生产
2 3
硝酸铜溶液的流程如图,下列说法不正确的是( )
A.“浸取”时适当提高硫酸浓度可加快反应速率
B.若反应中所加Zn过量,所得Cu(NO ) 溶液中含Zn(NO ) 杂质
3 2 3 2
C.滤液II含Zn2+、Fe2+、Fe3+、SO 2-等离子
4
D.由Cu(NO ) 溶液制备Cu(NO )·3H O,采用蒸发结晶的操作
3 2 3 2 2
8.(2022·沈阳市辽宁实验中学期末)常温下,c(H+)=0.1mol/L的某溶液中可能含有Na+、Fe3+、Fe2+、I-、
Cl-、CO2-中的某几种离子,现取100mL该溶液进行如图所示实验:
3
已知氧化性Fe3+>I 。根据实验结果,判断下列说法正确的是( )
2
A.Fe3+与Fe2+至少有一种
B.一定不存在CO2-,可能存在Na+和Cl-
3
C.一定存在Fe2+、I-、Cl-
D.该溶液中一定存在Fe2+、I-,可能含Cl-
9.(2022·浙江绍兴市期末)某混合物X由Fe O、Cu、SiO 三种物质组成,进行如图实验:
2 3 2
下列有关说法正确的是( )
A.由Ⅰ可知Cu能与过量的盐酸发生置换反应B.蓝色溶液中一定含有Cu2+、Fe2+,可能含有Fe3+
C.原混合物X中含Fe O 的质量是4.48g,SiO 的质量为3.0g
2 3 2
D.将Ⅰ和Ⅱ的顺序互换,不影响实验最后残留固体的质量
10.(2022·黑龙江省牡丹江一中高三期中)铜质电路板可采用酸性蚀刻与碱性蚀刻两种方法。将二者的废液
混合可实现回收再利用。其主要流程如图:
已知:①水合肼NH·H O具有强还原性,易被氧化为N
2 4 2 2
②Cu2++4NH Cu(NH )2+
3 3 4
(1)蚀刻
①酸性蚀刻铜的离子方程式:___________
②关于蚀刻的下列说法正确的是___________。
A.碱性蚀刻和酸性蚀刻分别利用了O、HO 的氧化性
2 2 2
B.酸性蚀刻时盐酸的主要作用是增强溶液的酸性
C.用HO、HSO 、NaCl也可以使Cu溶解
2 2 2 4
(2)滤液1的pH约为5,其中除少量Cu2+外,还大量存在的离子是___________。
(3)除铜
①利用水合肼NH·H O还原Cu2+的离子方程式是___________。
2 4 2
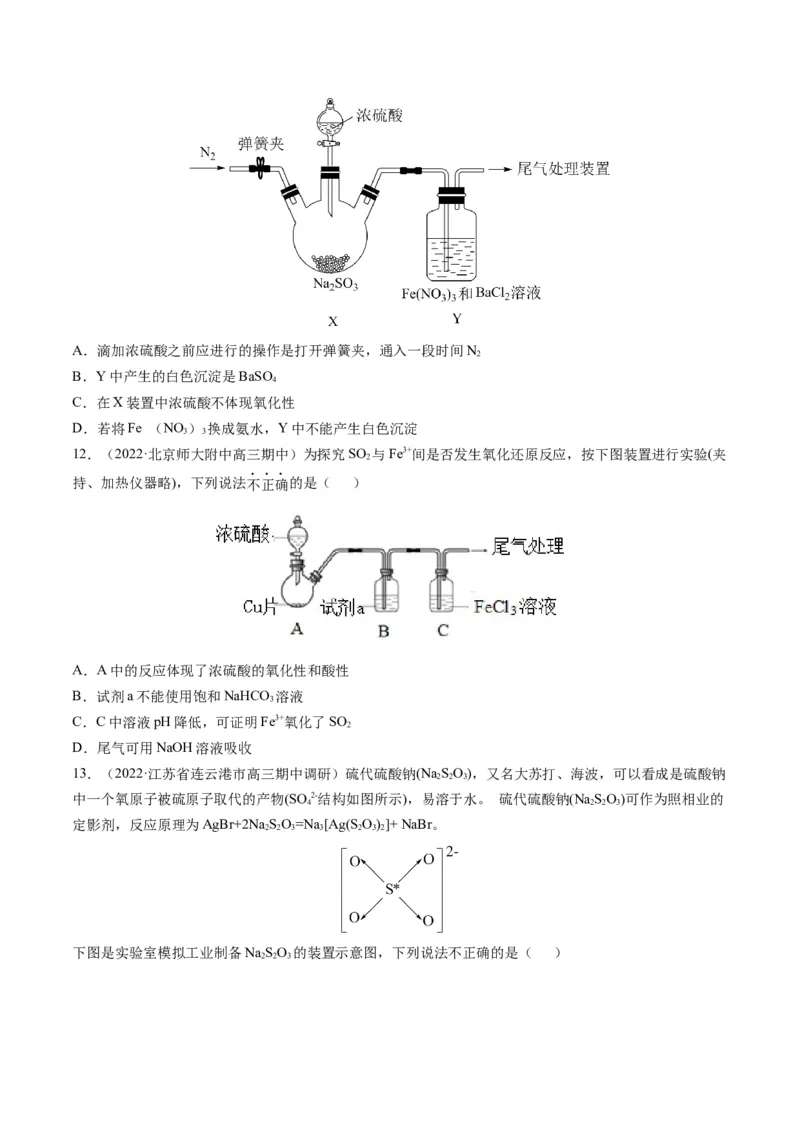
②已知该反应瞬间完成。滤渣成分只有Cu。测得铜去除率、水合肼还原能力随溶液pH的变化情况如图所
示。由图可知。随溶液pH增大,铜去除率先增加后减小,结合图给值息和己知信息分析其原因:
___________。
11.(2022·广东省广州六中高三月考)实验室探究 与Fe (NO ) 溶液反应的原理,装置如图,实验
3 3
中Y装置产生白色沉淀。下列说法错误的是( )A.滴加浓硫酸之前应进行的操作是打开弹簧夹,通入一段时间N
2
B.Y中产生的白色沉淀是BaSO
4
C.在X装置中浓硫酸不体现氧化性
D.若将Fe (NO ) 换成氨水,Y中不能产生白色沉淀
3 3
12.(2022·北京师大附中高三期中)为探究SO 与Fe3+间是否发生氧化还原反应,按下图装置进行实验(夹
2
持、加热仪器略),下列说法不正确的是( )
A.A中的反应体现了浓硫酸的氧化性和酸性
B.试剂a不能使用饱和NaHCO 溶液
3
C.C中溶液pH降低,可证明Fe3+氧化了SO
2
D.尾气可用NaOH溶液吸收
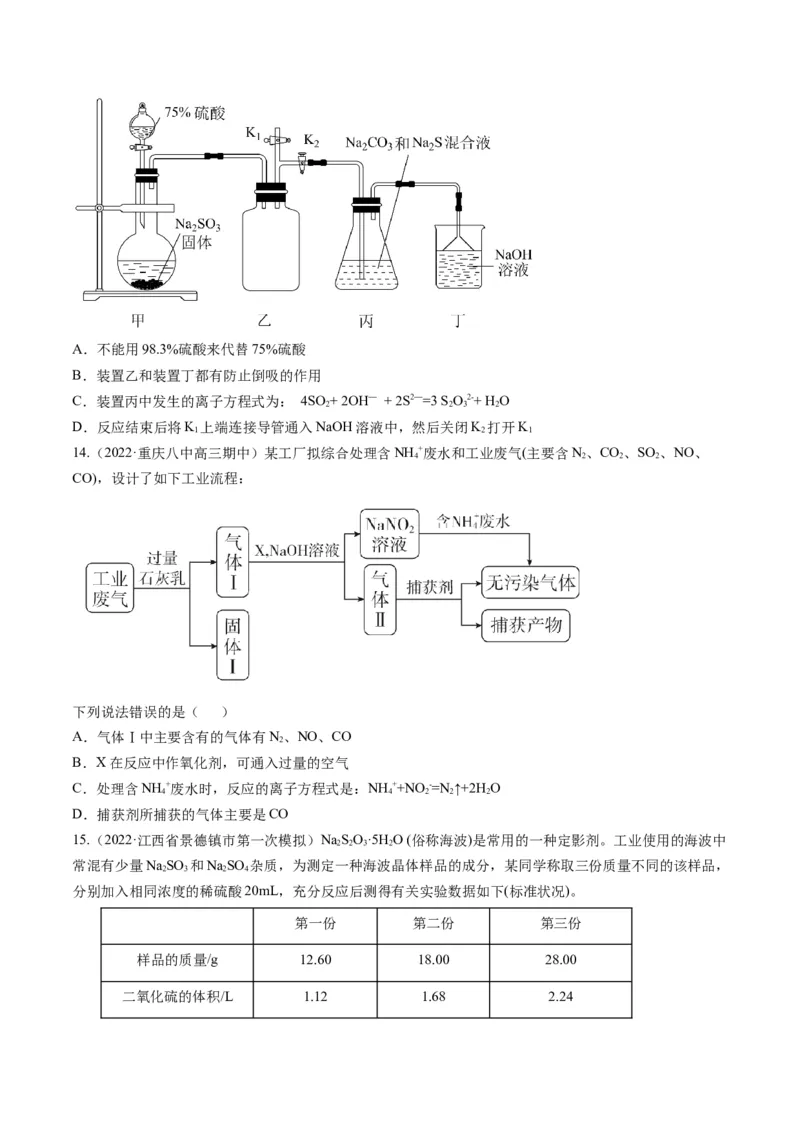
13.(2022·江苏省连云港市高三期中调研)硫代硫酸钠(Na SO),又名大苏打、海波,可以看成是硫酸钠
2 2 3
中一个氧原子被硫原子取代的产物(SO 2-结构如图所示),易溶于水。 硫代硫酸钠(Na SO)可作为照相业的
4 2 2 3
定影剂,反应原理为AgBr+2Na SO=Na [Ag(S O)]+ NaBr。
2 2 3 3 2 3 2
下图是实验室模拟工业制备NaSO 的装置示意图,下列说法不正确的是( )
2 2 3A.不能用98.3%硫酸来代替75%硫酸
B.装置乙和装置丁都有防止倒吸的作用
C.装置丙中发生的离子方程式为: 4SO + 2OH— + 2S2—=3 S O2-+ H O
2 2 3 2
D.反应结束后将K 上端连接导管通入NaOH溶液中,然后关闭K 打开K
1 2 1
14.(2022·重庆八中高三期中)某工厂拟综合处理含NH +废水和工业废气(主要含N、CO、SO 、NO、
4 2 2 2
CO),设计了如下工业流程:
下列说法错误的是( )
A.气体Ⅰ中主要含有的气体有N、NO、CO
2
B.X在反应中作氧化剂,可通入过量的空气
C.处理含NH +废水时,反应的离子方程式是:NH ++NO-=N ↑+2H O
4 4 2 2 2
D.捕获剂所捕获的气体主要是CO
15.(2022·江西省景德镇市第一次模拟)NaSO·5H O (俗称海波)是常用的一种定影剂。工业使用的海波中
2 2 3 2
常混有少量NaSO 和NaSO 杂质,为测定一种海波晶体样品的成分,某同学称取三份质量不同的该样品,
2 3 2 4
分别加入相同浓度的稀硫酸20mL,充分反应后测得有关实验数据如下(标准状况)。
第一份 第二份 第三份
样品的质量/g 12.60 18.00 28.00
二氧化硫的体积/L 1.12 1.68 2.24硫的质量/g 1.28 1.92 2.56
下列说法错误的是( )
A.第一份、第二份样品均完全反应,第三份样品过量
B.样品中n(NaSO·5H O): n(NaSO )=4:1
2 2 3 2 2 3
C.样品中除了含有NaSO·5H O、NaSO ,还含有NaSO
2 2 3 2 2 3 2 4
D.所加硫酸溶液的物质的量浓度为0.5mol/L