文档内容
易错题 12 反应热 热化学方程式
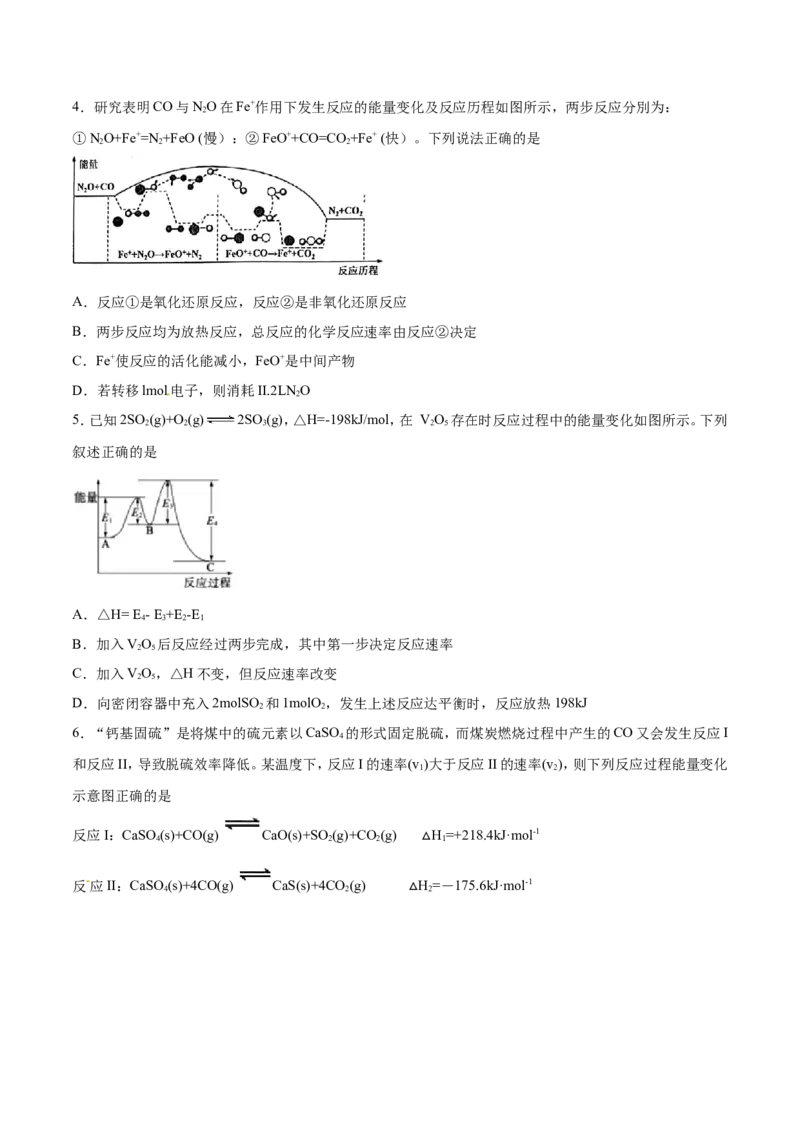
1.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示
意图如下:
下列说法中正确的是( )
A.CO和O生成了具有共价键的CO B.在该过程中,CO断键形成C和O
2
C.状态Ⅰ→状态Ⅲ表示CO与O 反应的过程 D.CO和O生成CO 是吸热反应
2 2
2.在1 200 ℃时,天然气脱硫工艺中会发生下列反应
HS(g)+3/2O (g)===SO (g)+HO(g) ΔH ①
2 2 2 2 1
2HS(g)+SO (g)==3/2S(g)+2HO(g) ΔH ②
2 2 2 2 2
HS(g)+1/2O (g)===S(g)+HO(g) ΔH ③
2 2 2 3
2S(g)===S (g) ΔH
2 4
则ΔH 的正确表达式为( )
4
A.ΔH=2/3(ΔH+ΔH-3ΔH) B.ΔH=2/3(3ΔH-ΔH-ΔH)
4 1 2 3 4 3 1 2
C.ΔH=2/3(ΔH+ΔH-2ΔH) D.ΔH=2/3(ΔH-ΔH-3ΔH)
4 1 2 3 4 1 2 3
3.已知: P(g)+6Cl (g)=4PCl (g) H=a kJ/mol P (g)+10Cl (g)=4PCl (g) H=b kJ/mol P 具有正四面体结
4 2 3 4 2 5 4
构,PCl 中P-Cl键的键能为c kJ/m△ol,PCl 中P-Cl键的键能为1.2c kJ/m△ol。 下列叙述正确的是 ( )
5 3
A.P-P键的键能大于P-Cl键的键能
B.可求Cl(g)+ PCl (g)=4PCl (s)的反应热△H
2 3 5
C.Cl-Cl键的键能为 kJ/mol
D.P-P键的键能为 kJ/mol4.研究表明CO与NO在Fe+作用下发生反应的能量变化及反应历程如图所示,两步反应分別为:
2
①NO+Fe+=N +FeO (慢):②FeO++CO=CO +Fe+ (快)。下列说法正确的是
2 2 2
A.反应①是氧化还原反应,反应②是非氧化还原反应
B.两步反应均为放热反应,总反应的化学反应速率由反应②决定
[来源:Zxxk.Com]
C.Fe+使反应的活化能减小,FeO+是中间产物
D.若转移lmol电子,则消耗II.2LN O
2
5.已知2SO (g)+O(g) 2SO (g),△H=-198kJ/mol,在 VO 存在时反应过程中的能量变化如图所示。下列
2 2 3 2 5
叙述正确的是
A.△H= E- E +E-E
4 3 2 1
B.加入VO 后反应经过两步完成,其中第一步决定反应速率
2 5
C.加入VO,△H不变,但反应速率改变
2 5
D.向密闭容器中充入2molSO 和1molO ,发生上述反应达平衡时,反应放热198kJ
2 2
6.“钙基固硫”是将煤中的硫元素以CaSO 的形式固定脱硫,而煤炭燃烧过程中产生的CO又会发生反应I
4
和反应II,导致脱硫效率降低。某温度下,反应I的速率(v)大于反应II的速率(v),则下列反应过程能量变化
1 2
示意图正确的是
反应I:CaSO(s)+CO(g) CaO(s)+SO (g)+CO (g) H=+218.4kJ·mol-1
4 2 2 1
△
反应II:CaSO(s)+4CO(g) CaS(s)+4CO (g) H=-175.6kJ·mol-1
4 2 2
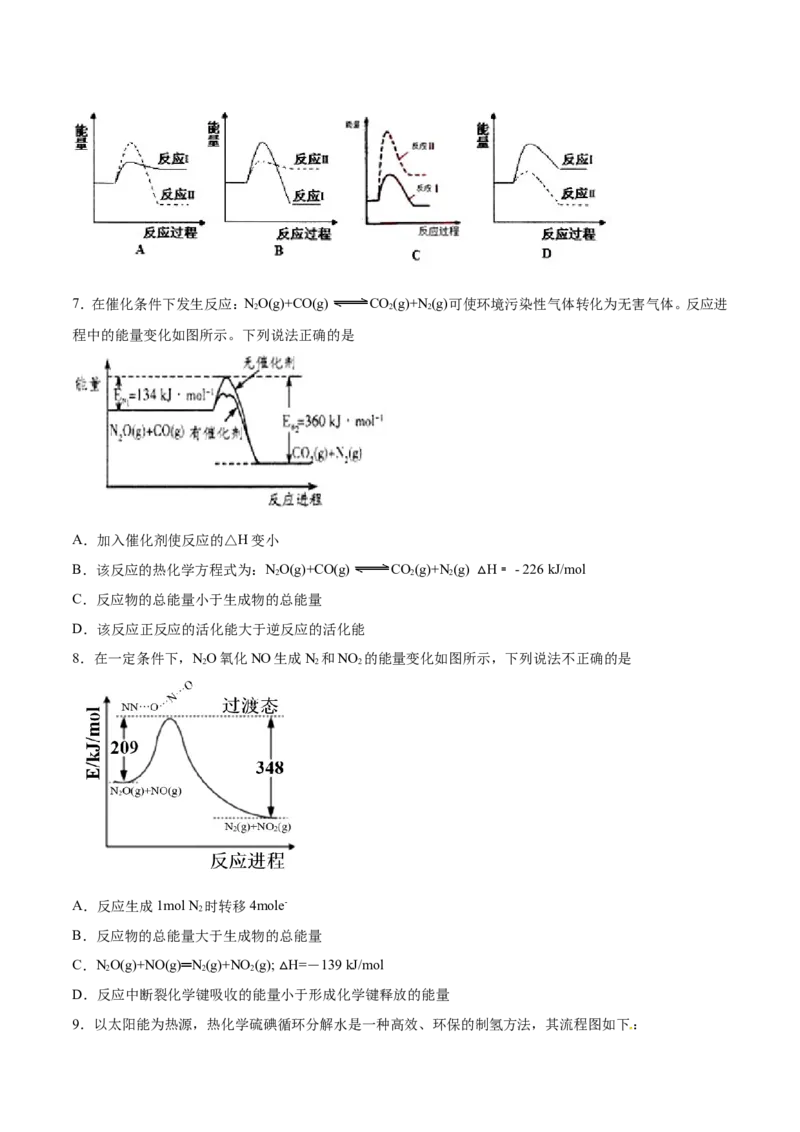
△7.在催化条件下发生反应:NO(g)+CO(g) CO(g)+N(g)可使环境污染性气体转化为无害气体。反应进
2 2 2
程中的能量变化如图所示。下列说法正确的是
A.加入催化剂使反应的△H变小
B.该反应的热化学方程式为:NO(g)+CO(g) CO(g)+N(g) H﹦ - 226 kJ/mol
2 2 2
C.反应物的总能量小于生成物的总能量 △
D.该反应正反应的活化能大于逆反应的活化能
8.在一定条件下,NO氧化NO生成N 和NO 的能量变化如图所示,下列说法不正确的是
2 2 2
A.反应生成1mol N 时转移4mole-
2
B.反应物的总能量大于生成物的总能量
C.NO(g)+NO(g)═N (g)+NO (g); H=-139 kJ/mol
2 2 2
D.反应中断裂化学键吸收的能量△小于形成化学键释放的能量
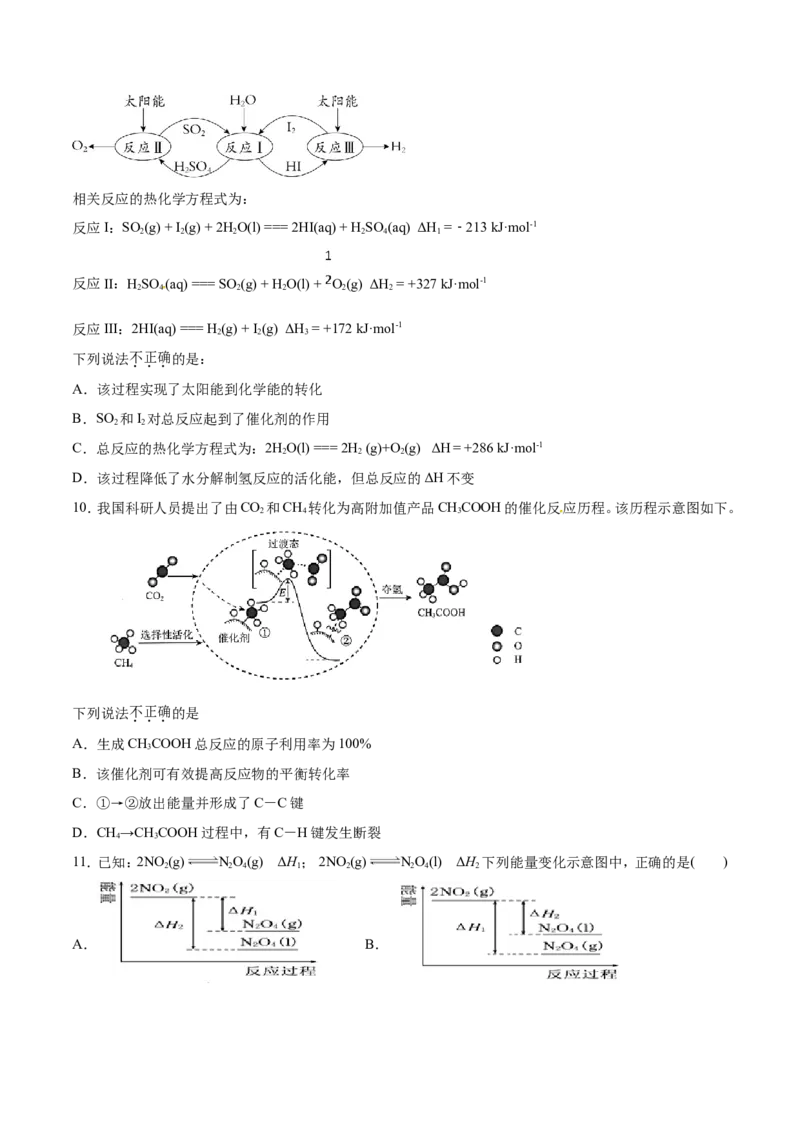
9.以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:相关反应的热化学方程式为:
反应I:SO (g) + I (g) + 2HO(l) === 2HI(aq) + H SO (aq) ΔH =﹣213 kJ·mol-1
2 2 2 2 4 1
反应II:HSO (aq) === SO (g) + HO(l) + O(g) ΔH = +327 kJ·mol-1
2 4 2 2 2 2
反应III:2HI(aq) === H (g) + I (g) ΔH = +172 kJ·mol-1
2 2 3
下列说法不正确的是:
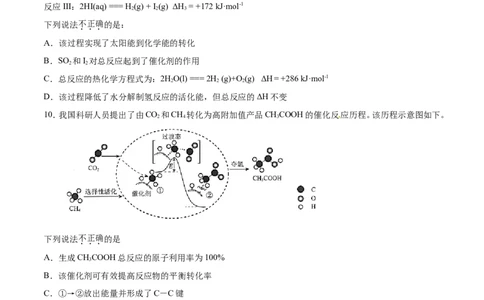
A.该过程实现了太阳能到化学能的转化
B.SO 和I 对总反应起到了催化剂的作用
2 2
C.总反应的热化学方程式为:2HO(l) === 2H (g)+O (g) ΔH= +286 kJ·mol-1
2 2 2
D.该过程降低了水分解制氢反应的活化能,但总反应的ΔH不变
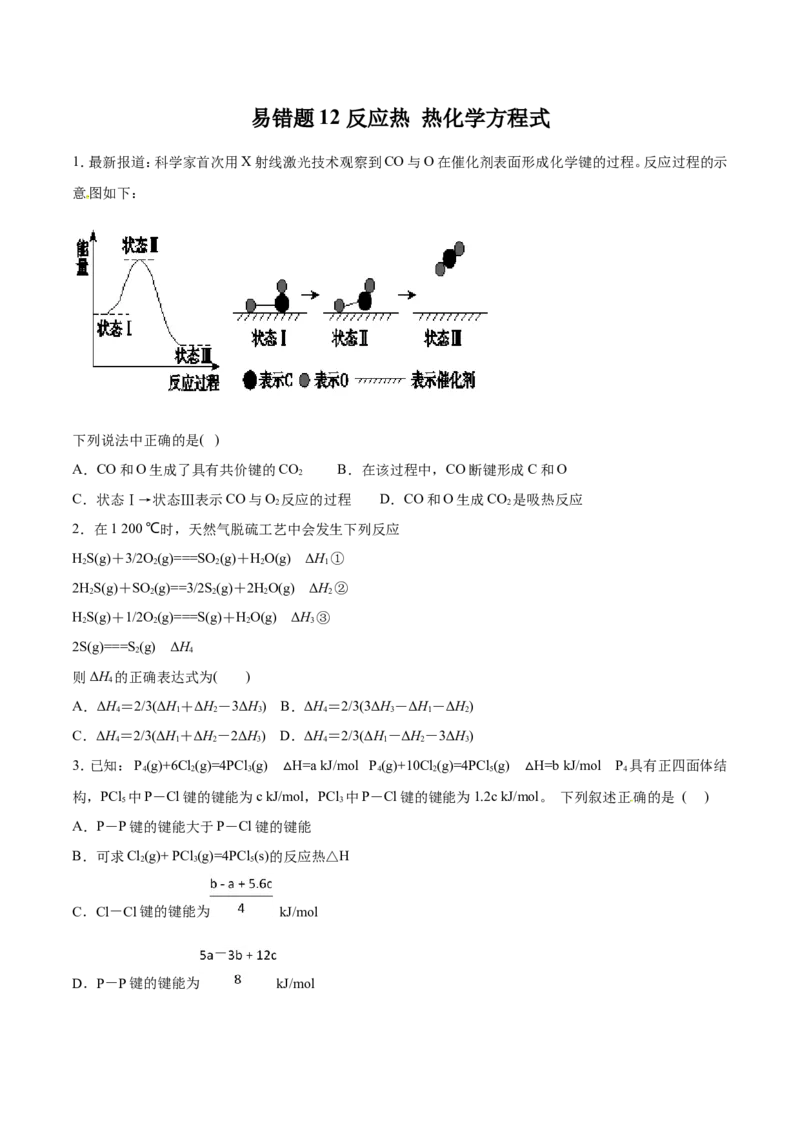
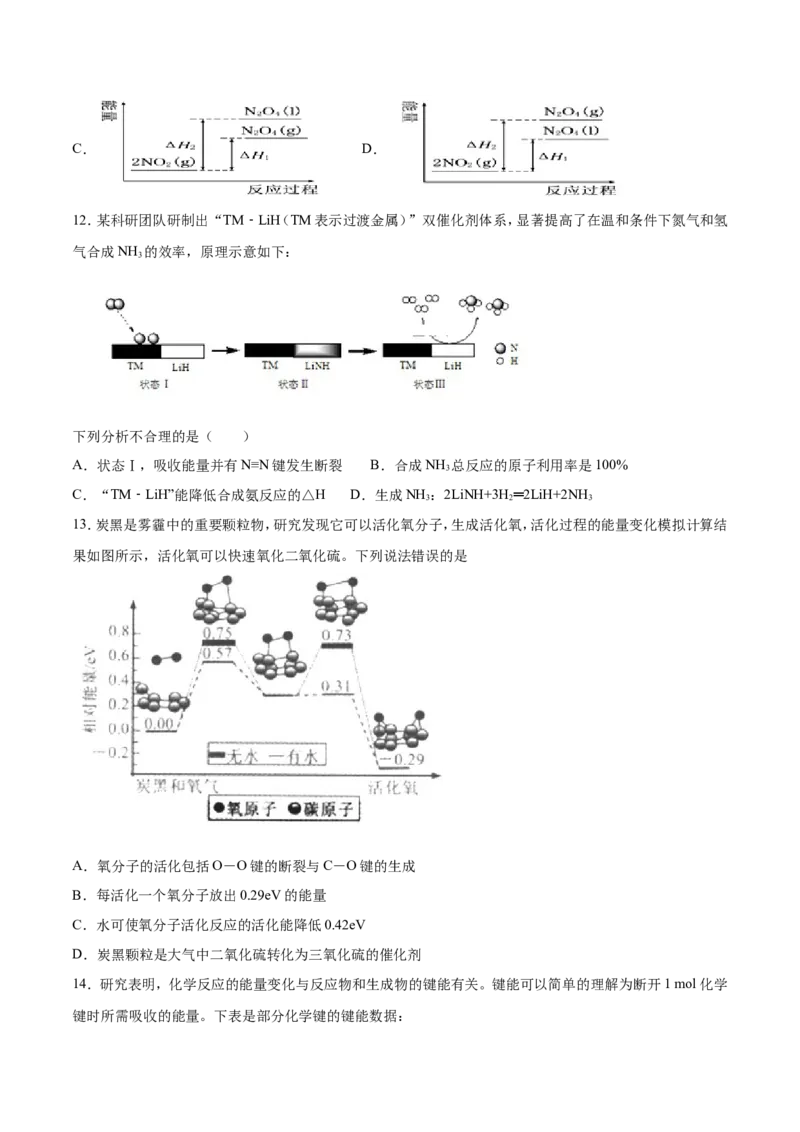
10.我国科研人员提出了由CO 和CH 转化为高附加值产品CHCOOH的催化反应历程。该历程示意图如下。
2 4 3
下列说法不正确的是
[来源:学|科|网Z|X|X|K]
A.生成CHCOOH总反应的原子利用率为100%
3
B.该催化剂可有效提高反应物的平衡转化率
C.①→②放出能量并形成了C-C键
D.CH→CHCOOH过程中,有C-H键发生断裂
4 3
11.已知:2NO (g) NO(g) ΔH; 2NO (g) NO(l) ΔH 下列能量变化示意图中,正确的是( )
2 2 4 1 2 2 4 2
A. B.C. D.
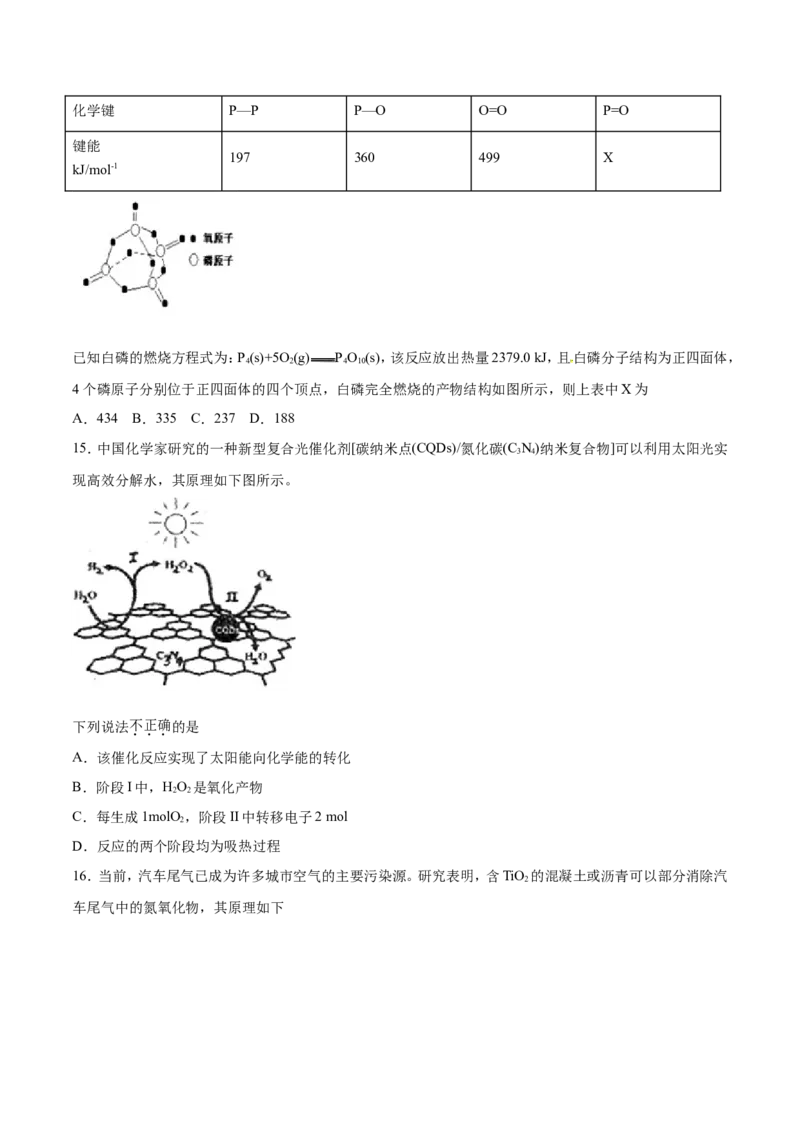
12.某科研团队研制出“TM﹣LiH(TM表示过渡金属)”双催化剂体系,显著提高了在温和条件下氮气和氢
气合成NH 的效率,原理示意如下:
3
下列分析不合理的是( )
A.状态Ⅰ,吸收能量并有N≡N键发生断裂 B.合成NH 总反应的原子利用率是100%
3
C.“TM﹣LiH”能降低合成氨反应的△H D.生成NH :2LiNH+3H ═2LiH+2NH
3 2 3
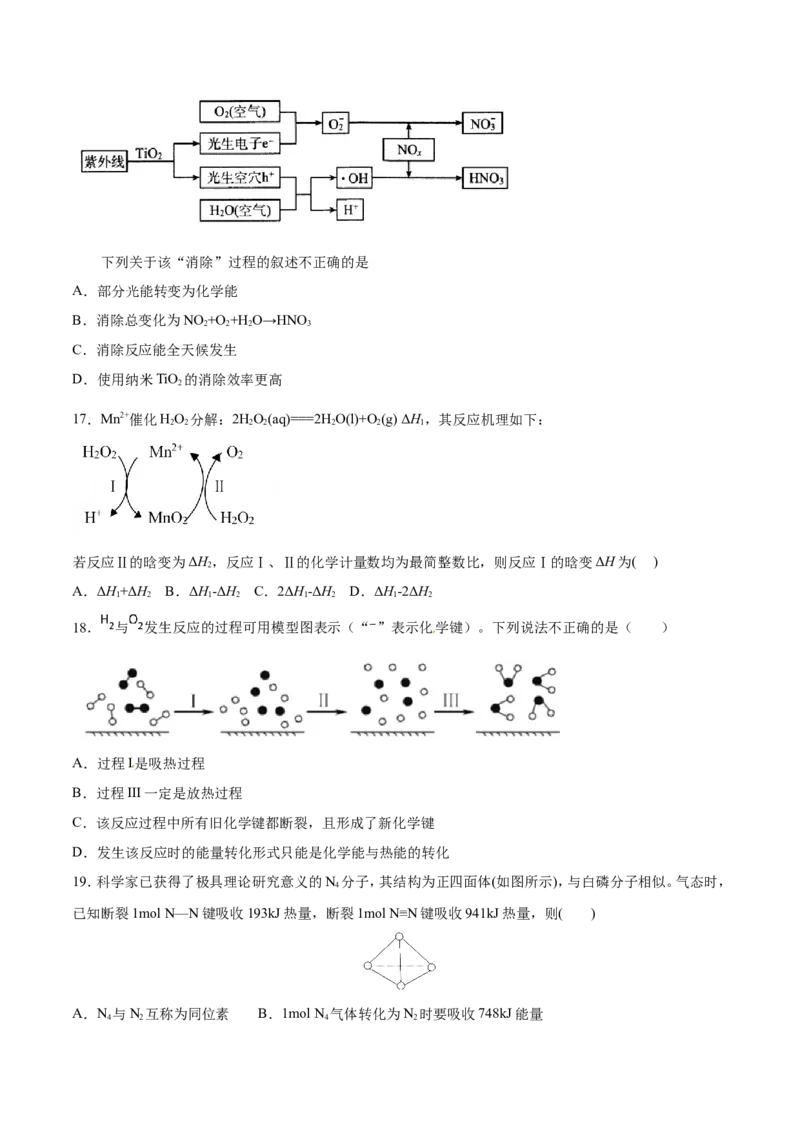
13.炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结
果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是
A.氧分子的活化包括O-O键的断裂与C-O键的生成
B.每活化一个氧分子放出0.29eV的能量
C.水可使氧分子活化反应的活化能降低0.42eV
D.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
14.研究表明,化学反应的能量变化与反应物和生成物的键能有关。键能可以简单的理解为断开1 mol 化学
键时所需吸收的能量。下表是部分化学键的键能数据:化学键 P—P P—O O=O P=O
[来源:学|科|网]
键能
197 360 499 X
kJ/mol-1
已知白磷的燃烧方程式为:P(s)+5O(g) PO (s),该反应放出热量2379.0 kJ,且白磷分子结构为正四面体,
4 2 4 10
4个磷原子分别位于正四面体的四个顶点,白磷完全燃烧的产物结构如图所示,则上表中X为
A.434 B.335 C.237 D.188
15.中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C N)纳米复合物]可以利用太阳光实
3 4
现高效分解水,其原理如下图所示。
下列说法不正确的是
A.该催化反应实现了太阳能向化学能的转化
B.阶段I中,HO 是氧化产物
2 2
C.每生成1molO ,阶段II中转移电子2 mol
2
D.反应的两个阶段均为吸热过程
16.当前,汽车尾气已成为许多城市空气的主要污染源。研究表明,含TiO 的混凝土或沥青可以部分消除汽
2
车尾气中的氮氧化物,其原理如下下列关于该“消除”过程的叙述不正确的是
[来源:学&科&网]
A.部分光能转变为化学能
B.消除总变化为NO +O +H O→HNO
2 2 2 3
C.消除反应能全天候发生
D.使用纳米TiO 的消除效率更高
2
17.Mn2+催化HO 分解:2HO(aq)===2H O(l)+O(g) ΔH,其反应机理如下:
2 2 2 2 2 2 1
若反应Ⅱ的晗变为ΔH,反应Ⅰ、Ⅱ的化学计量数均为最简整数比,则反应Ⅰ的晗变ΔH为( )
2
A.ΔH+ΔH B.ΔH-ΔH C.2ΔH-ΔH D.ΔH-2ΔH
1 2 1 2 1 2 1 2
18. 与 发生反应的过程可用模型图表示(“ ”表示化学键)。下列说法不正确的是( )
A.过程I是吸热过程
B.过程III一定是放热过程
C.该反应过程中所有旧化学键都断裂,且形成了新化学键
D.发生该反应时的能量转化形式只能是化学能与热能的转化
19.科学家已获得了极具理论研究意义的N 分子,其结构为正四面体(如图所示),与白磷分子相似。气态时,
4
已知断裂1mol N—N键吸收193kJ热量,断裂1mol N≡N键吸收941kJ热量,则( )
A.N 与N 互称为同位素 B.1mol N 气体转化为N 时要吸收748kJ能量
4 2 4 2C.N 是N 的同系物 D.1mol N 气体转化为N 时要放出724kJ能量
4 2 4 2
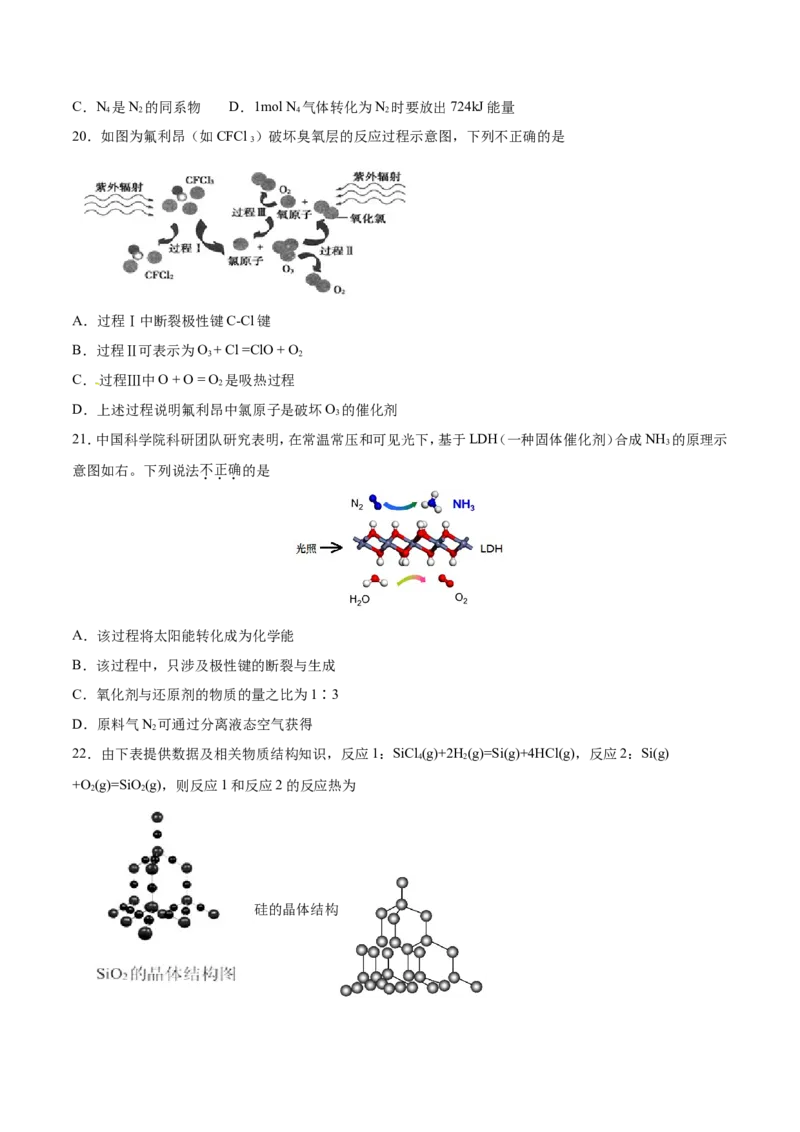
20.如图为氟利昂(如CFCl )破坏臭氧层的反应过程示意图,下列不正确的是
3
A.过程Ⅰ中断裂极性键C-Cl键
B.过程Ⅱ可表示为O + Cl =ClO + O
3 2
C.过程Ⅲ中O + O = O 是吸热过程
2
D.上述过程说明氟利昂中氯原子是破坏O 的催化剂
3
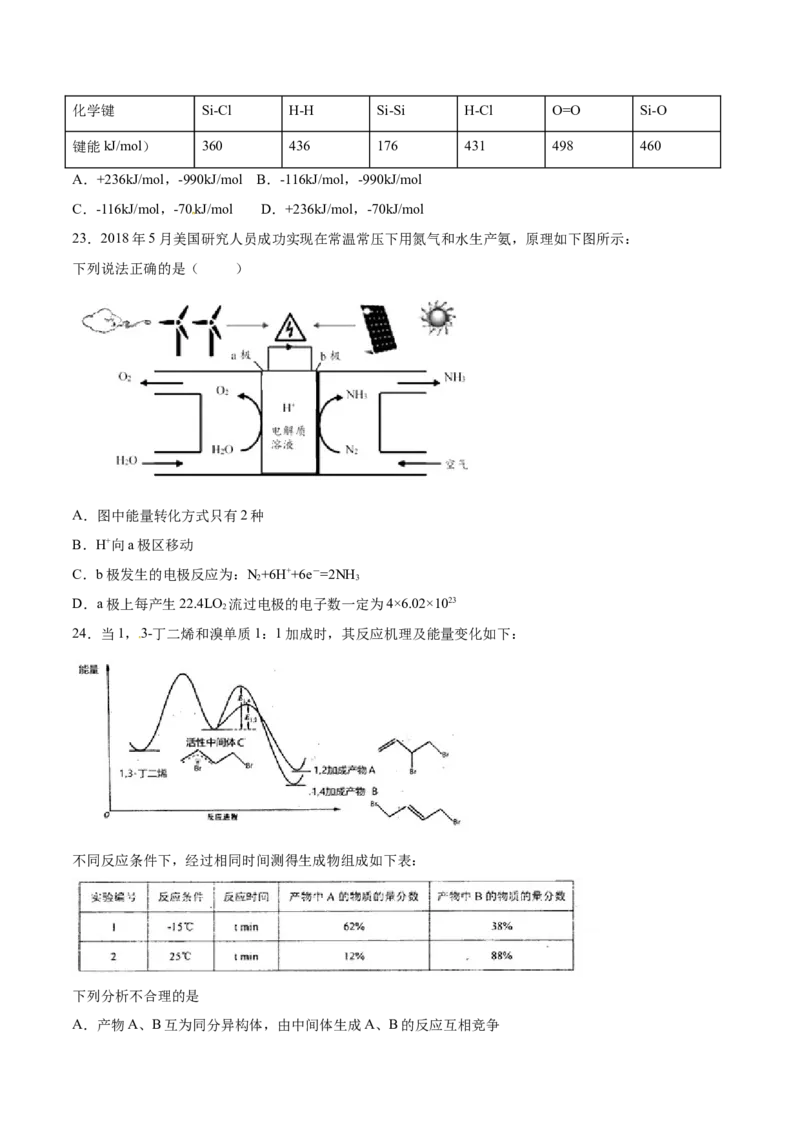
21.中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH 的原理示
3
意图如右。下列说法不正确的是
A.该过程将太阳能转化成为化学能
B.该过程中,只涉及极性键的断裂与生成
C.氧化剂与还原剂的物质的量之比为1∶3
D.原料气N 可通过分离液态空气获得
2
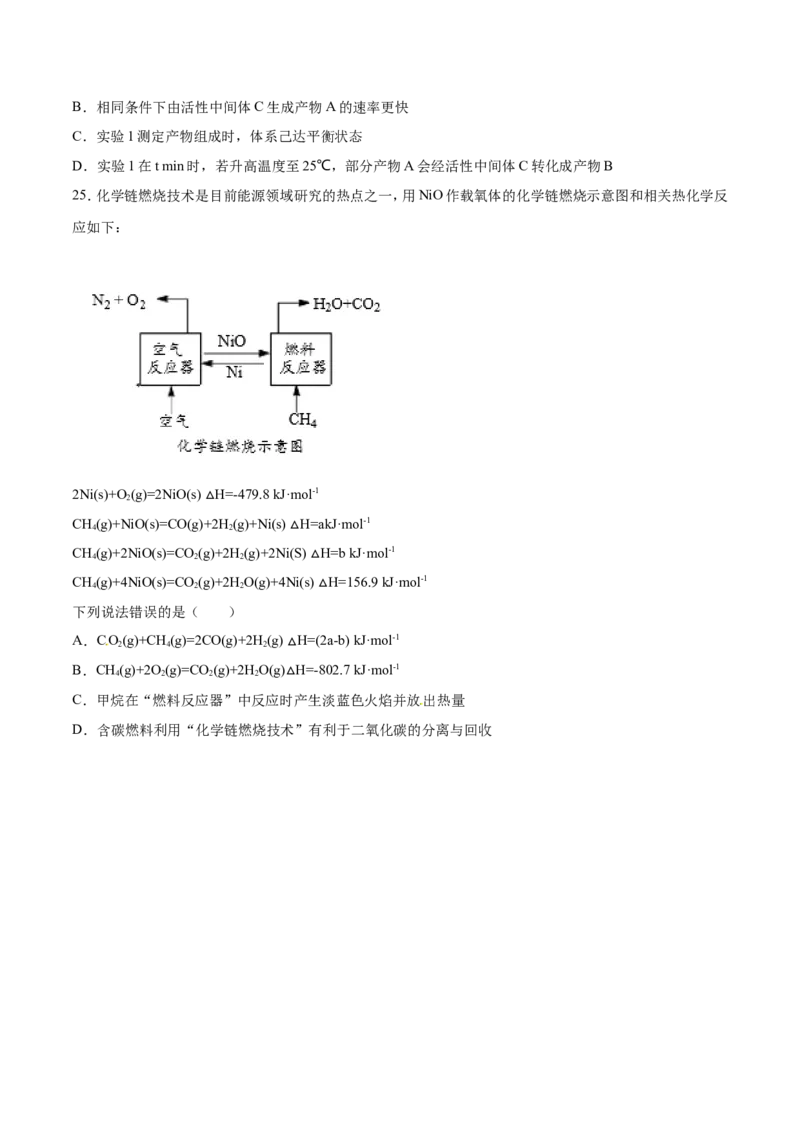
22.由下表提供数据及相关物质结构知识,反应1:SiCl (g)+2H(g)=Si(g)+4HCl(g),反应2:Si(g)
4 2
+O (g)=SiO (g),则反应1和反应2的反应热为
2 2
硅的晶体结构化学键 Si-Cl H-H Si-Si H-Cl O=O Si-O
键能kJ/mol) 360 436 176 431 498 460
A.+236kJ/mol,-990kJ/mol B.-116kJ/mol,-990kJ/mol
C.-116kJ/mol,-70kJ/mol D.+236kJ/mol,-70kJ/mol
23.2018年5月美国研究人员成功实现在常温常压下用氮气和水生产氨,原理如下图所示:
下列说法正确的是( )
A.图中能量转化方式只有2种
B.H+向a极区移动
C.b极发生的电极反应为:N+6H++6e-=2NH
2 3
D.a极上每产生22.4LO 流过电极的电子数一定为4×6.02×1023
2
24.当1,3-丁二烯和溴单质1:1加成时,其反应机理及能量变化如下:
不同反应条件下,经过相同时间测得生成物组成如下表:
[来源:学,科,网]
下列分析不合理的是
A.产物A、B互为同分异构体,由中间体生成A、B的反应互相竞争B.相同条件下由活性中间体C生成产物A的速率更快
C.实验1测定产物组成时,体系己达平衡状态
D.实验1在t min时,若升高温度至25℃,部分产物A会经活性中间体C转化成产物B
25.化学链燃烧技术是目前能源领域研究的热点之一,用NiO作载氧体的化学链燃烧示意图和相关热化学反
应如下:
2Ni(s)+O (g)=2NiO(s) H=-479.8 kJ·mol-1
2
CH
4
(g)+NiO(s)=CO(g)+△2H
2
(g)+Ni(s) H=akJ·mol-1
CH
4
(g)+2NiO(s)=CO
2
(g)+2H
2
(g)+2Ni(△S) H=b kJ·mol-1
CH
4
(g)+4NiO(s)=CO
2
(g)+2H
2
O(g)+4Ni(s)△ H=156.9 kJ·mol-1
下列说法错误的是( ) △
A.CO(g)+CH (g)=2CO(g)+2H(g) H=(2a-b) kJ·mol-1
2 4 2
B.CH
4
(g)+2O
2
(g)=CO
2
(g)+2H
2
O(g)△H=-802.7 kJ·mol-1
C.甲烷在“燃料反应器”中反应时△产生淡蓝色火焰并放出热量
D.含碳燃料利用“化学链燃烧技术”有利于二氧化碳的分离与回收