文档内容
专题 12 弱电解质的电离平衡
2021年化学高考题
一、单选题
c2(M)
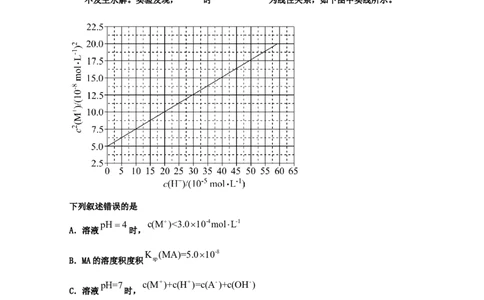
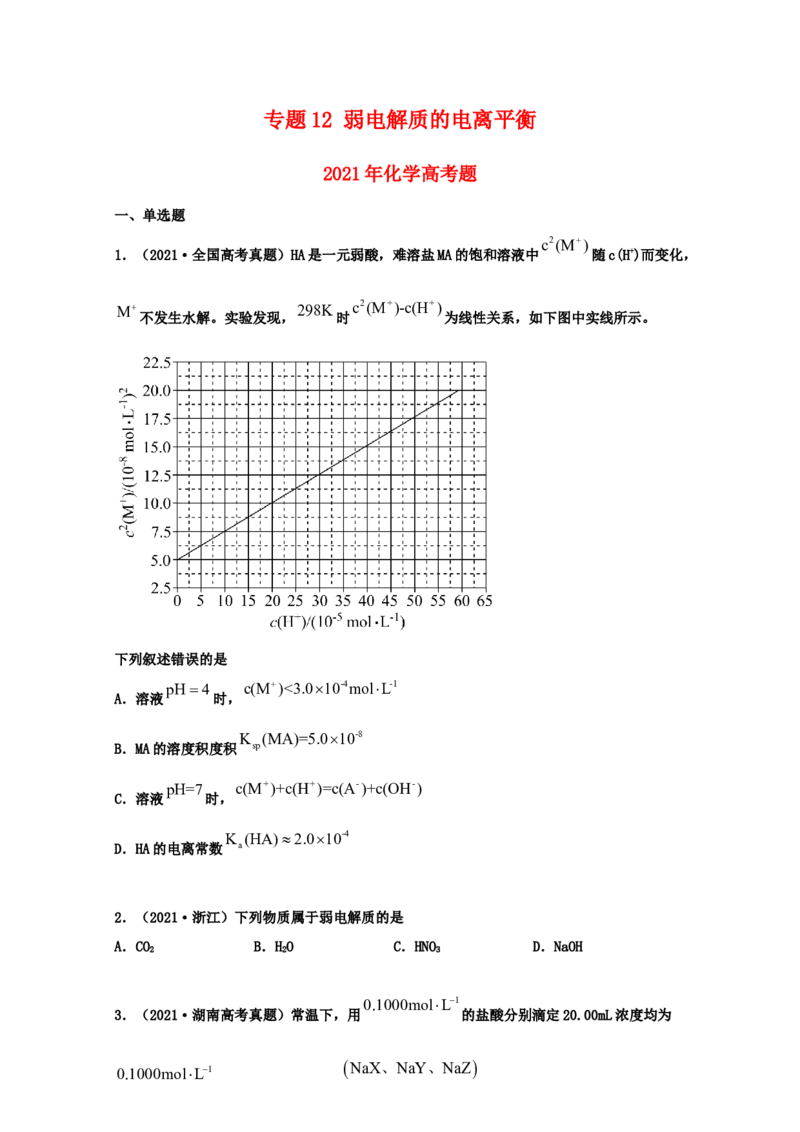
1.(2021·全国高考真题)HA是一元弱酸,难溶盐MA的饱和溶液中 随c(H+)而变化,
M 298K
c2(M+)-c(H+)
不发生水解。实验发现, 时 为线性关系,如下图中实线所示。
下列叙述错误的是
pH4 c(M)<3.010-4molL-1
A.溶液 时,
K (MA)=5.010-8
B.MA的溶度积度积 sp
pH=7 c(M+)+c(H+)=c(A-)+c(OH-)
C.溶液 时,
K (HA)2.010-4
D.HA的电离常数 a
2.(2021·浙江)下列物质属于弱电解质的是
A.CO B.HO C.HNO D.NaOH
2 2 3
0.1000molL1
3.(2021·湖南高考真题)常温下,用 的盐酸分别滴定20.00mL浓度均为
NaX、NaY、NaZ
0.1000molL1NaX、NaY、NaZ
0.1000molL1
三种一元弱酸的钠盐 溶液,滴定曲线如图所示。下列
判断错误的是
c
Na
c
X
c
OH
c
H
A.该NaX溶液中:
K (HX) K (HY) K (HZ)
B.三种一元弱酸的电离常数: a a a
c
X
c
Y
c
Z
C.当pH7时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
c
X
c
Y
c
Z
c
H
c
OH
4.(2021·浙江高考真题)实验测得10 mL 0.50 mol·L-1NHCl溶液、10 mL
4
0.50mol·L-1CHCOONa溶液的pH分别随温度与稀释加水量的变化如图所示。已知25 ℃时
3
CHCOOH和NH·HO的电离常数均为1.8×10-5.下列说法不正确的是
3 3 2A.图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
0.50
B.将NHCl溶液加水稀释至浓度 x mol·L-1,溶液pH变化值小于lgx
4
C.随温度升高,K增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D.25 ℃时稀释相同倍数的NHCl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-
4 3 3
c(NH4)
5.(2021·浙江高考真题)下列物质属于强电解质的是
A.KOH B.HPO C.SO D.CHCHO
3 4 3 3
二、多选题
6.(2021·山东高考真题)赖氨酸[HN+(CH)CH(NH)COO-,用HR表示]是人体必需氨基酸,
3 2 4 2
其盐酸盐(HRCl)在水溶液中存在如下平衡:HR2+ K 1 HR+ K 2 HR K 3 R-。向一定浓
3 2 3 2
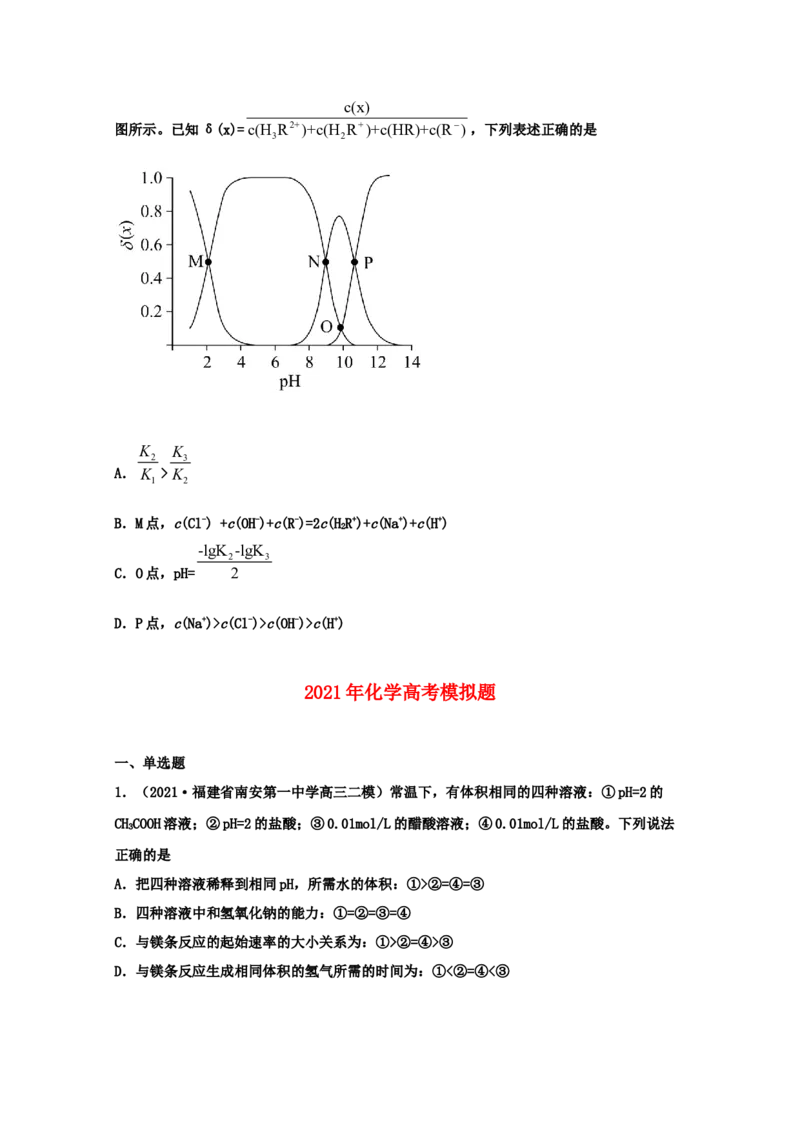
度的HRCl 溶液中滴加NaOH溶液,溶液中HR2+、HR+、HR和R-的分布系数δ(x)随pH变化如
3 2 3 2c(x)
图所示。已知δ(x)=c(H R2+)+c(H R+)+c(HR)+c(R) ,下列表述正确的是
3 2
K K
2 3
A. K >K
1 2
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(HR+)+c(Na+)+c(H+)
2
-lgK -lgK
2 3
C.O点,pH= 2
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
2021年化学高考模拟题
一、单选题
1.(2021·福建省南安第一中学高三二模)常温下,有体积相同的四种溶液:①pH=2的
CHCOOH溶液;②pH=2的盐酸;③0.01mol/L的醋酸溶液;④0.01mol/L的盐酸。下列说法
3
正确的是
A.把四种溶液稀释到相同pH,所需水的体积:①>②=④=③
B.四种溶液中和氢氧化钠的能力:①=②=③=④
C.与镁条反应的起始速率的大小关系为:①>②=④>③
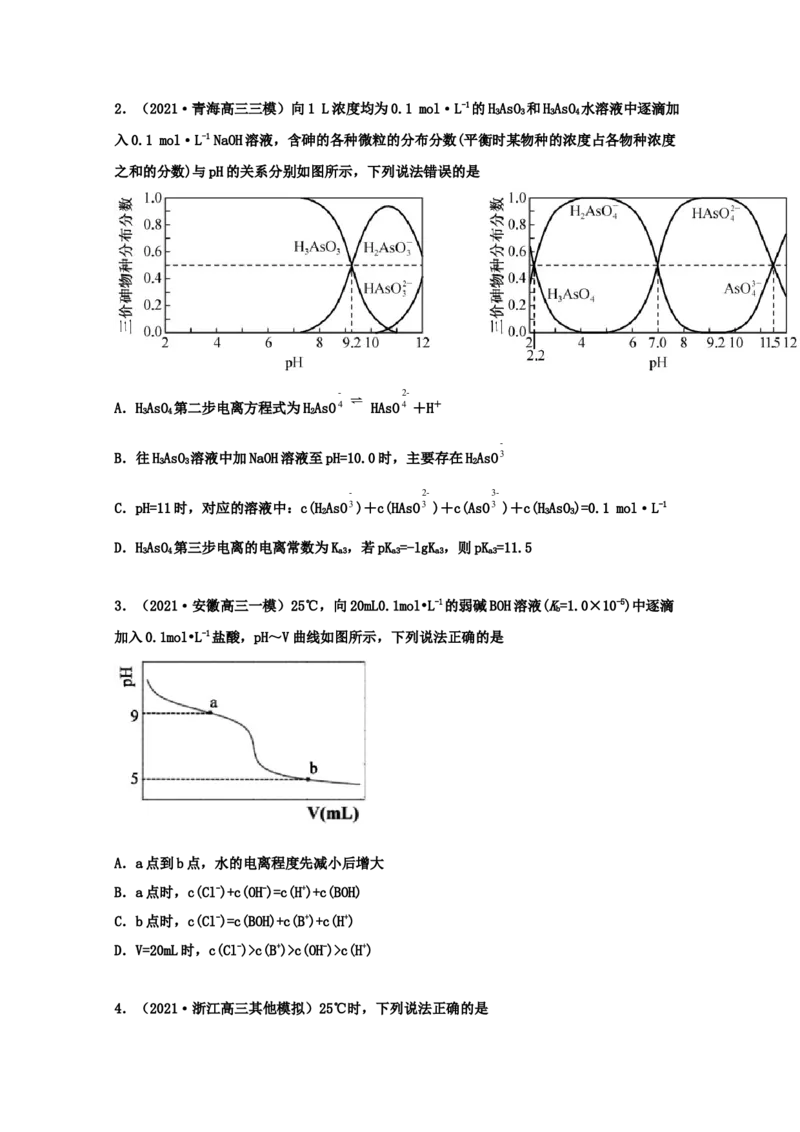
D.与镁条反应生成相同体积的氢气所需的时间为:①<②=④<③2.(2021·青海高三三模)向1 L浓度均为0.1 mol·L-1的HAsO 和HAsO 水溶液中逐滴加
3 3 3 4
入0.1 mol·L-1 NaOH溶液,含砷的各种微粒的分布分数(平衡时某物种的浓度占各物种浓度
之和的分数)与pH的关系分别如图所示,下列说法错误的是
- 2-
A.HAsO 第二步电离方程式为HAsO4 HAsO4 +H+
3 4 2
-
B.往HAsO 溶液中加NaOH溶液至pH=10.0时,主要存在HAsO3
3 3 2
- 2- 3-
C.pH=11时,对应的溶液中:c(HAsO3)+c(HAsO3 )+c(AsO3 )+c(HAsO)=0.1 mol·L-1
2 3 3
D.HAsO 第三步电离的电离常数为K ,若pK =-lgK ,则pK =11.5
3 4 a3 a3 a3 a3
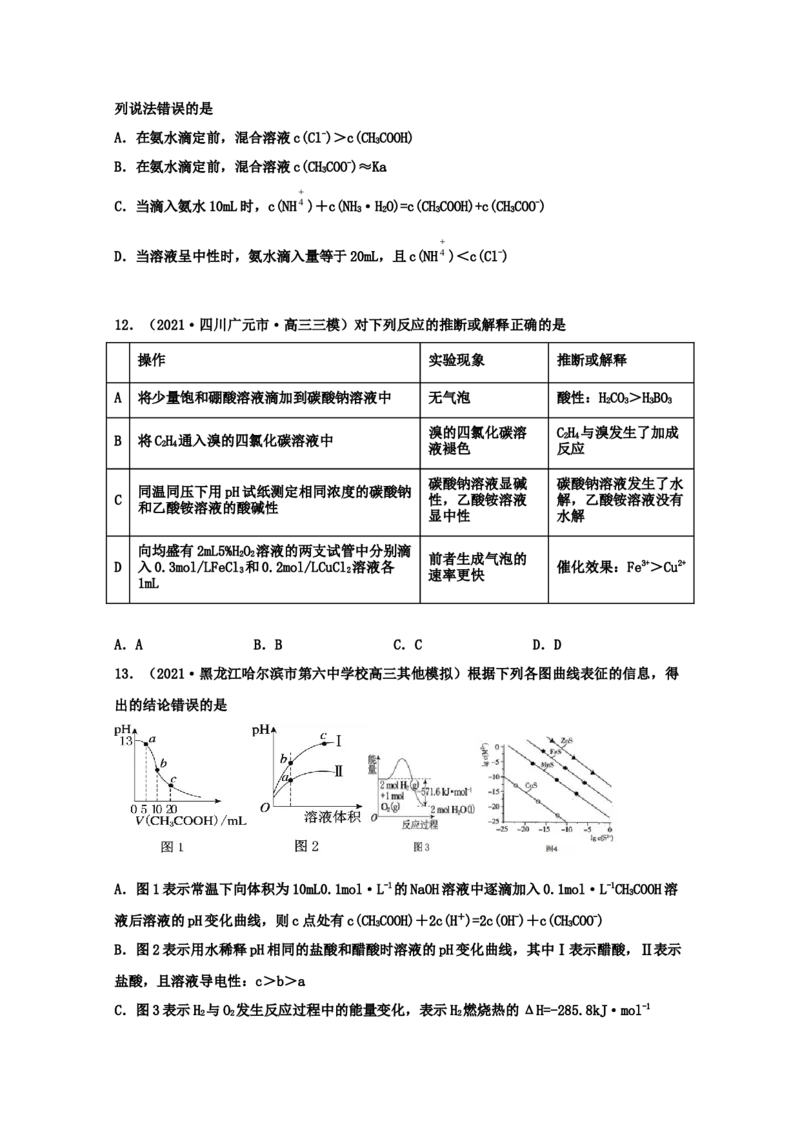
3.(2021·安徽高三一模)25℃,向20mL0.1mol•L-1的弱碱BOH溶液(K=1.0×10-5)中逐滴
b
加入0.1mol•L-1盐酸,pH~V曲线如图所示,下列说法正确的是
A.a点到b点,水的电离程度先减小后增大
B.a点时,c(Cl-)+c(OH-)=c(H+)+c(BOH)
C.b点时,c(Cl-)=c(BOH)+c(B+)+c(H+)
D.V=20mL时,c(Cl-)>c(B+)>c(OH-)>c(H+)
4.(2021·浙江高三其他模拟)25℃时,下列说法正确的是A.HA溶液与NaOH溶液按物质的量1:1恰好完全反应时,溶液酸碱性无法判断
2
B.可溶性正盐BA溶液呈中性,可以推测BA对水的电离没有影响
C.醋酸的电离度:pH=3的醋酸溶液大于pH=4的醋酸溶液
D.pH=2的HCl和pH=12的Ba(OH) 溶液等体积混合后,溶液显碱性
2
5.(2021·天津)草酸(HCO)是一种二元弱酸。实验室配制了0.0100mol·L-1NaCO 标准
2 2 4 2 2 4
溶液,现对25℃时该溶液的性质进行探究,下列所得结论正确的是
-
A.测得0.0100mol·L-1NaCO 溶液pH为8.6 ,此时溶液中存在:c (Na+)> c(HCO4)>
2 2 4 2
2-
c(CO4 )>c(H+)
2
- 2-
B.向该溶液中滴加稀盐酸至溶液pH=7, 此时溶液中存在,c(Na+)=c(HCO4 )+2c(CO4 )
2 2
C.已知25℃时K (CaCO)=2.5×10-9向该溶液中加入等体积0.0200mol·L-1CaCl 溶液,所得
sp 2 4 2
2-
上层清液中c(CO4 )=5.00×10-7 mol·L-1
2
2-
D.向该溶液中加入足量稀硫酸酸化后,再滴加KMnO 溶液,发生反应的离子方程式为CO4
4 2
-
+4MnO4 +14H+=2CO↑+4Mn2++7HO
2 2
6.(2021·阜新市第二高级中学高三其他模拟)常温下,下列说法正确的是
c
OH-
A.向0.1mol•L-1的氨水中加入少量硫酸铵固体,则溶液中 增大
cNH H O
3 2
B.向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度均先增大后减小
2- -
C.0.1mol•L-1NaCO 溶液和0.1mol•L-1NaHCO 溶液等体积混合:c(CO3 )+2c(OH-)=c(HCO3)
2 3 3
+3c(HCO)+2c(H+)
2 3
D.将CHCOONa、HCl两溶液混合后,溶液呈中性,则溶液中c(Na+)0,平衡时K(甲)1。下列说法正确的是
A.最高价含氧酸的酸性:Y>Z
B.氢化物的沸点:M>W>Z
C.W的单质可与M的氢化物发生置换反应
D.YW 分子中各原子最外层都达到8电子稳定结构
3
16.(2021·江苏高三其他模拟)室温下,通过实验研究亚硫酸盐的性质,已知
K(HSO)=1.54×10-2,K(HSO)=1.02×10-7
a1 2 3 a2 2 3
实验 实验操作和现象
1 把SO 通入氨水,测得溶液pH=7
2
2 向0.1mol/LNaSO 溶液中加入过量0.2mol/LCaCl 溶液,产生白色沉淀
2 3 2
3 向0.1mol/LNaHSO 溶液中滴入一定量NaOH溶液至pH=7
3
4 把少量氯气通入NaSO 溶液中,测得pH变小
2 3
下列说法错误的是c(NH)
4
A.实验1中,可算出c(HSO) =3.04
3
2
B.实验2反应静置后的上层清液中有c(Ca2+)·c(SO3 )=K(CaSO)
sp 3
2
C.实验3中:c(Na+)>2[c(HSO3 )+c(SO3 )+c(HSO)]
2 3
2 2
D.实验4中反应的离子方程式为:HO+Cl+SO3 =SO4 +2H++2Cl-
2 2
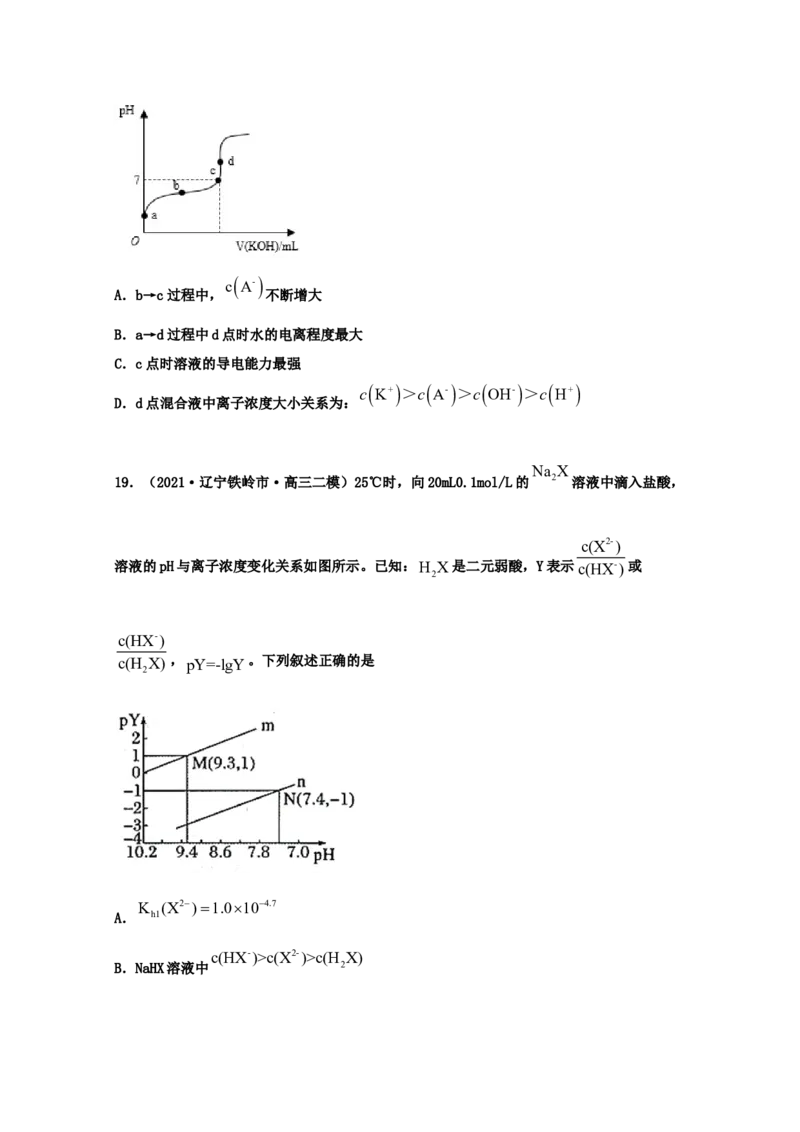
17.(2021·福建厦门外国语学校高三其他模拟)25℃时,0.10 L某二元弱酸HA用1.00
2
mol·L-1NaOH溶液调节其pH,溶液中HA、HA-及A2-的物质的量浓度变化如图所示:
2
下列说法正确的是
A.HA的Ka=1×10-11
2 2
B.在Z点,由水电离出的氢离子浓度约10-10 mol/L
C.在Y点时,c(Na+)>3c(A2-)
D.0.1 mol·L-1NaHA溶液中:c(Na+)>c(HA-)>c(HA)>c(A2-)
2
0.1molL1 KOH 10mL
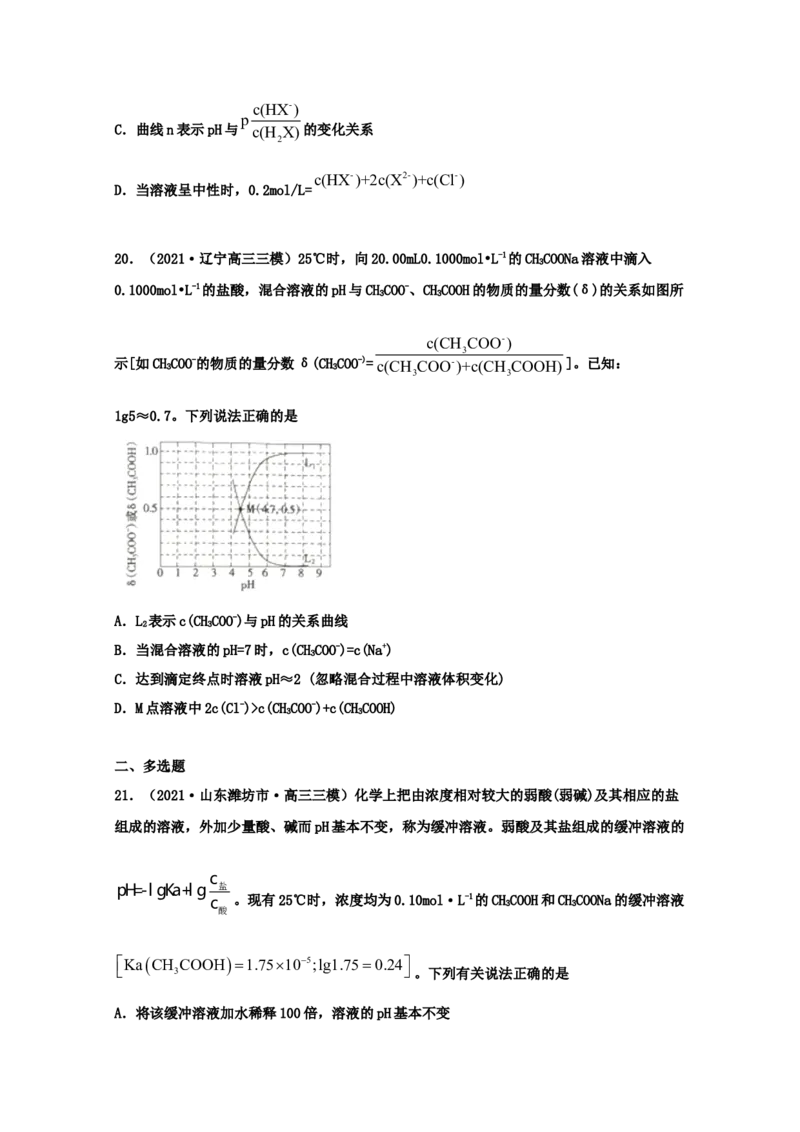
18.(2021·全国高三专题练习)常温下,用 溶液滴定
0.1molL1 HA
溶液的滴定曲线如图所示(d点为恰好反应点)。下列说法错误的是c
A-
A.b→c过程中, 不断增大
B.a→d过程中d点时水的电离程度最大
C.c点时溶液的导电能力最强
c
K+>c A->c OH->c H+
D.d点混合液中离子浓度大小关系为:
Na X
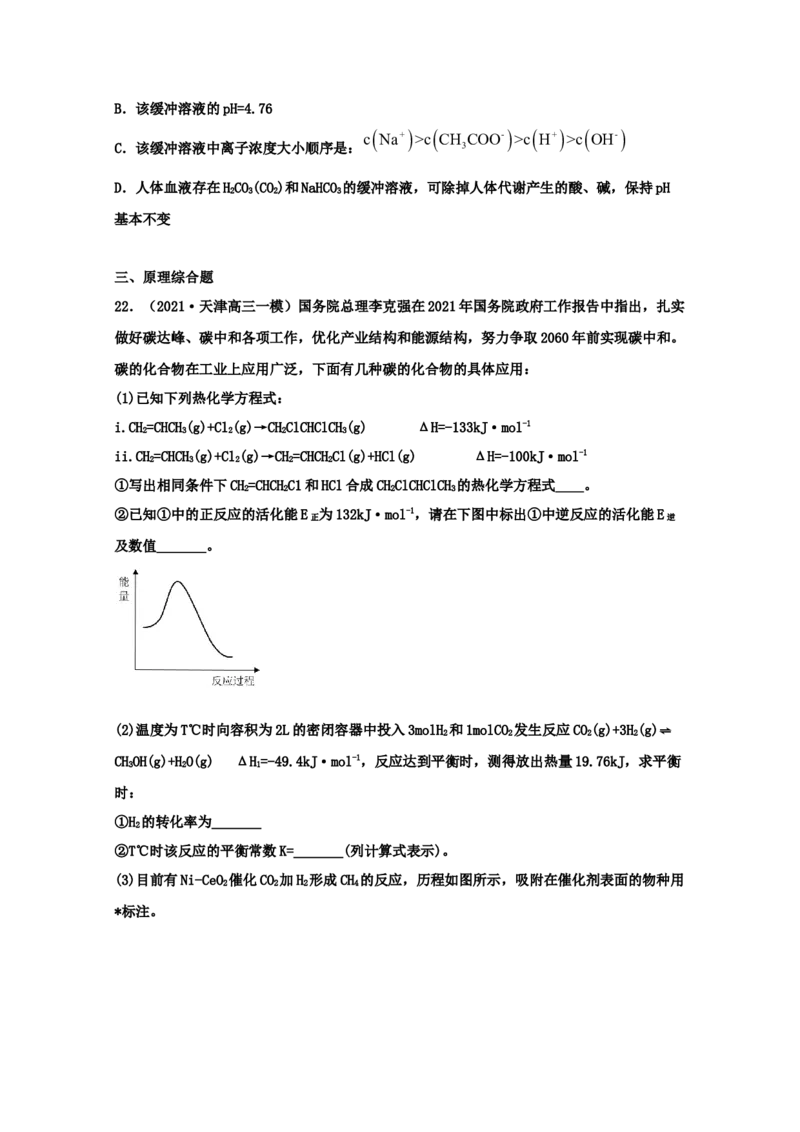
19.(2021·辽宁铁岭市·高三二模)25℃时,向20mL0.1mol/L的 2 溶液中滴入盐酸,
c(X2-)
溶液的pH与离子浓度变化关系如图所示。已知:H X是二元弱酸,Y表示c(HX-)或
2
c(HX-)
c(H X) ,pY=-lgY。下列叙述正确的是
2
K (X2)1.0104.7
A. h1
c(HX-)>c(X2-)>c(H X)
B.NaHX溶液中 2c(HX-)
p
C.曲线n表示pH与 c(H X)的变化关系
2
c(HX-)+2c(X2-)+c(Cl-)
D.当溶液呈中性时,0.2mol/L=
20.(2021·辽宁高三三模)25℃时,向20.00mL0.1000mol•L-1的CHCOONa溶液中滴入
3
0.1000mol•L-1的盐酸,混合溶液的pH与CHCOO-、CHCOOH的物质的量分数(δ)的关系如图所
3 3
c(CH COO-)
3
示[如CH
3
COO-的物质的量分数δ(CH
3
COO-)=c(CH COO-)+c(CH COOH)]。已知:
3 3
1g5≈0.7。下列说法正确的是
A.L 表示c(CHCOO-)与pH的关系曲线
2 3
B.当混合溶液的pH=7时,c(CHCOO-)=c(Na+)
3
C.达到滴定终点时溶液pH≈2 (忽略混合过程中溶液体积变化)
D.M点溶液中2c(Cl-)>c(CHCOO-)+c(CHCOOH)
3 3
二、多选题
21.(2021·山东潍坊市·高三三模)化学上把由浓度相对较大的弱酸(弱碱)及其相应的盐
组成的溶液,外加少量酸、碱而pH基本不变,称为缓冲溶液。弱酸及其盐组成的缓冲溶液的
c
pH=-lgKa+lg 盐
c 。现有25℃时,浓度均为0.10mol·L-1的CH 3 COOH和CH 3 COONa的缓冲溶液
酸
KaCH COOH1.75105;lg1.750.24
3 。下列有关说法正确的是
A.将该缓冲溶液加水稀释100倍,溶液的pH基本不变B.该缓冲溶液的pH=4.76
c
Na+
>c
CH
COO-
>c
H+
>c
OH-
C.该缓冲溶液中离子浓度大小顺序是: 3
D.人体血液存在HCO(CO)和NaHCO 的缓冲溶液,可除掉人体代谢产生的酸、碱,保持pH
2 3 2 3
基本不变
三、原理综合题
22.(2021·天津高三一模)国务院总理李克强在2021年国务院政府工作报告中指出,扎实
做好碳达峰、碳中和各项工作,优化产业结构和能源结构,努力争取2060年前实现碳中和。
碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)已知下列热化学方程式:
i.CH=CHCH(g)+Cl(g)→CHClCHClCH(g) ΔH=-133kJ·mol-1
2 3 2 2 3
ii.CH=CHCH(g)+Cl(g)→CH=CHCHCl(g)+HCl(g) ΔH=-100kJ·mol-1
2 3 2 2 2
①写出相同条件下CH=CHCHC1和HCl合成CHClCHClCH 的热化学方程式____。
2 2 2 3
②已知①中的正反应的活化能E 为132kJ·mol-1,请在下图中标出①中逆反应的活化能E
正 逆
及数值_______。
(2)温度为T℃时向容积为2L的密闭容器中投入3molH 和1molCO 发生反应CO(g)+3H(g)
2 2 2 2
CHOH(g)+HO(g) ΔH=-49.4kJ·mol-1,反应达到平衡时,测得放出热量19.76kJ,求平衡
3 2 1
时:
①H 的转化率为_______
2
②T℃时该反应的平衡常数K=_______(列计算式表示)。
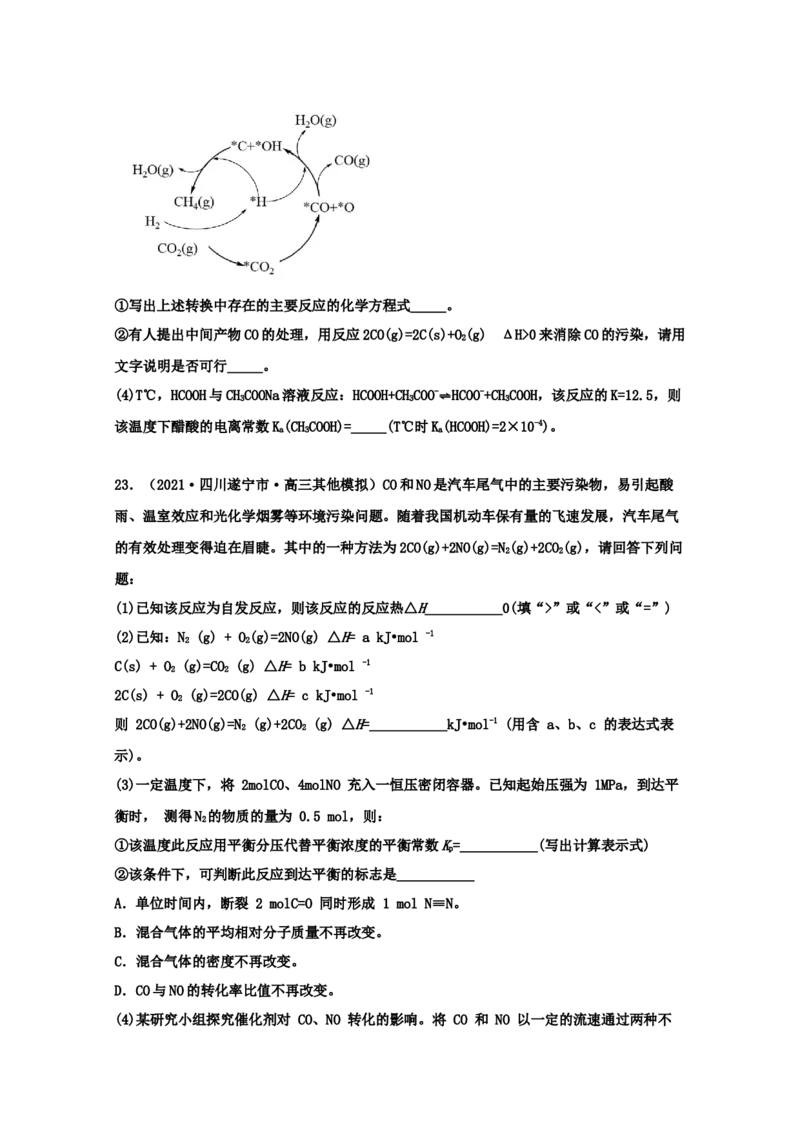
(3)目前有Ni-CeO 催化CO 加H 形成CH 的反应,历程如图所示,吸附在催化剂表面的物种用
2 2 2 4
*标注。①写出上述转换中存在的主要反应的化学方程式_____。
②有人提出中间产物CO的处理,用反应2CO(g)=2C(s)+O(g) ΔH>0来消除CO的污染,请用
2
文字说明是否可行_____。
(4)T℃,HCOOH与CHCOONa溶液反应:HCOOH+CHCOO- HCOO-+CHCOOH,该反应的K=12.5,则
3 3 3
该温度下醋酸的电离常数K(CHCOOH)=_____(T℃时K(HCOOH)=2×10-4)。
a 3 a
23.(2021·四川遂宁市·高三其他模拟)CO和NO是汽车尾气中的主要污染物,易引起酸
雨、温室效应和光化学烟雾等环境污染问题。随着我国机动车保有量的飞速发展,汽车尾气
的有效处理变得迫在眉睫。其中的一种方法为2CO(g)+2NO(g)=N(g)+2CO(g),请回答下列问
2 2
题:
(1)已知该反应为自发反应,则该反应的反应热△H___________0(填“>”或“<”或“=”)
(2)已知:N (g) + O(g)=2NO(g) △H= a kJ•mol -1
2 2
C(s) + O (g)=CO (g) △H= b kJ•mol -1
2 2
2C(s) + O (g)=2CO(g) △H= c kJ•mol -1
2
则 2CO(g)+2NO(g)=N (g)+2CO (g) △H=___________kJ•mol-1 (用含 a、b、c 的表达式表
2 2
示)。
(3)一定温度下,将 2molCO、4molNO 充入一恒压密闭容器。已知起始压强为 1MPa,到达平
衡时, 测得N 的物质的量为 0.5 mol,则:
2
①该温度此反应用平衡分压代替平衡浓度的平衡常数K=___________(写出计算表示式)
p
②该条件下,可判断此反应到达平衡的标志是___________
A.单位时间内,断裂 2 molC=O 同时形成 1 mol N≡N。
B.混合气体的平均相对分子质量不再改变。
C.混合气体的密度不再改变。
D.CO与NO的转化率比值不再改变。
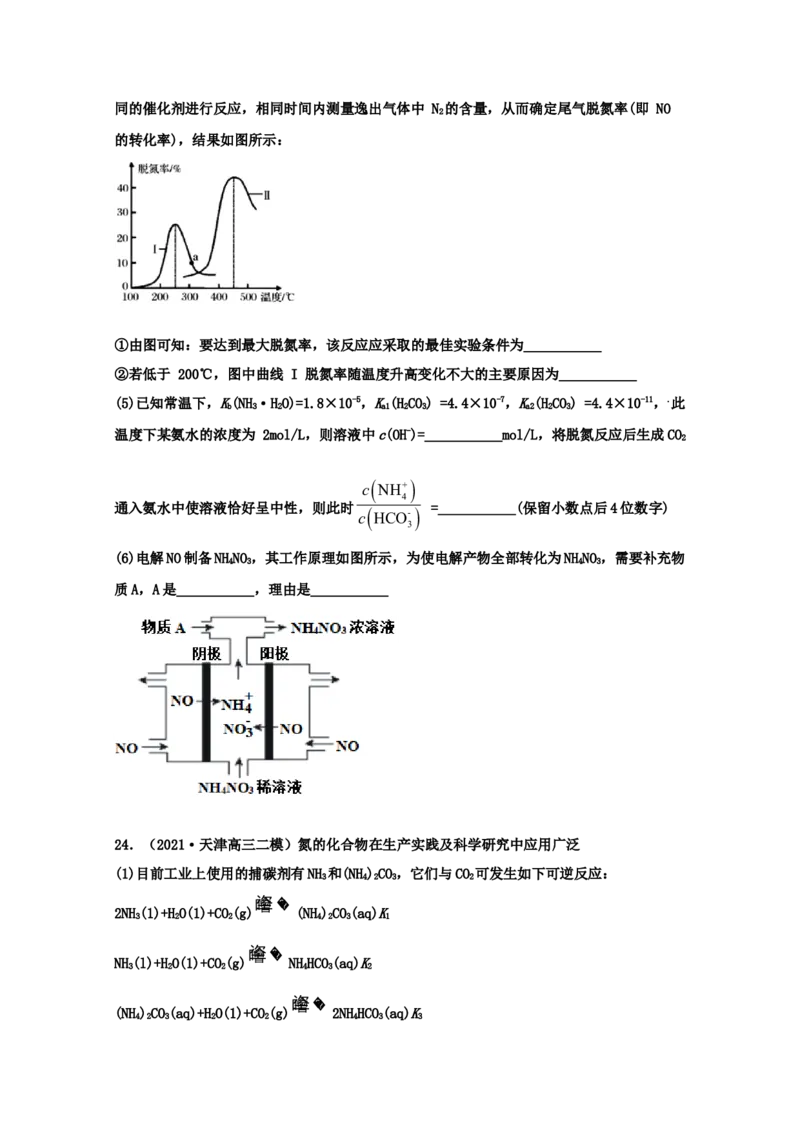
(4)某研究小组探究催化剂对 CO、NO 转化的影响。将 CO 和 NO 以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中 N 的含量,从而确定尾气脱氮率(即 NO
2
的转化率),结果如图所示:
①由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为___________
②若低于 200℃,图中曲线 I 脱氮率随温度升高变化不大的主要原因为___________
(5)已知常温下,K(NH·HO)=1.8×10-5,K(HCO) =4.4×10-7,K(HCO) =4.4×10-11,.此
b 3 2 a1 2 3 a2 2 3
温度下某氨水的浓度为 2mol/L,则溶液中c(OH-)=___________mol/L,将脱氮反应后生成CO
2
c
NH+
4
通入氨水中使溶液恰好呈中性,则此时 =___________(保留小数点后4位数字)
c
HCO-
3
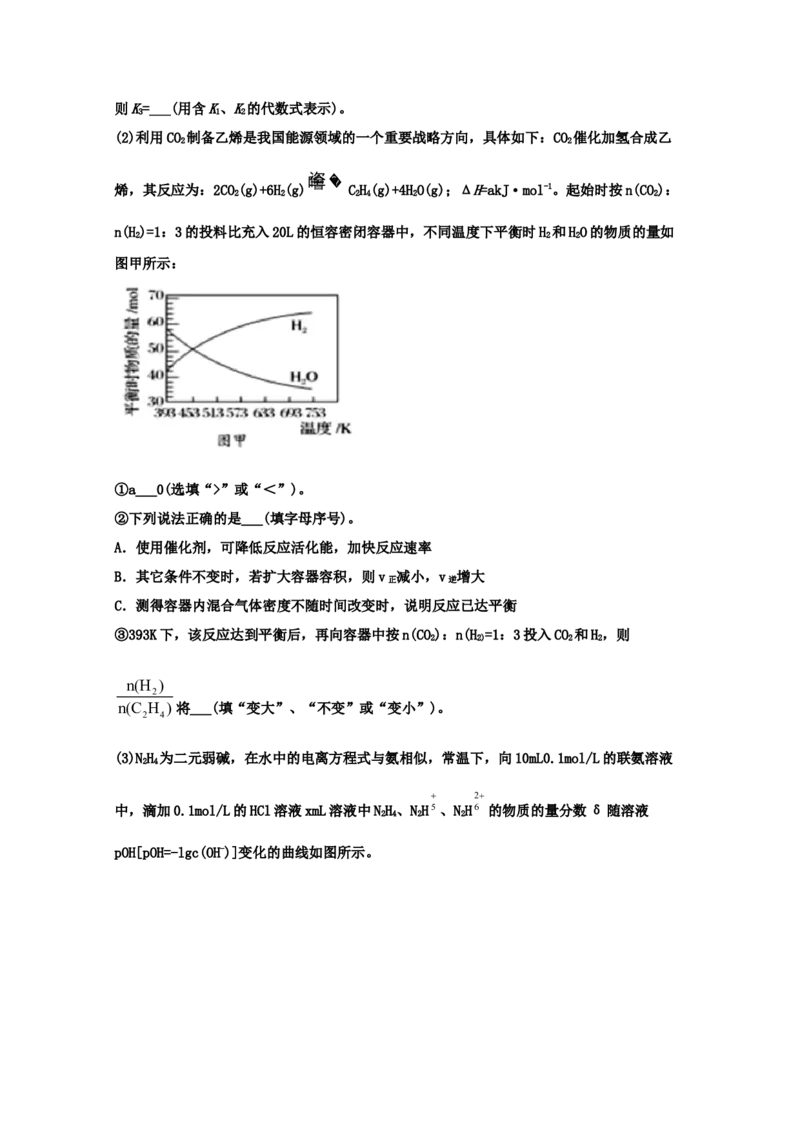
(6)电解NO制备NHNO,其工作原理如图所示,为使电解产物全部转化为NHNO,需要补充物
4 3 4 3
质A,A是___________,理由是___________
24.(2021·天津高三二模)氮的化合物在生产实践及科学研究中应用广泛
(1)目前工业上使用的捕碳剂有NH 和(NH)CO,它们与CO 可发生如下可逆反应:
3 4 2 3 2
噲垐 ��
2NH(1)+HO(1)+CO(g) (NH)CO(aq)K
3 2 2 4 2 3 1
噲垐 ��
NH(l)+HO(1)+CO(g) NHHCO(aq)K
3 2 2 4 3 2
噲垐 ��
(NH)CO(aq)+HO(1)+CO(g) 2NHHCO(aq)K
4 2 3 2 2 4 3 3则K=___(用含K、K的代数式表示)。
3 1 2
(2)利用CO 制备乙烯是我国能源领域的一个重要战略方向,具体如下:CO 催化加氢合成乙
2 2
噲垐 ��
烯,其反应为:2CO(g)+6H(g) CH(g)+4HO(g);ΔH=akJ·mol-1。起始时按n(CO):
2 2 2 4 2 2
n(H)=1:3的投料比充入20L的恒容密闭容器中,不同温度下平衡时H 和HO的物质的量如
2 2 2
图甲所示:
①a___0(选填“>”或“<”)。
②下列说法正确的是___(填字母序号)。
A.使用催化剂,可降低反应活化能,加快反应速率
B.其它条件不变时,若扩大容器容积,则v 减小,v 增大
正 逆
C.测得容器内混合气体密度不随时间改变时,说明反应已达平衡
③393K下,该反应达到平衡后,再向容器中按n(CO):n(H =1:3投入CO 和H,则
2 2) 2 2
n(H )
2
n(C H )将___(填“变大”、“不变”或“变小”)。
2 4
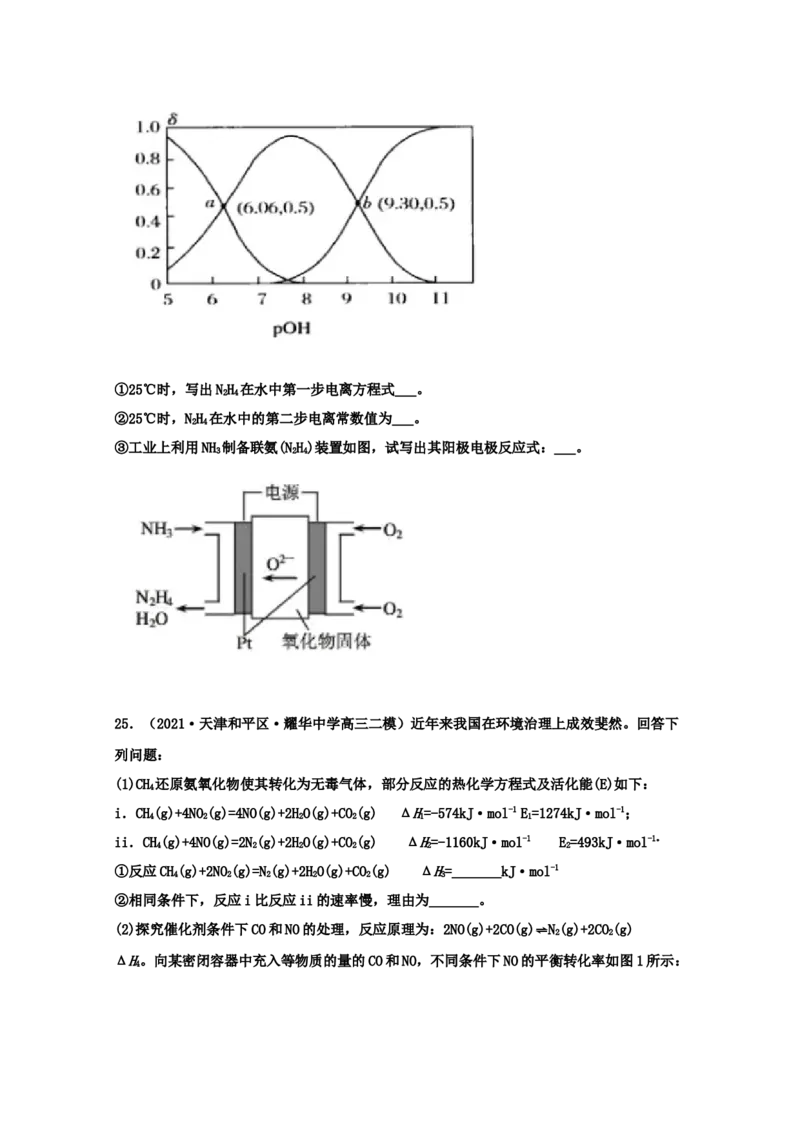
(3)NH 为二元弱碱,在水中的电离方程式与氨相似,常温下,向10mL0.1mol/L的联氨溶液
2 4
2
中,滴加0.1mol/L的HCl溶液xmL溶液中NH、NH5 、NH6 的物质的量分数δ随溶液
2 4 2 2
pOH[pOH=-lgc(OH-)]变化的曲线如图所示。①25℃时,写出NH 在水中第一步电离方程式___。
2 4
②25℃时,NH 在水中的第二步电离常数值为___。
2 4
③工业上利用NH 制备联氨(NH)装置如图,试写出其阳极电极反应式:___。
3 2 4
25.(2021·天津和平区·耀华中学高三二模)近年来我国在环境治理上成效斐然。回答下
列问题:
(1)CH 还原氨氧化物使其转化为无毒气体,部分反应的热化学方程式及活化能(E)如下:
4
i.CH(g)+4NO(g)=4NO(g)+2HO(g)+CO(g) ΔH=-574kJ·mol-1 E=1274kJ·mol-1;
4 2 2 2 1 1
ii.CH(g)+4NO(g)=2N(g)+2HO(g)+CO(g) ΔH=-1160kJ·mol-1 E=493kJ·mol-1。
4 2 2 2 2 2
①反应CH(g)+2NO(g)=N(g)+2HO(g)+CO(g) ΔH=_______kJ·mol-1
4 2 2 2 2 3
②相同条件下,反应i比反应ii的速率慢,理由为_______。
(2)探究催化剂条件下CO和NO的处理,反应原理为:2NO(g)+2CO(g) N(g)+2CO(g)
2 2
ΔH。向某密闭容器中充入等物质的量的CO和NO,不同条件下NO的平衡转化率如图1所示:
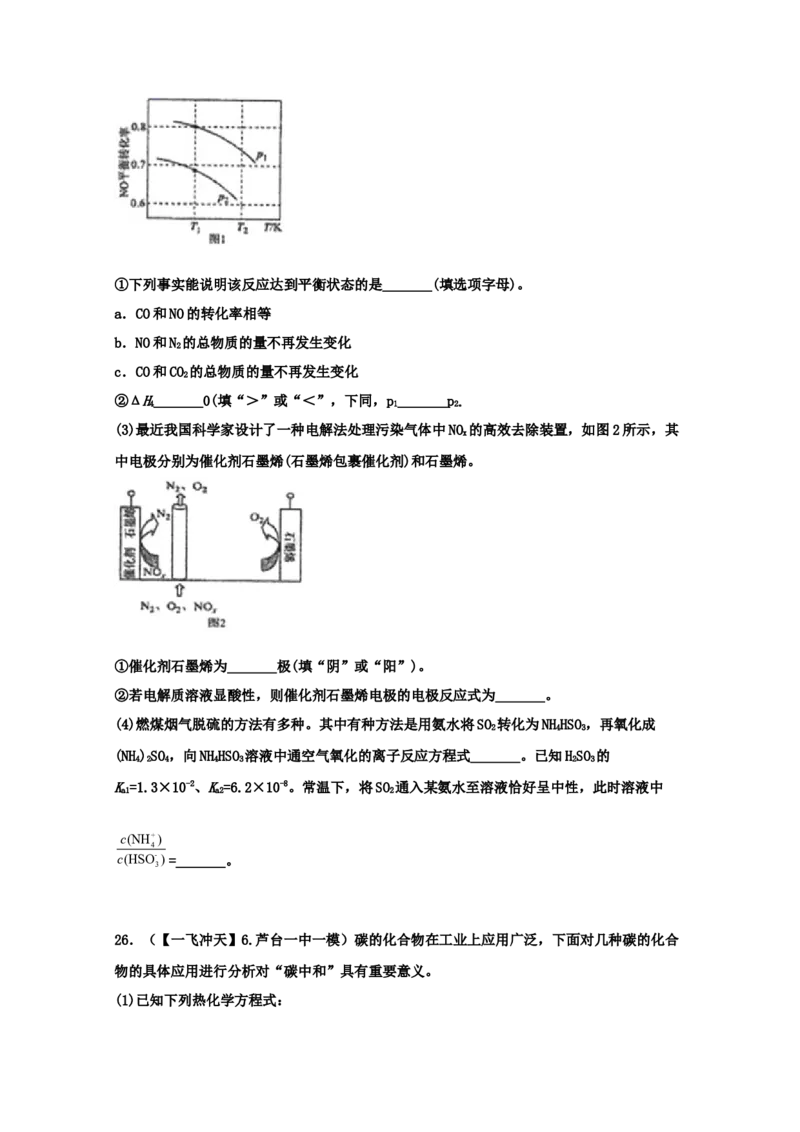
4①下列事实能说明该反应达到平衡状态的是_______(填选项字母)。
a.CO和NO的转化率相等
b.NO和N 的总物质的量不再发生变化
2
c.CO和CO 的总物质的量不再发生变化
2
②ΔH_______0(填“>”或“<”,下同,p_______p
4 1 2。
(3)最近我国科学家设计了一种电解法处理污染气体中NO 的高效去除装置,如图2所示,其
x
中电极分别为催化剂石墨烯(石墨烯包裹催化剂)和石墨烯。
①催化剂石墨烯为_______极(填“阴”或“阳”)。
②若电解质溶液显酸性,则催化剂石墨烯电极的电极反应式为_______。
(4)燃煤烟气脱硫的方法有多种。其中有种方法是用氨水将SO 转化为NHHSO,再氧化成
2 4 3
(NH)SO,向NHHSO 溶液中通空气氧化的离子反应方程式_______。已知HSO 的
4 2 4 4 3 2 3
K=1.3×10-2、K=6.2×10-8。常温下,将SO 通入某氨水至溶液恰好呈中性,此时溶液中
a1 a2 2
c(NH+)
4
c(HSO-) =_______。
3
26.(【一飞冲天】6.芦台一中一模)碳的化合物在工业上应用广泛,下面对几种碳的化合
物的具体应用进行分析对“碳中和”具有重要意义。
(1)已知下列热化学方程式:i.CH=CHCH(g)+Cl(g)→CHClCHClCH(g) ΔH=-133kJ·mol-1
2 3 2 2 3 1
ii.CH=CHCH(g)+Cl(g)→CH=CHCHCl(g)+HCl(g) ΔH=-100kJ·mol-1
2 3 2 2 2 2
噲垐 ��
又已知在相同条件下,CH=CHCHCl(g)+HCl(g) CHClCHClCH(g)的正反应的活化能E
2 2 2 3 a(正)
为132kJ·mol-1,则逆反应的活化能E 为___kJ·mol-1。
a(逆)
(2)查阅资料得知,反应CHCHO(aq)=CH(g)+CO(g)在含有少量I 的溶液中分两步进行:
3 4 2
第①步反应为CHCHO(aq)+I(aq)=CHI(l)+HI(aq)+CO(g)(慢反应);
3 2 3
第②步为快反应;增大I 的浓度能明显增大总反应的平均速率。理由为___。
2
噲垐 ��
(3)工业上可利用煤的气化产物(水煤气)合成甲醇:CO(g)+2H(g) CHOH(g)ΔH<0,在
2 3
一定条件下,将1molCO和2molH 通入密闭容器中进行反应,当改变某一外界条件(温度或压
2
强)时,CHOH的体积分数φ(CHOH)变化趋势如图所示:
3 3
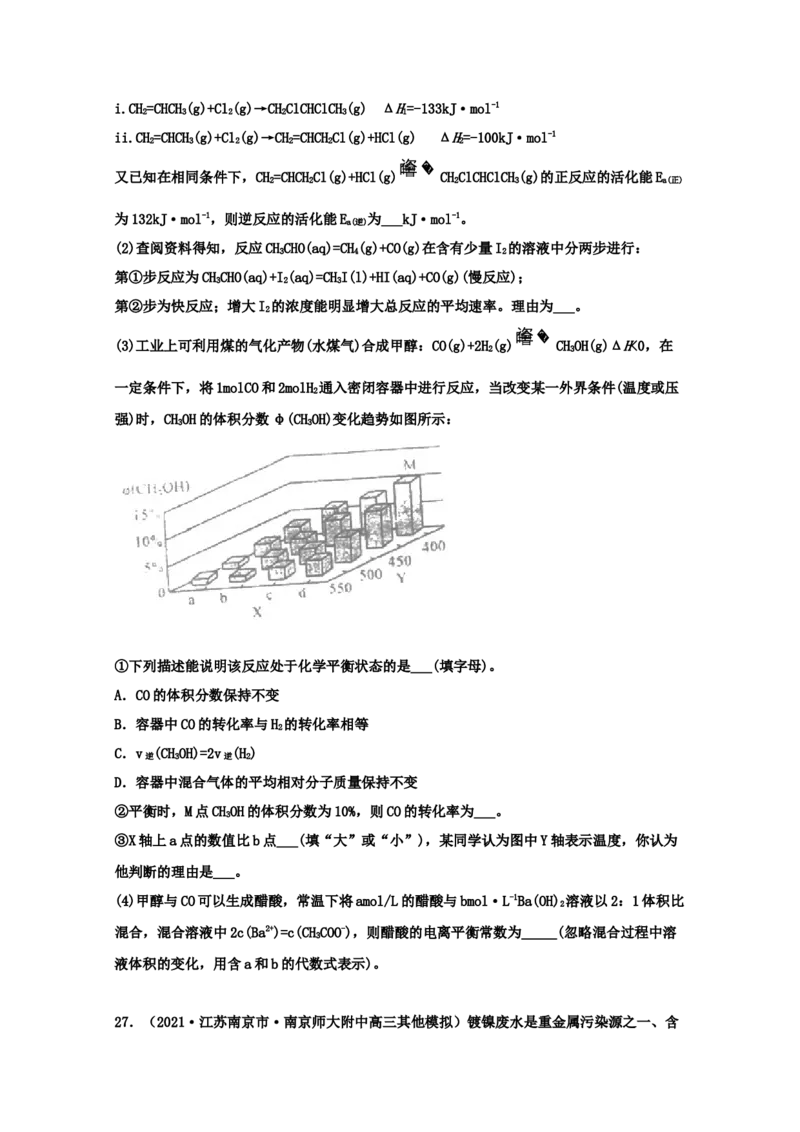
①下列描述能说明该反应处于化学平衡状态的是___(填字母)。
A.CO的体积分数保持不变
B.容器中CO的转化率与H 的转化率相等
2
C.v (CHOH)=2v (H)
逆 3 逆 2
D.容器中混合气体的平均相对分子质量保持不变
②平衡时,M点CHOH的体积分数为10%,则CO的转化率为___。
3
③X轴上a点的数值比b点___(填“大”或“小”),某同学认为图中Y轴表示温度,你认为
他判断的理由是___。
(4)甲醇与CO可以生成醋酸,常温下将amol/L的醋酸与bmol·L-1Ba(OH) 溶液以2:1体积比
2
混合,混合溶液中2c(Ba2+)=c(CHCOO-),则醋酸的电离平衡常数为_____(忽略混合过程中溶
3
液体积的变化,用含a和b的代数式表示)。
27.(2021·江苏南京市·南京师大附中高三其他模拟)镀镍废水是重金属污染源之一、含镍废水的处理方法常见的有络合法、离子交换法、沉淀法、电解法等。
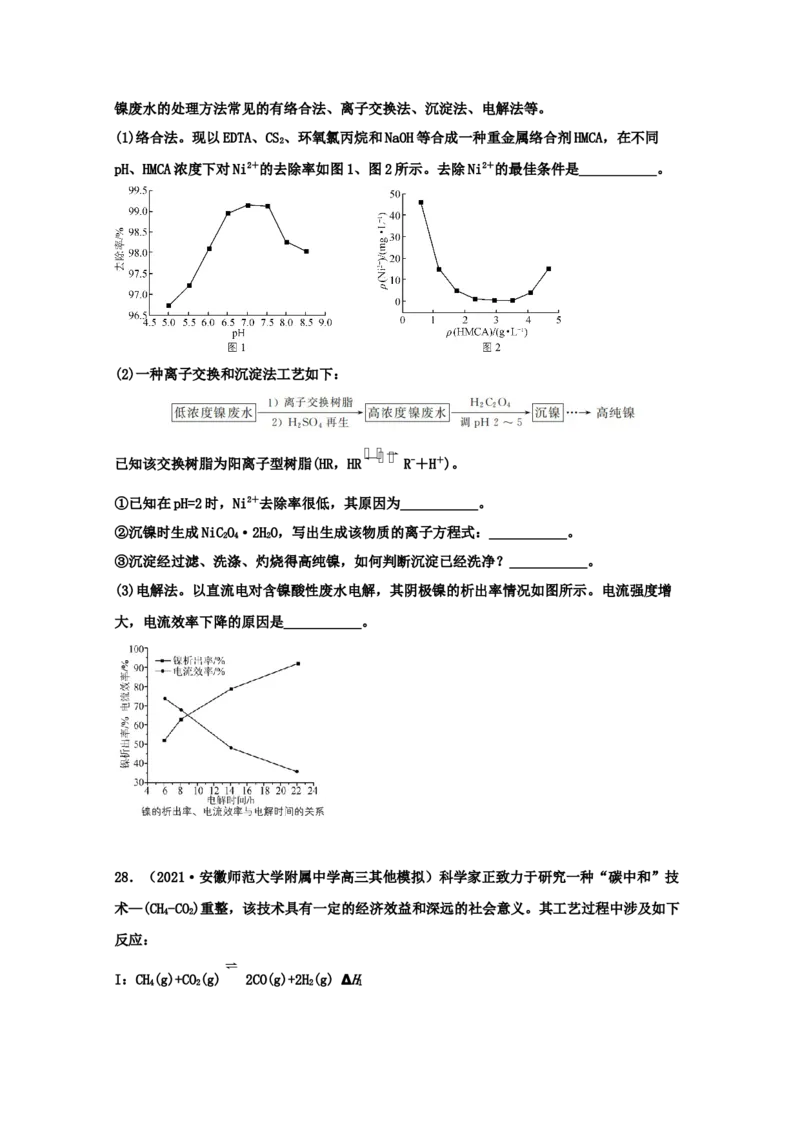
(1)络合法。现以EDTA、CS、环氧氯丙烷和NaOH等合成一种重金属络合剂HMCA,在不同
2
pH、HMCA浓度下对Ni2+的去除率如图1、图2所示。去除Ni2+的最佳条件是___________。
(2)一种离子交换和沉淀法工艺如下:
已知该交换树脂为阳离子型树脂(HR,HR
R-+H+)。
①已知在pH=2时,Ni2+去除率很低,其原因为___________。
②沉镍时生成NiCO·2HO,写出生成该物质的离子方程式:___________。
2 4 2
③沉淀经过滤、洗涤、灼烧得高纯镍,如何判断沉淀已经洗净?___________。
(3)电解法。以直流电对含镍酸性废水电解,其阴极镍的析出率情况如图所示。电流强度增
大,电流效率下降的原因是___________。
28.(2021·安徽师范大学附属中学高三其他模拟)科学家正致力于研究一种“碳中和”技
术—(CH-CO)重整,该技术具有一定的经济效益和深远的社会意义。其工艺过程中涉及如下
4 2
反应:
I:CH(g)+CO(g) 2CO(g)+2H(g) ∆H
4 2 2 1
II:H(g)+CO(g) HO(g)+CO(g) ∆H=+41kJ·mol−1
2 2 2 2
(1)已知部分化学键的键能数据如下表所示:
化学键 C—H H—H C=O C≡O(CO)
键能(kJ·mol−1) 413 436 803 1076
则∆H=____kJ·mol−1,反应I在一定条件下能够自发进行的原因是____,在密闭容器中加入
l
CO 与CH 发生反应,下列能够判断反应I达到平衡状态的是____(填标号)。
2 4
A.一定温度下,容积固定的容器中,密度保持不变
B.容积固定的绝热容器中,温度保持不变
C.一定温度和容积固定的容器中,平均相对分子质量保持不变
D.一定温度和容积固定的容器中,H 和HO物质的量之和保持不变
2 2
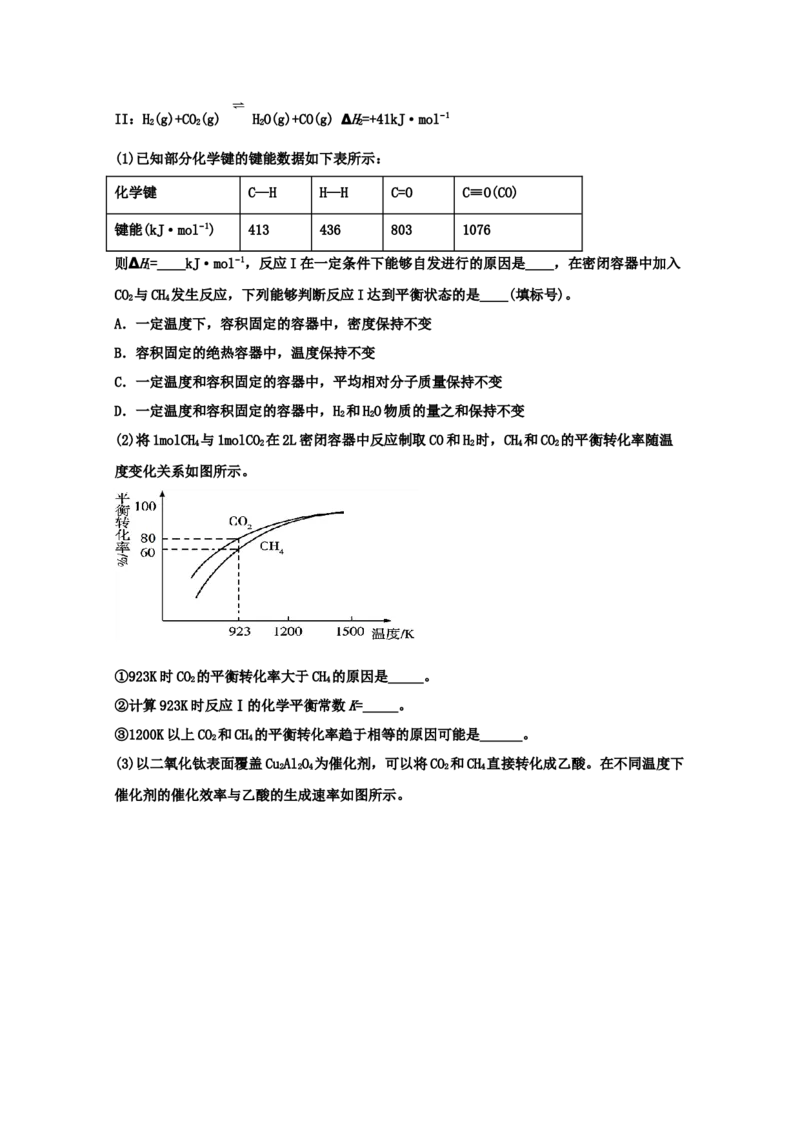
(2)将1molCH 与1molCO 在2L密闭容器中反应制取CO和H 时,CH 和CO 的平衡转化率随温
4 2 2 4 2
度变化关系如图所示。
①923K时CO 的平衡转化率大于CH 的原因是_____。
2 4
②计算923K时反应Ⅰ的化学平衡常数K=_____。
③1200K以上CO 和CH 的平衡转化率趋于相等的原因可能是______。
2 4
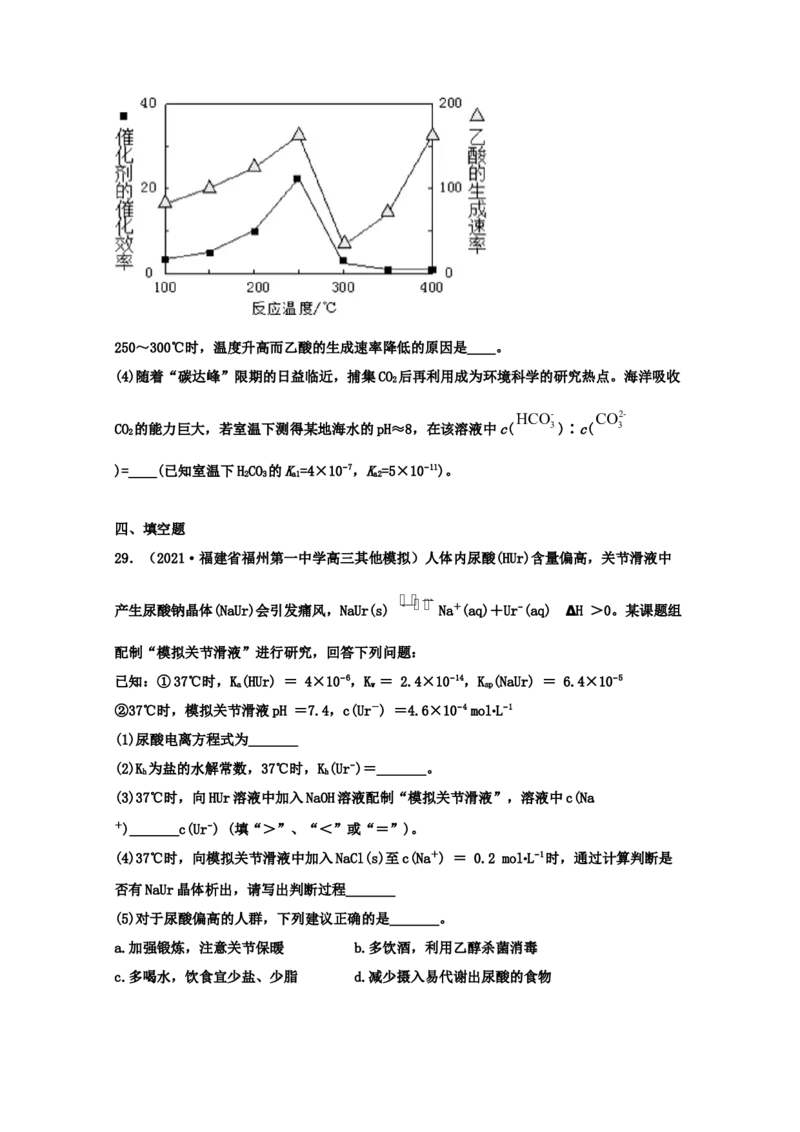
(3)以二氧化钛表面覆盖CuAlO 为催化剂,可以将CO 和CH 直接转化成乙酸。在不同温度下
2 2 4 2 4
催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是____。
(4)随着“碳达峰”限期的日益临近,捕集CO 后再利用成为环境科学的研究热点。海洋吸收
2
HCO- CO2-
CO 的能力巨大,若室温下测得某地海水的pH≈8,在该溶液中c( 3)∶c( 3
2
)=____(已知室温下HCO 的K=4×10−7,K=5×10−11)。
2 3 a1 a2
四、填空题
29.(2021·福建省福州第一中学高三其他模拟)人体内尿酸(HUr)含量偏高,关节滑液中
产生尿酸钠晶体(NaUr)会引发痛风,NaUr(s)
Na+(aq)+Ur−(aq) ∆H >0。某课题组
配制“模拟关节滑液”进行研究,回答下列问题:
已知:①37℃时,K(HUr) = 4×10−6,K = 2.4×10−14,K (NaUr) = 6.4×10−5
a w sp
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为_______
(2)K 为盐的水解常数,37℃时,K(Ur−)=_______。
h h
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na
+)_______c(Ur−) (填“>”、“<”或“=”)。
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是
否有NaUr晶体析出,请写出判断过程_______
(5)对于尿酸偏高的人群,下列建议正确的是_______。
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物五、工业流程题
30.(2021·四川遂宁市·高三其他模拟)工业利用硼矿石(2MgO·BO)制备单质B(硼)并联
2 3
产轻质MgO的流程如下,硼是第IIIA族中唯一的非金属元素,可以形成众多的化合物。回答
下列问题:
(1)硼烷泛指一切硼和氢组成的化合物。乙硼烷(BH)是最简单的硼烷。可以在乙醚介质中使
2 6
用LiAlH(离子化合物)还原BCl 获得,LiAlH 中H的化合价为___________,它的电子式为
4 3 4
___________,制备乙硼烷的化学方程式为___________。
硼酸(HBO)的溶解度
3 3
温度/℃ 0 10 20 30 40 80
溶解度/g 2.77 3.65 4.87 6.77 8.90 23.54
(2)回答下列问题:
①为了加快硼矿石与NaCO 溶液和CO 的反应速率,可以采取的措施有___________(填一种)。
2 3 2
②操作1是___________,洗涤,干燥。检验HBO 是否洗涤干净的操作方法为___________。
3 3
整个流程中可循环利用的物质是___________
③制备B发生反应的化学方程式是___________,过程中易生成金属硼化物杂质。该杂质的化
学式是___________
(3)硼酸(HBO)是一元弱酸,在溶液中能电离生成[B(OH)]-,硼酸的电离方程式为
3 3 4
___________;室温时测得0.1000 mol•L-1硼酸溶液的pH=5,硼酸的电离常数
K=___________
a