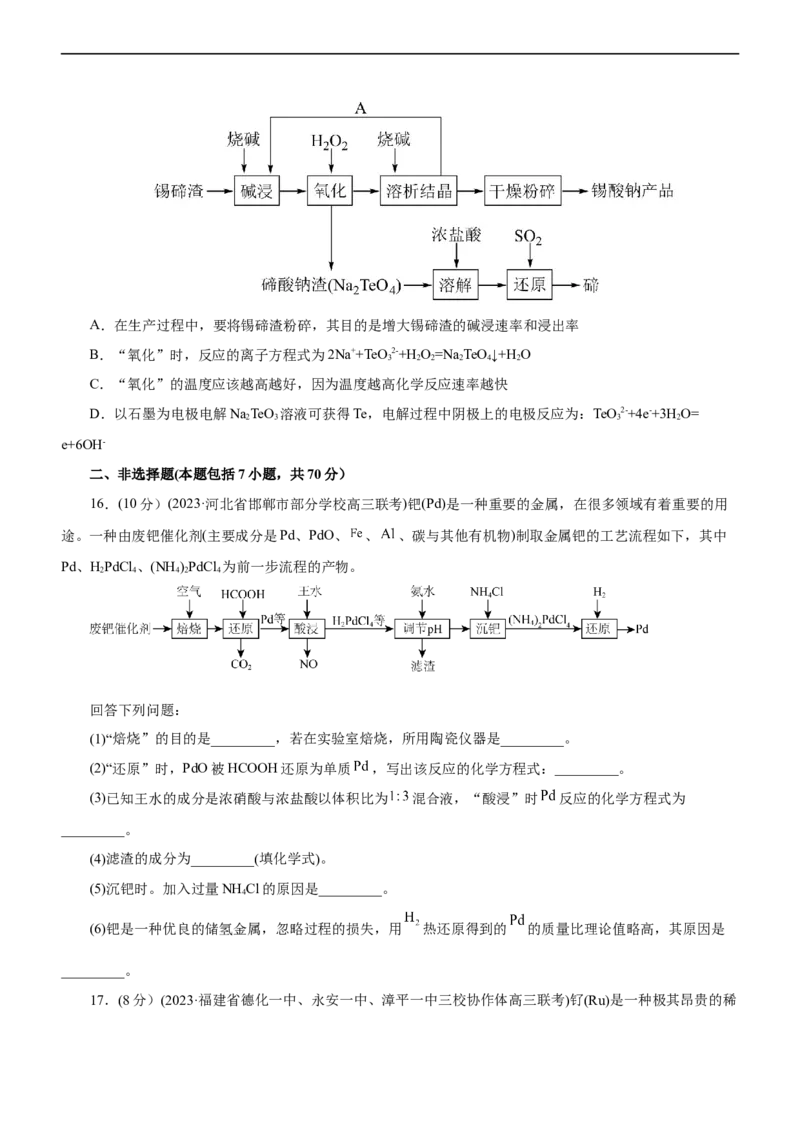
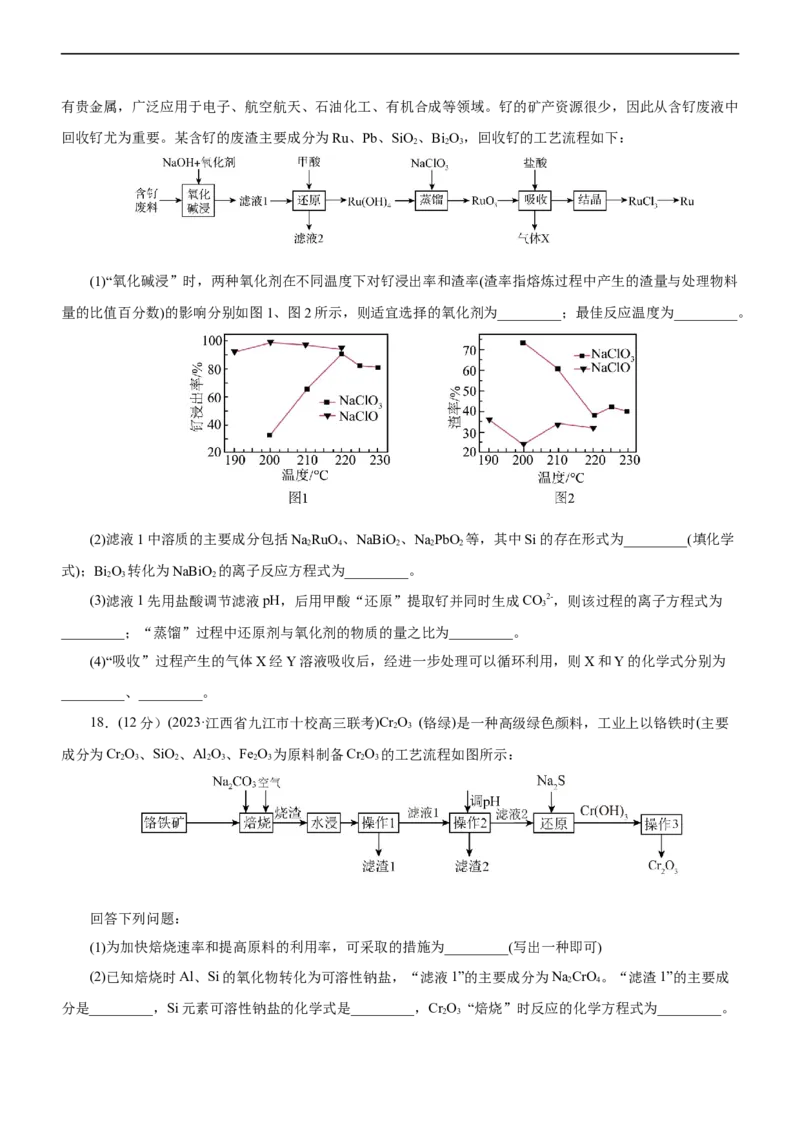
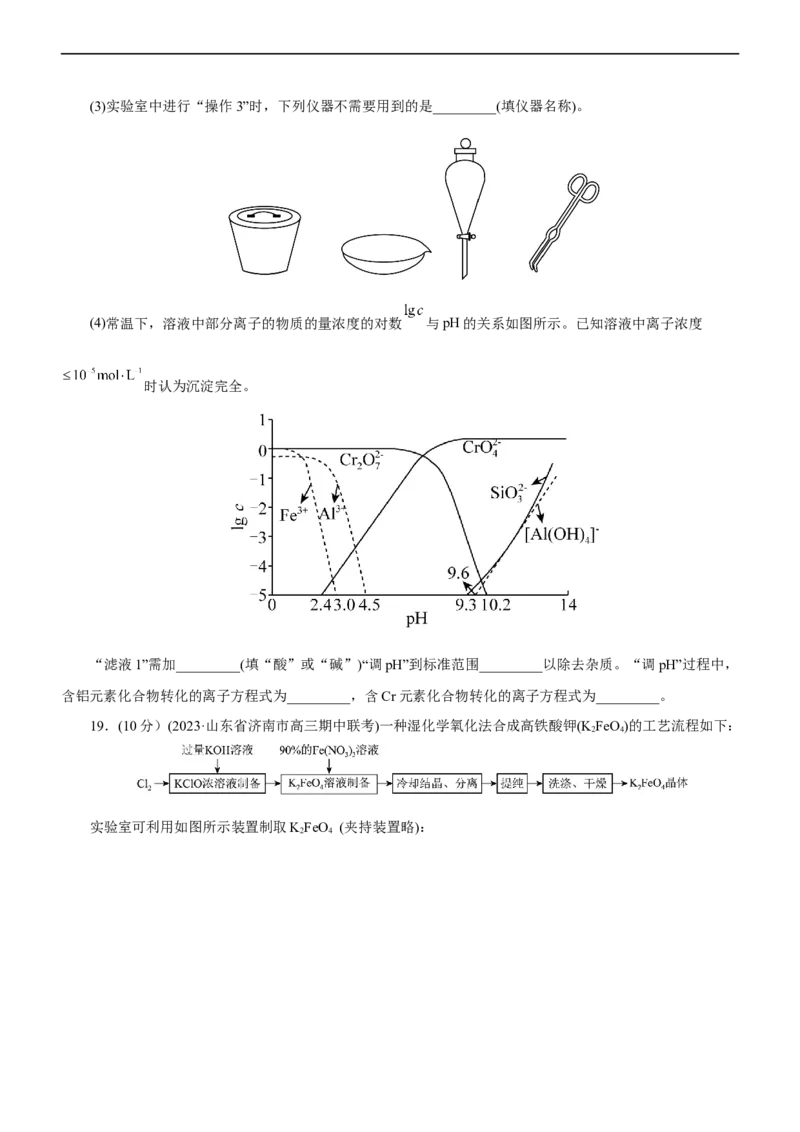
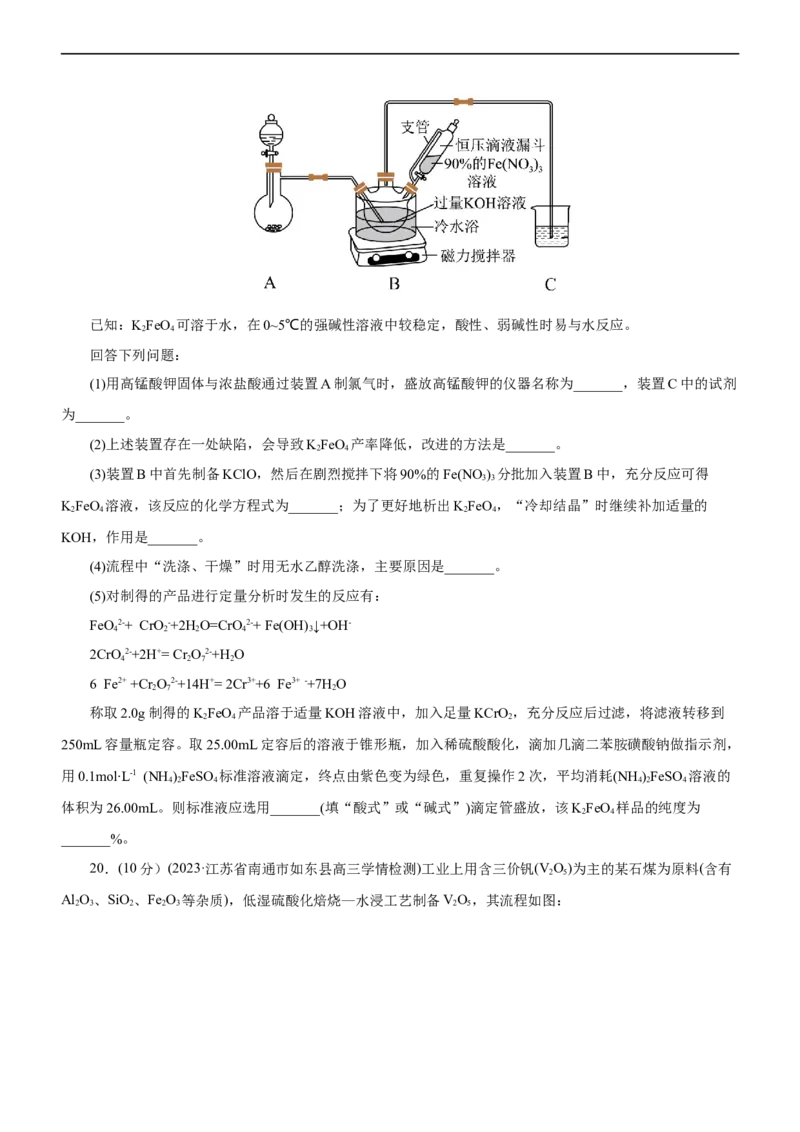
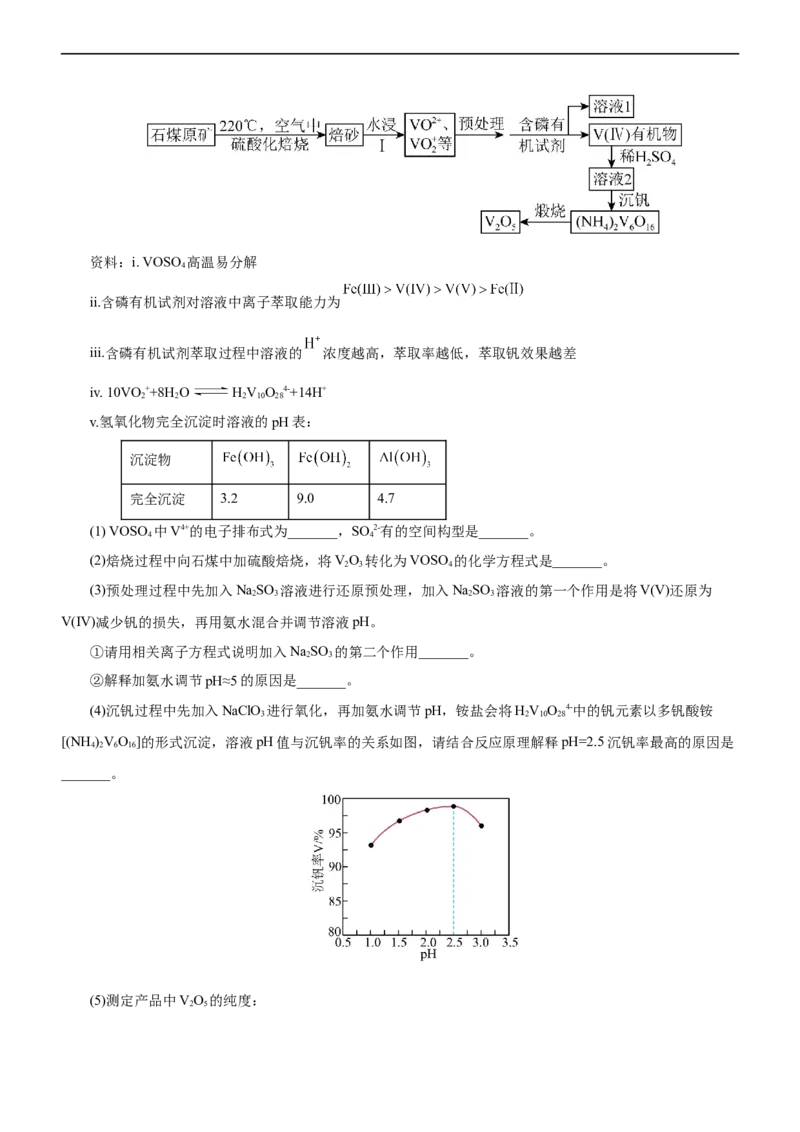
文档内容
专题 13 化学工艺流程
一、选择题(本题包括15小题,每小题2分,共30分,每小题只有一个选项符合题意)
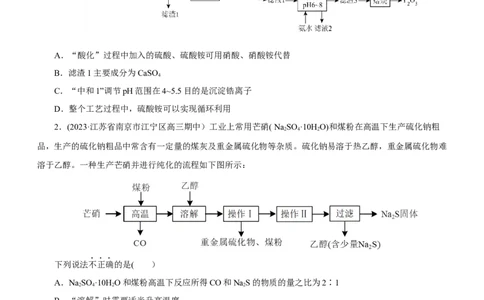
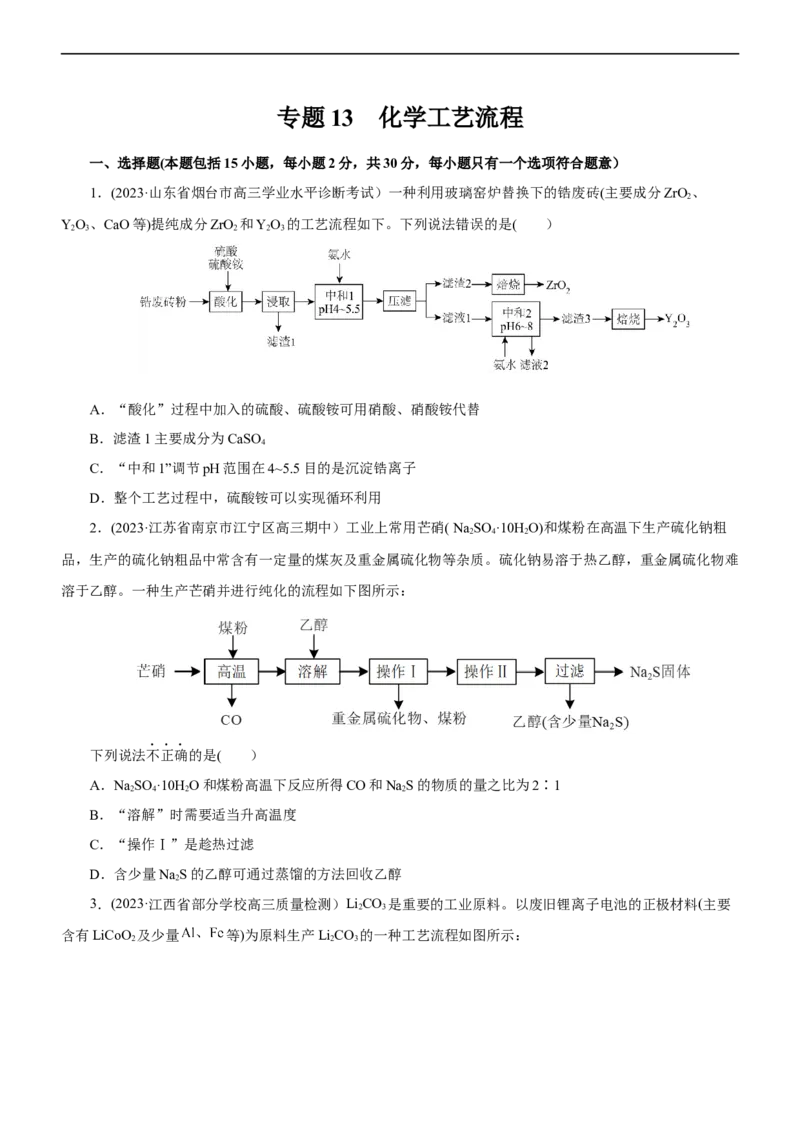
1.(2023·山东省烟台市高三学业水平诊断考试)一种利用玻璃窑炉替换下的锆废砖(主要成分ZrO、
2
YO、CaO等)提纯成分ZrO 和YO 的工艺流程如下。下列说法错误的是( )
2 3 2 2 3
A.“酸化”过程中加入的硫酸、硫酸铵可用硝酸、硝酸铵代替
B.滤渣1主要成分为CaSO
4
C.“中和1”调节pH范围在4~5.5目的是沉淀锆离子
D.整个工艺过程中,硫酸铵可以实现循环利用
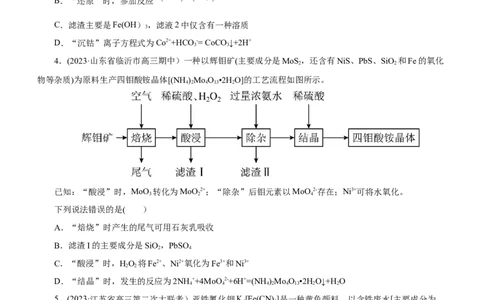
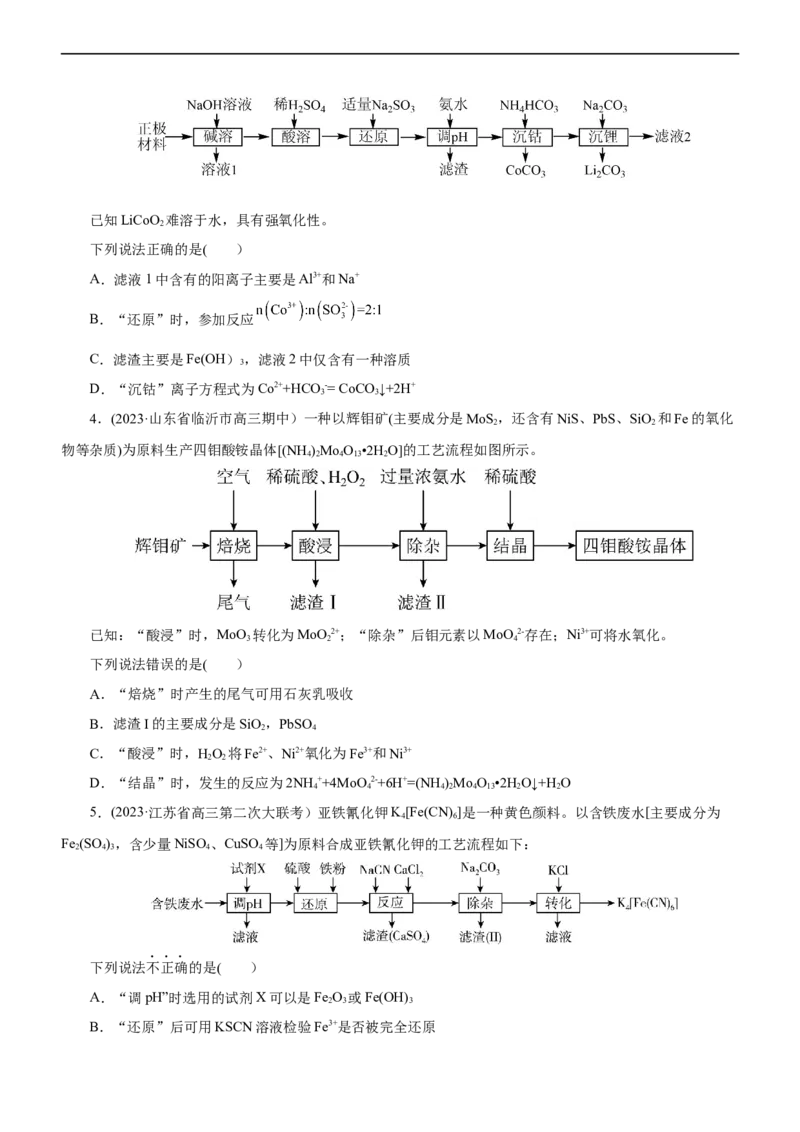
2.(2023·江苏省南京市江宁区高三期中)工业上常用芒硝( Na SO ·10H O)和煤粉在高温下生产硫化钠粗
2 4 2
品,生产的硫化钠粗品中常含有一定量的煤灰及重金属硫化物等杂质。硫化钠易溶于热乙醇,重金属硫化物难
溶于乙醇。一种生产芒硝并进行纯化的流程如下图所示:
下列说法不正确的是( )
A.NaSO ·10H O和煤粉高温下反应所得CO和NaS的物质的量之比为2∶1
2 4 2 2
B.“溶解”时需要适当升高温度
C.“操作Ⅰ”是趁热过滤
D.含少量NaS的乙醇可通过蒸馏的方法回收乙醇
2
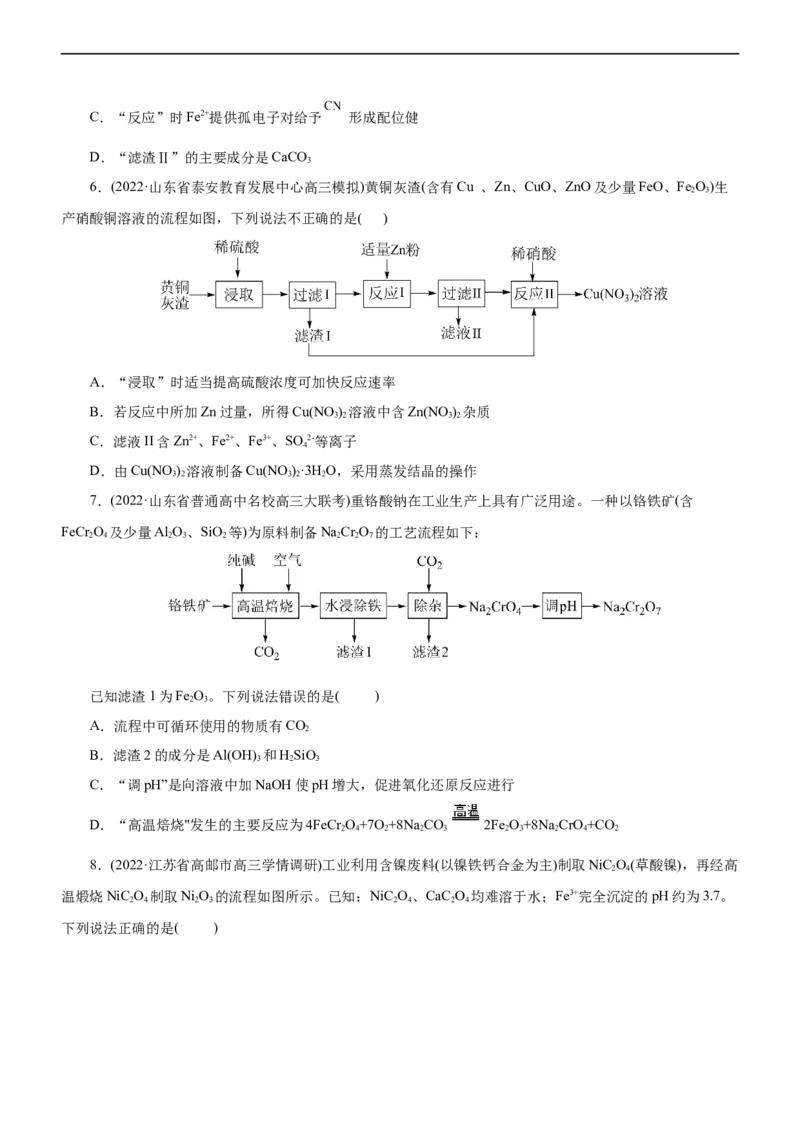
3.(2023·江西省部分学校高三质量检测)LiCO 是重要的工业原料。以废旧锂离子电池的正极材料(主要
2 3
含有LiCoO 及少量 等)为原料生产LiCO 的一种工艺流程如图所示:
2 2 3已知LiCoO 难溶于水,具有强氧化性。
2
下列说法正确的是( )
A.滤液1中含有的阳离子主要是Al3+和Na+
B.“还原”时,参加反应
C.滤渣主要是Fe(OH),滤液2中仅含有一种溶质
3
D.“沉钴”离子方程式为Co2++HCO-= CoCO↓+2H+
3 3
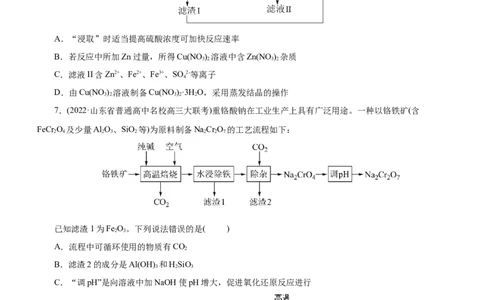
4.(2023·山东省临沂市高三期中)一种以辉钼矿(主要成分是MoS ,还含有NiS、PbS、SiO 和Fe的氧化
2 2
物等杂质)为原料生产四钼酸铵晶体[(NH )MoO •2H O]的工艺流程如图所示。
4 2 4 13 2
已知:“酸浸”时,MoO 转化为MoO 2+;“除杂”后钼元素以MoO 2-存在;Ni3+可将水氧化。
3 2 4
下列说法错误的是( )
A.“焙烧”时产生的尾气可用石灰乳吸收
B.滤渣I的主要成分是SiO,PbSO
2 4
C.“酸浸”时,HO 将Fe2+、Ni2+氧化为Fe3+和Ni3+
2 2
D.“结晶”时,发生的反应为2NH ++4MoO2-+6H+=(NH)MoO •2H O↓+HO
4 4 4 2 4 13 2 2
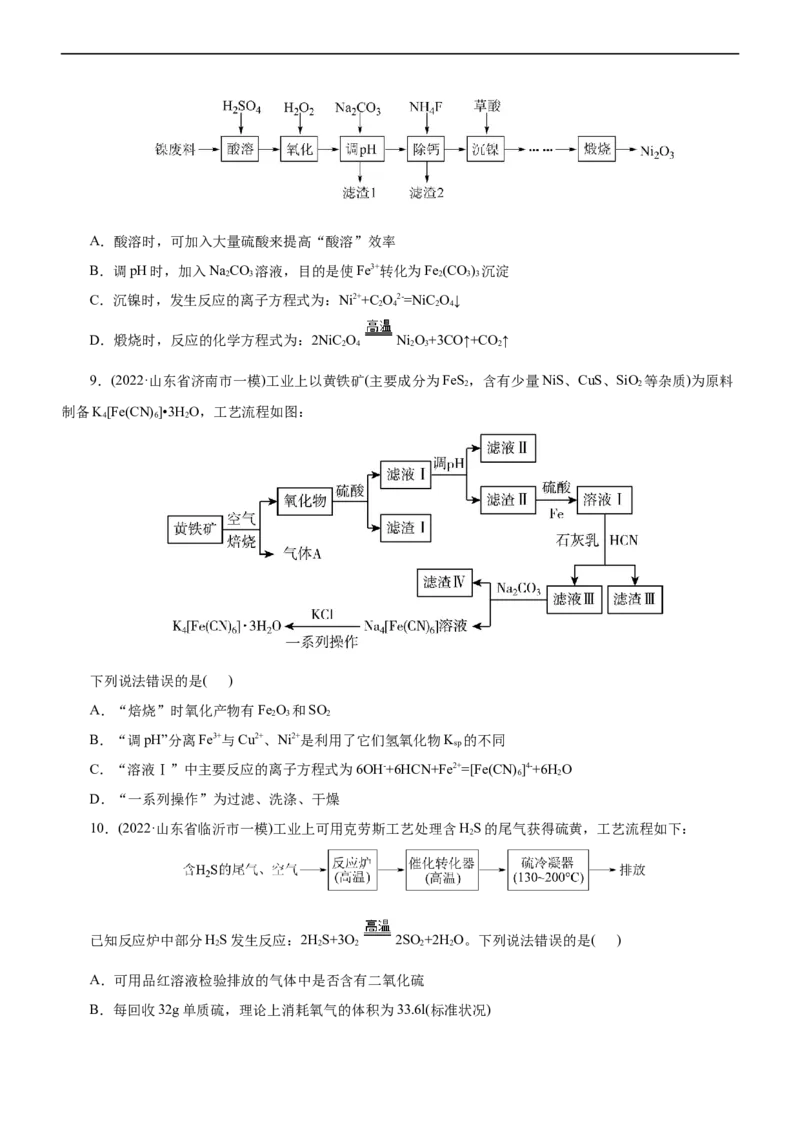
5.(2023·江苏省高三第二次大联考)亚铁氰化钾K[Fe(CN) ]是一种黄色颜料。以含铁废水[主要成分为
4 6
Fe (SO ),含少量NiSO 、CuSO 等]为原料合成亚铁氰化钾的工艺流程如下:
2 4 3 4 4
下列说法不正确的是( )
A.“调pH”时选用的试剂X可以是Fe O 或Fe(OH)
2 3 3
B.“还原”后可用KSCN溶液检验Fe3+是否被完全还原C.“反应”时Fe2+提供孤电子对给予 形成配位健
D.“滤渣Ⅱ”的主要成分是CaCO
3
6.(2022·山东省泰安教育发展中心高三模拟)黄铜灰渣(含有Cu 、Zn、CuO、ZnO及少量FeO、Fe O)生
2 3
产硝酸铜溶液的流程如图,下列说法不正确的是( )
A.“浸取”时适当提高硫酸浓度可加快反应速率
B.若反应中所加Zn过量,所得Cu(NO ) 溶液中含Zn(NO ) 杂质
3 2 3 2
C.滤液II含Zn2+、Fe2+、Fe3+、SO 2-等离子
4
D.由Cu(NO ) 溶液制备Cu(NO )·3H O,采用蒸发结晶的操作
3 2 3 2 2
7.(2022·山东省普通高中名校高三大联考)重铬酸钠在工业生产上具有广泛用途。一种以铬铁矿(含
FeCr O 及少量Al O、SiO 等)为原料制备NaCr O 的工艺流程如下:
2 4 2 3 2 2 2 7
已知滤渣1为Fe O。下列说法错误的是( )
2 3
A.流程中可循环使用的物质有CO
2
B.滤渣2的成分是Al(OH) 和HSiO
3 2 3
C.“调pH”是向溶液中加NaOH使pH增大,促进氧化还原反应进行
D.“高温焙烧"发生的主要反应为4FeCr O+7O +8Na CO 2Fe O+8Na CrO+CO
2 4 2 2 3 2 3 2 4 2
8.(2022·江苏省高邮市高三学情调研)工业利用含镍废料(以镍铁钙合金为主)制取NiC O(草酸镍),再经高
2 4
温煅烧NiC O 制取Ni O 的流程如图所示。已知:NiC O、CaC O 均难溶于水;Fe3+完全沉淀的pH约为3.7。
2 4 2 3 2 4 2 4
下列说法正确的是( )A.酸溶时,可加入大量硫酸来提高“酸溶”效率
B.调pH时,加入NaCO 溶液,目的是使Fe3+转化为Fe (CO) 沉淀
2 3 2 3 3
C.沉镍时,发生反应的离子方程式为:Ni2++C O2-=NiC O↓
2 4 2 4
D.煅烧时,反应的化学方程式为:2NiC O Ni O+3CO↑+CO ↑
2 4 2 3 2
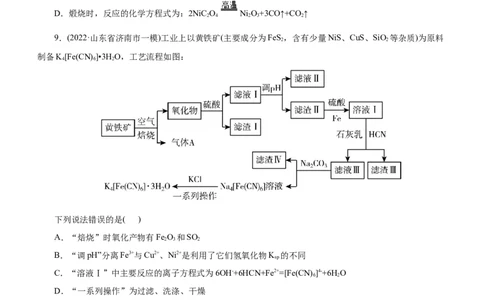
9.(2022·山东省济南市一模)工业上以黄铁矿(主要成分为FeS,含有少量NiS、CuS、SiO 等杂质)为原料
2 2
制备K[Fe(CN) ]•3H O,工艺流程如图:
4 6 2
下列说法错误的是( )
A.“焙烧”时氧化产物有Fe O 和SO
2 3 2
B.“调pH”分离Fe3+与Cu2+、Ni2+是利用了它们氢氧化物K 的不同
sp
C.“溶液Ⅰ”中主要反应的离子方程式为6OH-+6HCN+Fe2+=[Fe(CN)]4-+6H O
6 2
D.“一系列操作”为过滤、洗涤、干燥
10.(2022·山东省临沂市一模)工业上可用克劳斯工艺处理含HS的尾气获得硫黄,工艺流程如下:
2
已知反应炉中部分HS发生反应:2HS+3O 2SO +2H O。下列说法错误的是( )
2 2 2 2 2
A.可用品红溶液检验排放的气体中是否含有二氧化硫
B.每回收32g单质硫,理论上消耗氧气的体积为33.6l(标准状况)C.催化转化器中发生的反应为SO +2H S 3S+2HO
2 2 2
D.为提高HS转化为S的比例,理论上应控制反应炉中HS的转化率约为
2 2
11.(2022·福建省漳州市二模)高铁酸钾(K FeO)具有强氧化性,是一种环保、高效、多功能的饮用水处理
2 4
剂,可以用如下流程进行制备。下列说法正确的是( )
A.“酸溶”前,可用热的NaCO 溶液处理铁屑表面的油污
2 3
B.“氧化”过程的离子方程式为2Fe2++O +4H+=2Fe3++2H O
2 2
C.“制备Na FeO”中氧化剂和还原剂的物质的量之比为2:3
2 4
D.“转化”中析出KFeO 晶体的原因可能是相同条件下其溶解度大于Na FeO
2 4 2 4
12.(2022·山东省菏泽市一模)某新型纳米材料氧缺位铁酸盐ZnFe O(3