文档内容
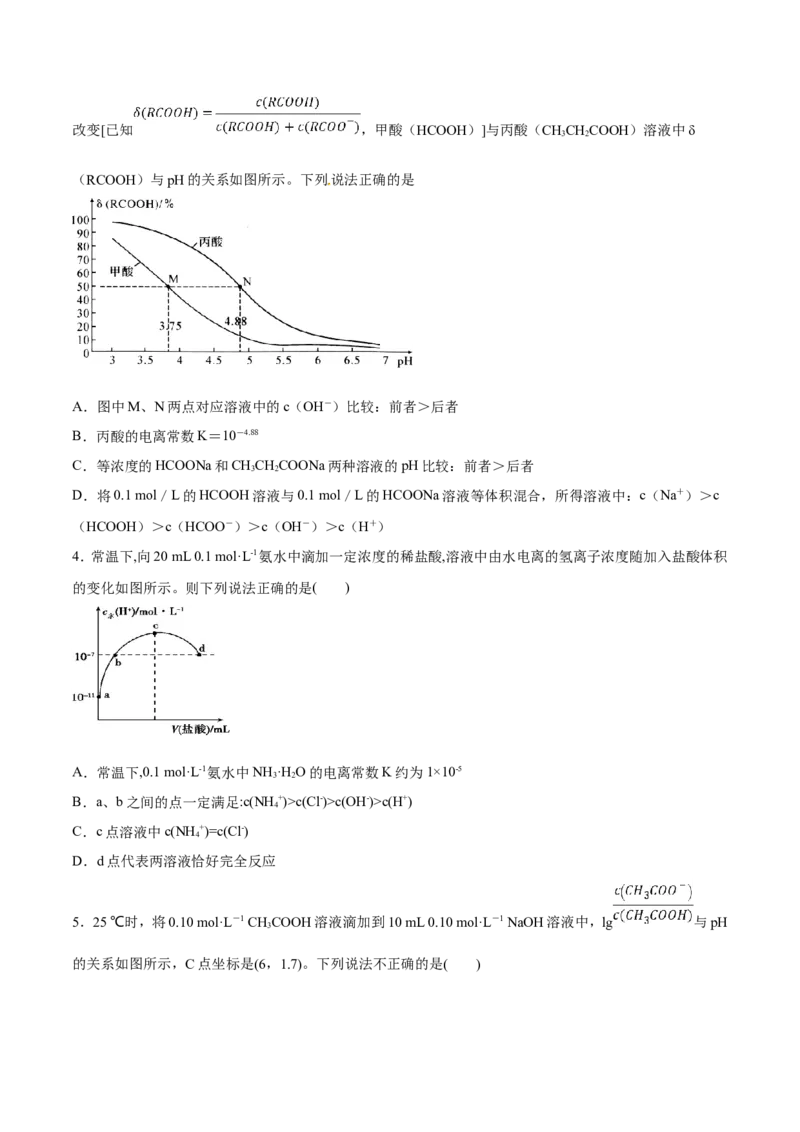
1.I 在KI溶液中存在平衡I(aq)+I(aq)=I—(aq)。某I、KI混合溶液中,I—的物质的量浓度c(I —)与温度T的
2 2 2 3 3
关系如图所示(曲线上的任何点都表示平衡状态)。下列说法正确的是
①I(aq)+I—(aq)=I —(ag) ΔH>0
2 3
②若温度为T、T 时反应的平衡常数分别为K、K,则K>K
1 2 1 2 1 2
③若反应进行到状态D时,一定有v >v
正 逆
④状态A与状态B相比,状态A的c(I )大
2
⑤保持温度不变,向该混合溶液中加水, 将变大
A.只有①② B.只有②③ C.①③④ D.①③⑤
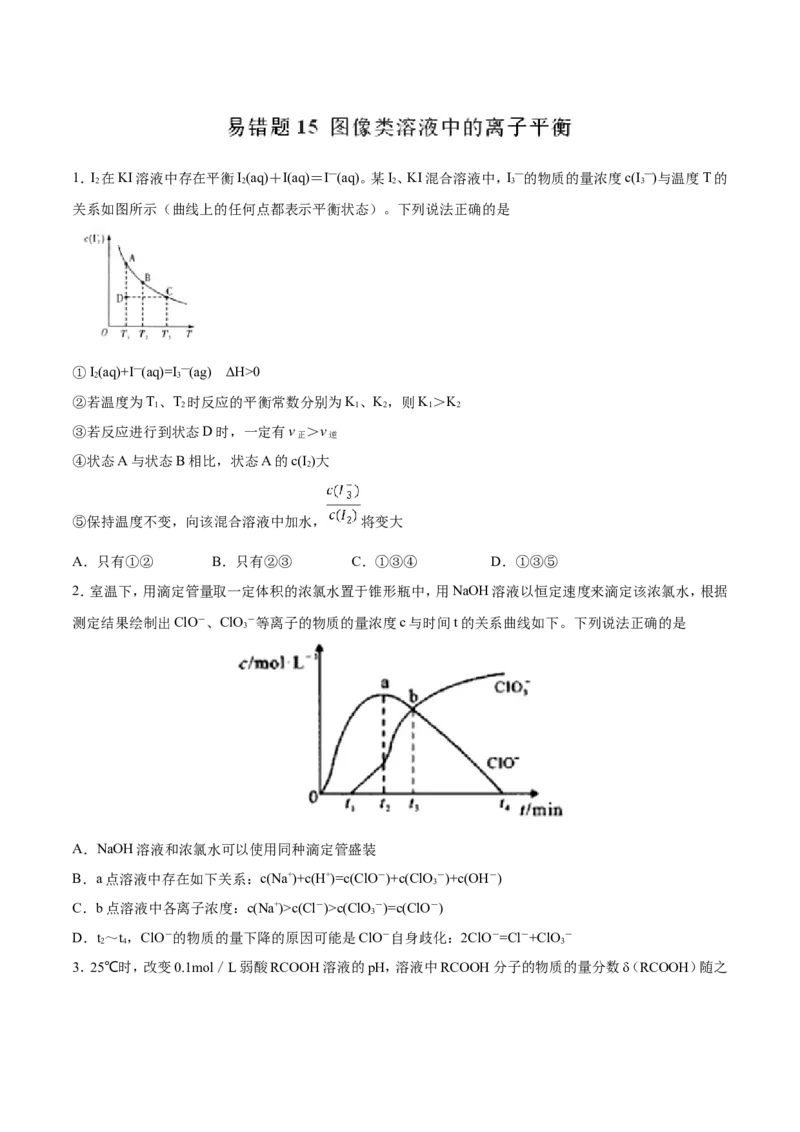
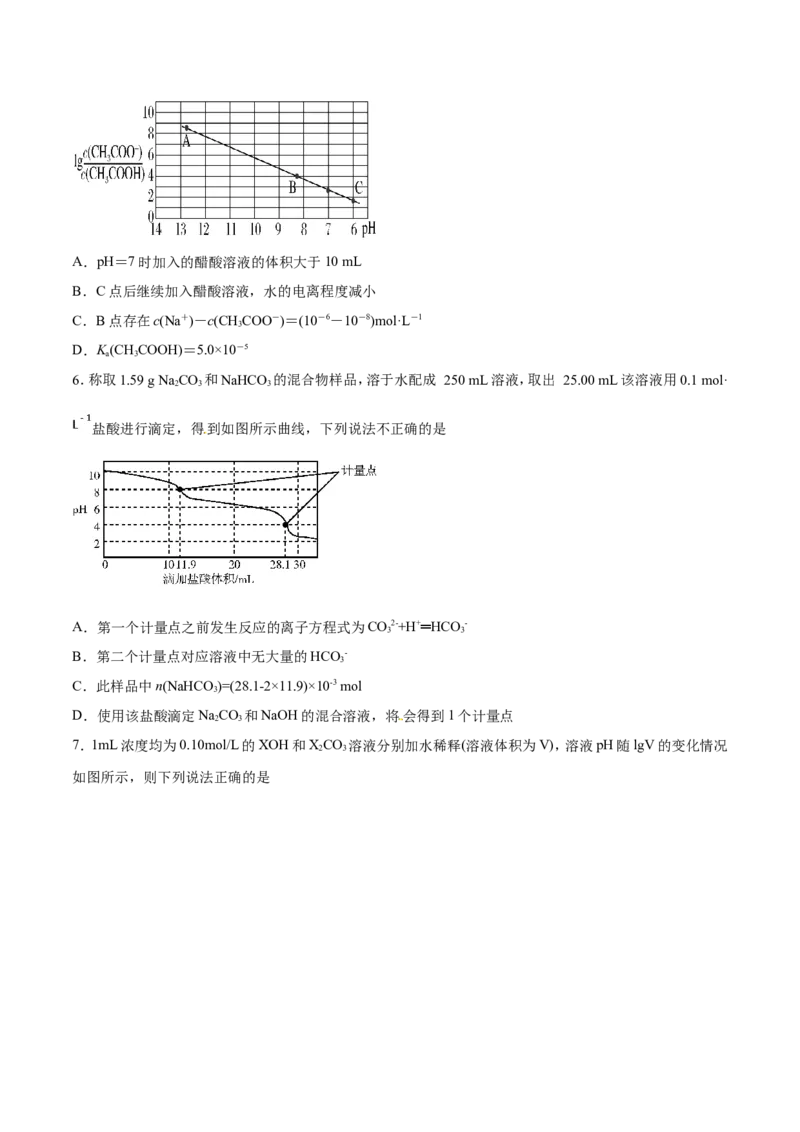
2.室温下,用滴定管量取一定体积的浓氯水置于锥形瓶中,用NaOH溶液以恒定速度来滴定该浓氯水,根据
测定结果绘制出ClO-、ClO -等离子的物质的量浓度c与时间t的关系曲线如下。下列说法正确的是
3
A.NaOH溶液和浓氯水可以使用同种滴定管盛装
B.a点溶液中存在如下关系:c(Na+)+c(H+)=c(ClO-)+c(ClO -)+c(OH-)
3
C.b点溶液中各离子浓度:c(Na+)>c(Cl-)>c(ClO -)=c(ClO-)
3
D.t~t,ClO-的物质的量下降的原因可能是ClO-自身歧化:2ClO-=Cl-+ClO -
2 4 3
3.25℃时,改变0.1mol/L弱酸RCOOH溶液的pH,溶液中RCOOH分子的物质的量分数δ(RCOOH)随之改变[已知 ,甲酸(HCOOH)]与丙酸(CHCHCOOH)溶液中δ
3 2
(RCOOH)与pH的关系如图所示。下列说法正确的是
A.图中M、N两点对应溶液中的c(OH-)比较:前者>后者
B.丙酸的电离常数K=10-4.88
C.等浓度的HCOONa和CHCHCOONa两种溶液的pH比较:前者>后者
3 2
D.将0.1 mol/L的HCOOH溶液与0.1 mol/L的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c
(HCOOH)>c(HCOO-)>c(OH-)>c(H+)
4.常温下,向20 mL 0.1 mol·L-1氨水中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积
的变化如图所示。则下列说法正确的是( )
A.常温下,0.1 mol·L-1氨水中NH ·H O的电离常数K约为1×10-5
3 2
B.a、b之间的点一定满足:c(NH+)>c(Cl-)>c(OH-)>c(H+)
4
C.c点溶液中c(NH +)=c(Cl-)
4
D.d点代表两溶液恰好完全反应
5.25 ℃时,将0.10 mol·L-1 CH COOH溶液滴加到10 mL 0.10 mol·L-1 NaOH溶液中,lg 与pH
3
的关系如图所示,C点坐标是(6,1.7)。下列说法不正确的是( )A.pH=7时加入的醋酸溶液的体积大于10 mL
B.C点后继续加入醋酸溶液,水的电离程度减小
C.B点存在c(Na+)-c(CHCOO-)=(10-6-10-8)mol·L-1
3
D.K(CHCOOH)=5.0×10-5
a 3
6.称取1.59 g Na CO 和NaHCO 的混合物样品,溶于水配成 250 mL溶液,取出 25.00 mL该溶液用0.1 mol·
2 3 3
盐酸进行滴定,得到如图所示曲线,下列说法不正确的是
A.第一个计量点之前发生反应的离子方程式为CO2-+H+═HCO -
3 3
B.第二个计量点对应溶液中无大量的HCO -
3[来源:学+科+网]
C.此样品中n(NaHCO )=(28.1-2×11.9)×10-3 mol
3
D.使用该盐酸滴定NaCO 和NaOH的混合溶液,将会得到1个计量点
2 3
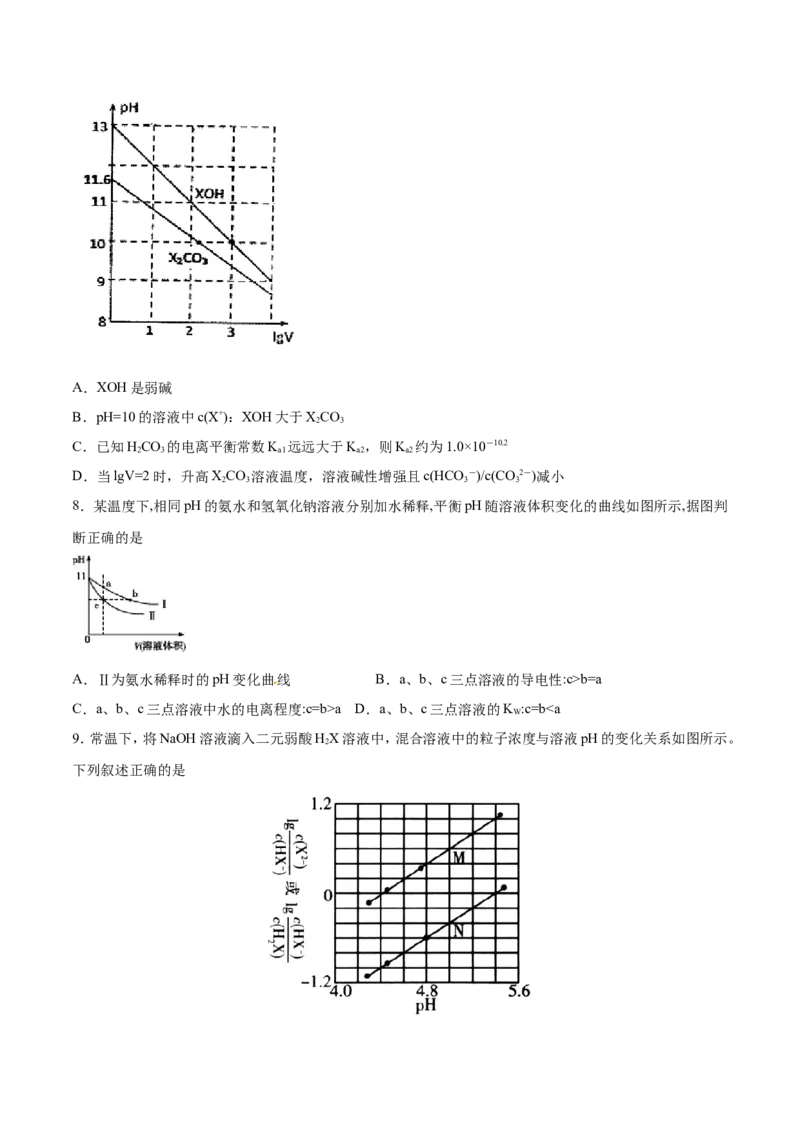
7.1mL浓度均为0.10mol/L的XOH和XCO 溶液分别加水稀释(溶液体积为V),溶液pH随lgV的变化情况
2 3
如图所示,则下列说法正确的是A.XOH是弱碱
B.pH=10的溶液中c(X+):XOH大于XCO
2 3
C.已知HCO 的电离平衡常数K 远远大于K ,则K 约为1.0×10-10.2
2 3 a1 a2 a2
D.当lgV=2时,升高XCO 溶液温度,溶液碱性增强且c(HCO -)/c(CO 2-)减小
2 3 3 3
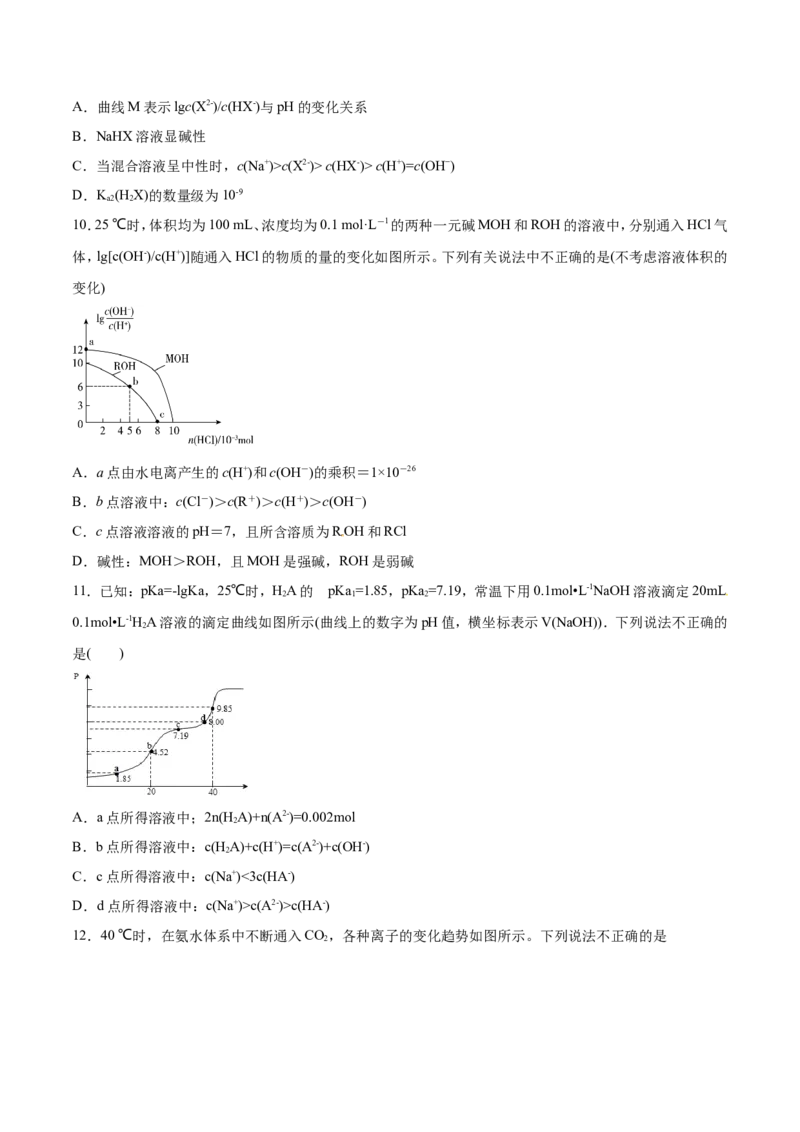
8.某温度下,相同pH的氨水和氢氧化钠溶液分别加水稀释,平衡pH随溶液体积变化的曲线如图所示,据图判
断正确的是
A.Ⅱ为氨水稀释时的pH变化曲线 B.a、b、c三点溶液的导电性:c>b=a
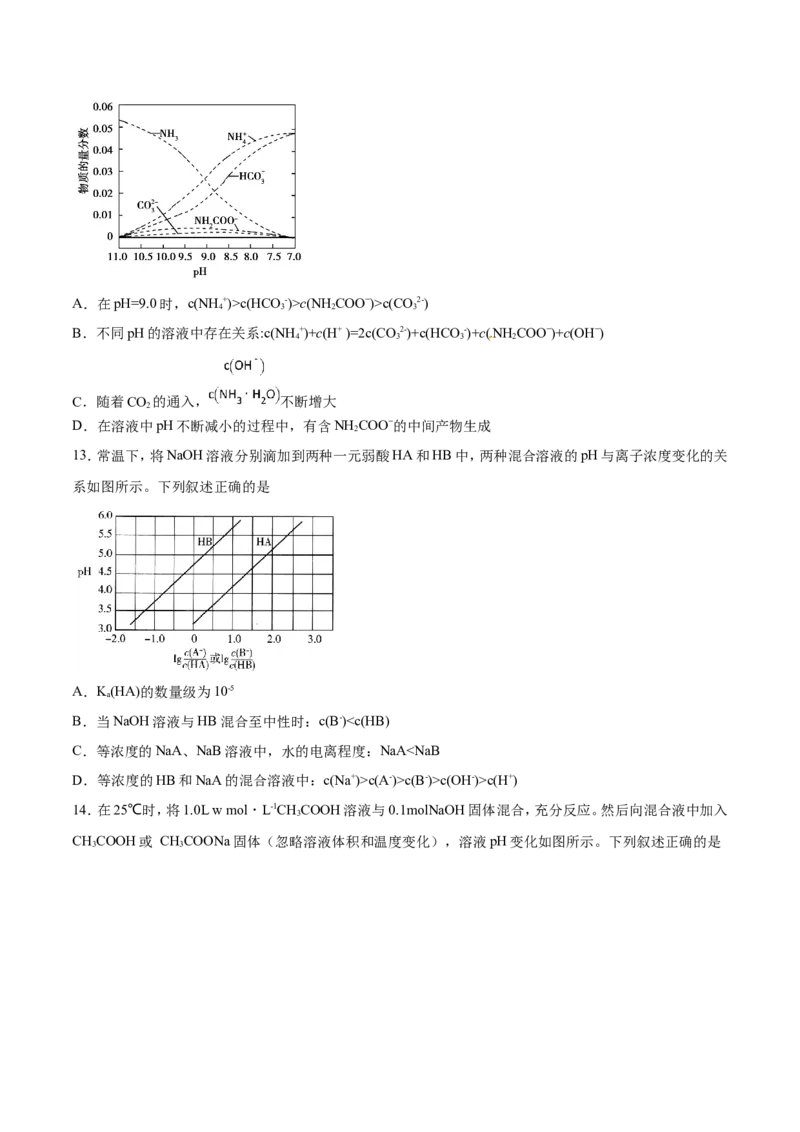
C.a、b、c三点溶液中水的电离程度:c=b>a D.a、b、c三点溶液的K :c=bc(X2-)> c(HX-)> c(H+)=c(OH−)
D.K (H X)的数量级为10-9
a2 2
10.25 ℃时,体积均为100 mL、浓度均为0.1 mol·L-1的两种一元碱MOH和ROH的溶液中,分别通入HCl气
体,lg[c(OH-)/c(H+)]随通入HCl的物质的量的变化如图所示。下列有关说法中不正确的是(不考虑溶液体积的
变化)
A.a点由水电离产生的c(H+)和c(OH-)的乘积=1×10-26
B.b点溶液中:c(Cl-)>c(R+)>c(H+)>c(OH-)
C.c点溶液溶液的pH=7,且所含溶质为ROH和RCl
D.碱性:MOH>ROH,且MOH是强碱,ROH是弱碱
11.已知:pKa=-lgKa,25℃时,HA的 pKa=1.85,pKa=7.19,常温下用0.1mol•L-1NaOH溶液滴定20mL
2 1 2
0.1mol•L-1HA溶液的滴定曲线如图所示(曲线上的数字为pH值,横坐标表示V(NaOH)).下列说法不正确的
2
是( )
A.a点所得溶液中;2n(H A)+n(A2-)=0.002mol
2
B.b点所得溶液中:c(HA)+c(H+)=c(A2-)+c(OH-)
2
C.c 点所得溶液中:c(Na+)<3c(HA-)
D.d 点所得溶液中:c(Na+)>c(A2-)>c(HA-)
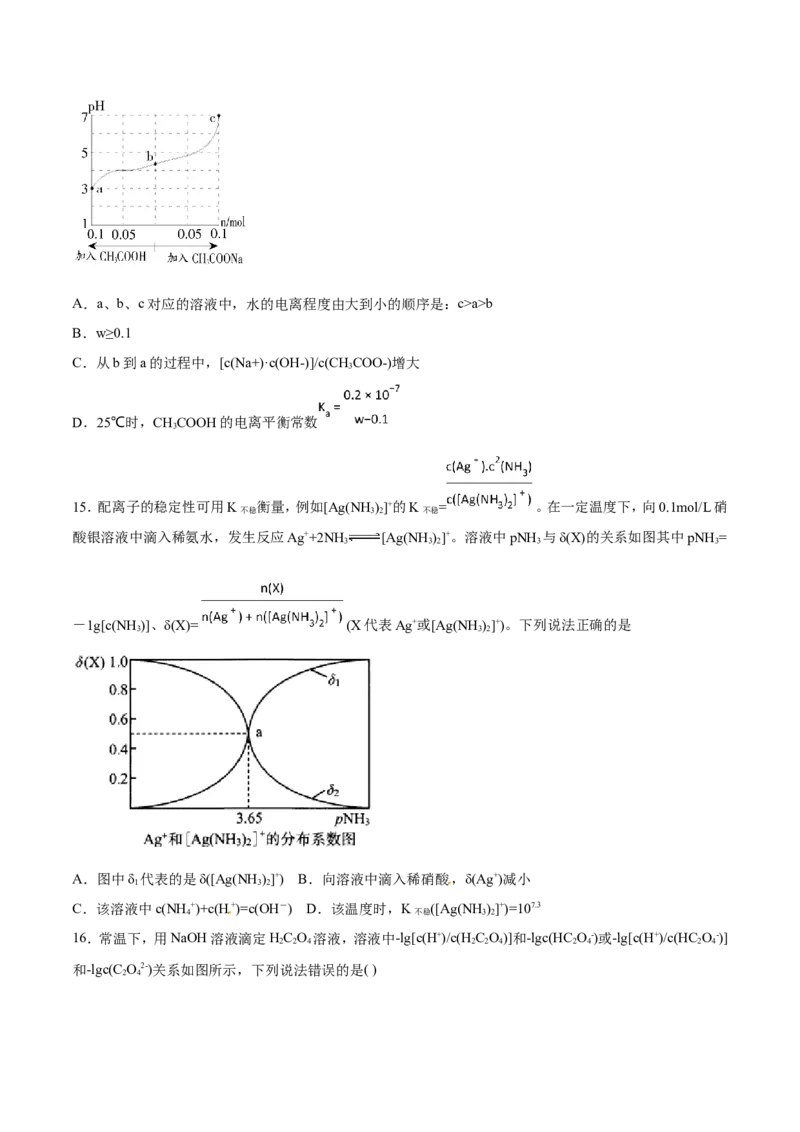
12.40 ℃时,在氨水体系中不断通入CO,各种离子的变化趋势如图所示。下列说法不正确的是
2A.在pH=9.0时,c(NH +)>c(HCO-)>c(NH COO−)>c(CO 2-)
4 3 2 3
B.不同pH的溶液中存在关系:c(NH+)+c(H+ )=2c(CO2-)+c(HCO-)+c(NH COO−)+c(OH−)
4 3 3 2
C.随着CO 的通入, 不断增大
2
D.在溶液中pH不断减小的过程中,有含NH COO−的中间产物生成
2
13.常温下,将NaOH溶液分别滴加到两种一元弱酸HA和HB中,两种混合溶液的pH与离子浓度变化的关
系如图所示。下列叙述正确的是
A.K(HA)的数量级为10-5
a
B.当NaOH溶液与HB混合至中性时:c(B-)c(A-)>c(B-)>c(OH-)>c(H+)
14.在25℃时,将1.0L w mol・L-1CHCOOH溶液与0.1molNaOH固体混合,充分反应。然后向混合液中加入
3
CHCOOH或 CHCOONa固体(忽略溶液体积和温度变化),溶液pH变化如图所示。下列叙述正确的是
3 3A.a、b、c对应的溶液中,水的电离程度由大到小的顺序是:c>a>b
B.w≥0.1
C.从b到a的过程中,[c(Na+)·c(OH-)]/c(CH COO-)增大
3
D.25℃时,CHCOOH的电离平衡常数
3
15.配离子的稳定性可用K 衡量,例如[Ag(NH)]+的K = 。在一定温度下,向0.1mol/L硝
不稳 3 2 不稳
酸银溶液中滴入稀氨水,发生反应Ag++2NH [Ag(NH)]+。溶液中pNH 与δ(X)的关系如图其中pNH =
3 3 2 3 3
-1g[c(NH )]、δ(X)= (X代表Ag+或[Ag(NH)]+)。下列说法正确的是
3 3 2
A.图中δ 代表的是δ([Ag(NH)]+) B.向溶液中滴入稀硝酸,δ(Ag+)减小
1 3 2
C.该溶液中c(NH +)+c(H+)=c(OH-) D.该温度时,K ([Ag(NH)]+)=107.3
4 不稳 3 2
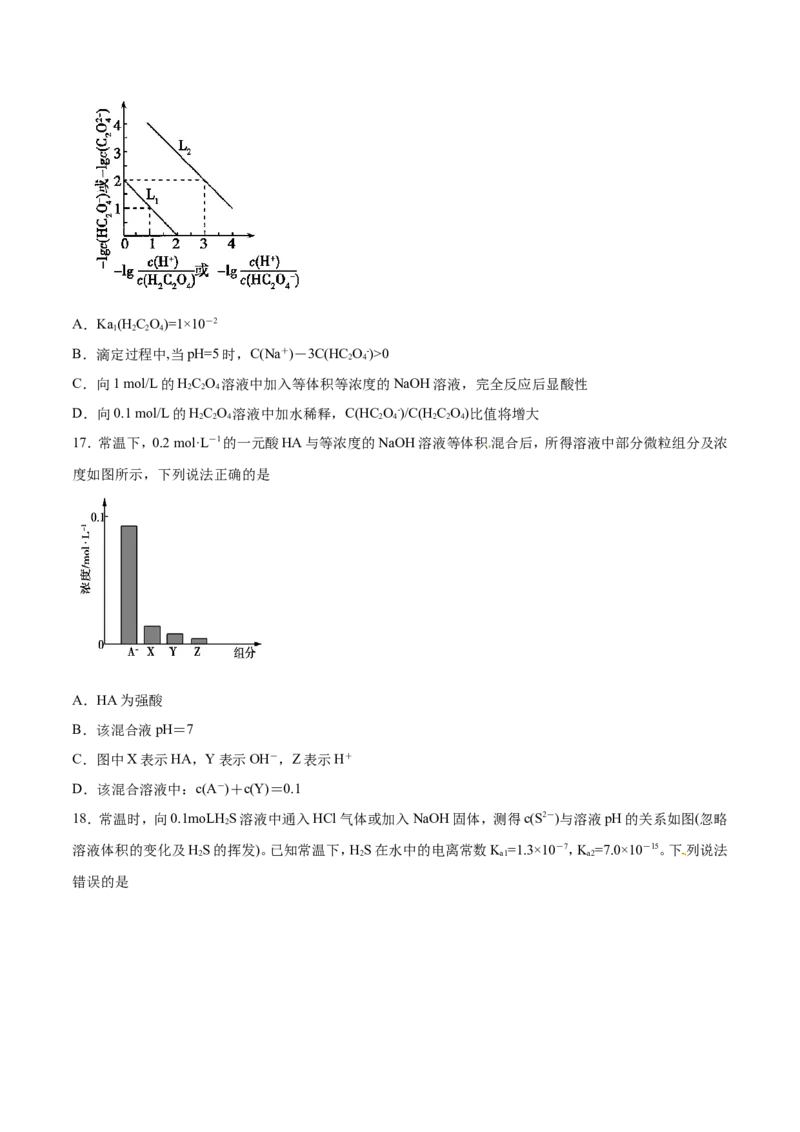
16.常温下,用NaOH溶液滴定HC O 溶液,溶液中-lg[c(H+)/c(H C O)]和-lgc(HC O-)或-lg[c(H+)/c(HC O-)]
2 2 4 2 2 4 2 4 2 4
和-lgc(C O2-)关系如图所示,下列说法错误的是( )
2 4A.Ka(H C O)=1×10-2
1 2 2 4
B.滴定过程中,当pH=5时,C(Na+)-3C(HC O-)>0
2 4
C.向1 mol/L的HC O 溶液中加入等体积等浓度的NaOH溶液,完全反应后显酸性
2 2 4
D.向0.1 mol/L的HC O 溶液中加水稀释,C(HC O-)/C(HC O)比值将增大
2 2 4 2 4 2 2 4
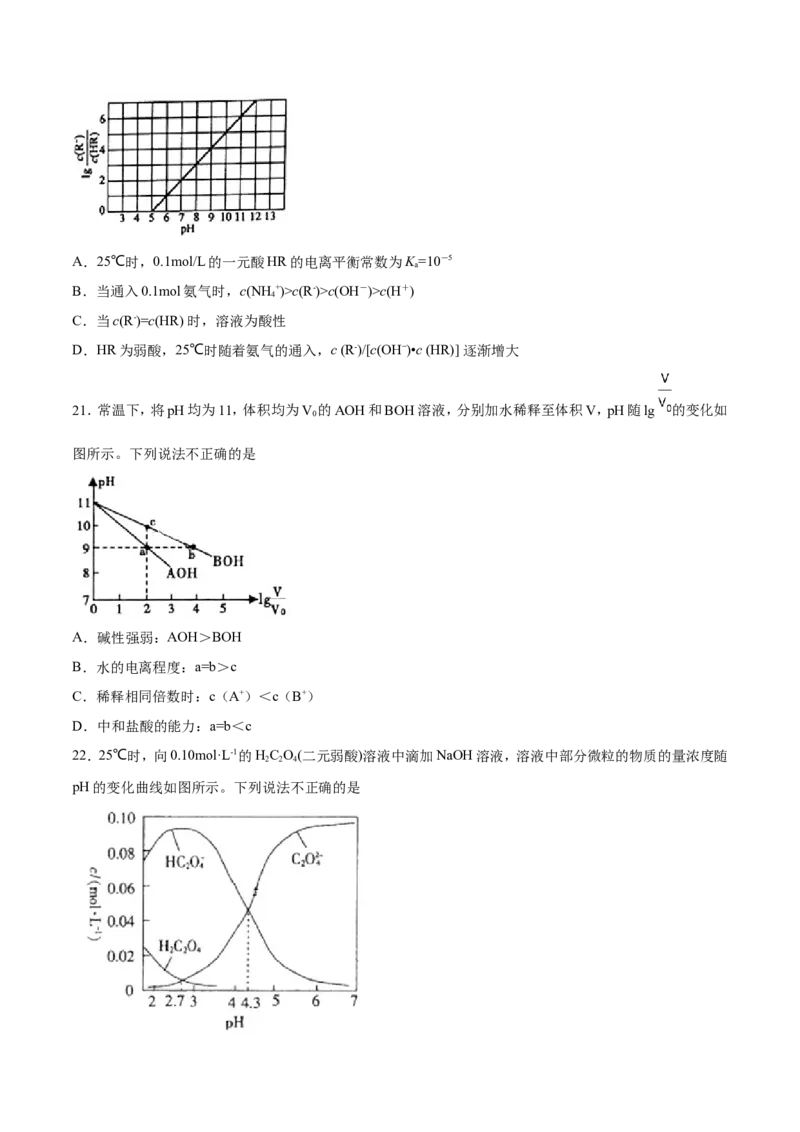
17.常温下,0.2 mol·L-1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓
度如图所示,下列说法正确的是
A.HA为强酸
B.该混合液pH=7
C.图中X表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=0.1
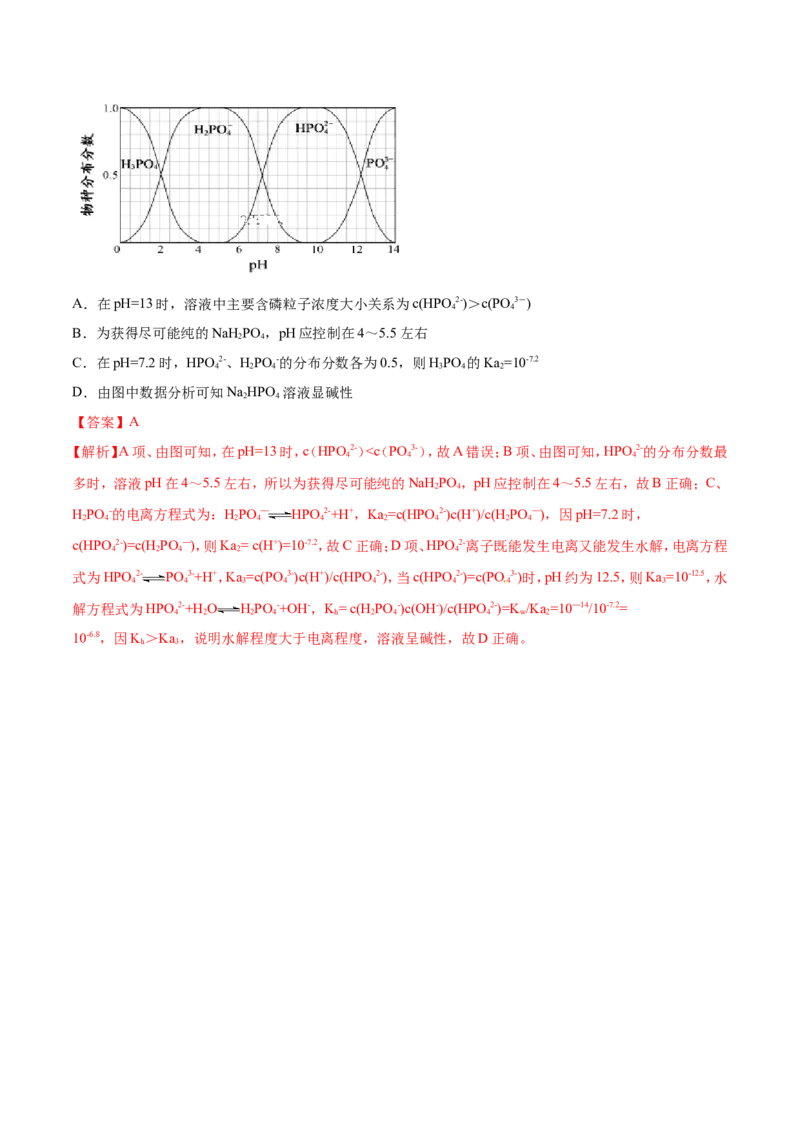
18.常温时,向0.1moLHS溶液中通入HCl气体或加入NaOH固体,测得c(S2-)与溶液pH的关系如图(忽略
2
溶液体积的变化及HS的挥发)。已知常温下,HS在水中的电离常数K =1.3×10-7,K =7.0×10-15。下列说法
2 2 a1 a2
错误的是A.当溶液中c(S2-)=1.4×10-19mol/L时,溶液中由水电离出的H+浓度为1.0×10-13mo/L
B.0.1mo/LNa S溶液中离子浓度之间的关系为:c(Na+)>c(HS-)+2c(S2-)
2
C.常温下,0.1 mol/L NaHS溶液的pH<7
D.当pH=13时,溶液中的c(HS)+c(HS-)=0.043mo/L
2
19.海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
Na+ Mg2+ Ca2+ Cl− HCO -
模拟海水中的离 [来源:学.科.网][来源:Zxxk.Com] [来源:Z。xx。k.Com] [来源:学_科_网] 3
子浓度(mol/L)
0.439 0.050 0.011 0.560 0.001
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;
实验过程中,假设溶液体积不变。
已知:K (CaCO)=4.96×10-9;K (MgCO )=6.82×10-6;
sp 3 sp 3
K [Ca(OH) ]=4.68×10-6;K [Mg(OH) ]=5.61×10-12。
sp 2 sp 2
下列说法正确的是
A.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH) 和Mg(OH) 的混合物
2 2
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.沉淀物X为CaCO
3
20.25℃时,向1L 0.1mol/L的一元酸HR溶液中逐渐通入氨气(已知25℃时一水合氨的电离平衡常数为
K=1.76×10-5),保持溶液的温度和体积不变,混合溶液的pH与粒子浓度比值的对数变化关系如图所示。下列
叙述错误的是A.25℃时,0.1mol/L的一元酸HR的电离平衡常数为K=10-5
a
B.当通入0.1mol氨气时,c(NH +)>c(R-)>c(OH-)>c(H+)
4
C.当c(R-)=c(HR) 时,溶液为酸性
D.HR为弱酸,25℃时随着氨气的通入,c (R-)/[c(OH−)•c (HR)] 逐渐增大
21.常温下,将pH均为11,体积均为V 的AOH和BOH溶液,分别加水稀释至体积V,pH随lg 的变化如
0
图所示。下列说法不正确的是
A.碱性强弱:AOH>BOH
B.水的电离程度:a=b>c
C.稀释相同倍数时:c(A+)<c(B+)
D.中和盐酸的能力:a=b<c
22.25℃时,向0.10mol·L-1的HC O(二元弱酸)溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随
2 2 4
pH的变化曲线如图所示。下列说法不正确的是A.25℃时HC O 的一级电离常数为K =10-4.3
2 2 4 a1
B.pH=2.7的溶液中:c(HC O)=c(C O2-)
2 2 4 2 4
C.pH=7的溶液中:c(Na+)>2c(C O2-)
2 4
D.滴加NaOH溶液的过程中始终存在:c(OH-)+2c(C O2-)+c(HC O-)=c(Na+)+c(H+)
2 4 2 4
【答案】A
23.常温时,改变饱和氯水的pH,得到部分含氯微粒的物质的量分数与pH的关系如图所示。下列叙述不正确
的是
A.该温度下,HClO H++ClO-的电离常数K 的对值lgK= -7.54
a a
B.氯水中的Cl、ClO-、HClO均能与KI发生反应
2
C.pH=1的氯水中,c(Cl )>c(Cl -)>c(HClO)>c(ClO-)
2 3
D.已知常温下反应Cl(aq)+Cl-(aq) Cl-(aq)的K=0.191,当pH增大时,K减小
2 3
【答案】D24.常温下,向20 mL某浓度的硫酸中滴入0.1 mol·L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体
积变化如图所示。下列分析正确的是
A.该硫酸的浓度为1 mol·L-1
B.b点所示溶液中:c( )=c( )
C.V=40
D.c点所示溶液中:c(H+)-c(OH-)=c(NH ·H O)
3 2
【答案】D
25.HPO 与NaOH溶液反应的体系中,含磷的各种粒子的分布分数(平衡时某粒子的浓度占各粒子浓度之和
3 4
的分数)与pH 的关系如下图所示。下列有关说法不正确的是A.在pH=13时,溶液中主要含磷粒子浓度大小关系为c(HPO 2-)>c(PO 3-)
4 4
B.为获得尽可能纯的NaH PO ,pH应控制在4~5.5 左右
2 4
C.在pH=7.2时,HPO 2-、HPO -的分布分数各为0.5,则HPO 的Ka=10-7.2
4 2 4 3 4 2
D.由图中数据分析可知NaHPO 溶液显碱性
2 4
【答案】A
【解析】A项、由图可知,在pH=13时,c(HPO 2-)