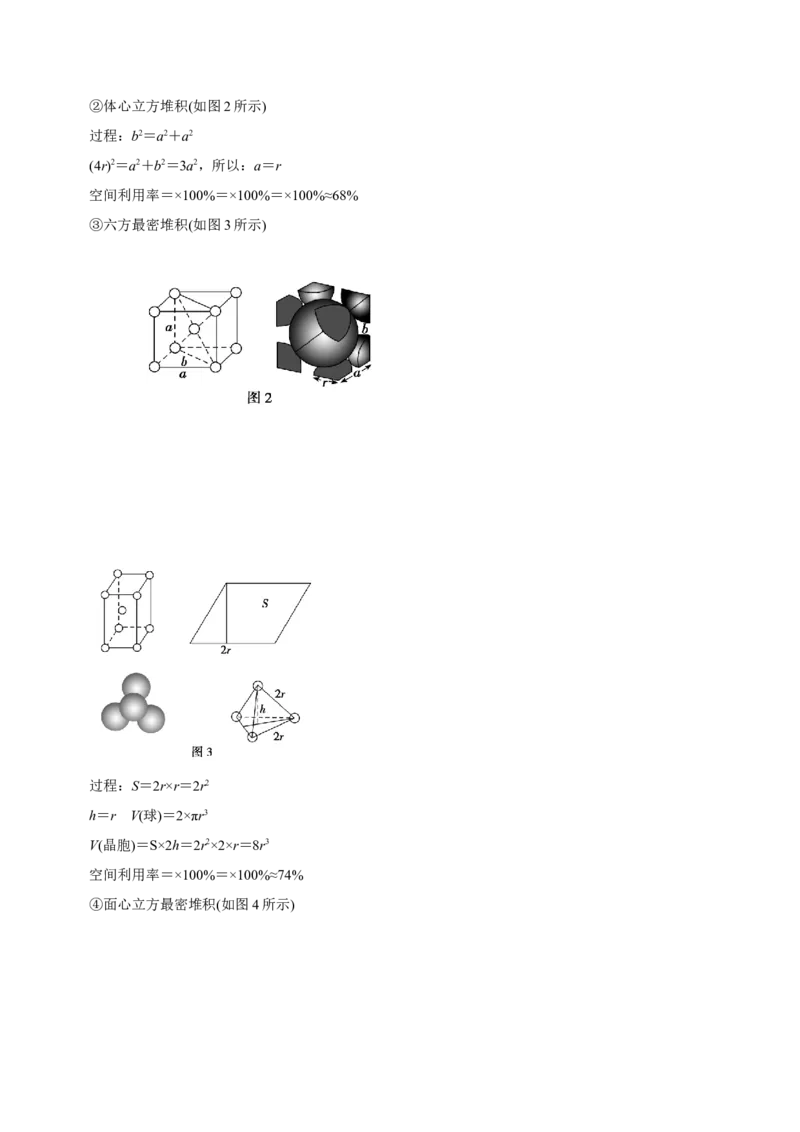
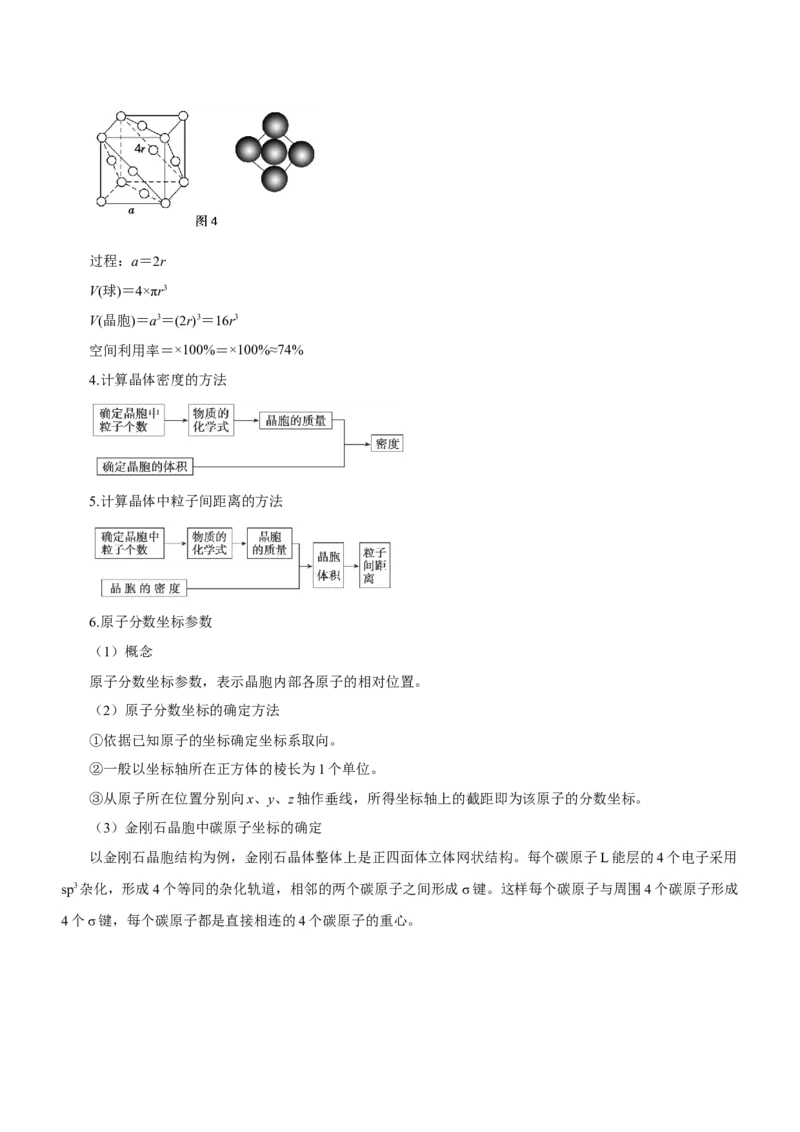
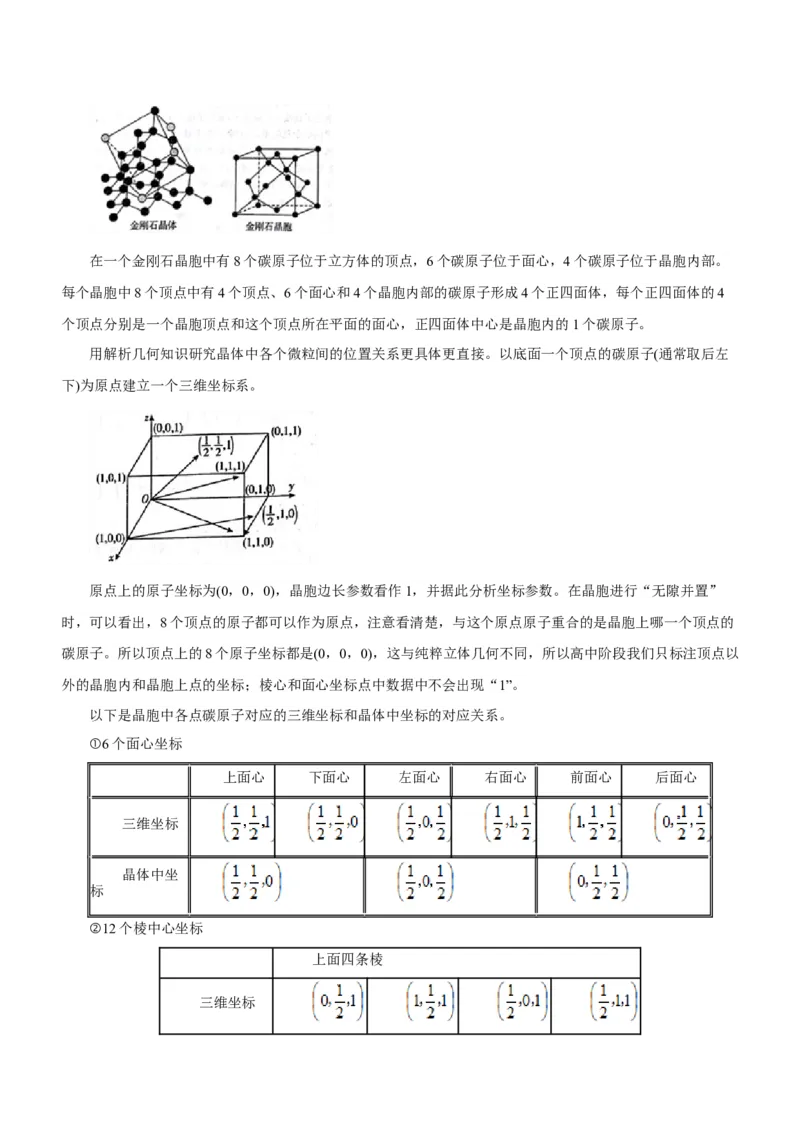
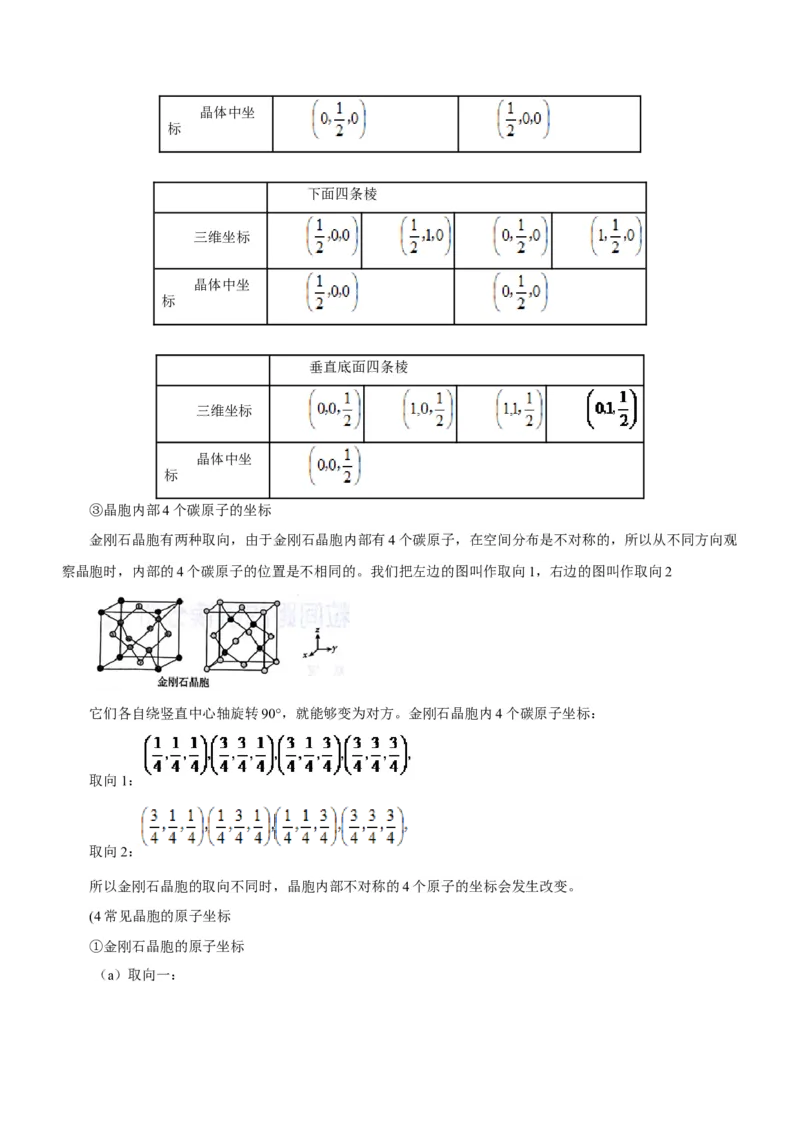
文档内容
专题 16 物质结构与性质综合题
稳定加创新是本专题的基本特点,命题采取结合新科技,新能源等社会热点为背景,命题的形式分为选择
题和填空题,原子的结构与性质、分子的结构与性质和晶体的结构与性质是命题的三大要点。从大题的构成来
看,给出一定的知识背景,然后设置成4—5个小题,每个小题考查一个知识要点是主要的命题模式,内容主
要考查基本概念,如电子排布式,轨道式,电离能,电负性,杂化方式以及空间构型等,也可联系有机考查有
机物中C原子的杂化,联系数学几何知识考查晶体的计算等,一般利用均摊法考查晶胞中的原子个数,或者
考查晶体的化学式的书写、晶体类型的判断等,考查的抽象思维能力、逻辑思维能力;同时培养学生的分析和
推理能力。
高频考点一 原子结构与性质
1.核外电子排布
(1)核外电子排布规律
(2)原子结构示意图
(3)基态原子的核外电子排布原理
①能量最低原理:即电子尽可能地先占有能量低的轨道,然后进入能量高的轨道,使整个原子的能量处于
最低状态。如图为构造原理示意图,即基态原子核外电子在原子轨道上的排布顺序图:②泡利不相容原理
每个原子轨道里最多只能容纳2个电子,且自旋状态相反。
如2s轨道上的电子排布为 ,不能表示为 。
③洪特规则
当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋状态相同。
如2p3的电子排布为
,不能表示为 或
洪特规则特例:当能量相同的原子轨道在全满(p6、d10、f14)、半满(p3、d5、f7)和全空(p0、d0、f0)状态时,
体系的能量最低,如: Cr的电子排布式为1s22s22p63s23p63d54s1。
24
(4)表示基态原子核外电子排布的四种方法
表示方法 举例
电子排布式 Cr:1s22s22p63s23p63d54s1
简化表示式 Cu:[Ar]3d104s1
价电子排布式 Fe:3d64s2
电子排布图
(或轨道表示式) O:
5.第一电离能、电负性
(1)元素第一电离能的周期性变化规律。
一般 同一周期,随着原子序数的增加,元素的第一电离能呈现增大的趋势,稀有气体元素的第一电离能最
规律 大,碱金属元素的第一电离能最小;同一主族,随着电子层数的增加,元素的第一电离能逐渐减小
特殊 第一电离能的变化与元素原子的核外电子排布有关。通常情况下,当原子核外电子排布在能量相等的轨道上形成全空(p0、d0、f0)、半满(p3、d5、f7)和全满(p6、d10、f14)结构时,原子的能量较低,该元素
情况 具有较大的第一电离能。如同周期主族元素,第ⅡA族元素的原子最外层s能级全充满、ⅤA族元素
的原子最外层p能级半充满,比较稳定,所以其第一电离能大于同周期相邻的主族元素
(2)电负性大小判断。
规律 在周期表中,同周期主族元素电负性从左到右逐渐增大,同主族从上往下逐渐减小
常常应用化合价及物质类别判断电负性的大小,如O与Cl的电负性比较:①HClO中Cl为+1价、O
方法
为-2价,可知O的电负性大于Cl;②Al O 是离子化合物、AlCl 是共价化合物,可知O的电负性大于Cl
2 3 3
核心考点二 分子结构与性质
1.与分子结构有关的两种理论
(1)杂化轨道理论
①基本观点:杂化轨道成键满足原子轨道最大重叠原理;杂化轨道形成的共价键更加牢固。
②杂化轨道类型与分子立体构型的关系
杂化轨道类型 杂化轨道数目 分子立体构型 实例
sp 2 直线形 CO、BeCl 、HgCl
2 2 2
平面三角形 BF、BCl 、CHO
3 3 2
sp2 3
V形 SO 、SnBr
2 2
四面体形 CH、CCl 、CHCl
4 4 3
sp3 4 三角锥形 NH 、PH 、NF
3 3 3
V形 HS、HO
2 2
注意:杂化轨道数=与中心原子结合的原子数+中心原子的孤电子对数。
(2)价层电子对互斥理论
①基本观点:分子的中心原子上的价层电子对(包括σ键电子对和中心原子上的孤电子对)由于相互排斥,
尽可能趋向彼此远离。
②价层电子对数的计算
中心原子的价层电子对数=σ键电子对数(与中心原子结合的原子数)+中心原子的孤电子对数=σ键电子
对数+(a-xb)
其中a为中心原子的价电子数,x、b分别为与中心原子结合的原子数及与中心原子结合的原子最多能接受
的电子数(H为1,其他原子为“8-该原子的价电子数”)。微粒为阳离子时,中心原子的价电子数要减去离子
所带电荷数;微粒为阴离子时,中心原子的价电子数要加上离子所带电荷数。如SO 中硫原子的孤电子对数为
2
=1;HO+中氧原子的孤电子对数为=1;CO中碳原子的孤电子对数为=0。
3
【易错提醒】在计算孤电子对数时,出现0.5或1.5,则把小数进位为整数,即1或2。如NO 的中心原子
2
N的孤电子对数为=0.5≈1,则价层电子对数为3,故VSEPR模型为平面三角形,分子立体构型为V形。
③利用价层电子对互斥理论判断分子(或离子)立体构型
价层电子对数 孤电子对数 分子(或离子)立体构型 示例2 0 CO、BeCl
2 2
3 0 BF、SO 、CO
3 3
3 1 SO
2
4 0 CH、NH、SO、CCl
4 4
4 1 NH 、PCl 、HO+
3 3 3
4 2 HO、HS
2 2
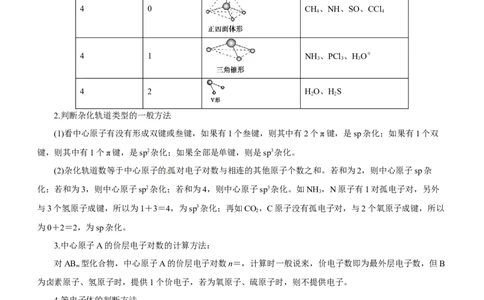
2.判断杂化轨道类型的一般方法
(1)看中心原子有没有形成双键或叁键,如果有1个叁键,则其中有2个π键,是sp杂化;如果有1个双
键,则其中有1个π键,是sp2杂化;如果全部是单键,则是sp3杂化。
(2)杂化轨道数等于中心原子的孤对电子对数与相连的其他原子个数之和。若和为2,则中心原子sp杂
化;若和为3,则中心原子sp2杂化;若和为4,则中心原子sp3杂化。如NH ,N原子有1对孤电子对,另外
3
与3个氢原子成键,所以为1+3=4,为sp3杂化;再如CO,C原子没有孤电子对,与2个氧原子成键,所以
2
为0+2=2,为sp杂化。
3.中心原子A的价层电子对数的计算方法:
对AB 型化合物,中心原子A的价层电子对数n=,计算时一般说来,价电子数即为最外层电子数,但B
m
为卤素原子、氢原子时,提供1个价电子,若为氧原子、硫原子时,则不提供电子。
4.等电子体的判断方法
(1)判断方法:一是同主族变换法,如CO 与CS、CF 与CCl 是等电子体,二是左右移位法,如N 与
2 2 4 4 2
CO,CO、NO 与SO 是等电子体。如果是阴离子,价电子应加上阴离子所带的电荷数;如果是阳离子,价
3
电子应减去阳离子所带的电荷数。如NH价电子为8,CO价电子为24。
(2)常见的等电子体
微粒 通式 价电子总数 立体构型
CH、NH AX 8e- 正四面体形
4 4
CO、N AX 10e- 直线形
2CO、CNS-、NO、N AX 16e- 直线形
2 2
SO 、O、NO AX 18e- V形
2 3 2
CO、NO、SO AX 24e- 平面三角形
3 3
PO、SO、ClO AX 26e- 三角锥形
3
SO、PO AX 32e- 正四面体形
4
5.分子性质
(1)分子极性
1)分子构型与分子极性的关系
2)键的极性与分子极性的关系
类型 实例 两个键之间的夹角 键的极性 分子的极性 空间构型
X H、N - 非极性键 非极性分子 直线型
2 2 2
XY HCl、NO - 极性键 极性分子 直线型
CO、CS 180° 极性键 非极性分子 直线型
2 2
XY (X Y) SO 120° 极性键 极性分子 三角形
2 2 2
HO、HS 104.5° 极性键 极性分子 V形
2 2
BF 120° 极性键 非极性分子 平面三角形
3
XY
3
NH 107.3° 极性键 非极性分子 三角锥形
3
XY CH、CCl 109.5° 极性键 非极性分子 正四面体
4 4 4
(2)溶解性——“相似相溶”规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂;
若存在氢键,则溶剂和溶质之间的氢键作用力越大,溶解性越好。
(3)无机含氧酸分子的酸性
无机含氧酸可写成(HO) RO,如果成酸元素R相同,则n值越大,R的正电性越高,使R—O—H中O的
m n
电子向R偏移,在水分子的作用下越易电离出H+,酸性越强,如酸性:HClO一氯乙烯>一氯乙炔 Cl参与形成的大π键越多,形成的C-Cl键的
键长越短
【解析】①一氯乙烯的结构式为 ,碳为双键碳,采取sp2杂化,因此C的一个sp2杂化轨道与Cl
的3p 轨道形成C-Clσ键。
x
题型五 杂化轨道及空间构型【例5】(2022·辽宁卷)理论化学模拟得到一种 离子,结构如图。下列关于该离子的说法错误的是
A. 所有原子均满足8电子结构 B. N原子的杂化方式有2种
C. 空间结构为四面体形 D. 常温下不稳定
【答案】B
【解析】由 的结构式可知,所有N原子均满足8电子稳定结构,A正确;中心N原子为 杂化,与
中心N原子直接相连的N原子为 杂化,与端位N原子直接相连的N原子为 杂化,端位N原子为 杂
化,则N原子的杂化方式有3种,B错误;中心N原子为 杂化,则其空间结构为四面体形,C正确;
中含叠氨结构( ),常温下不稳定,D正确;故选B。
【变式探究】(2022·辽宁卷)下列符号表征或说法正确的是
A. 电离: B. 位于元素周期表p区
C. 空间结构:平面三角形 D. 电子式:
【答案】C
【解析】 是二元弱酸,电离分步进行,其一级电离方程式为 ,A错误;基态
原子的价电子排布式是 ,最后一个电子填充在s能级,位于元素周期表s区,B错误; 中心碳原
子的价层电子对数为 ,故其空间结构为平面三角形,C正确; 是离子化
合物,电子式为 ,D错误;故选C。题型六 共价键的极性与分子极性的判断
【例6】(2022·江苏卷)下列说法正确的是
A. 金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C. 锗原子( )基态核外电子排布式为
D. ⅣA族元素单质的晶体类型相同
【答案】B
【解析】金刚石中的碳原子为正四面体结构, 夹角为109°28′,故A错误; 的化学键为Si-
H,为极性键,为正四面体,正负电荷中心重合,为非极性分子; 的化学键为Si-Cl,为极性键,为正四
面体,正负电荷中心重合,为非极性分子,故B正确;锗原子( )基态核外电子排布式为[Ar] ,故
C错误;ⅣA族元素中的碳元素形成的石墨为混合晶体,而硅形成的晶体硅为原子晶体,故D错误;故选B。
【变式探究】(2022·山东卷) GaN、AlN属于第三代半导体材料,二者成键结构与金刚石相似,晶体中
只存在N-Al键、N-Ga键。下列说法错误的是
A. GaN的熔点高于AlN B. 晶体中所有化学键均为极性键
C. 晶体中所有原子均采取sp3杂化 D. 晶体中所有原子的配位数均相同
【答案】A
【解析】Al和Ga均为第ⅢA元素,N属于第ⅤA元素,AlN、GaN的成键结构与金刚石相似,则其为共
价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似。AlN、GaN晶体中,N原子与其相邻
的原子形成3个普通共价键和1个配位键。因为AlN、GaN为结构相似的共价晶体,由于Al原子的半径小于
Ga,N—Al的键长小于N—Ga的,则N—Al的键能较大,键能越大则其对应的共价晶体的熔点越高,故GaN
的熔点低于AlN,A说错误;不同种元素的原子之间形成的共价键为极性键,故两种晶体中所有化学键均为极
性键,B说法正确;金刚石中每个C原子形成4个共价键(即C原子的价层电子对数为4),C原子无孤电子
对,故C原子均采取sp3杂化;由于AlN、GaN与金刚石互为等电子体,则其晶体中所有原子均采取sp3杂
化,C说法正确;金刚石中每个C原子与其周围4个C原子形成共价键,即C原子的配位数是4,由于AlN、
GaN与金刚石互为等电子体,则其晶体中所有原子的配位数也均为4,D说法正确。综上所述,故选A。
题型七 氢键和分子间作用力【例7】(2022·山东卷)在水中的溶解度,吡啶( )远大于苯,主要原因是①_______,②_______。
【答案】吡啶能与HO分子形成分子间氢键 吡啶和HO均为极性分子相似相溶,而苯为非极性分子
2 2
【解析】已知苯分子为非极性分子,HO分子为极性分子,且吡啶( )中N原子上含有孤电子对能与HO
2 2
分子形成分子间氢键,从而导致在水中的溶解度,吡啶远大于苯,故答案为:吡啶能与HO分子形成分子间
2
氢键;吡啶和HO均为极性分子相似相溶,而苯为非极性分子。
2
【变式探究】(2022·浙江卷)回答下列问题:两种有机物的相关数据如表:
物质 HCON(CH ) HCONH
3 2 2
相对分子质量 73 45
沸点/℃ 153 220
HCON(CH ) 的相对分子质量比HCONH 的大,但其沸点反而比HCONH 的低,主要原因是______。
3 2 2 2
【答案】HCON(CH ) 分子间只有一般的分子间作用力,HCONH 分子间存在氢键,破坏一般的分子间作
3 2 2
用力更容易,所以沸点低。
【解析】HCON(CH ) 分子间只有一般的分子间作用力,HCONH 分子间存在氢键,破坏一般的分子间作
3 2 2
用力更容易,所以沸点低。
题型八 晶体类型判断
【例8】(2022·江苏卷)下列说法正确的是( )
A. 金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C. 锗原子( )基态核外电子排布式为
D. ⅣA族元素单质的晶体类型相同
【答案】B
【解析】金刚石中的碳原子为正四面体结构, 夹角为109°28′,故A错误; 的化学键为Si-
H,为极性键,为正四面体,正负电荷中心重合,为非极性分子; 的化学键为Si-Cl,为极性键,为正四
面体,正负电荷中心重合,为非极性分子,故B正确;锗原子( )基态核外电子排布式为[Ar] ,故C错误;ⅣA族元素中的碳元素形成的石墨为混合晶体,而硅形成的晶体硅为共价晶体,故D错误;故选B。
【变式探究】(2021·辽宁卷)单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。下列
说法错误的是
A.S位于元素周期表p区 B.该物质的化学式为
C.S位于H构成的八面体空隙中 D.该晶体属于分子晶体
【答案】D
【解析】A.S的价电子排布式为:3s23p4,故S位于元素周期表p区,A正确;由该物质形成晶体的晶胞
可知,H、S原子个数比为3:1,故该物质的化学式为 ,B正确;S位于H构成的八面体空隙中,如图所示
,C正确;由于该晶体是一种新型超导材料,说明其是由阴、阳离子构成的,故该晶体属于离
子晶体,D错误;故选D。
题型九 晶胞粒子数与晶体化学式判断
【例9】(2022·湖北卷)某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错误的是(
)
A. 的配位数为6 B. 与 距离最近的是
C. 该物质的化学式为 D. 若 换为 ,则晶胞棱长将改变
【答案】B【解析】 配位数为与其距离最近且等距离的F-的个数,如图所示, 位于体心,F-位于面心,所
以 配位数为6,A正确; 与 的最近距离为棱长的 , 与 的最近距离为棱长的 ,所以与
距离最近的是 ,B错误; 位于顶点,所以 个数= =1,F-位于面心,F-个数= =3,
位于体心,所以 个数=1,综上,该物质的化学式为 ,C正确; 与 半径不同,替换后
晶胞棱长将改变,D正确;故选B。
【变式探究】(2022·广东卷)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其
热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之
一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
①X的化学式为_______。
②设X的最简式的式量为 ,晶体密度为 ,则X中相邻K之间的最短距离为_______ (列
出计算式, 为阿伏加德罗常数的值)。
【答案】 ① KSeBr ②
2 6
【解析】①根据晶胞结构得到K有8个, 有 ,则X的化学式为KSeBr ;
2 6
②设X的最简式的式量为 ,晶体密度为 ,设晶胞参数为anm,得到,解得 ,X中相邻K之间的最短距离为晶胞参数的一
半即 。
题型十 晶体密度及粒子间距的计算
【例10】(2022·全国甲卷)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离
2
子是_______;若该立方晶胞参数为a pm,正负离子的核间距最小为_______pm。
【答案】 Ca2+ a pm
【解析】根据萤石晶胞结构,浅色X离子分布在晶胞的顶点和面心上,则1个晶胞中浅色X离子共有
8×+6×=4个,深色Y离子分布在晶胞内部,则1个晶胞中共有8个深色Y离子,因此该晶胞的化学式应为
XY ,结合萤石的化学式可知,X为Ca2+;根据晶胞,将晶胞分成8个相等的小正方体,仔细观察CaF 的晶胞
2 2
结构不难发现F-位于晶胞中8个小立方体中互不相邻的4个小立方体的体心,小立方体边长为a,体对角线为
a,Ca2+与F-之间距离就是小晶胞体对角线的一半,因此晶体中正负的核间距的最小的距离为a pm。
【变式探究】(2022·全国乙卷) 晶体中 离子作体心立方堆积(如图所示), 主要分布在由
构成的四面体、八面体等空隙中。在电场作用下, 不需要克服太大的阻力即可发生迁移。因此,
晶体在电池中可作为_______。
已知阿伏加德罗常数为 ,则 晶体的摩尔体积 _______ (列出算式)。【答案】电解质
【解析】由题意可知,在电场作用下,Ag+不需要克服太大阻力即可发生迁移,因此α-AgI晶体是优良的
离子导体,在电池中可作为电解质;每个晶胞中含碘离子的个数为8×+1=2个,依据化学式AgI可知,银离子
个数也为2个,晶胞的物质的量n= mol= mol,晶胞体积V=a3pm3=(504×10-12)3m3,则α-AgI晶体的摩尔
体积V = = = m3/mol。
m
题型十一 综合考查
【例11】(2022·全国乙卷)卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问
题:
(1)氟原子激发态的电子排布式有_______,其中能量较高的是_______。(填标号)
a. b. c. d.
(2)①一氯乙烯 分子中,C的一个_______杂化轨道与Cl的 轨道形成 _______键,并
且Cl的 轨道与C的 轨道形成3中心4电子的大 键 。
②一氯乙烷 、一氯乙烯 、一氯乙炔 分子中, 键长的顺序是_______,
理由:(ⅰ)C的杂化轨道中s成分越多,形成的 键越强:(ⅱ)_______。
(3)卤化物 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为_______。解释X
的熔点比Y高的原因_______。
(4) 晶体中 离子作体心立方堆积(如图所示), 主要分布在由 构成的四面体、八面体等空
隙中。在电场作用下, 不需要克服太大的阻力即可发生迁移。因此, 晶体在电池中可作为_______。
已知阿伏加德罗常数为 ,则 晶体的摩尔体积 _______ (列出算式)。
【答案】(1)ad d
(2)①sp2 σ ②一氯乙烷>一氯乙烯>一氯乙炔 Cl参与形成的大π键越多,形成的C-Cl键的键长
越短
(3) CsCl CsCl为离子晶体,ICl为分子晶体 (4)电解质
【解析】
(1)F的原子序数为9,其基态原子电子排布式为1s22s22p5 1s22s22p43s1,基态氟原子2p能级上的1个电
。
子跃迁到3s能级上,属于氟原子的激发态,a正确;1s22s22p43d2,核外共10个电子,不是氟原子,b错误;
1s22s12p5,核外共8个电子,不是氟原子,c错误;1s22s22p33p2,基态氟原子2p能级上的2个电子跃迁到3p能
级上,属于氟原子的激发态,d正确;
答案选ad;而同一原子3p能级的能量比3s能级的能量高,因此能量最高的是1s22s22p33p2,答案选d。
(2)①一氯乙烯的结构式为 ,碳为双键碳,采取sp2杂化,因此C的一个sp2杂化轨道与Cl的
3p 轨道形成C-Clσ键。
x
②C的杂化轨道中s成分越多,形成的C-Cl键越强,C-Cl键的键长越短,一氯乙烷中碳采取sp3杂化,一
氯乙烯中碳采取sp2杂化,一氯乙炔中碳采取sp杂化,sp杂化时p成分少,sp3杂化时p成分多,因此三种物质
中C-Cl键键长顺序为:一氯乙烷>一氯乙烯>一氯乙炔,同时Cl参与形成的大π键越多,形成的C-Cl键的键长
越短,一氯乙烯中Cl的3p 轨道与C的2p 轨道形成3中心4电子的大π键( ),一氯乙炔中Cl的3p 轨道
x x x
与C的2p 轨道形成2套3中心4电子的大π键( ),因此三种物质中C-Cl键键长顺序为:一氯乙烷>一氯乙
x
烯>一氯乙炔。
(3)CsICl 发生非氧化还原反应,各元素化合价不变,生成无色晶体和红棕色液体,则无色晶体为
2CsCl,红棕色液体为ICl,而CsCl为离子晶体,熔化时,克服的是离子键,ICl为分子晶体,熔化时,克服的
是分子间作用力,因此CsCl的熔点比ICl高。
(4)由题意可知,在电场作用下,Ag+不需要克服太大阻力即可发生迁移,因此α-AgI晶体是优良的离子
导体,在电池中可作为电解质;每个晶胞中含碘离子的个数为8×+1=2个,依据化学式AgI可知,银离子个数
也为2个,晶胞的物质的量n= mol= mol,晶胞体积V=a3pm3=(504×10-12)3m3,则α-AgI晶体的摩尔体积
V = = = m3/mol。
m
【变式探究】(2022·全国甲卷)2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立
方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH=CH )与四氟乙烯(CF=CF )的共聚物
2 2 2 2
(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______。
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化
图是_______(填标号),判断的根据是_______;第三电离能的变化图是_______(填标号)。
(3)固态氟化氢中存在(HF)n形式,画出(HF) 的链状结构_______。
3
(4) CF =CF 和ETFE分子中C的杂化轨道类型分别为_______和_______;聚四氟乙烯的化学稳定性高于聚
2 2
乙烯,从化学键的角度解释原因_______。
(5)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是_______;若该立方晶
2
胞参数为a pm,正负离子的核间距最小为_______pm。【答案】(1)
(2) 图a 同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p能级为半充满状态,因此
N元素的第一电离能较C、O两种元素高 图b
(3)
(4) sp2 sp3 C-F键的键能大于聚乙烯中C-H的键能,键能越大,化学性质越稳定
(5) Ca2+ a pm
【解析】根据基态原子的电子表示式书写价电子排布式;根据电离能的排布规律分析电离能趋势和原因;
根据氢键的表示方法书写(HF) 的结构;根据键能影响物质稳定性的规律分析两种物质的稳定性差异;根据均
3
摊法计算晶胞中各粒子的个数,判断粒子种类。
(1)F为第9号元素其电子排布为1s22s22p5,则其价电子排布图为 。
(2)C、N、O、F四种元素在同一周期,同一周期第一电离能的总体趋势是依次升高的,但由于N元素的
2p能级为半充满状态,因此N元素的第一电离能较C、O两种元素高,因此C、N、O、F四种元素的第一电
离能从小到大的顺序为C