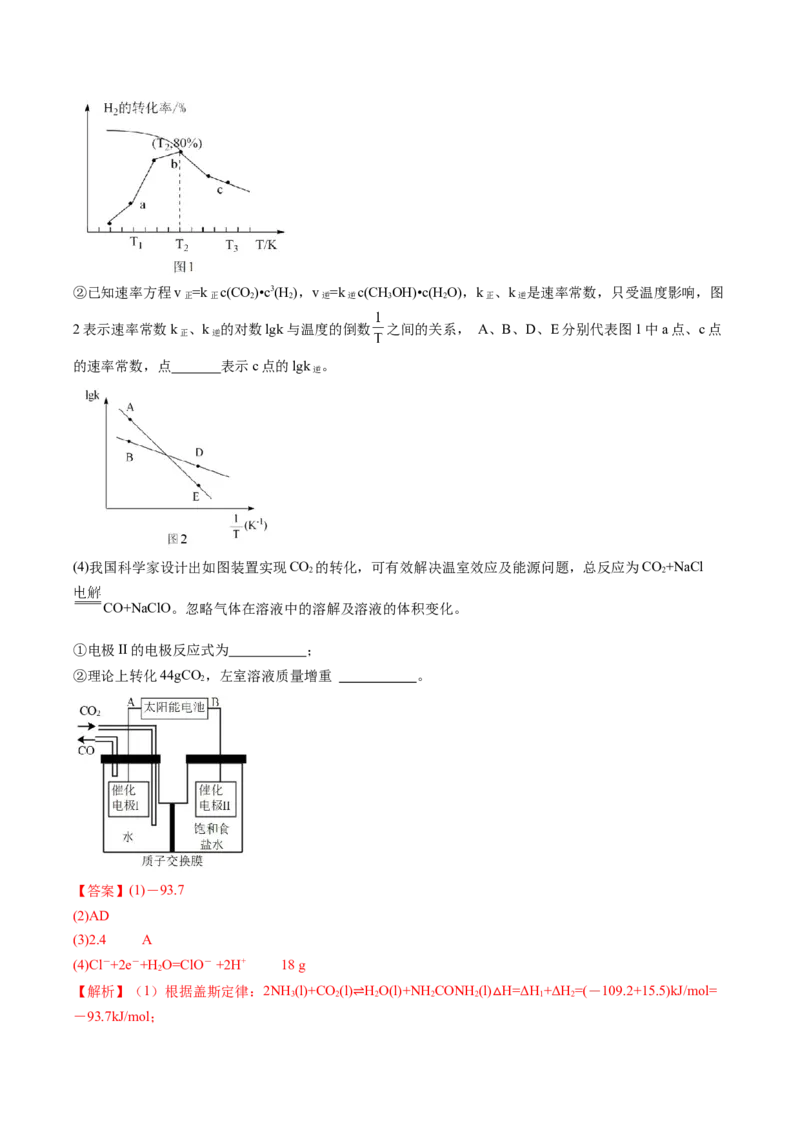
文档内容
专题 40 原理综合
(建议完成时间:45分钟 实际完成时间:_______分钟)
1.(2023·广西柳州·柳州高级中学校联考模拟预测)研究含氮元素物质的反应对生产、生活、科研等方面
具有重要的意义。
(1)NO 的排放主要来自于汽车尾气,包含NO 和NO,有人提出用活性炭对NO 进行吸收,发生如下反应:
x 2 x
C(s)+2NO(g) N(g)+CO (g) H=﹣34.0kJ/mol。对于反应T℃时,借助传感器测得反应在不同时间点上
2 2 1
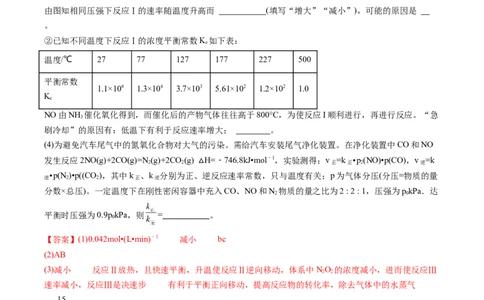
各物质的浓度如下:
△
0 10 20 30 40 50
NO 1.00 0.58 0.40 0.40 0.48 0.48
N 0 0.21 0.30 0.30 0.36 0.36
2
①0~10min内,NO的平均反应速率v(NO)= ,当升高反应温度,该反应的平衡常数K
(选填“增大”、“减小“或“不变”)。
②30min后。只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是
(填字母)。
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂。
(2)科研人员发现碘蒸气存在能大幅度提高NO的分解速率,反应历程为
2
第一步:I(g)→2I(g)(快反应)
2
第二步:I(g)+NO(g)→N (g)+IO(g)(慢反应)
2 2
第三步:2IO(g)+2N O(g)→2N (g)+2O(g)+I (g)(快反应)
2 2 2 2
实验表明,含碘时NO分解速率方程v=k•c(NO)•[(I )]0.5(k为速率常数),下列表述正确的是
2 2 2
(填字母)。
A.I(g)是反应的催化剂,I(g)浓度增大,NO分解反应速率增大
2 2 2
B.第二步是整个反应的决速步骤
C.I(g)能降低反应的焓变,从而化学反应速率增大
2
(3)工业生产硝酸的核心反应之一是在恒压装置中将NO转化为NO :
2
反应Ⅰ.NO(g)+ O(g) NO (g) H
2 2
目前认为反应Ⅰ分两步进行: △
反应Ⅱ.2NO(g) NO(g) H<0(快速平衡)
2 2
反应Ⅲ.N
2
O
2
(g)+O
2
(g) 2N△O
2
(g)
反应Ⅲ的速率方程为v=k•p(N O)•p(O )
2 2 2
1
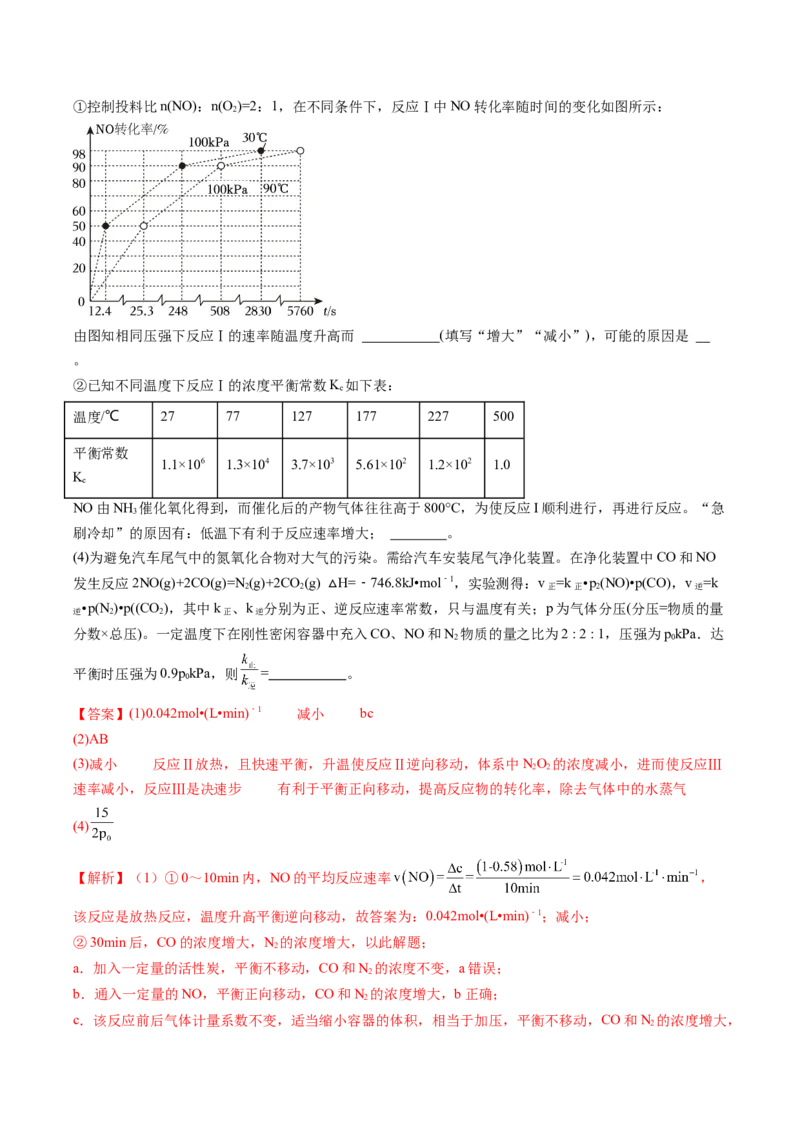
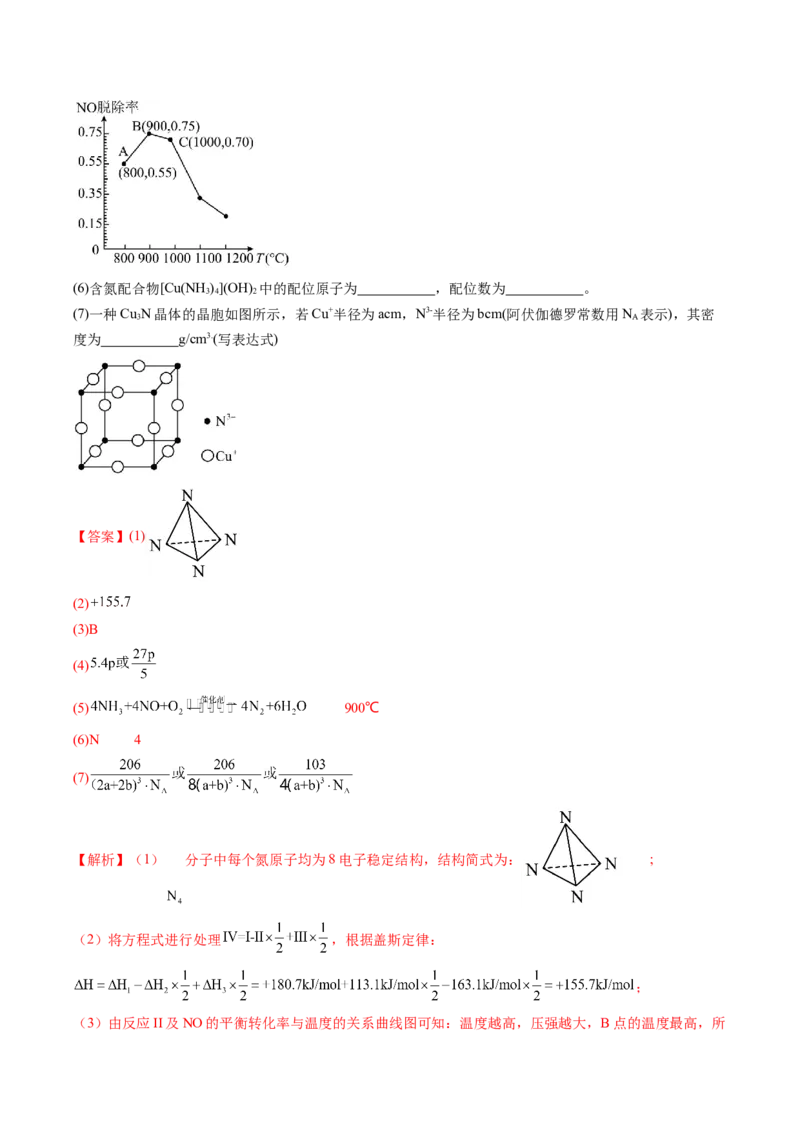
原创精品资源学科网独家享有版权,侵权必究!①控制投料比n(NO):n(O )=2:1,在不同条件下,反应Ⅰ中NO转化率随时间的变化如图所示:
2
由图知相同压强下反应Ⅰ的速率随温度升高而 (填写“增大”“减小”),可能的原因是
。
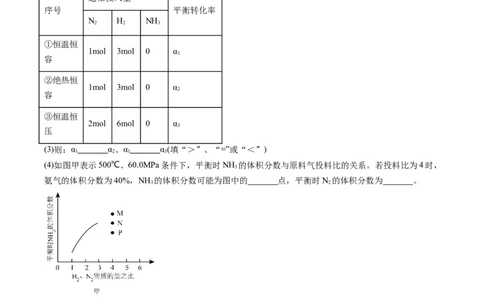
②已知不同温度下反应Ⅰ的浓度平衡常数K 如下表:
c
温度/℃ 27 77 127 177 227 500
平衡常数
1.1×106 1.3×104 3.7×103 5.61×102 1.2×102 1.0
K
c
NO由NH 催化氧化得到,而催化后的产物气体往往高于800°C,为使反应I顺利进行,再进行反应。“急
3
刷冷却”的原因有:低温下有利于反应速率增大; 。
(4)为避免汽车尾气中的氮氧化合物对大气的污染。需给汽车安装尾气净化装置。在净化装置中CO和NO
发生反应2NO(g)+2CO(g)=N (g)+2CO (g) H=﹣746.8kJ•mol﹣1,实验测得:v =k •p(NO)•p(CO),v =k
2 2 正 正 2 逆
•p(N )•p((CO ),其中k 、k 分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量
逆 2 2 正 逆 △
分数×总压)。一定温度下在刚性密闲容器中充入CO、NO和N 物质的量之比为2 : 2 : 1,压强为pkPa.达
2 0
平衡时压强为0.9pkPa,则 = 。
0
【答案】(1)0.042mol•(L•min)﹣1 减小 bc
(2)AB
(3)减小 反应Ⅱ放热,且快速平衡,升温使反应Ⅱ逆向移动,体系中NO 的浓度减小,进而使反应Ⅲ
2 2
速率减小,反应Ⅲ是决速步 有利于平衡正向移动,提高反应物的转化率,除去气体中的水蒸气
(4)
【解析】(1)①0~10min内,NO的平均反应速率 ,
该反应是放热反应,温度升高平衡逆向移动,故答案为:0.042mol•(L•min)﹣1;减小;
②30min后,CO的浓度增大,N 的浓度增大,以此解题;
2
a.加入一定量的活性炭,平衡不移动,CO和N 的浓度不变,a错误;
2
b.通入一定量的NO,平衡正向移动,CO和N 的浓度增大,b正确;
2
c.该反应前后气体计量系数不变,适当缩小容器的体积,相当于加压,平衡不移动,CO和N 的浓度增大,
2且增大的倍数相同,c正确;
d.加入合适的催化剂,不影响化学平衡,CO和N 的浓度不变,d错误;
2
故答案为:bc;
(2)由速率公式,即速率方程v=k•c(NO)•[(I )]0.2(k为速率常数),可知碘蒸气的浓度增大,NO分解反应
2 2 2
速率增大,
A.I(g)是反应的催化剂,I(g)浓度增大,NO分解反应速率增大,故A正确;
2 7 2
B.慢反应步骤是整个反应的决速步骤,第二步是整个反应的决速步骤,故B正确;
C.催化剂不改变反应的焓变,故C错误;
故选AB;
(3)(①由不同温度下的NO的转化率随着温度的变化示意图,相同压强条件下,低温条件下,在相同的
时间转化率最大,则反应速率大,温度低反应速率大,可能的原因是反应Ⅱ是放热反应,且快速平衡,升
温使反应Ⅱ逆向移动,体系中NO 的浓度减小,进而导致反应Ⅲ速率下降或者使反应Ⅲ的速率常数k的升
2 2
高不如NO 的浓度减小对其速率影响显著,故答案为:减小;反应Ⅱ放热,且快速平衡,升温使反应Ⅱ逆
2 2
向移动,体系中NO 的浓度减小,进而使反应Ⅲ速率减小,反应Ⅲ是决速步;
2 2
②由数据信息分析,反应放热,低温下有利于反应速率增大,冷凝水蒸气,同时有利于平衡向正向移动,
提高反应物的转化率,故答案为:有利于平衡正向移动,提高反应物的转化率,除去气体中的水蒸气;
(4)依据在净化装置中CO和NO发生反应,列出三段式:
,解得a = 0.1P,则该反应的压强平衡常数
0
。
2.(2023·江西·校联考模拟预测)I.如图为工业合成氨的流程图:
(1)图中采取的措施可提高原料转化率的是 (填序号)。
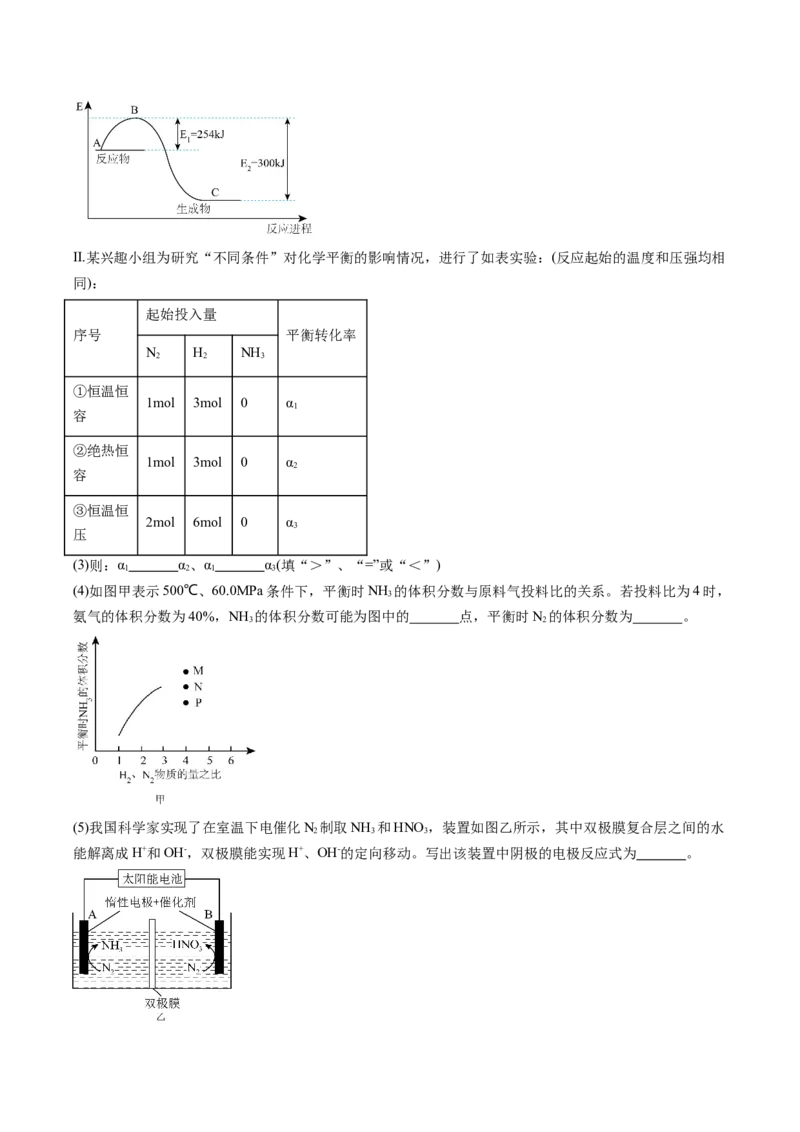
(2)如图是未用催化剂N(g)和H(g)反应生成1molNH (g)过程中能量的变化示意图,请在图中绘制同条件下
2 2 3
加入铁触媒后相应的能量变化曲线: ,并写出该条件下2molNH (g)分解对应的热化学方程式:
3
。II.某兴趣小组为研究“不同条件”对化学平衡的影响情况,进行了如表实验:(反应起始的温度和压强均相
同):
起始投入量
序号 平衡转化率
N H NH
2 2 3
①恒温恒
1mol 3mol 0 α
1
容
②绝热恒
1mol 3mol 0 α
2
容
③恒温恒
2mol 6mol 0 α
3
压
(3)则:α α 、α α (填“>”、“=”或“<”)
1 2 1 3
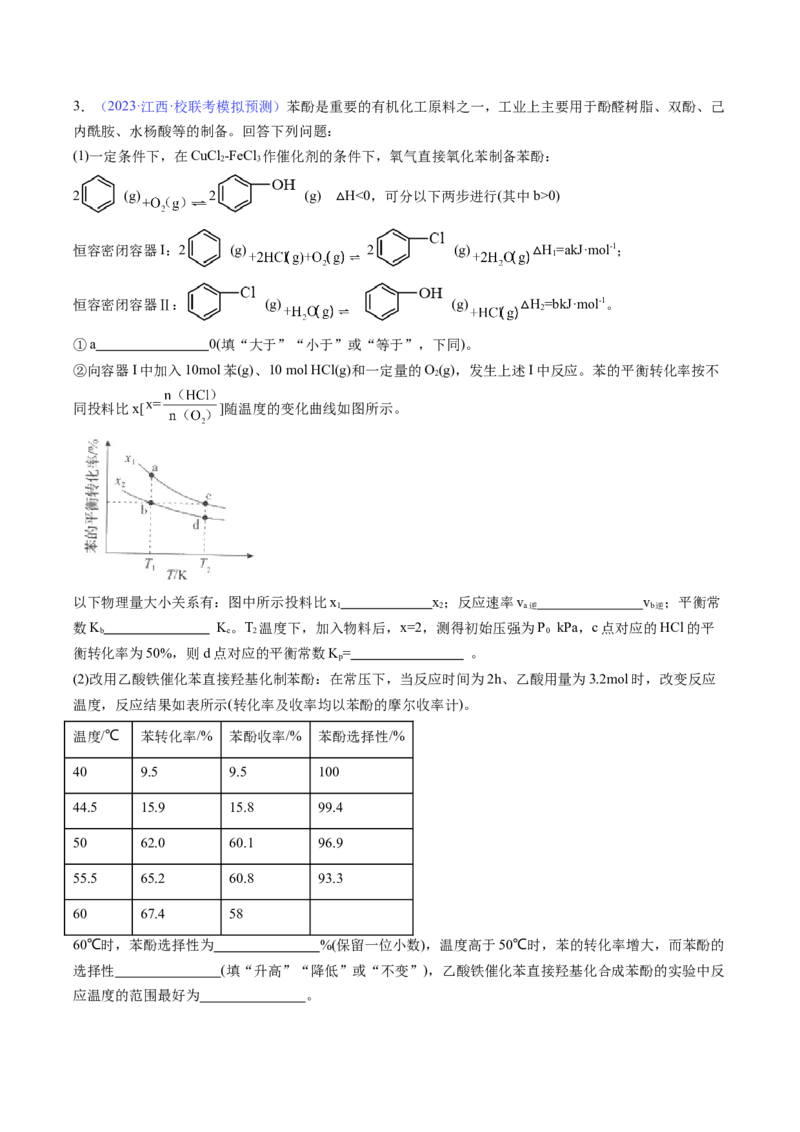
(4)如图甲表示500℃、60.0MPa条件下,平衡时NH 的体积分数与原料气投料比的关系。若投料比为4时,
3
氨气的体积分数为40%,NH 的体积分数可能为图中的 点,平衡时N 的体积分数为 。
3 2
(5)我国科学家实现了在室温下电催化N 制取NH 和HNO,装置如图乙所示,其中双极膜复合层之间的水
2 3 3
能解离成H+和OH-,双极膜能实现H+、OH-的定向移动。写出该装置中阴极的电极反应式为 。【答案】(1)②⑤⑥
(2) 2NH (g) N(g)+3H(g) H=+92kJ•mol-1
3 2 2
△
(3)> <
(4)P 8%
(5)N +6e-+6H+=2NH
2 3
【解析】(1)合成氨反应是气体体积减小的放热反应,增大压强和降低温度可以提高原料转化率,增大
反应物浓度或降低生成物浓度,也可以提高原料转化率;压缩机加压、将氨液化分离并将氮气和氢气送回
合成塔中都可以提高原料的转化率,故选②⑤⑥。
(2)铁触媒作为催化剂,能降低反应的活化能,则同条件下加入铁触媒后相应的能量变化曲线为
;从图中可以看出,1mol氨分解吸收300kJ-254kJ=46kJ的热
量,则2mol氨分解吸收92kJ的热量,热化学方程式为:2NH (g) N(g)+3H(g) H=+92kJ•mol-1。
3 2 2
(3)①和②比较:该反应放热,②中绝热,则②中温度升高,温度的升高会使平衡逆向移动,则α >α ;
△ 1 2
①和③比较:该反应为分子数减小的反应,恒容条件下,压强减小,会使平衡逆向移动,不利于氨气的生
成,则α <α 。
1 3
(4)合成氨反应中,当氢气和氮气的物质的量之比为方程式的系数比即3:1时,平衡时氨的体积分数最
大,所以投料比为4时,氨的体积分数减小,故为P点;设起始时投入的氢气为4mol,则氮气为1mol,设
转化的氮气为x mol,可列三段式:
,氨气的体积分数为40%,则有 ,x=
,氮气的体积分数为 =8%。
(5)在电解池中,阳离子向阴极移动,所以H+向阴极移动,在阴极,氮气得到电子生成氨气,则电极反
应式为N+6e-+6H+=2NH。
2 33.(2023·江西·校联考模拟预测)苯酚是重要的有机化工原料之一,工业上主要用于酚醛树脂、双酚、己
内酰胺、水杨酸等的制备。回答下列问题:
(1)一定条件下,在CuCl -FeCl 作催化剂的条件下,氧气直接氧化苯制备苯酚:
2 3
2 (g) 2 (g) H<0,可分以下两步进行(其中b>0)
△
恒容密闭容器I:2 (g) 2 (g) H=akJ·mol-1;
1
△
恒容密闭容器Ⅱ: (g) (g) H=bkJ·mol-1。
2
△
①a 0(填“大于”“小于”或“等于”,下同)。
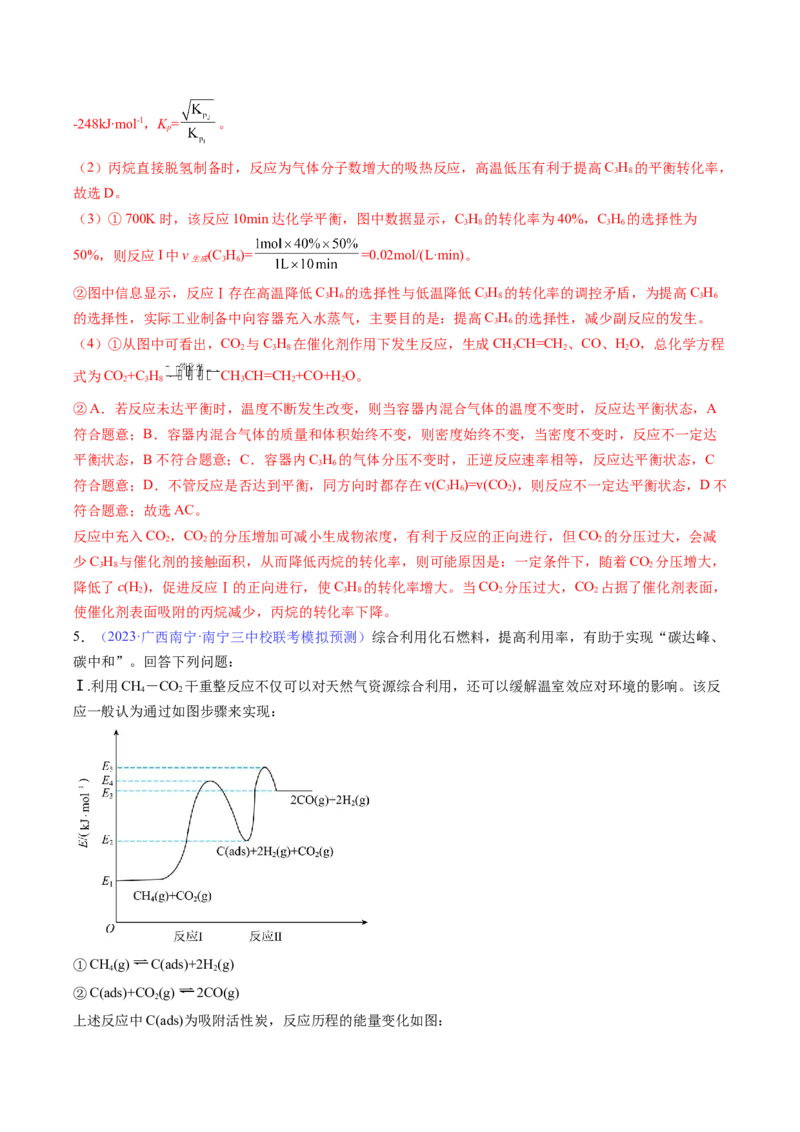
②向容器I中加入10mol苯(g)、10 mol HCl(g)和一定量的O(g),发生上述I中反应。苯的平衡转化率按不
2
同投料比x[ ]随温度的变化曲线如图所示。
以下物理量大小关系有:图中所示投料比x x;反应速率v v ;平衡常
1 2 a逆 b逆
数K K。T 温度下,加入物料后,x=2,测得初始压强为P kPa,c点对应的HCl的平
b c 2 0
衡转化率为50%,则d点对应的平衡常数K= 。
p
(2)改用乙酸铁催化苯直接羟基化制苯酚:在常压下,当反应时间为2h、乙酸用量为3.2mol时,改变反应
温度,反应结果如表所示(转化率及收率均以苯酚的摩尔收率计)。
温度/℃ 苯转化率/% 苯酚收率/% 苯酚选择性/%
40 9.5 9.5 100
44.5 15.9 15.8 99.4
50 62.0 60.1 96.9
55.5 65.2 60.8 93.3
60 67.4 58
60℃时,苯酚选择性为 %(保留一位小数),温度高于50℃时,苯的转化率增大,而苯酚的
选择性 (填“升高”“降低”或“不变”),乙酸铁催化苯直接羟基化合成苯酚的实验中反
应温度的范围最好为 。【答案】(1)小于 小于 大于 大于 (或 kPa-1)
(2)86.1 降低 50-55.5℃
【解析】(1)①根据盖斯定律I+Ⅱ得2 (g) 2 (g),△H=a+b<0 ,b>0,所
以a小于0。
②向容器I中加入10mol苯(g)、10 mol HClg)和一定量的O(g),增大氧气的物质的量,平衡正向移动,苯
2
的平衡转化率增大,a点对应苯的平衡转化率大于b点,则a点投入氧气的物质的量大,a点对应投料比小
于b点,故x”、“<”、“=”或“不确定”);B点时 的转化率=
(保留2位有效数字)。
(3)从图乙中获知反应Ⅰ存在着高温降低平衡产率与低温降低反应速率等调控矛盾。在提高合成氨的产率的
工业生产中,通常从以下多个视角来综合考虑合理的工业生产条件:
反应速率的视角:①加入催化剂;②提高温度(控制在催化剂的活性温度内)
平衡移动和原料的转化率的视角:③ ,④ 。
(4)科学家为避免直接破坏 键而消耗大量热能,通过新型催化剂降低了反应路径中决速步的能垒,使
该反应在常温、常压下采用电化学方法也能实现,反应装置如图所示,阴极上的电极反应式为
。
【答案】(1)+571.6
(2)0.075 = 82%
(3)增大压强 增大 的浓度
(4)
【解析】(1)依据盖斯定律可知Ⅰ×2+Ⅱ×3即得到反应2N(g)+6HO(l)=4NH (g)+3O(g),则
2 2 3 2;
故答案为:+571.6;
(2) ①反应前氮气浓度是mol/L,氢气浓度是1mol/L,0~10min内消耗氢气是浓度是1mol/L-0.25mol/L
=0.75mol/L,则 ;
故答案为:0.075;
②平衡常数只与温度有关系,则B、C两点的平衡常数K =K ,设B点时消耗氮气的物质的量是xmol,
B C
,此时氨气的体积分数是0.7,
,所以的转化率 ;
故答案为:=;82%;
(3)由于正反应是体积减小的放热反应,则从平衡移动和原料的转化率的视角应该是增大压强或增大的
浓度有利于平衡正向移动,可以提高氢气转化率;
故答案为:增大压强;增大 N 的浓度;
2
(4)阴极上氮气得到电子结合氢离子转化为氨气,电极反应式为 ;
故答案为: 。
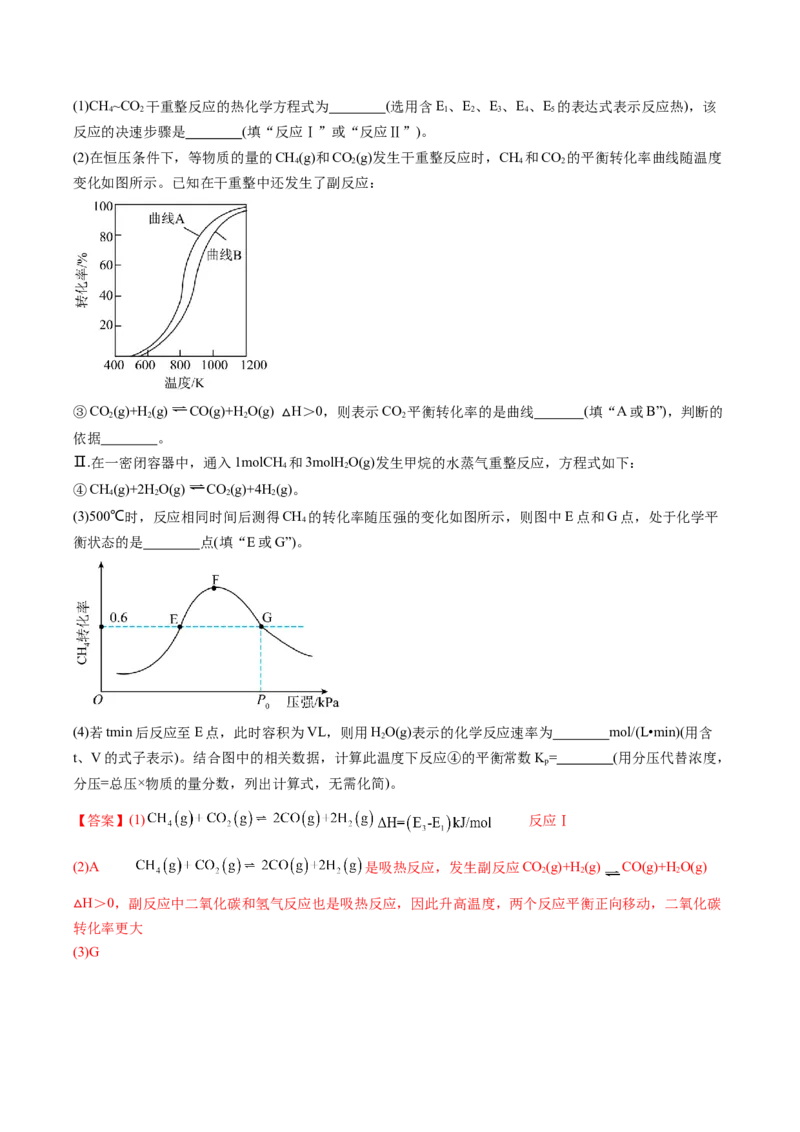
7.(2023·四川巴中·统考模拟预测)综合利用含碳资源、促进碳中和在保护生态环境等方面具有重要意义。
回答下列问题:
(1)中国科学院在国际上宣布首次实现CO 到淀粉的全合成,其中前两步涉及的反应如图1所示。
2
①反应:CO(g)+2H(g)=HCHO(g)+H O(g) H= (用△H、△H、△H、△H 表示)。
2 2 2 1 2 3 4
②反应I进行时,同时发生反应:2CO
2
(g)+△6H
2
(g) C
2
H
4
(g)+4H
2
O(g)。在1L恒容密闭容器中充入
4.0molCO 和6.0molH,一定温度下,达到平衡时,c(CO)=c(H O)=2.4mol/L,请回答下列问题:反应I的
2 2 2 2
平衡常数的表达式K= 。CHOH物质的量分数为 %(计算结果保留1位小数)。
3
(2)乙烯是合成工业的重要原料,一定条件下可发生反应:3C H(g) 2C H(g)分别在不同温度、不同催
2 4 3 6
化剂下,保持其他初始条件不变,重复实验,经相同时间测得C H 体积分数与温度的关系如图2所示。
2 4在催化剂甲作用下,图2中M点的速率V V (填“>”“<”或“=”),根据图中所给信息,应
正 逆
选择的反应条件为 。
(3)CO 氧化1-丁烯脱氢生产1,3-丁二烯,其反应原理为:CH=CHCHCH(g)
2 2 2 3
+CO (g)→CH =CHCH=CH (g)+HO(g)+CO(g)氧化脱氢反应可能的反应路径有两种,如图3所示:
2 2 2 2
①为确定反应路径,可检测反应体系中的物质是 (填化学式)。
②若为“两步路径”,在温度和总压相同时,1-丁烯氧化脱氢的平衡转化率高于直接脱氢的原因是
。
【答案】(1) H+ H+ H+ H 11.1
1 2 3 4
△ △ △ △
(2)< 催化剂乙、反应温度200℃
(3)H 通入CO 使容器体积增大,使平衡正向移动;CO 与H 反应,也使平衡向脱氢的方向移动
2 2 2 2
【解析】(1)①①CO(g)+3H(g)=HO(g)+CHOH(g) ΔH ;②CHOH(g)+O (g)=HO(l)+HCHO(g) ΔH ;
2 2 2 3 1 3 2 2 2 2
③2HO(l)=2H O(g)+O (g) ΔH ;④3HO(g)=3H (g)+ O(g) ΔH ,目标反应可由反应①+反应②+ ×反应
2 2 2 2 3 2 2 2 4
③+ ×反应④,ΔH= H+ H+ H+ H。
1 2 3 4
△ △ △ △②反应①CO(g)+3H(g)=HO(g)+CHOH(g),其平衡常数表达式K= 。设反应①消耗
2 2 2 3
COxmol,反应2CO(g)+6H(g) C H(g)+4HO(g)消耗COymol,则x+y=1.6mol,x+2y=2.4mol,解得
2 2 2 2 4 2 2
x=0.8mol,y=0.8mol。则平衡时各物质的物质的量为n(CO)=2.4mol,n(H O)=2.4mol,n(H )=1.2mol,
2 2 2
n(CHOH)=0.8mol,n(C H)=0.4mol,则甲醇的物质的量分数为0.8÷7.2=11.1%。
3 2 4
(2)从图中可知,M点C H 的体积分数呈增大的趋势,说明此时反应逆向进行,V