文档内容
物质结构与性质应用推理集训
1.(2024·黑吉辽,2)下列化学用语或表述正确的是( )
A.中子数为1的氦核素:1He
2
B.SiO 的晶体类型:分子晶体
2
C.F
2
的共价键类型:p⁃p σ键
D.PCl 的空间结构:平面三角形
3
2.(2024·湖北,5)基本概念和理论是化学思维的基石。下列叙述错误的是( )
A.VSEPR理论认为VSEPR模型与分子的空间结构相同
B.元素性质随着原子序数递增而呈周期性变化的规律称为元素周期律
C.泡利原理认为一个原子轨道内最多只能容纳两个自旋相反的电子
D.sp3杂化轨道由1个s轨道和3个p轨道混杂而成
3.(2023·湖南,4)下列有关物质结构和性质的说法错误的是( )
A.含有手性碳原子的分子叫做手性分子
B.邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
C.酰胺在酸或碱存在并加热的条件下可发生水解反应
D.冠醚(18⁃ 冠 ⁃6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子
4.(2024·湖南,4)下列有关化学概念或性质的判断错误的是( )
A.CH 分子是正四面体结构,则CH Cl 没有同分异构体
4 2 2
B.环己烷与苯分子中C—H键的键能相等
C.甲苯的质谱图中,质荷比为92的峰归属于
D.由R
N+与PF-
组成的离子液体常温下呈液态,与其离子的体积较大有关
4 6
5.(2024·河北,8)从微观视角探析物质结构及性质是学习化学的有效方法。下列实例与解释不符的是(
)
选项 实例 解释
A 原子光谱是不连续的线状谱线 原子的能级是量子化的
孤电子对与成键电子对的斥力大于成键电子对
B CO 、CH O、CCl 键角依次减小
2 2 4
之间的斥力
CsCl晶体中Cs+与8个Cl-配位,而
C Cs+比Na+的半径大
NaCl晶体中Na+与6个Cl-配位
D 逐个断开CH 中的C—H键,每步 各步中的C—H键所处化学环境不同
4所需能量不同
6.(2024·河北,9)NH ClO 是火箭固体燃料重要的氧载体,与某些易燃物作用可全部生成气态产物,如:
4 4
NH ClO +2C===NH ↑+2CO ↑+HCl↑。下列有关化学用语或表述正确的是( )
4 4 3 2
·· ··
A.HCl的形成过程可表示为H·+·Cl· ―→H+[ · Cl· ]-
· × ·
·· ··
B.NH ClO 中的阴、阳离子有相同的VSEPR模型和空间结构
4 4
C.在C 、石墨、金刚石中,碳原子有sp、sp2和sp3三种杂化方式
60
D.NH 和CO 都能作制冷剂是因为它们有相同类型的分子间作用力
3 2
7.(2024·湖北,8)结构决定性质,性质决定用途。下列事实解释错误的是( )
事实
解释
A
甘油是黏稠液体
甘油分子间的氢键较强
B
王水溶解铂
浓盐酸增强了浓硝酸的氧化性
C
冰的密度小于干冰
冰晶体中水分子的空间利用率相对较低
D
石墨能导电
未杂化的p轨道重叠使电子可在整个碳原子平面内运动
8.(2023·湖北,9)价层电子对互斥理论可以预测某些微粒的空间结构。下列说法正确的是( )
A.CH 和H O的VSEPR模型均为四面体
4 2
B.SO2-和CO2-的空间构型均为平面三角形
3 3
C.CF 和SF 均为非极性分子
4 4
D.XeF 与XeO 的键角相等
2 2
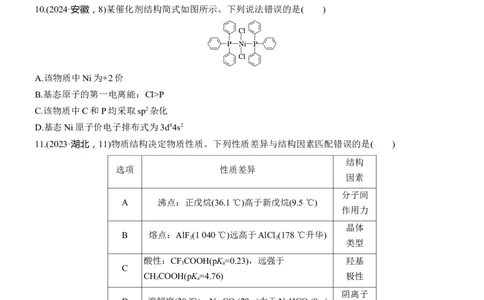
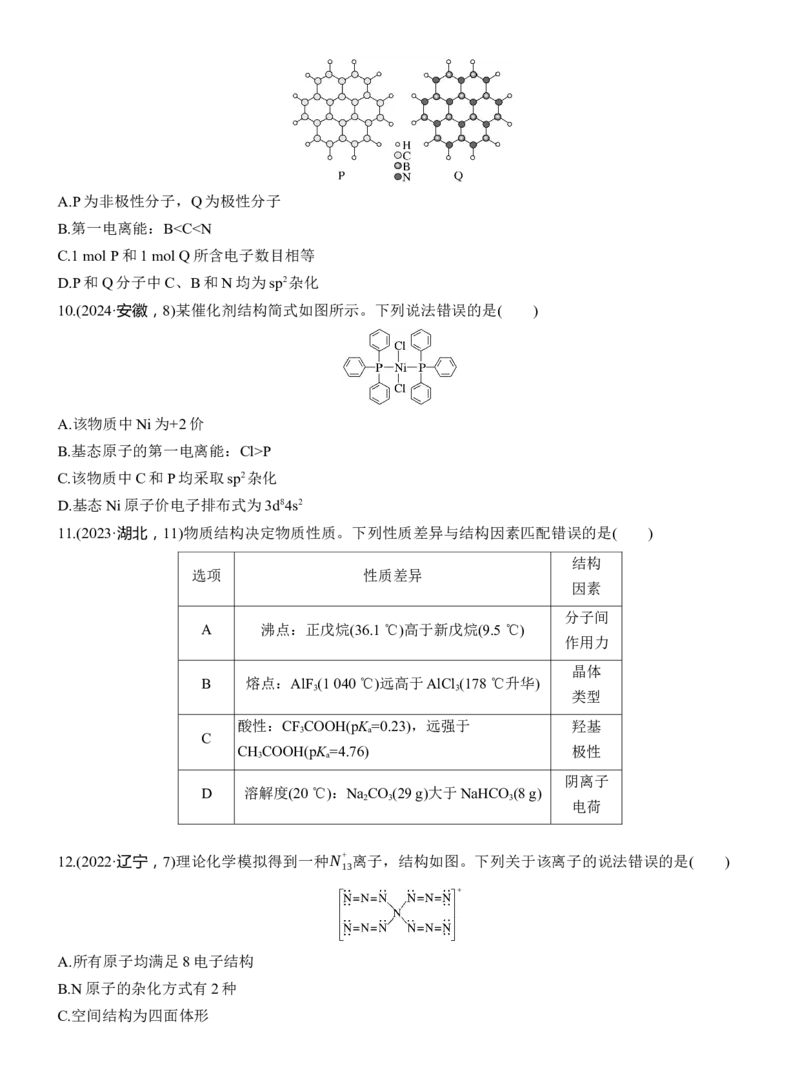
9.(2024·湖南,9)通过理论计算方法优化了P和Q的分子结构,P和Q呈平面六元并环结构,原子的连
接方式如图所示,下列说法错误的是( )A.P为非极性分子,Q为极性分子
B.第一电离能:BP
C.该物质中C和P均采取sp2杂化
D.基态Ni原子价电子排布式为3d84s2
11.(2023·湖北,11)物质结构决定物质性质。下列性质差异与结构因素匹配错误的是( )
结构
选项 性质差异
因素
分子间
A 沸点:正戊烷(36.1 ℃)高于新戊烷(9.5 ℃)
作用力
晶体
B 熔点:AlF (1 040 ℃)远高于AlCl (178 ℃升华)
3 3
类型
酸性:CF COOH(pK=0.23),远强于 羟基
3 a
C
CH COOH(pK=4.76) 极性
3 a
阴离子
D 溶解度(20 ℃):Na CO (29 g)大于NaHCO (8 g)
2 3 3
电荷
12.(2022·辽宁,7)理论化学模拟得到一种N+
离子,结构如图。下列关于该离子的说法错误的是( )
13
A.所有原子均满足8电子结构
B.N原子的杂化方式有2种
C.空间结构为四面体形D.常温下不稳定答案精析
1.C [中子数为1的He核素其质量数为1+2=3,故应表示为
3
He,A错误;两个F原子中2p轨道单电子
2
相互重叠形成p⁃p σ键,C正确;PCl
3
的中心原子价层电子对数为4,存在1个孤电子对,其VSEPR模型为
四面体形,PCl 的空间结构为三角锥形,D错误。]
3
2.A [VSEPR模型是价层电子对的空间结构模型,而分子的空间结构指的是成键电子对的空间结构,不包
括孤电子对,当中心原子无孤电子对时,两者空间结构相同,当中心原子有孤电子对时,两者空间结构不
同,故A错误;在一个原子轨道内,最多只能容纳2个电子,它们的自旋相反,这个原理被称为泡利原理,
故C正确;1个s轨道和3个p轨道混杂形成4个能量相同、方向不同的轨道,称为sp3杂化轨道,故D正
确。]
3.A [有手性异构体的分子被称为手性分子,A错误;邻羟基苯甲醛中含有分子内氢键,分子内氢键可以
降低物质的熔、沸点,因此邻羟基苯甲醛的熔、沸点低于对羟基苯甲醛的熔、沸点,B正确;超分子是由
两种或两种以上的分子通过分子间相互作用形成的分子聚集体,冠醚(18⁃冠⁃6)的空穴大小为260~320 pm,
可以适配K+(276 pm),冠醚与K+之间通过弱相互作用结合,D正确。]
4.B [CH Cl 为四面体结构,任何两个顶点都相邻,故CH Cl 没有同分异构体,故A正确;环己烷中碳原
2 2 2 2
子采用sp3杂化,苯分子中碳原子采用sp2杂化,由于同能层中s轨道更接近原子核,因此杂化轨道的s成
分越多,其杂化轨道更接近原子核,由此可知sp2杂化轨道参与组成的C—H共价键的电子云更偏向碳原子
核,即苯分子中的C—H键长小于环己烷,键能更高,故B错误; 带1个单位正电荷,其相
对分子质量为92,其质荷比为92,故C正确;当阴、阳离子体积较大时,其电荷较为分散,离子键作用
力较弱,以至于熔点接近室温,故D正确。]
5.B [CO 、CH O、CCl 的中心C原子都无孤电子对,故不能用孤电子对与成键电子对的斥力大于成键电
2 2 4
子对之间的斥力解释CO 、CH O、CCl 键角依次减小,B错误;离子晶体的配位数取决于正、负离子半径
2 2 4
比,离子半径比越大,配位数越大,Cs+周围最多能排布8个Cl-,Na+周围最多能排布6个Cl-,说明Cs+比
Na+半径大,故C正确;断开CH 的C—H键越多,碳原子周围共用电子对越少,原子核对共用电子对的吸
4
引力越大,需要的能量越大,所以各步中的C—H键所处化学环境不同,每步所需能量不同,故D正确。]
·· ·· ··
6.B
[HCl是共价化合物,其电子式为H·Cl· ,HCl的形成过程可表示为H·+·Cl· H·Cl·
,A错误;
· · · · ·
·· ·· ··
1
NH ClO 中N H+ 的中心N原子的孤电子对数为 ×(5-1-4)=0,价层电子对数为4,ClO- 的中心Cl原子的孤
4 4 4 2 4
1
电子对数为 ×(7+1-2×4)=0,价层电子对数为4,则二者的VSEPR模型和空间结构均为正四面体形,B正
2
确;C 、石墨、金刚石中碳原子的杂化方式分别为sp2、sp2、sp3,C错误;NH 易液化,液氨汽化时吸收
60 3大量热量,可作制冷剂,干冰易升华,升华时吸收大量热量,也可作制冷剂,NH 分子间作用力为氢键和
3
范德华力,CO 分子间作用力为范德华力,D错误。]
2
7.B [甘油分子中有3个羟基,分子间可以形成更多的氢键,且O元素的电负性较大,故其分子间形成的
氢键较强,因此甘油是黏稠液体,A正确;王水溶解铂,主要是因为浓盐酸提供的Cl-能与被硝酸氧化产生
的高价态的铂离子形成稳定的配合物从而促进铂的溶解,B不正确;冰晶体中水分子间形成较多的氢键,
氢键的方向性导致水分子间形成氢键后空隙变大,冰晶体中水分子的空间利用率相对较低,密度小于干冰,
C正确;在石墨晶体结构中,每个碳原子用3个价电子通过sp2杂化轨道与相邻的碳原子形成共价键,还有
1个价电子处于碳原子的未杂化的2p轨道上,层内碳原子的这些p轨道相互平行,相邻碳原子p轨道相互
重叠形成大π键,这些p轨道的电子可以在整个层内运动,因此石墨能导电,D正确。]
8.A [甲烷分子的中心原子的价层电子对数为4,水分子的中心原子价层电子对数也为4,所以VSEPR模
型均为四面体,A正确;SO2- 中中心原子的孤电子对数为1,CO2-
中中心原子的孤电子对数为0,所以S
3 3
O2- 的空间构型为三角锥形,CO2-
的空间构型为平面三角形,B错误;CF 为正四面体结构,为非极性分子,
3 3 4
SF 中心原子有孤电子对,为极性分子,C错误;XeF 和XeO 分子中,中心原子孤电子对数不相等,所以
4 2 2
键角不等,D错误。]
9.A [由题给分子结构图,P和Q分子都满足对称,正、负电中心均重合,都是非极性分子,A错误;同
周期从左到右,元素的第一电离能呈增大趋势,氮原子的2p轨道为稳定的半充满结构,第一电离能大于
相邻元素,则第一电离能由小到大的顺序为BP,B项正确;C
均存在于苯环上,采取sp2杂化,P价层电子对数为4,采取sp3杂化,C项错误;Ni的原子序数为28,位
于第四周期第Ⅷ族,基态Ni原子价电子排布式为3d84s2,D项正确。]
11.D [由于新戊烷支链多,对称性好,分子间作用力小,所以沸点较低,故A正确;AlF 为离子晶体,熔
3
点较高,AlCl 为分子晶体,熔点较低,则AlF 熔点远高于AlCl ,故B正确;由于电负性:F>H,C—F键
3 3 3
极性大于C—H键,使得羧基上的羟基极性增强,氢原子更容易电离,酸性增强,故C正确;碳酸氢钠在
水中的溶解度比碳酸钠小的原因是碳酸氢钠晶体中HCO-
间存在氢键,导致其不易溶于水,与阴离子电荷
3
无关,故D错误。]
12.B
[由N+
的结构式可知,所有N原子均满足8电子稳定结构,A正确;中心N原子为sp3杂化,与中心
13
N原子直接相连的N原子为sp2杂化,与端位N原子直接相连的N原子为sp杂化,端位N原子为sp2杂化,则N原子的杂化方式有3种,B错误;中心N原子为sp3杂化,则其空间结构为四面体形,C正确;N+
中
13
‥
N
含— ==N==N,常温下不稳定,D正确。]
‥
‥