文档内容
专题三 无机化学工艺流程
【考情分析】
命题点 五年考情 分析解读
2018·全国Ⅰ,T 化学工艺流程题是将化工生产中的
27
以物质制备为主线的 生产流程用框图形式表示出来,并
2018·全国Ⅲ,T
化学工艺流程 27 根据生产流程中有关的化学知识步
2017·全国Ⅲ,T 步设问,是无机框图的创新。它以
27
现代工业生产为基础,与化工生产
成本、产品提纯、环境保护等相融
2018·全国Ⅱ,T
26 合,考查物质的制备、检验、分离或
以分离提纯为主线的 提纯等基本实验原理在化工生产中
2017·全国Ⅰ,T
化学工艺流程 27 的实际应用,具有较强的实用性和
2016·全国Ⅲ,T 综合性,是近几年高考化学试题的
28
常考题型。
1.工艺流程题过程解读
(1)读流程图
①箭头:箭头进入的是投料(反应物)、出去的是主产物或副产物(生成物)。
②三线:出线和进线均表示物料流向或操作流程,可逆线表示物质循环。
(2)解题要点
①审题要点:a.了解生产目的、原料及产品,b.了解题目提供的信息,c.分析各步的
反应条件、原理及物质成分,d.理解物质分离、提纯、条件控制等操作的目的及要
点。
②答题切入点:a.原料及产品的分离提纯,b.生产目的及反应原理,c.生产要求及反
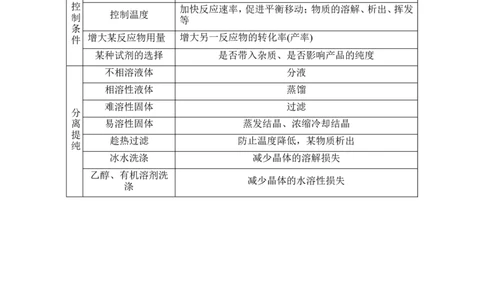
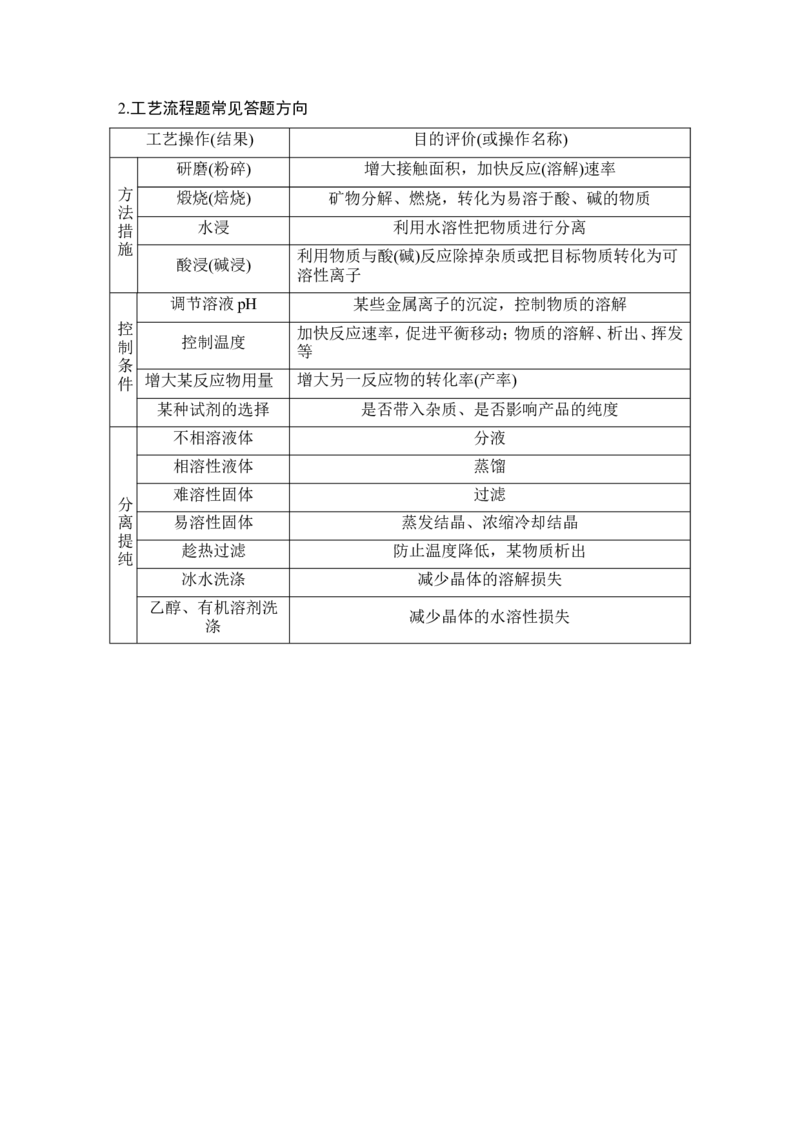
应条件,d.有关产率、产量及组成的计算,e.绿色化学。2.工艺流程题常见答题方向
工艺操作(结果) 目的评价(或操作名称)
研磨(粉碎) 增大接触面积,加快反应(溶解)速率
方 煅烧(焙烧) 矿物分解、燃烧,转化为易溶于酸、碱的物质
法
措 水浸 利用水溶性把物质进行分离
施
利用物质与酸(碱)反应除掉杂质或把目标物质转化为可
酸浸(碱浸)
溶性离子
调节溶液pH 某些金属离子的沉淀,控制物质的溶解
控
加快反应速率,促进平衡移动;物质的溶解、析出、挥发
控制温度
制
等
条
件 增大某反应物用量 增大另一反应物的转化率(产率)
某种试剂的选择 是否带入杂质、是否影响产品的纯度
不相溶液体 分液
相溶性液体 蒸馏
难溶性固体 过滤
分
离 易溶性固体 蒸发结晶、浓缩冷却结晶
提
趁热过滤 防止温度降低,某物质析出
纯
冰水洗涤 减少晶体的溶解损失
乙醇、有机溶剂洗
减少晶体的水溶性损失
涤考点指导1 以物质制备为目的化学工艺流程
【典例1】
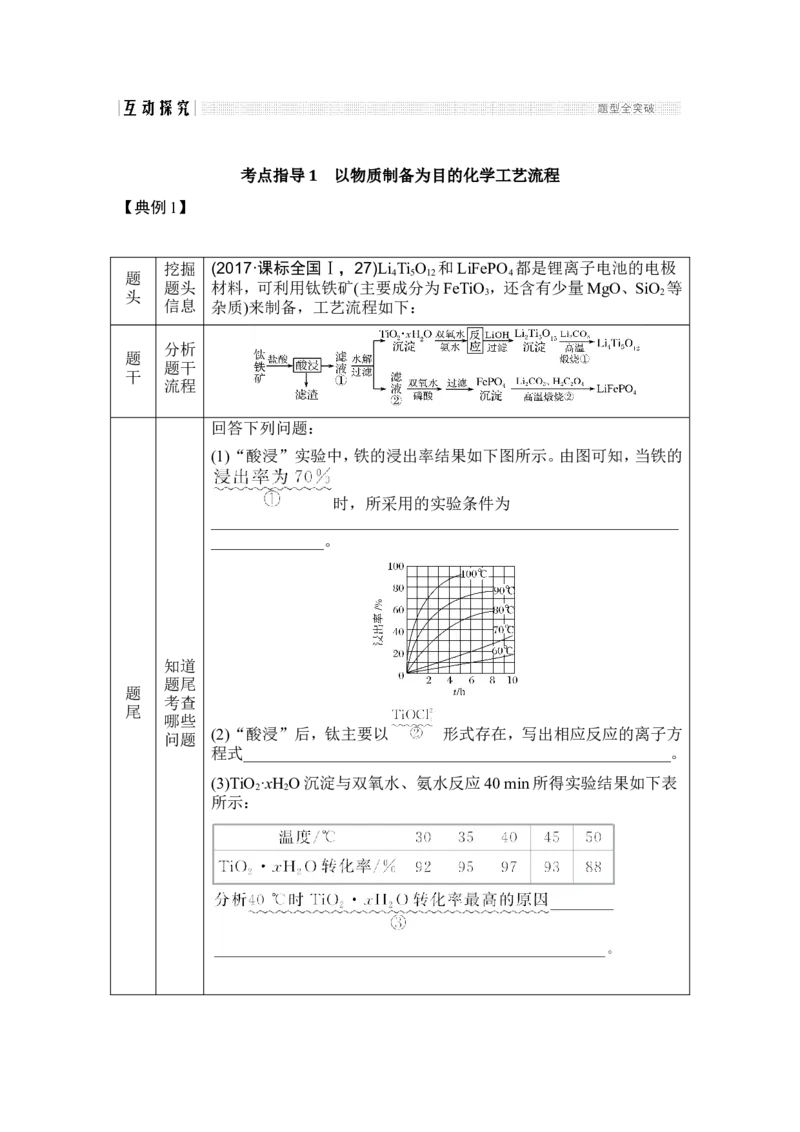
挖掘 (2017·课标全国Ⅰ,27)Li Ti O 和LiFePO 都是锂离子电池的电极
题 4 5 12 4
题头 材料,可利用钛铁矿(主要成分为FeTiO ,还含有少量MgO、SiO 等
头 3 2
信息 杂质)来制备,工艺流程如下:
分析
题
题干
干
流程
回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的
时,所采用的实验条件为
__________________________________________________________
______________。
知道
题尾
题
考查
尾
哪些
(2)“酸浸”后,钛主要以 形式存在,写出相应反应的离子方
问题
程式_____________________________________________________。
(3)TiO ·xH O沉淀与双氧水、氨水反应40 min所得实验结果如下表
2 2
所示:(4)Li Ti O 中Ti的化合价为+4,其中 为
2 5 15
________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol·L-1,加入双氧水和磷酸(设溶
液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1.0×
知道
10-5 mol·L-1,此时是否有Mg (PO ) 沉淀生成?
题尾 3 4 2
题
__________________________________________________________
考查
尾
哪些
_(列式计算)。
问题
(6)
写出“高温煅烧②”中由 的化学方程式
______________________________________________________。
【审题指导】
①分析图像,浸出率达到70%只有90 ℃、100 ℃两条曲线。
②反应物FeTiO +H++Cl-,生成物TiOCl+Fe2+,结合原子守恒和电荷守恒写出
3
离子方程式。
③可以从温度、浓度、压强等方面考虑转化率的因素,结合考虑双氧水在高温下易
分解、氨水中氨气会逸出。
④找出元素的常规价态,Li为+1价,O为-2价,Ti为+4价,O中O为-1价,化
学式变形为Li Ti (O ) O ,从化合价的代数和为零作答 2+4×5-2x-2(15-
2 5 2 x 15-2x
2x)=0,计算得出结果x=4。
⑤由K 公式入手计算,Q 与K 的关系得出结论。
sp c sp
⑥流程题已经给出化学反应的反应物是FePO 和Li CO 、草酸,生成物LiFePO ,
4 2 3 4
分析化合价变化的元素,结合原子守恒和得失电子守恒写出方程式。
【答题规范】
(1)100 ℃、2 h或90 ℃、5 h
(2)FeTiO + 4H++ 4Cl-===Fe2++TiOCl+2H O
3 2
(3)低于40 ℃,TiO ·xH O转化率随温度升高而增加;超过40 ℃,双氧水分解与氨
2 2
气逸出导致TiO ·xH O转化率下降
2 2
(4)4
(5)Fe3+恰好沉淀完全时, c(PO)= mol·L-1=1.3×10-17mol·L-1。c3(Mg2+)·c2(PO)值为0.013×(1.3×10-17)2=1.7×10-40”或“<”)。
3 4 2 4
②结合元素周期律解释①中结论:P和S电子层数相同,
____________________________________________________________________。
(3)酸浸时,磷精矿中Ca (PO ) F所含氟转化为HF,并进一步转化为SiF 除去。写
5 4 3 4
出生成HF的化学方程式:
____________________________________________________________________。
(4)H O 将粗磷酸中的有机碳氧化为CO 脱除,同时自身也会发生分解。相同投料
2 2 2
比、相同反应时间,不同温度下的有机碳脱除率如图所示。80 ℃后脱除率变化的原
因:_______________________________________________________。
(5) 脱 硫 时 , CaCO 稍 过 量 , 充 分 反 应 后 仍 有 SO 残 留 , 原 因 是
3
____________________________________________________________________;
加入BaCO 可进一步提高硫的脱除率,其离子方程式是
3______________________________________________________________________
____________________________________________________________________。
(6)取a g所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用 b mol·L-
1NaOH 溶液滴定至终点时生成 Na HPO ,消耗 NaOH 溶液 c mL。精制磷酸中
2 4
H PO 的质量分数是________。(已知:H PO 摩尔质量为98 g·mol-1)
3 4 3 4
解析 (1)流程中能加快反应速率的措施有将磷精矿研磨,酸浸时进行加热。(2)①
该反应符合复分解反应中“强酸制弱酸”的规律。②比较硫酸与磷酸的酸性强弱,
可以比较S与P的非金属性强弱。结合元素周期律可以比较S、P的原子半径、核
电荷数。(3)根据质量守恒可写出反应的化学方程式。(4)有机碳的脱除率受两个因
素的共同影响:一方面,温度越高,反应速率越快,在相同投料比、相同反应时间内
有机碳的脱除率越高;另一方面,温度升高可使较多的H O 分解,氧化剂的量减
2 2
少,使得有机碳的脱除率降低。80 ℃后,H O 分解对有机碳脱除率的影响超过了
2 2
温度升高的影响,导致脱除率逐渐降低。(5)脱硫是用CaCO 除去剩余的硫酸,由
3
于生成的硫酸钙是微溶物,所以即使CaCO 过量,充分反应后仍有SO残留。加入
3
BaCO 可使CaSO 转化为更难溶的BaSO ,进一步提高硫的脱除率。
3 4 4
(6) H PO + 2NaOH===Na HPO +2H O
3 4 2 4 2
98 g 2 mol
m(H PO ) 10-3bc mol
3 4
m(H PO )=4.9×10-2bc g,则精制磷酸中H PO 的质量分数为×100%=%。
3 4 3 4
答案 (1)研磨、加热
(2)①< ②核电荷数PS,得电子能力P