文档内容
2025新教材化学高考第一轮
专题九 化学反应的热效应
1.下列说法正确的是( )
1
A.2Na(s)+ O (g) Na O(s) ΔH ,2Na(s)+O (g) Na O (s) ΔH ,则ΔH >ΔH
2 2 1 2 2 2 2 1 2
2
B.H 的摩尔燃烧焓为-285.8 kJ·mol-1,则2H (g)+O (g) 2H O(g) ΔH=-571.6 kJ·mol-1
2 2 2 2
C.3O (g) 2O (g) ΔH>0,则完全破坏等质量的O 和O 中的化学键,O 需要的能量大
2 3 2 3 3
D.N (g)+3H (g) 2NH (g) ΔH=-92.4 kJ·mol-1,则28 g N 与足量H 反应放热92.4 kJ
2 2 3 2 2
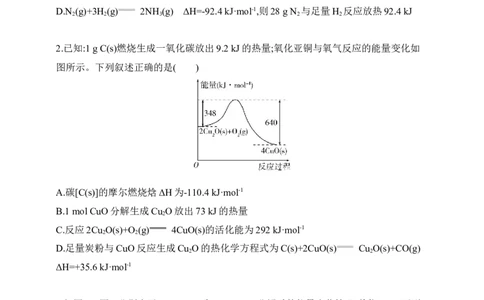
2.已知:1 g C(s)燃烧生成一氧化碳放出9.2 kJ的热量;氧化亚铜与氧气反应的能量变化如
图所示。下列叙述正确的是( )
A.碳[C(s)]的摩尔燃烧焓ΔH为-110.4 kJ·mol-1
B.1 mol CuO分解生成Cu O放出73 kJ的热量
2
C.反应2Cu O(s)+O (g) 4CuO(s)的活化能为292 kJ·mol-1
2 2
D.足量炭粉与CuO反应生成Cu O的热化学方程式为C(s)+2CuO(s) Cu O(s)+CO(g)
2 2
ΔH=+35.6 kJ·mol-1
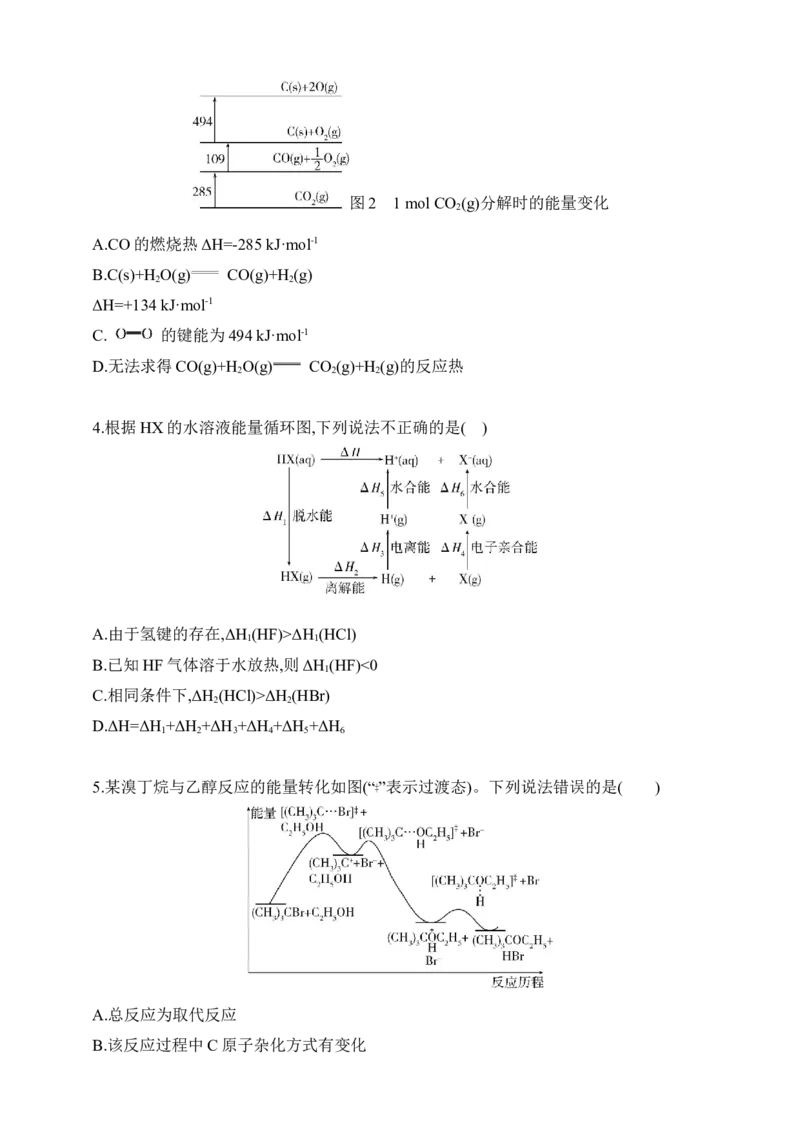
3.如图1、图2分别表示1 mol H O和1 mol CO 分解时的能量变化情况(单位:kJ)。下列
2 2
说法错误的是( )
图1 1 mol H O(g)分解时的能量变化
2图2 1 mol CO (g)分解时的能量变化
2
A.CO的燃烧热ΔH=-285 kJ·mol-1
B.C(s)+H O(g) CO(g)+H (g)
2 2
ΔH=+134 kJ·mol-1
C. 的键能为494 kJ·mol-1
D.无法求得CO(g)+H O(g) CO (g)+H (g)的反应热
2 2 2
4.根据HX的水溶液能量循环图,下列说法不正确的是( )
A.由于氢键的存在,ΔH (HF)>ΔH (HCl)
1 1
B.已知HF气体溶于水放热,则ΔH (HF)<0
1
C.相同条件下,ΔH (HCl)>ΔH (HBr)
2 2
D.ΔH=ΔH +ΔH +ΔH +ΔH +ΔH +ΔH
1 2 3 4 5 6
5.某溴丁烷与乙醇反应的能量转化如图(“”表示过渡态)。下列说法错误的是( )
A.总反应为取代反应
B.该反应过程中C原子杂化方式有变化C.适当升温,(CH ) COC H 产率增大
3 3 2 5
D.该过程正、逆反应的决速步骤不同
6.750 ℃时,NH 和O 发生以下两个反应:
3 2
①4NH (g)+5O (g) 4NO(g)+6H O(g) ΔH
3 2 2 1
②4NH (g)+3O (g) 2N (g)+6H O(g) ΔH
3 2 2 2 2
下列说法正确的是( )
A.反应①的平衡常数可表示为K =
c4(NO)
1
c4(NH )·c5(O )
3 2
B.反应②的ΔS<0
C.反应①中每生成2 mol NO,转移电子数约为6.02×1024
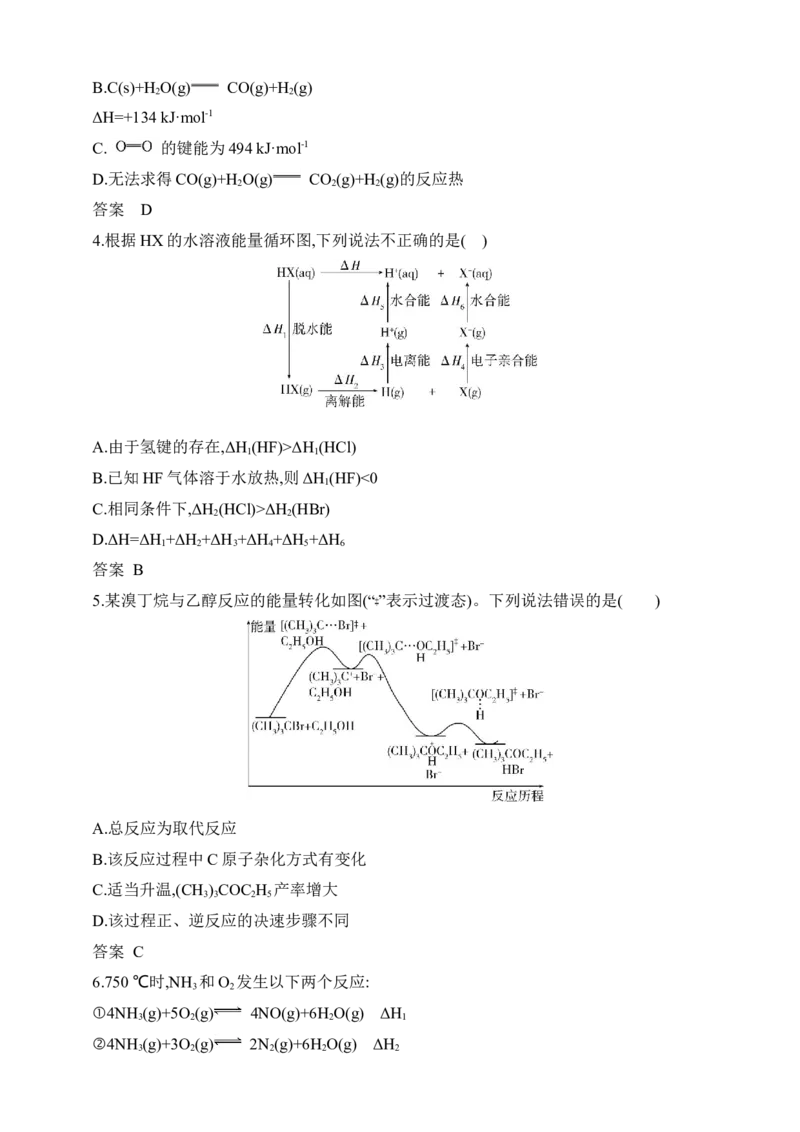
D.反应②的ΔH =2E( )+12E(H—O)-12E(N—H)-3E( )(E表示键能)
2
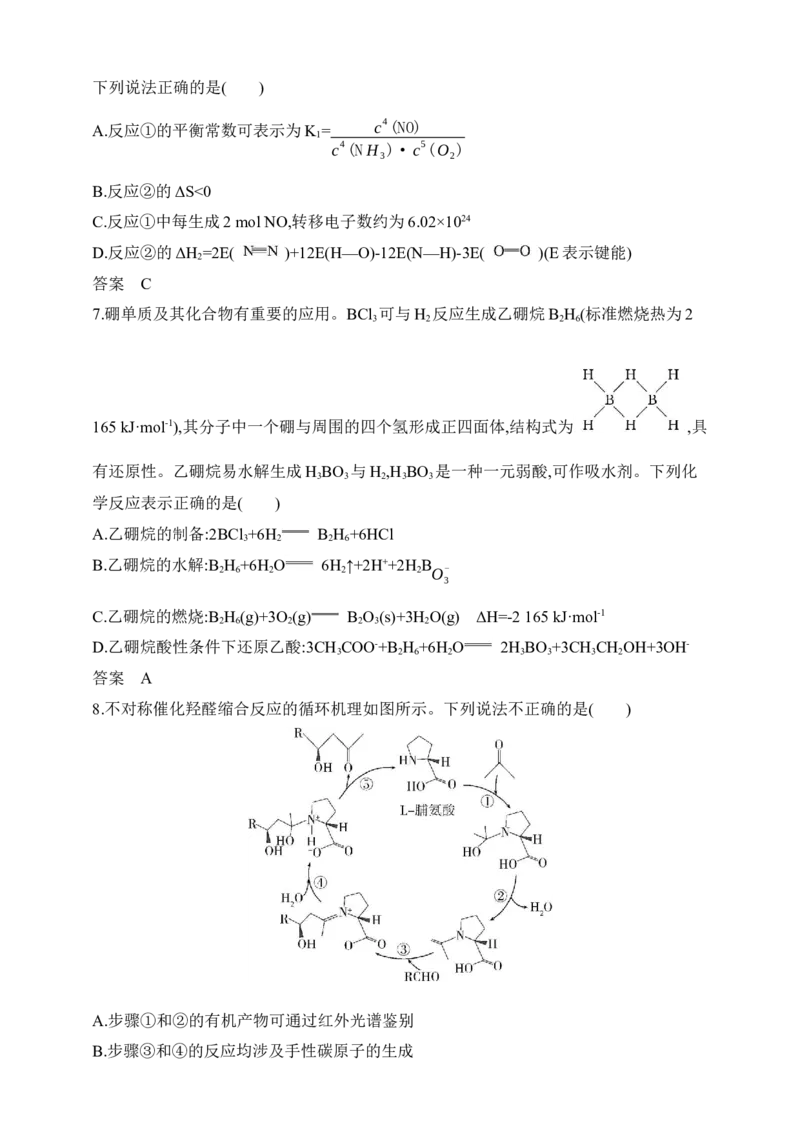
7.硼单质及其化合物有重要的应用。BCl 可与H 反应生成乙硼烷B H (标准燃烧热为2
3 2 2 6
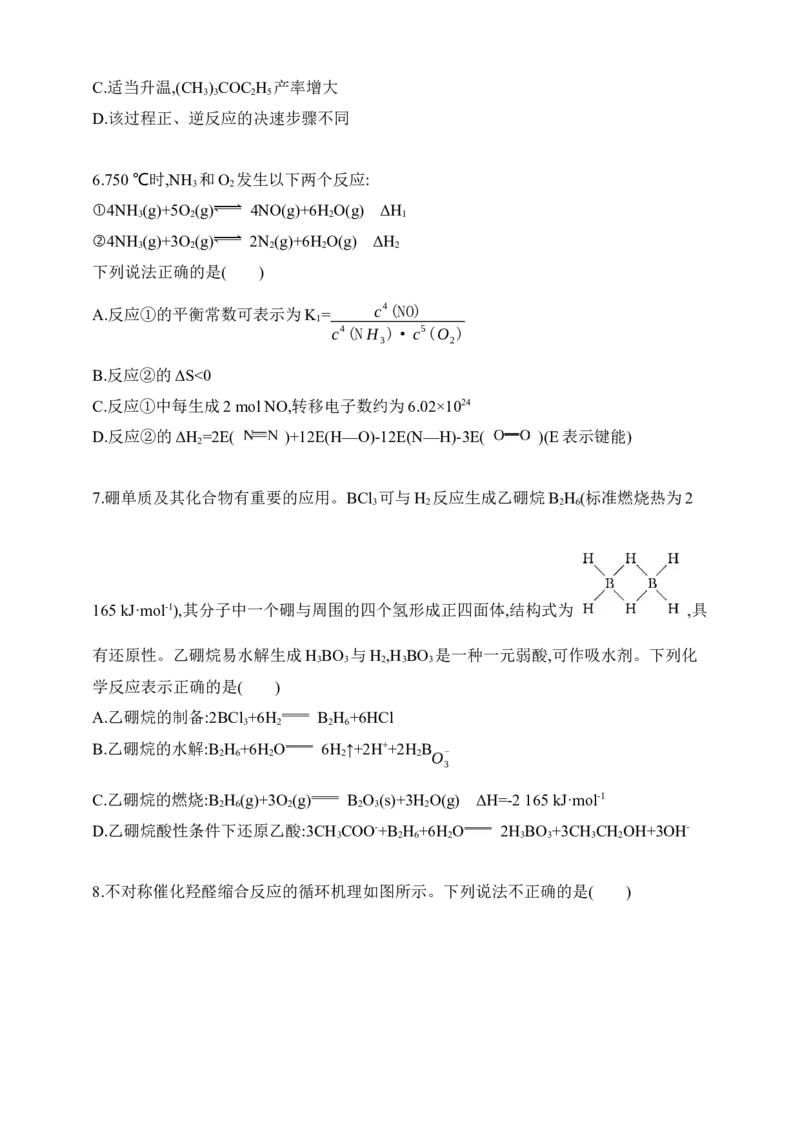
165 kJ·mol-1),其分子中一个硼与周围的四个氢形成正四面体,结构式为 ,具
有还原性。乙硼烷易水解生成H BO 与H ,H BO 是一种一元弱酸,可作吸水剂。下列化
3 3 2 3 3
学反应表示正确的是( )
A.乙硼烷的制备:2BCl +6H B H +6HCl
3 2 2 6
B.乙硼烷的水解:B H +6H O 6H ↑+2H++2H B
2 6 2 2 2 O-
3
C.乙硼烷的燃烧:B H (g)+3O (g) B O (s)+3H O(g) ΔH=-2 165 kJ·mol-1
2 6 2 2 3 2
D.乙硼烷酸性条件下还原乙酸:3CH COO-+B H +6H O 2H BO +3CH CH OH+3OH-
3 2 6 2 3 3 3 2
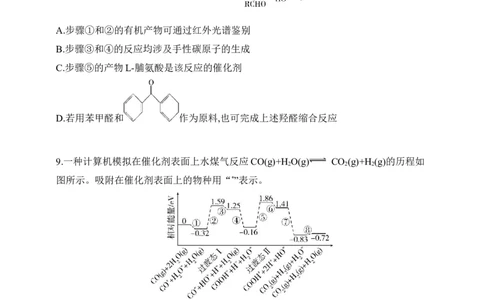
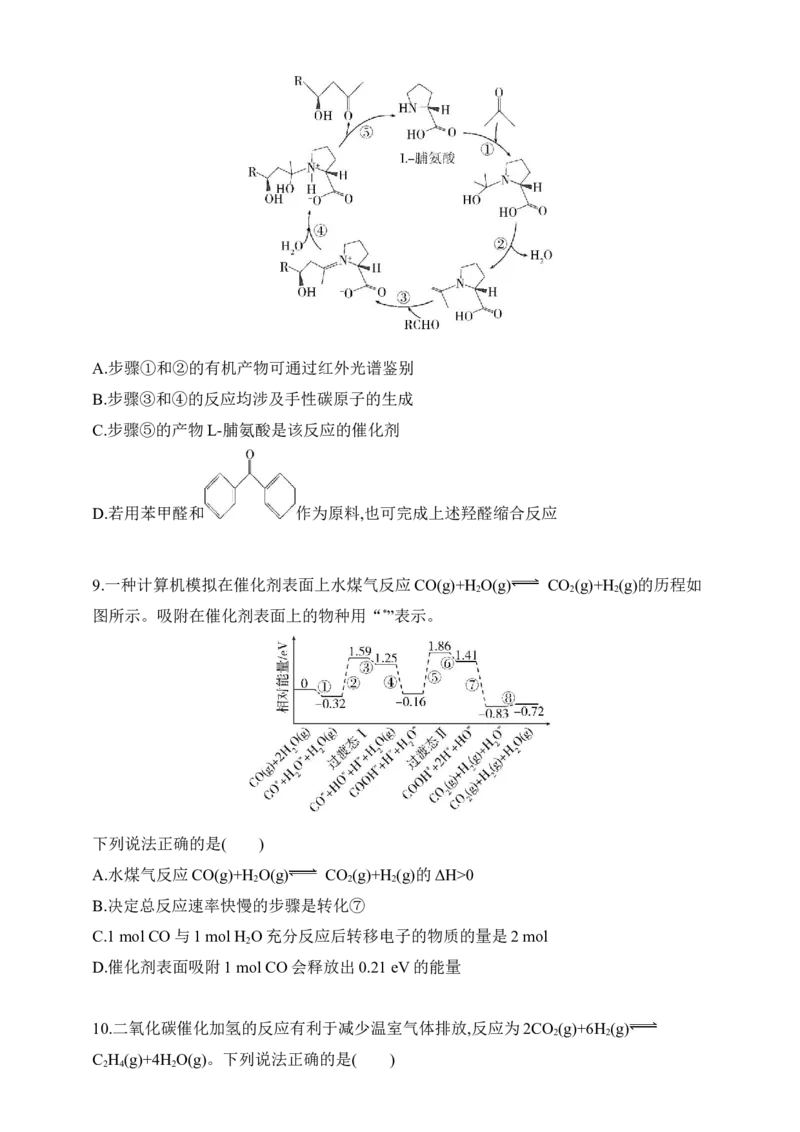
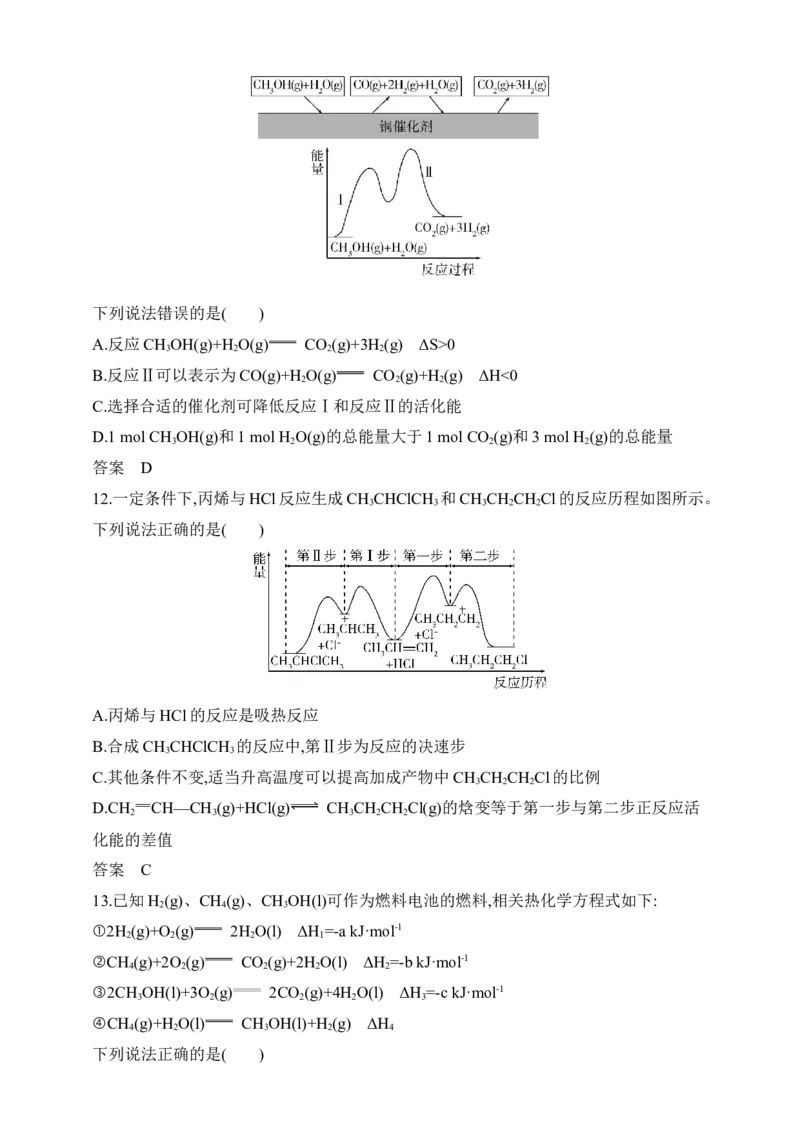
8.不对称催化羟醛缩合反应的循环机理如图所示。下列说法不正确的是( )A.步骤①和②的有机产物可通过红外光谱鉴别
B.步骤③和④的反应均涉及手性碳原子的生成
C.步骤⑤的产物L-脯氨酸是该反应的催化剂
D.若用苯甲醛和 作为原料,也可完成上述羟醛缩合反应
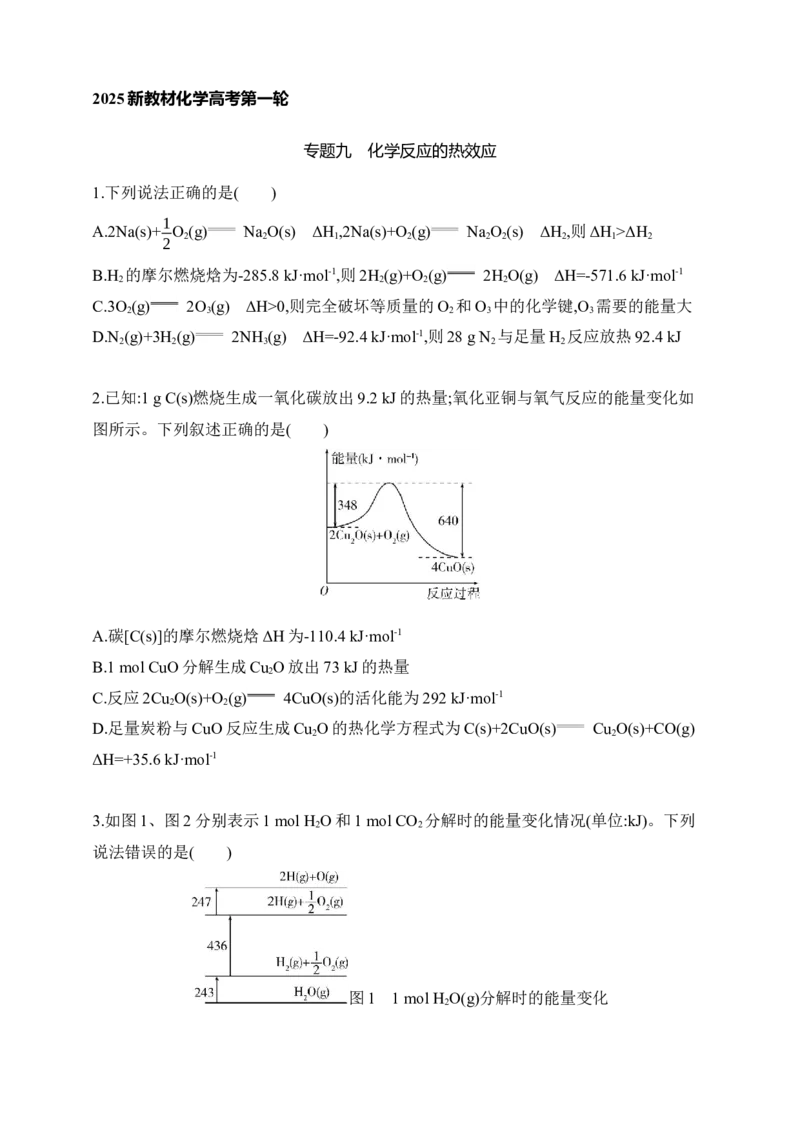
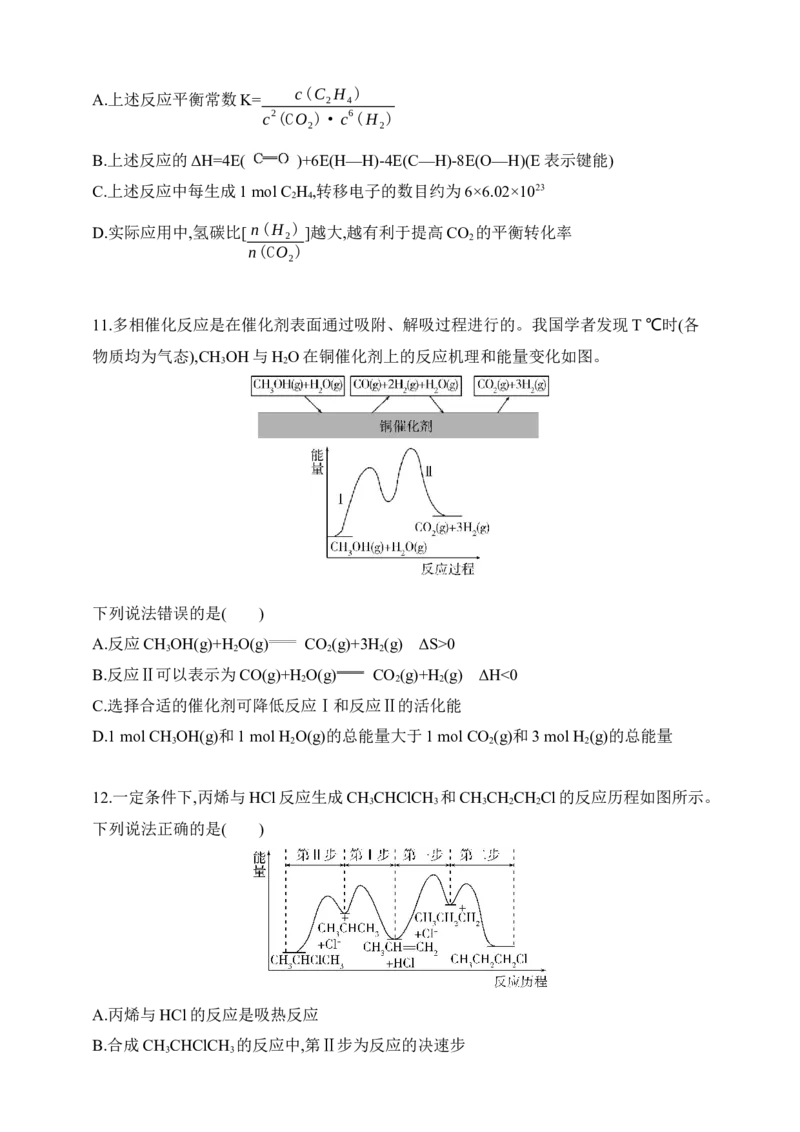
9.一种计算机模拟在催化剂表面上水煤气反应CO(g)+H O(g) CO (g)+H (g)的历程如
2 2 2
图所示。吸附在催化剂表面上的物种用“*”表示。
下列说法正确的是( )
A.水煤气反应CO(g)+H O(g) CO (g)+H (g)的ΔH>0
2 2 2
B.决定总反应速率快慢的步骤是转化⑦
C.1 mol CO与1 mol H O充分反应后转移电子的物质的量是2 mol
2
D.催化剂表面吸附1 mol CO会释放出0.21 eV的能量
10.二氧化碳催化加氢的反应有利于减少温室气体排放,反应为2CO (g)+6H (g)
2 2
C H (g)+4H O(g)。下列说法正确的是( )
2 4 2c(C H )
A.上述反应平衡常数K=
2 4
c2(CO )·c6(H )
2 2
B.上述反应的ΔH=4E( )+6E(H—H)-4E(C—H)-8E(O—H)(E表示键能)
C.上述反应中每生成1 mol C H ,转移电子的数目约为6×6.02×1023
2 4
D.实际应用中,氢碳比[ n(H ) ]越大,越有利于提高CO 的平衡转化率
2 2
n(CO )
2
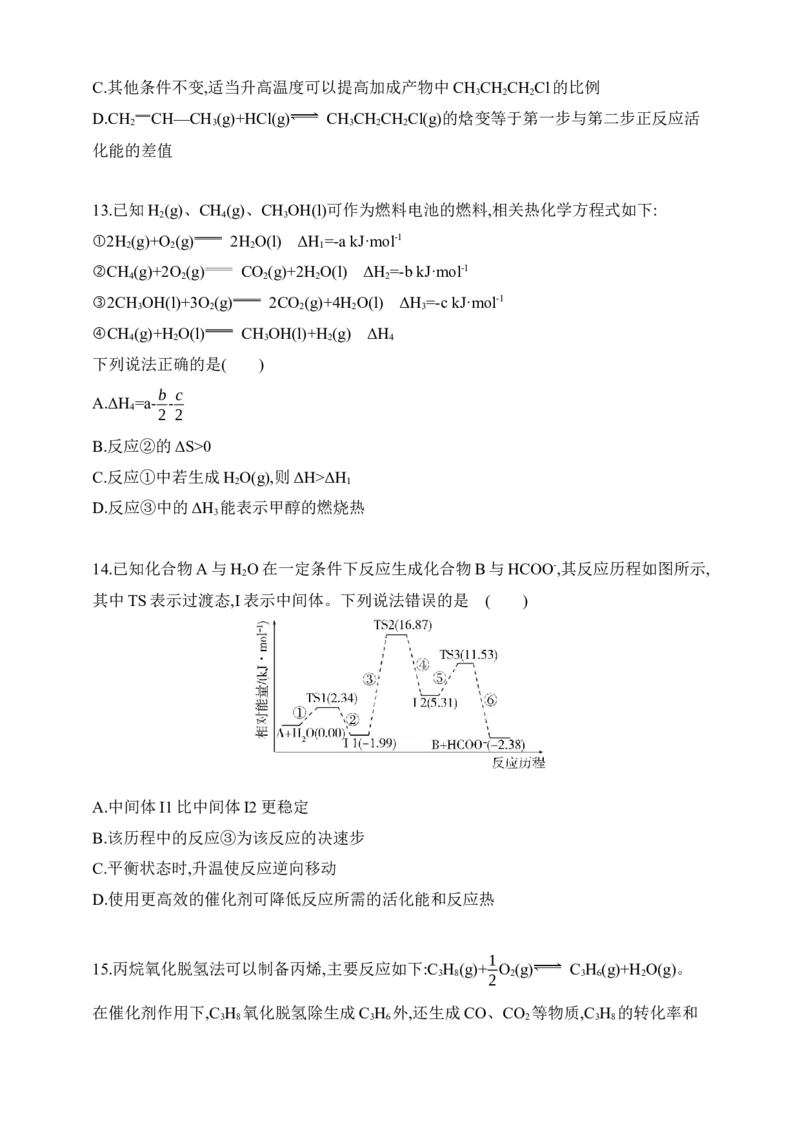
11.多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T ℃时(各
物质均为气态),CH OH与H O在铜催化剂上的反应机理和能量变化如图。
3 2
下列说法错误的是( )
A.反应CH OH(g)+H O(g) CO (g)+3H (g) ΔS>0
3 2 2 2
B.反应Ⅱ可以表示为CO(g)+H O(g) CO (g)+H (g) ΔH<0
2 2 2
C.选择合适的催化剂可降低反应Ⅰ和反应Ⅱ的活化能
D.1 mol CH OH(g)和1 mol H O(g)的总能量大于1 mol CO (g)和3 mol H (g)的总能量
3 2 2 2
12.一定条件下,丙烯与HCl反应生成CH CHClCH 和CH CH CH Cl的反应历程如图所示。
3 3 3 2 2
下列说法正确的是( )
A.丙烯与HCl的反应是吸热反应
B.合成CH CHClCH 的反应中,第Ⅱ步为反应的决速步
3 3C.其他条件不变,适当升高温度可以提高加成产物中CH CH CH Cl的比例
3 2 2
D.CH CH—CH (g)+HCl(g) CH CH CH Cl(g)的焓变等于第一步与第二步正反应活
2 3 3 2 2
化能的差值
13.已知H (g)、CH (g)、CH OH(l)可作为燃料电池的燃料,相关热化学方程式如下:
2 4 3
①2H (g)+O (g) 2H O(l) ΔH =-a kJ·mol-1
2 2 2 1
②CH (g)+2O (g) CO (g)+2H O(l) ΔH =-b kJ·mol-1
4 2 2 2 2
③2CH OH(l)+3O (g) 2CO (g)+4H O(l) ΔH =-c kJ·mol-1
3 2 2 2 3
④CH (g)+H O(l) CH OH(l)+H (g) ΔH
4 2 3 2 4
下列说法正确的是( )
b c
A.ΔH =a- -
4
2 2
B.反应②的ΔS>0
C.反应①中若生成H O(g),则ΔH>ΔH
2 1
D.反应③中的ΔH 能表示甲醇的燃烧热
3
14.已知化合物A与H O在一定条件下反应生成化合物B与HCOO-,其反应历程如图所示,
2
其中TS表示过渡态,I表示中间体。下列说法错误的是 ( )
A.中间体I1比中间体I2更稳定
B.该历程中的反应③为该反应的决速步
C.平衡状态时,升温使反应逆向移动
D.使用更高效的催化剂可降低反应所需的活化能和反应热
1
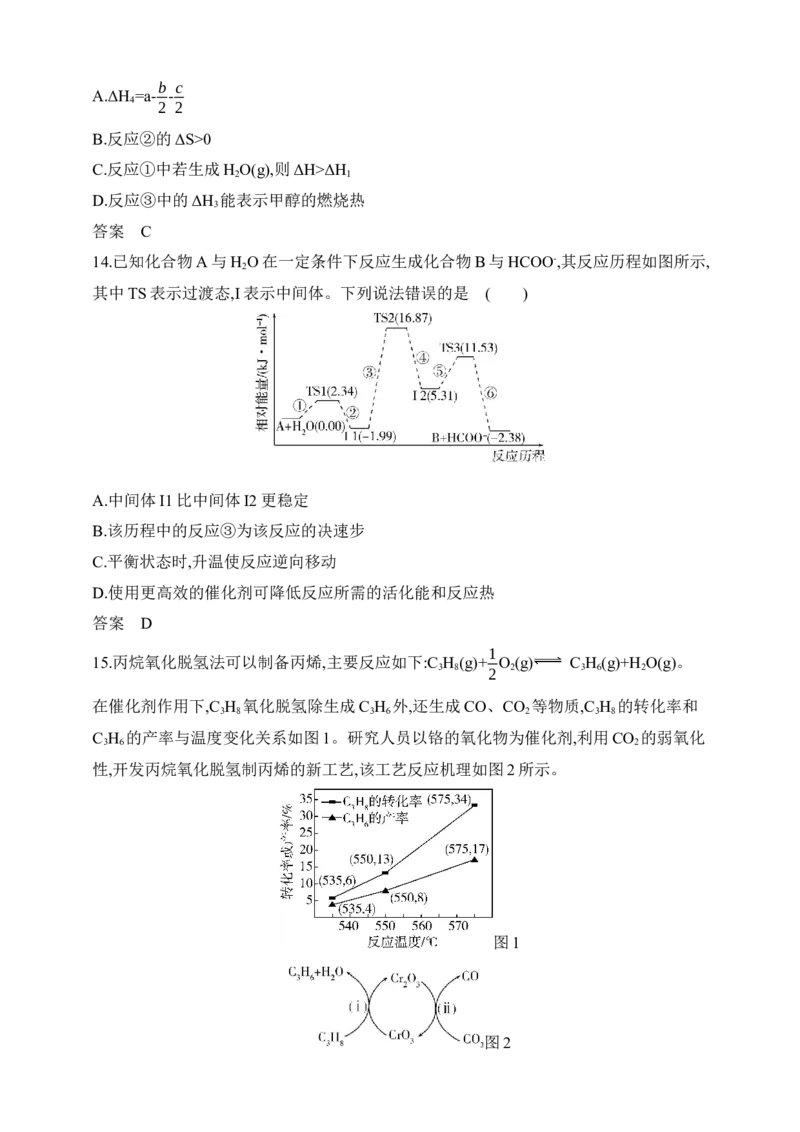
15.丙烷氧化脱氢法可以制备丙烯,主要反应如下:C H (g)+ O (g) C H (g)+H O(g)。
3 8 2 3 6 2
2
在催化剂作用下,C H 氧化脱氢除生成C H 外,还生成CO、CO 等物质,C H 的转化率和
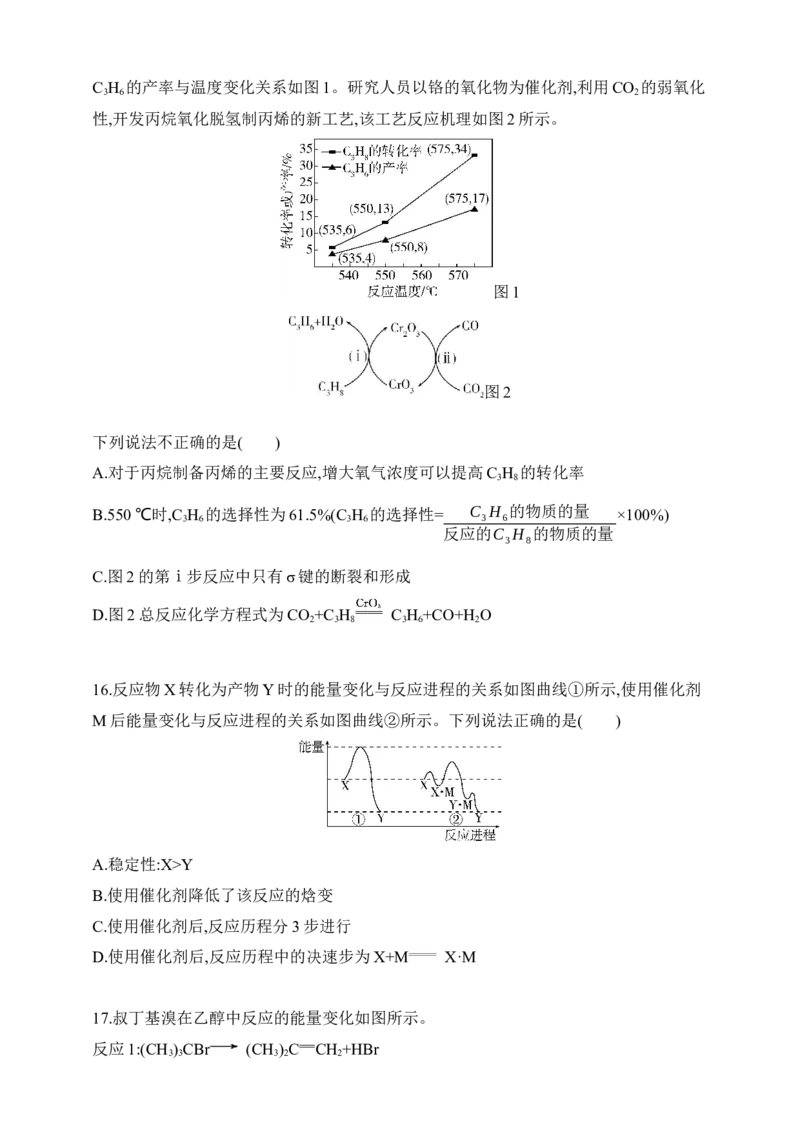
3 8 3 6 2 3 8C H 的产率与温度变化关系如图1。研究人员以铬的氧化物为催化剂,利用CO 的弱氧化
3 6 2
性,开发丙烷氧化脱氢制丙烯的新工艺,该工艺反应机理如图2所示。
图1
图2
下列说法不正确的是( )
A.对于丙烷制备丙烯的主要反应,增大氧气浓度可以提高C H 的转化率
3 8
B.550 ℃时,C H 的选择性为61.5%(C H 的选择性= C H 的物质的量 ×100%)
3 6 3 6 3 6
反应的C H 的物质的量
3 8
C.图2的第ⅰ步反应中只有σ键的断裂和形成
D.图2总反应化学方程式为CO +C H C H +CO+H O
2 3 8 3 6 2
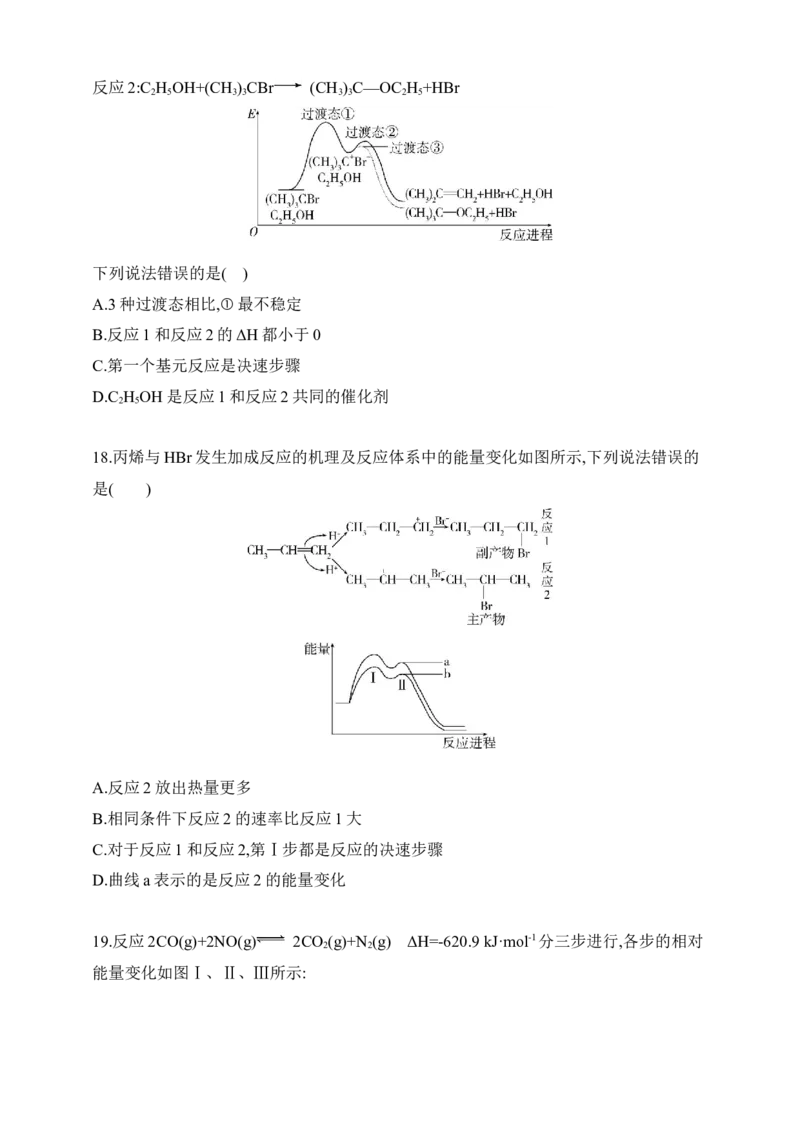
16.反应物X转化为产物Y时的能量变化与反应进程的关系如图曲线①所示,使用催化剂
M后能量变化与反应进程的关系如图曲线②所示。下列说法正确的是( )
A.稳定性:X>Y
B.使用催化剂降低了该反应的焓变
C.使用催化剂后,反应历程分3步进行
D.使用催化剂后,反应历程中的决速步为X+M X·M
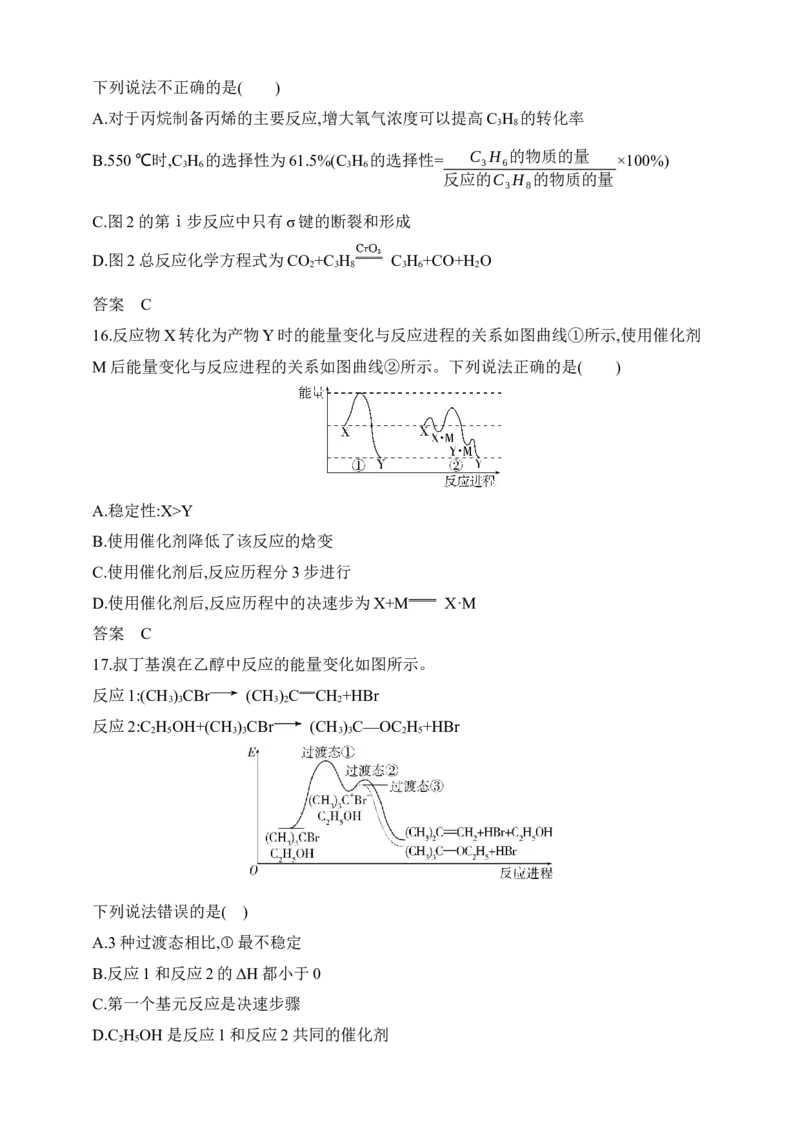
17.叔丁基溴在乙醇中反应的能量变化如图所示。
反应1:(CH ) CBr (CH ) C CH +HBr
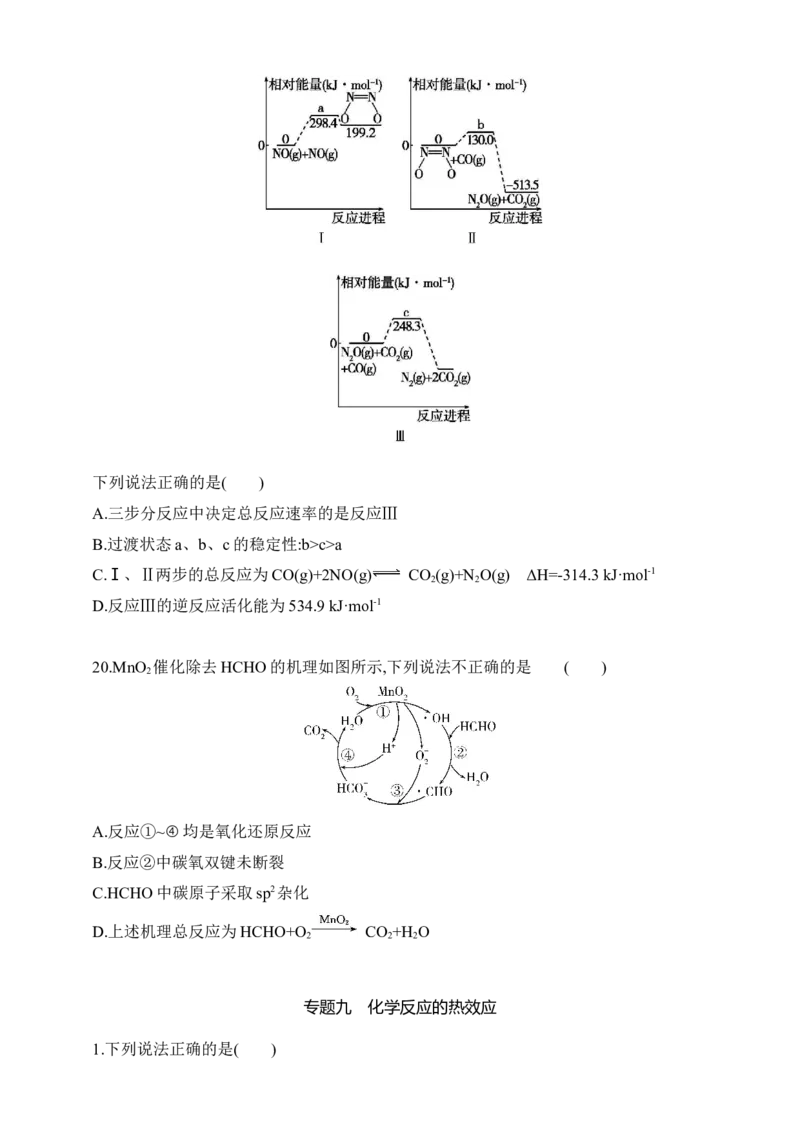
3 3 3 2 2反应2:C H OH+(CH ) CBr (CH ) C—OC H +HBr
2 5 3 3 3 3 2 5
下列说法错误的是( )
A.3种过渡态相比,①最不稳定
B.反应1和反应2的ΔH都小于0
C.第一个基元反应是决速步骤
D.C H OH是反应1和反应2共同的催化剂
2 5
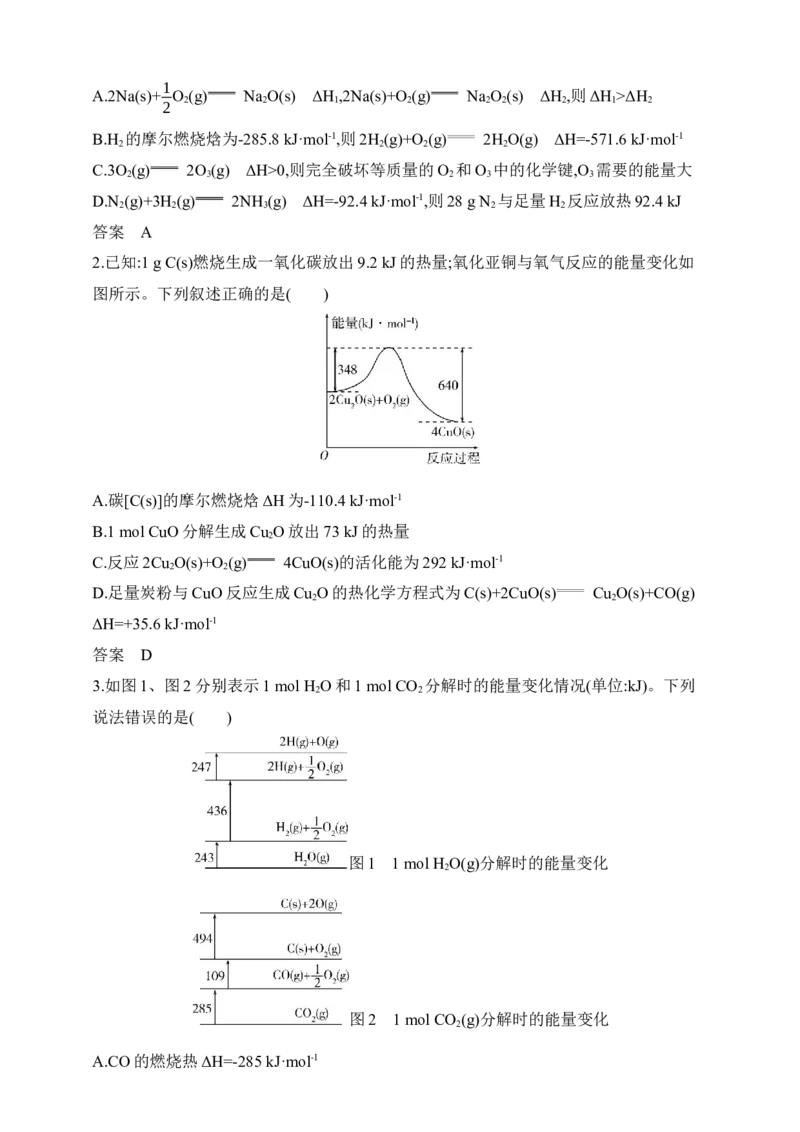
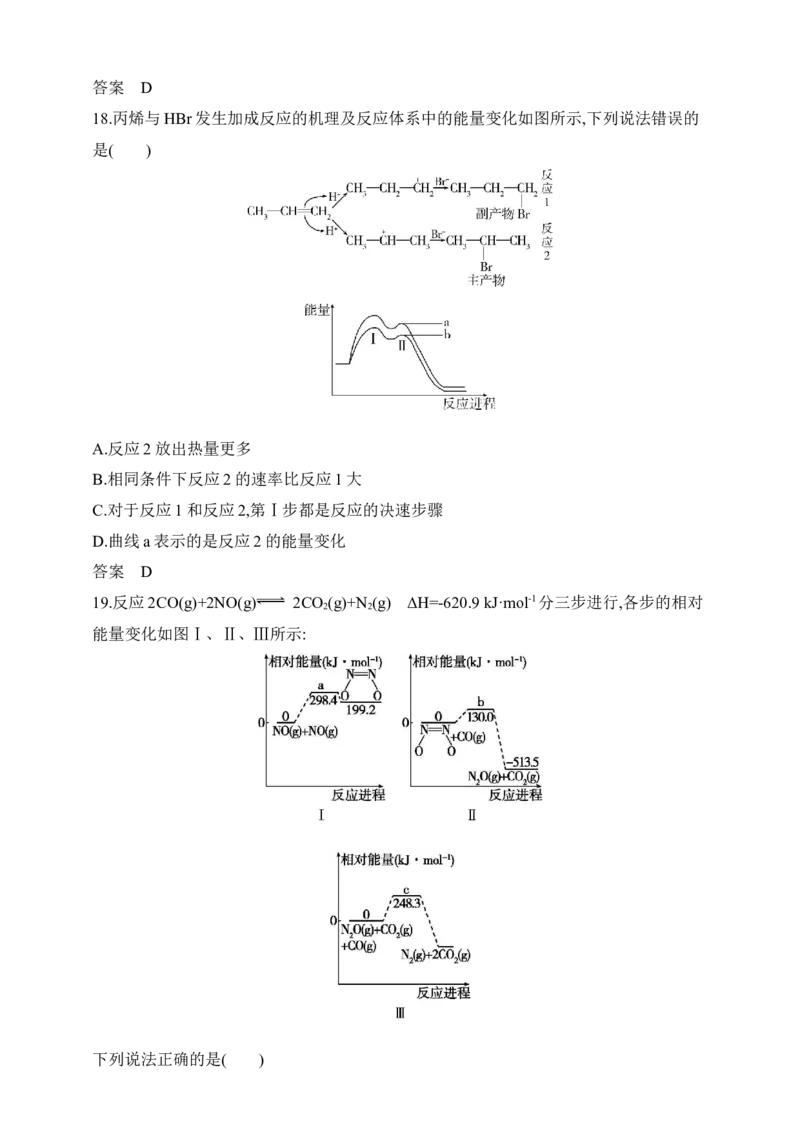
18.丙烯与HBr发生加成反应的机理及反应体系中的能量变化如图所示,下列说法错误的
是( )
A.反应2放出热量更多
B.相同条件下反应2的速率比反应1大
C.对于反应1和反应2,第Ⅰ步都是反应的决速步骤
D.曲线a表示的是反应2的能量变化
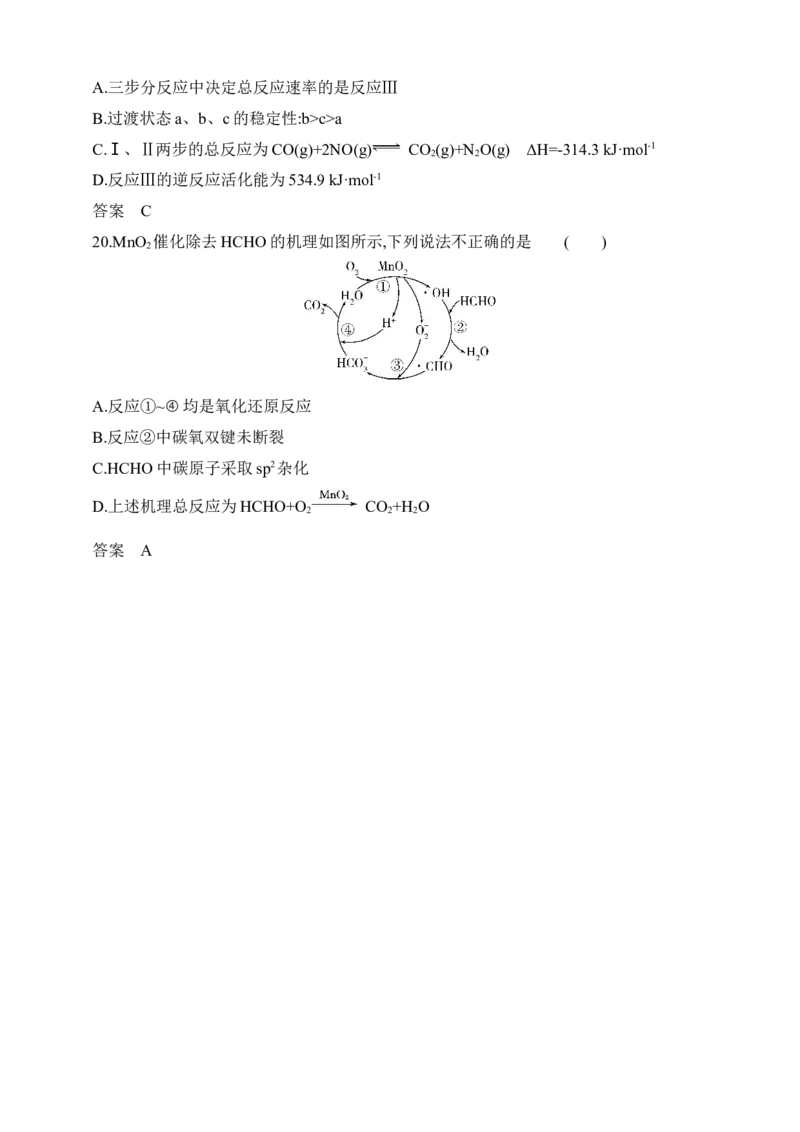
19.反应2CO(g)+2NO(g) 2CO (g)+N (g) ΔH=-620.9 kJ·mol-1分三步进行,各步的相对
2 2
能量变化如图Ⅰ、Ⅱ、Ⅲ所示:下列说法正确的是( )
A.三步分反应中决定总反应速率的是反应Ⅲ
B.过渡状态a、b、c的稳定性:b>c>a
C.Ⅰ、Ⅱ两步的总反应为CO(g)+2NO(g) CO (g)+N O(g) ΔH=-314.3 kJ·mol-1
2 2
D.反应Ⅲ的逆反应活化能为534.9 kJ·mol-1
20.MnO 催化除去HCHO的机理如图所示,下列说法不正确的是 ( )
2
A.反应①~④均是氧化还原反应
B.反应②中碳氧双键未断裂
C.HCHO中碳原子采取sp2杂化
D.上述机理总反应为HCHO+O CO +H O
2 2 2
专题九 化学反应的热效应
1.下列说法正确的是( )1
A.2Na(s)+ O (g) Na O(s) ΔH ,2Na(s)+O (g) Na O (s) ΔH ,则ΔH >ΔH
2 2 1 2 2 2 2 1 2
2
B.H 的摩尔燃烧焓为-285.8 kJ·mol-1,则2H (g)+O (g) 2H O(g) ΔH=-571.6 kJ·mol-1
2 2 2 2
C.3O (g) 2O (g) ΔH>0,则完全破坏等质量的O 和O 中的化学键,O 需要的能量大
2 3 2 3 3
D.N (g)+3H (g) 2NH (g) ΔH=-92.4 kJ·mol-1,则28 g N 与足量H 反应放热92.4 kJ
2 2 3 2 2
答案 A
2.已知:1 g C(s)燃烧生成一氧化碳放出9.2 kJ的热量;氧化亚铜与氧气反应的能量变化如
图所示。下列叙述正确的是( )
A.碳[C(s)]的摩尔燃烧焓ΔH为-110.4 kJ·mol-1
B.1 mol CuO分解生成Cu O放出73 kJ的热量
2
C.反应2Cu O(s)+O (g) 4CuO(s)的活化能为292 kJ·mol-1
2 2
D.足量炭粉与CuO反应生成Cu O的热化学方程式为C(s)+2CuO(s) Cu O(s)+CO(g)
2 2
ΔH=+35.6 kJ·mol-1
答案 D
3.如图1、图2分别表示1 mol H O和1 mol CO 分解时的能量变化情况(单位:kJ)。下列
2 2
说法错误的是( )
图1 1 mol H O(g)分解时的能量变化
2
图2 1 mol CO (g)分解时的能量变化
2
A.CO的燃烧热ΔH=-285 kJ·mol-1B.C(s)+H O(g) CO(g)+H (g)
2 2
ΔH=+134 kJ·mol-1
C. 的键能为494 kJ·mol-1
D.无法求得CO(g)+H O(g) CO (g)+H (g)的反应热
2 2 2
答案 D
4.根据HX的水溶液能量循环图,下列说法不正确的是( )
A.由于氢键的存在,ΔH (HF)>ΔH (HCl)
1 1
B.已知HF气体溶于水放热,则ΔH (HF)<0
1
C.相同条件下,ΔH (HCl)>ΔH (HBr)
2 2
D.ΔH=ΔH +ΔH +ΔH +ΔH +ΔH +ΔH
1 2 3 4 5 6
答案 B
5.某溴丁烷与乙醇反应的能量转化如图(“”表示过渡态)。下列说法错误的是( )
A.总反应为取代反应
B.该反应过程中C原子杂化方式有变化
C.适当升温,(CH ) COC H 产率增大
3 3 2 5
D.该过程正、逆反应的决速步骤不同
答案 C
6.750 ℃时,NH 和O 发生以下两个反应:
3 2
①4NH (g)+5O (g) 4NO(g)+6H O(g) ΔH
3 2 2 1
②4NH (g)+3O (g) 2N (g)+6H O(g) ΔH
3 2 2 2 2下列说法正确的是( )
A.反应①的平衡常数可表示为K =
c4(NO)
1
c4(NH )·c5(O )
3 2
B.反应②的ΔS<0
C.反应①中每生成2 mol NO,转移电子数约为6.02×1024
D.反应②的ΔH =2E( )+12E(H—O)-12E(N—H)-3E( )(E表示键能)
2
答案 C
7.硼单质及其化合物有重要的应用。BCl 可与H 反应生成乙硼烷B H (标准燃烧热为2
3 2 2 6
165 kJ·mol-1),其分子中一个硼与周围的四个氢形成正四面体,结构式为 ,具
有还原性。乙硼烷易水解生成H BO 与H ,H BO 是一种一元弱酸,可作吸水剂。下列化
3 3 2 3 3
学反应表示正确的是( )
A.乙硼烷的制备:2BCl +6H B H +6HCl
3 2 2 6
B.乙硼烷的水解:B H +6H O 6H ↑+2H++2H B
2 6 2 2 2 O-
3
C.乙硼烷的燃烧:B H (g)+3O (g) B O (s)+3H O(g) ΔH=-2 165 kJ·mol-1
2 6 2 2 3 2
D.乙硼烷酸性条件下还原乙酸:3CH COO-+B H +6H O 2H BO +3CH CH OH+3OH-
3 2 6 2 3 3 3 2
答案 A
8.不对称催化羟醛缩合反应的循环机理如图所示。下列说法不正确的是( )
A.步骤①和②的有机产物可通过红外光谱鉴别
B.步骤③和④的反应均涉及手性碳原子的生成C.步骤⑤的产物L-脯氨酸是该反应的催化剂
D.若用苯甲醛和 作为原料,也可完成上述羟醛缩合反应
答案 D
9.一种计算机模拟在催化剂表面上水煤气反应CO(g)+H O(g) CO (g)+H (g)的历程如
2 2 2
图所示。吸附在催化剂表面上的物种用“*”表示。
下列说法正确的是( )
A.水煤气反应CO(g)+H O(g) CO (g)+H (g)的ΔH>0
2 2 2
B.决定总反应速率快慢的步骤是转化⑦
C.1 mol CO与1 mol H O充分反应后转移电子的物质的量是2 mol
2
D.催化剂表面吸附1 mol CO会释放出0.21 eV的能量
答案 D
10.二氧化碳催化加氢的反应有利于减少温室气体排放,反应为2CO (g)+6H (g)
2 2
C H (g)+4H O(g)。下列说法正确的是( )
2 4 2
c(C H )
A.上述反应平衡常数K=
2 4
c2(CO )·c6(H )
2 2
B.上述反应的ΔH=4E( )+6E(H—H)-4E(C—H)-8E(O—H)(E表示键能)
C.上述反应中每生成1 mol C H ,转移电子的数目约为6×6.02×1023
2 4
D.实际应用中,氢碳比[ n(H ) ]越大,越有利于提高CO 的平衡转化率
2 2
n(CO )
2
答案 D
11.多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T ℃时(各
物质均为气态),CH OH与H O在铜催化剂上的反应机理和能量变化如图。
3 2下列说法错误的是( )
A.反应CH OH(g)+H O(g) CO (g)+3H (g) ΔS>0
3 2 2 2
B.反应Ⅱ可以表示为CO(g)+H O(g) CO (g)+H (g) ΔH<0
2 2 2
C.选择合适的催化剂可降低反应Ⅰ和反应Ⅱ的活化能
D.1 mol CH OH(g)和1 mol H O(g)的总能量大于1 mol CO (g)和3 mol H (g)的总能量
3 2 2 2
答案 D
12.一定条件下,丙烯与HCl反应生成CH CHClCH 和CH CH CH Cl的反应历程如图所示。
3 3 3 2 2
下列说法正确的是( )
A.丙烯与HCl的反应是吸热反应
B.合成CH CHClCH 的反应中,第Ⅱ步为反应的决速步
3 3
C.其他条件不变,适当升高温度可以提高加成产物中CH CH CH Cl的比例
3 2 2
D.CH CH—CH (g)+HCl(g) CH CH CH Cl(g)的焓变等于第一步与第二步正反应活
2 3 3 2 2
化能的差值
答案 C
13.已知H (g)、CH (g)、CH OH(l)可作为燃料电池的燃料,相关热化学方程式如下:
2 4 3
①2H (g)+O (g) 2H O(l) ΔH =-a kJ·mol-1
2 2 2 1
②CH (g)+2O (g) CO (g)+2H O(l) ΔH =-b kJ·mol-1
4 2 2 2 2
③2CH OH(l)+3O (g) 2CO (g)+4H O(l) ΔH =-c kJ·mol-1
3 2 2 2 3
④CH (g)+H O(l) CH OH(l)+H (g) ΔH
4 2 3 2 4
下列说法正确的是( )b c
A.ΔH =a- -
4
2 2
B.反应②的ΔS>0
C.反应①中若生成H O(g),则ΔH>ΔH
2 1
D.反应③中的ΔH 能表示甲醇的燃烧热
3
答案 C
14.已知化合物A与H O在一定条件下反应生成化合物B与HCOO-,其反应历程如图所示,
2
其中TS表示过渡态,I表示中间体。下列说法错误的是 ( )
A.中间体I1比中间体I2更稳定
B.该历程中的反应③为该反应的决速步
C.平衡状态时,升温使反应逆向移动
D.使用更高效的催化剂可降低反应所需的活化能和反应热
答案 D
1
15.丙烷氧化脱氢法可以制备丙烯,主要反应如下:C H (g)+ O (g) C H (g)+H O(g)。
3 8 2 3 6 2
2
在催化剂作用下,C H 氧化脱氢除生成C H 外,还生成CO、CO 等物质,C H 的转化率和
3 8 3 6 2 3 8
C H 的产率与温度变化关系如图1。研究人员以铬的氧化物为催化剂,利用CO 的弱氧化
3 6 2
性,开发丙烷氧化脱氢制丙烯的新工艺,该工艺反应机理如图2所示。
图1
图2下列说法不正确的是( )
A.对于丙烷制备丙烯的主要反应,增大氧气浓度可以提高C H 的转化率
3 8
B.550 ℃时,C H 的选择性为61.5%(C H 的选择性= C H 的物质的量 ×100%)
3 6 3 6 3 6
反应的C H 的物质的量
3 8
C.图2的第ⅰ步反应中只有σ键的断裂和形成
D.图2总反应化学方程式为CO +C H C H +CO+H O
2 3 8 3 6 2
答案 C
16.反应物X转化为产物Y时的能量变化与反应进程的关系如图曲线①所示,使用催化剂
M后能量变化与反应进程的关系如图曲线②所示。下列说法正确的是( )
A.稳定性:X>Y
B.使用催化剂降低了该反应的焓变
C.使用催化剂后,反应历程分3步进行
D.使用催化剂后,反应历程中的决速步为X+M X·M
答案 C
17.叔丁基溴在乙醇中反应的能量变化如图所示。
反应1:(CH ) CBr (CH ) C CH +HBr
3 3 3 2 2
反应2:C H OH+(CH ) CBr (CH ) C—OC H +HBr
2 5 3 3 3 3 2 5
下列说法错误的是( )
A.3种过渡态相比,①最不稳定
B.反应1和反应2的ΔH都小于0
C.第一个基元反应是决速步骤
D.C H OH是反应1和反应2共同的催化剂
2 5答案 D
18.丙烯与HBr发生加成反应的机理及反应体系中的能量变化如图所示,下列说法错误的
是( )
A.反应2放出热量更多
B.相同条件下反应2的速率比反应1大
C.对于反应1和反应2,第Ⅰ步都是反应的决速步骤
D.曲线a表示的是反应2的能量变化
答案 D
19.反应2CO(g)+2NO(g) 2CO (g)+N (g) ΔH=-620.9 kJ·mol-1分三步进行,各步的相对
2 2
能量变化如图Ⅰ、Ⅱ、Ⅲ所示:
下列说法正确的是( )A.三步分反应中决定总反应速率的是反应Ⅲ
B.过渡状态a、b、c的稳定性:b>c>a
C.Ⅰ、Ⅱ两步的总反应为CO(g)+2NO(g) CO (g)+N O(g) ΔH=-314.3 kJ·mol-1
2 2
D.反应Ⅲ的逆反应活化能为534.9 kJ·mol-1
答案 C
20.MnO 催化除去HCHO的机理如图所示,下列说法不正确的是 ( )
2
A.反应①~④均是氧化还原反应
B.反应②中碳氧双键未断裂
C.HCHO中碳原子采取sp2杂化
D.上述机理总反应为HCHO+O CO +H O
2 2 2
答案 A